Изобретение относится к материалам для медицины, применяемых для заполнения костных полостей в травматологии, ортопедии, реконструкционно-восстановительной хирургии, стоматологии, челюстно-лицевой пластики.
Известно применение для заполнения дефектов кости аутотрансплантатов из кортикального и спонгиозного участков костей самого больного (Травматология и ортопедия /под ред. Юмашева.Г.С. М.:Медицина, 1990, с.576; Ono K., Yamamuro T. - J. Biomed. Mat. Res. - 1982, 22, N 10, p.869-885; Ашкенази А.И., Хирургия кистевого сустава, М.:Медицина,1990,с.352).
Однако во всех случаях подготовка и взятие аутотрансплантата травматично: взятый из большого вертела или крыла подвздошной аутотрансплантат образует еще один дефект, который надо заполнять. Не всегда возможно приготовление трансплантата требуемых размеров, а введение а узкие отверстия, образованные туннелированием, спицами, компрессионно-дистракционными конструкциями не выполняется из-за технологических трудностей.
В настоящее время из-за пандемии СПИДа разумно избегают применения ксенотрансплантатов от трупов и продуктов трупной кости: костной стружки, препаратов ДКТ.
В практике 20 - 30-х годов нашего века было широко распространено применение разнообразных неорганических материалов для заполнения костных полостей: от яичной скорлупы до гипса и смесей карбонатов, фосфатов кальция с риванолом и креозотом, предложенных в 1892 г. Дрессманом под названием "парижский пластырь" (Hulbert S.F., Hench L.R., Torberts D., Bouman D.C. - History of bioceramics // J. Cer. Int. 1982, 8, N 4, p.131-140).
Трудности имплантирования порошковых неорганических материалов, выпадение (эксплантация) таких пломб, их отторжение тканями, а также плохая регенерация костной ткани в контакте с применявшимися материалами определили в свое время отказ от них как от неэффективных и небиосовместимых.
Разработанные специально в 70 - 80-е годы активно взаимодействующие с костью биокерамические материалы не преодолели указанных недостатков при применении в качестве самостоятельно пломбирующих материалов (Ермакова Т.П., Болдырев Р.А., Лысенок Л.Н., Биоактивные стекла и стеклокристаллические материалы - новые перспективные материалы для эндопротезирования/ обзор// Производство медицинского стекла и пластмасс/М.:ВНИИСЭНТИ, 1990, вып.3, с.41 библ. 71 назв).
При заполнении костных дефектов стеклокристаллическими и биокерамическими материалами в виде гранул установлено, что набиваемые в дефект гранулы выталкиваются током крови и лимфы в окружающие ткани, т.е. не удерживаются в полости, так как отсутствует сцепление с костью. Неудовлетворительность гистохимических результатов - наличие соединительно-тканой капсулы на границе контакта - обусловило обязательное условие применения остеосовместимых материалов: плотный контакт с костной тканью (Jonicka S., Wagner W., Wohluvova U. - Histologic reactions to afferents HPA-granuls // Impbant. Mat. Biofunct: Proc. Zth., Eu., Conf. Biomaterials, Amsterdam. Sept. 8 - 14, 1987, p.67-82).
Указанные недостатки не преодолеваются предложенными тогда же сложно-составными биокомпозициями, соединяющими гидроксилаппатит, трикальций фосфат, стеклокристаллические материалы с природными биополимерами - желатином, коллагеном, фибрином, протеиновой массой белков крови, фибронектином, которые предотвращают кровотечение в зоне контакта. Композиции могут вводиться в пастообразном состоянии в доступные открытые полости и должны быстро закрываться прилегающими тканями (Westerfeld H., de Groot P. Patent literatur a soures of Information for researsch and development: A investigation for calcium phosphate containinung // J. Biomed. Mat. Rssearch: Applied Biomat., 1989, v. 23(1)A, p. 41-71).
В обзоре прореферированы 171 патентный источник с 1975 по 1989 г. (Innovative Bioceramik // Innov. and Mаaagement. - 1991 - N 1-2, s.30-33).
Таким образом, ни одна из известных композиций не нашла широкого применения в практике, так как не отвечает требованиям удобства имплантирования: быстрого заполнения всего объема дефекта, создание при переходе из консистентного в твердое состояние плотного контакта с костью,- и функциональным требованиям основного назначения материала композиции: в течение времени пребывания в организме способствовать замещению дефекта собственной ламеллярной костью за счет биодеградируемых компонентов-"строительных кирпичей" регенеративного процесса, длящегося 7 - 10 нед.
Вместе с тем известны отвергаемые в качестве материалов для эндопротезирования из-за недостаточной биостойкости (биодеградация вызвана избирательной сорбцией белков и липидов из крови и сопровождается утратой механических и прочностных свойств материала) биоинертные силиконовые полимеры (Полимеры специального назначения/пер.с япон. //под ред.Н.Исе, И.Такабуси. М.:Мир, 1983, с. 208).
Силиконовые компаунды холодного отверждения применяются в системе паста-жидкость как высокоточные оттисковые материалы (СОМы), разделительные материалы для изоляции пришеечной части зуба от гипса при изготовлении и подгонке деталей протезов, фасеток, базисных прокладок. Их основа - жидкие кремнеорганические каучуки: олигомерные силоксаны HO(R2SiO)n, где R - углеводородный радикал (метил), а n ≥ 40 - образуют пространственную структуру (отверждаются) за счет сшивки по концевым гидроксильным группам с помощью полифункциональных отвердителей в обязательном присутствии катализаторов. Наиболее эффективно для получения беспористого, безусадочного, механически прочного вулканизата применение оловоорганических соединений: октоата олова Sn(O. CO(CH2)6•CH3)2; эфиров  , где
, где  - метиловый, бутиловый, этиловый радикал; а OCOR''1 - ацетил, каприл-, лаурил-; например (C4H9)2. Sn(OCO•C11H23 - дибутилоловодилаурилат или (C2H5)2. Sn(OCO•C7H13)2 - диэтилоловодикаприлат (Материаловедение в стоматологии/под ред.А.И.Рыбакова. М.:Медицина, 1984, 424 с.).
- метиловый, бутиловый, этиловый радикал; а OCOR''1 - ацетил, каприл-, лаурил-; например (C4H9)2. Sn(OCO•C11H23 - дибутилоловодилаурилат или (C2H5)2. Sn(OCO•C7H13)2 - диэтилоловодикаприлат (Материаловедение в стоматологии/под ред.А.И.Рыбакова. М.:Медицина, 1984, 424 с.).
Действие этих соединений связано с образованием промежуточного комплекса с координационной связью между O-OH группами полидиметилсилоксана и кислорода этоксигрупп, в результате распада которого происходит образование пространственных связей между макромолекулами и выделение газообразных продуктов полимеризации H2O, CH3COOH.
Но применение остротоксичных канцерогенных веществ, какими являются все известные катализаторы при получении силиконовых эластомеров, в т.ч. и силиконовых оттисковых материалов, разрешают (при обязательной биологической защите работающего медперсонала) потому, что контакт материала с тканями организма (для СОМов - однократный, в течение 4 - 6 мин со слизистой рта) проходит с приготовленной вне организма композицией или с той, где с момента смешения основной пасты со сшивателем и катализатором уже пошли реакции полимеризации, поликонденсации.
Состав оттискового силиконового материала (10, с.199) является наиболее близким по химическому составу предлагаемой композиции и потому выбран в качестве прототипа.
Паста густой консистентности, мас.%:
Каучук СКТН - 29,5
Каучук СКТ - 34,4
Диатомит - 19,7
Карбонат кальция - 14,9
ПАВ - корректоры вкуса - 1,5
Жидкость для отверждения:
Дибутилоловодилауринат - 50
Тетраэтоксисилан - 50
Гидрополисилоксан - 100
Анализ состава композиции-прототипа устанавливает присутствие остротоксичных, бластогенных веществ, выступающих в роли обязательных катализаторов, сшивателей, аппретирующих добавок, вводимых для модифицирования поверхности дисперсного наполнителя и получения беспористого, неусаживающегося оттискового вулканизата. Отсюда - невозможность прямого заимствования, перенесения для заполнения дефектов костных полостей известных составов силиконовых материалов, разработанных для сугубо специфичной области использования в стоматологии, вне длительного контакта со средами и тканями организма.
Цель изобретения - повышение биологической и технологической эффективности заполоняющей костные дефекты композиции на силиконовой основе.
Поставленная цель достигается тем, что предлагаемая композиция, содержащая биологически инертные функциональные компоненты: полиэтилгидридсилоксан и жидкий силиконовый каучук СКТН отличается тем, что в нее введены коллаген, лекарственные средства и остеосовместимый биоситалл М-31, содержащий в качестве единственной кристаллической соли аппатит (даллит) при следующих концентрационных соотношениях, в мас.%:
Силиконовый эластомер (СКТНБ) - 46 - 23
Полиэтилгидридсилоксан (ГКЖ-94) - 7 - 5
Коллаген марки А - 15 - 23
Лекарственные средства - 1 - 2
Биоситалл М-31 - 31 - 47
в составе которого оксиды-компоненты представлены в следующих концентрациях, в мас.%:
SiO2 - 37,2 - 38,5;
P2O5 - 15,5 - 13,2
Al2O3 - 6,2 - 6,5
CaO - 33,5 - 35,0
MgO - 3,1 - 1,8
ZnO - 4,5 - 5,0
Из сопоставительного анализа предлагаемого и известных решений следует, что тождественности по химическому составу и технологическому решению поставленных задач не имеется.
Предлагаемая композиция представляет собой эластичный, механически прочный, пористый (до 40% объема представляют открытые и закрытые поры) материал, наполненный только биосовместимыми с костной тканью компонентами в биодоступной для организма форме. Силиконовая система: матрица пасты (СКТН) - отвердитель (полиэтилгидридсилоксан) при комнатной температуре структурируется в течение 35 - 40 мин в виде хрупких стеклообразных комков. Введение дисперсного наполнителя-биоситалла М-31 в матрицу СКТН не позволяет получить эластичный и прочный компакт. Введение отдельно коллагена в матрицу СКТН также не достигает цели. Получение эластичного продукта, увеличивающего свой объем при структурировании, оказалось возможным в совместном присутствии биоситалла и коллагена в наполнителе.
В отсутствии обычно применяемых оловоорганических катализаторов их роль в инициации полимеризационного процесса (при концентрации ≥ 14-15% по массе) выполняют аминные группы коллагена, т. е. собственно глицина, пролина (оксипролина) - концевые группы пептидных цепей и сорбированные на поверхности ситалла, чьи силанольные и силоксановые группы ≡ Si-O-; ≡ Si-OH; ≡Si-O-←_ NH
В составе ситалла отсутствуют щелочные катионы, которые при гидроксилировании поверхности за счет взаимодействия с водными парами, имеющимися во влажной атмосфере еще при приготовлении пасты или затем при контакте со средами организма во время структурирования могли бы существенно изменить pH и заряд поверхности и уменьшить сорбционную способность по отношению к аминным группировкам.
Принципиальное отличие в составе и свойствах предлагаемого биоситалла М-31, разработанного в системе SiO2-P2O5-Al2O3-RO, где R = Ca, Mg, Zn достигается иным, чем в известных решениях присутствием оксидов-компонентов, их концентрационным соотношением, мол.: SiO2/P2O5 = 6 (для основных стеклообразователей) Ro/P2O5= 8,3, а CaO/MgO/ZnO = 5:0,5:4, а также отсутствием инициатора кристаллизации, в качестве которого в известных решениях выступают фтористые соединения: CaF2, Na2SiF6 и т.д.
В процессе термообработки исходного стекла предлагаемого состава получен ситалл с единственной кристаллической фазой - аппатитом с дефектной кристаллической решеткой - даллитом Ca9(PO4(4,5OH0,5•(CO3)1,5. При инициации кристаллической фазы, чье содержание составляет r 30%, создании дополнительных дефектов при помоле в процессе получения дисперсного порошка биоситалла, именно она обеспечивает биодоступность "основных строительных блоков" для регенерации собственной костной ткани. Биодеградация стекловидной фазы биоситалла поставляет в зону контакта ионы Si, Mg, Zn, инициирующие процесс синтеза коллагенового матрикса ламеллярной кости.
За счет оптимизации соотношений в активном наполнителе биоситалла и коллагена осуществляется регулирование консистентности пасты на основе СКТН от жидкой до густой и переминаемой, а также времени структурирования - важной технологической характеристики композиции, определяющей действия оператора.
При приготовлении паст применялись следующие материалы:
жидкий ненаполненный силиконовый каучук СКТНв-2мед (разрешенный к применению в медицине) ЛОЗ ВНИИСК - ТУ 38.403.587.88 с молекулярной массой 35-40 тыс.Д., lgη25°C = 25-30 пз., плотность d 25oC = 0,98 г/см3;
коллаген медицинский марки А (завод "Белкозин", ТУ 78-860-77);
остеосовместимый биоситалл М-31 в порошковой фракции с удельной поверхностью 3200 г/см2, размером частиц ср. 60 мкм;
в качестве лекарственных средств использовались фармацевтические препараты (антибиотики, сульфопрепараты), а также специально приготавливаемые по прописям отвары, настои, растворы.
В качестве отвердителя композиции применяли полиэтилгидридсилоксан марки ГКЖ-94 (ГОСТ 10834-76), разрешенным также к применению в фармацевтических, косметических средствах, с молекулярной массой 20-30 тыс.Д., плотность d 25oC = 1,0 г/см3.
Близкие к 1 г/см3 значения плотностей силиконовых жидкостей позволяли быстро пересчитать объем, отмеряемого дозирующим устройством СКТНв и ГКЖ-94, на его массу, вводимую в композицию.
Пример 1. Приготовление композиции с густой пастой для заполнения доступного дефекта большого объема.
Предварительно стерилизованные порошковые компоненты (биоситалл, коллаген, расфасованные в упаковки по 10 г) подаются в стерильных упаковках на стол, где с помощью шпателя в фарфоровой стерильной чашке (100 мл) смешиваются в соотношении: коллаген 10 г : биоситалл М-31 20 г.
Затем в чашку вводится 30 мл жидкого каучука СКТНв- 2мед, отмеряемого также из предварительно стерильной дозирующей упаковки. Смесь тщательно перетирается и образуется густая по консистентности паста. После этого добавляется 10 мл отвердителя ГКЖ-94, в композицию вводятся лекарственные средства по предписанию врача. Приготовленная композиция имеет время структурирования 10 - 11 мин при 25oC. Этого времени обычно достаточно, чтобы заполнить дефект, впрессовывая массу (техника пломбирования). При 37oC время структурирования уменьшается до 6 - 7 мин. Все это время оператор удерживает под давлением пломбирующего инструмента (лопаточки, ложки, шпателя) композицию в дефекте заполняемой полости. По окончании времени отверждения происходит увеличение объема на 20 - 25% от исходного, занимаемого композицией в момент ее приготовления, поэтому композиция плотно прилегает к краю дефекта и не эксплантируется током крови. Если все-таки предварительно рассчитанный объем материала оказался большим, то по окончании времени отверждения скальпелем можно удалить избыток материала, выступающий над кортикальной частью кости, и приступить к ушиванию прилежащих мягких тканей.
Пример 2. Приготовление композиции с жидкой пастой для заполнения узких отверстий и каналов.
Непосредственно в момент использования в цилиндр шприца всасывается 1,5 мл жидкого ненаполненного каучука СКТНв-2мед из стерилизованной упаковки, в цилиндр с заглушкой, одетой на выпускное отверстие, вводятся предварительно стерилизованные расфасованные в маленькие упаковки по 0,5 г наполнители: 1 г биоситалла и 0,5 г коллагена. Жидкая паста получается перемешиванием движением поршня в шприцевом цилиндре. Она вводится в дефект малого объема - отверстие, канал, из второго шприца туда же вводится 0,5 мл ГКЖ-95, лекарственные формы. Время отверждения и плотного заполнения дефекта 3 -5 мин. Увеличение объема заполняемого дефекта обуславливает кратное (2,5,10 крат) увеличение применяемых масс материалов.
Пример 3. Приготовление композиции для замещения дефекта в черепно-лицевой хирургии.
Производимый промышленностью препарат - коллагеновая губка выкраивается в виде лоскута, необходимого по размерам, затем в соотношении по массе примера 2 пропитывается приготовленной жидкой пастой в лотке. Затем в губку вводится отвердитель. Время отверждения составляет 7 - 8 мин, это позволяет поставить имплантируемый фрагмент в заполняемый дефект, плотное заполнение которого эластичным прочным пористым материалом, содержащем лечебные компоненты (например, губка с облепиховых маслом) происходит после отверждения.
Технико-экономическое обоснование преимуществ применения предлагаемой композиции для заполнения костных дефектов.
Предлагаемая композиция представляет для практического применения следующие преимущества:
1. Удобство имплантирования: заполнение костного дефекта любого объема в момент введения обеспечены вязкостно-пластичными реологическими свойствами пасты - от жидкой, применяемой в технике шприцевания, до переминаемой, применяемой в пломбировочной технике при ручном давлении оператора.
2. Структурирование без применения ультразвуковых или инфракрасных источников энергии, подаваемой в зону дефекта; приобретение плотного состояния в контакте с кровью, плазмой в пределах 5 - 12 мин, достаточных для оператора и приемлемых для длительности оперативного вмешательства.
3. Увеличение объема до 20 - 25% в компакте, что обеспечивает плотно прилегающее контактирование материала с костной тканью. Сохраняя присущее, по-видимости, всем силиконовым материалам свойство, воспроизводить контактную поверхность, с которой материал контактировал при твердении, композиция может точно воспроизводить объемы спонгиозных пор при их заполнении, создавая механическое закрепление в дефекте, которое препятствует эксплантации композиции из дефекта.
4. Наличие у структурированного компакта пористости как закрытой, так и открытой до 40% объема со средним радиусом пор ra = 57 - 100 мкм и удельной поверхностью S = 1,4 м2/г. Экспериментально определенные параметры структуры композиции объясняют активное проникновение нативных сред организма: крови, лимфы в материал, быстрое поступление продуктов деградации "строительных блоков" для регенерации, свободное прорастание в поры материала коллагеновых нитей - каркаса ламмелярной костной ткани в объеме деградирующего материала и полное ее восстановление к 8 - 10 нед после имплантирования.
5. Содержание только биоинертных или биосовместимых с костью компонентов коллагена, биоситалла М-31, сводная сравнительная таблица состава которого и других известных биоситаллов приведена на с.9.
6. Поскольку при лечении многих костных заболеваний возникает необходимость дальнейшего подавления патогенной флоры, хотя закрытию дефекта обязательно предшествует тщательно выполняемые операции по санированию полости и удалению секвестров, нежизнеспособных тканей, в композицию, закрывающую дефект, должны быть введены лекарственные препараты. Установлено, что одномоментно с отвердителем можно вводить до 1 - 2% по массе композиции антибиотиков широкого спектра, сульфопрепаратов (как в порошке, так и растворе), интерферон лейкоцитарный, которые затем медленно будут переходить из депо-компакта в окружающую ткань. Для подавления продолжающихся все-таки процессов можно, не удаляя композицию из дефекта, подавать лекарственные формы иглой шприца в толщу компакта. Специфика данного раздела лечения костных заболеваний требует большой вариабельности лекарственных форм, используемых при лечении конкретного больного. Показана возможность введения в указанных концентрациях биопрепаратов с различными функциями: стимуляторов остеосинтеза: витаминов, солей марганца и железа (фумарат и аскорбинат железа), протеолитических ферментов, экстрактов прополиса и мумие, которые существенно расширяют лечебные функции композиции предлагаемого состава.
7. Все вещества композиции могут стерилизоваться имеющимися в распоряжении лечебных учреждений средствами (автоклав, текущий пар, гамма-воздействие), могут подаваться в стерильных упаковках, предварительно расфасованные в любую операционную, травматологический пункт, что важно при оказании экстренной помощи.
8. Основные препараты, вещества композиции являются нетоксичными соединениями, разрешены к применению в медицине. Силиконовые материалы недефицитны, недороги, доступны, так как выпускаются на предприятиях Санкт-Петербурга. Отечественные материалы целиком исключают необходимость закупки каких-либо компонентов за границей, а ее состав не требует организации новых специальных производств в случае необходимости может быть организован на любом предприятии отрасли в бинарном комплекте: паста (в тубе, цилиндре) - отвердитель в дозаторе.
9. Применение предлагаемой композиции по прилагаемой формуле делает реальным создание новых методов лечения костных заболеваний, новых медицинских технологий.
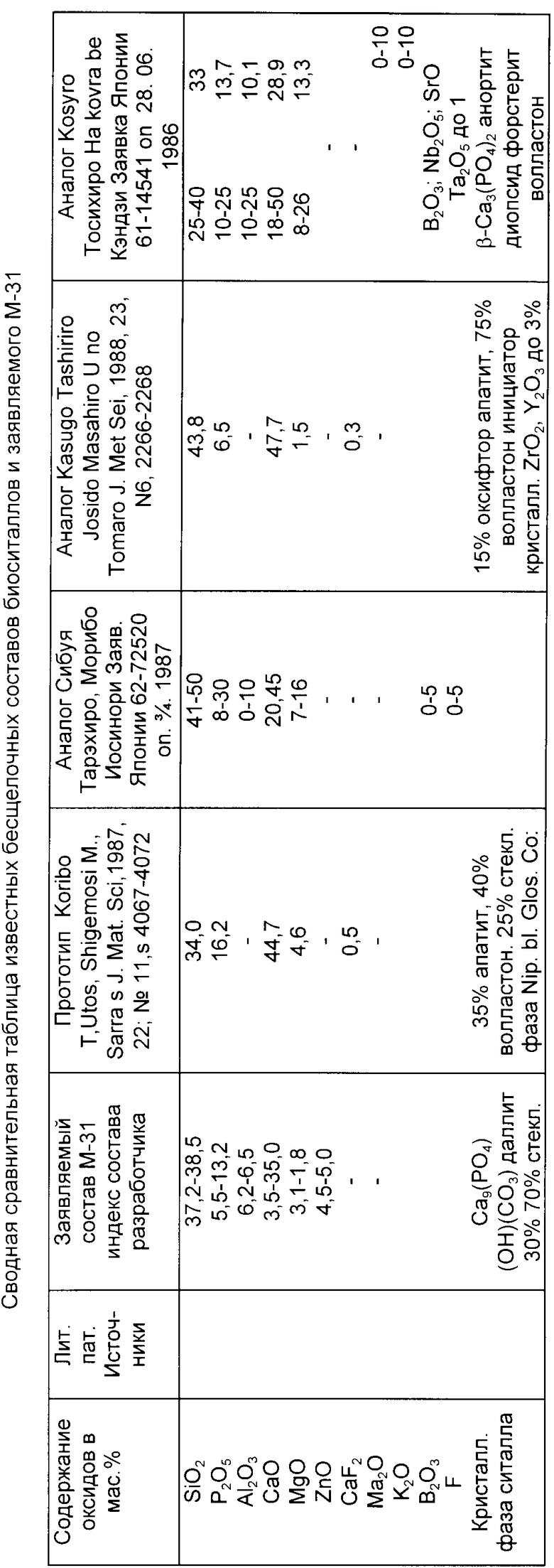
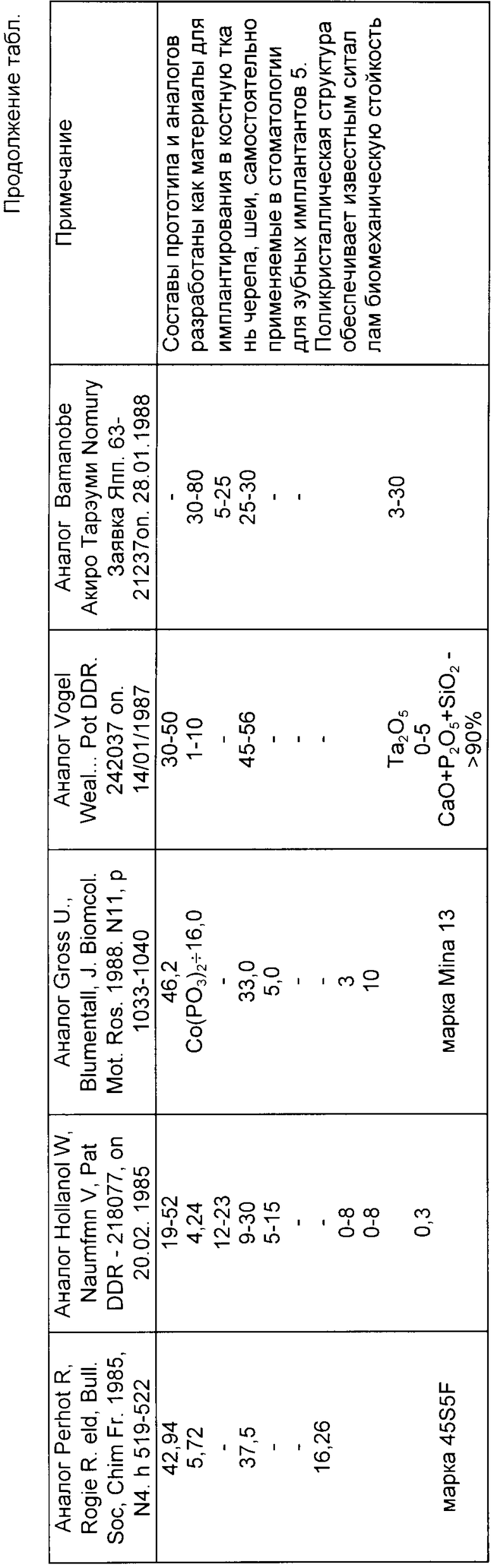
Предлагаемый состав композиции для заполнения костных полостей и дефектов, содержащий биологически инертные компоненты: жидкий силиконовый эластомер СКТН (матрица пасты) и полиэтилгидридсилоксан (отвердитель), отличающийся тем, что в него в качестве функциональных компонентов введены лекарственные средства, коллаген и остеосовместимый биоситалл М-31, содержащий в качестве единственной кристаллической фазы - апатит (даллит) при следующих концентрационных соотношениях компонентов в мас. %: силиконовый эластомер (СКТНв-2мед) 46 - 23; полиэтилгидридсилоксан (ГКЖ-94) 7 - 5; коллаген А 15 - 23; лекарственные средства 1 - 2; биоситалл М-31 31 - 47, содержащий SiO2 37,2 - 38,5; P2O5 15,5 - 13,2; Al2O3 6,2 - 6,5; CaO 33,5 - 35,0; MgO 3,1 - 1,8; ZnO 4,5 - 5,0. Предлагаемый состав отличается удобством имплантирования (вязкостно-пластичные свойства паст регулируются составом) и временем структурирования (5 - 12 мин), удобным для заполнения дефектов разного вида и объема в эластично-упругом, пористом компакте, прилегает плотно к границам костной ткани и без эксплантации замещается собственной тканью в процессе регенерации через 7 - 10 нед. 1 табл.
Композиция для заполнения костных полостей, содержащая жидкий силиконовый каучук СКТНв и полиэтилгидридсилоксан, отличающаяся тем, что она дополнительно содержит коллаген, антисептик и биоситалл, содержащий SiO2, P2O5, Al2O3, CaO, MgO, ZnO при следующем соотношении компонентов, мас.
Жидкий силиконовый каучук СКТНв 46 23
Полиэтилгидридсилоксан ГКЖ-94 5 7
Коллаген 15 23
Антисептик 1 2
Биоситалл 31 47
содержащий, мас.
SiO2 37,2 38,5
P2O5 15,5 13,2
Al2O3 6,2 6,5
CaO 33,5 35,0
MgO 3,1 1,8
ZnO 4,5 5,0
| Материаловедение в стоматологии | |||
| Под ред | |||
| А.И.Рыбакова , -М.: Медицина, 1984, с | |||
| Способ приготовления хлебного вина | 1925 |
|
SU424A1 |
Авторы
Даты
1998-01-27—Публикация
1992-02-24—Подача