Изобретение относится к медицинской промышленности, в частности к производству человеческого лейкоцитарного интерферона с применением индуктора интерферона.
В производстве человеческого лейкоцитарного интерферона [1] предусматривается использование в качестве вируса-индуктора интерферона вакцинного штамма "H" вируса болезни Ньюкасла (ВБН). Этот штамм используется во многих странах мира, выпускающих человеческий лейкоцитарный интерферон для медицинской и ветеринарной практики или в научных исследованиях. Это наиболее безопасный вирус-индуктор, обладающий индуцирующими свойствами при получении лейкоцитарного интерферона человека или животных.
Известен способ получения вируса-индуктора интерферона [1] путем культивирования штамма "H" вируса болезни Ньюкасла в 9-10 дневных куриных эмбрионах. Заражающая доза вируса составляет 0,2 мл 104 ЦПД/50/ мл. Эта доза вводится в аллантоисную полость эмбриона шприцем с соблюдением условий стерильности. Затем эмбрионы инкубируют в течение 48 ч при (37±0,5)oC. После инкубации эмбрионы охлаждают при 4oC и отсасывают вируссодержащую аллантоисную жидкость, которая после необходимых контролей используется в качестве вируса-индуктора интерферона. Вируссодержащая жидкость должна отвечать следующим требованиям: быть бактериологически стерильной, иметь гемаглютинирующую активность (ГА) 256 ед, инфекционный титр не ниже 108 ЦПД/50 в 1 мл. При использовании этого индуктора в производстве интерферона по регламенту производства человеческого лейкоцитарного интерферона 302-82 получают интерферон с противовирусной активностью 4000-5000 МЕ/мл.
Однако вирус-индуктор, полученный известным способом, обладает цитопатическим действием и пониженной интерферониндуцирующей способностью.
Цель изобретения - снижение цитопатического действия и повышение интерферониндуцирующей способности вирусного индуктора.
С этой целью в способе получения вируса-индуктора интерферона путем введения вируса болезни Ньюкасла, штамм "H", в аллантоисную полость куриных эмбрионов, их последующего инкубирования и отбора вируссодержащей жидкости, вирус вводят в аллантоисную полость куриных эмбрионов в концентрации 107 - 108 ЦПД/50 мл.
Сравнительный анализ существенных признаков известного и предлагаемого способов показывает, что отличительной особенностью последнего является использование для заражения куриных эмбрионов более высокой концентрации вируса, а именно, в концентрации 107 - 108 ЦПД/50 мл. В способе - прототипе эмбрионы заражают вирусом в концентрации 104 ЦПД/50 мл.
При введении в эмбрионы высоких концентраций вируса в аллантоисной полости накапливаются дефектные вирусные частицы, которые характеризуются резким возрастанием ГА до 1000 ед. в 1 мл вируссодержащей аллантоисной жидкости и утратой способности к размножению. Наблюдение было сделано при исследовании вируса гриппа [2].
Использование для индукции интерферона вируса, содержащего дефектные частицы, не способные размножаться в лейкоцитах и угнетать таким образом синтез интерферона, позволяет сохранять лейкоцитам свою жизнеспособность и продукцию интерферона, что отражается на повышении выходов интерферона.
Приведенный анализ свидетельствует, что предлагаемый способ позволяет получить вирус-индуктор с новыми свойствами, которые обеспечивают получение технического результата - более интенсивную индукцию интерферона.
Влияние приведенных отличительных признаков на достижение технического результата не следует из известного уровня знаний и, следовательно, разработанный способ соответствует критериям "новизна" и "изобретательский уровень".
Способ осуществляют следующим образом.
В аллантоисную полость куриного эмбриона вводят с соблюдением условий стерильности 0,1-0,2 мл жидкой вирусной суспензии, содержащей 107 - 108 ЦПД/50 вируса болезни Ньюкасла штамм "H". Затем эмбрионы инкубируют в течение 48 ч при (37±0,5)oC. После инкубации эмбрионы охлаждают при 4oC в течение 18-20 ч и отсасывают аллантоисную жидкость, которую применяют в дальнейшем в качестве вируса-индуктора. Полученный жидкий вирус-индуктор контролируют на стерильность, определяют инфекционный титр и гемагглютинирующую активность.
Пример 1. Берут 9-10-дневные куриные эмбрионы в количестве 100 шт. Скорлупу эмбрионов обрабатывают 3% перекисью водорода. С помощью шприца вводят в аллантоисную полость куриного эмбриона с соблюдением стерильности 0,2 мл жидкой вирусной суспензии, содержащей 107 ЦПД/50 вируса болезни Ньюкасла. Эмбрионы инкубируют в течение 48 ч при 37,5oC. После инкубации эмбрионы охлаждают при 4oC в течение 18-20 ч и затем из эмбрионов отсасывают аллантоисную жидкость, которую в дальнейшем применяют в качестве вируса-индуктора. Получено 400 мл вируссодержащей аллантоисной жидкости. Полученный вирус-индуктор имеет инфекционный титр 108 ЦПД/50 в 1 мл аллантоисной жидкости, гемагглютинирующую активность - 1000 ед, бактериологически стерилен.
Пример 2. Берут 9-10-дневные куриные эмбрионы в количестве 100 шт. Шприцем вводят в аллантоисную полость каждого куриного эмбриона по 0,1 мл жидкой-вирусной суспензии, содержащей 108 ЦПД/50 вируса болезни Ньюкасла. Эмбрионы инкубируют в течение 48 ч при температуре 37,0oC. После инкубации и охлаждения из эмбрионов отсасывают аллантоисную жидкость. Полученный вирус-индуктор в количестве 370 мл имеет инфекционный титр 108 ЦПД/50 в 1 мл аллантоисной жидкости, гемагглютинирующую активность 1500 ед, бактериологически стерилен.
Пример 3. Определение количества вырабатываемого интерферона при использовании полученного по примерам 1, 2 вируса-индуктора.
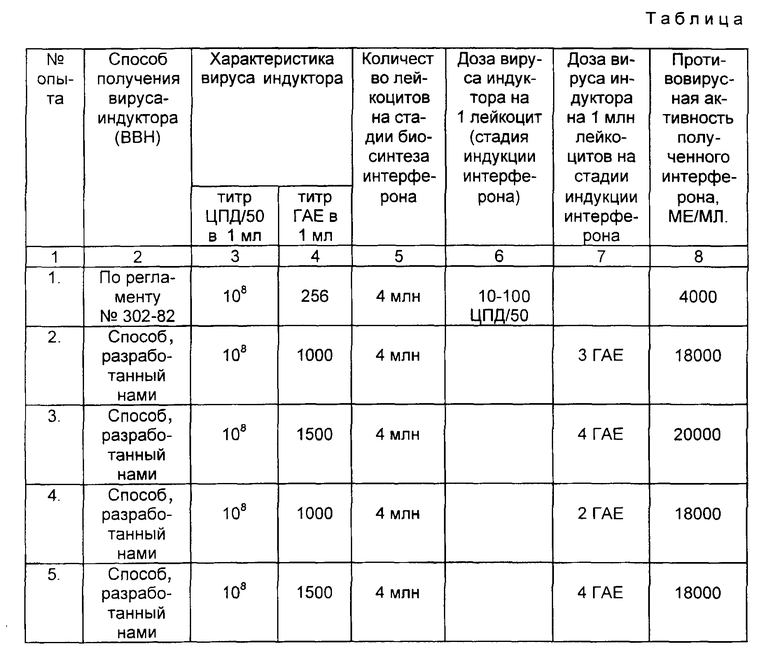
К 3 л питательной среды, содержащей в 1 мл 20 млн лейкоцитов добавляют 1500-3000 МЕ/мл человеческого лейкоцитарного интерферона и 0,0015 ед/мл инсулина и выдерживают суспензию при 37,5oC в течение 2-5 ч (стадия прайминга). Затем в суспензию с лейкоцитами добавляют вирус-индуктора из расчета 2-4 ГАЕ на 1 млн лейкоцитов и суспензию выдерживают 1-2 ч при той же температуре (стадия индукции интерферона). Затем вирус-индуктор удаляют, а осадок лейкоцитов разводят свежей порцией питательной среды 199 с антибиотиками и гепарином из такого расчета, чтобы в 1 мл среды содержалось 4 млн лейкоцитов. В суспензию вводят 5-10% плазмы. Суспензию выдерживают при 37,5oC в течение 18-20 ч. На этом этапе происходит биосинтез интерферона в лейкоцитах и накопление его в питательной среде. После инкубации лейкоциты отделяют центрифугированием, а в надосадочной жидкости определяют активность интерферона. Противовирусная активность полученного интерферона 18000-20000 МЕ/мл (см. таблицу).
Таким образом, разработанный способ позволяет получить вирус-индуктор с повышенной интерферониндуцирующей способностью и не оказывающий цитотоксичного действия на клетки-продуценты интерферона.
Литература
1. Регламент производства человеческого лейкоцитарного интерферона 302-82, 1982.
2. Жданов В.М., Букринская А.Г. Репродукция миксовирусов, Изд. "Медицина", М. 1969, с. 232.
| название | год | авторы | номер документа |
|---|---|---|---|
| ХОЛОДОАДАПТИРОВАННЫЙ ШТАММ "Н" ВИРУСА БОЛЕЗНИ НЬЮКАСЛ, ИСПОЛЬЗУЕМЫЙ В КАЧЕСТВЕ ИНДУКТОРА ИНТЕРФЕРОНА | 1999 |
|
RU2154104C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВИРУСА-ИНДУКТОРА ИНТЕРФЕРОНА | 2000 |
|
RU2175555C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЧЕЛОВЕЧЕСКОГО ЛЕЙКОЦИТАРНОГО ИНТЕРФЕРОНА | 1998 |
|
RU2140284C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЧЕЛОВЕЧЕСКОГО ЛЕЙКОЦИТАРНОГО ИНТЕРФЕРОНА | 1993 |
|
RU2080873C1 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ВИРУСНЫХ ЗАБОЛЕВАНИЙ | 1994 |
|
RU2118163C1 |
| СПОСОБ ИНАКТИВАЦИИ ВИРУСНОЙ КОНТАМИНАЦИИ В ПРЕПАРАТЕ ЧЕЛОВЕЧЕСКОГО ЛЕЙКОЦИТАРНОГО ИНТЕРФЕРОНА | 1994 |
|
RU2080877C1 |
| ПРЕПАРАТ, ОБЛАДАЮЩИЙ ПРОТИВОВИРУСНЫМ И ИММУНОКОРРИГИРУЮЩИМ ДЕЙСТВИЕМ | 2004 |
|
RU2262946C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА "АФФИНОЛЕЙКИН" ДЛЯ ПРОТИВОИНФЕКЦИОННОЙ ИММУНОТЕРАПИИ | 1991 |
|
RU2076715C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИНТЕРФЕРОНА ИЗ ЛЕЙКОЦИТОВ СВИНЬИ | 1992 |
|
RU2057545C1 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК PIF16, КОДИРУЮЩАЯ ЗРЕЛЫЙ ЛЕЙКОЦИТАРНЫЙ ИНТЕРФЕРОН α ЧЕЛОВЕКА, ШТАММ ESCHERICHIA COLI - ПРОДУЦЕНТ ЗРЕЛОГО ЛЕЙКОЦИТАРНОГО ИНТЕРФЕРОНА α ЧЕЛОВЕКА | 1992 |
|
RU2054041C1 |
Изобретение относится к медицинской промышленности и касается получения вируса-индуктора, применяющегося в производстве человеческого лейкоцитарного интерферона. Способ получения вируса-индуктора интерферона проводят путем введения вируса болезни Ньюксала, штамм "Н", который вводят в аллантоисную полость куриных эмбрионов в концентрации 107 - 108 ЦПД/50 мл. Эмбрионы инкубируют в течение 48 ч при температуре /37; ± 0,5/oC, затем охлаждают при 4oC и отсасывают из них аллантоисную жидкость. Полученный вирус-индуктор не оказывает цитопатического действия на лейкоциты и обладает повышенной интерферониндуцирующей способностью. 1 табл.
Способ получения вируса-индуктора интерферона, включающий введение вируса болезни Ньюкасла, штамм Н, в аллантоисную полость куриных эмбрионов с последующим их инкубированием и отбором вируссодержащей аллантоисной жидкости, отличающийся тем, что вирус вводят в аллантоисную полость куриных эмбрионов в концентрации 107 - 108 ЦПД/50/мл.
| Дровопильное устройство | 1921 |
|
SU302A1 |
| Жданов В.М., Букринская А.Г | |||
| Репродукция миксовирусов | |||
| - М.: Медицина, 1969, с.232 | |||
| Руководство по вакционному и сывороточному делу | |||
| Под ред.акад | |||
| Бургасова П.Н | |||
| - М.: Медицина, 1978, с.176. | |||
Авторы
Даты
1998-05-20—Публикация
1994-01-12—Подача