Изобретение относится к новым композициям, к способам доставки биологически активных веществ в кишечник и к способам лечения животных от поражения кишечными патогенами.
Тонкий кишечник животных играет важную роль в абсорбции биологически активных материалов, таких как компоненты переваренной пищи, антибиотики, витамины и т.п.
Биологически активные материалы часто оказываются неустойчивыми к воздействию кислот, а поэтому могут разлагаться или инактивироваться при прохождении через желудок на пути к тонкому кишечнику, где они должны абсорбироваться или оказывать свое биологическое действие.
Ранее предполагалось, что материалы, используемые для энтеросолюбильных покрытий и содержащие кислотостойкие растворимые в щелочи вещества, такие как ацетофталат целлюлозы, предохраняют биологические вещества от разложения при их прохождении через желудок, способствуя тем самым последующему их высвобождению в кишечнике. У молодых животных, например у поросят, прохождение материалов с энтеросолюбильным покрытием через кишечник происходит настолько быстро, что это энтеросолюбильное покрытие не успевает разрушиться, что приводит к экскреции материалов с энтеросолюбильным покрытием либо к высвобождению биологически активных веществ в неподходящих областях кишечника, например в толстой кишке.
Кроме того, биологически активный материал, такой как протеазы, может быть неприятным на вкус и вызывать раздражение и воспаление ротовой полости, а также эзофагит.
Поэтому необходимо, чтобы новые композиции и методы способствовали бы эффективной и приемлемой доставке биологически активного вещества в области тонкого кишечника животных.
В соответствии с одним из своих вариантов, настоящее изобретение относится к композиции, которая включает в себя:
(I) гранулы, содержащие биологически активное вещество в сочетании со слабым основанием и частично покрытые растворимым материалом с пролонгированным высвобождением в кишечном соке;
(II) подкисляющий агент, имеющий pH в растворе 1,5 - 6;
(III) гелеобразующий агент.
В соответствии с другим своим вариантом настоящее изобретение относится к композиции, которая включает в себя подкисленный гель, имеющий pH около 1,5 до около 6; и микрогранулы, содержащие белок в сочетании со слабой кислотой и частично покрытые растворимым материалом, обеспечивающим замедленное высвобождение активного вещества в кишечном соке.
Биологически активным веществом может быть белок, такой как фермент, фактор роста, цитокин или гормон. Если используемый фермент является протеолитическим ферментом, то такой фермент предпочтительно выбирать из бромелина, папаина, фицина, химотрипсина, трипсина, рибонуклеазы, карбоксипептидазы A или B, или субтилизина. Из них наиболее предпочтительным является бромелин. Факторами роста являются гормоны, инсулин, и т.п.
В соответствии с настоящим изобретением под термином "белок" также подразумеваются пептиды. Однако пептид включает в себя от 2 до 100 аминокислот, тогда как белок содержит 100 или более аминокислот.
Биологически активными веществами могут быть вещества небелкового происхождения, например, витамины, кофакторы, ионы металлов, антибиотики и т.п.
Биологически активные вещества могут быть получены в виде микрочастиц, например, в виде порошка.
Термин "слабое основание" означает подщелачивающий агент, такой как дикальцийфосфат, карбонат кальция, бикарбонат кальция, гидроксид алюминия, бикарбонат натрия и т.п. Предпочтительно, если указанное слабое основание является умеренно растворимым. Слабое основание обычно используют в виде микрочастиц, способных растворяться в соответствующей среде, такой как желудочный сок. Если слабое основание и биологически активное вещество используются в виде микрочастиц, то перед покрытием они могут быть смешаны друг с другом.
Гранулы могут быть получены путем частичного покрытия смеси, состоящей из микрочастиц, биологически активных веществ и буферных агентов, материалом пролонгированного высвобождения (известного под названием "энтеросолюбильное покрытие"), растворимым в кишечном соке. Флюидизированные частицы могут быть покрыты раствором из материала пролонгированного высвобождения путем напыления. Размер гранул, полученных в результате покрытия флюидизированных частиц в псевдоожиженном слое путем распыления, может регулироваться и зависит от скорости потока частиц и от давления, под которым подается раствор для покрытия при распылении. Например, быстрый поток гранул и высокое давление распыления приводят к образованию мелких гранул. В основном диаметр гранул составляет 50 - 500 микрон, однако указанный диапазон не должен рассматриваться как ограничение объема настоящего изобретения. Такие гранулы называются микрогранулами.
В соответствии с настоящим изобретением гранулы могут лишь частично покрыты материалом пролонгированного высвобождения. Это является очень важным аспектом настоящего изобретения, поскольку в этом случае предусматривается быстрое высвобождение биологически активного вещества в кишечник. Такое частичное покрытие может быть, в основном, осуществлено путем покрытия распылением псевдоожиженного материала. Степень покрытия может быть определена с помощью микроскопического анализа гранул. В основном материалом пролонгированного высвобождения может быть покрыто 10 - 90 от всей поверхности гранул, а предпочтительно 50 - 80% всей поверхности гранул.
Материалами пролонгированного высвобождения могут быть любые материалы, которые являются в основном непроницаемыми и сохраняют свою целостность при pH ниже 6,0, и которые разлагаются, растворяются, становятся проницаемыми или теряют свою структурную целостность при щелочном pH, то есть при pH около 7,0 и выше. Примерами таких материалов являются ацетофталат целлюлозы или другие типы энтеросолюбильных покрытий.
Подкисляющие агенты могут быть использованы в виде микрочастиц, которые после их солюбилизации в растворе делают этот раствор кислым, то есть раствор с pH около 1,5 до около 6, а предпочтительно от 3,5 до около 6. Любой нетоксичный агент, удовлетворяющий вышеуказанным критериям, входит в объем настоящего изобретения. Примерами подкисляющих агентов являются лимонная кислота, молочная кислота, винная кислота, янтарная кислота, щавелевая кислота, фумаровая кислота, масляная кислота, соляная кислота, пропионовая кислота и т.п.
Гелеобразующие агенты также используются в основном в форме микрочастиц, которые способны образовывать гелевую матрицу в соответствующих условиях, например, в дисперсиях или смесях с водными или органическими растворами (такими как глицерин или полиэтиленгликоль). Примерами гелеобразующих агентов являются карагинаны; альгинаты; поливинилпирролидон (PVP);метилметакрилат, замещенный растворимыми в желчи жирными кислотами; декстран и т.п. Подкисленный гель может быть получен путем гидратации или диспергирования гелевой матрицы в кислотном растворе или в присутствии подкисляющего агента, описанного выше.
В одном из вариантов настоящего изобретения композицию получают в виде микрочастиц, представляющих собой смесь гранул с частицами подкисляющего агента и гелеобразующего агента. В этой форме композиция хорошо сохраняется и легко транспортируется. Перед использованием данной композиции в целях доставки биологически активного вещества в области тонкого кишечника животного, к этой композиции добавляют небольшое количество воды или другого нетоксичного раствора, в результате чего получают подкисленный гель, образующийся вследствие перехода гелеобразующего агента в гель в присутствии подкисляющего агента, микрогранулы которого содержатся в данной композиции. Эту процедуру осуществляют для получения подкисленной гелеобразной композиции, описанной в данной заявке.
Соотношения компонентов (I) - (III) - композиции настоящего изобретения в основном не являются критическими параметрами, однако это отношение может составлять, например, 10:1:1 (по массе). Аналогично отношение биологически активного вещества к буферному агенту не является критическим, но в основном оно может составлять, например, 1:4 (по массе).
Композиция настоящего изобретения может, кроме того, содержать один или несколько антибиотиков. Если в этом варианте настоящего изобретения композиция изготовляется в гранулированной форме, то антибиотик может быть использован в виде порошка или гранул, которые смешивают с другими компонентами. Если, согласно этому варианту настоящего изобретения, композицию изготавливают в виде геля, то один или несколько антибиотиков обычно растворяют в процессе получения гелевой матрицы, в результате чего этот антибиотик (или антибиотики) распределяются по всей гелевой матрице.
В композиции настоящего изобретения могут быть использованы антибиотики любого класса, например, такие как пенициллин, цефалоспорин, эритромицин, тетрациклин, тиенамицин, неомицин и другие соединения, включая производные, обладающие антибиотической активностью.
Как будет показано ниже, очевидно, что указанные антибиотики синергически взаимодействуют с композициями настоящего изобретения (в частности, с композициями, в которых биологически активным материалом является протеаза), в случае, когда они вместе с указанными композициями используются для лечения кишечных бактериальных инфекций, ассоциированных с различными заболеваниями.
В еще одном из своих вариантов настоящее изобретение относится к способу доставки биологически активного вещества в верхний отдел тонкого кишечника животного, заключающемуся во введении этому животному композиции, описанной выше. Если указанная композиция является гелеобразной, то ее непосредственно вводят животному. Если вышеописанная композиция используется в виде гранул, то в этом случае ее сначала диспергируют или смешивают с соответствующим раствором, в результате чего образуется гель, и затем (уже в виде геля) вводят животному.
В другом своем варианте настоящее изобретение относится к способу обработки кишечных патогенов и/или лечения заболеваний, ассоциированных с инфекциями, вызываемыми кишечными патогенами у животных, который заключается в том, что животному перорально вводят терапевтически эффективное количество композиции, определенной выше. Предпочтительно, если указанная композиция содержит протеазу, например, бромелин в сочетании (но, необязательно) с одним или несколькими антибиотиками. В альтернативном варианте осуществления настоящего изобретения один или несколько антибиотиков могут быть введены одновременно или почти одновременно.
Кишечными патогенами, которые могут быть подвергнуты обработке в соответствии с настоящим изобретением, являются бактерии, вирусы или паразиты. Примерами таких патогенов могут служить энтеротоксикогенные бактерии Escherichia coli, шигелла Shigella, Yersinia, Pleisomonas, вибрионы, Aeromonas, кампилобактер (Campylobacter), ротавирусы, криптоспоридии (Cryptosporidia) или кокцидии (Coccidosis).
Кроме того, настоящее изобретение относится к способу лечения диареи у животных, заключающемуся во введении указанному животному композиции, включающей в себя подкисленный гель, имеющий pH 1,5 - 6; причем указанный гель содержит микрогранулы, которые включают в себя протеолитический фермент в сочетании со слабой кислотой и которые частично покрыты материалом пролонгированного высвобождения, растворимым в кишечном соке. Одна композиция может содержать, но, необязательно, один или несколько антибиотиков, либо указанные один или несколько антибиотиков могут быть введены одновременно или почти одновременно с композицией.
Способы настоящего изобретения могут быть использованы для лечения любого животного, предпочтительно млекопитающего, такого как человек, свинья, крупный рогатый скот, лошадь, овца, а также птицы, рыбы или ракообразные. В частности, предпочтительными животными являются моножелудочные, такие как детеныши свиньи или человека, либо неполовозрелое жвачное животное, такое как бычок.
Хотя в различных вариантах своего осуществления настоящее изобретение предпочтительно применяется к моножелудочным и неполовозрелым жвачным животным, однако оно может быть также применено и в водном хозяйстве для лечения кишечных заболеваний у рыб (и ракообразных), которые могут возникать и интенсивно распространяться, например, в прудах, водоемах и т.п. Действие композиций, содержащих протеазы, направлено на удаление участков адгезии патогенов в тонких кишках рыб и ракообразных, а также на повышение системного иммунитета.
Если композиции настоящего изобретения применяются для лечения человека, то они могут быть подмешаны к питью, например, к воде или буферному раствору, имеющему pH от около 4 - 7. Степень покрытия микрогранул, используемых для введения человеку, составляет около 20%.
В соответствии с настоящим изобретением введение подкисленного геля может быть осуществлено любыми стандартными способами. Например, гель может быть влит или инъецирован в ротовую полость животного. Альтернативно указанный гель может быть нанесен на пищу, например, на корм животного, или смешан с нею.
Количество подкисленного геля, вводимого животному в целях добавки биологически активного вещества в области тонкого кишечника животного или в целях лечения диареи, не является решающим фактором, как, впрочем, и частота введения, и зависит от многих факторов, таких как вес и физическое состояние животного, его режим питания, условия обработки и другие факторы, и может быть определено фермером, ветеринаром, или врачом. Например, поросенку в его ротовую полость может быть введено 1-5 мл подкисленного геля и помощью шприца. Аналогично эффективное количество композиции настоящего изобретения может составлять от около 0,01 г/кг веса тела до около 5 г/кг веса тела.
Как было показано авторами настоящей заявки, эффективная доставка биологически активных протеаз в верхние отделы тонкого кишечника животного, обеспечиваемая композициями настоящего изобретения, приводит к деструкции (вероятно, путем протеолиза) кишечных мембранных рецепторов для патогенов (например, рецепторов для патогенной бактерии E. coli K 88) и к деструкции рецепторов токсинов в кишечнике. Композиции настоящего изобретения, содержащие протеазу, способствуют ограничению естественной физиологии организма посредством использования пищеварительных ферментов, благодаря которым происходит временное удаление бактериальных и других рецепторов патогенов со слизистой оболочки тонкого кишечника животного. Без этих рецепторов патогенные организмы не могут образовывать колонии на поверхности выстилки кишки. Поэтому, не имея возможности образовывать большие колонии, патогенные микробы неспособны вызвать заболевание. Такой уникальный способ предупреждения микробных инфекций, который осуществляют путем модификации хозяина, а не патогена, позволяет решить проблемы, связанные с применением традиционных антибиотиков, приводящим в конечном счете к появлению микробов, устойчивых к этим антибиотикам.
Кроме того, было неожиданно обнаружено, что композиции настоящего изобретения являются эффективными против патогенных микробов, которые не обладают известным адгезивным механизмом или рецептором (например, таких как протозойные организмы), а также против вирусов, таких как ротавирусы и вирусы инфекционного гастроэнтерита (TGE). Этот факт свидетельствует о том, что композиции настоящего изобретения, в частности композиции, содержащие протеазы (например, протеазы растительного и животного происхождения, такие как бромометил, папаин, фицин, химотрипсин, рибонуклеаза, субтилизин, карбопептидаза A или B и т.п.) могут действовать как неспецифические иммуностимуляторы. Это иммуностимулирующее действие композиций настоящего изобретения не совсем ясно. Хотя, если иммуностимулирующее действие может быть специфичным для конкретного патогена, то, вероятно, оно может быть неспецифичным и просто способствовать усилению продуцирования IgG.
Использование композиции, содержащей протеазу, в сочетании с антибиотиками дает синергическое действие при лечении кишечных микробных инфекций. Такой синергический эффект может возникать вследствие неспецифического действия композиции, направленного на повышение иммунного ответа с образованием антител и тем самым благоприятствующего противомикробному действию антибиотиков. Также неожиданно было обнаружено, что вышеупомянутые композиции, содержащие протеазу и антибиотик, способствуют повышению системной абсорбции антибиотика из кишечника. Механизм, приводящий к такому эффекту, остается неясным. Указанный эффект наблюдается также при одновременном или почти одновременном введении антибиотиков и композиции настоящего изобретения, изготовленной в виде подкисленного геля.
Композиции настоящего изобретения, содержащие протеазу, также обладают широким спектром противопоносного действия у животных, способствуют увеличению веса и снижению смертности среди животных, в частности, неполовозрелых моножелудочных животных, таких как поросята.
В соответствии с другим своим вариантом настоящее изобретение относится к способу, который не относится к стимуляции иммунной системы животных и который предусматривает пероральное введение животному композиции, состоящей из подкисленного геля, имеющего pH от около 1,5 до около 6 и содержащего микрогранулы, включающие в себя биологически активное вещество, в частности протеазу, в сочетании со слабыми основанием, и частично покрытые материалом пролонгированного высвобождения, растворимым в кишечном соке. Указанная протеаза может быть животного или растительного происхождения и может быть выбрана, например, из таких протеаз, как бромелин, папаин, фицин, химотрипсин, трипсин, рибонуклеаза, карбоксипептидаза A или B, или субтилизин и т.п.
Как будет показано в нижеприведенных примерах, композиции настоящего изобретения, содержащие протеазу, способствуют значительному снижению патогенной флоры кишечника. Это неожиданное явление предоставляет прекрасную возможность для повторного заселения кишечника животного предпочтительными непатогенными бактериями от здоровых животных, такими как молочнокислые бактерии, стрептококки и т.п.
В другом своем варианте, настоящее изобретение относится к способу, включающему в себя стадию перорального введения животному композиции, состоящей из подкисленного геля, имеющего pH от около 1,5 до около 6, и содержащего микрогранулы, которые включают в себя протеазу в сочетании со слабым основанием и которые частично покрыты материалом пролонгированного высвобождения, растворимым в кишечном соке; и последующую стадию перорального введения животному микроорганизмов, которые могут содержать один или несколько компонентов кишечной флоры здорового животного.
Организмы, вводимые животному в соответствии с вышеуказанным вариантом настоящего изобретения, могут быть названы "пробиотиками" и введены одновременно с композицией подкисленного геля, либо немного позднее, то есть через промежуток времени, составляющий от нескольких минут до 24 ч.
Указанные пробиотики могут быть введены в лиофилизованной форме или в любой другой подходящей форме, например, в виде питательного раствора или суспензии микроорганизмов и т.п.
В еще одном своем варианте настоящее изобретение относится к вышеописанной композиции в виде микрогранул или подкисленного геля, которую подмешивают к обычному корму животного, хорошо известному специалистам, например, такому как гранулированный корм.
Отличительные особенности композиций настоящего изобретения и их преимущества обусловлены следующими факторами:
1. Получение гранул небольшого размера, а именно: 50 - 500 микрон (в результате чего они могут быть названы "микрогранулами"), способствует замедлению высвобождения материала в полости рта (защищая тем самым полость рта от воздействия протеаз, таких как бромелин) и в желудке. Небольшой размер частичек облегчает также их прохождение через желудок.
2. Присутствие буферного агента внутри гранул, обеспечивающего pH в пределах 3 - 6, способствует ингибированию протеолитической активности пепсина в желудке, нейтрализации желудочного pH, предохранению от инактивации чувствительного к воздействию кислоты биологического вещества, такого как протеаза, и поддерживанию оптимального pH биологического вещества, такого как протеолитический фермент, например бромелин.
3. Частичное покрытие гранул материалом пролонгированного высвобождения защищает биологическое вещество от инактивации кислотой и способствует постепенному высвобождению биологического вещества в тонком кишечнике, начиная с двенадцатиперстной кишки, а также служит для маскировки неприятного вкуса. Гранулы, полностью покрытые энтеросолюбильным покрытием, не могут высвобождать биологические вещества, особенно, у молодых моножелудочных или жвачных животных, а поэтому эти вещества будут выводиться из организма, либо они будут высвобождаться в неподходящих участках кишечника. Неожиданно было обнаружено, что частичное покрытие гранул материалом пролонгированного высвобождения не вызывает инактивации биологически активных веществ в желудке. Этот факт можно, вероятно, объяснить присутствием буферного агента, описанного выше, в п.2.
4. Подкисляющий агент стимулирует у животного слюноотделение, повышает вкусовые качества композиции, а также снижает желудочный pH, что способствует сохранению целостности материала пролонгированного высвобождения в желудке.
5. Если используемая композиция имеет форму геля, то гелеобразующий агент способствует снижению диффузии вещества из гранул и поддерживает гранулы в легко текучей суспензии. Указанный гель также защищает слизистую оболочку щеки, поскольку он ограничивает диффузию свободного фермента (или другого биологического вещества) из гранул. Благодаря присутствию в геле подкисляющего агента, у животного стимулируется слюноотделение и улучшаются вкусовые ощущения.
Нижеприведенные примеры осуществления настоящего изобретения приводятся лишь в иллюстративных целях и не должны рассматриваться как ограничение изобретения.
Пример 1. Получение композиций.
Были получены следующие композиции, содержащие протеолитический фермент бромелин:
(I) Гранула:
Бромелин - 25 мас.%
Дикальцийфосфат - 65 мас.%
Ацетофталат целлюлозы - 10 мас.% - 100 мас.%
(II) Подкисляющий агент:
Лимонная кислота - 5% по массе гранулы
(III) Гелеобразующий агент:
Карбоксиметилцеллюлоза - 10% по массе гранулы
Способ.
1. 1 кг ацетофталата целлюлозы диспергировали в 10 л воды.
2. К раствору, полученному в стадии I, добавляли достаточное количество карбоната натрия или гидроксида натрия, в результате чего получали натрийсодержащий ацетофталат целлюлозы (натрий-АФЦ) приблизительно при pH 6,5.
3. Бромелин (2,5 кг) и дикальцийфосфат (6,5 кг) взвешивали и загружали в контейнер, находящийся в распылителе для нанесения покрытий GIAtt (торговая марка) или Aeromatic торговая марка. Порошок флюидизировали и нагревали до 50oC.
4. На флюидизированный порошок распыляли найтрий-АФЦ при давлении 2 бар, а после завершения покрытия материал оставляли для осушки на 30 мин.
5. Затем частично покрытый материал смешивали с лимонной кислотой (0,6 кг) и с карбоксиметилцеллюлозой (1 кг), используя стандратный смеситель.
Способ покрытия флюидизированных частиц путем распыления является особенно подходящим для изготовления частично покрытых гранул. Для получения частичного покрытия в отношении (мас./мас.) биологически активного вещества/слабого основания к покрытию, в основном, составляет около 1:0,1 или 1: < 0,1.
В последующих примерах полученную гранулированную композицию обозначали "Detach".
"Дозу" в 5 мл Detach получали путем добавления воды (около 4 мл) к 1 г (объем приблизительно 1 мл) гранул с образованием геля объемом 5 мл.
Пример 2. Определение времени прохождения через кишечник бромелина, введенного в виде разовой дозы 5 мл "Detach", содержащей 1 г гранул, к которым добавляли воду для получения подкисленной гелевой основы.
Восемнадцать 4-недельных поросят, еще не отлученных от матери, и примерно одной массы были произвольно распределены на группы: "Detach" - обработанную группу и необработанную (контрольную) группу в отношении 2:1 (т.е. два поросенка обрабатываемой группы на одного поросенка контрольной группы). Поросятам давали искусственное молоко (500 мл каждому) два раза в день.
В самом начале эксперимента всем поросятам обрабатываемой группы перорально вводили стандартную 5 мл-дозу "Detach" (т.е. суспензии, содержащей 1 г гранул, растворенных в воде в целях получения кислой гелеобразной основы). Через 1 ч, 12 ч, 28 ч, 48 ч 72 ч и 144 ч после инокуляции, произвольно отобранные группы из трех поросят (два обработанных поросенка и один контрольный) умерщвляли с помощью большой дозы барбитурата и удаляли у них тонкую кишку. Делали срезы из 5 участков тонкого кишечника, а именно: двенадцатиперстной кишки, нижней подвздошной кишки, среднего отдела тощей кишки, и из участков, расположенных посередине между указанными участками; после чего эти срезы сразу помещали на хранение при -20oC.
После завершения эксперимента срезы тонкой кишки от каждого поросенка оттаивали, вскрывали путем продольного рассечения и соскребали слизистую оболочку предметным стеклом. Эти соскобы (0,2 г) суспендировали в 1,8 мл буфера для серийного разведения (WDB), состоящего из фосфатно-буферного раствора (PBS, 0,1 М, pH 7,2), к которому были добавлены Твин 30 (0,05% об./об. ), альбумин бычьей сыворотки (BSA, 0,25% мас./об.), этилендиаминтетрауксусная кислота (ЭДТК < 1 мМ) и азид натрия (0,1% мас./об.). Затем суспензию соскобов анализировали на присутствие бромелина с помощью иммуноферментного анализа (ИФА, процедура 1 описана ниже). Чувствительность этого анализа была установлена предварительно (как 2 нг) путем титрования той же самой партии фермента, что присутствовала в "Detach", но суспендированной в фосфатно-солевом буфере.
Остаточный бромелин из Detach-доз был обнаружен во всех участках тонкой кишки обработанных поросят, умерщвленных через 1 и 12 ч после введения дозы. Был также обнаружен бромелаин у одного поросенка (лишь в участках 4 и 5), умерщвленного через 28 ч после введения дозы. Ни один из кишечных соскобов, взятых от контрольных поросят, не обнаруживал реакции в ИФА; такой реакции также не обнаруживал ни один материал, полученный от поросят, умерщвленных через 48 ч или более после введения дозы.
Результаты.
Время прохождения бромелина через тонкий кишечник поросят является таким же, как и время прохождения других пищевых продуктов. Бромелин легко высвобождался в тонкий кишечник.
Процедура 1.
Иммуноферментный анализ на присутствие бромелина.
Планшеты: Nunc (Торговая марка).
Сенсибилизация планшета: в этих целях получали иммуноглобулины (IgG), продуцированные против бромелина в кроликах. Для покрытия (2ч/37oC) разводили в карбоната: бикарбонатном буфере (0,05 М, pH 9,6), содержащем 10 мкг/мл IgG (100 мкл на лунку). До использования хранили при 4oC.
Образцы для испытаний: кишечные соскобы разводили (1:10 мас./об.) в буфере для серийных разведений (WDB), описанном выше. Затем инкубировали 30 мин при 37oC.
Конъюгат: авидин-уреазу (Allilix Inc. , Mississaugu, Торонто, Канада) разводили (1:4100 об./об.) в буфере для конъюгирования (Chandler, D.S. и др. , Vet Mecrobiol. 11: 153-161, 1986). Инкубировали 30 мин при 37oC.
Субстрат: раствор уреазного субстрата (CSL; Parkville). Считывали при 540 нм (приближенные значения).
Пример 3. Влияние Detach на активность кишечного рецептора К88.
Рецептор E.coli К88 является одним из характерных протеиновых или гликопротеиновых рецепторов, которые играют важную роль в патогенезе серьезных микробиологических нарушений в тонком кишечнике. Было показано, что рецепторы, расположенные на мембране щеточной каемки эпителия тонкой кишки, участвуют в прикреплении (колонизации) кишечных патогенов и способствуют внедрению в клетку и доставке токсинов. Было проиллюстрировано также, что некоторые из этих рецепторов, включая рецепторы К88, легко инактивируются протеолитическими ферментами, например протеазами, которые обычно являются активными в тонком кишечнике (WellWood R., Biochmim. Biophys. Acta 632: 326-335, 1980; StAley T.E. и Wins on, J.B. Mol. Cell. Biochemn. 52: 177-1889, 1983; Mouricourt, M.A. и Julien R.A., Infect. Immun, 55: 1216-1233, 1987).
Через 7-14 дней после рождения поросят накладывали фистулы с помощью "У"-образного приспособления из нержавеющей стали.
На морды поросят надевали плоские приспособления для скорейшего отъема от матери и выкармливали восстановленным молоком до тех пор, пока поросята не достигнут по крайней мере 4-недельного возраста.
Активность рецептора К88 оценивали с помощью иммуноанализа (Chandler 1985, Supra, обозначаемого далее KPEIA). Кишечные образцы собирали по крайней мере в 10% об./об. WDB, к которому добавляли 0,1% мас./об. TI. Этот буфер обозначали WDB/TI.
При этом использовали непрерывную процедуру взятия образцов. Эта процедура заключалась в том, что тефлоновую трубку (с внутренним диаметром 4 мм) соединяли с винтовым концом фистулы, а другой конец трубки пропускали через перистальтический насос, работающий на низкой скорости (0,5-1,0 мл/мин) и соединяли со сборником образцов. Эти пробирки, содержащие 1 мл WDB/TI, помещали в коллектор фракций, который обычно используют в колоночной хроматографии для перманентного контроля в области химии белков (Frac 100, Pharmacia). В начале каждого дня испытаний в резервуар в виде чана, окружающий стойку с пробирками, помещали лед. Каждая пробирка осуществляла сбор на выходе из насоса в течение 10 мин. Для снижения количества материала на фистуле во время сбора образцов, на трубку, находящуюся между свиньей и насосом, положенную на опору, подвешивали уравновешивающую гирю.
Обработка композицией "Detach".
Для получения базовой рецепторной активности у поросят брали пробы за 24-28 ч до проведения лекарственной терапии с использованием "Detach". Затем поросят обрабатывали 5 мл-дозой Detach-суспензии (содержащей 1 г гранул) за 30 мин до утреннего кормления. Затем проводили непрерывный сбор образцов в течение последующих 48-72 ч.
Результаты.
В течение трехдневных периодов непосредственно до и после введения лекарственного средства было собрано около 1000 образцов. При этом поросят выдерживали на молочной диете. Гораздо больше образцов было собрано в промежуточные периоды, когда был выявлен более четкий, но, в основном, равномерный характер рецепторной активности.
Результаты сбора образцов, осуществляемого в периоды времени непосредственно до и после Detach-терапии поросят, у которых проводили непрерывный сбор проб, показаны в табл. 1. Наблюдалось снижение рцепторной активности после лекарственной обработки, и это снижение подтверждалось односторонним анализом (с дисперсией в пределах статистической значимости (P = 0,05), проведенным в период 0-1 и 1-2 дня после введения лекарственной дозы. Эти данные подтверждают предварительные наблюдения относительно разрушительного воздействия бромелина на связывание между различными колониями (включая К88) и токсинами, и их кишечными рецепторами в in vitro-экспериментах. Полученные результаты также подтверждают высказанную ранее гипотезу, что бромелин, который высвобождается в кишечник благодаря продемонстрированным свойствам композиции "Detach", оказывает разрушающее действие на рецепторы патогенов, предупреждая тем самым возникновение ряда кишечных инфекций. Величины, показанные в табл. 1, представляют собой средние значения оптической плотности (А540) +/- стандартное отклонение. Число проб, взятых в течение каждого периода времени, показано в скобках, ниже указанных средних значений.
Пример 4. Профилактические меры по борьбе с диареей в течение длительного периода времени (6 дней жизни до отъема примерно на 21 день).
Для демонстрации эффективности Detach-обработки в целях предупреждения диареи у поросят был проведен ряд экспериментов в естественных условиях. Эти эксперименты показали, что Detach-обработка с использованием разовой пероральной дозы является хорошей профилактической мерой для предупреждения диареи у поросят после отъема (которая обычно ассоциируется с патогенами К88 + E.coli). Кроме того, было обнаружено, что терапевтическая Detach-обработка является эффективной мерой (также в виде разовой пероральной дозы) для борьбы против диареи у поросят до их отъема (сосунки). Понос у поросят до их отъема у матери обычно ассоциируется с ротавирусной или кокцидальной инфекцией, и проявляется обычно у поросят в возрасте 1 недели и продолжается в течение 1-3 недель в виде хронического пастеобразного поноса. Несмотря на более хроническую природу этих заболеваний, одноразовая доза Detach, вводимая поросятам в том возрасте, когда у них обычно начинаются симптомы диареи, способствовала предупреждению у них этого заболевания.
Методы.
Эксперименты проводили на ферме в центрально-западной части штата Виктория в Австралии, которая представляет собой коммерческое хозяйство по разведению животных.
Альтернативно молодых племенных свинок и свиноматок распределяли на Detach-обрабатываемые группы и контрольные группы.
В этом испытании было использовано всего 30 пометов поросят: 15 в обрабатываемой группе и 15 в контрольной группе. Поросят выкармливали одновременно до трехдневного возраста, после чего каждый приплод взвешивали.
Detach-обрабатываемой группе поросят вводили разовую (5 мл) пероральную дозу Detach на 6 день. Контрольной группе Detach не вводили.
Затем поросят снова взвешивали в день отъема и переноса в условия аккодомации к отъему.
До отъема поросят регистрировали случаи возникновения диареи, режим обработки и смертность.
Измеряли также прирост массы и смертность для конкретного режима обработки.
Результаты.
Данные, полученные до отъема поросят, представлены в табл. 2.
Значимость полученных результатов вычисляли с помощью анализа дисперсии ковариантов (если они имелись) по параметрам "поросята-помет" и "вес на день 3". Возрасты при отъеме были в основном одинаковыми и выбирались, исходя из практики содержания животных, а не исходя из продуктивности свиньи. Однако критерии по другим параметрам дали высокозначимые результаты, которые показали снижение заболеваемости на 82%.
Этот эксперимент ярко продемонстрировал эффективность разовой дозы Detach для предупреждения поноса у поросят до отъема. Все релевантые критерии показали высокозначимый положительный результат обработки. Прирост в весе поросят-отъемышей составлял 2 кг, а заболеваемость у обработанных поросят снижалась на 80%. Поскольку гибели животных не наблюдалось, то сравнение по этому параметру было сделать невозможно.
Несмотря на фармакологически кратковременное действие Detach, оказалось, что ранняя доза этой композиции, введенная до отъема поросят, имеет стойкое воздействие.
Как показал этот эксперимент, что, если только нет клинических или экспериментальных данных о наличии поноса у поросят до их отъема, то предпочтительной схемой обработки композицией Detach является введение ее разовой дозы поросятам до их отъема от матери. Эффективность Detach-обработки для предупреждения поноса у поросят до отъема совершенно очевидна.
Для оценки эффективности Detach-обработки в целях предупреждения поноса у поросят до отъема (сосунков) было проведено еще пять экспериментов (данные не приведены). В этих экспериментах поросятам через 5 дней после рождения была перорально (с использованием шприца) введена 5 мл-доза Detach (как в примере 1). Эти эксперименты со всей очевидностью продемонстрировали снижение заболеваемости поносом у поросят-сосунков, а также успешное лечение поносов у поросят после отъема. Поросята, обработанные Detach, также обнаруживали прирост в весе, улучшение общего состояния и снижение заболеваемости в целом.
Гистологические анализы ряда контрольных и обработанных поросят показали, что значительное число поросят были ротавирус-положительными, а в образцах, взятых после смерти, были обнаружены кокцидии. В противоположность этому у Detach-обработанных поросят указанных инфекций обнаружено не было.
Для определения эффективности и Detach в предупреждении поноса у отъемышей был проведен ряд дополнительных экспериментов. Всего в этих испытаниях участвовало 1705 поросят, из которых 502 использовали как негативный контроль, 100 - как позитивный контроль, 503 поросят вводили 1 г Detach в виде геля (как в примере 1), а 600 поросятам проводили альтернативные съемы обработки. Эти исследования со всей очевидностью проиллюстрировали эффективность Detach. Ни один поросенок, которому вводили разовую дозу Detach, не погиб от поноса, вызываемого E.coli. По сравнению с 16 контрольными или обработанными антибиотиком поросятами, погибшими от поноса, из Detach-обработанных поросят погибли только 2. Кроме того, Detach-композиция является высокоэффективной в снижении смертности поросят при данной обработке. По-видимому, наиболее значительные результаты описанных экспериментов заключались в том, что композиция Detach позволяет в три раза снизить количество вводимых лекарственных средств, необходимых для традиционного лечения поноса у поросят-отъемышей.
Пример 5. Роль энтеротеротоксикогенной бактерии Escherichia coli (ETEC) как важного этиологического фактора при возникновении диареи у человека была хорошо описана в литературе (Sussman M., The Virulence of E.coli, Reviews of Method. Soc. Gen. Micro., 1985). Эти микроорганизмы отличаются своей способностью продуцировать как один, так и оба - термостойкий (LT) энтеротоксин и неустойчивый к воздействию тепла (LT) энтеротксин (Gaastra, W. и de Graaf, F. K. , Micro. Rev. 46: 129-161, 1982). Некоторые штаммы этих бактерий также продуцируют антигенные факторы колонизации (CFA) или пили, позволяющие ETEC-штаммам "приклеиваться" к слизистой оболочке кишки. Эти пили облегчают колонизацию и позволяют доставлять энтеротоксины, вырабатываемые указанными микроорганизмами, непосредственно к эпителиальным клеткам-мишеням (Gaastra и др., см. выше).
В этом эксперименте описана модель RITARD Spira и др. (Infect, Immun. 32: 739-747, 1981), которую использовали для испытания эффективности in vivo Detach-композиции примера 1 в ингибировании связывания CFA/12-положительных E.coli со слизистой оболочкой кишечника кролика.
Материалы и методы.
Животные: в эксперименте использовали новозеландских белых племенных кроликов обоих полов, полученных от одного производителя. Вес кроликов составлял 1,5 - 2,7 кг.
Бактерии: используемые в этом эксперименте штаммы ETEC были первоначально выделены от пациентов с диареей, проживающих в Бангладеш. Штамм H10407p был легко получен D.C.Evans (Хьюстон, Техас) (Infect. Immun. 19: 727-736, 1978). Штамм E13392/75 7A (серотип 06:K15:H16) был получен B. Rowe (Лондон, Великобритания). Штамм 110407 продуцирует как ST-, так и LT-токсины, и обладает антигеном факторов колонизации (CFA/1). Штамм H10407p продуцирует как ST-, так и LT-токсин, однако он не продуцирует CFA/1. Штамм E1392/75 7A не имеет пилей и является нетоксикогенным спонтанным лабораторным производным CFA/II ± E.coli 1392 (Sack R.B. и др., Infect. Immun. 56: 378-3974, 1988), причем было установлено, что этот штамм неспособен к колонизации и не способен индуцировать диарею в RITARD-модели (Wanke, C.A и др., Infect. Immun 55: 1924-1926, 1987).
Штаммы инокулировали в CFA-агар (Evans, см. выше) и культивировали в течение ночи при 37oC. Затем бактерии собирали, промывали в стерильном фосфатно-солевом буферном растворе (0,01 М, pH 7,2; PBS) и разводили до нужной оптической плотности. Бактериальную концентрацию также определяли путем подсчета жизнеспособных клеток на чашках (в дубликате) с кровяным агаром после серийного разведения в PBS. Все культуры анализировали на CFA/1- и LT-процудирование с помощью специфического иммуноферментного анализа (ИФА) до инокуляции кроликов.
Модель RITARD.
В данном эксперименте использовали модель RITARD, разработанную Sprira и др. (см. выше), но с небольшой модификацией, описанной ниже. До контрольного заражения половине кроликов от каждой группы (табл. 1) вводили пероральные дозы 0,42 г гранулированной композиции примера 1, под названием Detach, и этих кроликов держали на голодной диете 18 ч (но, при этом воду давали ad libitum).
Наблюдение за развитием заболевания.
В течение 24 ч после контрольного заражения, кроликов ежечасно контролировали на диарею, слабость или смертность. При анализе на диарею всех кроликов распределяли по категориям в соответствии со следующей шкалой оценок: 0 - диарея отсутствует; 1 - легкая диарея с испражнениями более жидкими, чем нормальный кал; 2 - умеренная диарея по крайней мере с тремя водянистыми испражнениями; 3 - тяжелая диарея с частыми водянистыми испражнениями. При отхождении кала у кроликов собирали фекальные пробы, а в том случае, если отхождение кала не было, то брали ректальные пробы. Штаммы контрольного заражения идентифицировали с помощью форфологического анализа путем сравнения с типичными колониями E.coli и с помощью ИФА.
Сбор образцов тканей.
Через 24 ч после контрольного заражения всех животных умерщвляли и исследовали жидкость, находящуюся внутри тонкой кишки. Путем исследования больших объемов жидкости, взятой из тонкой кишки (> 60 мл) эутанизированных или погибших кроликов, было установлено, что диарея является главной причиной гибели животных. Были получены срезы (2 • 3 см) тонкой кишки из пяти различных участков, а именно: из двенадцатиперстной кишки (S1); проксимальной области тощей кишки (S2); срединной области тощей кишки (S3); дистальной области тощей кишки (S4); из подвздошной кишки (S5). Каждый сегмент был вскрыт путем продольного разреза и тщательно промыт в стерильном PBS для определения прочно связывающихся бактерий; либо был оставлен непромытым для определения полного числа присутствующих бактерий. Количественные культуры получали путем гомогенизации ткани в течение 1 мин с использованием гомогенизатора SorvaII на полной скорости. Серийные разведения проводили в PBS и 25 мкл-аликвоты культивировали на кровяном агаре и CFA-агаре. После 187-часового инкубирования при 37oC определяли число бактерий на 1 см ткани. Другие образцы были сразу обработаны путем фиксации в 10% нейтральном забуфференном формалине для использования в гистологическом анализе. После того как образцы были залиты в парафин, проводили окрашивание гематоксилин-эозином и окрашивание тканей по Граму.
Статистические анализы.
Результаты бактериального подсчета преобразовывали в логарифмические величины для стабилизации дисперсий и анализировали с использованием Genstat 5. Эффективность Detach-защиты определяли в соответствии с программой Fortran-Finney, которая используется для определения эффективности (%) в хемотерапевтических тестах (Finney D.J., Statisti cal Method in Biology cal Assay, Pub. Charles Griffin and Cvompany Ltd., 1952).
Результаты.
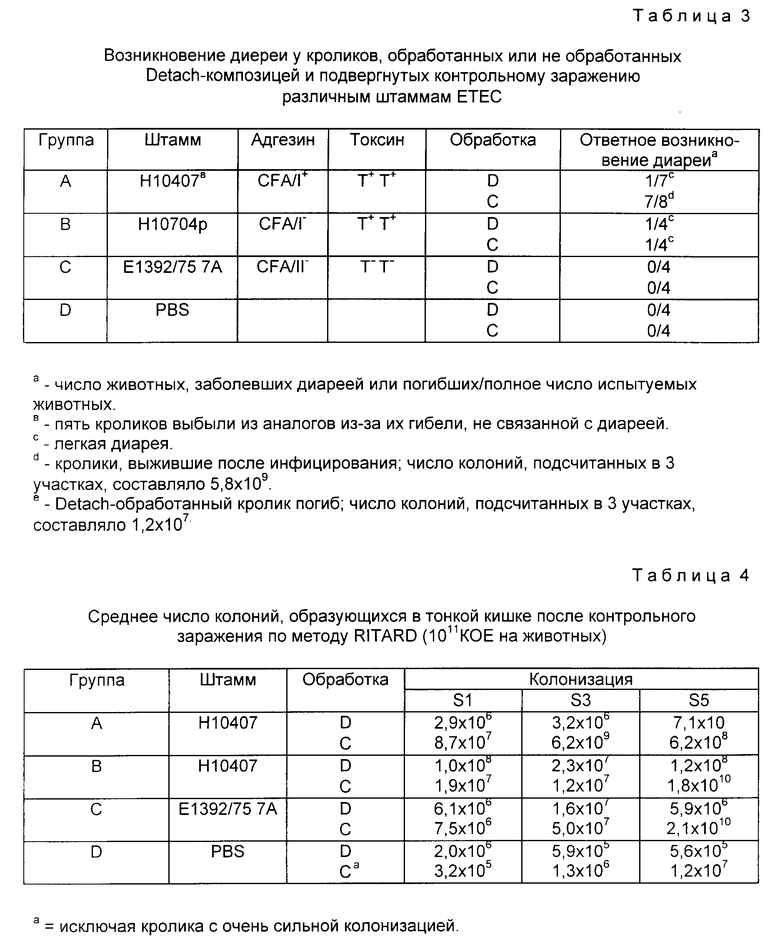
Группам кроликов вводили 1 • 1011 бактерий различных штаммов E.coli и стерильный PBS; в течение 24-часового инкубационного периода наблюдали реакцию продуцирования диареи. Полученные результаты представлены в табл. 3. В целях введения энтеротоксикогенного штамма, содержащего пили (H10407); лишь энтеротоксикогенного штамма (H10407p) и нетоксикогенного, и не имеющего пилей штамма (E1392/75/7A) отбирали различные комбинации энтеротоксинов и факторов колонизации E.coli. Для наблюдения за результатами операции и Detach-обработки без контрольного заражения бактериями использовали PBS-контроль.
Ни один из кроликов, обработанных 10 миллилитрами стерильного PBS, не заболел диареей. Аналогично ни один из кроликов, подвергнутых контрольному заражению не имеющими пилей штаммами H10407p и E1392/75/7A, не заболел диареей. При аутопсии объемы жидкостей в тонком кишечнике от привратникового сфинктера до места соединения подвздошной и слепой кишки составляли 10 - 50 мл.
Из восьми контрольных (не обработанных Detach) кроликов, подвергнутых провокационному заражению штаммов H10407, семь погибали или имели обильный водянистый понос. При аутопсии объем жидкости в их тонком кишечнике составлял 20 - 105 мл. Однако полный объем жидкости в малой и большой кишках составлял 130 - 165 мл (по сравнению с 10-50 миллилитрами у кроликов, инокулированных штаммами E13923/75 7A и H10407p и PBS).
Из кроликов, которые до H10407-заражения были обработаны композицией Detach, погиб лишь один. Этот кролик погиб через 11 ч после контрольного заражения с отхождением частых жидких испражнений. Из остальных шести кроликов, обработанных композицией Detach, ни один не имел поноса, а большинство (4 из 6) имели фекалии нормальной формы с отхождением кала через 24 ч. При аутопсии содержимое толстой кишки было твердым, а накопление жидкости в тонкой кишке составляло 12 - 60 мл.
Бактериальная адгезия.
В целях исследования адгезии бактерий контрольного заражения в различных участках тонкого кишечника от всех животных получали культуры для количественного анализа. Все образцы промывали стерильным PBS и определяли число бактерий, прикрепившихся к слизистой оболочке кишки. Присутствие бактерий контрольного заражения наблюдалось во всех участках; причем наиболее обильная колонизация обнаруживалась для CFA/1+-штамма H10407. Средние результаты, полученные для культур CFA/1+-бактерий в различных участках кишки не обработанных Detach кроликов, варьировались от более низких значений при S1, S2, S4 и S5 (8,7 • 107, 6,2 • 107, 1,04 • 108 и 6,2 • 108 колониеобразующих единиц (КОЕ) (см. соответственно) до постоянно более высоких значений при S3 (6,2 • 109). Эти результаты показаны в табл. 4. В последующих анализах для сравнения были использованы культуры бактерий из S3.
Число CFA/1+-бактерий, прикрепленных к слизистой оболочке кишечника Detach-обработанных кроликов, варьировалось от 1,3 • 104 (минимальное количество) до 1,2 • 107 КОЕ/см (в среднем 2,6 • 106 КОЕ/см). Это число КОЕ/см в 2000 раз меньше, чем величина КОЕ/см для контрольных кроликов, зараженных тем же самым штаммом (p < 0,05). В табл. 4 проиллюстрировано различие в числе колоний для Detach-обоработанных и необработанных животных.
Из эксперимента, описанного в этом примере, видно, что Detach-препараты значительно уменьшают кишечную флору. Очевидно также, что обедняемая микрофлора относится к патогенным микроорганизмам. Поэтому эти микроорганизмы могут быть заменены предпочтительными микроорганизмами, например, происходящими от здоровых животных. Примерами таких микроорганизмов могут служить так называемые "пробиотики", такие как стрептококки и молочнокислые бактерии.
Число бактерий, связанных со слизистой тонкого кишечника кроликов, инфицированных CFA/1--H10407p, варьируется от 1,3 • 104 КОЕ/см (минимальное количество) до 6,6 • 107 КОЕ/см для кроликов с легкой диареей (в среднем 1,6 • 107 КОЕ/см). Колонизация CFA/11- происходит на аналогичном уровне, т.е. число колоний (КОЕ/см) составляет от 1,3 • 104 (минимальное число) до 1,3 • 108, а в среднем равно 3,9 • 107. Таким образом, не наблюдалось значительного различия в числе бактериальных колоний для Detach-обработанных и необработанных животных, подверженных контрольному заражению любым штаммом, не содержащим пилей.
У кроликов, которые получали лишь PBS, в тонкой кишке присутствовало относительно небольшое количество бактерий (в среднем равно 1,3 • 104 КОЕ/см).
Выделение бактерий с фекалиями.
От кроликов, у которых было отхождение кала, получали мазки. У всех животных, подвергнутых контрольному заражению, в фекалиях обнаруживались бактерии. При аутопсии были взяты ректальные мазки. Присутствие в прямой кишке штамма контрольного заражения наблюдалось у всех кроликов, включая тех, у которых не было отхождения кала до окончания эксперимента. Во всех случаях 100% культивированных колоний были от штамма контрольного заражения.
Гистология.
При гистологическом исследовании под оптическим микроскопом тканей тонкой кишки, полученных от всех кроликов, не было обнаружено каких-либо аномалий слизистой оболочки. Тот факт, что микроорганизмы лишь изредка обнаруживаются на слизистой оболочке, позволяет предположить, что бактерии прикрепляются в определенных участках, а не по всей кишке.
Обсуждение.
Известно, что имеется большое сходство между механизмами патогенеза ETEC-инфекций человека и животных. Большинство штаммов ETEC, происходящих от человека и животных, используют для своей адгезии пили и после адгезии образуют колонии в тонкой кишке. Как у человека, так и у животных, диарея возникает в результате продуцирования и эффективной доставки энтеротоксинов, вырабатываемых этими бактериями, к тканям кишечника.
В данном эксперименте было показано, что пероральное введение Detach, то есть препарата, содержащего протеазу, позволило успешно снизить заболеваемость диареей и смертность от диареи (на 86%, 6 из 7) у кроликов, инфицированных CFA/1-положительным штаммом H10407 87% (7 из 8) контрольных кроликов, не получивших Detach, погибали от диареи или страдали тяжелой диареей.
Ранее Wanke и др. (см. выше) сообщали, что пороговое значение для появления клинических симптомов инфекционной диареи составляет 108 КОЕ на 1 см площади тонкого кишечника. В этом эксперименте кролики, подвергнутые контрольному заражению бактериальными штаммами, о которых известно, что они не обладают факторами колонизации, не заболевали диареей, а уровень колонизации бактерий у них был ниже порогового значения 107. У этих кроликов не наблюдалось различия в уровнях колонизации между различными группами обработки. Альтернативно у Detach-необработанных кроликов, подвергнутых контрольному заражению штаммом H10407, обладающим пилями, уровень бактериальной колонизации составлял значительно выше 107 (в среднем равен 6,2 • 109). УК Detach-обработанных кроликов, подверженных контрольному заражению тем же самым бактериальным штаммом, наблюдалась колонизация лишь на уровнях, аналогичных уровням, наблюдавшимся для бактерий, которые, как известно, не обладают CFA (в среднем = 2,6 • 106). В соответствии с вышеуказанным, очевидно, что пероральная Detach-обработка способствует эффективной модификации поверхности слизистой оболочки тонкого кишечника кролика таким образом, что колонизация CFA/1+-бактерий значительно снижается (p < 0,05).
Результаты, полученные для кроликов, могут быть вполне полезны и для человека, поскольку между ETEC-патогенными инфекциями у человека и животных имеется большое сходство. Действительно, кролики представляют собой стандартную модель для исследования бактериальных инфекций у человека.
Лечение человека с использованием Detach-препартаов может служить защитой, например, от заболеваний, вызываемых энтеротоксикогенными Escherichia coli. Такая защита может быть обусловлена, например, деградацией/модификацией кишечных рецепторов для вирулентных детерминант ETEC человека, вызывающих диарею, таких как антигены факторов колонизации CFA/1, CFA/II, CFA/II и CFA/IV.
Эксперименты, проведенные заявителем (данные не приводятся), показали, что обработка тонкой кишки человека протеазой (папаином) приводит к значительному снижению бактериальной адгезии энтеротоксиногенной бактерии Escherichia coli, а в частности, к снижению связывания CFA/I и энтеротоксина с кишечными препаратами и полному ингибированию связывания CFA/II. Эти данные показали, что Detach-препараты должны быть эффективными при введении in vivo человеку в целях предупреждения заболеваний, вызываемых энтеротоксикогенными E. coli.
Пример 6. Повышение уровней глобулина после обработки Detach-композицией.
Этот эксперимент был разработан для моделирования физиологии человека с использованием модели свиньи в целях определения влияния больших доз Detach (> 1 г) на биохимические параметры сыворотки. Для исследования изменения в сывороточных уровнях глобулина были использованы 10-кратные дозы.
Эксперимент.
Для эксперимента использовали 15 свиней в возрасте 10-16 недель.
Группа A - 8 необработанных свиней.
Группа E - 7 свиньям вводили Detach (10 г) 3 раза в день в течение 2 или 5 дней.
Для обеих групп биохимические параметры сыворотки, взятой до обработки и после обработки, сравнивали в целях выявления воздействия обработки.
Результаты.
Полученные результаты показали значительное увеличение (p = 0,043) уровней глобулина в сыворотке у свиней, которые были обработаны большими дозами Detach. Более низкие дозы Detach (10 г) не дали значительных изменений (данные не приводятся).
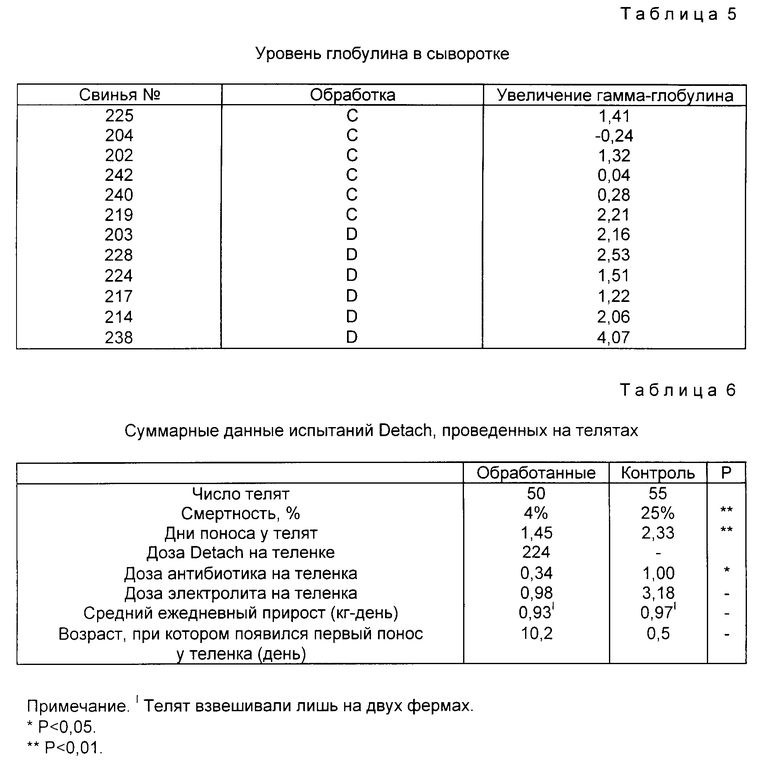
Уровни глобулина были исследованы дополнительно. Уровни альфа-, бета- и гамма-глобулина были проанализированы посредством электрофореза с использованием ацетата целлюлозы и количественно оценены с помощью денситометра. Результаты представлены в табл. 5.
В среднем увеличение уровня гамма-глобулина составило 170%. Относительно уровней альфа- и бета-глобулина трудно сделать какие-либо определенные выводы, поскольку эти уровни варьировались от образца к образцу. Однако наблюдалось постоянное увеличение уровней гамма-глобулина.
Изменения уровней гамма-глобулина от уровней до обработки и до уровней после обработки для двух указанных групп были проанализированы путем оценки дисперсии данных. В результате этой оценки было установлено, что полученное увеличение уровней является статистически значимым (P = 0,03, 0-99,5%). Кроме того, была определена антигенная специфичность (и класс антитела) гамма-глобулинов.
Полученные результаты показали увеличение уровней гамма-глобулина в сыворотке, которое могло иметь место за счет уровней неспецифического гамма-глобулина, возрастающих после введения Detach-комбинации. Повышение уровней IgG в сыворотке может также иметь важное значение для защитных свойств слизистой оболочки кишечника. Эти выводы могут служить объяснением для широкого спектра противомикробного действия Detach-комбинации, которая как было установлено, является эффективной против бактериальной, вирусной и протозойной инфекций.
Пример 7. Предупреждение поносов у телят.
Для оценки эффективности композиции Detach в предупреждении поносов у телят проводили испытания на ферме близ Warragul в штате Виктория. Эти испытания проводили в конце периода весеннего отдела в Gippuland, где главным микроорганизмом, выделенным от зараженных животных, в течение нескольких последних лет был Cryptosporidia.
Испытания проводили на шести молочных фермах. На всех этих фермах фермеры в течение многих лет имели убытки в результате высокой заболеваемости животных, вызываемой этим микроорганизмом.
Материалы.
Композиция "Detach" в соответствии с примером 1.
Доза: 35 мл в виде геля.
Метод. Дозу Detach, составляющую 35 мл, повторно вводили (если это было необходимо) примерно через интервалы времени 3-4 дня. Всего каждому теленку вводили не более пяти доз.
Вообще в естественных условиях у телят возникает понос в основном в возрасте от 1 до 4 недель. Обычно на 28 день телят удаляют из бокса для выращивания молодняка в загон для телят, поскольку к этому возрасту телята становятся менее восприимчивыми к заболеваниям. Регистрировались дни заболевания поносом, дозы вводимых антибиотиков и электролитов. Кроме того, регистрировались даты гибели животных с указанием причины гибели, если таковая была известна. Образцы кала посылались в лабораторию для анализа. С ферм, на которых имели место случае гибели животных, также посылали для анализа образцы кишечного содержимого.
Для того, чтобы определить имеются ли значительные различия в степени роста между двумя группами, телят на двух фермах взвешивали в конце испытаний. При этом никакой разницы в степени роста между этими группами обнаружено не было.
Данные относительно количества дней заболевания поносом и количества используемых антибиотиков на 1 теленка были проанализированы с помощью двустороннего критерия. Данные относительно смертности были проанализированы с помощью критерия хиквадрат.
Результаты испытания систематизированы в табл. 6.
Почти на каждой ферме Detach-обработка способствовала значительному снижению смертности у телят, а также снижению необходимой дозы антибиотиков и электролитов. Смертность снизилась на 25 - 4% (P < 0,01). Необходимая доза антибиотиков снизилась до 1 - 0,34 дозы на теленка. Дозы электролита показали небольшое изменение, а именно 3,18 доз на контрольного теленка и 2,98 доз на обработанного теленка.
Число дней, в которые у теленка регистрировали понос, также снизилось, то есть от 2,33 дней для контрольных телят до 1,46 дней для обработанных телят (разница P < 0,01),
Наилучший эффект наблюдался в отношении данных по смертности. Как предполагается, причиной смертности телят от поноса является Sryprosporidia, доминирующий патоген, выделенный из фекалий или образцов, взятых после смерти животных. Cryptosporidia является в высокой степени патогенным кишечником паразитом молодых телят, против которого все имевшиеся до настоящего времени способы обработки были неэффективны. При этом у теленка, страдающего поносом, вызванным этим патогенном, смерть наступала уже через один-два дня после возникновения поноса. В некоторых случаях животное выживало после введения электролитов в течение нескольких недель, но находилось в состоянии крайнего истощения. Композиция Detach может дать реальный эффект при лечении этого заболевания.
Было показано, что две или более дозы Detach (35 мл) способствуют предохранению телят от инфекции, вызываемой Cryptosporidial, и снижают потребность в лечении антибиотиками.
Пример 8. Способ приготовления стимулятора роста животных.
a) 2-5% (мас./об.) k-карагенана смешивали с очищенной водой при температуре 65oC до полного растворения. Этот раствор затем охлаждали до 50oC;
b) 1% (мас./об.) равных ферментативных активностей (равные ферментативные активности определяются как количество фермента, способное расщепить один и тот же вес своего специфического субстрата) амилазы, целлюлазы, протеазы и липазы растворяли в изотоническом растворе фосфатного буфера с pH 6 (40% 0,067 М NaH1PO4 - 60% 0,67 M Na2HPO4) при 50oC. Этот раствор добавляли к раствору (a) и гомогенизировали на 500 об./мин в течение 15 мин. Затем к раствору добавляли 2 - 5% (мас./об.) ионизированного кальция в воде и полученный раствор гомогенизировали еще один час на 50 об./мин, а затем охлаждали до 210oC, получая гель и водную фазу;
c) Полученный гель и водную фазу охлаждали до 5oC, декантировали, фильтровали и лиофилизировали. Лиофилизированный материал смалывали до получения гранул размером 25-100 мк. Эти гранулы затем промывали отверждающим агентом, таким как 2,5% (по массе) глутаровый альдегид или формальдегид.
Альтернативно, гелевую фазу стадии (b) прессовали выдавливанием, распыляли через поры размером 50 мкм под давлением 3 кПа/см2 и сбрасывали с высоты 1-5 м в 2,5% (мас./об.) раствор глутарового альдегида или формалин, в результате чего получали гранулы;
d) Эти гранулы затем отфильтровывали и промывали умягчающим агентом, таким как глицерин. Можно использовать любой пленочный умягчитель;
e) Полученные гранулы отфильтровывали, псевдоожижали и высушивали нагреванием при 40oC;
f) На гранулы с предшествующей стадии наносили покрытие путем распыления 1-2% (мас./об.) водного раствора желатина при 40oC;
g) Далее на гранулы путем распыления наносили кислотоустойчивое, растворимое в щелочной среде покрытие до достижения конечного веса 120% (мас./об. ). Это покрытие включало:
6% (мас./мас.) фталата ацетата целлюлозы,
30% (мас./мас.) изопропанола,
0,5% (мас./мас.) касторового масла,
ацетон до 100% (мас./мас.);
h) В качестве альтернативы стадии (g) на гранулы путем распыления наносили высокомолекулярный полимер со структурой, прерывающейся промежутками или окнами жирной кислоты, до достижения конечного веса 105% (мас./об.). Это покрытие включало:
3% полибутилметакрилата,
0,15% дибутилфталата,
0,05% стеариновой кислоты,
и этилацетат до 100% (мас./об.).
На этапе (a) k-карагенан можно заменять любым гелеобразующим агентом, таким как альгиновая кислота, желатин или целлюлоза и ее производные.
На стадии (b) кальций можно заменять ионами любого другого щелочного металла, такими как K+, Rb+, Cs+ или ионами щелочноземельного металла, такими как Mg2+, St2+, или ионами двух- или трехвалентного металла, такими как Al3+, Mn2+, Ba2+, Co2+, Ni2+, Zn2+, Pb2+, и т.д., или ионами NH
Следует взять часть просеянных гранул стадии (a) и нанести кислотное водное или водно-спиртовое покрытие, обеспечивающее замедленное высвобождение (для предотвращения растворения прежде нанесенного энтеросолюбильного покрытия), которое содержит покрывающий материал, обеспечивающий замедленное высвобождение, например, этилцеллюлозу. Точный состав и толщина этого покрытия, обеспечивающего замедленное высвобождение, зависит от продолжительности задержки высвобождения, требующейся для достижения нужного участка-мишени в желудочно-кишечном тракте, и от физиологии вида, подвергаемого лечению.
Пример 9. Приготовление микрогранул, содержащих витамин B2 (рибофлавин).
Способ приготовления.
1. Смешивали 7500 мг рибофлавина (стандарт Британской фармакопеи) с 5000 мл 0,3% раствора ледяной уксусной кислоты. Нагревали на водяной бане и встряхивали до растворения.
2. Смешивали 250 мг k-карагенана с 5000 мл очищенной воды при 65oC до растворения карагенана. Этот раствор охлаждали до 50oC, а затем смешивали с раствором рибофлавина.
3. Полученный гель/раствор затем гомогенизировали на 500 об./мин в течение 15 мин.
4. К гелю/раствору добавляли 5 л 10% раствора хлорида кальция в дистиллированной воде, а затем гомогенизировали в течение 1 ч на 50 об./мин. Охлаждали до 5oC и декантировали гелевую фазу.
5(a). 100 г декантированного геля лиофилизировали и гранулировали с получением гранул весом около 100 мкг.
5(b). Остаток гелевой фазы фильтровали и распыляли через поры размером 50 мкм под давлением 3 кПа/см2 в 2,5% раствор глутарового альдегида с высоты 3 м.
6. Гранулы стадии 5(b) отфильтровывали и промывали 0,5% водным раствором глицерина. Полученные гранулы отфильтровывали, псевдоожижали и высушивали нагреванием при 40oC. Все гранулы собирали.
7. На гранулы предшествующего этапа наносили покрытие путем распыления 2% водного раствора желатина при 40oC до конечного веса 104o% (мас./мас.).
8. На гранулы затем наносили покрытие путем распыления 3% бутилметакрилата, 0,15% дибутилфталата, 0,05% стеариновой кислоты в растворе этилацетата до конечного веса 105% (мас./об.).
9. Гранулы просеивали таким образом, чтобы их средний размер составлял менее 500 микрон.
Испытание in vitro.
1. 5 г "испытуемых гранул" и 5 г "контрольных гранул" помещали в отдельные мешочки из нейлоновой ткани размером 6 • 6 см.
2. Мешочки герметизировали, погружали на 2 ч в разбавленный раствор хлористоводородной кислоты с pH 1 и перемешивали на 60 об./мин.
3. Затем мешочки извлекали из раствора кислоты, промывали под струей воды в течение 30 мин и оставляли стекать до сухости.
4. Из рубца коровы через фистулу отбирали 200 мл сока.
5. Оба мешочка суспендировали в соке рубца и инкубировали в течение 24 ч при 37oC.
6. Оба мешочка промывали, затем высушивали при 40oC.
7. Содержимое каждого мешочка взвешивали и определяли содержание в нем рибофлавина.
Результаты.
В нейлоновом мешочке контрольных гранул не осталось.
Из нейлонового мешочка, содержавшего испытуемые гранулы, извлекли 4,52 г испытуемых гранул. Потеря 0,48 г испытуемых гранул, возможно, была обусловлена разрушением тех микрогранул, которые были недостаточно хорошо сформированы во время технологического процесса.
По результатам исследования 1 г обработанных соком рубца испытуемых гранул было рассчитано, что 4,52 г испытуемых гранул в мешочке содержали всего 114 мг рибофлавина. 4,52 грамма необработанных гранул содержали около 114 мг рибофлавина.
Два грамма испытуемых гранул вновь поместили в нейлоновый мешочек, суспендировали в 100 мл дуоденального сока, собранного на скотобойне, и инкубировали при 37oC. Гранулы разрушились через два часа.
Методика анализа.
1. Обработанные соком рубца испытуемые гранулы помещали в 100 мл раствора этилацетата в воде 50%/50% и гомогенизировали на 500 об./мин в течение часа.
2. Фазу растворителя декантировали, а водную фазу оставляли.
3. Эту процедуру повторяли три раза.
4. Затем к конечной водной фазе добавляли 3 мл ледяной уксусной кислоты. Смесь нагревали на водяной бане при частом встряхивании до растворения, фильтровали через фильтр из ватмана N 1 и разбавляли до 1000 мл. Добавляли 5 мл 0,1 М раствора ацетата натрия и полученный раствор разбавляли водой до 50 мл. Поглощение полученного раствора измеряли с максимумом приблизительно на 444 нм. Подсчитывали содержание рибофлавина, принимая 323 как величину А (1%, 1 см) на максимуме приблизительно 444 нм.
Брали часть просеянных гранул стадии (a) и наносили кислотное водное или водно-спиртовое покрытие, обеспечивающее замедленное высвобождение (для предотвращения растворения прежде нанесенного энтеросолюбильного покрытия), которое содержало покрывающий материал, обеспечивающий замедленное высвобождение, например, этилцеллюлозу. Точный состав и толщина этого покрытия, обеспечивающего замедленное высвобождение, зависят от продолжительности задержки высвобождения, требующейся для достижения нужного участка-мишени в желудочно-кишечном тракте, и от физиологии вида, подвергаемого лечению.
Пример 10. Микрогранулярный препарат, содержащий метионин.
Способ и приготовление.
Микрогранулы, содержащие метионин, изготавливали способом примера 2, за исключением того, что на этапе 1 использовали 30 г пищевого DL-метионина. Гранулы, содержащие метионин, далее упоминаются как "испытуемые гранулы". "Контрольные гранулы изготавливали согласно способу примера 2.
Испытание in vitro.
1. 5 г "испытуемых гранул" и 5 г "контрольных гранул" помещали в отдельные мешочки из нейлоновой ткани размером 6 • 6 см.
2. Мешочки герметизировали, погружали на 2 ч в разбавленный раствор хлористоводородной кислоты с pH 1 и перемешивали на 60 об./мин.
3. Затем мешочки извлекали из раствора кислоты, промывали под струей воды в течение 30 мин и оставляли стекать до сухости.
4. Из рубца коровы через фистулу отбирали 200 мл сока.
5. Оба мешочка суспендировали в соке рубца и инкубировали в течение 24 ч при 37oC.
6. Оба мешочка промывали, затем высушивали при 40oC.
7. Содержимое каждого мешочка взвешивали и определяли содержание в нем метионина.
Результаты.
В нейлоновом мешочке контрольных гранул не осталось.
Из нейлонового мешочка, содержавшего испытуемые гранулы, извлекали 4,40 г испытуемых гранул. Потеря 0,6 г испытуемых гранул, возможно, была обусловлена разрушением дефектных микрогранул.
По результатам исследования 1 г обработанных соком рубца испытуемых гранул было рассчитано, что 4,40 г испытуемых гранул в мешочке содержали всего 563 мг метионина, 4,4 г необработанных гранул содержали 563 мг метионина.
Два грамма испытуемых гранул вновь поместили в нейлоновый мешочек, суспендировали в 100 мл дуоденального сока, собранного на скотобойне, и инкубировали при 37oC. Гранулы разрушились через два часа.
Методика анализа.
1. Обработанные соком рубца испытуемые гранулы помещали в 500 мл колбы со стеклянными пробками. Добавляли 200 мл раствора этилацетата в воде 50%/50% и гомогенизировали на 500 об./мин в течение часа.
2. Фазу растворителя декантировали, а водную фазу оставляли.
3. Эту процедуру повторяли три раза.
4. Затем к конечной водной фазе добавляли воду до 20 мл. Добавляли 10 г двуосновного фосфата калия, 4 г одноосновного фосфата калия и 4 г иодида калия и тщательно перемешивали по растворимости.
5. Добавляли ровно 100 мл 0,1H йода: колбу закупоривали: тщательно перемешивали и оставляли стоять в течение 30 мин, затем избыток иода оттитровывали 0,1H тиосульфатом натрия. Производили контрольное определение и вносили необходимые коррективы. Каждый мл 0,1H иода эквивалентен 7,461 мг DL-метионина.
Брали часть просеянных гранул этапа (a) и наносили кислотное водное или водно-спиртовое покрытие, обеспечивающее замедленное высвобождение (для предотвращения растворения прежде нанесенного энтеросолюбильного покрытия), которое содержало покрывающий материал, обеспечивающий замедленное высвобождение, например, этилцеллюлозу. Точный состав и толщина этого покрытия, обеспечивающего замедленное высвобождение, зависит от продолжительности задержки высвобождения, требующейся для достижения нужного участка-мишени в желудочно-кишечном тракте, и от физиологии вида, подвергаемого лечению.

Изобретение относится к лечению млекопитающих. Описаны композиции, включающие в себя: гранулы, которые содержат биологически активное вещество в сочетании со слабым основанием и частично покрыты материалом пролонгированного высвобождения, растворимым в кишечном соке; подкисляющий агент, имеющий рН 1,5 - 6; гелеобразующий агент. Также описана композиция, состоящая из подкисленного геля, имеющего рН 1,5 - 6 и содержащего микрогранулы, которые включают в себя биологически активное вещество в сочетании со слабым основанием и являются частично покрытыми материалом пролонгированного высвобождения, растворимым в кишечном соке. Указанные композиции могут быть использованы для лечения заболеваний, ассоциированных с кишечными патогенами у животных, предупреждая появление антибиотикоустойчивых микроорганизмов. 4 c. и 7 з.п.ф-лы, 6 табл.
| EP, 91767 А (Mezck), 19.10.83, A 61 K 9/16. |
Авторы
Даты
1998-06-20—Публикация
1992-07-23—Подача