Изобретение относится к способам построения костей у человека и животных, то есть к лечению остеопороза и родственных заболеваний. В частности, изобретение относится к таким способам лечения, которые включают введение активно действующих на кости фосфонатов и эстрогена.
Наиболее частным метаболическим заболеванием костей является остеопороз. Остеопороз можно в общих чертах определить как ухудшение качества костей или атрофию тканей скелета. Вообще существуют два типа остеопороза: первичный и вторичный. Вторичный остеопороз является результатом идентифицируемого процесса заболевания или действия агента. Однако приблизительно 90% всех случаев остеопороза являются идиопатическим первичным остеопорозом. Такой первичный остеопороз включает остеопороз, связанный с постменопаузой, остеопороз возрастной (поражающий в основном пациентов в возрасте 70 - 80 лет) и идеопатический остеопороз, поражающий людей среднего возраста и более молодых мужчин и женщин.
У некоторых больных остеопорозом утрата костной ткани бывает столь велика, что вызывает механическое разрушение костной структуры. Часто происходят переломы костей, например, бедра или позвоночника у женщин, страдающих остеопорозом постменопаузы. Может также наблюдаться кифоз (ненормальное искривление позвоночника).
Считают, что механизм утраты костной ткани при остеопорозе связан с дисбалансом процесса "ремоделирования костной ткани". Реконструкция костей происходит в течение всей жизни, обновляя скелет и поддерживая прочность костей. Такая реконструкция включает эрозию и заполнение отдельных участков на поверхности костей за счет организованной группы клеток, называемых "основными мультиклеточными фрагментами" или "BMU". BMU в основном состоят из остеокластов, остеобластов и их клеточных предшественников. При реконструкции кости ресорбируются в определенном месте, "активированном" BMU за счет остеокластов, образуя ресорбционную полость. Эта полость затем заполняется костной тканью за счет остеобластов.
Обычно у взрослых цикл реконструкции приводит к некоторому дефициту костей в результате неполного заполнения ресорбционной полости. Так, даже у здоровых взрослых наблюдается потеря костной ткани с возрастом. Однако при остеопорозе наблюдается увеличение числа BMU, которые активированы. Такое увеличение активации ускоряет реконструкцию костей, что приводит к ненормально большой потери костной ткани.
Хотя этиология остеопороза не полностью понятна, существует множество факторов риска, которые, как считают, связаны с остеопорозом. Они включают низкий вес тела, плохое поглощение кальция, отсутствие физической активности и дефицит эстрогена.
Многие композиции и способы их применения для лечения остеопороза описаны в медицинской литературе. Многие из этих композиций и способов направлены на попытки либо замедлить потерю костной ткани, либо увеличить чистый вес костной массы. (R.C.Haynes, Jr.et al., "Agents offecting Calerfication", The Phacmacological Basis of The rapentics, Jth Edition (A.G.Gilman, L.S. Goodman et al, Editors 1985); G.D.Whedon et al., "An Analysis of Current Concepts and Research Jnterest in Osteoporosis", Current Advances in Skeletogenesis (A. Ornoy et al., Editors., 1985); and W.A. Pick, et al., Physieian's Resanrel Manual on Osteoporosis (1987), published by the Notional Ostioporosis Fondation).
Среди способов лечения остеопорозов, предложенных в литературе, встречается введение биофосфонатов или других активно действующих на кости фосфонатов (Storm et al., "Effect of Intermittent Cyclical Etidronate Therapy on Rone Mineralization and Fracture Rate in Women with Post Menopausal Osteoporosis", 322 New England Journal of Medicine 1265 (1990); and Watts et al., "Intermittent Cyclical Etidronate Treatment of Post-Menapanial Osteoporosis", 323 New England Journal of Medicine 73 (1990).
Такие способы лечения, использующие различные бисфофонаты, описаны в патенте США N 4761406, 1988, 4812304, 1989, 4812311, 1989, 4822609, 1989. Использование таких фосфонатов для лечения остеопороза и других заболеваний, включая ненормальный кальциевый и фосфатный метаболизм, описаны также в патенте США N 3683080, 1972, 4330537, 1980, 4267108, 1981, в европейской патентной публикации N 298553, 1989, и в работе Francis et al. Химические, биохимические и медицинские свойства дифосфонатов. Роль фосфонатов в живых системах, 55, 1983.
Введение эстрогена также используют как средство предотвращения остеопороза в период постменопауз у женщин. Такое лечение обычно включает ежедневный прием от около 0,625 до около 1,25 мг конъюгата экстрогена или эквивалентного количества других экстрогенных гормонов. Эстроген можно также использовать для лечения остеопороза (то есть актуального построения костей при остеопорозе), хотя это и не было общепринято (Barzel, "Estrogens in the Preventroa and Treatment of Post-Menopanial Osteoporasis: a Review", 85 American Jornal of Medicine 847 (1988); Barzel, "Estrogen Therapy for Osteoporosis: Js it Effective?", Hospital Prastice 95 (1990); Ettinger, et al. , "Post Menopausal Rone Loss is Prerented by Treatment winh Low. Dosage Estrogen with Calcium", 106 Annals in Internal Medicine 40 (1987); Lindsay, et al. , "The Minimum Effective Dose of. Estrojen for Prevention of Post-Menepausal Rone Loss", 63 Obstetrcs and Gynecology 759 (1984); and "Estrogen Drug Information 1765 (1990)).
Кроме того, использование эстрогена было связано с некоторыми побочными эффектами, например маточными кровотечениями (Rudy. Hormone Replacement Nhe rapy (Как выбрать лучший препарат и режим), 88, Postgraduate Medicine, 157,1990).
Обнаружено, что остеопороз можно предотвратить или лечить, принимая активно действующие на кости фосфонаты с низкими, неэффективными в других случаях дозами эстрогена. Далее, эти способны позволяют также использовать низкие, в других случаях малоэффективные или вовсе не эффективные дозы фосфонатов. Соответственно способы изобретения представляют эффективные способны предотвращения и лечения остеопороза с пониженными побочными эффектами по сравнению с способами, известными специалистам.
В изобретении предложены способы лечения остеопороза у людей или животных, включающие прием активно действующего на кости фосфоната указанным субъектом в количестве по крайней мере около 0,1 LED в день и введение гормона эстрогена указанному субъекту в количестве от около 0,2 до около 0,8 LED в день. Активно действующие на кости фосфонаты являются предпочтительно бисфосфонатом или фосфоноалкилфосфонатом.
Способы лечения включают введение активно действующих на кости фосфонатов и эстрогенного гормона человеку или животному. Конкретные соединения и композиции, которые следует использовать в этих способах, должны быть, естественно, фармацевтически приемлемыми. В том смысле, как здесь использован термин "фармацевтически приемлемый" компонент, подразумевают компонент, который пригоден для использования людьми и/или животными без нежелательных вредных воздействий (таких, как токсичность, раздражение и аллергическая реакция) одновременно с разумным отношением выгода/риск. Кроме того, термин "безопасное и эффективное количество" относится к такому количеству компонента, которого достаточно для достижения нужного терапевтического действия без нежелательных побочных эффектов (таких, как токсичность, раздражение или аллергическая реакция) наряду с разумным отношением выгода/риск, если его используют в способе изобретения. Конкретно "безопасное и эффективное количество" будет, очевидно, меняться в зависимости от таких факторов, как конкретное состояние, которое нужно лечить, от физического состояния больного, длительности лечения, характера одновременной терапии (если она есть) и конкретных используемых композиций.
Способы изобретения включают введение активно воздействующих на кость фосфонатов. "Фосфонаты, активно воздействующие на кость" включают одно или более соединений общей формулы: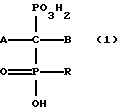
и их фармацевтически приемлемые соли и сложные эфиры, где A, B и R имеют значения, указанные ниже.
В формуле (1) R представляет собой гидроксогруппу (для бисфосфонатов), водород или алкильную группу (для фосфоноалкилфосфинатов). В фосфоноалкилфосфинатах R предпочтительно представляет собой незамещенный алкил, особенно низший алкил. Если R представляет собой замещенный алкил, предпочтительные заместители включают галоид, замещенный или незамещенный фенил, незамещенный или замещенный пиридинил, незамещенную аминогруппу, аминогруппу, замещенную одной или двумя низшими алкильными группами, гидрокси- или карбоксигруппы. Более предпочтительными заместителями являются фтор, фенил, незамещенные амино- и гидроксигруппы, наиболее предпочтительными - фтор (особенно когда представлен как трифторметил) и фенил.
Особенно предпочтительными R фрагментами в фосфоноалкилфосфинатах являются незамещенные низшие алкильные группы, особенно незамещенные, насыщенные низшие алкильные группы с неразветвленной цепью. Также предпочтительными R фрагментами являются метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил и н-гексил. Более предпочтительно, чтобы R представлял собой метил, этил, н-пропил или н-бутил. Наиболее предпочтительно, чтобы R представлял собой метил.
В формуле (I) А является водородом, галоидом, нитрогруппой, алкилом, гетероциклом, арилом, гетероарилом, незамещенной аминогруппой или ее амидом, полученным из карбоновой кислоты замещающей группы, амином, замещенным одной замещающей группой или его амидом, полученным из карбоновой кислоты замещающей группы, аминогруппой, замещенной независимо одной алкильной группой и одной замещающей группой, гидроксигруппой, или ее сложным эфиром, полученным из карбоновой кислоты замещающей группы, простым эфиром, имеющим замещающую группу, тиолом или тиоловым сложным эфиром, полученным из карбоновой кислоты замещающей группы, тиоэфиром, имеющим замещающую группу, или сульфоксидным или сульфоновым его производным, -SO3H, фармацевтически приемлемыми ее солями, ее сложным эфиром, полученным из спирта замещающей группы, ее незамещенным амидом или ее амидом, замещенным одной или двумя алкильными группами, -CO2H, ее фармацевтически приемлемыми солями, ее сложным эфиром, полученным из спирта замещающей группы, ее незамещенным амидом или ее амидом, замещенным одной или двумя алкильными группами, альдегидом, кетоном, имеющим замещающую группу, карбаматом, незамещенным, или замещенным одной или двумя алкильными группами, пептидами, содержащими от около 1 до около 100 аминокислотных фрагментов, или фрагментов A и B, ковалентно соединенных с образованием кольца, содержащего 3 - 7 атомов, причем 0 - 3 гетероатома выбраны из группы, состоящей из азота, серы, фосфора и кислорода, причем кольцо не замещено или замещено одним или более из заместителей A, указанных выше; или фрагменты A и B заменены незамещенным или замещенным алкильным фрагментом, присоединенным к геминальному углероду (углерод изображен в структуре 1 выше) двойной связью.
Предпочтительно A представляют собой один из следующих фрагментов:
1) водород;
2) галоид (предпочтительно фтор или хлор, более предпочтительно фтор):
3) замещенный или замещенный алкил общей структуры.
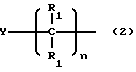
где
a) n=1-10, целое число, предпочтительно 1 - 5, более предпочтительно 1 - 2, более предпочтительно 1;
b) каждый R1 - независимо водород, галоид, низший алкил, незамещенная аминогруппа или ее амид, полученный из карбоновой кислоты низшей алкильной группы, аминогруппа, замещенная одной низшей алкильной группой или ее амидом, полученным из карбоновой кислоты низшей алкильной группы, аминогруппа, замещенная независимо двумя низшими алкильными группами, гидроксигруппой или ее эфиром, полученным из карбоновой кислоты низшей алкильной группы, -CO2H или фармацевтически приемлемые соли ее или ее сложный эфир, полученный из спирта низшей алкильной группы, или незамещенный ее амид, или ее амид, замещенный одной или двумя низшими алкильными группами, простой эфир, имеющий низшую алкильную группу, -PO3H2 или фармацевтически приемлемые соли ее, или нитрогруппой, или два R1 у одного атома углерода - =0 или = NR9 (где R9 - низший алкил или водород, если другой атом азота присоединен к тому же атому углерода, что и =NR9 фрагмент), или два R1 на соседних атомах углерода могут быть заменены дополнительной связью между атомами углерода; или R1 первого атома углерода (с правой стороны на структуре (2)) и B (см. структуру (1) могут быть замещенные дополнительной связью; и
c) y - галоид: нитрогруппа; цианогруппа; гетероцикл; арил; гетероарил; незамещенная аминогруппа и ее амид, полученный из карбоновой кислоты алкильной, гетероциклической, ариловой или гетероариловой группы; аминогруппа, замещенная одной алкильной, гетероциклической, арильной или гетероарильной группой и ее амидом, полученным из карбоновой кислоты алкильной группы; аминогруппа, замещенная независимо одной алкильной группой и одной алкильной, гетероциклической, арильной или гетероарильной группой; гидроксигруппа и ее эфир, полученный из карбоновой кислоты алкильной, гетероциклической, арильной или гетероарильной группы; простой эфир с алкильной, гетероциклической арильной или гетероарильной группой; тиол и тиоловый сложный эфир его, полученный из карбоновой кислоты алкильной, гетероциклической, арильной или гетероарильной групп; простой тиоэфир, имеющий алкильную, гетероциклическую, арильную или гетероарильную группу и сульфоксидными и сульфоновыми его производными; -SO3H, фармацевтически приемлемые ее соли, ее сложный эфир, полученный из спирта алкильной группы, незамещенный его амид и его амид, замещенный одной или двумя алкильными группами; -CO2H, фармацевтически приемлемые ее соли, ее сложный эфир, полученный из спирта алкильной группы, ее незамещенный амид и ее амидом, замещенным одной или двумя алкильными группами; PO3H2, фармацевтически приемлемы ее соли, ее сложный эфир, полученный из спирта алкильной группы, ее незамещенный амид и ее амид, замещенный одной или двумя алкильными группами -(R8)PO2H (где R8 - водород или незамещенный низший алкил), ее фармацевтически приемлемая соль, ее сложный эфир, полученный из спирта алкильной группы, ее незамещенный амид и ее амид, замещенный одной или двумя алкильными группами; альдегид; кетон, имеющий алкильную группу; карбамат, незамещенный или замещенный одной или двумя алкильными группами; или пептидил. Для бисфосфонатов Y предпочтительно является гетероциклом (предпочтительно гетероциклом с 5 - 7 членами, имеющими два или один атом азота); аминогруппой; замещенной аминогруппой. Особенно предпочтительные Y фрагменты включают пиридинил, аминогруппу и аминогруппу, замещенную одной или двумя низшими алкильными группами. Для фосфоноалкилфосфинатов предпочтительно, чтобы Y представлял галоид (предпочтительно фтор); трифторметил; простой эфир с низшей алкильной группой; незамещенную аминогруппу и ее амид, полученный из карбоновой кислоты низшей алкильной группы, аминогруппу, замещенную одной низшей алкильной группой и ее амид, полученный из карбоновой кислоты низшей алкильной группы; аминогруппу, независимо замещенную двумя низшими алкильными группами; или пептидил, включающий от одного до около шести аминокислотных фрагментов;
4) циклоалкил с 4 - 10 атомами углерода, предпочтительно с 5 или 6 атомами;
5) гетероцикл с 5 или 6 атомами в кольце; предпочтительно с одним или двумя атомами азота в кольце, более предпочтительно с одним атомом азота в кольце. Особенно предпочтительными гетероциклами являются незамещенный или замещенный пиперидинил, пирролидинил, пиперазинил и морфолинил;
6) незамещенный или замещенный фенил и нафтил;
7) незамещенные или замещенные гетероарилы с 5 или 6-членными кольцами с одним или двумя гетероатомами (особенно гетероатомами и азота), предпочтительно пиридинил;
8) аминосодержащий фрагмент общей структуры: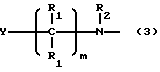 ,
,
где
a) m = 0-10, целое число, предпочтительно 0-5, более предпочтительно 0 или 1, более предпочтительно 0;
b) R1 и Y представлены, как описано выше; и
c) R2 - водород, низший алкил или ацильная группа, полученная из карбоновой кислоты низшего алкила;
9) кислородсодержащий фрагмент, имеющий общую структуру: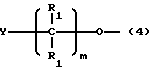 ,
,
где
a) m = 0-10, целое число, предпочтительно 0-5, более предпочтительно 0 или 1, более предпочтительно 0 или 1, более предпочтительно 0; и
b) R1 и Y представлены, как описано выше;
10) серусодержащий фрагмент общей структуры: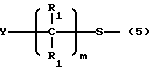 ,
,
где
a) m = 0-10, целое число, предпочтительно 0 - 5, более предпочтительно 0 или 1, более предпочтительно 0; и
b) R1 и Y представлены, как описано выше.
В формуле (1) B является водородом; галоидом; незамещенным или замещенным низшим алкилом; незамещенным или замещенным циклоалкилом с кольцом, состоящим из 3 - 7 атомов; незамещенным или замещенным гетероциклом с кольцом, состоящим из 3 - 7 атомов; незамещенным или замещенным фенилом; гидроксигруппой или ее сложным эфиром, полученным из карбоновой кислоты низшей алкильной группы; тиолом; незамещенной аминогруппой или ее амидом, полученным из карбоновой кислоты низшей алкильной группы; аминогруппой, замещенной одной низшей алкильной группой, или ее амидом, полученным из карбоновой кислоты низшей алкильной группы; аминогруппой, замещенной независимо двумя низшими алкильными группами; или -CO2H, ее фармацевтически приемлемыми солями, ее сложным эфиром, полученным из спирта низшей алкильной группы, ее незамещенным амидом, или ее амидом, замещенным одной или двумя низшими алкильными группами.
Для поддержания химической стабильности этих соединений фрагменты A и B оба предпочтительно не содержат гетероатомов (азота, кислорода или серы) или гетероатома и галоида, присоединенных к фосфонатному фрагменту (т.е. атом углерода геминально замещен двумя атомами фосфора). Таким образом, когда фрагмент A содержит атом кислорода, серы, азота или галоида, присоединенный к фосфорозамещенному метиленовому углероду, тогда B выбирают из ряда: водород; незамещенный или замещенный низший алкил, циклоалкил, гетероцикл (где атом углерода гетероцикла присоединен к геминальным атомам углерода) или фенил; -CO2H или ее фармацевтически приемлемые соли, ее сложный эфир, полученный из спирта низшей алкильной группы, ее незамещенный амид и ее амид, замещенный одной или двумя низшими алкильными группами.
Предпочтительно B является галоидом, водородом, незамещенным или замещенным низшим алкилом, незамещенным или замещенным фенилом, незамещенным или замещенным бензилом, гидроксигруппой или ее эфиром, полученным из карбоновой кислоты низшей алкильной группы, тиолом, ее незамещенной аминогруппой или ее амидом, полученным из карбоновой кислоты низшей алкильной группы, аминогруппой, замещенной одной низшей алкильной группой или ее амидом, полученным из карбоновой кислоты низшей алкильной группы, аминогруппой, замещенной независимо двумя низшими алкильными группами или -CO2H или фармацевтически приемлемыми ее солями и ее сложным эфиром, полученным из спирта низшей алкильной группы, и ее незамещенным амидом или ее амидом, замещенным одной или двумя низшими алкильными группами.
Более предпочтительно B является водородом, хлором, метильной группой, этильной группой, гидроксигруппой, тиолом, незамещенной аминогруппой, (N-метил)амино-, (N,N-диэтил)амино-группами, -CO2H или фармацевтически приемлемыми ее солями, -CO2CH3 или -CONH2. Более предпочтительно, чтобы B являлся водородом, метильной группой, хлором, аминогруппой или гидроксигруппой; более предпочтительно водородом, или гидроксигруппой, или аминогруппой, или тиолом; более предпочтительно гидроксигруппой. Особенно предпочтительно, чтобы активно воздействующие на кость фосфонаты включали те, в которых A является фрагментом групп (3) или (8), а B - гидроксигруппой.
Особенно предпочтительными бисфосфонатами, используемыми здесь, являются бисфосфонаты общей формулы: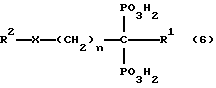 ,
,
где
n = 0-7, целое число (предпочтительно 0 - 2, более предпочтительно 1); R1 - водород, хлор, аминогруппа или гидроксигруппа (предпочтительно водород или гидроксигруппа); X - -NH-, кислород или простая связь (предпочтительно - NH- или простая связь); R2 - 5- или 7-членный гетероцикл, имеющий 1 - 3 гетероатомов (предпочтительно 6-членным гетероциклом, имеющим 1 или 2 атома азота), аминогруппа, аминогруппа, замещенная одной или двумя низшими алкильными группами, или водород; и их фармацевтически приемлемые соли и сложные эфиры.
Термин "фармацевтически приемлемые соли и сложные эфиры", используемый здесь, означает гидролизуемые сложные эфиры и соли, активно воздействующие на кость фосфонатов, которые имеют такие же общие фармакологические свойства, как и кислотная форма, из которой их получают, и которые являются фармацевтически приемлемыми. Фармацевтически приемлемые соли включают, например, соли щелочных металлов (например, натрия и калия), щелочноземельных металлов (например, кальция и магния), нетоксичных тяжелых металлов (например, олова и индия) и аммония и замещенного аммония с малым молекулярным весом (например, моно-, ди-, и триэтаноламин). Предпочтительными соединениями являются соли натрия, калия, аммония. Фармацевтически приемлемые сложные эфиры включают незамещенные и замещенные алкильные, арильные и фосфорильные сложные эфиры. Неограничивающие примеры фармацевтически приемлемых сложных эфиров включают, например, изопропил, третичный бутил, 2-хлорэтил, 2,2,2-трихлорэтил, 2,2,2-трифторэтил, n-толуолсульфонилэтил, глицил, саркозил, бензил, фенил, 1,2-гексаноилглицерил, п-нитрофенил, 2,2-диметил-1,3-диоксолен-4-метил, изопентенил, o-карбометоксифенил, пиралоилоксиметилсалицил, диэтиламидофосфорил, пивалоилоксиметил, ацилоксиметил, пропионилоксиметил, изобутирилоксиметил, додецил, октадецил и изопропилоксиметил.
Конкретные примеры и определения для заместителей, применимых в соединениях формул (1-6), описаны в европейской патентной публикации N 298553, Ebetino, 1989. Эта публикация также описывает фосфоноалкилфосфинаты, используемые в способах этого открытия (где R является водородом или алкильной группой), и методы получения этих соединений. Методы получения фосфоноалкилфосфинатов также описаны в европейской патентной публикации N 298555, Ebetino, 1989.
Биофосфонаты, используемые в способах этого открытия (где R является гидроксигруппой), и методы получения таких соединений описаны в следующих патентных документах, включены в качестве ссылок: патенты США N 3553314, Fronris, 1971; N 3683080, Francis, 1972; N 3846420, Wollman et. al, 1974; N 3899496, Schindler et al., 1975; N 3941772, Ploger et al., 1976; N 3957160, Ploger et al., 1976; N 3962432, Schmidt - Dunker, 1976; N 3979385, Wollmann et al., 1976; N 3988443, Ploger et al., 1976; N 4054598, Blum et al/, выданный 1977; N 4113861, Fleisch et al. , 1978; N 4117090, Ploger, 1978; N 4134969, Schmidt-Dunker, 1979; N 4267108, Blum et al., 1981; N 4304734, Jary et al. , 1981; N 4330537, Francis, 1982; N 4407761, Blum et al., 1983; N 4469686, Andrews, 1984; N 4578376, Bosini, 1986; N 4608368, Blum et al., 1986; N 4621077, Rosini et al., 1986; N 4687767, Basies et al., 1987; N 4687768, Benedict et. al., 1987; N 4711880, Stahl et. al., 1987; N 4719203, Basies et. al. , 1988; N 4927814, Gall et al., 1990; N 4990503, Jsomura et al. , 1991; Западногерманские открытые патентные выкладки N 2104476, Worms, 1972; N 2343147, Ploger et. al., 1975; N 2360798, Worml et. al, 1975; N 2513966, Schmidt - DunKer, 1976; N 2541981, Ermers et. al, 1977; N 3334211, Blum, 1985; патентные публикации Японии N 78/59674, Suzuk; et. al, 1978; N 79/13524, Suzuk et. al, 1979; N 80/98193, Suzuki et. al, 1980; Европейские патентные публикации N 88359, Blum et. al 1983; N 100718, Rceliere et. al, 1984; N 186405, Renedict et. al, 1986; N 197478, Rosies et al, 1986; N 230068, Benedict et. al, 1987; N 273514, Ebetino et. al, 1988; N 274158, Ebetino et. al, 1988; N 282309, Sakamoto et. al, 1988; N 282320, Jsomura et. al, 1988; PCT патентные публикации N 87/03598, Binderug et. al, 1987; N 88/00590, Gall et. al, 1988.
Предпочтительные активно воздействующие на кости фосфонаты, пригодные для использования в способе изобретения, включают: N-(2'-(3'-метил)-пиридинил)аминометанфосфонометилфосфиновую кислоту; N-(2'-(5'-метил)-пиридинил)-аминометанфосфонометилфосфиновую кислоту; N-(2'-(3'-метил)-пиперидинилиден)аминометанфосфонометилфосфиновую кислоту; N-(2'-(5'-метил)-пиперидинилиден)аминометанфосфонометилфосфиновую кислоту; 2-(2'-пиридинил)этан)-1-фосфоно-1-метилфосфиновую кислоту; 2-(2'-пиперидинил)этан-1-фосфоно-1-метилфосфиновую кислоту; 2-(пара-аминофенил)-1-гидрокси-этан-1-фосфоно-1-метилфосфиновую кислоту; 2-(м-аминофенил)-1-гидроксиэтан-1-фосфоно-1-метилфосфиновую кислоту; N-(1-(5-амино-2-метил-1-оксо)-пентил)аминометанфосфонометилфосфиновую кислоту; N-(2'-(3'-метил)-пиперидинилиден)аминометанфосфонобутилфосфиновую кислоту; S-(2'-пиридинил)тиометанфосфонометилфосфиновую кислоту; 2-(2-пиридил)-1-гидроксиэтан-1-фосфоно-1-метилфосфиновую кислоту; 2-(3-пиридил)-1-гидроксиэтан-1-фосфоно-1-метилфосфиновую кислоту; 2(N- имидазоил)-1-гидроксиэтан-1-фосфоно-1-метилфосфиновую кислоту; 3-(N-пентил-N-метиламино)-1-гидроксипропан-1-фосфоно-1-метилфосфиновую кислоту; 4-амино-1-гидроксибутан-1-фосфоно-1-метилфосфиновую кислоту; 3-(N-пирролидино)-1-гидроксипропан-1-фосфоно-1-метилфосфиновую кислоту; N- циклогептиламинометанфосфонометилфосфиновую кислоту; S-(пара-хлорфенил)тиометанфосфонометил/фосфиновую кислоту; (7- дигидро-1-пириндин)-метанфосфонометилфосфиновую кислоту; (7-дигидро-1-пириндин)гидроксиметанфосфонометилфосфиновую кислоту; (6-дигидро-2-пириндин)гидроксиметанфосфонометилфосфиновую кислоту; 2-(6-пирролипиридин)-1-гидроксиэтан-1-фосфоно-1-метилфосфиновую кислоту; 1-гидроксиэтан-1,1-бисфосфоновую кислоту; 1-гидрокси-пентан-1,1-фосфоновую кислоту; метанбисфосновую кислоту; дихлорметанбисфосфоновую кислоту; гидроксиметанбисфосфоновую кислоту; 1-аминоэтан-1,1-бисфосфоновую кислоту; 2-аминоэтан-1,1-бисфосфоновую кислоту; 3-аминопропан-1,1-бисфосфоновую кислоту; 3-аминопропан-1-гидрокси-1,1-бисфосфоновую кислоту; 3-(диметиламино)-1-гидроксипропан-1,1-бисфосфоновую кислоту; 3,3-диметил-3-амино-1-гидроксипропан-1,1-бисфосфоновую кислоту; фениламинометанбисфосфоновую кислоту; N,N-диметиламинометанбисфосфоновую кислоту; N-(2-гидроксиэтил)аминометанбисфосфоновую кислоту; 4-амино-1-гидроксибутан-1,1-бисфосфоновую кислоту; 5-амино-1-гидроксипентан-1,1-бисфосфоновую кислоту; 6-амино-1-гидроксигексан-1,1-бисфосфоновую кислоту; 6-амино-1-гидроксигексан-1,1-бисфосфоновую кислоту; индан-2,2-бисфосфоновую кислоту; гексагидроиндан-2,2-бисфосфоновую кислоту; 2-метилциклобутан-1,1-бисфосфоновую кислоту; 3-хлорпентан-1,1-бисфосфоновую кислоту; циклогексан-1,1-бисфосфоновую кислоту; 2-(2-пиридил)-1-гидроксиэтан-1,1-бисфосфоновую кислоту; N-2-(5-амино)-пиридиламинометанбисфосфоновую кислоту; N-(2-(5-хлор)-пиридил)-аминометанбисфосфоновую кислоту; N-(2-/3-пиколил)-аминометанбисфосфоновую кислоту; N-(2-/4-пиколил)аминометанбисфосфоновую кислоту; N-(2-/5-пиколил)-аминометанбисфосфоновую кислоту; N-(2-/6-пиколил)-аминометанбисфосфоновую кислоту; N-(2-/3,4-лютидин)-аминометанбисфосфоновую кислоту; N-(2-пиримидил)-аминометанбисфосфоновую кислоту; N-(2-пиридил)-2-аминоэтан-1,1-бисфосфоновую кислоту; 2-(2-пиридил)-этан-1,1-бисфосфоновую кислоту; 2-(3-пиридил)-этан-1,1-бисфосфоновую кислоту; 2-(4-пиридил)-этан-1,1-бисфосфоновую кислоту; 2-(2-/3-пиколил)оксоэтан-1,1-бисфосфоновую кислоту; 2-(3-пиридил)-1-гидроксиэтан-1,1-бисфосфоновую кислоту; 2-(N-имидазолил)-1-гидроксиэтан-1,1-бисфосфоновую кислоту; 3-(N-пентил-N-метиламино)-1-гидроксипропан-1,1-бисфосфоновую кислоту; 3-(N-пирролидино)-1-гидроксипропан-1,1-бисфосфоновую кислоту; N-циклогептиламинометанбисфосфоновую кислоту; S-(пара-хлорфенил)тиометанбисфосфоновую кислоту; (7-дигидрок-1-пиридин)метанбисфосфоновую кислоту; (7-дигидро-1-пиридин)гидроксиметанбисфосфоновую кислоту; (6-дигидро-2-пиридин)гидроксиметанбисфосфоновую кислоту; 2-(6-пиролопиридин)-1-гидроксиэтан-1,1-бисфосфоновую кислоту; и их фармацевтически приемлемые соли и сложные эфиры.
Наиболее предпочтительные активно воздействующие на кости фосфонаты, пригодные в способе изобретения, включают: 1-гидроксиэтан-1,1-бисфосфоновую кислоту; дихлорметанбисфосфоновую кислоту; 3-амино-1-гидроксипропан-1,1-бисфосфоновую кислоту; 6-амино-1-гидроксигексан-1,1-бисфосфоновую кислоту; 4-амино-1-гидроксибутан-1,1-бисфосфоновую кислоту; 2-(3-пиридил)-1-гидроксиэтан-1,1-бисфосфоновую кислоту; 2-(N-имидазолил)-1-гидроксиэтан-1,1-бисфосфоновую кислоту; 3-(N-пентил-N-метиламино)-1-гидроксипропан-1,1-бисфосфоновую кислоту; 3-(N-пирролидино)-1-гидроксипропан-1,1-бисфосфоновую кислоту; N-циклопентиламин метанбисфосфоновую кислоту; (7-дигидро-1-пиридин)метанбисфосфоновую кислоту; (7-дигидро-1-пиридин)-гидроксиметанбисфосфоновую кислоту; (6-дигидро-2-пиридин)-гидроксиметанбисфосфоновую кислоту; 2-(6-пирилидин)-1-гидроксиэтан-1,1-бисфосфоновую кислоту; и фармацевтически-приемлемые их соли и сложные эфиры.
Эстрогенные гормоны.
Способы изобретения включают также введение экстрогенных гормонов. Как было указано, термин "эстрогенный гормон" относится к природным гормонам, синтетическим стероидным соединениям и нестероидным соединениям, а также к их конъюгатам, метаболитам и производным, которые обладают эстрогенной активностью. Природные эстрогенные гормоны представляют собой стероиды, которые содержат циклопентанпергидрофенантреновую кольцевую систему. Такие природные эстрогенные гормоны получают из мочи беременных кобыл или синтетическим путем, используя способы, хорошо известные специалистам ("Estrogens", Drug Information, 1765 (1990); Rudy, "Hormone Replacement Therapy-Howto Select the Best Preparation and Regimen", 88 Postgraduate Medicine, 157 (1990); C. Christiansen et. al, "Estrogenes, Rone Loss adn Prevention" 1 Osteoporosis Int, 7 (1990).
Эстрогенные гормоны, природные для использования в способах изобретения, включают например, эстрадиол, эстрон, эстриол, эквилин, эквиленин, эстрадиолципионат, эстрадиолвалерат, этинилэстрадиол, полиэстрадиолфосфат, эстропипат, диэтилстилбестрол, диенэстрол, хлортрианизен и их смеси. Предпочтительным эстрогенным гормоном, пригодным для способа изобретения, является "конъюгированный эстроген", который представляет собой смесь натриевых солей водорастворимых сульфатных эфиров эстрона и эквилина. Такие конъюгированные эстрогены могут также содержат другие эстрогенные вещества, встречающиеся в моче беременных кобыл, например, 17- α -дигидроэквилин, 17- α -эстрадиол, эквиленин и 17- α -дигидроэквиленин.
Способы лечения.
В изобретении предложены способы лечения остеопорозов у человека и животных, которые включают: введение активно действующего на кости фосфоната указанному субъекту в количестве по крайней мере около 0,1 LED (МЭД) в день во время лечения и введение указанному субъекту эстрогенного гормона в количестве от около 0,2 до около 0,8 LED (МЭД) в день на протяжении указанного лечения. Предпочтительный способ включает введение от около 0,1 до около 2 LED (МЭД) активно воздействующего на кости фосфоната. И наиболее предпочтительный способ включает введение от около 0,1 до около 0,9 LED (МЭД) фосфоната. Предпочтительно введение от около 0,3 до около 0,6 LED (МЭД) экстрогенного гормона.
В том смысле, как здесь использован, термин "LED", или "Least effective dose", представляет собой минимальную дозу активного вещества, которая эффективно сама по себе вызывает заметное ингибирование ресорбции кости (в том смысле, как здесь использован, термин "активное вещество" относится либо к активно действующему на кость фосфонату, либо к экстрогенному гормону, либо к ним обоим). Что касается фармацевтически активных материалов, то конкретные LED (МЭД) активных соединений могут меняться в зависимости от их химических компонентов и способов их введения (например, орально или парентерально). Тем не менее LED (МЭД) для конкретных активных веществ, пригодных для целей изобретения, можно определить, используя хорошо известные специалистам способы.
В частности, LED (МЭД) для активных по отношению к костной ткани соединений можно определить, используя любые известные специалистам модели in vivo. Одной такой моделью является тиропаратироидэктомайзд (ТРТХ), модель на крысах. В этом способе соединения оценивают по in vivo ингибирующей костную ресорбцию способности, определяя их способность повышать уровни кальция в крови за счет введения паратироидного гормона крысам, у которых были удалены паратироидные железы. Эта модель описана в Russel et al, b Calcified Tissue Rescarch 183 (1970); Muhebouer et al, 5 Mineral Electrolite Metabolism 296 (1981), в патенте N США 761406, Flora et al, 1988, и в Европейской патентной публикации N 298553, Ebetino, 1989.
Другой модель является "модель Схенка", в которой определяют действие активного по отношению к костной ткани фосфоната на рост костей у молодых крыс. Эта модель описана в Schenk et al, 11 Caleif. Tissul Res. 196 (1973); Slinoda et al, 35 Calcif. Tissne Int., 87 (1983), патенте США N 4761406, Flora et al, 1988 и в Европейской патентной публикации N 298553, Ebetino, 1989.
Другой моделью является модель на "овариэктомизованных" или "OVX" крысах, в которой определяют способность активных по отношению к костям фосфонатов предотвращать потери костной ткани у самок крыс, вызываемой удалением яичников (овариэктомия). Эта модель описана Вронским с сотр. 125 Endocrinology 810 (1989).
LED (МЭД) для парентеральных доз предпочтительных активно действующих на кости фосфонатов, используемых в изобретении, составляет 1,0 мг P/кг для 1-гидроксиэтан-1,1-бисфосфоновой кислоты; 0,5 мг P/кг для дихлорметанбисфосфоновой кислоты; 0,03 мг/кг для 3-амино-1-гидроксипропан-1,1-бисфосфоновой кислоты; 0,01 мг P/кг для 4-амино-1-гидроксибутан-1,1бисфосфоновой кислоты; 0,1 мг P/кг для 6-амино-1-гидроксигексан-1,1-бисфосфоновой кислоты; 0,01 мг P/кг для N-(2-пиридил)аминометан-1,1-бисфосфоновой кислоты; 0,0003 мг P/кг для 2-(3-пиридил)-1-гидроксиэтан-1,1-бисфосфоновой кислоты; 0,0001 мг/кг для N-(циклогептил)-аминометанбисфосфоновой кислоты; 0,0001 мг P/кг для 3-(N-пентил-N-метиламино)-1-гидроксипропан-1,1-бисфосфоновой кислоты; 0,01 мг P/кг для 3-(диметиламино)-1-гидроксипропан-1,1-бисфосфоновой кислоты; 0,01 мг P/кг для 3-(N-пирролидино)-1-гидроксипропан-1,1-бисфосфоновой кислоты; 0,03 мг P/кг для N-циклогептиламинометанбисфосфоновой кислоты; 0,3 мг P/кг для S-(пара-хлорфенил)тиометанбисфосфоновой кислоты.
LED для орального введения должны быть выше в связи с системой адсорбции фосфонатов. Обычно адсорбция при оральном введении составляет около 1 - 10%. Таким образом, LED для орального введения обычно бывают в 10 - 100 раз выше, чем для парентерального введения.
В том смысле, как он здесь использован, термин "мг Р/кг" означает количество соединения, выраженное в миллиграммах фосфора в соединении на кг веса пациента. Выражение количества соединения в единицах содержания в нем фосфора ("мг Р") дано для того, чтобы можно было стандартизовать количество фосфонатов, используемых в фармацевтических композициях и способах изобретения. Так, например, 2-(2'-пиперидинил)-этан-1-фосфоно-1- метилфосфоновая кислота имеет молекулярный вес 271 г/моль, из которых 22,9% (62 г/моль) связано с двумя атомами фосфора, присутствующими в этой молекуле. Поэтому 1 мг этого соединения, по расчетам, содержит 0,229мг Р (1 мг х 22,9%). Поэтому для получения фармацевтической композиции, содержащей 1,0 мг Р этого соединения, композиция должна содержать около 4,4 мг этого соединения; для дозы 1,0 мг Р/кг этого соединения для пациента весом 50 кг доза должна составлять около 220 мг этого соединения.
Аналогично LED эстрогенного гормона представляет собой количество гормона, которое само по себе эффективно для предотвращения потерь костной ткани у пациентов, страдающих остеопорозом. Этот уровень обычно считается около 0,625 мг в день конъюгированного эстрогена или эквивалента дозе других экстрогенных гормонов (например, 25 мг в день этинил-эстрадиола или 2 мг в день 17- β -экстрадиола) (Barzil. Экстрогены для предотвращения или лечения остеопороза, связанного с постменопаузой. Обзор, 85, American Journal of Meolieine 847 (1988); Lindsay ef al. Минимальная эффективная доза эстрогена для предотвращения потерь костной ткани в связи с постменопаузой, 63, Obstetries anb Gynecology 759 (1984); Genantet. al. Влияние экстронсульфата на потерю костной ткани в связи с постменопаузой, 76, Dbstetries and Gynecology 529 (1990).
Активно действующий на кости фосфонат и эстрогенный гормон можно вводить параллельно или последовательно. Предпочтительно эстрогенный гормон принимать ежедневно при дневной дозе от около 0,2 до около 0,8 LED. Медроксипрогестерон (и/или эквивалентный гормон, например прогестерон) можно вводить параллельно, чтобы уменьшить возможность побочных эффектов эстрогенного гормона. Эстрогенный гормон можно также вводить в режиме циклов. Один такой цикл включает прием эстрогенного гормона в течение одного или более дней, а затем следует "свободный" период из одного или более дней, в течение которого активное соединение не принимают; при этом циклы повторяются. Один такой циклический режим для приема эстрогенного гормона состоит в приеме эстрогенного гормона в течение 21 дня, с последующим свободным от приема промежутком в 7 дней. Медоксипрогестерон можно принимать и во время свободного периода. Другой такой циклический режим для приема эстрогенного гормона сводится к приему эстрогенного гормона в течение около 14 дней, а затем приема эстрогенного гормона вместе с медоксипрогестероном в течение около 11 дней. Такие режимы описаны в статье: Ruby. Гормональная замещающая терапия - Как выбрать лучший препарат и режим, 88, Postgraduate Medicine 157 (1990).
Предпочтительный способ введения активно действующего на кости фосфоната - ежедневный, при условии приема по крайней мере около 0,1 LED активного соединения. Другой предпочтительный способ введения активно действующего на кости фосфоната - циклический режим, включающий введение по крайней мере около 0,1 LED активного соединения в течение одного или более дней, после чего следует один или более день, когда активно действующий на кости фосфонат не принимают, с повторением цикла. Такие циклические режимы описаны в патентах США N 4761406, Flora et. al, 1988; N 4812304, Anderson et. al, 1989; N 4822609, Flora, 1989. Предпочтительный способ изобретения выключает циклическое введение 1-гидроксиэтан-1,1-бисфосфоновой кислоты или ее фармацевтически приемлемой соли, а циклы включают прием фосфоната в течение около 14 дней с последующим свободным периодом около 76 дней. В течение этого свободного периода можно принимать дополнительный кальций в продуктах питания.
Способы изобретения включают лечение остеопороза на всех стадиях заболевания. Так как остеопороз является повседневным процессом утраты костной ткани, а не заболеванием с определенным началом или конечной точкой, "лечение", как здесь указано, состоит в любом из способов, которые останавливают, замедляют или обращают процесс потери костной ткани, который происходит при остеопорозе. Соответственно предпочтительным способом изобретения является способ, который включает лечение женщин в период постменопаузы до того, как у пациентки произошли значительные потери массы скелета. Такие предпочтительные способы являются, по существу, способами предотвращения остеопороза. Предпочтительно, чтобы такие способа включали лечение указанных пациентов в период постменопаузы, начиная непосредственно с менопаузы. Такое лечение предпочтительно длится по крайней мере пять лет.
Предпочтительный способ изобретения также включает лечение остеопороза у пациентов, которые уже потеряли скелетную массу (здесь и далее употребляется термин "установившийся остеопороз"). Такие способы изобретения для лечения установившегося остеопороза предпочтительно включают введение активных соединений в течение промежутка времени, достаточного для достижения возрастания чистой скелетной массы указанного пациента. Повышение массы может происходить в кортикулярной кости или трабекулярной кости или в них обоих. Предпочтительно, чтобы чистая масса скелета увеличилась по крайней мере на около 1% и более предпочтительно по крайней мере на около 5%.
Конкретный промежуток времени, достаточный для достижения увеличения массы скелета пациента, может зависеть от целого ряда факторов. Такие факторы включают, например, конкретно используемые активные соединения, количество вводимых активных соединений, возраст и пол пациента, конкретное заболевание, подлежащее лечению, сопутствующую терапию (если она есть), общее физическое состояние пациента (включая наличие других заболеваний), степень утраты костной ткани у пациента и привычную пищу пациента.
Способы изобретения предпочтительно продолжаются в течение по крайней мере около 6 мес, и предпочтительно по крайней мере около 12 мес. Естественно, такой прием можно продолжать неопределенно, в соответствии с известной в медицине практикой. Предпочтительно лечить пациента до тех пор, пока скелетная масса не достигнет такого значения, при котором клинически определят отсутствие опасности переломов у пациента (B. L. Riggs et. al. Jnvolntional Osteoporasis, 314, New England J. of Medicine (1986).
В способе изобретения "введение" относится к любому используемому способу, который в медицинской практике обеспечивает поступление активного соединения в организм пациента, подлежащего лечению таким образом, чтобы он был эффективен в построении костной ткани. Активные соединения можно вводить известными способами, например орально, через кожу или слизистую (например, через кожу, под язык, через нос, ректально), парентерально (например, подкожными инъекциями, внутримышечными инъекциями, внутривенными инъекциями) и с помощью ингаляций. Таким образом, конкретный тип введения включает, например, оральный, через кожу, через слизистую, под язык, внутримышечно, внутривенно, внутрибрюшинно, под кожу и поверхностное нанесение.
Предпочтительный способ лечения остеопороза включает начальную стадию диагностики для определения наличия заболевания. Так, предпочтительный способ изобретения включает стадии диагностики организма человека для определения остеопороза и после получения положительных результатов этой диагностики введение активного соединения в соответствии со способами изобретения. Для таких способов лечения пациенток в стадии постменопаузы до заметной потери костной ткани указанная начальная диагностическая стадия включает проведение диагностики для определения менопаузы. Такие способы хорошо известны специалистам и включают определение костной массы и степени реконструкции костей. Скорость реконструкции костей можно определить измерением с помощью биохимических маркеров Hui et. al. Вклад потери костной ткани в остеопороз во время менопауз, 1, Osteoporosis Jnt, 30(1990).
Подходящие диагностики для определения установившегося остеопороза также хорошо известны специалистам. Такие способы включают измерение радиоплотности радиограмм скелета, количественную компьютерную томографию, простую абсорбометрию энергии протонов и двойную абсорбометрию энергии протонов. Диагностические методики наряду с этими описаны в W.A. PecK et al. Руководство по физическим методам при остеопорозе (1987), опубликованном Национальным фондом остеопороза.
Активно действующие на кости фосфонаты и эстрогенные гормоны можно вводить в любые фармацевтически приемлемые композиции. Такие композиции могут содержать активное соединение и фармацевтически приемлемый носитель или могут содержать оба активных соединения и фармацевтически приемлемый носитель. Соответственно композиции для совместного приема обоих активных соединений включают:
а) по крайней мере около 0,1 LED активно действующего на кости фосфоната;
в) от около 0,2 до около 0,8 LED эстрогенного гормона;
с) фармацевтически приемлемый носитель.
Фармацевтически приемлемые носители включают твердые или жидкие разбавители или наполнители или инкапсулированные вещества, их смеси, которые пригодны для введения человеку или низшим животным. Термин "совместимый" относится к компонентам фармацевтических композиций, которые можно смешивать с активными соединениями и друг с другом таким образом, что между ними нет взаимодействия, которое могло бы существенно снизить фармацевтическую эффективность фармацевтической композиции в обычных условиях использования. Фармацевтически приемлемый носитель, естественно, должен быть достаточно высокой степени чистоты и достаточно низкой токсичности для того, чтобы его можно было принимать людям или низшим животным.
Некоторые примеры веществ, которые могут служить в качестве фармацевтически приемлемых носителей, включают: сахара, такие, как лактоза, глюкоза и сахароза, такие крахмалы, как кукурузный и картофельный; целлюлозу и ее производные, такие, как натрийкарбоксиметилцеллюлоза, этилцеллюлоза, ацетат целлюлозы" порошок трагаканта; солод; желатин, тальк, стеариновую кислоту, стеарат магния, растительные масла, такие, как арахисовое масло, хлопковое масло, кунжутное масло, оливковое масло, кукурузное масло и масло теоброма; такие полиоли, как пропиленгликоль, глицерин, сорбит, маннит и полиэтиленгликоль; агар, альгининовую кислоту, воду, очищенную от пирогенов, изотонический физиологический раствор; растворы фосфатных буферов, смачивающие агенты и такие смазки, как натрийлаурилсульфат, окрашивающие агенты, отдушки и вкусовые агенты, и консерванты. Другие совместимые фармацевтические добавки и активные соединения также могут быть включены в фармацевтические приемлемые носители для использования в композициях изобретения.
Выбор фармацевтически приемлемого носителя для использования вместе с активным соединением определяется тем способом, которым предстоит вводить активное соединение. Если активное соединение вводят путем инъекции, предпочтительным фармацевтическим носителем является стерильная вода, физиологический раствор или их смеси. pH таких композиций для парентерального введения предпочтительно устанавливают около 7,4. Подходящие фармацевтически приемлемые носители для поверхностного нанесения включают такие, которые известны специалистам для использования в кремах, гелях, повязках, пластырях и аналогичных способах поверхностного нанесения.
Фармацевтически приемлемый носитель, используемый вместе с активными ингредиентами, используют в концентрациях, достаточных для того, чтобы обеспечить практически использование и размер, соотносимый с дозой. Фармацевтически приемлемые носители обычно могут составлять около 0,1 - 99,9 мас.% фармацевтической композиции изобретения, предпочтительно около 5 - 80%, и наиболее предпочтительно около 10 - 50%.
Предпочтительный способ введения активных соединений - оральный прием в форме единичной дозы (то есть в дозах, содержащих такое количество активного вещества, которое пригодно для приема в единичной дозе в соответствии с известной медицинской практикой). Предпочтительные единичные дозированные формы включают таблетки, капсулы, суспензии и растворы, содержащие безопасное и эффективное количество активного соединения. Фармацевтически приемлемые носители, пригодные для приготовления единичных дозированных форм для орального приема, хорошо известны специалистами. Их выбор зависит от таких вторичных факторов, как вкус, стоимость, стабильность, которые не являются критическими для целей и которые могут быть учтены с легкостью специалистами. Предпочтительно, чтобы оральные единичные дозовые формы активно действующих на кости фосфонатов содержали от около 1 мг P до около 600 мг P фосфоната.
В изобретении предложены также наборы для удобного и эффективного воплощения способов изобретения. Такие наборы включают одну или более единичных доз активного для костей фосфоната, одну или более единичных доз эстрогенного гормона и средства для облегчения соответствия способам изобретения. Такие комплекты обеспечивают эффективные средства для обеспечения того, чтобы пациент, подлежащий лечению, принял соответствующее активное соединение в правильной дозе и правильным образом. Такие комплекты особенно предпочтительны в способах изобретения, в которых используются циклические режимы для введения каждого или обоих активных соединений.
Согласующие средства таких комплектов включают средства, которые облегчают введение активных соединений по способу изобретения. Такие вспомогательные средства включают инструкции, упаковки и распределительные средства и их комбинации. Примеры упаковок и распределительных средств хорошо известны специалистам и включают те, которые описаны в патентах США N 4761496, Flora et. al, 1988, и N 4812311, Uchtmon, 1989.
Следующие примеры иллюстрируют композиции и способы применения изобретения, но не ограничивают его.
Пример 1. Женщину весом около 60 кг, страдающую остеопорозом, в связи с менопаузой лечат способом согласно изобретению. Более конкретно - в течение двух лет:
1) динатрий-1-гидроксиэтан-1,1-бисфосфонат вводят в циклическом режиме, причем каждый цикл состоит из орального приема таблеток1, содержащих 200 мг фосфоната ежедневно в течение 14 дней, затем следует 76-дневный перерыв (свободный период), во время которого пациентка не принимает никаких активно действующих на кости фосфонатов;
2) вводят конъюгированный эстроген при ежедневном приеме таблеток2, содержащих по 0,3 мг активного соединения. В этом режиме активно действующий на кости фосфонат вводят в количестве около 0,5 LED, а эстрогенный гормон вводят в количестве около 0,5 LED. Плотность позвоночника пациентки определяют фотонной абсорбциометрией с двойной энергией, которая свидетельствует о повышении массы костной ткани.
1. Продается Norvich Eaton Pharmacentical, Jnc. под торговой маркой "Didronel" в таблетках, содержащих 200 мг активного соединения, в носителе-стеарате магния, микрокристаллической целлюлозе и крахмале.
2. Продается Wyeth - Ayerst Laboratories под торговой маркой "Premarin" в носителе - трехосновном фосфонате кальция, безводном сульфате кальция, воске rarnanba, глицеринмоноолеате, лактозе, стеарате магния, метилцеллюлозе, микрокристаллической целлюлозе, полиэтиленгликоле, стеариновой кислоте, тальке и двуокиси титана.
Пример 2. Пациентку, женщину весом около 60 кг, страдающую остеопорозом, связанным с менопаузой, лечат способом согласно изобретению. Конкретно - в течение одного года:
1) ежедневно дают 2-(3-пиридид)-1-гидроксиэтан-1,1-бисфосфоновую кислоту в таблетках, содержащих 15 мг активного соединения;
2) ежедневно дают 17- β -эстрадиол в виде накожного пластыря, поставляющего 0,03 мг активного соединения в день.
В таком режиме активно действующий на кости фосфонат вводят в количество около 1,0 LED, а эстрогенный гормон вводят в количестве около 0,5 LED. Плотность тканей позвоночника пациентки измеряют с помощью фотонной абсорбциометрии с удвоенной энергией и получают свидетельство возрастания костной массы. В этом примере нижеследующие активно действующие на кости фосфонаты: дихлорметанбисфосфоновая кислота, 3-амино-1-гидроксипропан-1,1-бисфосфоновая кислота, 4-амино-1-гидроксибутан-1,1-бисфосфоновая кислота, 6-амино-1-гидроксигексан-1,1-бисфосфоновая кислота; N-(2-пиридил)аминометан-1,1-бисфосфоновая кислота; -2-(2-пиридил)-1-гидроксиэтан-1-фосфоно-1-метилфосфиновая кислота, 2-(3-пиридил)-1-гидроксиэтан-1-фосфоно-1-метил-фосфиновая кислота; 2-(N-имидазол)-1-гидроксиэтан-1-фосфоно-1-метилфосфиновая кислота; 3-(N-метиламино)-1-гидроксипропан-1-фосфоно-1-метилфосфиновая кислота; 4-амино-1-гидроксибутан-1-фосфоно-1-метилфосфиновая кислота; 3-(N-пирролидино)-1-гидроксипропан-1-фосфоно-1-метилфосфиновая кислота, N-циклогептилметанфосфонометилфосфиновая кислота, S-(пара-хлорфенил)тиометанфосфонометилфосфиновая кислота, (7-дигидро-1-пириндин)метанфосфонометилфосфиновая кислота, (7-дигидро-1-пириндин)гидроксиметанфосфонометилфосфиновая кислота, (6-дигидро-2-пириндин)гидроксиметанфосфонометилфосфиновая кислота, 2-(6-пиролопиридин)-1-гидроксиэтан-1-фосфоно-1-метилфосфиновая кислота, 2-(3-пиридил)-1-гидроксиэтан-1; 1-бисфосфоновая кислота, 2-(N-имидазоил)-1-гидроксиэтан-1,1-бисфосфоновая кислота, 3-(N-пентил-N-метиламино)-1-гидроксипропан-1,1-бисфосфоновая кислота, 3-(N-пирролидино)-1-гидроксипропан-1,1-бисфосфоновая кислота, N-циклогептиламинометанбисфосфоновая кислота, S-(пара-хлорфенил)тиометанбисфосфоновая кислота, (7-дигидро-1-пириндин)метанбисфосфоновая кислота, (7-дигидро-1-пириндин)гидроксиметанбисфосфоновая кислота, (6-дигидро-1-пириндин)гидроксиметанбисфосфоновая кислота и 2-(6-пиролопиридин)-1-гидроксиэтан-1,1-бисфосфоновая кислота могут быть заменой 2-(2-пиридил)-1-гидроксиэтан-1,1-бисфосфоновой кислоты в сравнимых количествах и с практически аналогичными результатами.
Пример 3. Пациентку весом примерно 60 кг осматривают спустя примерно 6 мес после спонтанной менопаузы и обнаруживают, что у нее низкая костная масса и ненормально высокая скорость реконструкции костей. После этого пациентку лечат способом согласно изобретению для предотвращения остеопороза. Конкретно ежедневно в течение 5 лет пациентка принимает таблетку со следующим содержанием:
Компонент - мг в таблетке
2-(2'-Пиперидинил)-этан-1-фосфоно-метилфосфиновая кислота - 120
Конъюгированный эстроген - 0,5
Лактоза - 80
Микрокристаллическая целлюлоза - 50
Натрийкрахмалгликолят - 7,5
Стеарат магния - 1,5
Каждая таблетка содержит около 0,3 LED активно действующего на кости фосфоната и около 0,8 LED эстрогенного гормона. Плотность позвоночника пациентки определяют, и оказывается, что не происходит заметного снижения костной массы.
Способ лечения остеопороза у человека или животных включает введение активно действующего на кости фосфоната указанному субъекту в количестве по крайней мере около 0,1 LED и эстрогенного гормона в количестве от около 0,2 до около 0,8 LED в день в течение курса лечения. Активно действующим на кости фосфонатом является предпочтительно бисфосфонат или фосфоноалкилфосфонат. Изобретение позволяет остановить, замедлить или предотвратить процесс потери костной ткани, происходящий при остеопорозе. 3 с. и 16 з.п. ф-лы.
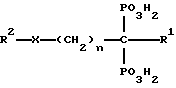
где n = 0-7 целое число;
R1 - водород, хлор, амино или гидрокси;
X - N4 - кислород или простая связь;
R2 - 5-7-членным гетероциклом, содержащим 1-3 гетероатомов, амино, амин, замещенный одной или двумя низшими алкильными группами, или водород,
и их фармацевтически приемлемые соли и сложные эфиры.
| US 4812311 C (Еhe Procter & Gamble Company), 14.03.89, A 61 K 31/66. |
Авторы
Даты
1998-06-27—Публикация
1992-01-31—Подача