Изобретение относится к способам увеличения костной массы человека и других животных, например, к способам лечения остеопороза и связанных с ним нарушений обмена веществ в костях. В частности, настоящее изобретение относится к таким способам лечения, которые предусматривают введение фосфоната, активного по отношению к костям, и гормона околощитовидной железы.
Наиболее частым нарушением обмена веществ в костях является остеопороз. Остеопороз можно в общих чертах определить как уменьшение количества костной ткани или атрофию скелетной ткани. Можно выделить два типа остеопороза: первичный и вторичный. "Вторичный остеопороз" является результатом действия вполне идентифицируемого болезненного процесса или агента. Однако приблизительно 90% всех случаев остеопороза является "первичным остеопорозом". Такой первичный остеопороз включает постклиматический остеопороз, возрастной остеопороз (который поражает большинство людей в возрасте от 70 до 80 лет) и остеопороз неясного происхождения, который поражает людей среднего возраста, а также мужчин и женщин более младшего возраста.
Для некоторых людей, подверженных остеопорозу, потеря костных тканей настолько значительна, что она вызывает механическое разрушение структуры кости. Разрушение кости часто возникает, например, в области тазобедренного сустава и позвоночника у женщин, страдающих постклимактерическим остеопорозом. Можно также возникнуть горб (ненормальное высокое искривление грудной кости).
Механизм потери костной ткани при остеопорозе, как полагают, включает дисбаланс процесса "коррекции кости". Коррекция кости происходит в течение всей жизни человека и обеспечивает обновление скелета и поддержание прочности кости. Эта коррекция включает эрозию и восполнение дискретных (незаполненных) участков на поверхности кости с помощью самоорганизованной группы клеток, которые называют "основными многоклеточными единицами" или ОМЕ. ОМЕ в основном состоит из "остеокластов", "остеобластов" и их клеточных предшественников. Во время цикла коррекции кость рассасывается по месту "активированного" ОМЕ с помощью остеокласта с образованием впадины рассасывания. Эта впадина затем заполняется костной тканью с помощью остеобластов.
Обычно у взрослых людей цикл коррекции приводит (вследствие неполного заполнения впадины рассасывания) к небольшому дефициту костной ткани. Таким образом, даже у здоровых взрослых людей наблюдается связанная с возрастом потеря костной ткани. Однако при остеопорозе наблюдается повышение количества активированных ОМЕ. Эта повышенная активность приводит к ускорению процесса коррекции кости, в результате чего происходит увеличение потери костной ткани.
Хотя этиология процесса неясна, существует много факторов риска, которые, как полагают, связаны с остеопорозом. Они включают небольшой вес тела, низкий уровень усвоения кальция, недостаточную физическую активность и недостаток эстрогена.
В медицинской литературе описаны многочисленные составы и способы для "лечения" остеопороза. Во многих из этих составов и способов предпринимаются попытки замедлить потерю костной ткани или вызвать общее увеличение костной массы (например, сообщения в P.C.Haynes, Jr.et al., "Agents Affecting Calcification, The Pharmacological Basis of Therapeutics, 7 th Edition (A.G. Gilman, L. S. Goodman et al., Editors, 1985); G.D. Whedon et al., "An analysis of Current Concepts and Research Interest in Osteoporosis", Current Advances in Skeletogenesis (A. Ornoy, et. al., Editors, 1985); и W.A. Peck et al., Physician's Resource Manual on Osteoporosis, 1987 - опубликованные Национальной ассоциацией остеопороза).
Одним из способов лечения остеопороза, предложенных в литературе, является введение бисфосфонатов или других активных по отношению к костям фосфонатов (например, Storm et al., "Effect of Intermittent Cyclical Etidronate Therapy on Bone Mineralyation and Fracture Rate in Women with Post-Menopausal Osteoporosis", 322, New England Journal of Medicine, 1265 (1990); u Watts et al. , "Intermittent Cyclical Etidronate Treatment of Post-Menopausal Octeoporosis", 323, New England Journal of Medicine, 73, 1990). Такое лечение с использованием многочисленных бисфосфонатов описано в патенте США 4761406 (авторы Флора и др. , опубликован 2 августа 1988), патенте США 4812304 (авторы Андерсон и др. , опубликован 14 марта 1989), патенте США 4812311 (автор Ухтман, опубликован 14 марта 1989), и патенте США 4822609 (автор Флора, опубликован 18 апреля 1989). Использование указанных фосфонатов для лечения остеопороза и других расстройств, включающих ненормальных обмен кальция и фосфора, описано также в патенте США 3683080 (автор Фрэнсис, опубликован 8 августа 1972), патенте США 4267108 (авторы Блюм и др., опубликован 12 мая 1981), Европейском патенте 298553 (автор Эбетино, опубликован 11 января 1989), и Fancis et al., Chemical, Biochemical and Medicinal Ptoperties of the Diphosphonates", The Role of Phosphonates in Living Systems, Chapter 4; 1983.
Гормон околощитовидной железы также предлагался в качестве терапевтического средства для лечения остеопороза. Такие способы лечения с применение гормона околощитовидной железы приводятся в следующих публикациях: Hefti et al., "Jucnase of whole-Bode Calcium and skeleton Mass in Normal and Osteoporosis Adult Rats Freated wirth Paratheroid Hormone", 62, Clin. Sci, p. 389-396, 1982, патент Германии 3935738 (автор Форссман, опубликован 8 мая 1991), патент США 4698328 (авторы Неер и др., опубликован 6 октыбря 1987), и патент США 4833125 (авторы Неер и др., опубликован 23 мая 1989).
Воздействие, вызываемое введение бисфосфонатов и гормона околощитовидной железы, изучалось на крысах. Исследования показали, что увеличение костной массы в большей степени наблюдается у крыс, которым вводили бисфофонаты и гормон околощитовидной железы, нежели у крыс, которым вводили лишь гормон околощитовидной железы (Hock et al., "Resorbtion is not Essential for the Stimulation of Bone Growth by hPTH-(1-34) in Rats in Vivo", 4(3), Inl. of Bone and Mineral Res. 449-458, 1989).
В качестве терапии при остеопорозе у людей были предложены циклические назначения гормона околощитовидной железы и активных по отношению к костям фосфонатов. Такие способы лечения с использованием бисфосфонатов и гормона околощитовидной железы приводятся в следующих публикациях, которые представлены здесь для справки: патент США 4822609 (автор Флора, опубликован 18 апрель 1989), патент США 4812304 (авторы Андерсон и др., опубликован 14 марта 1989), патент Германии 3243358 (автор Хеш, опубликован 24 мая 1984), и Hesch et al. , "Results of a Stimulatory Therapy of Low Bone Metabolism in Osteoporosis with (1-38) hPTH and Diphosphonate EHDP", 66(19), Klin, Wschr., p. 976-984 (Oct. 1988).
Далее, короткий цикл использования гормона околощитовидной железы и активного по отношению к костям фосфоната описывается в следующих публикациях: патент Германии 3243358 (автор Хеш и др., опубликован 24 мая 1984 (далее обозначается как "DE 3243358"), Hesch et al., "Results of stimulatory Therapy of Low Bone Metabolism in Osteoporosis with (1-38) hPTH and Diphosphonate EHDP" 66 (19) Klin. Wschr. 976-984 (Oct 1988) (далее обозначается как "Хеш и др. "), Delling et al., "Morpholic Study of Pelvic Crest Spongiosa in Patients with Osteoporosis Luring ADFR Therapy with Paratheroid Hormone and Diphosphonates", 128(1), Z. Orthop.,
1-5 (1990) (далее обозначается как "Деллинг и др."), и Delmas et al., "The In Vivo Anabolic Effect of hPTH - (1-34) Is Blunted when Bone Resorbtion Is Blocked by a Bisphosphonate", 6(1), J.Bone Mineral Res., S 136 # 214 Ang, 1991 (далее обозначается как "Делмас").
Однако методы, приведенные в DE 3243358, Хешем и др., Деллингом и др., хотя и полезны для активирования процесса обмена в костях, не приводят к эффективному увеличению костной массы. Деллинг и др. особенно скептически оценивают эффективность терапии с использованием гормона околощитовидной железы - бисфосфоната для увеличения костной массы. Деллинг и др. делают вывод, что значительные изменения в костной структуре не наблюдаются и что полезность такой терапии является спорной. Далмас также скептически относится к эффективности терапии с использованием гормона околощитовидной железы и бисфосфоната, поскольку клинические испытания показывают, что гормон околощитовидной железы сам по себе эффективен для образования костной ткани, однако его сочетание при введении с бисфофонатом является менее эффективным для увеличения костной ткани по сравнению с контрольной группой (т.е. не подвергавшейся воздействию).
Заявителями неожиданно обнаружено, что введение активного по отношению к костям фосфоната и гормона околощитовидной железы приводит к увеличению костной массы. Такие образом, в способах по настоящему изобретению заявляются эффективные методы предотвращения и лечения остеопороза, которые обладают меньшими побочными эффектами по сравнению с известными в данной области техники.
В настоящем изобретении заявляются способы увеличения костной массы у людей или других животных, пораженных остеопорозом, представляющие собой 30-дневный период лечения и включения схемы назначения гормона околощитовидной железы и схемы назначения бисфосфоната, в которых:
а) указанные схемы назначения гормона околощитовидной железы включают введение указанному пациенту гормона околощитовидной железы в количестве приблизительно 4 - 15 ME /кг в день при условии, что указанный гормон околощитовидной железы вводят по крайней мере один раз в семь дней в течение каждого указанного 30-дневного периода лечения; и в которых
б) указанные схемы назначения бисфосфоната включают введение указанному пациенту бисфосфоната в количестве приблизительно 0,0005 - 1,0 мгР/кг в день при условии, что указанный бисфосфонат вводят по крайней мере один день в течение каждого указанного 30-дневного периода лечения.
Способы по настоящему изобретению включают назначение активного по отношению к костям фосфоната и гормона околощитовидной железы человеку или другому животному. Конкретные соединения и композиции, которые необходимо использовать в этих способах, должны, таким образом, быть фармацевтически приемлемыми. В контакте настоящего изобретения термин "фармацевтически приемлемый" означает такой компонент, который пригоден для использования для людей и/или животных и не проявляет нежелательных побочных эффектов (таких как токсичность, раздражающее действие и аллергическое воздействие), соразмерных с разумным отношением польза/риск. Далее, в контексте настоящего изобретения термин "безопасное и эффективное количество" относится к такому количеству компонента, которое достаточно для получения желаемого терапевтического воздействия, не оказывающего нежелательных побочных эффектов (таких как токсичность, раздражающее действие и аллергическое воздействие), соразмерных с разумным отношением польза/риск, при использовании предлагаемого изобретения. Конкретное "безопасное и эффективное количество" будет, очевидно, изменяться в зависимости от таких факторов, как конкретное состояние, лечение которого приводится, физическое состояние пациента, продолжительность лечения, вид конкретной терапии и конкретные используемые составы.
Способы по настоящему изобретению, включают введение активных по отношению к костям фосфонатов. По предлагаемому изобретению "активный по отношению к костям фосфонат" включает один или несколько соединений общей формулы: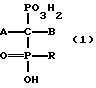
и их фармацевтически приемлемые соли или простые эфиры, где значения A, B или R указаны ниже.
В формуле (I) R обозначает гидроксил (для бисфофонатов) или атом водорода или алкил (в фосфоноалкилфосфонатах). В фосфоноалкилфосфонатах R преимущественно является незамещенным алкилом, в частности, низшим алкилом. Если P обозначает замещенный алкил, то предпочтительным заместителями являются галоген, незамещенный или замещенный фенил, незамещенный или замещенный пиридил, незамещенная аминогруппа, аминогруппа, замещенная одной или двумя низшими алкильными группами, гидроксил или карбоксильная группа. Более предпочтительными заместителями являются атом фтора, фенил, незамещенная аминогруппа и гидроксил; наиболее предпочтительным является атом фтора (особенно, если он присутствует в составе трифторметильной группы) и фенил.
Наиболее предпочтительными фрагментами R в фосфоноалкилфосфонатах являются незамещенные низшие алкильные группы, в частности, незамещенные насыщенные алкильные группы с прямой цепью. Также предпочтительными фрагментами R являются метил, этил, н-пропил, изо-пропил, н-бутил, изо-бутил, втор-бутил, трет-бутил и н-гексил. Более предпочтительно, если R обозначает метил, этил, н-пропил или н-бутил. Наиболее предпочтительным значением R является метил.
В формуле (I) A обозначает атом водорода, атом галогена, нитрогруппу, алкил, гетероцикл, арил, гетероарил, незамещенную аминогруппу или ее амид, получаемый конденсацией с карбоновой кислотой замещающей группы, аминогруппу, замещенную одним заместителем, или ее амид, получаемый конденсацией с карбоновой кислотой замещающей группы; аминогруппу, независимо замещенную алкильной группой и одним заместителем, гидроксил или его сложный эфир, полученный конденсацией с карбоновой кислотой замещающей группы; тиол или его тиоловый эфир, получаемый конденсацией с карбоновой кислотой замещающей группы; тиоэфир, имеющий заместитель, или его сульфоксидное или сульфонильное производное; сульфогруппу, ее фармацевтически приемлемые соли, ее сложный эфир, получаемый конденсацией со спиртом замещающей группы, ее незамещенный амид или ее амид, замещенный одной или двумя алкильными группами; карбоксильную группу, ее фармацевтически приемлемые соли, ее сложный эфир, получаемый конденсацией со спиртом замещающей группы, ее незамещенный амид или ее амид, замещенный одной или двумя алкильными группами; альдегидную группу, кетонную группу, имеющую заместитель; карбаматную группу, незамещенную или замещенную одной или двумя алкильными группами; пептидильные группы, включающие остатки от 1 до 100 аминокислот; или фрагменты A и B ковалентно связаны и образуют кольцо, содержащее 3 - 7 атомов с 0 - 3 гетероатомами, выбранными из группы, включающей атом азота, серы, фосфора или кислорода, при этом кольцо является незамещенным или замещенным одним или большим количеством заместителей, указанных выше для A; или же фрагменты A и B замещаются незамещенными или замещенными алкильными фрагментами, которые присоединены к геминальному атому углерода (атому углерода, показанному в структуре (I), приведенной выше) с помощью двойной связи.
A преимущественно обозначает следующие фрагменты:
(I) атом водорода,
(2) атом галогена (преимущественно атом фтора или атом хлора, наиболее предпочтительно атом фтора).
(3) замещенный или незамещенный алкил, имеющий общую структуру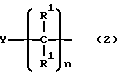
где
а) n обозначает целое число 1 - 10, предпочтительно 1 - 5, еще более предпочтительно 1 - 2, наиболее предпочтительно 1,
b) каждый R1 независимо является атом водорода, атомом галогена, низшим алкилом, незамещенной аминогруппой или ее амидом, полученным концентрацией с карбоновой кислотой низшей алкильной группы; аминогруппой, замещенной одной алкильной группой или ее амидом, полученным конденсацией с карбоновой кислотой низшей алкильной группы; аминогруппой, независимо замещенной двумя алкильными группами; гидроксилом или его сложным эфиром, полученным конденсацией с карбоновой кислотой низшей группы; карбоксильной группой, ее фармацевтически приемлемыми солями, ее сложным эфиром, получаемым конденсацией со спиртом низшей группы, ее незамещенным амидом или ее амидом, замещенным одной или двумя алкильными группами; группой -PO3H2 или ее фармацевтически приемлемыми слоями, и нитро-группой или два радикала R1 у одного атома углерода обозначают группы =O или =NR9 (где группа R9 является низшим алкилом или может обозначать атом водорода в том случае, если имеется другой атом азота, присоединенный к тому же атому углерода, что и группа =NR), или два радикала R1 у соседних атомах углерода могут замещаться на дополнительную связь между атомами углерода; или радикал R1 у первого атома углерода (в правой части формулы (2) и B (см. структуру (1), приведенную выше) могут замещаться на дополнительную связь; и
c) Y обозначает атом галогена, нитрогруппу, цианогруппу, гетероцикл, арил, гетероарил, незамещенную аминогруппу или ее амил, получаемый конденсацией с карбоновой кислотой алкила, гетероцикла, арила или гетероарильной группы; аминогруппу, замещенную одним алкилом, гетероциклом, арилом или гетероарильной группой, и ее амид, получаемый конденсацией с карбоновой кислотой алкильной группы; аминогруппу, независимо замещенную алкильной группой и одним алкилом, гетероциклом, арилом или гетероарильной группой; гидроксил и его эфир, полученный конденсацией с карбоновой кислотой алкила, гетероцикла, арила или гетероарильной группы; тиол и его тиоловый эфир, получаемый конденсацией с карбоновой кислотой алкила, гетероцикла, арила и гетероарильной группы; тиоэфир, содержащий алкил, гетероцикл, арил или гетероарильную группу, или его сульфоксидное или сульфонильное производное; сульфогруппу, ее фармацевтически приемлемые соли, ее эфир, получаемый конденсацией со спиртом алкильной группы, ее незамещенный амид или ее амид, замещенный одной или двумя алкильными группами; карбоксильную группу, ее фармацевтически приемлемые соли, ее эфир, получаемый конденсацией со спиртом алкильной группы, ее незамещенный амид или ее амид, замещенный одной или двумя алкильными группами; группу -PO3H2, ее фармацевтически приемлемые соли, ее эфир, полученный конденсацией со спиртом алкильной группы, ее незамещенный амид и ее амид, замещенный одной или двумя алкильными группами; группу -(R8)POOH (где R8 обозначает атом водорода или незамещенный низший алкил), ее фармацевтически приемлемые соли, ее эфир, полученный конденсацией со спиртом алкильной группы, ее незамещенный амид и ее амид, замещенный одной или двумя алкильными группами; альдегидную группу, кетонную группу, имеющую алкильную группу; карбаматную группу, незамещенную или замещенную одной или двумя алкильными группами; или пептидил. В случае бисфосфонатов Y преимущественно обозначает гетероцикл (предпочтительно 5- или 7-членный гетероцикл, содержащий один или два атома азота); аминогруппу, и замещенную аминогруппу. Наиболее предпочтительные фрагменты Y включают пиридил, аминогруппу и аминогруппу, замещенную одной или двумя алкильными группами. В фосфоноалкилфосфонатах Y преимущественно является атомом галогена (предпочтительно фтора); трифторметильной группой, простым эфиром, содержащим алкильную группу; незамещенной аминогруппой и ее амидом, полученным конденсацией с карбоновой кислотой низшей алкильной группы; аминогруппой, замещенной одной алкильной группой и ее амидом, полученным конденсацией с карбоновой кислотой низшей алкильной группы; аминогруппой, независимо замещенной двумя низшими алкильными группами; или пептидилом, содержащим от одной до приблизительно шести остатков аминокислот.
(4) циклоалкил, содержащий 4 - 10 атомов углерода, преимущественно 5 - 6 атомов углерода;
(5) гетероцикл, имеющий 5 или 6 атомов в кольце; более предпочтительно с одной или двумя атомами азота в кольце, еще более предпочтительно с одним атомом азота в кольце. Наиболее предпочтительным гетероциклами являются незамещенный или замещенный пиперидил, пиперазинил и морфолинил;
(6) незамещенный и замещенный фенил или нафтил;
(7) незамещенный или замещенный 5- или 6-членные циклические гетероарилы, содержащие один или два гетероатома (в частности, гетероатомы азота), преимущественно пиридинил;
(8) амино-содержащий фрагмент, имеющий общую структуру: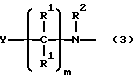
где а) m является целым числом 0 - 10, предпочтительно 0 - 5, более предпочтительно 0 - 1, наиболее предпочтительно 0;
b) значение R1 и Y указаны ранее, и
c) R2 обозначает атом водорода, низший алкил или ацил, полученный из карбоновой кислоты низшего алкила;
(9) кислородсодержащий фрагмент общей структуры: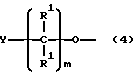
где а) m является целым числом 0 - 10, предпочтительно 0 - 5, более предпочтительно 0 - 1, наиболее предпочтительно 0;
b) значения R1 и Y указаны ранее;
(10) серусодержащий фрагмент общей структуры: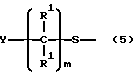
где а) m является целым числом 0 - 10, предпочтительно 0 - 5, более предпочтительно 0 - 1, наиболее предпочтительно 0;
b) значения R1 и Y указаны ранее.
В формуле (1) B обозначает атом водорода, атом галогена; незамещенный или замещенный низший алкил незамещенный или замещенный циклоалкил, содержащий 3 - 7 атомов в кольце; незамещенный или замещенный гетероцикл, содержащий 3 - 7 атомов в кольце; незамещенный или замещенный фенил; гидрокси или его сложный эфир, полученный конденсацией с карбоновой кислотой низшей алкильной группы; незамещенную аминогруппу или ее амид, полученный конденсацией с карбоновой кислотой низшей алкильной группы; аминогруппу, замещенную одной низшей алкильной группой, или ее амид, полученный конденсацией с карбоновой кислотой низшей алкильной группы; амино-группу, независимо замещенную двумя низшими алкильными группами; или карбоксильную группу, ее фармацевтически приемлемые соли, ее сложный эфир, полученный конденсацией со спиртом низшей алкильной группы, ее незамещенный амид или ее амид, замещенный одной или двумя низшими алкильными группами.
С целью обеспечения химической стабильности этих соединений, фрагменты А и В преимущественно обе не содержат гетероатомы (азот, кислород или серу) или гетероатом и атом галогена, связанные с фосфонатным фрагментом (т.е. атом углерода, геминально замещенный атомами фосфора). Так, когда фрагмент А содержит атомы кислорода, серы, азота или галогена, связанные с фосфорзамещенным метиленовым углеродом, то В выбирают из атома водорода, незамещенного или замещенного низшего алкила, циклоалкила, гетероцикла ( в котором атом углерода гетероцикла связан с гениальными атомами углерода) или фенила; карбоксильной группы, ее фармацевтически приемлемых солей, ее сложного эфира, полученного конденсацией со спиртом низшей алкильной группы, ее незамещенным амидом и ее амидом, замещенным одной или двумя алкильными группами.
Преимущественно В является атомом водорода, атомом галогена, незамещенным или замещенным низшим алкилом, незамещенным или замещенным фенилом, незамещенным или замещенным бензолом, гидроксилом или его сложным эфиром, полученным конденсацией с карбоновой кислотой низшей алкильной группы, тиолом, незамещенной аминогруппой или ее амидом, полученным конденсацией с карбоновой кислотой низшей алкильной группы, аминогруппой, замещенной одной низшей алкильной группой, или ее амидом, полученным конденсацией с карбоновой кислотой низшей алкильной группы, аминогруппой, независимо замещенной двумя низшими алкильными группами, или карбоксильной группой, ее фармацевтически приемлемыми солями, ее сложным эфиром, полученным конденсацией со спиртом низшей алкильной группы, ее незамещенным амидом или ее амидом, замещенным одной или двумя низшими алкильными группами.
Более предпочтительно, когда В является атомом водорода, атомом хлора, метилом, этилом, гидроксилом, тиолом, незамещенной аминогруппой, (N-метил)аминогруппой, N, N-диметил)аминогруппой, карбоксильной группой или ее фармацевтически приемлемой солью, группой -COOCH3 или -CONH2. Еще более предпочтительно В является атомом водорода, метилом, атомом хлора, аминогруппой или гидроксилом; более предпочтительно атомом водорода, или гидроксилом, или аминогруппой, или тиогруппой; наиболее предпочтительно гидроксилом. Наиболее предпочтительные активные по отношению к костям фосфонаты включают такие, в которых А являются фрагментом групп (3) или (8), представленных выше, а В является гидроксилом.
Наиболее предпочтительные бисфосфонаты, полезные согласно настоящему изобретению, имеют формулу: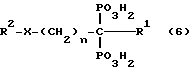
где n обозначает целое число 0 - 7 (преимущественно 0 - 2, еще более преимущественно 1): R1 является атомом водорода, атомом хлора, аминогруппой или гидроксилом (преимущественно атомом водорода или гидроксилом); X обозначает группу -NH-, атом кислорода или простую связь (преимущественно группу -NH- или простую связь); R2обозначает 5 - 7 - членный гетероцикл, содержащий 1 - 3 гетероатомов (преимущественно 6-членный гетероцикл, содержащий 1 или 2 атома азота), аминогруппу, аминогруппу, замещенную одной или двумя алкильными группами, или атом водорода, и их фармацевтически приемлемые соли и простые эфиры.
Термин "фармацевтически приемлемые соли и простые эфиры" в контексте настоящего изобретения означает способные гидролизоваться простые эфиры и соли активных по отношению к костям фосфонатов, обладающие теми же общими фармакологическими свойствами, что и кислоты, из которых они образованы, и являющиеся фармацевтически приемлемыми. Фармацевтически приемлемые соли включают, например, соли щелочных металлов (в частности, натрия и калия), соли щелочно-земельных металлов ( в частности, олова и индия), соли аммония и соли производных аммиака с низкомолекулярными заместителями ( в частности, моно-, ди- и триэтаноламин). Предпочтительными являются соли натрия, калия и аммония. Фармацевтически приемлемыми простыми эфирами являются незамещенные и замещенные алкильные, арильные и фосфорильные эфиры. Не ограничивающие настоящее изобретение примеры фармацевтически приемлемых эфиров включают, например, изо-пропильный, трет-бутильный, 2-хлорэтильный, 2,2,2-трихлорэтильный, 2,2,2, -трифторэтильный, n-толуолсульфонилэтильный, салицильный, саркозильный, бензильный, фенильный, 1,2-гексаноилглицерильный, n-нитрофенильный, 2,2-диметил-1,3-диоксолен-4-метильный, изопентенильный, о-карбометоксифенильный, паралоилоксиметилсалицилильный, диэтиламидофосфорильный, пивалоилоксиметильный, пропионилоксиметильный, изо-бутирилоксиметильный, додецильный, октадецильный и изо-пропилоксиметильный.
Конкретные примеры и определения для заместителей, полезных в соединениях по формулам (1) - (6), приводятся в Европейском патенте 298553 (автор Эбетино, опубликован 11 января 1989). В нем также приводятся фосфоноалкилфосфонаты, полезные в способах по настоящему изобретению (когда Р обозначает атом водорода или алкил) и в способах получения таких соединений. Способы получения фосфоноалкилсульфонатов описаны также в Европейском патенте 298555 (автор Эбетино, опубликован 11 января 1989), который приводится здесь для справки.
Бисфосфонаты, полезные в способах по настоящему изобретению (когда R обозначает гидроксил), и способы получения таких соединений описаны в следующих патентных публикациях, которые все приводятся здесь для справки: патент США 3553314 (автор Фрэнсис, опубликован 5 января 1971); патент США 3683080 (автор Фрэнсис, опубликован 8 августа 1972); патент США 3846420 (авторы Уолманн и др., опубликован 5 ноября 1974); патент США 3899496 (авторы Шиндлер и др., опубликован 12 августа 1975); патент США 3941772 (авторы Плоджер и др., опубликован 2 марта 1976); патент США 3957160 (авторы Плоджер и др., опубликован 18 мая 1976); патент США 3962432 (автор Шмидт-Дункер, опубликован 8 июня 1976); патент США 3979385 (авторы Уолманн и др., опубликован 7 сентября 1975); патент США 3988443 (авторы Плоджер и др., опубликован 26 октября 1976); патент США 4054598 ( авторы Блюм и др., опубликован 18 октября 1977); патент США 4113861 (авторы Флейш и др., опубликован 12 сентября 1978); патент США 4117090 (автор Плоджер, опубликован 26 сентября 1978); патент США 4134969 (автор Шмидт-Дункер, опубликован 16 января 1979); патент США 4267108 (авторы Блюм и др. , опубликован 12 мая 1981); патент США 4304734 (авторы Джери и др., опубликован 8 декабря 1981); патент США 4330537 (автор Фрэнсис, опубликован 18 мая 1982); патент США 4407761 (авторы Блюм и др., опубликован 4 октября 1983); патент США 4469686 (автор Эндрюс, опубликован 4 сентября 1984); патент США 4578376 (автор Розини, опубликован 25 марта 1986); патент США 4608368 (авторы Блюм и др., опубликован 26 августа 1986); патент США 4621077 (авторы Розини и др., опубликован 4 ноября 1986); патент США 4687767 (авторы Босиз и др. , опубликован 18 августа 1987); патент США 4687768 (авторы Бенедикт и др. , опубликован 10 октября 1987); патент США 5711830 (авторы Шталь и др., опубликован 8 декабря 1987); патент США 4719203 (авторы Босиз и др., опубликован 12 января 1988); патент США 4927814 (авторы Галл и др. опубликован 22 мая 1990); патент США 4990503 (авторы Изомура и др., опубликован 5 февраля 1991); патент Германии 2104476 (автор Вормс, опубликован 17 августа 1972); патент Германии 2343147 (авторы Плегер и др., опубликован 3 апреля 1975); патент Германии 2104476 (авторы Вормс и др., опубликован 26 июня 1975); патент Германии 2513966 (автор Шмидт-Дункер, опубликован 7 октября 1976); патент Германии 2541981 (авторы Эймерс и др., опубликован 24 марта 1977); патент Германии 3334211 (автор Блюм, опубликован 4 апреля 1985); патент Японии 78/59674 (авторы Судзуки и др., опубликован 22 октября 1979); патент Японии 80/98193 (авторы Судзуки и др., опубликован 25 июля 1980); Европейский патент 88359 (авторы Блюм и др., опубликован 14 сентября 1983); Европейский патент 100718 (авторы Брельер и др., опубликован 15 февраля 1984), Европейский патент 186405 (авторы Бенедикт и др., опубликован 2 июля 1986); Европейский патент 197478 (авторы Босиз и др., опубликован 15 октября 1985), др. опубликован 15 февраля 1984); Европейский патент 230068 (авторы Бенедикт и др., опубликован 29 июля 1987); Европейский патент 273514 (авторы Эбетино и др., опубликован 6 июля 1988); Европейский патент 274158 (авторы Эбетино и др., опубликован 13 июля 1988); Европейский патент 282309 (авторы Сакамото и др., опубликован 14 сентября 1988); Европейский патент 282320 (авторы Изомура и др., опубликован 14 сентября 1988); Международный патент 87/03598 (авторы Биндеруп и др., опубликован 18 июня 1987); Международный патент 88/00590 (авторы Галл и др., опубликован 28 января 1988).
Предпочтительными активными по отношению к костям фосфонатами, полезными в способах по настоящему изобретению, являются: N-(2'-(3'-метил)пиридинил)аминометанфосфонометилфосфиновая кислота, N-(2'-(5'-метил)пиридинил)аминометанфосфонометилфосфиновая кислота, N-(2'(3'-метил)пиперидинилиден)аминометанфосфонометилфосфиновая кислота, N-(2'-(5'-метил)пиперидинилиден)аминометанфосфонометилфосфиновая кислота, 2-(2'-пиридинил)этан-1-фосфоно-1-метилфосфиновая кислота, 2-(2'-пиперидинил)этан-1-фосфоно-1-метилфосфиновая кислота, 2-(п-аминофенил)-1-гидроксиэтан-1-фосфоно-1-метилфосфиновая кислота, 2-(М-аминофенил)-1-гидроксиэтан-1-фосфоно-1-метилфосфиновая кислота, N-(1-(5-амино-2-метил-1-оксо)-пентил)аминометанфосфонометилфосфиновая кислота, N-(2'(3'-метил(пипиридинилиденаминометанфосфонометилфосфиновая кислота, S-(2'-пиридинил)тиометанфосфонометилфосфиновая кислота, 2-(2-пиридил)-1-гидроксиэтан-1-фосфоно-1-метилфосфиновая кислота, 2-(3-пиридил)-1-гидроксиэтан-1-фосфоно-1-метилфосфиновая кислота, 2-(N-имидазоил)-1-гидроксиэтан-1-фосфоно-1-метилфосфиновая кислота, 3-(N-метил-N-метиламино)-1-гидроксипропан-1-фосфоно-1-метилфосфиновая кислота, 4-амино-1-гидроксибутан-1-фосфоно-1-метилфосфиновая кислота, 3-(N-пироллидино)-1-гидроксипропан-1-фосфоно-1-метилфосфиновая кислота, N-циклогептиламинометанфосфонометилфосфиновая кислота, S-(п-хлорфенил)тиометанфосфонометилфосфиновая кислота, (7-дигидро-1-пиридин)метанфосфонометилфосфиновая кислота, (7-дигидро-1-пиридин)гидроксиметанфосфонометилфосфиновая кислота, (6-дигидро-2-пиридин)гидроксиметанфосфонометилфосфиновая кислота, 2-(6-пиролопиридин)-1-гидроксиэтан-1-фосфоно-1-метилфосфиновая кислота, 1-гидроксиэтан-1,1-бисфосфоновая кислота, 1-гидроксипентан-1,1-бисфосфоновая кислота, метанбисфосфоновая кислота, дихлорметанбисфосфоновая кислота, гидроксиметанбисфосфоновая кислота, 1-аминоэтан-1,1-бисфосфоновая кислота, 2-аминоэтан-1,1-бисфосфоновая кислота, 3-аминопропан-1,1-бисфосфоновая кислота, 3-аминопропан-1-гидрокси-1,1-бисфосфоновая кислота, 3,3-диметил-3-амино-1-гидроксипропан-1,1-бисфосфоновая кислота, фениламинометанбисфосфоновая кислота, N,N-диметиламинометанбисфосфоновая кислота, N-(2-гидроксиэтил)аминометанбисфосфоновая кислота, 4-амино-1-гидроксибутан-1,1-бисфосфоновая кислота, 4-амино-1-гидроксипентан-1,1-бисфосфоновая кислота, 4-амино-1-гидроксигексан-1,1-бисфосфоновая кислота, индан-2,2-бисфосфоновая кислота, гидроксииндан-2,2-бисфосфоновая кислота, 2-метилциклобутан-1,1-бисфосфоновая кислота, циклогексан-1,1-бисфосфоновая кислота, 2-(2-пиридил)-1-гидроксиэтан-1,1-бисфосфоновая кислота, N-(2-(5-амино)пиридил)аминометанбисфосфоновая кислота, N-(2-(5-хлор) пиридил)аминометанбисфосфоновая кислота, N-(2-(3-пиколил)аминометанбисфосфоновая кислота, N-(2-(4-пиколил)аминометанбисфосфоновая кислота, N-(2-(5-пиколил)аминометанбисфосфоновая кислота, N-(2-(6-пиколил))аминометанбисфосфоновая кислота, N-(2-(3,4-лутидин))аминометанбисфосфоновая кислота, N-(2-пиримидил)аминометанбисфосфоновая кислота, N-(2-пиридил)-2-аминометан-1,1-бисфосфоновая кислота, 2-(2-пиридил)этан-1,1-бисфосфоновая кислота, 2-(3-пиридил)этан-1,1-бисфосфоновая кислота, 2-(4-пиридил)этан-1,1-бисфосфоновая кислота, 2-(2-(3-пиколил)оксэтан-1,1-бисфосфоновая кислота, 2-(3-пиридил)-1-гидроксиэтан-1,1-бисфосфоновая кислота, 2-(N-имидазоил)-1-гидроксиэтан-1,1-бисфосфоновая кислота, 3-(N-пентил-N-метиламино)-1-гидроксипропан-1,1-бисфосфоновая кислота, 3-(N-пироллидино)-1-гидроксипропан-1,1-бисфосфоновая кислота, N-циклогептиламинометанбисфосфоновая кислота, S-(п-хлорфенил)тиометанбисфосфоновая кислота, (7-дигидро-1-пиридин)метанбисфосфоновая кислота, (7-дигидро-1-пиридин)гидроксиметанбисфосфоновая кислота, (6-дигидро-2-пиридин)гидроксиметанбисфосфоновая кислота, 2-(6-пиролопиридин)-1-гидроксиэтан-1,1-бисфосфоновая кислота, и их фармацевтически приемлемые соли и простые эфиры.
Наиболее предпочтительными активными по отношению к костям фосфонатами, полезными в методах по настоящему изобретению, является : 1-гидроксиэтан-1,1-бисфосфоновая кислота, дихлорметанбисфосфоновая кислота, 3-амино-1-гидроксипропан-1,1-бисфосфоновая кислота, 6-амино-1-гидроксигексан-1,1-бисфосфоновая кислота, 4-амино-1-гидроксибутан-1,1-бисфосфоновая кислота, 2-(3-пиридил)-1-гидроксиэтан-1,1-бисфосфоновая кислота, 2-(N-имидазоил)-1-гидроксиэтан-1,1-бисфосфоновая кислота, 3-(N-пентил-N-метиламино)-1-гидроксипропан-1,1-бисфосфоновая кислота, 3-(N-пироллидино)-1-гидроксипропан-1,1-бисфосфоновая кислота, N-циклогептиламинометанбисфосфоновая кислота, S-(п-хлорфенил)тиометанбисфосфоновая кислота, (7-дигидро-1-пиридин)метанбисфосфоновая кислота, (7-дигидро-1-пиридин)гидроксиметанбисфосфоновая кислота, (6-дигидро-2-пиридин)гидроксиметанбисфосфоновая кислота, 2-(6-пиролопиридин)-1-гидроксиэтан-1,1-бисфосфоновая кислота, и их фармацевтически приемлемые соли и простые эфиры.
Способы по настоящему изобретению предусматривают также введение гормона околощитовидной железы. В контексте настоящего изобретения термин "гормон околощитовидной железы" обозначает природный гормон околощитовидной железы человека, его синтетические аналоги, гормон околощитовидной железы и фрагменты гормона околощитовидной железы, изготавливаемые по технологии рекомбинантной ДНК, и фрагменты гормона околощитовидной железы и аналоги фрагментов околощитовидной железы. Гормоны околощитовидной железы, полезными по настоящему изобретению, являются, например, hPTH (1-38), hPTH (1-34), hPTH (1-37). Подобное описание типов имеющихся гормонов околощитовидной железы и способов получения гормона околощитовидной железы приведены в следующих публикациях, которые приводят здесь для справки: патент США 4105602 (авторы Коулскотт и др. , опубликован 8 августа 1978); патент США 4698328 (авторы Неер и др., опубликован 6 октября 1987); патент США 4833125 (авторы Неер и др. , опубликован 23 мая 1987); патент Германии 3243358 (автор Хеш, опубликован 24 мая 1984); патент Германии 3935738 (авторы Форссманн и др., опубликован 8 мая 1991).
Настоящее изобретение относится также к способам увеличения костной массы у людей или других животных, пораженных остеопорозом, представляющих собой 30-дневной период лечения и включающим схемы назначения гормона околощитовидной железы и схемы назначения бисфосфоната, в которых:
а) указанные схемы назначения гормона околощитовидной железы включают введение указанному пациенту гормона околощитовидной железы в количестве приблизительно 4 - 15 МЕ/кг в день, при условии, что указанный гормон околощитовидной железы вводят по крайней мере один раз в семь дней в течение каждого указанного 30-дневного периода лечения;
б) указанные схемы назначения бисфосфоната включают введение указанному пациенту бисфосфоната в количестве приблизительно 0,0005 - 1,0 мгР/кг в день при условии, что указанный бисфосфонат вводят по крайней мере один день в течение каждого указанного 30-дневного периода лечения.
Таким образом, 30-дневный период лечения предусматривает раздельные схемы назначения для каждого активного вещества, т.е. одну для гормона околощитовидной железы и одну для бисфосфоната. Гормон околощитовидной железы должен вводиться по крайней мере один раз в семь дней каждого 30-дневного периода с целью поддержания физиологического воздействия гормона околощитовидной железы на пациента. Гормон околощитовидной железы может приниматься ежедневно в указанный 30-дневный период лечения, или через день, или раз в три дня, или раз в четыре дня, или раз в пять дней, или раз в шесть дней каждого указанного 30-дневного периода лечения. Единственным ограничением является то, что гормон околощитовидной железы следует назначать в количестве 4-15 МЕ/кг в день раз в семь дней указанного 30-дневного периода лечения. Если гормон околощитовидной железы вводится в количестве 4-15 МЕ/кг в день, его можно назначать различными дозами в интервале 4-15 МЕ/кг в день в различные дни до тех пор, пока он вводится раз в семь дней указанного 30-дневного периода лечения. Может оказаться желательным вводить один вид гормона околощитовидной железы в некоторые дни лечения и другой вид в другой день лечения.
Далее, бисфосфонат следует вводить по крайней мере в течение одного дня каждого 30-дневного периода лечения. Однако бисфосфонат можно назначать ежедневно в указанный 30-дневный период лечения, или через день указанного 30-дневного периода лечения, или раз в три дня, или раз в четыре дня, ил раз в пять дней, или раз в шесть дней указанного 30-дневного периода лечения. Единственным ограничением является то, что бисфосфонат следует вводить в количестве 0,0005 - 1,0 мгР/кг в день по крайней мере в течение одного дня указанного 30-дневного периода лечения. Если бисфосфонат вводится в количестве 0,0005 - 1,0 мгР/кг в день, его можно назначать различными дозами в интервале 0,0005 - 1,0 мгР/кг в день в различные дни до тех пор, пока он вводится по крайней мере в течение одного дня указанного 30-дневного периода лечения. Может оказаться желательным вводить один тип бисфосфоната в некоторые дни лечения и другой тип в другой день лечения.
Указанные схемы назначения применяются последовательно, одна за другой, пока не достигается общее увеличение скелетной массы. Иллюстративными, но не лимитирующими настоящее изобретение примерами режимов лечения, возможных в соответствии с настоящим изобретением, являются следующие: 1) гормон околощитовидной железы назначается в количестве 13 МЕ/кг ежедневно в течение указанного 30-дневного периода лечения; на 7 день указанного 30-дневного периода лечения назначают высокоэффективный бисфосфонат в количестве приблизительно 0,001 мгР/кг в день в течение одного (1-го) дня; 2) бисфосфонат средней эффективности назначают в количестве 0,01 мгР/кг в день в течение 5 дней; на 6 день назначают гормон околощитовидной железы в количестве 5 МЕ/кг в течение 15 дней, на 21 день назначают бисфосфонат средней эффективности в течение 5 дней, и на 26 день назначают гормон околощитовидной железы в течение 5 дней; 3) бисфосфонат средней эффективности назначают в количестве приблизительно 0,002 мгР/кг в день в течение 14 дней, на 4 день назначают гормон околощитовидной железы в количестве 5 МЕ/кг в течение 26 дней; 4) гормон околощитовидной железы назначают в течение 30 дней в количестве около 4 мгР/кг в день, на 15 день назначают бисфосфонат низкой эффективности в количестве приблизительно 0,2 мгР/кг в день в течение 5 дней; 5) гормон околощитовидной железы назначают в течение 30 дней в количестве 8 МЕ/кг в день; на 10 день, на 17 и 23 день назначают бисфосфонат высокой эффективности в количестве 0,001 мгР/кг в день, 6) бисфосфонат низкой эффективности назначают в количестве приблизительно 0,2 мгР/кг в день в течение 14 дней, на 7 день назначают гормон околощитовидной железы в количестве 4 МЕ/кг в течение 23 дней; 7) бисфосфонат высокой эффективности в количестве приблизительно 0,01 мгР/кг в день в течение 20 дней, на 7 - через день назначают гормон околощитовидной железы в количестве приблизительно 10 МЕ/кг в день в течение 23 дней; 8) бисфосфонат средней эффективности назначают через день в количестве приблизительно 0,02 мгР/кг в течение 7 дней, на 3 день назначают гормон околощитовидной железы в количестве приблизительно 10 МЕ/кг в день в течение 15 дней, и на 18 день назначают через день бисфосфонат в течение 12 дней в количестве приблизительно 0,02 мгР/кг в день, и на 25 день назначают гормон околощитовидной железы в количестве 10 МЕ/кг в день в течение 5 дней; 9) гормон околощитовидной железы назначают в количестве 4 МЕ/кг в день в течение 15 дней, на 20 день и 25 день назначают бисфосфонат высокой эффективности в количестве приблизительно 0,002 мгР/кг в день, и на 23 день и 27 день назначают гормон околощитовидной железы в количестве приблизительно 4 МЕ/кг в день.
Термины "низкой эффективности", "средней эффективности" и "высокой эффективности" используют для описания антирассасывающей способности бисфосфоната. Например, бисфосфонаты низкой эффективности имеют НЭД в интервале 1,0-0,5, бисфосфонат средней эффективности имеют НЭД в интервале 0,5-0,03, а бисфосфонаты высокой эффективности имеют НЭД, больший чем 0,03-0,0001.
Эффективность конкретного бисфосфоната может быть выражена в терминах ее НЭД или "наименьшей эффективной дозы", которая является минимальной дозой бисфосфоната, выраженной в мгР/кг, которая сама по себе является эффективной, чтобы вызвать значительное ингибирование процесса рассасывания кости. Конкретные величины НЭД бисфосфонатов будут изменяться в зависимости от их химического состава и от способа назначения (т.е. орального или парентерального). Чем меньше значение НЭД, тем более эффективным является бисфосфонат, и в общем случае желательно назначать бисфосфонаты высокой эффективности в меньших дозах и меньшее количество дней в указанном 30-дневном периоде лечения. Аналогично, чем больше значение НЭД, тем меньше эффективность бисфосфоната и, как правило, желательно назначать бисфосфонаты низкой эффективности большими дозами и большее количество дней в течение указанного 30-дневного периода лечения.
В частности, величины НЭД для активных по отношению к костям фосфонатов могут быть определены в условиях in vivo с использованием одной из принятых моделей. Одной из таких моделей является модель крысы с удаленной щитовидной и околощитовидной железами. В этой модели соединения оцениваются на предмет ингибирующей способности в условиях in vivo по отношению к рассасыванию кости путем измерения их способности подавлять увеличение количества кальция в сыворотке, вызываемого введением гормона околощитовидной железы крысам, у которых удалены околощитовидные железы. Эта модель описана в таких публикациях как Russel et al., 6, Calcified Tissue Research, 183 (1970); Muhlbauer et al. , 5., Mineral Electrolite Metabolism, 296 (1981); патент США 4761406 (авторы Флора и др., опубликован 2 августа 1988); Европейский патент 298553 (автор Эбетино, опубликован 11 января 1989), которые все приводятся здесь для справки.
Другой моделью является "модель Шенка", в которой оценивают воздействие активных по отношению к костям фосфонатов на рост костей молодых крыс. Эта модель описана в таких публикациях, как Schenk et al, 11, Calcif. Tissue Res. 196 (1973), Shinoda et al., 35, Calcif. Tissue Res. 87 (1983), и Европейский патент 298553 (автор Эбетино, опубликован 11 января 1989), которое все приводятся здесь для справки.
Еще одной моделью является модель крыс с удаленными яичниками, в которой определяют способность активных по отношению к костям фосфонатов предотвращать потерю костной ткани у женских особей крыс, вызываемую удалением яичников. Эта модель описана в статье Wrouski et al., 125, Endocrinology, 810 (1989), которая приводится здесь для справки.
Величины НЭД при параллельном введении предпочтительных активных по отношению к костям фосфонатов, которые используются по настоящему изобретению, следующие: 1,0 мгР/кг для 1-гидроксиэтан-1,1-бисфосфоновой кислоты, 0,5 мгР/кг для дихлорметанбисфосфоновой кислоты, 0,03 мгР/кг для 3-амино-1-гидроксипропан-1,1-бисфосфоновой кислоты, 0,001 мгР/кг для 4-амино-1-гидроксибутан-1,1-бисфоcфоновой кислоты, 0,1 мгР/кг для 6-амино-1-гидросигексан-1,1-бисфосфоновой кислоты, 0,01 мгР/кг для N-(2-пиридил)аминометан-1,1-бисфосфоновой кислоты, 0,0003 мгР/кг для 2-(3-пиридил)-1-гидроксиэтан-1.1-бисфосфоновой кислоты, 0,0001 мгР/кг для N-циклогептиламинометанбисфосфоновой кислоты, 0,0001 мгР/кг для 3(N-пентил-N-метиламино)-1-гидроксипропан-1,1-бисфосфоновой кислоты, 0,01 мгР/кг для 3-(диметиламино)-1-гидроксипропан-1,1-бисфосфоновой кислоты, 0,01 мгР/кг для 3-(П-пироллидино)-1-гидроксипропан-1,1-бисфосфоновой кислоты, 0,03 мгР/кг для N-циклогептиламинометанбисфосфоновой кислоты, 0,3 мгР/кг для S-(n-хлорфенил) тиометанбисфосфоновой кислоты. Значение НЭД для орального назначения будут больше, чем определяется систематическим поглощением фосфоната. Как правило, поглощение при оральном назначении составляет приблизительно 1% - 10%. Так значения НЭД при оральном назначении обычно приблизительно от десяти до приблизительно ста раз больше, чем величины НЭД при парентеральном назначении).
В контексте настоящего изобретения термин "мгР/кг" обозначает количество соединения, выраженное в миллиграммах фосфора в соединении, на килограмм веса тела пациента, лечение которого проводится. Поскольку бисфосфонаты имеют разную молекулярную массу, то выражение введенного количества по величине мгР/кг позволяет провести сравнение между бисфосфонатами разной эффективности. Чтобы определить количество в мгР/кг, назначенное пациенту в соответствии с настоящим изобретением, используют следующую переводную формулу: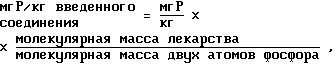
Например, 2-(3-пиридил)-1-гидроксиэтан-1,1-бисфосфоновая кислота имеет молекулярную массу 350. Два атома фосфора имеют молекулярную массу 62. Таким образом, если пациенту введена доза 0.01 мг/кг соединения, то назначено около 0,002 мг/кг.
Доза гормона околощитовидной железы, как это принято, измеряется в интернациональных единицах (ME).
Способ по настоящему изобретению предусматривает лечение остеопороза на всех стадиях развития болезни. Поскольку остеопороз является развивающимся процессом потери костной ткани, а не заболеванием, которое имеет конкретное начало или окончание, то "лечение" в контексте настоящего изобретения заключается в способе, который прекращает, замедляет или обращает процесс потери костной ткани, протекающий при остеопорозе.
Предпочтительные способы по настоящему изобретению включают лечение остеопороза у пациентов, у которых уже произошла потеря скелетной массы (далее этот случай называют "установленным остеопорозом"). Такие методы по настоящему изобретению для лечения установленного остеопороза преимущественно включают назначение активных соединений в течение времени, достаточного для увеличения скелетной массы указанного пациента. Увеличение массы может происходить в кортикальной кости, трабекулярной кости или в обеих костях. Преимущественно общая скелетная масса увеличивается приблизительно на 1% в год.
Конкретный период времени, достаточный для увеличения общей скелетной массы пациента может зависеть от множества факторов. Они включают, например, конкретные применяемые активные соединения, количество введенных активных соединений, возраст и пол пациента, конкретное заболевание, которое лечат, сопутствующие терапии (если они применяются), общее физическое состояние пациента (в том числе наличие других заболеваний), величину потери костной массы пациентов и пищу, обычно употребляемую пациентом.
Терапевтические режимы с использованием способов по настоящему изобретению преимущественно продолжаются в течение по крайней мере двенадцати месяцев. Конечно, терапевтические режимы могут быть продлены в течение неограниченного количества времени в соответствии с принятой медицинской практикой. Пациента лечат преимущественно до тех пор, пока не достигается общее увеличение скелетной массы, соразмерное с уменьшением риска перелома, что устанавливается лечащим врачом.
В способах по настоящему изобретению термин "назначение" относится к любому способу, принятому в медицинской практике, с помощью которого пациенту, лечение которого проводится, вводится активные соединения, используемые в настоящем изобретении, с тем, чтобы они были активными в построении костной ткани. Активные соединения могут назначаться любым из известных способов введения, в частности, орально, через слизистую оболочку кожи (например, через кожу, подъязычно, через нос и ректально), парентерально (например, подкожной инъекцией, внутримышечной инъекцией, внутрисуставной инъекцией, внутривенной инъекцией) и ингаляцией. Так, конкретные способы назначения включают, но ими не ограничиваются, оральное введение, введение через кожу, введение через слизистую оболочку, подъязычно, внутримышечное, внутривенное, внутрибрюшинное, подкожное введение и местное применение.
Преимущественный способ лечения остеопороза включает первоначальный этап диагностики с целью определить наличие заболевания. Так, предпочтительный способ по настоящему изобретению включает этап проведения диагностического исследования пациента с целью выявления остеопороза, и при получении положительного результата этого диагностического исследования - назначение активных соединений в соответствии со способами по настоящему изобретению. Для указанных способов лечения постклимактерических пациенток прежде, чем происходит значительная потеря костной массы, указанный первый этап диагностического исследования заключается в проведении диагностики наступления климакса. Такие методы хорошо известны и включают определение костной массы и скорость реконструкции костной ткани. Скорость реконструкции костной ткани может быть определена с помощью биохимических меток (Hui et al., "Tle Contvibution of Bone Loss to Postmenopausal Osteoporosis", 1, Osteoporosis Luf), 30 (1990), которая приводится здесь для справки.
Подходящие диагностики для определения наличия остеопороза хорошо известны в данной области техники. Такие методы включают измерение радиоплотности методом скелетной радиографии, количественной компьютерной томографии, фотонной абсорбциометрии. Методы диагностики, которые используются по настоящему изобретению, описываются в монографии (W. A. Peck et al., Physician's Resource Manual on Osteoporosis. 1987 (опубликован Национальной ассоциацией остеопороза) - приводится здесь для справки).
Активные по отношению к костям фосфонаты и гормон околощитовидной железы могут назначаться в виде разнообразных фармацевтически приемлемых композиций. Такие композиции могут включать активное соединение и фармацевтически приемлемый носитель. Фармацевтически приемлемые носители включают твердые или жидкие наполнители, разбавители или вещества для инкапсулирования и их смеси, пригодные для назначения человеку или животным. Термин "совместимый" в контексте настоящего изобретения означает, что компоненты фармацевтической композиции способны смешиваться с активными соединениями и друг с другом, так что между ними не происходит взаимодействия, которое значительно снижает фармацевтическую эффективность фармацевтической композиции при ее использовании в обычных ситуациях. Фармацевтически приемлемые носители должны, конечно, обладать достаточно высокой чистотой и достаточно низкой токсичностью, с тем чтобы они были пригодны для назначения человеку или животному, лечение которого проводится.
Некоторыми примерами соединений, которые могут служить фармацевтическими носителями, являются: сахар, такие как лактоза, глюкоза и сахароза, крахмалы, такие как кукурузный крахмал и картофельный крахмал, целлюлоза и ее производные, такие как натриевая соль карбоксиметилцеллюлозы, этилцеллюлоза, ацетат целлюлозы, порошок трагаканта, солод, желатин, тальк, стеариновая кислота, стеарат магния, растительные масла, такие как арахисовое масло, хлопковое масло, кунжутное масло, оливковое масло, кукурузное масло и масло какао, полиолы, такие как пропиленгликоль, глицерин, сорбит, маннит и полиэтиленгликоль, агар, альгиновая кислота, апирогенная вода, изотонический солевой раствор, растворы фосфатного буфера, смачивающие агенты и смазывающие соединения, такие как лаурилсульфонат натрия, красители, ароматизирующие вещества, и консерванты. Другие совместимые фармацевтические добавки и активные соединения могут включаться в фармацевтически приемлемый носитель для использования в композициях по настоящему изобретению.
Выбор фармацевтически приемлемого носителя для использования с активным соединением определяется тем способом, которым вводится активное соединение. Если активное соединение необходимо ввести в виде инъекции, то преимущественным фармацевтическим носителем является стерильная вода, физиологический солевой раствор или их смесь, pH такой парентеральной композиции преимущественно доводят до значения 7,4. Подходящими фармацевтически приемлемыми носителями для местного назначения является известные в данной области техники носители, используемые для приготовления кремов, гелей, бинтов, бляшек и аналогичные средства для местного назначения лекарств.
Фармацевтически приемлемый носитель, используемый в сочетании с активным соединением, применяется в концентрации, достаточной для достижения практического соотношения размера - доза. Фармацевтически приемлемый носитель в общем случае может составлять 0,1 - 99,9 мас.% фармацевтической композиции по настоящему изобретению, предпочтительно приблизительно 5 - 80%, а наиболее предпочтительно приблизительно 10 - 50%.
Предпочтительным способом назначения бисфосфонатов является оральное назначение в форме стандартной дозы (т.е. дозировочной формы, содержащей количество активного соединения, пригодное для введения в виде одной дозы в соответствии с медицинской практикой). Предпочтительными формами стандартной дозы для бисфосфонатов являются таблетки, капсулы, суспензии и растворы, содержащие безопасное и эффективное количество активного вещества. Фармацевтически приемлемые носители, пригодные для приготовления форм стандартной дозы для орального назначения, хорошо известны в данной области техники. Их выбор зависит от критериев второго порядка, таких как вкус, пена, устойчивость при хранении, которые не являются критичными для целей настоящего изобретения, и могут без труда быть получены специалистом. Стандартная доза активного по отношению к костям фосфоната для орального назначения преимущественно включает приблизительно 0,0005 - 1,0 мгР/мг орально в день.
Преимущественным способом назначения гормона околощитовидной железы является подкожная инъекция в виде стандартной дозы. Предпочтительные формы стандартной дозы для инъекции гормона околощитовидной железы включают стерильные водные растворы, физиологический солевой раствор или их смеси. pH указанных растворов должен быть доведен до 7,4. Стандартные дозы гормона околощитовидной железы преимущественно включают приблизительно 4 - 15 МЕ/кг в день.
В настоящем изобретении заявляются также наборы для удобного и эффективного использования способов по настоящему изобретению. Указанные наборы включают одну или несколько стандартных доз активных по отношению к костям фосфонатов, одну или несколько стандартных доз гормона околощитовидной железы и средства для освоения способов по настоящему изобретению. Такие наборы предоставляют удобные и эффективные средства, гарантирующие, что пациент, лечение которого проводится, получит активные соединения в правильной дозировке и правильным способом. Вспомогательные средства указанных наборов включают средства, которые облегчают введение активных соединений в соответствии со способами по настоящему изобретению. Указанные вспомогательные средства включают инструкции, упаковку и средства для приготовления лекарств в различных сочетаниях. Примеры упаковки и средств для приготовления лекарств хорошо известны в данной области техники и описаны, в том числе в патенте США 4761406 (авторы Флора и др., опубликован 2 августа 1988), патенте США 4812311 (автор Ухтман, опубликован 14 марта 1989) и патенте США 4833125 (авторы Неер и др., опубликован 23 мая 1989), которые все приводятся здесь для справки.
Следующие не ограничивающие настоящее изобретение примеры поясняют составы и способы по настоящему изобретению и его применение.
Пример 1. Пациентку - женщину кавказской национальности - весом приблизительно 60 кг с диагнозом постклимактерический остеопороз лечат способом по настоящему изобретению. Конкретно в течение одного года:
1) гормон околощитовидной железы (фрагмент 1-34 синтетического гормона человека или hPTH 1-34) вводится самостоятельно подкожно с дозой 13 МЕ/кг с помощью шприца для введения инсулина в переднюю часть бедра в течение пяти дней еженедельно и
2) бисфосфонат, 2-(3-пиридил(-1-гидроксиэтан-1,1-бисфосфоновая кислота, принимается орально в виде таблетки, содержащей 0,002 мгР/кг в день.
В конце года берут биопсию из области подвздошного гребня и устанавливают увеличение средней толщины стенки реконструктивных единиц (ОМЕ) по сравнению с предыдущей базовой биопсией пациентки. Активационная частота и глубина полостей рассасывания губчатых кортикальных и эндокортикальных поверхностей незначительно увеличена по сравнению с аналогичными величинами в базовой биопсии.
Пример 2. Мужчину афро-американского происхождения (имеющего самопроизвольный перелом), весом приблизительно 68 кг лечат от остеоропороза неясного происхождения способом по настоящему изобретению. А именно, ежедневно в течение двух лет пациент самостоятельно вводит себе подкожно инъекции гормона околощитовидной железы (hPTH 1-38) с дозой 8 МЕ/кг. Далее, раз в неделю орально принимается бисфосфонат, 4-амино-1-гидроксибутан-1,1-бисфосфоновая кислота, в виде таблетки, содержащей 0,03 мгР/кг в день. Терапевтическое воздействие на губчатые кости контролируют количественной компьютерной томографией позвоночника, по прошествии двух лет у пациента зафиксировано увеличение на 14,5 мг/куб. см. костной ткани позвоночника по сравнению с его базовым значением. Воздействие терапии на кортикальную кость определяют, измеряя методом фотонной абсорпциометрии радиус, который указывает на отсутствие потери минеральной составляющей кости (на самом деле небольшой прирост) по сравнению с базовыми измерениями. Дальнейшие самопроизводные переломы не наблюдаются.
Пример 3. У женщины восточного типа, страдающей хронической астмой, весом приблизительно 60 кг диагноз устанавливает остеопороз глюкокортикоидного происхождения. Пациентку лечат способом по настоящему изобретению. А именно, пациентка принимает hPTH 1-34 ежедневно через нос в виде аэрозоля с дозой 5 МЕ/кг. Далее, пациентке накладывается еженедельно бляшка, из которой поступает общая доза 0,005 мгР/кг ежедневно бисфосфоната, 4-амино-1-гидроксибутан-1,1-бисфосфоновой кислоты. По окончании месячного курса берут анализ крови и исследуют на наличие специфической метки, остеокальцина, а также выделенной из кости и общей алкалинфосфатазы. Значения для остеокальцина увеличены на 57%, а концентрация алкалинфосфатаза из кости и общей алкалинфосфатазы несколько повышены по сравнению со значениями до лечения. Эти результаты согласуются с повышением функции остеобластов без заметного ускорения оборота веществ в костях.
Пример 4. Мужчину кавказкой национальности весом приблизительно 65 кг лечат способом по настоящему изобретению, а именно: лечение - гормоном околощитовидной железы непосредственно предшествует лечению бисфосфонатом, 1-гидрокси-этан-1,1-бисфосфонатом. Конкретно, гормон околощитовидной железы hPTH 1-34 вводится пациентом самостоятельно в виде инъекции в течение 3 месяцев с дозой 10 МЕ/кг. Сканирование плотности кости методом фотонной абсорпциометрии показывает увеличение массы кости. Для закрепления достигнутого результата прием гормона околощитовидной железы прекращают и назначают курс бисфосфоната, 1-гидроксиэтан-1,1-бисфосфоната в виде таблеток с содержанием 0,90 мгР/кг в день, которые принимаются орально раз в неделю, начиная со следующей недели, и продолжают в течение 3 месяцев. Исследование кости методом денситометрии по окончании терапии 1-гидроксиэтан-1,1-бисфосфонатом показывает сохранение костной массы. Пациента вновь переводят на режим приема гормона околощитовидной железы, если оказывается, что по прошествии следующего трехмесячного периода наблюдается значительная потеря костной массы.
Изобретение относится к медицине. Предложенный способ лечения остеопороза предусматривает 30-дневный период лечения и включает схемы назначения гормона околощитовидной железы в количестве 4-15 МЕ/кг в день, по крайней мере один раз в семь дней в течение каждого указанного 30-дневного периода лечения. При этом бисфосфонат вводят в количестве приблизительно 0,0005-1,0 мгР/кг в день, по крайней мере один день в течение каждого указанного 30-дневного периода лечения. 9 з.п.ф-лы.
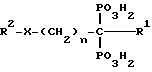
где n - целое число от 0 до 7;
R1 - атом водорода, атом хлора, аминогруппа или гидроксил;
X - группа -NH-, атом кислорода или простая связь;
R2 является 5 - 7-членным гетероциклом, содержащим от 1 до 3 гетероатомов, аминогруппой, аминогруппой, замещенной одной или двумя низшими алкильными группами, или атомом водорода,
и их фармацевтически приемлемые соли и простые эфиры.
Авторы
Даты
1998-06-10—Публикация
1992-12-15—Подача