Изобретение относится к новым фармацевтическим композициям на основе циклопептидов, имеющих следующие формулы 1(a)- (r):
(a) cyclo(-Arg-Gly-Asp-D-Phe-Val-Ala);
(b) cyclo(-Arg-Gly-Asp-D-Phe-Leu-Ala);
(c) cyclo(-Arg-Gly-Asp-Phe-Val-D-Ala);
(d) cyclo(-Arg-Gly-Asp-Phe-Leu-D-Ala);
(e) cyclo(-Arg-Gly-Asp-D-Phe-Val-Gly);
(f) cyclo(-Arg-Gly-Asp-D-Phe-Leu-Gly);
(g) cyclo(-D-Arg-Gly-Asp-Phe-Val-Ala);
(h) cyclo(-D-Arg-Gly-Asp-Phe-Val-Gly);
(i) cyclo(-Arg-Gly-Asp-Phe-Pro-Gly);
(j) cyclo(-Arg-Gly-Asp-Phe-D-Pro-Gly);
(k) cyclo(-Arg-Gly-Asp-Phe-Pro-Ala);
(l) cyclo(-Arg-Gly-Asp-Phe-D-Pro-Ala);
(m) cyclo(-D-Arg-Gly-Asp-Phe-Val);
(n) cyclo(-Arg-D-Ala-Asp-Phe-Val);
(o) cyclo(-Arg-Gly-Asp-D-Phe-Val);
(p) cyclo(-Arg-Ala-Asp-D-Phe-Val);
(q) cyclo(-Arg-Gly-Asp-Phe-D-Val);
(r) cyclo(-Arg-Gly-D-Asp -Phe-Val),
и их солям c физиологически совместимыми кислотами.
Аббревиатуры аминокислотных радикалов, представленных выше и ниже, обозначают радикалы следующих аминокислот:
Ala - аланин
Arg - аргинин
Asp - аспартовая кислота
Gly - глицин
His - гистидин
Len - лейпин
Phe - фенилаланин
Pro - пролин
Val - валин
Кроме того, следующие аббревиатуры имеют нижеприведенные значения:
BOC - трет.-бутоксикарбонил
CBZ - бензилоксикарбонил
DCCI - дициклогексилкарбодиимид
DMF - диметилформамид
FAB - бомбардировка ускоренными атомами
HOBT - гидроксибензотриазол
M+ - моль-ионный пик
OMe - метокси
Ближайшим аналогом является патент EP 406428, описывающий циклические пептиды - ингибиторы адгезии.
Соединения формул 1 (a) - (r) и их соли с физиологически совместимыми кислотами известны.
Известно, что соединения, которые специфически подавляют взаимодействие β3 интегринового рецептора с лигандом (антагонист связывания с рецептором, "ARA"), могут; использоваться как терапевтические средства для лечения остеопороза, тромбоза, инфаркта миокарда, артериосклероза, воспалений, кровоизлияний, стенокардии и опухолей. Кроме того, эти соединения подавляют клеточную адгезию в случае образования остеокластов и пригодны как средства, поддерживающие ангиогенез и при лечении ран.
Целью изобретения является нахождение таких ARA, которые могут блокировать связывание фибриногеном β3 интегрина, чтобы получить улучшенные препараты для вышеназванных целей.
Таким образом, целью одного из аспектов этого изобретения является создание новых фармацевтических композиций, которые могут быть использованы в качестве лекарственных препаратов. Среди других целей - способы воздействия на фармакологическую активность.
Неожиданно, что соединения формул 1 (a) - (r) и их соли с физиологически совместимыми кислотами обладают, как было обнаружено, такими антагонистическими свойствами для адгезии с рецептором, о которых для этих соединений ранее не упоминалось.
Этот эффект был обнаружен при использовании метода J. W. Smith, L.M. Ruggeri, T.J Kunicki and D.A Cheresh описанного в J. Biol. Chem. 265, 12 267 - 12 271 (1990).
Метод заключается в следующем : 96-ячеечную необработанную плоскодонную плату покрывали кроющим буфером, содержащим 1 мкг/мл рецептора 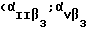 по 100 мкл/на ячейку и инкубировали на качалке при 4oC в течение ночи. Плату промывали однократно связывающим буфером и затем блокировали блокирующим буфером (100 мкл/на ячейку) в течение двух часов при 30oC. После дополнительного промывания связывающим буфером добавляли биотинилированный лиганд и конкурент.
по 100 мкл/на ячейку и инкубировали на качалке при 4oC в течение ночи. Плату промывали однократно связывающим буфером и затем блокировали блокирующим буфером (100 мкл/на ячейку) в течение двух часов при 30oC. После дополнительного промывания связывающим буфером добавляли биотинилированный лиганд и конкурент.
Лигандный фиброноген применяли в конечной концентрации 1 мкг/мл. Конкурент добавляли в повышающихся концентрациях. Как лиганд, так и конкурент добавляли в объеме 50 мкл/на ячейку при двойной конечной концентрации и разводили связывающим буфером.
Плату накрывали и инкубировали в течение трех часов при 30oC. Чтобы удалить несвязанный материал, плату трехкратно отмывали буфером для связывания (100 мкл/на ячейку).
Добавлялся конъюгат козьих антибиотиковых антител с щелочной фосфатазой (разведение 1: 2000) в буфере для связывания (100 мкл/на ячейку), и плату инкубировали в течение часа при 30oC.
Плату отмывали три раза буфером для связывания, добавляли раствор субстрата и проявляли в темноте при комнатной температуре в течение 1-5 мин.
Реакцию останавливали добавлением 100 мкл/на ячейку 0,4 М NaOH и считывали на считывающем устройстве для ELISA при λ = 405 нм.
Все точки выводились из серий трех повторностей.
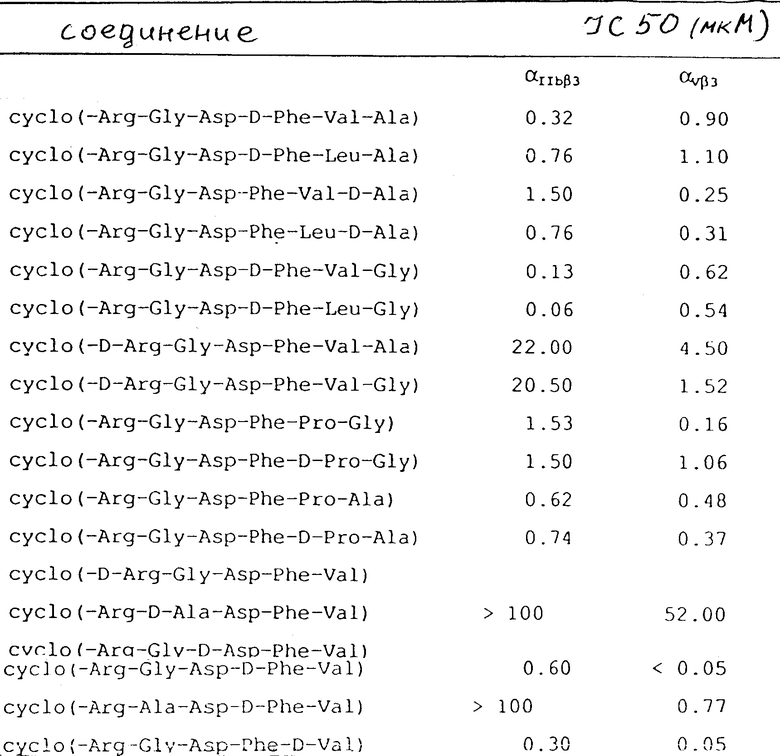
Полученные значения IC50 приведены в таблице.
Изобретение также относится к использованию соединений формулы 1 и их физиологически приемлемых солей для получения фармацевтических лекарственных форм, в особенности с помощью нехимических средств. С этой целью они могут быть превращены в удобную для введения форму в сочетании по крайней мере с одним твердым, жидким и/или полужидким носителем (наполнителем) или вспомогательным веществом и, где оправдано, в сочетании с одним (или более) другим активным соединением.
Изобретение также относится к средствам, особенно фармацевтическим лекарственным формам, содержащим по крайней мере одно соединение формулы 1, и/или их физиологически приемлемых солей.
Эти лекарственные формы могут использоваться как лекарственные препараты в медицине и ветеринарии. Подходящими носителями являются органические и неорганические вещества, которые подходят для энтерального (например, перорального), парентерального или местного применения и которые не реагируют с новыми соединениями, например вода, растительные масла, бензиловые спирты, алкиленгликоли, полиэтиленгликоли, глицеролтриацетат, желатин, углеводы, такие как лактоза или крахмал, магнезия, стеарат, тальк и вазелин. Для перорального применения используются таблетки, пилюли, таблетки с покрытием, капсулы, порошки, гранулы, сиропы, соки и капли; для ректального введения используются свечи; для парентерального введения в частности используются растворы, предпочтительно масляные или водные растворы, а также суспензии, эмульсии или имплантаты; для местного применения используются мази, кремы или порошки.
Новые вещества могут быть также лиофилизированы, и полученный лиофилизат может быть использован, например для получения препаратов для инъекций. Указанные лекарственные формы могут быть стерилизованы и/или содержать вспомогательные вещества, такие как скользящие вещества, консерванты, стабилизаторы и/или увлажняющие средства, эмульгаторы, соли, чтобы влиять на осмотическое давление, буферные вещества, подкрашивающие, вкусовые и/или ароматические вещества. Если желательно, они могут также содержать одно или более других активных веществ, например один или более витаминов.
Соединения могут также использоваться как фармакологически активные вещества в медицине и ветеринарии, в частности для лечения и профилактики тромбоза, инфаркта миокарда, стенокардии, кровоизлияний и опухолей, что означает и раковые заболевания.
Изобретение также относится к использованию веществ формулы 1 для борьбы с болезнями, в частности, и к их использованию для терапевтического лечения людей и животных. В частности, они являются ингибиторами клеточной адгезии, применимы для подавления, например, агрегации клеток крови и опухолевых клеток. Таким образом, соединения могут быть использованы для подавления адгезии у клеток животных, например соматических или раковых клеток млекопитающих.
Вещества, соответствующие этому изобретению, как правило, применяются по аналогии с другими известными коммерчески доступными пептидами, в частности по аналогии с веществами, описанными в патенте США 4472305, предпочтительно в дозах около 0,05 - 500, в частности 0,5 - 100 мг на единицу дозирования. Суточная доза предпочтительно около 0,01 - 2 мг/кг веса тела. Специфическая доза, назначаемая каждому отдельному пациенту, зависит, однако, от многих различных факторов, например, от активности специфического используемого вещества, возраста, веса тела, общего состояния здоровья, пола, времени и пути введения, скорости выведения, фармацевтической комбинации тяжести специфического заболевания, при котором применяется терапия. Предпочтительно парентеральное применение. Следующие предпочтенные конкретные примеры выполнения иллюстрируют, но не ограничивают предложенное изобретение.
В предшествующих и последующих примерах все температуры, если нет других указаний, представлены неоткорректированными в градусах Цельсия, все части и проценты даны по весу.
Полные данные по всем заявкам, патентам и публикациям, процитированным выше и ниже, представлены здесь для справки.
Пример 1. 2,0 г BOC-ARG-Gly-Asp-D-Phe-Val-Ala - OMe в 60 мл метанола, добавляют 1,5 мл 2N раствора гидроксида натрия и смесь перемешивают в течение 3 ч при 20oC. Остаток после выпаривания извлекают водой, подкисляют до pH 3 разбавленной HCl и экстрагируют этилацетатом. Экстракт высушивают над Na2SO4, опять выпаривают и полученный BOC-Arg-Gly-Asp-D-Phe-Val-Ala-OH взбалтывают при 20oC течение 2 ч с 20 мл 2 N HCl в диоксане. Смесь выпаривают, и полученный H-Arg-Gly-Asp-D-Phe-Val-Ala-OH растворяют в смеси 1800 мл дихлорметана и 200 мл диметилформамида (DMF) и охлаждают до 0oC, и при помешивании постепенно добавляют 0,5 г дициклогексилкарбодиимида (DCCI) 0,3 г 1-гидроксибензотриазола (HOBt) и 0,23 мл N - метилморфолина, и смесь взбалтывали а течение последующих 24 ч при 0oC и 48 ч при 20oC. Раствор концентрируют и пропускают через ионообменник со смешанным слоем, чтобы освободить его от солей. Затем этот раствор фильтруют, фильтрат выпаривают и остаток очищают с помощью хроматографии. Получают цикло (-Arg-Gly-Asp-D-Phe-Val-Ala) M+ : 646 (бомбардировка ускоренными атомами FAB);
Следующие соединения получены аналогично :
cyclo(-Arg-Gly-Asp-D-Phe-Leu-Ala); M+: 660;
cyclo(-Arg-Gly-Asp-Phe-Val-D-Ala); M+: 646;
cyclo(-Arg-Gly-Asp-Phe-Leu-D-Ala); M+: 660;
cyclo(-Arg-Gly-Asp-D-Phe-Val-Gly); M+: 632;
cyclo(-Arg-Gly-Asp-D-Phe-Leu-Gly); M+: 645;
cyclo(-D-Arg-Gly-Asp-Phe-Val-Ala); M+: 646;
cyclo(-D-Arg-Gly-Asp-Phe-Val-Gly); M+: 632;
cyclo(-Arg-Gly-Asp-Phe-Pro-Gly); M+: 630;
cyclo(-Arg-Gly-Asp-Phe-D-Pro-Gly); M+ 630;
cyclo(-Arg-Gly-Asp-Phe-Pro-Ala); M+: 644;
cyclo(-Arg-Gly-Asp-Phe-D-Pro-Ala); M+: 644;
cyclo(-D-Arg-Gly-Asp-Phe-Val); M+: 575
cyclo(-Arg-D-Ala-Asp-Phe-Val); M+: 589;
cyclo(-Arg-Gly-Asp-D-Phe-Val); M+: 575;
cyclo(-Arg-Ala-Asp-D-Phe-Val); M+: 589;
cyclo(-Arg-Gly-Asp-Phe-D-Val); M+: 575
cyclo(-Arg-Gly-D-Asp-Phe-Val); M+: 575;
Нижеприведенные примеры относятся к фармацевтическим лекарственным формам, которые содержат вещества формулы 1 и их соли с кислотами.
Пример 2. Таблетки.
Смесь 1 кг цикло-((Arg-Gly-Asp-D-Phe-Val-Ala), 10 кг лактозы, 6 кг микрокристаллической целлюлозы, 6 кг картофельного крахмала, 1 кг поливинилпирролидона, 0,8 кг талька и 0,1 кг стеарата магния прессуют в таблетки обычным путем, так что каждая таблетка, содержат 10 мг активного вещества.
Пример 3. Таблетки с покрытием.
Таблетки прессуются аналогично примеру 2, затем покрываются обычным путем покрытием из сахарозы, картофельного крахмала, талька, трагаканта и красящего вещества.
Пример 4. Капсулы.
Твердые желатиновые капсулы наполняют цикло (-Arg-Gly-Asp-D-Phe-Val-Ala) обычным путем, так что каждая капсула содержит 5 мг активного соединения.
Пример 5. Ампулы.
Раствор 1 кг цикло (-Arg-Gly-Asp-D-Phe-Val-Gly) в 30 л 1,2 - пропандиола подвергают стерильному фильтрованию, ампулы наполняют раствором и стерильно запаивают. Каждая ампула содержит 2 мг активного вещества.
Пример 6. Мазь.
500 мг цикло (-Arg-Gly-Asp-D-Phe-Leu-Gly) смешивается c 99,5 г вазелина в асептических условиях.
Пример 7. Флаконы для инъекций.
Раствор 100 г цикло (-Arg-Gly-Asp-D-Phe-Leu-Glyl) и 5 г динатрийгидрофосфата в 3 л бидистиллированной воды доводят до pH 6,5, соляной кислотой, стерилизуют фильтрованием, разливают по флаконам для инъекции и лиофилизируют в стериальных условиях, флаконы закрывают в стериальных условиях. Каждый флакон для инъекций содержит 5 мг активного соединения.
Фармацевтические лекарственные формы, которые содержат одно или более активных соединений формул (1) (а) -(r) и/или их физиологически приемлемые соли с кислотами могут быть получены аналогично.
Предыдущие примеры могут быть повторены при замене использованных в предшествующих примерах реагентов или изменении условий процесса на какие-то общие специфические реагенты или условия.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЦИКЛОПЕПТИДЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, СОДЕРЖАЩИЕ ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1994 |
|
RU2130030C1 |
| ЦИКЛОПЕПТИДЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1996 |
|
RU2157379C2 |
| ЦИКЛОПЕПТИДЫ ИЛИ ИХ СОЛИ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ И СПОСОБ ИХ ПОЛУЧЕНИЯ, СПОСОБ ЛЕЧЕНИЯ | 1993 |
|
RU2129563C1 |
| ЦИКЛИЧЕСКИЕ ИНГИБИТОРЫ АДГЕЗИИ | 1997 |
|
RU2184121C2 |
| ЦИКЛИЧЕСКИЕ АЗАПЕПТИДЫ С АНГИОГЕННЫМ ДЕЙСТВИЕМ | 1998 |
|
RU2188205C2 |
| ЖИДКИЙ ПРЕПАРАТ, СОДЕРЖАЩИЙ ОЛИГОПЕПТИДЫ И ЭТЕРИФИЦИРОВАННЫЙ ЦИКЛОДЕКСТРИН | 2003 |
|
RU2322254C2 |
| БИОТИНОВЫЕ ПРОИЗВОДНЫЕ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1996 |
|
RU2171807C2 |
| КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ЦИКЛИЧЕСКИЕ ПЕПТИДЫ, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2009 |
|
RU2555357C2 |
| ПРОИЗВОДНЫЕ ЦИКЛОПЕПТИДОВ | 1997 |
|
RU2202557C2 |
| ЦИКЛОПЕПТИДЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ | 1995 |
|
RU2151776C1 |
Изобретение относится к области медицины. Композиция содержит циклопептид, выбранный из группы:
cyclo (-Arg-Gly-Asp-D-Phe-Val-Ala);
cyclo (-Arg-Gly-Asp-D-Phe-Leu-Ala);
cyclo (-Arg-Gly-Asp-Phe-Val-D-Ala);
cyclo (-Arg-Gly-Asp-Phe-Leu-D-Ala);
cyclo (-Arg-Gly-Asp-D-Phe-Val-Gly);
cyclo (-Arg-Gly-Asp-D-Phe-Leu-Gly);
cyclo (-D-Arg-Gly-Asp-Phe-Val-Ala);
cyclo (-D-Arg-Gly-Asp-Phe-Val-Gly);
cyclo (-Arg-Gly-Asp-Phe-Pro-Gly);
cyclo (-Arg-Gly-Asp-Phe-D-Pro-Gly);
cyclo (-Arg-Gly-Asp-Phe-Pro-Ala);
cyclo (-Arg-Gly-Asp-Phe-D-Pro-Ala);
cyclo (-D-Arg-Gly-Asp-Phe-Val);
cyclo (-Arg-D-Ala-Asp-Phe-Val);
cyclo (-Arg-Gly-Asp-D-Phe-Val);
cyclo (-Arg-Ala-Asp-D-Phe-Val);
cyclo (-Arg-Gly-Asp-Phe-D-Val);
cyclo (-Arg-Gly-D-Asp-Phe-Val);
или его соль. Указанная композиция может быть использована для лечения и профилактики тромбоза, инфаркта миокарда, кровоизлияния, артериосклероза, воспаления, стенокардии и/или опухолей, остеопороза. 2 с. и 4 з.п. ф-лы; 1 табл.
cyclo (-Arg-Gly-Asp-D-Phe-Val-Ala);
cyclo (-Arg-Gly-Asp-D-Phe-Leu-Ala);
cyclo (-Arg-Gly-Asp-Phe-Val-D-Ala);
cyclo (-Arg-Gly-Asp-Phe-Leu-D-Ala);
cyclo (-Arg-Gly-Asp-D-Phe-Val-Gly);
cyclo (-Arg-Gly-Asp-D-Phe-Leu-Gly);
cyclo (-D-Arg-Gly-Asp-Phe-Val-Ala);
cyclo (-D-Arg-Gly-Asp-Phe-Val-Gly);
cyclo (-Arg-Gly-Asp-Phe-Pro-Gly);
cyclo (-Arg-Gly-Asp-Phe-D-Pro-Gly);
cyclo (-Arg-Gly-Asp-Phe-Pro-Ala);
cyclo (-Arg-Gly-Asp-Phe-D-Pro-Ala);
cyclo (-D-Arg-Gly-Asp-Phe-Val);
cyclo (-Arg-D-Ala-Asp-Phe-Val);
cyclo (-Arg-Gly-Asp-D-Phe-Val);
cyclo (-Arg-Ala-Asp-D-Phe-Val);
cyclo (-Arg-Gly-Asp-Phe-D-Val);
cyclo (-Arg-Gly-D-Asp-Phe-Val),
или его физиологически приемлемую соль в эффективном количестве.
cyclo (-Arg-Gly-Asp-D-Phe-Val-Ala);
cyclo (-Arg-Gly-Asp-D-Phe-Leu-Ala);
cyclo (-Arg-Gly-Asp-Phe-Val-D-Ala);
cyclo (-Arg-Gly-Asp-Phe-Leu-D-Ala);
cyclo (-Arg-Gly-Asp-D-Phe-Val-Gly);
cyclo (-Arg-Gly-Asp-D-Phe-Leu-Gly);
cyclo (-D-Arg-Gly-Asp-Phe-Val-Ala);
cyclo (-D-Arg-Gly-Asp-Phe-Val-Gly);
cyclo (-Arg-Gly-Asp-Phe-D-Pro-Gly);
cyclo (-Arg-Gly-Asp-Phe-D-Pro-Gly);
cyclo (-Arg-Gly-Asp-Phe-Pro-Ala);
cyclo (-Arg-Gly-Asp-Phe-D-Pro-Ala);
cyclo (-D-Arg-Gly-Asp-Phe-Val);
cyclo (-Arg-D-Ala-Asp-Phe-Val);
cyclo (-Arg-Gly-Asp-D-Phe-Val);
cyclo (-Arg-Ala-Asp-D-Phe-Val);
cyclo (-Arg-Gly-Asp-Phe-D-Val);
cyclo (-Arg-Gly-D-Asp-Phe-Val),
и фармацевтически приемлемый носитель в количестве 0,01 - 2,0 мг на 1 кг массы тела в сутки.
| EP 406428 A1 (Asahi Glass Company LTD), 09.01.91, C 07 K 5/12 | |||
| US, 447230 5 A (Sterling Drug Inc.), 18.09.84, C 07 C 103/52 | |||
| Автоматический огнетушитель | 0 |
|
SU92A1 |
| SU, 1048702 A (Институт органического синтеза АН Латвийской СССР), 30.08.89, A 61 K 38/12. | |||
Авторы
Даты
1998-07-27—Публикация
1993-07-05—Подача