Изобретение относится к биотиновым соединениям общей формулы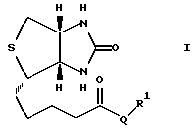
где Q отсутствует или обозначает -NH-(CH2)5-CO-,
R1 обозначает X-Arg-Gly-Asp-y,
X - трипептид: Gly-Gly-Gly-,
y - дипептид: -Ser-PrO
или R1 обозначает A-Cys(R2)-B-U,
R2 обозначает Н, Trt;
А обозначает Asp или пептидный фрагмент, выбранный из группы, состоящей из:
Ala-Asp, Thr-Ala-Asp, Lys-Thr-Ala-Asp, Lys-Ala-Ala-Asp,
Arg-Thr-Ala-Asp, Ser-Ala-Asp, Gln-Ser-Ala-Asp,
Gly-Lys-Thr-Ala-Asp, Ile-Ser-Ala-Gly, Arg-Ser-Ala-Gly
Gly-Lys-Thr-Cys (Trt)-Asp
В отсцтствиет или обозначает Pro или N-метилированное производное Ala,
причем, если R1 обозначает A-Cys(R2)-B-U, то лишь один из остатков А или В может отсутствовать,
U обозначает ОН или NH2,
или R1 обозначает цикло (Arg-Gly-Asp-Z), Z в боковой цепи связан с Q или, если Q отсутствует, с биотином,
Z обозначает ди- или трипептидный остаток,
причем аминокислоты, независимо друг от друга, выбирают из группы, состоящей из Ala, Val, Тyr, Trp, Phe, Cys, Lys, М, при этом указанные аминокислоты могут быть дериватизированы, а аминокислотные остатки связаны друг с другом пептидоподобно через N-амино- и α -карбоксильные группы, причем М содержится всегда и обозначает:
NH(R8) - CH(R3) - COOH,
R3 = R6 - R4
где R4 = ОН,
R6 = алкиленфенил с 7-14 C-атомами,
R8 = H, алкил с 1-6 C-атомами,
причем, если речь идет об остатках оптически активных аминокислот и аминокислотных производных, то включаются как D-, так L-формы;
а также к их солям.
Подобные соединения биотинилированных пептидов описывается, например, в ВОИС 9415956 (биотинилированные антагонисты эндотелинового рецептора), в ВОИС 9413313 (биотинилированные LHRH - антагонисты) или в ВОИС 9418325 (биотинилированный некрозный фактор).
Биотинилирование пептидов во время синтеза в твердой фазе на смоле с целью улучшенной возможности очистки описывается T.J.Lobi и др. в Anal.Biochem. 170, 502 (1988).
Подобные соединения циклических и линейных пептидов известны из патентов ФРГ 43 10 643 и 43 36 758, европейского патента EP-0 406 428 и ВОИС 89/05150.
В основу изобретения положена задача получения новых соединений с ценными свойствами, в частности таких, которые можно применять для приготовления лекарственных средств.
Найдено, что соединения формулы I и их соли при хорошей переносимости обладают очень ценными фармакологическими свойствами. Прежде всего, они действуют как ингибиторы интегрина, причем, в частности, они подавляют взаимодействия αv-, β3 - или β5 - интегриновых рецепторов с лигандами, как, например, связывание фибриногена с β3 - интегриновым рецептором. Особую эффективность соединения проявляют в случае интегринов αvβ3 , αvβ5, α∥вβ3, а также αvβ1, αvβ6 и αvβ8 . Это действие можно обнаружить, например, по методу, который описывается J. W. Smith и др. в J.Biol. Chem., 265, 12267- 12271 (1990).
Зависимость возникновения ангиогенеза от взаимодействия между сосудистыми интегринами и внеклеточными матричными протеинами описывается P.С.Brooks, R.A.Clark и D.A.Cheresh в Science 264, 569-71 (1994).
Возможность ингибирования этого взаимодействия и вместе с этим начала апоптоза (программированная гибель клетки) ангиогенных сосудистых клеток за счет циклического пептида описывается Р.С. Brooks, A.M.Montgomery, M.Rosenfeld, R. A. Reisfeld, Т. -Hu, G.Klier и D.A.Cheresh в Cell, 79, 1157-64 (1994).
Соединения формулы I, которые блокируют взаимодействие интегриновых рецепторов с лигандами, как, например, фибриногена с фибриногенным рецептором (гликопротеин IIb/IIIa), в качестве GP IIb/ IIIa - антагонистов предотвращают распространение опухолевых клеток за счет метастаз. Это доказывается следующими наблюдениями:
Распространение опухолевых клеток от локальной опухоли в сосудистую систему происходит за счет образования микроагрегатов (микротромбов) благодаря взаимодействию опухолевых клеток с тромбоцитами. Опухолевые клетки экранируются за счет защиты в микроагрегате и не распознаются клетками иммунной системы. Микроагрегаты могут внедряться в стенки сосудов, благодаря чему облегчается дальнейшее проникновение опухолевых клеток в ткань. Так как образованию микротромбов способствует связывание фибриногена с фибриногенными рецепторами на активированных тромбоцитах, то GP IIa/IIIb - антагонисты можно рассматривать как эффективные ингибиторы метастаза.
Соединения формулы I можно применять в качестве биологически активных веществ в лекарственных средствах в медицине и ветеринарии, в частности для профилактики и/или терапии таких заболеваний, как тромбоз, миокардиальный инфаркт, артериосклероз, воспаления, апоплексия, стенокардия, опухолевые заболевания, остеолитические заболевания, как остеопороз, патологические ангиогенные заболевания, как, например, воспаления, офтальмологические заболевания, диабетическая ретинопатия, дегенеративные изменения в области желтого пятна (сетчатки), близорукость, гистоплазмоз, ревматический артрит, остеоартрит, рубеотическая глаукома, язвенный колит, болезнь Крона, атеросклероз, псориаз, рестеноз после ангиопластики, вирусная инфекция, бактериальная инфекция, грибковая инфекция, при острой почечной недостаточности и при заживлении ран для поддерживания процесса заживления.
Соединения формулы I можно применять в качестве антимикробно действующих веществ при операциях, где используются биоматериалы, имплантаты, катетеры или электростимуляторы сердца. При этом они действуют антисептически. Эффективность антимикробной активности можно обнаруживать с помощью способа, описанного Р. Valentin-Weigund и др. в Infection and Immunity, 2851-2855 (1988).
Так как соединения формулы I представляют собой ингибиторы связывания фибриногена и вместе с этим лигандов фибриногенных рецепторов с тромбоцитами, их можно применять ин виво в качестве диагностических средств с целью выявления и локализации тромбов в сосудистой системе, так как биотинильный остаток является УФ- обнаруживаемым остатком.
Соединения формулы I можно применять в качестве ингибиторов связывания фибриногена, так же как в качестве эффективного лечебного средства для изучения метаболизма тромбоцитов в различных стадиях активирования или внутриклеточных сигнальных механизмов фибриногенного рецептора. Обнаруживаемая единица "биотиновой метки" позволяет, после связывания с рецептором, исследовать указанные механизмы.
Выше- и нижеуказанные сокращения аминокислотных остатков обозначают остатки следующих аминокислот:
Abu - 4-аминомасляная кислота; Aha - 6-аминогексановая кислота; 6-аминокапроновая кислота; Ala - аланин; Asn - аспарагин; Asp - аспарагиновая кислота; Arg - аргинин; Cys - цистеин; Dab - 2,4-диаминомасляная кислота; Dab - 2,3-диаминопропионовая кислота; Gln - глутамин; Glp - пироглутаминовая кислота; Glu - глутаминовая кислота; Gly - глицин; His - гистидин; Homo-Phe - гомо-фенилаланин; IIe - изолейцин; Leu - лейцин; Lys - лизин; Met - метионин; Nle - норлейцин; Orn - орнитин; Phe - фенилаланин; Phg - фенилглицин; 4-Нal-Рhe - 4-галоген-фенилаланин; Pro - пролин; Ser - серин; Thr - треонин; Trp - триптофан; Tyr - тирозин; Val -валин; а также Bit: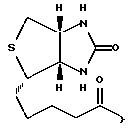
Далее приводятся следующие обозначения:
ВОС - трет.-бутоксикарбонил; CBZ - бензилоксикарбонил; DCCI - дициклогексилкарбодиимид; ДМФ - диметилформамид; Et - этил; Fmoc - 9-флуоренилметоксикарбонил; HOBt - 1-гидроксибензотриазол; Ме - метил; МВНА - 4-метил-бензгидриламин; Mtr - 4-метокси-2, 3,6-триметилфенил-сульфонил; OBut - сложный трет. -бутиловый эфир; OMe -сложный метиловый эфир; OEt - сложный этиловый эфир; РОА - феноксиацетил; ТFА (ТФК) - трифторуксусная кислота; Trt - тритил (трифенилметил).
Поскольку вышеуказанные аминокислоты могут находиться в различных энантиомерных формах, то включаются все выше- и нижеуказанные эти формы и также их смеси (например, DL - формы), например, в качестве составной части соединений формулы I. Далее, аминокислоты, например, в качестве составной части соединений формулы I, могут быть снабжены соответствующими, само по себе известными защитными группами.
Предлагаемые согласно изобретению соединения также включают так называемые пролекарственные производные, т.е. измененные, например, с помощью алкильных или ацильных групп, cахаров или олигопептидов соединения формулы I, которые в организме быстро расщепляются до эффективных, предлагаемых согласно изобретению соединений.
Предметом изобретения, далее, является способ получения соединений формулы I по п.1 формулы изобретения, а также их солей, отличающийся тем, что
(а) соединение формулы II: H-Q-R1, II,
где Q и R1 имеют указанное в п.1 формулы изобретения значение, путем реакции ацилирования вводят во взаимодействие с соединением формулы III: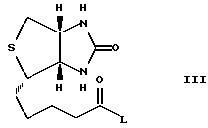
где L обозначает Cl, Br, J или свободную или реакционноспособную, функционально измененную OH-группу и в случае необходимости полученное при этом основание или кислое соединение формулы I путем обработки кислотой или основанием переводят в одну из его солей.
Выше- и нижеуказанные остатки Q, R1 и L, имеют указанные в случае формул II и III значения, если не указано ничего другого.
В вышеприведенных формулах, алкил предпочтительно обозначает метил, этил, изопропил или трет.-бутил.
Алкилен предпочтительно обозначает метилен, этилен, пропилен, бутилен, пентилен или гексилен.
Алкиленфенилом предпочтительно является бензил или фенетил.
Алкиленфенилалкилен предпочтительно обозначает 4-метилен-бензил или 4-этилен-бензил.
Остаток -R6-R4 предпочтительно обозначает 2-, 3- или 4-гидроксибензил; 2-, 3- или 4-гидроксифенетил.
Указанные в значениях X, Y и Z аминокислоты и аминокислотные остатки могут быть также дериватизированы, причем предпочтительны N-метильные, N-этильные, N-пропильные, N-бензильные или Cα-метильные производные.
Далее, предпочтительны производные Asp и Glu, в частности сложные метиловые, этиловые, пропиловые, бутиловые, трет.- бутиловые, неопентиловые или бензиловые эфиры карбоксильных групп боковых цепей; далее, также производные Arg, который в -NН- C(=NH)-NH2-группе может быть замещен ацетильным, бензоильным, метоксикарбонильным или этоксикарбонильным остатком. Далее, указанные в значениях для X и Y аминокислоты и аминокислотные остатки могут быть снабжены соответствующими, само по себе известными защитными группами.
Z предпочтительно обозначает М; далее предпочтительно обозначает последовательность N 1 (см. в конце описания).
Соединения формулы I могут иметь один или несколько хиральных центров и поэтому могут находиться в различных стереоизомерных формах. Формула I охватывает все эти формы.
Соответственно этому, предметом изобретения являются, в частности, те соединения формулы I, в которых, по меньшей мере, один из указанных остатков имеет одно из вышеуказанных предпочтительных значений. Некоторые предпочтительные группы соединений могут быть выражены следующими частичными формулами Ia : Ie, которые соответствуют формуле I и где подробнее не указанные остатки имеют данные в случае формулы I значения, где, однако,
в Ia: Q отсутствует и R1 обозначает X-Arg- Gly-Asp-Y;
в Iб: Q обозначает -NH-(CH2)5-СО- и R1 обозначает X-Arg-Gly-Asp-Y;
в Iв; Q обозначает -NH-(CH2)5-CO- и R1 обозначает цикло-(Arg-Gly-Asp-Z);
в Iг: Q обозначает -NH-(CH2)5-СО и R1 обозначает цикло-(Arg-Gly-Asp-M);
в Iд: Q обозначает -NH-(CH2)5-СО- и R1 обозначает A-Cys (R2)-В; и
в Iе: Q обозначает -NH-(CH2)n-СО; R1 обозначает X-Arg-Gly-Asp-Y и "n" обозначает 1, 2, 3, 4, 5 или 6.
Соединения формулы I и также исходные вещества для их получения получают впрочем само по себе известными способами, которые описаны в литературе (например, как Губен-Вейл, Методы органической химии, изд. Georg-Thieme, Штутгарт), а именно при реакционных условиях, которые известны и пригодны для указанных взаимодействий. При этом можно употреблять также сами по себе известные, здесь подробнее не упомянутые варианты.
Исходные вещества, если желательно, также можно получать in situ, так что их не выделяют из реакционной смеси, а тотчас вводят во взаимодействие далее для получения соединений формулы I.
Соединения формулы I предпочтительно можно получать тем, что соединения формулы II вводят во взаимодействие с соединениями формулы III.
Соединения формул II и III как правило известны. Если они неизвестны, то их можно получать само по себе известными способами.
В соединениях формулы III остаток -CO-L, обозначает предварительно активированную карбоновую кислоту, предпочтительно галоидангидрид карбоновой кислоты, симметричный или смешанный ангидрид или сложный активированный эфир. Такого рода остатки для активирования карбоксильной группы в типичных реакциях ацилирования описаны в литературе (например, в Губен- Вейл, Методы органической химии, изд. Georg - Thieme, Штутгарт).
Активированные сложные эфиры целесообразно получают in situ, например, путем добавки HOBt или N-гидрокси-сукцинимида.
L обозначает предпочтительно H, Cl, Br или -ON - сукцинимид.
Взаимодействие осуществляется как правило в инертном растворителе, в присутствии кислотосвязующего средства, предпочтительно органического основания, как триэтиламин, диметиланилин, пиридин или хинолин, или избытка карбоксильного компонента формулы III.
Также может оказаться благоприятной добавка гидроксида, карбоната или бикарбоната щелочного или щелочноземельного металла или другой соли слабой кислоты щелочного или щелочноземельного металла, предпочтительно калия, натрия, кальция или цезия.
Время реакции, в зависимости от применяемых условий, составляет от нескольких минут до 14 дней; реакционная температура составляет от -30oC до + 140oC, обычно от -10oC до + 90oC, в особенности от примерно 0oC до примерно 70oC.
В качестве инертных растворителей пригодны, например, углеводороды, как гексан, петролейный эфир, бензол, толуол или ксилол; хлорированные углеводороды, как трихлорэтилен, 1,2-дихлорэтан, тетрахлорид углерода, хлороформ или дихлорметан; спирты, как метанол, этанол, изопропанол, н-пропанол, н-бутанол или трет.-бутанол; простые эфиры, как диэтиловый эфир, диизопропиловый эфир, тетрагидрофуран (ТГФ), или диоксан; простые гликолевые эфиры, как этиленгликольмонометиловый и -моноэтиловый простой эфир(метилгликоль или этилгликоль), этиленгликольдиметиловый простой эфир (диглим); кетоны, как ацетон или бутанон; амиды, как ацетамид, диметилацетамид или диметилформамид (ДМФ); нитрилы, как ацетонитрил; сульфоксиды, как диметилсульфоксид (ДМСО); сероуглерод; карбоновые кислоты, как муравьиная кислота или уксусная кислота; нитросоединения, как нитрометан или нитробензол; сложные эфиры, как этилацетат; вода, или смеси указанных растворителей.
Соединения формулы I, далее, можно получать тем, что соединения формулы IY вводят во взаимодействие с соединениями формулы Y. Исходные соединения формулы IY и формулы Y как правило известны. Если они неизвестны, то их можно получать само по себе известными способами.
В соединениях формулы Y остаток -CO-L обозначает предварительно активированную карбоновую кислоту, предпочтительно галоидангидрид карбоновой кислоты, симметричный или смешанный ангидрид или активированный сложный эфир. Такого рода остатки для активирования карбоксильной группы в типичных реакциях ацилирования описаны в литературе (например, Губен-Вейл, Методы органической химии, изд. Georg - Thieme, Штутгарт).
L предпочтительно обозначает Cl, Br или -ON-сукцинимид.
Взаимодействие соединений формулы IY с соединениями формулы Y протекает при таких же условиях относительно реакционного времени, и температуры и растворителя, как это описано для взаимодействия соединений формулы II с соединениями формулы III.
Линейные соединения формулы I с открытой цепью, в которых R1 обозначает X-Arg-Gly-Asp-Y или A-Cys(R2)-B, далее, можно получать тем, что в последней стадии твердофазного синтеза биотин вводят в реакцию сочетания в том же цикле, как и обычную защищенную на N-конце аминокислоту, в качестве последнего компонента и биотинпептид при обычных условиях отщепляют от смолы. Твердофазный синтез, отщепление и очистку осуществляют как описывается A. Jonczyk и J.Meienhofer в Peptides. Proc. 8th Am. Pept. Symp. Eds. V.Hruby и D.H.Rich, Pierce Comp III, с. 73-77 (1983), или аналогично способам, описанным в Angew. Chem. 104, 375-391 (1992).
Линейные соединения с открытой цепью формул II и IY впрочем можно получать обычными способами аминокислотного и пептидного синтеза, которые, например, описаны в указанных стандартных работах и патентных заявках, например, также по твердофазному синтезу согласно Merrifield (B.F.Gysin и R.B.Merrifield, J.Am.Chem.Soc., 94, 3102 и последующие (1972)).
Циклические соединения формулы II и формулы IY, в которых R1 обозначает цикло-(Arg-Gly-Asp-Z), можно получать путем циклизации линейных соединений, как, например, описывается в патенте ФРГ 4310643 или в Губен-Вейл, указано выше, том 15/II, с.1-806 (1974).
Соединения формулы I, далее, можно получать тем, что их высвобождают из их функциональных производных путем сольволиза, в частности гидролиза, или путем гидрогенолиза.
Предпочтительными исходными веществами для сольволиза, соответственно, гидрогенолиза, являются такие, которые вместо одной или нескольких свободных амино- и/или гидроксильных групп содержат соответствующие защищенные амино- и/или гидроксильные группы, предпочтительно такие, которые вместо H-атома, связанного с N-атомом, несут защитную для аминной функции группу, например, такие, которые соответствуют формуле I, однако вместо NH2- группы содержат NHR1 - группу (где R1 обозначает защитную для аминной функции группу, например, BOC или CBZ).
Далее, предпочтительны исходные вещества, которые вместо H-атома гидроксильной группы содержат защитную для гидроксильной функции группу, например, такие, которые соответствуют формуле I, однако, вместо гидроксифенильной группы содержат R''O-фенильную группу (где R'' обозначает защитную для гидроксильной функции группу).
В молекуле исходного вещества может быть несколько одинаковых или разных - защищенных амино- и/или гидроксильных групп.
В случае, если имеющиеся защитные группы отличаются друг от друга, то их во многих случаях можно отщеплять селективно.
Выражение "защитная для аминной функции группа" общеизвестно и относится к группам, которые пригодны для защиты (блокирования) аминогруппы от химических взаимодействий, которые, однако, легко отщепляются, после того, как в других местах молекулы прошла желательная химическая реакция. Типичными для таких групп являются, в частности, незамещенные или замещенные ацильные, арильные, аралкоксиметильные или аралкильные группы. Так как защитные для аминной функции группы удаляют после желательной реакции (или последовательности реакций), то их род и величина не критические; однако, предпочтительны группы с 1-20, в особенности 1-8, C-атомами. Выражение "ацильная группа" в связи с настоящим способом нужно понимать в самом широком смысле. Оно охватывает производимые от алифатических, аралифатических, ароматических или гетероциклических карбоновых кислот или сульфокислот ацильные группы, а также, в частности, алкоксикарбонильные, арилоксикарбонильные и прежде всего аралкоксикарбонильные группы. Примерами такого рода ацильных групп являются алканоил, как ацетил, пропионил, бутирил; аралканоил, как фенилацетил; ароил, как бензоил или толуил; арилоксиалканоил, как POA; алкоксикарбонил, как метоксикарбонил, этоксикарбонил, 2,2.2-трихлорэтоксикарбонил, ВОС, 2-иодэтоксикарбонил; аралкилоксикарбонил, как СВZ ("карбобензокси"), 4-метоксибензилоксикарбонил, FMOC; арилсульфонил, как Mtr. Предпочтительными, защитными для аминной функции группами являются BOC и Mtr далее, CBZ, Fmoc, бензил и ацетил.
Выражение "защитная для гидроксильной функции группа" также общеизвестно и относится к группам, которые пригодны для защиты гидроксильной группы от химических взаимодействий, которые, однако, легко удаляются, после того, как в других местах молекулы прошла желательная химическая реакция. Типичными для таких групп являются вышеуказанные незамещенные или замещенные арильные, аралкильные или ацильные группы; далее, также алкильные группы. Природа и величина защитных для гидроксильной функции групп не критические, так как их снова удаляют после желательной химической реакции или последовательности реакций; предпочтительны группы с 1-20, в особенности 1-10 C-атомами. Примерами защитных для гидроксильной функции групп являются, между прочим, бензил, п- нитробензоил, п-толуолсульфонил, трет.-бутил и ацетил, причем особенно предпочтительны бензил и трет.-бутил. COOH-группы в аспарагиновой кислоте и глутаминовой кислоте предпочтительно защищаются в форме их сложных трет.-бутиловых эфиров (например, ASR (О but)).
Высвобождения соединений формулы I из их функциональных производных достигают в зависимости от используемой защитной группы-, например, с помощью сильных кислот, целесообразно с помощью ТФК или хлорной кислоты, однако, также с помощью других сильных неорганических кислот, как соляная кислота или серная кислота; сильных органических карбоновых кислот, как трихлоруксусная кислота, или сульфокислот, как бензол- или п-толуолсульфокислота. Присутствие дополнительного инертного растворителя возможно, но не всегда необходимо. В качестве инертных растворителей пригодны предпочтительно органические, например карбоновые, кислоты, как уксусная кислота; простые эфиры, как тетрагидрофуран или диоксан; амиды, как ДМФ; галогенированные углеводороды, как дихлорметан; далее, также спирты, как метанол, этанол или изопропанол, а также вода. Далее, применяют смеси вышеуказанных растворителей. ТФК предпочтительно применяют в избытке без добавки другого растворителя; хлорную кислоту используют в виде смеси из уксусной кислоты и 70%-ной хлорной кислоты в соотношении 9:1. Температуры реакции для расщепления целесообразно составляют примерно от 0o до примерно 50oC, предпочтительно работают при температуре 15-30oC (комнатная температура).
Группы BOC, OBut и Mtr можно отщеплять, например, предпочтительно с помощью ТФК в дихлорметане или с помощью примерно 3-5 н. HCl в диоксане при 15-30oC; FМОС-группу можно предпочтительно отщеплять с помощью примерно 5-50%-ного раствора диметиламина, диэтиламина или пиперидина в ДМФ при 15-30oC.
Тритильную группу используют для защиты аминокислот гистидина, аспарагина, глутамина и цистеина. Отщепление осуществляют, в зависимости от желательного целевого продукта, с помощью ТФК/10% тиофенола, причем тритильная группа отщепляется от всех указанных аминокислот; при использовании смеси ТФК/анизол или ТФК/тиоанизол отщепляется только тритильная группа от His, Asn, и Glu, в противоположность чему она остается в Cys - боковой цепи.
Гидрогенолитически удаляемые защитные группы (например, CBZ или бензил) можно отщеплять, например, путем обработки водородом в присутствии катализатора (например, катализатора на основе благородного металла, как палладий, целесообразно на носителе, как уголь). В качестве растворителей при этом пригодны вышеуказанные, в особенности, например, спирты, как метанол или этанол, или амиды, как ДМФ. Гидрогенолиз, как правило, проводят при температурах примерно 0-100oC и давлениях примерно 1-200 бар, предпочтительно при 20-30oC и давлении 1-10 бар. Гидрогенолиз CBZ - группы протекает, например, хорошо в присутствии 5-10%-ного палладия-на-угле в метаноле или с помощью формиата аммония (вместо водорода) в присутствии Pd/C в смеси метанола с ДМФ при 20-30oC.
Основание формулы I с помощью кислоты можно переводить в соответствующую соль присоединения кислоты, например, путем взаимодействия эквивалентных количеств основания и кислоты в инертном растворителе, как этанол, и последующего выпаривания. Для этого взаимодействия применяют, в частности, кислоты, которые дают физиологически приемлемые соли. Так, можно применять неорганические кислоты, например, серную кислоту, азотную кислоту; галогенводородные кислоты, как соляная кислота или бромоводородная кислота; фосфорные кислоты, как ортофосфорная кислота; сульфаминовую кислоту; далее, органические кислоты, в частности алифатические, алициклические, аралифатические, ароматические или гетероциклические одно- или многоосновные карбоновые, сульфоновые или серные кислоты, например, как муравьиная кислота, уксусная кислота, пропионовая кислота, пивалиновая кислота, диэтилуксусная кислота, малоновая кислота, янтарная кислота, пимелиновая кислота, фумаровая кислота, малеиновая кислота, молочная кислота, винная кислота, яблочная кислота, лимонная кислота, глюконовая кислота, аскорбиновая кислота, никотиновая кислота, изоникотиновая кислота, метан- или этансульфокислота, этандисульфокислота, 2- гидроксиэтансульфокислота, бензолсульфокислота, п- толуолсульфокислота, нафталин-моно- и -ди-сульфокислоты, лаурилсерная кислота. Соли с физиологически неприемлемыми кислотами, например, пикраты, можно применять для выделения и/или очистки соединений формулы I.
С другой стороны, кислоту формулы I путем введения во взаимодействие с основанием можно переводить в одну из ее физиологически приемлемых солей металла или аммония. В качестве солей применяют при этом, в частности, соли натрия, калия, магния, кальция и аммония; далее, замещенные аммониевые соли, например, диметил-, диэтил- или диизопропил- аммониевые соли; моноэтанол-, диэтанол- или диизопропил- аммониевые соли; циклогексил-, дициклогексил-аммониевые соли; дибензилэтилендиаммониевые соли; далее, например, соли с аргинином или лизином.
Предметом изобретения, далее, является применение соединений формулы I и/или их физиологически приемлемых солей для приготовления фармацевтических композиций, в частности, нехимическим путем. При этом их вместе, по меньшей мере, с одним твердым, жидким и/или полужидким носителем или вспомогательным веществом и в случае необходимости в комбинации с одним или несколькими другими биологически активными веществами доводят до пригодной дозировочной формы.
Предметом изобретения, далее, являются фармацевтические композиции, содержащие, по меньшей мере, одно соединение формулы I и/или одну из его физиологически приемлемых солей.
Эти композиции можно применять в качестве лекарственных средств в медицине или ветеринарии. В качестве носителей применяют органические или неорганические вещества, которые пригодны для кишечного (например, перорального), парентерального, топического введения или для введения в форме ингаляционного распыления и не реагируют с новыми соединениями, например, как вода, растительные масла, бензиловые спирты, алкиленгликоли, полиэтиленгликоли, триацетат глицерина, желатина, углеводы, как лактоза или крахмал, стеарат магния, тальк, вазелин. Для орального применения, в частности, служат таблетки, пилюли, драже, капсулы, порошки, грануляты, сиропы, соки и капли; для ректального применения служат свечи; для парентерального применения служат, в частности растворы, предпочтительно масляные или водные растворы, далее, суспензии, эмульсии или имплантаты; для топического применения служат в особенности мази, кремы или пудры. Новые соединения можно также лиофилизовать и полученные лиофилизаты применять, например, для приготовления инъецируемых препаратов. Указанные композиции могут быть стерилизованы и/или они могут содержать вспомогательные вещества, как придающие скользкость, например, таблеткам, вещества, консерванты, стабилизаторы и/или смачиватели, эмульгаторы, соли для влияния на осмотическое давление, буферные вещества, красители, вкусовые вещества и/или некоторые другие биологически активные вещества, например, один или несколько витаминов. Для введения в виде ингаляционного распыления можно применять распылители, которые содержат биологически активное вещество либо растворенным, либо суспендированным в выталкивающем (рабочем) газе или смеси выталкивающих газов (например, CO2 или фторхлоруглеводороды). Целесообразно при этом применять биологически активное вещество в микронизированной форме, причем может быть добавлен один или несколько дополнительных, физиологических приемлемых растворителей, например, этанол. Растворы для ингаляций можно вводить с помощью обычных ингаляторов.
Соединения формулы I и их физиологически приемлемые соли можно применять в качестве ингибиторов интегрина при борьбе с заболеваниями, в частности патологическими ангиогенными заболеваниями, тромбозами, инфарктом сердца, коронарными заболеваниями сердца, артериосклерозами, опухолями, остеопорозом, воспалениями и инфекциями.
При этом предлагаемые согласно изобретению вещества, как правило, можно вводить по аналогии с другими известными, имеющимися в продаже пептидами, в частности, однако, по аналогии с описанными в патенте США А-4472305 соединениями, предпочтительно в дозировках примерно 0,05-500 мг, в особенности 0,5-100 мг, на дозировочную единицу. Суточная дозировка составляет примерно 0,01-2 мг/кг веса тела. Специальная доза для каждого пациента, однако, зависит от самых различных факторов, например, от эффективности используемого специального соединения, от возраста, веса тела, общего состояния здоровья, пола, от стоимости, от момента и пути введения, от скорости выделения, комбинации лекарственных средств и тяжести соответствующего заболевания, которая имеет значение для терапии. Предпочтительно парентеральное введение.
Далее, новые соединения формулы I можно применять в аналитической биологии и молекулярной биологии. При этом используют способность к комплексообразованию между биотинильным остатком и гликопротеином авидином. Применения комплекса биотин-авидин известны из статьи E.A.Bayer и M.Wilchek в Methods of Biochemical Analysis, 26, 1-45 (1980) [1].
Новые соединения формулы I можно применять в качестве интегриновых лигандов для приготовления колонок для аффинной хроматографии с целью получения в чистом виде интегрина. Комплекс из дериватизированного авидином носителя, например сефарозы, и новых соединений формулы I получается само по себе известными способами, как описывается, например, в [1]. По этой причине здесь далее не останавливаются на этом способе, а отсылают к соответствующей литературе, например [1].
В качестве полимерных носителей пригодны само по себе известные в химии пептидов полимерные твердые фазы предпочтительно с гидрофильными свойствами, например, сшитые полисахара, как целлюлоза, сефароза или сефадекс® акриламиды, полимеры на основе полиэтиленгликоля или Tentakel-полимеры®
Новые соединения формулы I также можно применять в качестве диагностических маркеров для анти-биотин-антитело-реакций в анализе ферментного иммуносорбентного типа и FACS-анализе (с флуоресцентным активированием установка для сортировки клеток). Известно применение антибиотин-антител для обнаружения биотина согласно M. Berger, Biochemistry, 14, 2338-2342 (1975). Применение дериватизированного биотином иммуноглобулина lqG в иммуноферментном анализе (ELISA) описано U.Holmkov-Nielsen и др., в Journal of Chromatogr., 297, 225- 233 (1984).
В J.Immunol.Methods., 181, 55-64 (1995) J.Gao и S.J.Shattil описывается ELlSA - тест на обнаружение веществ, которые ингибируют 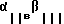 -активирование интегрина. Для обнаружения используют здесь биотинилированный фибриноген.
-активирование интегрина. Для обнаружения используют здесь биотинилированный фибриноген.
Применение поточной цитометрии в клинической диагностике клеток описано G. Schmitz и G.Rothe в DG Klinische Chemie Mitteilungen, 24 (1993) часть 1, с. 1- 14.
Далее, соединения формулы I можно использовать в микроскопии с силовым полем (атомная силовая микроскопия АFМ) для измерения силы взаимодействий лиганд-рецептор. Лиганд предпочтительно обозначает комплекс из авидина и новых соединений формулы I. Рецептор предпочтительно обозначает интегриновый рецептор.
E. -L. Florin и др. в Science 264, 415- 417 (1994) описали измерения адгезионных сил между функционализированным авидином микроскопом с силовым полем и биотинилированной агарозой.
Выше и нижеуказанные, все температуры указываются в oC. В нижеследующих примерах "обычная обработка" обозначает: добавляют, если необходимо, воду; устанавливают, если необходимо, в зависимости от строения целевого продукта, pH-значения в пределах 2-10; экстрагируют этилацетатом или дихлорметаном, разделяют, органическую фазу сушат над сульфатом натрия, растворитель выпаривают и остаток очищают путем хроматографии на силикагеле и/или путем кристаллизации. Rf - значения указываются при использовании силикагеля; растворитель: смесь этилацетата с метанолом в соотношении 9:1.
RZ - время удерживания (минуты) в случае ВЭЖХ (высокоэффективной жидкостной хроматографии) в следующих системах:
[A]:
Колонка: Nucleosil 7C 18 250х4 мм; элюент А: 0,1% ТФК в воде; элюент В: 0,1% ТФК в ацетонитриле; истечение: 1 мл/мин.; градиент: 20-50% B /30 мин.
[B]:
50-минутный градиент 0-80% пропан-2-ола в воде с 0,3% ТФК при 1 мл/мин, на колонке с Lichrosorb® RP Select B (7 мкм) 250х4 мм.
[C]:
Колонка: Lichrospher (5 мкм) 100 RP 8 125х4 мм; элюент A: 0,01M фосфат натрия, pH 7,0; элюент В: 0,005 М фосфат натрия, pH 7,0/60 объемн.% пропан-2-ола; истечение: 0,7 мл/мин; градиент: 1-99% В/50 мин.
Масс-спектрометрия (MS): EI (ионизация электронным ударом) М+ FAB (бомбардировка быстрыми атомами) (М+Н)+
DMPP - смола обозначает 4-(2',4'-диметоксифенил-гидроксиметил) феноксисмолу; сверхкислая лабильная (неустойчивая) смола, которая позволяет осуществлять синтез защищенных в боковых цепях пептидов.
Примеры см. в конце описания.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЦИКЛОПЕПТИДЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, СОДЕРЖАЩИЕ ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1994 |
|
RU2130030C1 |
| ЦИКЛИЧЕСКИЕ АЗАПЕПТИДЫ С АНГИОГЕННЫМ ДЕЙСТВИЕМ | 1998 |
|
RU2188205C2 |
| ЦИКЛОПЕПТИДЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1996 |
|
RU2157379C2 |
| ПРОИЗВОДНЫЕ ЦИКЛОПЕПТИДОВ | 1997 |
|
RU2202557C2 |
| ЦИКЛОПЕПТИДНЫЕ ПРОИЗВОДНЫЕ | 1996 |
|
RU2174520C2 |
| ЦИКЛОПЕПТИДЫ ИЛИ ИХ СОЛИ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ И СПОСОБ ИХ ПОЛУЧЕНИЯ, СПОСОБ ЛЕЧЕНИЯ | 1993 |
|
RU2129563C1 |
| ЦИКЛИЧЕСКИЕ ИНГИБИТОРЫ АДГЕЗИИ | 1997 |
|
RU2184121C2 |
| НАПРАВЛЕННОЕ ИНГИБИРОВАНИЕ TGF БЕТА | 2015 |
|
RU2752424C2 |
| ЖИДКИЙ ПРЕПАРАТ, СОДЕРЖАЩИЙ ОЛИГОПЕПТИДЫ И ЭТЕРИФИЦИРОВАННЫЙ ЦИКЛОДЕКСТРИН | 2003 |
|
RU2322254C2 |
| ИНГИБИТОРЫ ТРОМБИНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1994 |
|
RU2138275C1 |























Описываются новые биотиновые соединения общей формулы I где Q отсутствует или обозначает -NH-(CH2)5-CO-, R1 обозначает X-Arq-Gly-Asp-y, X = трипептид: Gly-Gly-Gly-, y = дипептид: -Ser-Pro, или R1 обозначает A-Cys(R2)-B-U, R2 обозначает Н, Trt; А обозначает Asp или пептидный фрагмент, выбранный из группы, состоящей из: Ala-Asp, Thr-Ala-Asp, Lys- Thr-Ala-Asp, Lys- Ala-Ala-Asp, Arq-Thr-Ala-Asp, Ser-Ala-Asp, Gln-Ser- Ala-Asp. Gly-Lys-Thr- Ala-Asp, Ile-Ser-Ala-Gly, Arq-Ser-Ala-Gly-Lys-Thr-Cys(Trt)-Asp, В отсутствует или обозначает Pro или N-метилированное производное Ala, причем, если R1 обозначает A-Cys(R2)-B-U, то лишь один из остатков А или В может отсутствовать, U обозначает Он или NH-2, или R1 обозначает цикло(Arq-Gly-Asp-Z), Z в боковой цепи связан с Q или, если Q отсутствет, с биотином, z обозначает ди- или трипептидный остаток, причем аминокислоты независимо друг от друга выбирают из группы, состоящей из Ala, Val, Tyr, Trp, Phe, Cys, Lys, M, при этом указанные аминокислоты могут быть дериватизированы, а аминокислотные остатки связаны друг с другом пептидоподобно через N-амино- и α-карбоксильные группы, причем М содержится всегда и обозначает NH(R8)-CH(R3)-COOH, R3 = R6 - R4, где R4 = ОН, R6 = алкиленфенил с 7 - 14 С-атомами, R8 = Н, алкил с 1 - 6 С-атомами, причем, если речь идет об остатках оптически активных аминокислот и аминокислотных производных, то включаются, как D-, так и L-формы, а также их соли. Описывается способ из получения, фармацевтические композиции и способ их получения. Соединение можно применять в качестве интегриновых ингибиторов, в частности, для профилактики и лечения заболеваний круга крообращения, при тромбозах, инфаркте сердца, артериосклерозе и в терапии опухолей. 4 с. и 1 з.п.ф-лы, 1 табл. 

где Q отсутствует или обозначает -NH-(CH2)5-CO-;
R1 обозначает X-Arq-Gly-Asp-y;
X - трипептид: Gly-Gly-Gly-,
y - дипептид: -Ser-PrO,
или R1 обозначает A-Cys(R2)-B-U,
R2 обозначает H, Trt;
A обозначает Asp или пептидный фрагмент, выбранный из группы, состоящей из: Ala-Asp, Thr-Ala-Asp, Lys-Thr-Ala-Asp, Lys-Ala-Ala-Asp, Arq-Thr-Ala-Asp, Ser-Ala-Asp, Gln-Ser-Ala-Asp, Gly-Lys-Thr-Ala-Asp, Ile-Ser-Ala-Gly, Arq-Ser-Ala-Gly, Gly-Lys-Thr-Cys(Trt)-Asp,
B отсутствует или обозначает Pro или N-метилированное производное Ala, причем, если R1 обозначает A-Cys(R2)-B-U, то лишь один из остатков A или B может отсутствовать;
U обозначает OH или NH-2;
или R1 обозначает цикло(Arq-Gly-Asp-Z), Z в боковой цепи связи с Q или если Q отсутствует, с биотином;
z обозначает ди- или трипептидный остаток,
причем аминокислоты, независимо друг от друга выбирают из группы, состоящей из Ala, Val, Tyr, Trp, Phe, Cys, Lys, M, при этом указанные аминокислоты могут быть дериватизированы, а аминокислотные остатки связаны друг с другом пептидоподобно через N-амино- и α-карбоксильные группы, причем M содержится всегда и обозначает:
NH(R8)-CH(R3)-COOH,
R3 = R6 - R4,
где R4 = OH,
R6 = алкиленфенил с 7 - 14 C-атомами;
R2 = H, алкил с 1 - 6 C-атомами,
причем, если речь идет об остатках оптически активных аминокислот и аминокислотных производных, то включаются как D-, так и L-формы, а также их соли.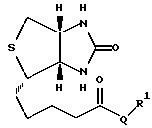
где а) Q отсутствует и R1 обозначает цикло-(Arq-Gly-Asp-D-Phe-Lys); б) Q отсутствует и R1 обозначает Gly-Gly-Gly-Arq-Gly-Asp-Ser-Pro-Lys-OH; в) Q отсутствует и R1 обозначает Gly-Gly-Gly-Lys-Thr-Ala-Asp-Cys(Trt)-Pro-OH; г) Q обозначает -NH-(CH2)5-CO- и R1 обозначает цикло-(Arq-Gly-Asp-D-Phe-Lys); д) Q обозначает -NH-(CH2)5-CO- и R1 обозначает цикло-(Arq-Gly-Asp-D-Phe-Lys-Gly); е) Q обозначает -NH-(CH2)5-CO- и R1 обозначает цикло-(Arq-Gly-Asp-D-Phe-Val-Lys); ж) Q обозначает -NH-(CH2)5-CO- и R1 обозначает цикло-(Arq-Gly-Asp-D-Trp-Lys); з) Q обозначает -NH-(CH2)5-CO- и R1 обозначает цикло-(Arq-Gly-Asp-D-Tyr-Lys),
а также физиологически приемлемые соли указанных соединений.
H-Q-R11,
где Q и R1 имеют значения, указанные в п.1,
ацилируют соединения формулы III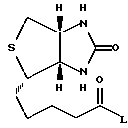
где L обозначает CL, Br, J или свободную, или реакционноспособную, функционально измененную OH-группу,
и, в случае необходимости, полученное при этом основание или кислое соединение формулы I путем обработки кислотой или основанием переводят в одну из его солей.
| RU 94015842 A1, 10.01.1996 | |||
| НИЖНЯЯ ЧАСТЬ ПОДЗЕМНОГО ПОЖАРНОГО ГИДРАНТА | 2010 |
|
RU2446256C1 |
| DE 4310643 A1, 06.10.1994 | |||
| DE 4336758 A1, 04.05.1995 | |||
| US 5087561 A1, 11.02.1992 | |||
| Автоматический огнетушитель | 0 |
|
SU92A1 |
| EP 0406428 A1, 09.01.1991. | |||
Авторы
Даты
2001-08-10—Публикация
1996-09-13—Подача