Изобретение относится к гибридомной технологии и касается получения моноклональных антител. Штамм назван GMVd - 3(268). Он депонирован в специализированной коллекции перевиваемых соматических клеток позвоночных Всероссийской коллекции клеточных культур под номером ВСКК(П) 650 Д.
Одним из направлений усовершенствования иммунодиагностических препаратов является использование в качестве основы для их производства специфических моноклональных иммуноглобулинов, продуцируемых стабильными гибридными клеточными линиями.
Для ускоренного обнаружения возбудителей сапа и мелиоидоза с помощью экспресс-методов производимые в настоящее время коммерческие иммунодиагностические препараты изготавливают на основе иммуноглобулинов специфических сывороток различных видов животных, гетерогенных по составу антител, иммунологической структуре, активности и специфичности.
Основные трудности в производстве эритроцитарного препарата связаны с получением стандартного иммуноглобулинового сырья для его производства. Технология изготовления диагностикума эритроцитарного иммуноглобулинового сапного включает в себя продолжительный этап иммунизации различных видов животных с использованием разнообразных приемов введения антигенов. Однако получение гипериммунных специфических сывороток нередко затруднено, зависит от индивидуальных функциональных особенностей иммунной системы животного - продуцента (Волков Е.В., Рыбкин В.С. Оптимизация условий получения сапного иммуноглобулинового эритроцитарного диагностикума. Дезинфекция и стерилизация. Перспективы развития: Материалы Всесоюз. науч. конф. - Волгоград, 1983, с. 23-27). Вследствие этого полное воспроизведение всех этапов накопления сырья для производства эритроцитарного диагностикума невозможно, что приводит к получению относительно нестандартных по свойствам препаратов.
Цель изобретения - получение штамма гибридомы-продуцента специфических гомогенных по составу и свойствам моноклональных антител (МКА), обладающих высокой гемосенситивной активностью в отношении формалинизированных эритроцитов барана - сырья для производства диагностикума эритроцитарного иммуноглобулинового сапного моноклонального.
Получение гибридомы достигается иммунизацией мышей BALB/c целыми клетками Pseudomonas pseudomallei с последующей гибридизацией лимфоцитов селезенки иммунизированных мышей с миеломными клетками мыши. Концентрация иммуноглобулинов (IgM) в среде составляет в среднем 0,46-0,62 мг/мл, активность иммуноглобулинов в культуральной среде в ТИФА 1:640, в асцитической жидкости 1: 100000. Стабильность продуцирования сохраняется на протяжении 20 пассажей в культуре. Антитела обладают высокой гемосенситивной активностью в отношении формалинизированных танизированных эритроцитов барана, вследствие чего данный тип моноклональных иммуноглобулинов отобран для использования в качестве сырья для производства диагностикума эритроцитарного иммуноглобулинового сапного моноклонального.
Гибридома получена слиянием миеломы мышей P3-X63-Ag 8.653 и спленоцитов мыши линии BALB/c. Слияние проведено с помощью полиэтиленкликоля с последующим клонированием штамма-продуцента методом лимитирующих разведений. Полученный штамм назван GMVd-3(2G8) и характеризуется следующими признаками.
Культурные признаки. Культивирование in vitro. Среда для культивирования - среда RPMI-1640 с добавлением 15%-ной эмбриональной телячьей сыворотки, 2мМ L-глютамина, 10 мМ ГЭПЭС, 4 мМ пирувата натрия.
Клетки культивируют при 37oC в атмосфере 5%-ного СО2 и 70-80%-ной влажности. Клетки пассируют один раз в 3-4 дня, контролируя микроскопически интенсивность роста. Кратность рассева 1:4-1:10. Культура суспензионная.
Культивирование в организме животного. Для накопления асцита клетки гибридомы вводят праймированным мышам линии BALB/c в дозе 1• 105 - 1• 106 клеток на мышь. Асцит образуется через 2-4 недели.
Продуктивность штамма. Продукция МКА в среде культивирования составляет 0,46 - 0,62 мг/мл, в асцитической жидкости 35-40 мг/мл. Продукция МКА в культуральной жидкости сохраняется на протяжении 20 пассажей.
Характеристика получаемого продукта. Антитела относятся к классу IgM. Они специфически взаимодействуют с определенным эпитопом термостабильного антигена возбудителя сапа. Специфичность взаимодействия определяется с помощью ТИФА и НМФА.
Криоконсервирование. 2-4•106 клеток штамма консервируют в 1 мл среды RPMI-1640 c 20%-ной эмбриональной телячьей сывороткой и 7%-ного диметилсульфоксида в пластиковых ампулах. Замораживание производят при 4oC (30 мин), а затем помещают в комплекс криоконсервирования биоматериалов, предназначенный для контролируемого замораживания клеточных культур тканей в заданном режиме: до температуры -20oC со скоростью 1,0 град/мин, до -40oC со скоростью 1,5 град/мин, до - 70oC со скоростью 5,0 град/мин. Затем ампулы погружают в жидкий азот и хранят в нем до момента использования. Размораживание производят быстро при -37oC на водяной бане. Жизнеспособность после размораживания составляет 65-75%.
Пример 1. Штамм получают следующим образом. Мышей линии BALB/c иммунизируют ультразвуковыми дезинтегратами клеток P. pseudomallei C-141. Первые две инъекции с интервалом в одну неделю производят подкожно в дозе 5•108 м.к. с неполным адъювантом Фрейнда (1:1) в объеме 0,3 мл и внутрибрюшинно в дозе 1•109 м. к. в объеме 0,5 мл физиологического раствора. Бустирующее введение антигена производят на 21-22-й день после начала иммунизации внутриселезеночно в дозе клеток 5•108 м.к. в 0,1 мл физиологического раствора. Через 3 дня после этого 1•108 спленоцитов иммунных мышей гибридизируют с 1•107 клеток мышиной миеломы P3-X63-Ag8.653 в присутствии 1 мл 50%-ного полиэтиленгликоля с мол.м. 4000 в течение 2 мин. Затем к этой смеси при постоянном перемешивании последовательно вносят 1,2,4 и 8 мл бессывороточной среды, каждую порцию в течение 2 мин. После этого клетки центрифугируют при 1000 об/мин в течение 10 мин. Осадок ресуспендируют в селективной среде ГАТ-среде с 15%-ной эмбриональной телячьей сывороткой, 2мМ L-глютамина, 4 мМ пирувата натрия. Клетки высевают в 96-луночную пластину с фидером по 2,5 - 5•105 клеток в лунку. Смену среды производят через 3-4 дня. Отбор гибридом-продуцентов в лунках опытной пластины определяют по наличию специфических иммуноглобулинов в культуральной среде с помощью ТИФМ. Выявленные гибридомы-продуценты клонируют не менее двух раз методом предельных разведений на среде RPMI-1640 с 15%-ной эмбриональной телячьей сывороткой с добавками в 96-луночных плато с фидером-мышиными перитонеальными макрофагами (4•104 клеток в лунке). После второго клонирования практически все 100% субклонов продуцируют МКА.
Среди продуктивных клонов, секретирующих МКА против антигенных детерминант возбудителей сапа и мелиоидоза, селекционирован клон-продуцент GMVd-3(2G8).
Пример 2. Накопление МКА. Ампулы с клетками гибридомы вынимают из сосуда с жидким азотом и быстро оттаивают на водяной бане при 37oC. Размороженные клетки переносят в центрифужную пробирку с 20 мл бессывороточной среды RPMI-1640, осторожно наслаивают взвесь клеток на среду. Клетки осаждают центрифугированием и после удаления отмывающей среды высевают на матрас 25 см2 на среду RPMI-1640 с 15%-ной эмбриональной телячьей сывороткой. Матрас инкубируют во влажной атмосфере с 5%-ным CO2 при 37oC. Когда колония клеток покрывает более трети дна матраса, осуществляют отбор проб культуральной среды с целью определения титра МКА с помощью ТИФА. При полном покрытии дна матраса гибридными клетками производят их рассев на несколько матрасов. Таким способом тиражируют клетки гибридомы in vitro.
Для получения более концентрированного препарата антител гибридомы-продуценты накапливают в асцитической жидкости мышей BALB/c. Животных предварительно сенсибилизируют внутрибрюшинным введением пристана - 2,6,10,14-тетраметилпентадекана (0,3 мл на мышь) или неполного адъюванта Фрейнда (0,5 мл на мышь). Через неделю мышам внутрибрюшинно вводят по 1•105-1•106 клеток гибридомы, После появления у мышей асцитической жидкости и солидных опухолей собирают содержимое брюшной полости. Клетки осаждают центрифугированием, к надосадочной жидкости добавляют сульфат аммония до 50% его насыщения. Рыхлый осадок центрифугируют при 10000 об/мин в течение 20 мин, надосадочную жидкость удаляют. Плотный осадок растворяют в физиологическом растворе до исходного исходного объема, диализуют против этого же раствора в течение суток при 4oC до полного удаления сульфата аммония. Осаждение МКА сульфатом аммония до 50% его насыщения повторяют трижды как описано выше. В полученном растворе очищенных МКА определяют концентрацию белка спектрофотометрически. В качестве стандартного используют 1%-ный раствор бычьего сывороточного альбумина.
Специфическую активность МКА определяют с помощью ТИФА и НМФА. При постановке ТИФА полистироловые пластины обрабатывают в течение ночи при 4oC водно-солевым экстрактом P. pseudomallei 56830 или P. mallei 10230, разделенным на 0,05 M карбонатно-бикарбонатном буфере, pH 9,5, до концентрации 1-10 мкг/мл по белку. Затем пластины трижды отмывают забуференным физраствором с 0,05% твина -20. На этом же растворе производят титрование образцов МКА в объеме 100 мкл, которые выдерживают в пластинах в течение 1 ч при 37oC. После очередного трехкратного отмывания пластин вносят антивидовой конъюгат в рабочем разведении, приготовленный на ЗФР с твином-20. Конъюгат представляет собой кроличьи антимышиные IgG, меченные пероксидазой хрена. Время инкубации 1 ч при 37oC, объем 100 мкл на лунку. Вновь повторяют отмывание. В заключение вносят смесь - перекись водорода с 5-аминосалициловой кислотой. После инкубации при комнатной температуре в течение 40 - 60 мин измеряют оптическую плотность жидкости в каждой лунке при длине волны 405 нм. МКА, выделенные из асцитической жидкости, в ТИФА активны в разделении 1: 5•103-1•104.
Специфическую активность МКА оценивают в непрямом методе флюоресцирующих антител с коммерческим антивидовым конъюгатом люминесцирующих иммуноглобулинов против глобулинов мыши. МКА, выделенные из асцитической жидкости мышей, в НМФА активны в разведении 1:1•104-1:105.
Средний объем асцитической жидкости, получаемый при культивировании гибридомы GMVd-3(2G8) в организме животных, составляет 3,8 + 0,12 мл, продуцирующая активность in vivo - 35-40 мг моноклональных иммуноглобулинов на 1 мл асцитической жидкости.
Пример 3. Использование МКА GMVd-3(2G8) для конструирования диагностикума эритроцитарного иммуноглобулинового сапного моноклонального. Образцы МКА используют в качестве сырья для изготовления диагностикума эритроцитарного иммуноглобулинового сапного моноклонального. Для оценки гемосенсибилизирующей активности моноклональных иммуноглобулинов необходимый для работы объем формализированных и танизированных эритроцитов отмывают 0,9%-ным раствором NaCl, pH 6,4, центрифугируя взвесь клеток при 3000 об/мин в течение 10 мин. Осадок ресуспендируют этим же раствором до концентрация 2,5% и прогревают до 45oC. Прогретые эритроциты и приготовленные разведения МКА на 0,9%-ном NaCl, pH 6,4 c концентрацией белка от 250 до 1500 мкг/мл смешивают в равных объемах. Смесь инкубируют при 45oC и постоянном встряхивании в течение 1,5-2 ч. За 30 мин до окончания сенсибилизации эритроцитов в смесь добавляют формалин до концентрации 0,5-1,0%. Затем пробы эритроцитов трижды отмывают раствором 0,9%-ного NaCl, pH 7,2 с добавлением 0,25%-ной нормальной кроличьей сыворотки. Осадок трижды ресуспендируют этим же раствором до концентрации эритроцитов 2,5%.
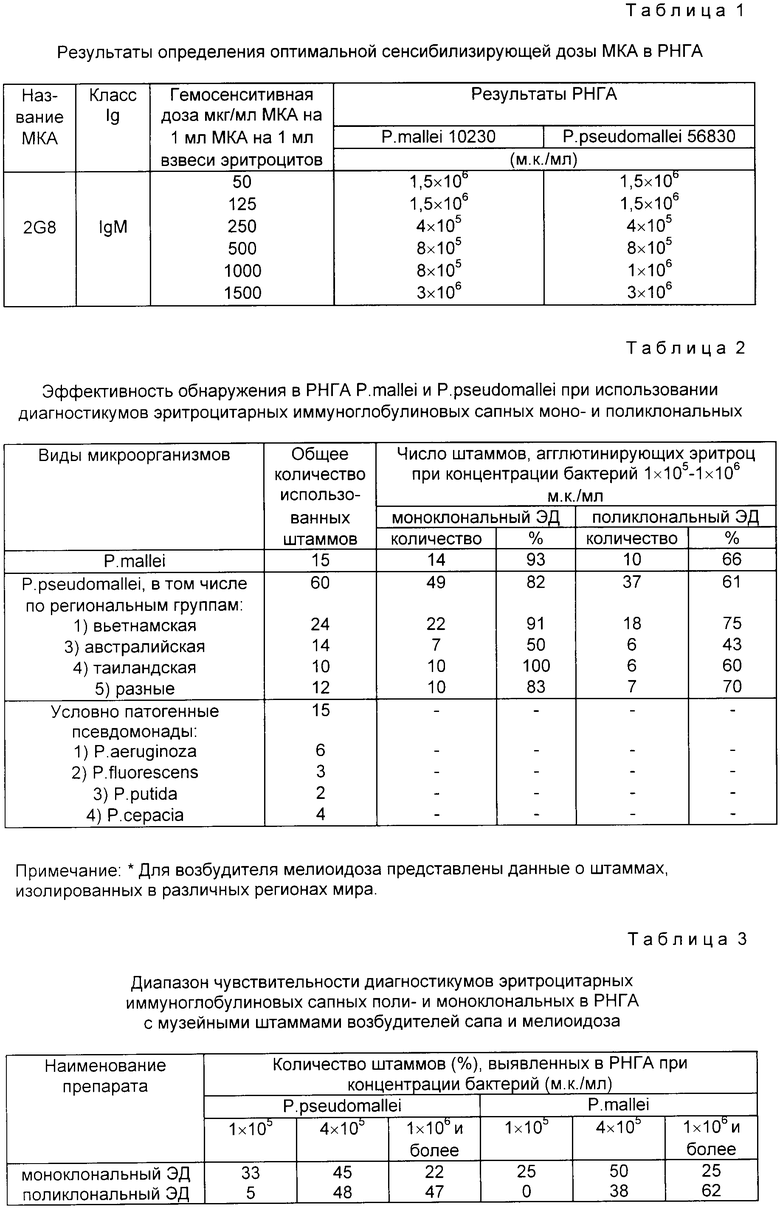
Активность полученных образцов эритроцитов, нагруженных специфическими МКА, проверяют в РНГА со взвесью Pseudomonas mallei 10230 и P. pseudomallei 56830. Оптимальной сенсибилизирующей дозой иммуноглобулинов считают такую концентрацию МКА, которая обеспечивает получение образцов эритроцитарного диагностикума с максимальной чувствительностью (не ниже 1•106 м.к./мл). Результаты определения оптимальной гемосенсибилизирующей дозы МКА в РНГА представлены в табл.1.
Данные, представленные в табл. 1, свидетельствуют о том, что оптимальная гемосенситивная доза МКА составляла 250-500 мкг/на 1 мл 2,5%-ной взвеси формалинизированных и танизированных эритроцитов.
Опытную серию препарата готовят так, как описано выше. Танизированные эритроциты смешивают с МКА, взятыми в удвоенной концентрации по отношению к оптимальной сенсибилизирующей дозе МКА.
После поверки эритроцитарного диагностикума в РНГА со взвесью P.mallei и P. pseudomallei ампулы с 10%-ной взвесью эритроцитов в защитной среде (15% реополиглюкина и 7,5% сахарозы) подвергают лиофилизации и хранят при +4oC.
Пример 4. Оценка активности, чувствительности и специфичности диагностикума эритроцитарного иммуноглобулинового сапного моноклонального. При постановке РНГА используют живые, обеззараженные 4%-ным нейтральным формалином, с экспозицией 1 ч или автоклавированные при 120oC в течение 30 мин взвеси бактерий различных штаммов возбудителей сапа и мелиоидоза.
Установлено, что спектр специфической активности моноклонального сапного эритроцитарного диагностикума в отношении штаммов P.mallei и P.pseudomalei шире, чем у коммерческого диагностикума эритроцитарного иммуноглобулинового сапного (прототип). Данные результатов РНГА отражены в табл.2.
В соответствии с представленными в табл. 2 результатами диагностикум эритроцитарный иммуноглобулиновый сапный моноклональный позволяет выявлять в РНГА до 93% штаммов P.mallei и 82% P.pseudomallei при концентрации бактерий 1•105-106 м.к./мл, не взаимодействуя с другими видами псевдомонад.
В ходе испытаний отмечено, что чувствительность препарата на основе МКА с рядом штаммов P. mallei и P. pseudomallei превышала показатель чувствительности коммерческого препарата. Результаты этих исследований представлены в табл. 3.
Анализ полученных результатов экспериментов позволил сделать заключение о высокой чувствительности и специфичности диагностикума эритроцитарного иммуноглобулинового сапного моноклонального и об эффективности его использования в РНГА для обнаружения патогенных псевдомонад (возбудителей сапа и мелиоидоза).
Преимуществом сапных моноклональных иммуноглобулинов, используемых в качестве основы для конструирования эритроцитарного диагностикума, является стабильность иммуноглобулинового сырья, практически 100%-ная воспроизводимость результатов опытов по сенсибилизации эритроцитов, что выгодно отличает данную основу от поликлональных иммуноглобулинов при производстве эритроцитарного диагностикума для РНГА.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ДИАГНОСТИКУМА ЭРИТРОЦИТАРНОГО САПНОГО ИММУНОГЛОБУЛИНОВОГО МОНОКЛОНАЛЬНОГО | 2017 |
|
RU2658434C1 |
| ШТАММ КУЛЬТИВИРУЕМЫХ ГИБРИДНЫХ КЛЕТОК ЖИВОТНОГО MUS. MUSCULUS - ПРОДУЦЕНТ МОНОКЛОНАЛЬНОГО АНТИТЕЛА К ТЕРМОСТАБИЛЬНОМУ ПОВЕРХНОСТНОМУ АНТИГЕНУ ВОЗБУДИТЕЛЯ МЕЛИОИДОЗА | 1997 |
|
RU2116344C1 |
| ШТАММ КУЛЬТИВИРУЕМЫХ ГИБРИДНЫХ КЛЕТОК ЖИВОТНОГО MUS MUSCULUS - ПРОДУЦЕНТ МОНОКЛОНАЛЬНОГО АНТИТЕЛА К ТЕРМОСТАБИЛЬНОМУ КОМПОНЕНТУ КАПСУЛОПОДОБНОЙ СУБСТАНЦИИ ВОЗБУДИТЕЛЯ МЕЛИОИДОЗА | 1997 |
|
RU2117042C1 |
| ШТАММ КУЛЬТИВИРУЕМЫХ ГИБРИДНЫХ КЛЕТОК ЖИВОТНОГО MUS MUSCULUS L. BPM VD-10 - ПРОДУЦЕНТ МОНОКЛОНАЛЬНОГО АНТИТЕЛА 5H/E К АНТИГЕНУ 200 KDA ВОЗБУДИТЕЛЯ МЕЛИОИДОЗА | 2014 |
|
RU2570638C1 |
| СПОСОБ ПОЛУЧЕНИЯ АНТИГЕННОГО ЭРИТРОЦИТАРНОГО ДИАГНОСТИКУМА ДЛЯ ОБНАРУЖЕНИЯ АНТИТЕЛ К АНТИГЕНАМ ВОЗБУДИТЕЛЕЙ САПА И МЕЛИОИДОЗА | 2013 |
|
RU2540902C1 |
| ШТАММ КУЛЬТИВИРУЕМЫХ ГИБРИДНЫХ КЛЕТОК ЖИВОТНОГО MUS MUSCULUS L. BPM VD-11 - ПРОДУЦЕНТ МОНОКЛОНАЛЬНОГО АНТИТЕЛА 6A/G К АНТИГЕНУ 200 kDA ВОЗБУДИТЕЛЯ МЕЛИОИДОЗА | 2014 |
|
RU2570634C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИАГНОСТИКУМА ЭРИТРОЦИТАРНОГО АНТИГЕННОГО САПНОГО | 2001 |
|
RU2188036C1 |
| ДИАГНОСТИКУМ ПСЕВДОТУБЕРКУЛЕЗНЫЙ ЭРИТРОЦИТАРНЫЙ МОНОКЛОНАЛЬНЫЙ | 2008 |
|
RU2377308C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ЭРИТРОЦИТАРНОГО ДИАГНОСТИКУМА ИММУНОГЛОБУЛИНОВОГО ТУЛЯРЕМИЙНОГО | 2020 |
|
RU2747420C1 |
| ШТАММ КУЛЬТИВИРУЕМЫХ ГИБРИДНЫХ КЛЕТОК ЖИВОТНОГО MUS musculus Вpm Vd-8 - ПРОДУЦЕНТ МОНОКЛОНАЛЬНОГО АНТИТЕЛА 3C/A К АНТИГЕНУ 200 kDa ВОЗБУДИТЕЛЯ МЕЛИОИДОЗА | 2014 |
|
RU2555544C1 |
Штамм предназначен для получения моноклонального антитела к термостабильному антигену, общему для возбудителей сапа и мелиоидоза. Антитела относятся к изотопу Ig M. Концентрация иммуноглобулинов в культуральной среде составляет 0,46 - 0,62 мг/мл. Моноклональные антитела обладают высокой гемосенситивной активностью в отношении формалинизированных эритроцитов барана и поэтому могут использоваться для получения эритроцитарного диагностикума сапа и медиоидоза. 3 табл.
Штамм культивируемых гибридных клеток животного Mus musculus ВСКК(П) 650Д - продуцент моноклонального антитела к термостабильному антигену, общему для возбудителей сапа и мелиоидоза.
| Волков Е.В., Рыбкин В.С | |||
| Оптимизация условий получения сапного иммуноглобулинового эритроцитарного диагностикума | |||
| Дезинфекция и стерилизация | |||
| Перспективы развития: Материалы всесоюзной научной конференции | |||
| - Волгоград, 1983, с.23 - 27. |
Авторы
Даты
1998-08-10—Публикация
1997-07-02—Подача