Изобретение относится к биотехнологии, в частности к способу получения гибридом-продуцентов моноклональных антител (МКА) заданной специфичности, и может быть использовано в практической работе специализированных лабораторий, занимающихся вопросами эпиднадзора за возбудителями особо опасных инфекций, для решения научно-исследовательских задач по изучению свойств различных видов буркхольдерий и разработке новых схем обнаружения и идентификации возбудителей сапа и мелиоидоза, а также быть использовано для получения целевого продукта - моноклональных антител, необходимых для конструирования на их основе высокоэффективного препарата иммуноглобулинов диагностических флуоресцирующих для метода флуоресцирующих антител (МФА), применяемого при экспресс-обнаружении микроорганизмов II группы патогенности в пробах с различных объектов внешней среды и клинического материала, в том числе патогенных буркхольдерий, к которым относятся возбудители мелиоидоза (Burkholderia pseudomallei) и сапа (Burkholderia mallei). Штамм-продуцент моноклональных антител к антигену 200 kDa назван Bpm Vd-11 (6A11/G12). Штамм депонирован в Государственную коллекцию патогенных микроорганизмов и клеточных культур «ГКПМ-Оболенск» под номером Н-41.
Порядок выполнения работ по обнаружению и идентификации возбудителей мелиоидоза и сапа описан в «Практических руководствах» [1, 2] и «Методических указаниях» [3, 4]. Согласно этим источникам одним из регламентированных методов быстрого и достоверного обнаружения возбудителей особо опасных инфекций в различных объектах исследования является МФА. Он позволяет получить предварительный (ориентировочный) ответ в течение 1-2 ч от момента начала исследования, а также идентифицировать искомый микроорганизм на этапе ускоренного анализа.
Для воспроизведения данного метода в условиях работы специализированных лабораторий, занимающихся вопросами индикации и идентификации патогенных микроорганизмов, была разработана технология изготовления двух препаратов. В качестве основы этих иммунобиологических средств использовали МКА к антигенам поверхностных структур патогенных буркхольдерий [5, 6]. Иммуноглобулины диагностические флуоресцирующие мелиоидозные моноклональные (№ ФСР 2011/11615) и иммуноглобулины диагностические флуоресцирующие сапные моноклональные (№ ФСР 2011/11614) предназначены для обнаружения В. pseudomallei и В. mallei соответственно. Оба препарата в рабочем разведении позволяют дифференцировать в МФА В. pseudomallei и В. mallei - два близких в антигенном отношении вида буркхольдерий. В то же время при работе с препаратом «Иммуноглобулины диагностические флуоресцирующие мелиоидозные моноклональные» необходимо учитывать факт того, что этот препарат обладает кросс-реактивностью в отношении В. thailandensis, близкородственной буркхольдерий III группы патогенности.
В последние годы в рамках совершенствования средств индикации и идентификации возбудителя мелиоидоза получило развитие новое направление по созданию высокоэффективных диагностических препаратов на основе МКА к поверхностно локализованному гликопротеину - антигену 200 kDa В. pseudomallei, одному из маркеров вирулентности возбудителя мелиоидоза [7]. Известно, что данный антиген (АГ) отсутствует на поверхности микробных клеток авирулентных штаммов В. pseudomallei [8, 9].
Получение МКА к антигену 200 kDa В. pseudomallei открывает эффективный путь дифференциации патогенных и непатогенных видов буркхольдерий, а также внутривидового типирования возбудителя мелиоидоза [10].
При этом использование моноклональных антител заданной специфичности позволяет реализовывать основной принцип современной иммунодиагностики, заключающийся в применении на практике методов, обладающих высокими уровнями пороговой чувствительности в сочетании с исключительными преимуществами МКА к диагностически значимым антигенам искомых возбудителей опасных инфекционных заболеваний.
Изготовление диагностических препаратов для иммунофлуоресцентного анализа на основе моноклональных антител имеет ряд известных преимуществ [11, 12]. Основным технологическим преимуществом является возможность работы с гомогенным по составу и свойствам сырьем, которое при наличии постоянного источника МКА, соответствующей гибридомы-продуцента, можно накопить в необходимом количестве в любой запланированный промежуток времени и получить серию стандартизированного препарата высокого качества с известной эпитопной направленностью.
Цель изобретения - получение штамма гибридомы-продуцента моноклонального антитела против эпитопа в составе антигена 200 kDa, экспонированного на поверхности микробных клеток патогенных буркхольдерий (В. pseudomallei и В. mallei).
Получение гибридомы достигается гибридизацией двух типов клеток: спленоцитов инбредной мыши линии BALB/c, иммунизированной антигеном 200 kDa возбудителя мелиоидоза, и клеток мышиной миеломы.
Гибридома-продуцент МКА 6A11/G12 получена в результате слияния спленоцитов иммунной мыши линии BALB/c с клетками мышиной миеломы P3-X63.Ag8.653 в присутствии конъюгирующего агента - полиэтиленгликоля (ПЭГ-4000), последующего рассева взвеси клеток в лунки 96-луночных культуральных пластин, выращивания в селективных средах в течение трех недель с постепенным переходом на полную среду культивирования гибридных клеток, отбора первичного клона по показателю продукции специфических антител к антигену 200 kDa возбудителя мелиоидоза, его клонирования и реклонирования с использованием метода лимитирующих разведений. Полученный штамм назван Bpm Vd-11 (6A11/G12), депонирован в Государственную коллекцию патогенных микроорганизмов и клеточных культур «ГКПМ-Оболенск» под номером Н-41, характеризуется перечисленными ниже признаками.
Условия культивирования гибридомы in vitro. Оптимальной средой выращивания гибридомы in vitro является среда RPMI-1640 с 15% эмбриональной телячьей сыворотки (ЭТС), 2 mМ L-глютамина, 10 mM Hepes, 4 mМ пирувата натрия, pH 7,1-7,2.
Клетки культивируют при 37°C в атмосфере 5-7% СO2 и влажности 70-80%. Интенсивность роста популяции клеток контролируют при просмотре лунок пластин в инвертированном микроскопе. Пересевы делают каждые 3-4 сут, кратность рассева 1:4-1:8.
Условия культивирования гибридомы in vivo в организме сингенного животного. Для накопления асцита in vivo клетки гибридомы вводят внутрибрюшинно предварительно праймированным мышам линии BALB/c, по 1·106-2·106 клеток на мышь. Наблюдают за животными ежедневно, начиная с 10 дня после введения клеток до конца месяца. Чаще всего асцит образуется через 2-4 недели.
Культуральные признаки. Характер роста культуры in vitro - полусуспензионный, in vivo - прививаемость гибридных клеток в брюшной полости хорошая, до 90%.
Продуктивность штамма. Продукция МКА в среде культивирования составляет 0,31 мкг/мл, в асцитической жидкости - 10-14 мг/мл. Объем асцитической жидкости в среднем равен 3-3,5 мл.
Характеристика получаемого продукта. Антитела относятся к классу IgM. Они специфически взаимодействуют с эпитопом в составе антигена 200 kDa патогенных буркхольдерий. Специфичность взаимодействия определяют с помощью твердофазного иммуноферментного метода (ТИФМ).
Криоконсервирование. Вне периода экспериментов по накоплению препаративных количеств МКА 6A11/G12 клетки гибридомы сохраняют в криоконсервированном состоянии. Для перевода их в такое состояние взвесь клеток гибридомы в количестве 4·106 клеток в 1 мл защитной среды, состоящей из среды RPMI-1640 с 20% ЭТС и 7% диметилсульфоксида, переносят в пластиковые ампулы. Ампулы помещают в аппарат для криоконсервирования биологического материала. Используют режим постепенного программируемого понижения температуры: в течение 20 минут - снижение температуры образца до 0°C, далее со скоростью 1°C в минуту до температуры минус 40°C и далее со скоростью 5°C в минуту - от минус 40°C до минус 70°C. Затем ампулы погружают в биохранилище с жидким азотом и хранят до момента использования. Размораживание производят при 37°C на водяной бане в течение 2-3 минут. Жизнеспособность клеток после размораживания составляет не менее 85-90%.
Пример 1. Получение штамма гибридомы-продуцента.
Получение штамма гибридомы-продуцента состоит из последовательных стадий по подготовке клеток-партнеров (В-лимфоцитов мыши линии BALB/c, иммунизированной антигеном 200 kDa, и клеток мышиной миеломы P3-X63.Ag8.653) к соматической гибридизации, последующего выращивания в селективных средах спленоцитов и клеток мышиной миеломы, клонирования методом предельных разведений и отбора моноклонов, секретирующих иммуноглобулины к эпитопам антигена, применяемого для стимуляции лимфоцитов.
Все манипуляции выполняют в ламинарном потоковом шкафу с горизонтальным потоком воздуха (тип "защита продукта").
Иммунизация мыши-донора В-лимфоцитов. Мышь линии BALB/c иммунизируют гликопротеином капсулы возбудителя мелиоидоза (антигеном 200 kDa В. pseudomallei), экстрагированным формамидом из обеззараженных ацетоном и высушенных клеток вирулентного штамма возбудителя мелиоидоза по методу Фуллера в модификации Пивеня Н.Н. [13, 14]. Схема иммунизации состоит из четырех инъекций. Дни введения: 0, 7, 17 и 21. Способы введения АГ: 1-я инъекция - подкожное введение 25 мкг антигена (по белку) в объеме 0,3 мл в сочетании с неполным адъювантом Фрейнда (1:1 по объему), 2-я и 3-я - внутрибрюшинное введение 0,3 мл раствора антигена, разведенного в 0,15 M NaCl, по 20 мкг, 4-я заключительная бустирующая - внутриселезеночное введение антигена (20 мкг), за 3 сут до гибридизации. Суммарная нагрузка на одно животное - 85 мкг на цикл. Эта доза является предельно допустимой, так как превышение антигенной нагрузки приводит к падению титров гуморальных антител и толерантности [15].
Подготовка миеломных клеток. В качестве злокачественного партнера в опытах по соматической гибридизации клеточных линий используют клетки одной из наиболее распространенных мышиных миеломных линий Р3-X63-Ag 8.653.
К моменту гибридизации клетки миеломы должны находиться в экспоненциальной фазе роста. Это достигается последовательным выполнением следующих этапов: культивирование в среде с 8-азагуанином в течение 2 недель и в основной среде культивирования с 10% эмбриональной телячьей сывороткой в течение последующих 2 недель с регулярной сменой среды каждые 3 суток.
Гибридизация спленоцитов и клеток мышиной миеломы. Процедуру соматической гибридизации спленоцитов и клеток миеломы выполняют в присутствии полиэтиленгликоля (ПЭГ-4000) по следующей схеме:
- взвесь иммунных спленоцитов (1·108 клеток) и миеломных клеток (1·107) объединяют в центрифужном стаканчике с круглым дном, центрифугируют при 800-1000 об/мин в течение 10 мин, надосадочную среду декантируют.
- к осадку клеток медленно (в течение 2 мин) добавляют 1 мл 50% раствора ПЭГ. Затем вносят 1, 2, 4 и 8 мл бессывороточной среды, по 2 минуты каждое внесение. Во время добавления реактивов центрифужный стакан непрерывно вращают. После завершения данной манипуляции клеточную суспензию центрифугируют, надосадочную жидкость декантируют, осадок клеток ресуспендируют в 20 мл селективной НАТ-среды с 15% эмбриональной телячьей сывороткой. Суспензию вносят в лунки двух 96-луночных пластин с предварительно подготовленным слоем фидерных клеток. Сроки выращивания клеток в НАТ-среде - 2 недели, в НТ-среде - 1 неделя. Смену среды производят каждые 3-4 дня.
Все этапы последующего культивирования гибридных клеток, отбор растущих клонов, секретирующих специфические иммуноглобулины, клонирование, тиражирование культур и накопление МКА in vivo выполняют согласно общепринятому протоколу [11].
Тестирование образцов проб культуральной среды на наличие в них специфических иммуноглобулинов, отобранных из тех лунок, в которых обнаружены растущие клоны, выполняют с помощью непрямого варианта ТИФМ: АГ + исследуемая проба + антивидовой иммунопероксидазный конъюгат против иммуноглобулинов мыши. Скрининг антителопродуцирующих гибридных клонов выполняют не ранее 7-10 суток после рассева в 96-луночные пластины. Из лунок пластины до смены среды отбирают не более 50 мкл для исследования в непрямом варианте ТИФМ. Положительные результаты этого метода скрининга, полученные с пробой из одной и той же лунки не менее трех раз, являются основанием для отбора первичного клона-продуцента целевого продукта. Все первичные клоны, отобранные в течение месяца, клонируют и реклонируют методом лимитирующих разведений.
После второго клонирования каждого из первичных вариантов клонов формируют рабочую коллекцию гибридом-продуцентов МКА заданной специфичности. Среди продуктивных клонов, секретирующих моноклональные иммуноглобулины против антигена 200 kDa В. pseudomallei, селекционирован клон-продуцент МКА 6А11/G12.
Пример 2. Накопление МКА в препаративных количествах.
При необходимости накопления МКА в препаративных количествах ампулу с клетками соответствующей гибридомы достают из биохранилища с жидким азотом, размораживают содержимое в течение 2-3 минут на водяной бане при 37°C и проверяют жизнеспособность клеток [16]. Затем для отмывания восстановленной суспензии клеток от примесей защитной среды ее переносят в центрифужную пробирку с бессывороточной средой (8-10 мл), осторожно наслаивая ее на поверхность жидкости. Клетки осаждают центрифугированием при 800-1000 об/мин, удаляют надосадок, а осевшие клетки вновь ресуспендируют в полной среде для выращивания гибридом.
Клетки, выведенные из криоконсервированного состояния, переносят в лунки 96-луночной пластины с подготовленным накануне слоем фидера. Условия культивирования in vitro аналогичны описанным выше. По мере роста популяции производят рассев клеток в пластины с лунками большего объема (48-, 24-, 12-, 6-луночные). При последовательном выполнении этих условий продукция МКА 6A11/G12 восстанавливается до уровня 0,30-0,31 мкг/мл. Из собранных образцов среды культивирования клеток с подтвержденной функцией антителопродукции выделяют моноклональные иммуноглобулины.
Тиражирование клеток гибридомы in vivo в брюшной полости сингенного животного - наиболее эффективный способ накопления высоких концентраций МКА. Животным предварительно внутрибрюшинно вводят по 0,4 мл стерильного минерального масла, пристана - 2, 6, 10, 14-тетраметил-пентадекана или неполного адъюванта Фрейнда. Через 5-7 суток мышам внутрибрюшинно вводят по 2·106-4·106 клеток гибридомы. После накопления асцитической жидкости ее собирают. Клетки осаждают центрифугированием, надосадочную жидкость отделяют и используют для выделения антител методом сульфатного трехкратного переосаждения белка при 50% насыщении сульфата аммония. Рыхлый осадок центрифугируют при 12000 об/мин в течение 20 минут, надосадочную жидкость удаляют. Осадок растворяют в 0,01 M фосфатном буфере, диализуют до полного удаления ионов сульфата аммония. Полученный раствор моноклональных иммуноглобулинов стерилизуют методом мембранной фильтрации, ампулируют и хранят при минус 20°C до момента использования. Концентрацию белка в растворе МКА определяют спектрофотометрически при длине волны 280 нм.
Пример 3. Контроль антителопродукции клеток гибридомы-продуцента МКА 6A11/G12.
Антителопродукцию гибридомы контролируют на этапах накопления МКА как in vitro, так и in vivo.
Специфическую активность МКА определяют с помощью ТИФМ по общепринятой методике [17]. В лунки полистироловой пластины для иммуноферментного анализа вносят по 100 мкл раствора антигена 200 kDa В. pseudomallei (с концентрацией 10 мкг/мл по белку) в 0,05 Μ карбонатно-бикарбонатном буфере, pH 9,5. Пластину для иммуноферментного анализа в течение ночи выдерживают при 4-8°C, затем трижды отмывают фосфатным буферным раствором с 0,05% твина-20 (ФБР-Т) и блокируют свободные участки пластика 1% раствором бычьего сывороточного альбумина, внося на 30 минут в каждую лунку по 100 мкл этого раствора. Пластину вновь трижды отмывают. Затем на 1 ч при 37°C вносят в лунки пластины по 100 мкл различных разведений МКА, приготовленных на 0,1 M фосфатном буфере, pH 7,4, с 0,05% твина-20, с последующей трехкратной отмывкой и внесением антивидового конъюгата в рабочем разведении по 100 мкл. Конъюгат является коммерческим препаратом антител диагностических против IgG (H+L) белой мыши, меченных пероксидазой. Пластину инкубируют при 37°C в течение 1 ч, трижды отмывают. В завершение реакции на 15 мин в лунки вносят по 100 мкл смеси перекиси водорода с хромогеном. Пластину помещают в защищенное от света место. Реакцию останавливают стоп-реагентом. Результаты реакции регистрируют на планшетном фотометре при длине волны, соответствующей характеристике применяемого хромогена. МКА 6A11/G12, выделяемые из среды выращивания клеток и из асцитической жидкости, активны в разведениях 5·10-2 и 5·10-4 соответственно. Для изготовления диагностического препарата иммуноглобулинов флуоресцирующих предпочтительнее использовать МКА, накопленные in vivo.
Пример 4. Определение диагностических возможностей МКА 6A11/G12 в методе флуоресцирующих антител.
При использовании МКА в качестве сырья для изготовления диагностического препарата для МФА их метят флуорохромом - флуоресцеинизо-тиоцианатом (ФИТЦ) [18]. Процедуру конъюгирования МКА с флуорохромом выполняют с соблюдением следующих условий: метку выполняют при комнатной температуре и постоянном перемешивании реагентов. Нагрузка ФИТЦ не должна превышать 25 мг на 1 г иммуноглобулинов. Внесение раствора флуорохрома дробное в течение первых 30 минут. Суммарное время конъюгирования - 2,5 ч. Все перечисленные этапы выполняют при постоянном контроле pH раствора, не допуская превышения этого показателя более 9,0. Последующую очистку конъюгата от немеченого белка и несвязавшегося красителя проводят на колонке с сефадексом G-25, используя для элюирования 0,1 M фосфатный буфер, pH 7,2. При расчете показателей концентрации белка и молярного соотношения МФИТЦ/Мбелок используют методику The Т.Н. и Feltkamp Т.Е. [18]. Для определения рабочего разведения конъюгата МКА-ФИТЦ используют обеззараженные мазки-препараты, приготовленные из взвеси В. pseudomallei 100 с концентрацией 5·108 м.к./мл. После этого готовый препарат ампулируют, лиофилизируют или хранят при минус 20°С.
Целевое назначение препарата - обнаружение патогенных буркхольдерий в пробах с объектов внешней среды и биологического материала методом МФА.
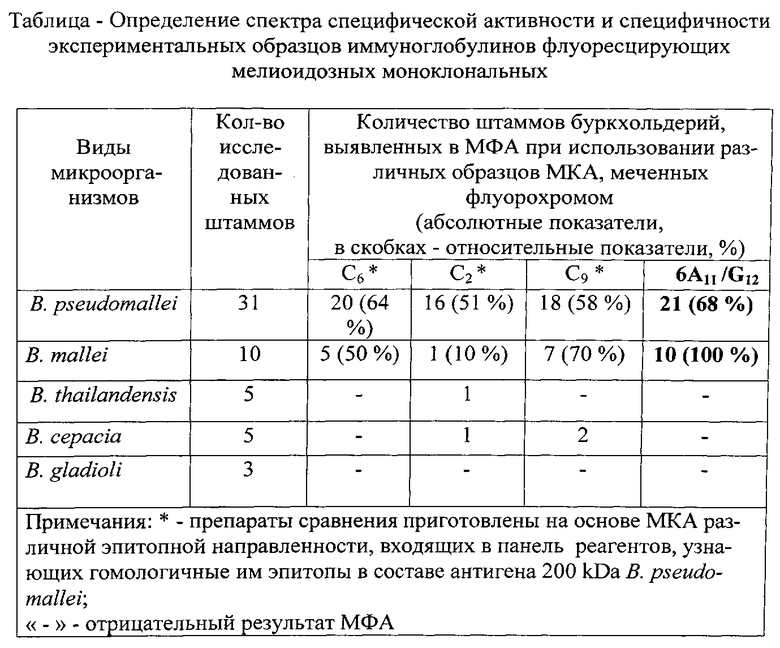
Диагностические возможности экспериментального препарата иммуноглобулинов флуоресцирующих моноклональных, приготовленного на основе иммуноглобулинов 6A11/G12, были проверены в МФА с использованием фиксированных и обеззараженных мазков-препаратов чистых культур коллекционных штаммов буркхольдерий II группы патогенности (В. pseudomallei - 31 штамм, В. mallei - 10 штаммов) и условно-патогенных буркхольдерий III-IV группы патогенности (В. thailandensis - 5 штаммов, В. cepacia - 5 штаммов, В. gladioli - 3 штамма) (таблица). В качестве препаратов сравнения применяли образцы экспериментальных конъюгатов, приготовленных на основе МКА, против различных эпитопов антигена 200 kDa В. pseudomallei. Эти варианты МКА входят в состав реагентов для работы с буркхольдериями. Как свидетельствуют данные таблицы, иммуноглобулины диагностические флуоресцирующие моноклональные 6A11/G12 имеют существенные преимущества по сравнению с препаратами «С6, С2, С9» в части показателей спектра специфической активности в отношении патогенных буркхольдерий: этот препарат в МФА специфически окрашивает м.к. коллекционных штаммов возбудителей мелиоидоза и сапа, 68% и 100% соответственно. Но, что особенно ценно, он не взаимодействует с м.к. близкородственных буркхольдерий III-IV группы патогенности (В. thailandensis, В. cepacia, В. gladioli).
Таким образом, перечисленные выше свойства гибридомы-продуцента МКА 6А11/G12 позволили сделать следующее заключение. Штамм культивируемых гибридных клеток животного Mus muscuius L. (авторское название клеточной линии Bpm Vd-11) предназначен для получения моноклонального антитела 6А11/G12 против эпитопа в составе антигена 200 kDa, экспонированного на поверхности микробных клеток патогенных буркхольдерий (В. pseudomallei и В. mallei), пригодного для применения в качестве основы для получения высокоспецифичного диагностического препарата для МФА, не обладающего перекрестной активностью в отношении близкородственных условно-патогенных буркхольдерий.
Список использованных источников
1. Специфическая индикация патогенных биологических агентов: Практическое руководство / Под ред. Г.Г. Онищенко. - М., 2006. - 288 с.
2. Лабораторная диагностика опасных инфекционных болезней: Практическое руководство / Под редакцией академика РАМН Г.Г. Онищенко, академика РАМН В.В. Кутырева. Изд. 2-е, переработанное и дополненное. - М.: ЗАО «Шико», 2013. - 560 с.
3. Лабораторная диагностика мелиоидоза (МУ 4.2.2787-10.4.2) / Демина Ю.В., Пакскина Н.Д., Илюхин В.И., Алексеев В.В., Храпова Н.П. и др. // Изданы ФЦГиЭ. - 2011. - 160 с.
4. Лабораторная диагностика сапа (МУ 4.2.2831-11.4.2) / Демина Ю.В., Пакскина Н.Д., Илюхин В.И., Алексеев В.В., Храпова Н.П. и др. // Изданы ФЦГиЭ. - 2011. - 140 с.
5. Перспективы совершенствования иммуноглобулиновых препаратов для обнаружения и идентификации возбудителей сапа и мелиоидоза / Храпова Н.П., Тихонов Н.Г., Прохватилова Е.В., Кулаков М.Я. // Мед. паразитология и паразитарные болезни. - 1995. - №4. - С. 49-53.
6. О разработке новых иммунобиологических препаратов на основе моноклональных антител к Burkholderia mallei и Burkholderia pseudomallei / Прохватилова E.B., Храпова Н.П., Алексеев В.В., Кулаков М.Я. // Проблемы особо опасных инфекций. - Саратов, 2003. - Вып. 86. - С. 153-158.
7. Anuntagool N., Panichakul Т., Aramsri P., Sirsinha S. Shedding of lipo-polysaccharide and 200-kDa surface antigen during the in vitro growth of virulent Ara- and avirulent Ara+ Burkholderia pseudomallei // Acta Tropica. - 2000. - V. 74. - P. 221-228.
8. Short report: a rapid method for the differentiation of Burkholderia pseudomallei and Burkholderia thailandensis / Wuithiekanun V., Anuntagool N., White N.J. et al. // Am. J. Med. Hyg. - 2002. - V. 66, №6. - P. 759-761.
9. Antigenic differences between clinical and environmental isolates of Burkholderia pseudomallei / Sirisinha S., Anuntagool N., Intachote P. et al. // Microbiol. Immunol. - 1998. - V. 42, №11. - P. 731-737.
10. Храпова Н.П., Пивень H.H., Корсакова И.И. и др. Перспективы создания диагностических средств индикации и идентификации вирулентных штаммов возбудителя мелиоидоза // Матер. науч. - практич. конф. «Соврем. аспекты эпидемиологического надзора за особо опасными инфекционными заболеваниями на юге России» (21-22.03.07). - Ставрополь, 2007. - Ч. 2. - С. 155-156.
11. Goding, J.W. Monoclonal antibodies: principles and practice // Acad. Press. - 1986, 315 p.
12. Храпова Н.П., Алексеев B.B., Прохватилова E.B., Липницкий А.В. Некоторые итоги и перспективы производства моноклональных диагностических средств обнаружения возбудителей опасных инфекционных заболеваний // Сб. науч. трудов, посвящ. 75-летию НИИ микробиологии МО РФ. - Киров, 2003. - С. 176-177.
13. Пивень H.Н. Выделение, очистка и химический состав поверхностного полисахаридного антигенного комплекса возбудителя мелиоидоза / Н.Н. Пивень, В.И. Смирнова // Особо опасные инфекционные заболевания: диагностика, профилактика и биологические свойства возбудителей. Вып. 4 / Волгоградский научно-исследовательский противочумный институт, 1990. - С. 111-117.
14. Пивень Н.Н., Илюхин В.И. Патогенность Burkholderia pseudomallei как функция его внеклеточных и поверхностных антигенов // Журн. микробиол., эпидемиол. и иммунобиол. - 2000. - №6. - С. 94-99.
15. Способ определения предельно допустимой антигенной нагрузки, стимулирующей продукцию гуморальных антител / Храпова Н.П., Корсакова И.И., Ломова Л.В. и др. // Патент РФ на изобретение №2371196 от 27.10.2009/.
16. Фрешни Р.Я. Культура животных клеток: практическое руководство / Р.Я. Фрешни; пер. 5-го англ. изд. - М.: БИНОМ. Лаборатория знаний, 2011. - 691 с.
17. Антитела. Методы. Пер. с англ. / Под ред. Д. Кэтти. - М.: Мир, 1991. - 384 с., ил.
18. The Т.Н., Feltkamp T.E.W. Conjugation of fluorescein isothiocyanate to antibodies. I. Experiments on the conditions of conjugation // Immunology. - 1970. - V. 18. - P. 865-873.
Изобретение относится к области биохимии, в частности к получению гибридом-продуцентов моноклональных антител заданной специфичности. Заявлен штамм культивируемых гибридных клеток животного Mus musculus-продуцент моноклональных антител к эпитопу в составе антигена 200 kDa, экспонированного на поверхности микробных клеток патогенных буркхольдерий В. pseudomallei и В. mallei. Штамм депонирован в Государственную коллекцию патогенных микроорганизмов и клеточных культур «ГКПМ-Оболенск» под номером Н-41. Изобретение позволяет получить высокоспецифичные моноклональные антитела, пригодные для изготовления на их основе диагностического препарата для МФА, способного обнаруживать в различных пробах только патогенные буркхольдерии, но не взаимодействовать с непатогенными видами буркхольдерий. 1 табл., 4 пр.
Штамм культивируемых гибридных клеток животного Mus musculus L. Bpm Vd-11, депонированный в Государственную коллекцию патогенных микроорганизмов и клеточных культур «ГКПМ-Оболенск» под номером Н-41, является продуцентом моноклонального антитела 6A11/G12 к эпитопу в составе антигена 200 kDa, экспонированного на поверхности микробных клеток двух патогенных буркхольдерий (В. pseudomallei и В. mallei), пригодного для изготовления на его основе диагностического препарата для МФА, предназначенного для обнаружения патогенных буркхольдерий в различных пробах с объектов внешней среды и клинического материала.
| Штамм гибридных культивируемых клеток MUS мUSсULUS L - продуцент моноклональных антител к поверхностному антигену типичных штаммов возбудителя сапа РSеUDомоNаS маLLеI | 1991 |
|
SU1791451A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПРЕДЕЛЬНО ДОПУСТИМОЙ АНТИГЕННОЙ НАГРУЗКИ, СТИМУЛИРУЮЩЕЙ ПРОДУКЦИЮ ГУМОРАЛЬНЫХ АНТИТЕЛ | 2008 |
|
RU2371196C1 |
| ХРАПОВА Н.П | |||
| и др., Применение сапных и мелиоидозных моноклональных антител различной эпитопной направленности для обнаружения и идентификации патогенных буркхольдерий, Проблемы особо опасных инфекций, 2011, вып | |||
| Счетный сектор | 1919 |
|
SU107A1 |
| АНТОНОВ В.А | |||
| и др., Современные подходы к диагностике сапа и | |||
Авторы
Даты
2015-12-10—Публикация
2014-10-13—Подача