Изобретение относится к гибридомной технологии и касается получения моноклональных антител. Штамм назван MVd-4 (2A6). Штамм депонирован в специализированной коллекции перевиваемых соматических клеток позвоночных Всероссийской коллекции клеточных культур под номером BCKK(П) 649Д.
Применение моноклональных антител в качестве основы для конструирования иммуноферментных тест-систем открывает новые перспективы усовершенствования ТИФМ во всех его вариантах.
Для обнаружения возбудителей сапа и медиоидоза и их антигенов в различных объектах исследования на основе иммуноглобулинов гипериммунных сывороток разработана тест-система для ТИФМ (Яковлев А.Т., Рыбкин В.С., Ахмедов А. Н. Усовершенствование технологии возбудителей сапа и мелиоидоза. - Особо опасные инф. заболевания: иммунология, генетика и биология. Сб. науч. работ. - Волгоград, 1989, с. 111 - 115). Однако опыт работы различных авторских коллективов свидетельствует о том, что в числе иммунодиагностических средств, представленных для выбора исследователя, должны быть препараты к общим и видеоспецифическим антигенам (антигенным маркерам) возбудителей сапа и мелиоидоза.
Для обнаружения экзотоксина Pseudomonas pseudomallei была разработана и испытана иммуноферментная тест-система с применением МКА (Ismail G., Embi M. N. , Omar O. A competitive immunosorbent assay for detection of Pseudomonas pseudomallei extoxin. - J.Med. Microbiol, 1987, Vol. 23, N 4, p. 353 - 357). МКА проявили себя как высокоспецифичные реагенты в ТИФМ для выявления экзотоксина P. pseudomallei в предельно низких концентрациях в крови больных людей. Предложенная тест-система для ТИФМ с МКА обладала высокой чувствительностью (16 нг/мл) и была рекомендована в качестве надежного теста ранней диагностики мелиоидоза.
Цель изобретения - получение штамма гибридомы-продуцента специфических гомогенных по составу и свойствам моноклональных антител (МКА), взаимодействующих с термостабильным компонентом капсулоподобной субстанции возбудителя мелиоидоза - основы для конструирования иммуноферментной тест-системы.
Получение гибридомы достигается иммунизацией мышей BALВ/c цельными клетками Pseudomonas pseudomallei с последующей гибридизацией лимфоцитов селезенки иммунизированных мышей с миеломными клетками мыши. Концентрация иммуноглобулинов (IgG3) в среде составляет в среднем 0,46 - 0,62 мг/мл, активность иммуноглобулинов в культуральной среде в ТИФА 1 : 640, в асцитической жидкости 1 : 1 • 107. Стабильность продуцирования сохраняется на протяжении 20 пассажей в культуре. Антитела взаимодействуют с эпитопами, локализованными на участке антигенного комплекса 8 (гликопротеин с м.м. 800 кД) - одного из основных факторов патогенности возбудителя мелиоидоза, экспонированного внеклеточно в капсулоподобной субстанции, окружающей клетку мелиоидозной бактерии (Пивень Н. Н., Смирнова В.И., Викторов Д.В. Иммуногенность и гетерогенность поверхностного антигена 8 P. pseudomallei. - Журн. микробиологии, эпидемиологии и иммунобиологии, 1996, N4, с. 75 - 78).
Гибридома получена слиянием миеломы мышей P3-X63-Ag 8.653 и спленоцитов мыши линии BALB/c. Слияние проведено с помощью полиэтиленкликоля с последующим клонированием штамма-продуцента методом лимитирующих разведений. Полученный штамм назван MVd-4(2A6) и характеризуется следующими признаками.
Культуральные признаки. Культивирование in vitro. Среда для культивирования - среда RPMI-1640 с добавлением 15% эмбриональной телячьей сыворотки, 2 мМ L-глютамина, 10 мМ ГЭПЭС, 4 мМ пирувата натрия.
Клетки культивируют при 37oC в атмосфере 5% CO2 и 70 - 80% влажности. Клетки пассируют один раз в 3 - 4 дня, контролируя микроскопически интенсивность роста. Кратность рассева 1 : 4 - 1 : 10. Культура суспензионная.
Культивирование в организме животного. Для накопления асцита клетки гибридомы вводят праймированным мышам линии BALB/c в дозе 1 • 105 - 1 • 106 клеток на мышь. Асцит образуется через 2 - 4 недели.
Продуктивность штамма. Продукция МКА в среде культивирования составляет 0,46 - 0,62 мг/мл, в асцитической жидкости 35 - 40 мг/мл. Продукция МКА в культуральной жидкости сохраняется на протяжении 20 пассажей.
Характеристика получаемого продукта. Антитела относятся к классу IgG3. Они специфически взаимодействуют с определенным эпитопом термостабильного антигена возбудителя мелиодоза. Специфичность взаимодействия определяют с помощью ТИФМ.
Криоконсервирование. 2 - 4 • 106 клеток штамма консервируют в 1 мл среды RPMI-1640 с 20% эмбриональной телячьей сыворотки и 7% диметилсульфоксида в пластиковых ампулах. Замораживание производят при 4oC (30 мин), а затем помещают в комплекс криоконсервирования биоматериалов, предназначенный для контролируемого замораживания клеточных культур тканей в заданном режиме: до температуры -20oC со скоростью 1oC/мин, до -40oC со скоростью 1,5 град/мин, до -70oC со скоростью 5 град/мин. Затем ампулы погружают в жидкий азот и хранят в нем до момента использования. Размораживание производят быстро при -37oC на водяной бане. Жизнеспособность после размораживания составляет 70 - 75%.
Пример 1. Штамм получают следующим образом. Мышей линии BALB/c иммунизируют ультразвуковыми дезинтегратами клеток P. pseudomallei C-141. Первые две инъекции с интервалом в одну неделю производят подкожно в дозе 5 • 108 м.к. с неполным адъювантом Фрейнда в объеме 0,3 мл и внутрибрюшинно в дозе 1 •109 м. к. в объеме 0,5 мл физиологического раствора. Бустирующее введение антигена производят на 21 - 22-й день после начала иммунизации внутриселезеночно в дозе клеток 5 • 108 м.к. в 0,1 мл физиологического раствора. Через 3 дня после этого 1 • 108 спленоцитов иммунных мышей гибридизируют с 1 • 107 клеток мышиной миеломы P3-X63-Ag8.653 в присутствии 1 мл 50%-ного полиэтиленгликоля с мол.м. 4000 в течение 2 мин. Затем к этой смеси при постоянном перемешивании последовательно вносят 1, 2, 4 и 8 мл бессывороточной среды, каждую порцию в течение 2 мин. После этого клетки центрифугируют при 1000 об/мин в течение 10 мин. Осадок ресуспендируют в селективной среде ГАТ-среде с 15%-ной эмбриональной телячьей сывороткой, 2 мМ L-глютамина, 4 мМ пирувата натрия. Клетки высевают в 96-луночную пластину с фидером по 2,5 - 5 • 105 клеток в лунку. Смену среды производят через 3 - 4 дня. Отбор гидридом-продуцентом в лунках опытной пластины определяют по наличию специфических иммуноглобулинов в культуральной среде с помощью ТИФМ. Выявленные гибридомы-продуценты клонируют не менее двух раз методом предельных разведений на среде RPMI-1640 с 15% эмбриональной телячьей сыворотки с добавками в 96-луночных плато с фидером-мышиными перитонеальными макрофагами (4 • 104 клеток в лунке). После второго клонирования практически все 100% субклонов продуцируют МКА.
Среди продуктивных клонов, секретирующих МКА против антигенных детерминант возбудителей сапа и мелиоидоза, селекционирован клон-продуцент MVd-4(2A6).
Пример 2. Накопление МКА. Ампулы с клетками гибридомы вынимают из сосуда с жидким азотом и быстро оттаивают на водяной бане при 37oC. Размороженные клетки переносят к центрифужную пробирку с 20 мл бессывороточной среды RPMI-1640 осторожно наслаивают взвесь клеток на среду. Клетки осаждают центрифугированием и после удаления отмывающей среды высевают на матрас 25 см2 на среду RPMI-1640 с 15% эмбриональной телячьей сыворотки. Матрас инкубируют во влажной атмосфере с 5% CO2 при 37oC. Когда колония клеток покрывает более трети дна матраса, осуществляют отбор проб культуральной среды с целью определения титра МКА с помощью ТИФА. При полном покрытии дна матраса гибридными клетками производят их рассев на несколько матрасов. Таким способом тиражируют клетки гибридомы in vitro.
Для получения более концентрированного препарата антител гибридомы-продуценты накапливают в асцитической жидкости мышей BALB/c. Животных предварительно сенсибилизируют внутрибрюшинным введением пристана - 2, 6, 10, 14-тетраметилпентадекана (0,3 мл на мышь) или неполного адъюванта Фрейнда (0,5 мл на мышь). Через неделю мышам внутрибрюшинно вводят по 1 • 105 - 1 • 106 клеток гибридомы. После появления у мышей асцитической жидкости и солидных опухолей собирают содержимое брюшной полости. Клетки осаждают центрифугированием, к надосадочной жидкости добавляют сульфат аммония до 50% его насыщения. Рыхлый осадок центрифугируют при 10000 об/мин в течение 20 мин, надосадочную жидкость удаляют. Плотный осадок растворяют в физиологическом растворе до исходного объема, диализуют против этого же раствора в течение суток при 4oC до полного удаления сульфата аммония. Осаждение МКА сульфатом аммония до 50%-ного его насыщения повторяют трижды как описано выше. В полученном растворе очищенных МКА определяют концентрацию белка спектрофотометрически. В качестве стандартного используют 1%-ный раствор бычьего сывороточного альбумина.
Специфическую активность МКА определяют с помощью ТИФМ. При постановке ТИФА полистироловые пластины обрабатывают в течение ночи при 4oC водно-солевым экстрактом P. pseudomallei 56830 или P. mallei 10230, разведенным на 0,05 М карбонатно-бикарбонатном буфере, pH 9,5, до концентрации 1 - 10 мкг/мл по белку. Затем пластины трижды отмывают забуференным физраствором с 0,05% твина-20. На этом же растворе производят титрование образцов МКА в объеме 100 мкл, которые выдерживают в пластинах с течением 1 ч при 37oC. После очередного трехкратного отмывания пластин вносят антивидовой конъюгат в рабочем разведении, приготовленный на ЗФР с твином-20. Конъюгат представляет собой кроличьи антимышиные IgG, меченые пероксидазой хрена. Время инкубации 1 ч при 37oC, объем 100 мкл на лунку. Вновь повторяют отмывание. В заключение вносят смесь - перекись водорода с 5-аминосалициловой кислотой. После инкубации при комнатной температуре в течение 40 мин 1 ч измеряют оптическую плотность жидкости в каждой лунке при длине волны 405 нм. МКА, выделенные из асцитической жидкости в ТИФА, активны в разведении 1 : 1 • 105 - 1 • 107.
Средний объем асцитической жидкости, получаемый при культивировании гибридомы MVd-4(2A6) в организме животных, составляет 3,5 + 0,12 мл, продуцирующая активность in vivo 35 - 40 мг иммуноклональных иммуноглобулинов на 1 мл асцитической жидкости.
Пример 3. Конструирование тест-системы для ТИФМ с МКА MVd-4(2A6) для обнаружения антигена 8 P. pseudomallei в различных объектах исследования. Обнаружение антигена 8 в различных антигенных смесях, фракциях и клеточных взвесях P. mallei и P. pseudomallei осуществляли с помощью "сэндвич"-варианта ТИФМ с МКА. Иммунопероксидазный конъюгат на основе МКА MVd-4(2A6) получают по методу Mathisen с соавт. (Enzyme-linked immunosorbent assay for detection of hepatitis A antigen in sera: comparison with solid phasе radioimmunoassay, immune electron microscopy and immune adherence hemagglutination assay/ Mathiesen L.R., Feinstone S.M., Wong D.S. et al.// J. Clin. Microbiol, 1987, N7, p. 184 - 193). При этом 5 мг пероксидазы хрена растворяют в 1 мл 0,3 М NaHCO3 и добавляют 0,25 мл 0,32%-ного раствора формалина. Затем в раствор дробно добавляют 1 мл 0,04 М NaIO4, 1 мл 0,16 М этиленкликоля и диализуют против 0,01 М карбонатно-бикарбонатного буфера, pH 9,5 при 4oC в течение 18 ч. Конъюгирование иммуноглобулинов (5 мг/мл на 0,01 М карбонатно-бикарбонатном буфере, pH 9,5) с ферментом осуществляют в течение 2 ч при комнатной температуре. Затем в полученный раствор дробно добавляют 5 мг NaBH4 и проводят диализ против 0,01 М фосфатного буфера, pH 7,4 при 4oC в течение 18 ч. Очистку конъюгата проводят на колонках с Г-100 элюирующим 0,1 М фосфатным буфером, pH 7,4. Показатели оптической плотности фракций конъюгата определяют спектрофотометрически при длине волны 403 и 280 нм. Объединяют фракции с соотношением оптических плотностей (ОП403 : ОП280) 0,4 - 0,5. Концентрация белка в конъюгате колеблется от 0,2 - 0,3 мг/мл, RZ = 0,45 - 0,5, рабочее разведение 1 : 150 - 1 : 200. Активность конъюгата оценивают в ТИФМ с водно-солевым экстрактом P. pseudomallei 56830 методом шахматного титрования. Конъюгат используют в "сэндвич"-варианте ТИФМ для выявления антигена 8 P. pseudomallei.
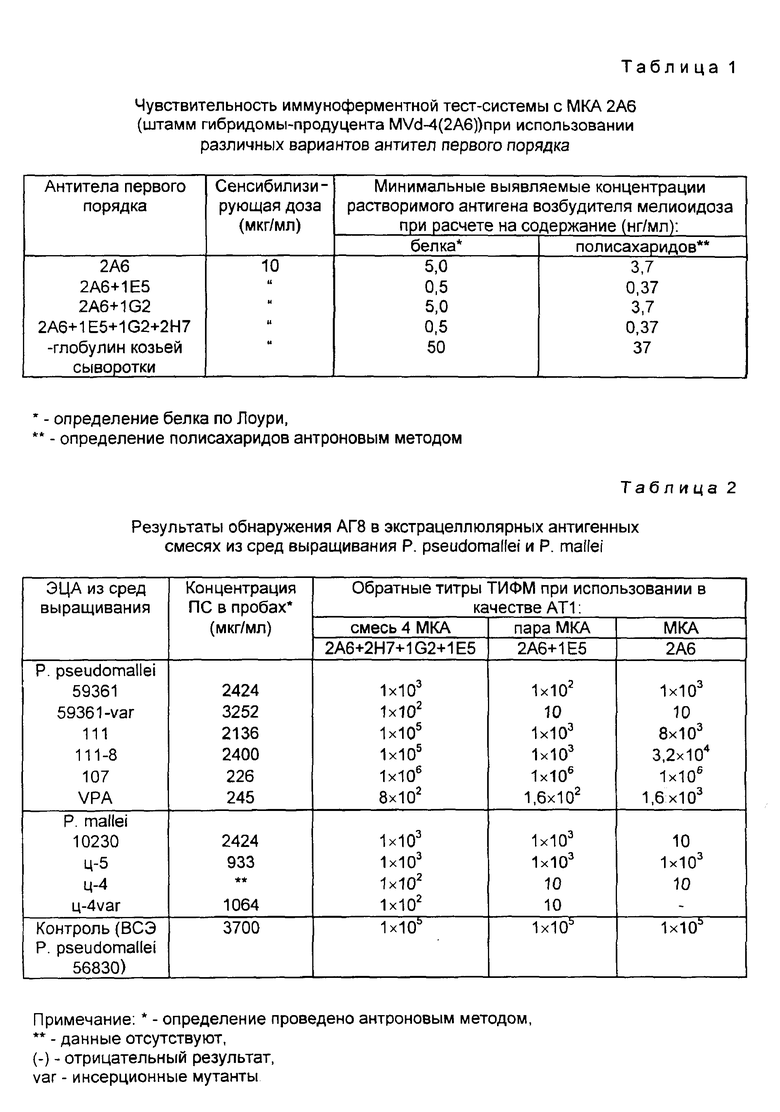
В качестве антител первого порядка для сенсибилизации пластин используют: 1) образцы МКА 2 A6, взаимодействующие с антигеном 8 (АГ8); 2) аддитивные смеси МКА 2 - 4 типов. МКА, разведенные на карбонатно-бикарбонатном буфере, pH 9,5, до концентрации 10 мкг/мл, наносят на пластину по 100 мкл, инкубируют при 4oC в течение 18 ч. Затем пластины трижды отмывают забуференным физраствором с 0,05% твина-20. Дополнительно лунки пластины обрабатывают 1%-ным раствором бычьего сывороточного альбумина (по 100 мкл). После 30 мин экспозиции лунки промывают забуференным физраствором с 0,05% твина-20. На этом же растворе производят титрование образцов исследуемого материала, содержащего антиген, в объеме 100 мкл, которые выдерживают в пластинах в течение 1 ч при 37oC. После очередного трехкратного отмывания пластин вносят иммунопероксидазный конъюгат в рабочем разведении, приготовленный на ЗФР с твином-20. Время инкубации 1 ч. при 37oC, объем 100 мкл на лунку. Вновь повторяют отмывание. В заключение вносят смесь - перекись водорода с 5-аминосалициловой кислотой. После инкубации при комнатной температуре в течение 40 - 60 мин измеряют оптическую плотность жидкости в каждой лунке при длине волны 405 нм. Чувствительность разработанной иммуноферментной тест-системы с МКА представлена в табл.1.
Высокая эффективность использования МКА по сравнению с традиционно применяемыми поликлональными иммуноглобулинами отражена в графе 5 по горизонтали (табл.1). При использовании в качестве "подложки" глобулинов, выделенных из гипериммуной мелиоидозной козьей сыворотки (аналог), чувствительность не превышала 50 нг/мл белка в 1 мл, т.е. была в 1 - 100 раз ниже.
Максимальная чувствительность ТИФМ отмечена в случаях применения пар МКА (2A6 + 2H7 или 2A6 + 1E5) для сенсибилизации пластин МКА с индексом аддитивности более 40%. Использование пары МКА или большего количества моноклональных ингредиентов, близких по специфической направленности, но взаимодействующих с различными эпитопами АГ8, повышало вероятность обнаружения антигена с тестируемых образцах экспериментального материала.
Применение смесей МКА при подготовке планшет к реакции обеспечивало обнаружение 0,37 - 3,7 нг/мл ПС и 0,5 - 5 нг/мл белка (2A6 + 1E5 и 2A6 + 1E5 + 1G2 + 2H7). Специфичность разработанной иммуноферментной тест-системы подтверждали отрицательные результаты ТИФМ при использовании в качестве антител первого порядка смеси МКА к эпитопам антигена 6 (белковолипополисахаридный комплекс, локализованный в клеточной стенке возбудителей сапа и мелиоидоза).
Таким образом, максимальная чувствительность метода в отношении АГ8 отмечена при использовании в качестве наслаиваемых на пластик антител первого порядка моноклональных ингредиентов: 1) смеси из четырех типов МКА; 2) пар МКА (2A6 + 1E5 и 2A6 + 1G2); 3) МКА 2A6.
Пример 4. Использование иммуноферментной тест-системы с МКА для обнаружения АГ8 в экстрацеллюлярных антигенных смесях из сред культивирования Pseudomonas pseudomallei и Pseudomonas mallei.
Антиген 8, один из факторов патогенности возбудителя мелиоидоза, выявлен также у ряда штаммов возбудителя сапа. Для изучения динамики накопления данного антигена и оценки его суммарного содержания в жидких питательных средах культивирования микроорганизмов может быть использована разработанная тест-система для ТИФМ с МКА.
Представленные в табл. 2 данные результатов исследований свидетельствуют об эффективности применения предлагаемой иммуноферментной тест-системы на основе МКА для обнаружения минимальных концентраций АГ8 в экстрацеллюлярных антигенных смесях из сред культивирования P. pseudomallei и P. mallei.
Данные табл. 2 свидетельствуют о том, что уровни содержания гликопротеина (АГС) в среде выращивания подвержены широким колебаниям и зависят от видовой и штаммовой принадлежности культивируемого в жидкой среде микроорганизма.
Кроме того, данная тест-система для ТИФМ с МКА может быть использована для выявления искомого антигена при исследовании фракций экстрацеллюлярных антигенов, полученные в процессе гель-хроматографии, в антигенных смесях и бактериальных взвесях P. pseudomallei и P. mallei.
Таким образом, на основе МКА 2А6 (штамм гибридной клеточной линии MVd-4(2A6)) к эпитопам АГ8 разработана высокочувствительная иммуноферментная тест-система, предназначенная для выявления 0,5 - 5,0 нг/мг белка (по Лоури), 0,37 - 3,7 нг/мл ПС (антроновым методом) данного антигена в экстрацеллюлярных антигенных смесях и средах культивирования P. pseudomallei и P. mallei.
Преимуществом использования мелиоидозных моноклональных антител MVd-4(2A6) в качестве основы для конструирования иммуноферментной тест-системы для обнаружения антигена 8, одного из основных факторов патогенности P. pseudomallei, является стабильность свойств моноклонального иммуноглобулинового сырья, при наличии клона-продуцента практически 100%-ная воспроизводимость результатов опытов, что выгодно отличает данную основу от поликлональных иммуноглобулинов при производстве диагностических средств.
Штамм предназначен для получения моноклонального антитела к термостабильному компоненту капсулоподобной субстанции возбудителя мелиоидоза. Антитела относятся к изотипу Ig G3. Концентрация иммуноглобулинов в культуральной среде составляет 0,46 - 0,62 мг/мл. Антитела взаимодействуют с эпитопами, локализованными на участке антигенного комплекса 8 (гликопротеин с м.м 800 кДа) - одного из основных факторов патогенности возбудителя мелиоидоза. Предложенный штамм позволяет создать тест-систему с использованием полученных антител, обладающую высоким уровнем чувствительности. 2 табл.
Штамм культивируемых гибридных клеток животного Mus musculus ВСКК(П) 649Д - продуцент моноклонального антитела к термостабильному компоненту капсулоподобной субстанции возбудителя мелиоидоза.
| Jsmail G, Embi M.N., Omar O | |||
| A competitive immunosorbent assay for detection of Pseudomonas pseudollei extoxin // J.Med | |||
| Microbiol | |||
| Кузнечная нефтяная печь с форсункой | 1917 |
|
SU1987A1 |
Авторы
Даты
1998-08-10—Публикация
1997-07-02—Подача