Настоящее изобретение относится к получению сложных эфиров баккатина-III и 10-дезацетил-баккатина-III общей формулы (I):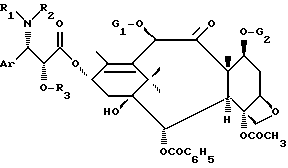
путем этерификации до сложного эфира соответствующим образом защищенного баккатина-III или 10-дезацетил-баккатина-III общей формулы (II):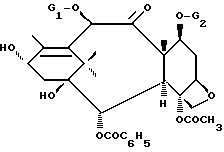
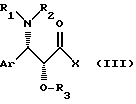
с помощью активированной кислоты общей формулы (III):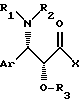
В общих формулах (I), (II) и (III) различные символы имеют следующие значения:
Ar обозначает арильный радикал;
или а) R1 обозначает ароильный радикал или радикал формулы R4-O-CO-, в которой R4 обозначает:
линейный или разветвленный алкильный радикал с 1-8 C-атомами; алкенильный радикал с 2-8 C-атомами; алкинильный радикал с 3-8 C-атомами; циклоалкильный радикал с 3-6 C-атомами или бициклоалкильный радикал с 7-10 C-атомами, причем эти радикалы в случае необходимости замещены одним или несколькими заместителями, выбираемыми в группе, включающей атомы галогена и гидроксильный радикал; алкилоксирадикал с 1-4 C-атомами; диалкиламино-радикал, каждая алкильная часть которого содержит 1-4 C-атома; пиперидино-, морфолинорадикал; пиперазин-1-ильный радикал (в случае необходимости замещенный в положении 4 алкильным радикалом с 1-4 C-атомами или фенилалкильным радикалом, алкильная часть которого содержит 1-4 C-атома); циклоалкильный радикал с 3-6 C-атомами; циклоалкенильный радикал с 4-6 C-атомами; фенильный радикал; циано-группу, карбокси-группу или алкилоксикарбонильный радикал, алкильная часть которого содержит 1-4 C-атомами;
или фенильный радикал, в случае необходимости замещенный одним или несколькими атомами или радикалами, выбираемыми среди атомов галогена и алкильных радикалов с 1-4 C-атомами или алкилокси-радикалов с 1-4 C-атомами;
или гетероциклический азотсодержащий радикал, насыщенный или ненасыщенный, 4-6-членный и в случае необходимости замещенный одним или несколькими алкильными радикалами с 1-4 C-атомами; имея в виду, что циклоалкильные, циклоалкенильные или бициклоалкильные радикалы в случае необходимости могут быть замещены одним или несколькими алкильными радикалами с 1-4 C-атомами;
R2 обозначает атом водорода и
R3 обозначает защитную для гидроксильной функции группу;
или еще б) R1 имеет вышеуказанное значение и, кроме того, может обозначать атом водорода, R2 и R3 вместе образуют насыщенный 5- или 6-членный гетероцикл;
G1 обозначает ацетильный радикал или защитную для гидроксильной функции группу;
G2 обозначает защитную для гидроксильной функции группу; и
X обозначает ацилокси- или ароилокси-радикал или атом галогена.
Преимущественно Ar и арильная часть ароильного радикала, обозначаемого R1, одинаковые или разные, обозначают фенильный радикал или в случае необходимости замещенный α- или β- нафтил, причем заместители можно выбирать в группе, включающей атомы галогена (фтор, хлор, бром, иод) и алкильные, алкенильные алкинильные, арильные, арилалкильные, алкоксильные, алкилтио-, арилокси-, арилтио-, гидроксильный, гидроксиалкильные, меркапто-, формильные, ацильные, ациламино-, ароиламино-, алкоксикарбониламино-, амино-, алкиламино-, диалкиламино-, карбоксильные, алкоксикарбонильные, карбамоильные, диалкилкарбамоильные, циано-, нитро- и трифторметильный радикалы, имея в виду, что алкильные радикалы и алкильные части других радикалов содержат 1-4 C-атомов, алкенильные и алкинильные радикалы содержат 3-8 атомов и арильные радикалы представляют собой фенильные или α- или β- нафтильные радикалы.
Преимущественно еще, Ar и арильная часть ароильного радикала, обозначаемого R1, одинаковые или разные, обозначают фенильный радикал, в случае необходимости замещенный атомом хлора или фтора или алкильным радикалом (метильным), алкилокси-радикалом (метокси), диалкиламино-радикалом (диметиламино), ациламино-радикалом (ацетиламино) или алкилоксикарбониламино-радикалом (трет.-бутоксикарбониламино).
Преимущественно, R3 обозначает защитную для гидроксильной функции группу, выбираемую среди метоксиметильного, 1-этокси-этильного, бензилоксиметильного, β- -триметилсилилэтоксиметильного, тетрагидропиранильного, 2,2,2,-трихлор-этоксиметильного, 2,2,2-трихлор-этоксикарбонильного радикалов или - CH2 -Ph -радикала, в котором Ph обозначает фенильный радикал, в случае необходимости замещенный одним или несколькими, одинаковыми или разными, атомами или радикалами, выбираемыми среди атомов галогена и алкильных радикалов с 1-4 C-атомами или алкилокси-радикалов с 1-4 C-атомами.
Преимущественно, когда R2 и R3 вместе образуют насыщенный 5- или 6-членный гетероцикл, то он обозначает оксазолидиновый цикл, замещенный в положении 2 одним или двумя заместителями, одинаковыми или разными, выбираемыми в группе, включающей атомы водорода и алкильные радикалы с 1-4 C-атомами; алкоксильные радикалы с 1-4 C-атомами; аралкильные радикалы, алкильная часть которых содержит 1-4 C-атома; или арильные радикалы, причем арильные радикалы предпочтительно представляют собой фенильные радикалы, в случае необходимости замещенные одним или несколькими алкилокси-радикалами с 1-4 C-атомами, и 2 заместителя в положении 2 вместе с атомом углерода, с которым они связаны, могут образовывать 4-7-членный цикл; или еще оксазолидиновый цикл, замещенный в положении 2 тригалогенметильным радикалом или фенильным радикалом, замещенным тригалогенметильным радикалом, причем символ R1 может обозначать, кроме того, атом водорода.
Преимущественно, G1 обозначает ацетильный радикал или защитную группу, выбираемую среди 2,2,2,-трихлор-этоксикарбонильного или 2-(2-трихлорметил-пропокси)-карбонильного радикалов.
Преимущественно, G2 обозначает защитную для гидроксильной функции группу, выбираемую среди 2,2,2-трихлор-этоксикарбонильного или 2-(2-трихлорметил-пропокси)-карбонильного радикалов или триалкилсилильного, диалкиларилсилильного, алкилдиарилсилильного или триарилсилильного радикалов, где каждая алкильная часть содержит 1-4 C-атома, а каждая арильная часть предпочтительно обозначает фенильный радикал.
Преимущественно, X обозначает ацилокси-радикал с 1-5 C-атомами в линейной или разветвленной цепи или ароилокси-радикал, в котором арильная часть обозначает фенильный радикал, в случае необходимости замещенный 1-5, одинаковыми или разными, заместителями, выбираемыми среди атомов галогена и нитро-, метильного или метокси-радикалов, или еще X обозначает атом галогена, выбираемого среди хлора или брома.
Преимущественно еще, X обозначает трет.-бутилкарбонилокси- или 2,4,6-трихлор-бензоилокси-радикал или атом хлора.
Известно получение сложных эфиров общей формулы (I), работая в условиях, описанных, например, в европейских патентных заявках 0336840 и 0336841 или в международной заявке ВОИС 92/09589. Согласно известным способам, этерификацию до сложного эфира защищенного баккатина-III или 10-дезацетил-баккатина-III с помощью кислоты общей формулы (IV):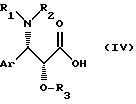
в которой
Ar, R1, R2 и R3 имеют вышеуказанное значение, осуществляют в присутствии имида, такого, как дициклогексилкарбодиимид, и диалкиламинопиридина, при температуре 60-90oC.
Осуществление этих способов требует применения значительного избытка кислоты общей формулы (IV) по отношению к производному баккатина.
Более того, применение агента конденсации, такого, как дициклогексилкарбодиимид, в промышленном масштабе может вызывать некоторое число проблем, которые важно по возможности ограничить или уменьшить. В самом деле, дициклогексилкарбодиимид представляет собой дорогостоящий реагент, который вследствие своих вызывающих аллергию свойств, требует особых условий осуществления и который, в процессе его использования, приводит к образованию дициклогексилмочевины, полное удаление которой часто затруднительно.
В настоящее время найдено, и это составляет предмет настоящего изобретения, что сложные эфиры общей формулы (I) могут быть получены путем этерификации до сложного эфира соответствующим образом защищенного баккатина-III или 10-дезацетил-баккатина-III с помощью активированного производного общей формулы (III) в условиях, которые позволяют избежать вышеуказанных недостатков.
Согласно изобретению, активированное производное общей формулы (III), в случае необходимости полученное in situ, конденсируют с баккатином-III или 10-дезацетил-баккатином-III в присутствии основания, предпочтительно азотсодержащего органического основания, работая в инертном органическом растворителе при температуре 0-90oC.
В качестве органических азотсодержащих оснований, которые особенно хорошо пригодны, можно назвать третичные алифатические амины, такие, как триэтиламин, пиридин, или аминопиридины, такие, как 4-диметиламино-пиридин или 4-пирролидино-пиридин.
В качестве инертных органических растворителей можно назвать простые эфиры, такие, как тетрагидрофуран, диизопропиловый эфир, метил-трет.-бутиловый эфир или диоксан; кетоны, такие, как метилизобутилкетон; сложные эфиры, такие, как этилацетат, изопропилацетат или н-бутилацетат; нитрилы, такие, как ацетонитрил, алифатические углеводороды, такие, как пентан, гексан или гептан; алифатические галогенированные углеводороды, такие, как дихлорметан или 1,2-дихлор-этан; и ароматические углеводороды, такие, как бензол, толуол или ксилолы, этилбензол, изопропилбензол или хлорбензол. Особый интерес представляют ароматические углеводороды.
Обычно активированное производное общей формулы (III) используют в стехиометрическом количестве по отношению к продукту формулы (II), но может быть предпочтительным использование вплоть до 3-х эквивалентов продукта формулы (III) по отношению к продукту формулы (II).
Обычно используют по крайней мере 1 эквивалент органического азотсодержащего основания по отношению к применяемому продукту общей формулы (II) или по отношению к производному общей формулы (III).
Предпочтительно, этерификацию до сложного эфира реализуют при температуре около 20oC.
Активированные производные общей формулы (III) могут быть получены в случае необходимости in situ, путем воздействия галоидангидрида кислоты общей формулы (V):
R5-CO-Y,
в которой
Y обозначает атом галогена, предпочтительно атом хлора, и R5 обозначает алкильный радикал с 1-5 C-атомами в линейной или разветвленной цепи или арильные радикал, представляющий собой предпочтительно фенильный радикал, в случае необходимости замещенный 1-5 одинаковыми или разными заместителями, выбираемыми среди атомов галогена и нитро-, метильного или метокси-радикалов; или тионилгалогенида, предпочтительно тионилхлорида, на кислоту общей формулы (IV).
Обычно реакцию осуществляют в инертном органическом растворителе, в присутствии органического азотсодержащего основания, при температуре 0-30oC.
В качестве органических растворителей могут быть использованы простые эфиры, такие, как тетрагидрофуран, диизопропиловый эфир, метил-трет.-бутиловый эфир или диоксан; кетоны, такие как метилизобутилкетон; сложные эфиры, такие, как этилацетат, изопропилацетат или н-бутилацетат; нитрилы, такие, как ацетонитрил; алифатические углеводороды, такие как пентан, гексан или гептан; алифатические галогенированные углеводороды, такие, как дихлорметан или 1,2-дихлорэтан; и ароматические углеводороды, такие, как бензол, толуол, ксилолы, этилбензол, изопропилбензол или хлорбензол.
В качестве азотсодержащих органических оснований можно назвать третичные алифатические амины, такие, как триэтиламин, пиридин; или аминопиридины, как 4-диметиламино-пиридин или 4-пирролидино-пиридин.
Обычно используют по крайней мере один эквивалент продукта общей формулы (V) или тионилгалогенида по отношению к кислоте общей формулы (IV).
Сложные эфиры общей формулы (I) особенно пригодны для получения производных таксана общей формулы (VI):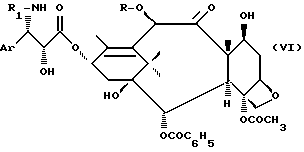
в которой
Ar и R1 имеют вышеуказанное значение, которые обладают замечательными антилейкемическими и противоопухолевыми свойствами.
Особый интерес представляют продукты общей формулы (VI), в которой Ar имеет вышеуказанное значение, R обозначает атом водорода или ацетильный радикал и R1 обозначает бензоильный или трет.-бутоксикарбонильный радикал.
Продукт общей формулы (VI), в которой R обозначает ацетильный радикал, R1 обозначает бензоильный радикал и Ar обозначает фенильный радикал, известен под названием таксол.
Продукт общей формулы (VI), в которой R обозначает атом водорода, R1 обозначает трет. -бутоксикарбонильный радикал и Ar обозначает фенильный радикал, который известен под названием Таксотер (Taxotere), составляет предмет изобретения европейского патента 0253738.
Аналогичные Таксотеру продукты составляют предмет изобретения международной заявки ВОИС 92/09589.
В зависимости от значений R1, R2 и R3, продукты общей формулы (VI) могут быть получены из продукта общей формулы (I)
- либо, когда R1 имеет вышеуказанное значение, R2 обозначает атом водорода и R3 обозначает защитную для гидроксильной функции группу, непосредственно путем замены защитных групп R3, G1 и G2 атомами водорода;
- либо, когда R1 имеет вышеуказанное значение, R2 и R3 вместе образуют 5- или 6-членный гетероцикл, в случае необходимости проходя промежуточно через продукт общей формулы (VII):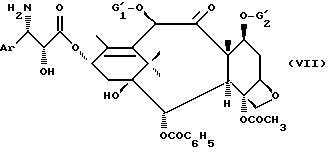
в которой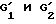 идентичны G1 и G2 и, кроме того, могут обозначать атом водорода, который подвергают воздействию ароилгалогенида или реакционноспособного производного общей формулы (VIII):
идентичны G1 и G2 и, кроме того, могут обозначать атом водорода, который подвергают воздействию ароилгалогенида или реакционноспособного производного общей формулы (VIII):
R4 - O - CO - Z
в которой
R4 имеет вышеуказанное значение и Z обозначает атом галогена или один из остатков -O-R4 или -O-CO-OR4, в которых R4 имеет вышеуказанное значение, для получения продукта общей формулы (IX):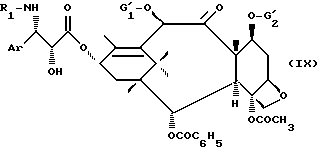
защитные группы 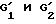 которого, если необходимо, заменены атомами водорода.
которого, если необходимо, заменены атомами водорода.
В особенности, когда в общей формуле (I), R2 и R3 вместе образуют оксазолидиновый цикл, гем-дизамещенный в положении 2, продукт общей формулы (VI) получают, проходя промежуточно через продукт общей формулы (VII).
Когда, в общей формуле (I), R1 обозначает радикал R4-O-CO- и когда R2 и R3 вместе образуют монозамещенный в положении 2 оксазолидиновый цикл, продукт общей формулы (IX), в которой R1 = R4-O-CO-, может быть получен непосредственно из продукта общей формулы (I).
Продукт общей формулы (VII), в которой 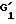 обозначает атом водорода или ацетильный радикал и
обозначает атом водорода или ацетильный радикал и  обозначает атом водорода, может быть получен из продукта общей формулы (I), в которой R1 обозначает радикал R4-O-CO-, в котором R4 обозначает алкильный радикал, замещенный одним или несколькими атомами галогена, R2 и R3 вместе образуют оксазолидиновый цикл, монозамещенный или гем-дизамещенный в положении 2.
обозначает атом водорода, может быть получен из продукта общей формулы (I), в которой R1 обозначает радикал R4-O-CO-, в котором R4 обозначает алкильный радикал, замещенный одним или несколькими атомами галогена, R2 и R3 вместе образуют оксазолидиновый цикл, монозамещенный или гем-дизамещенный в положении 2.
Продукт общей формулы (VII) также может быть получен из продукта общей формулы (I), в которой R1 обозначает атом водорода и R2 и R3 вместе образуют оксазолидиновый цикл, замещенный в положении 2 тригалогенметильным радикалом или фенильным радикалом, замещенным тригалогенметильным радикалом.
Прямую замену защитных групп R3, G1 и G2 в продукте общей формулы (I) или 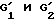 в продукте общей формулы (IX) атомами водорода осуществляют путем обработки цинком, в случае необходимости комбинированным с медью, в присутствии уксусной кислоты при температуре 30-60oC, или с помощью неорганической или органической кислоты, такой, как соляная или уксусная кислота в виде раствора в алифатическом спирте с 1-3 C-атомами или алифатическом сложном эфире, таком, как этилацетат, изопропилацетат или н-бутилацетат, в присутствии цинка, в случае необходимости комбинированного с медью, когда R3, G1 и/или G2 обозначают 2,2,2-трихлор-этоксикарбонильный радикал; или путем обработки в кислой среде, такой, как, например, хлороводород в виде раствора в алифатическом спирте с 1-3 C-атомами (метанол, этанол, пропанол, изопропанол) или водная фтороводородная кислота, при температуре 0-40oC, когда R3, G1 и/или G2 обозначают силилированный радикал. Когда R3 обозначает группу -CH2-Ph, то эту защитную группу необходимо заменять атомом водорода путем гидрогенолиза в присутствии катализатора, после замены защитных групп G1 и G2 атомами водорода в вышеописанных условиях.
в продукте общей формулы (IX) атомами водорода осуществляют путем обработки цинком, в случае необходимости комбинированным с медью, в присутствии уксусной кислоты при температуре 30-60oC, или с помощью неорганической или органической кислоты, такой, как соляная или уксусная кислота в виде раствора в алифатическом спирте с 1-3 C-атомами или алифатическом сложном эфире, таком, как этилацетат, изопропилацетат или н-бутилацетат, в присутствии цинка, в случае необходимости комбинированного с медью, когда R3, G1 и/или G2 обозначают 2,2,2-трихлор-этоксикарбонильный радикал; или путем обработки в кислой среде, такой, как, например, хлороводород в виде раствора в алифатическом спирте с 1-3 C-атомами (метанол, этанол, пропанол, изопропанол) или водная фтороводородная кислота, при температуре 0-40oC, когда R3, G1 и/или G2 обозначают силилированный радикал. Когда R3 обозначает группу -CH2-Ph, то эту защитную группу необходимо заменять атомом водорода путем гидрогенолиза в присутствии катализатора, после замены защитных групп G1 и G2 атомами водорода в вышеописанных условиях.
Продукт общей формулы (VII) может быть получен из продукта общей формулы (I), в которой R2 и R3 вместе образуют гем-дизамещенный в положении 2 оксазолидиновый цикл, путем обработки с помощью муравьиной кислоты, в случае необходимости в спирте, таком, как этанол, или газообразного хлороводорода в спирте, таком, как этанол.
Продукт общей формулы (IX), в которой R1 обозначает радикал R4-O-CO, может быть получен непосредственно из продукта общей формулы (I), в которой R1 обозначает радикал R4-O-CO- и R2 и R3 вместе образуют монозамещенный в положении 2 оксазолидиновый цикл, путем обработки с помощью кислоты, такой, как метансульфокислота, при температуре 0-40oC.
Продукт общей формулы (VII), в которой 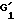 обозначает атом водорода или ацетильный радикал, а
обозначает атом водорода или ацетильный радикал, а  обозначает атом водорода, могут быть получены из продукта общей формулы (I), в которой R1 обозначает радикал R4-O-CO-, в котором R4 обозначает алкильный радикал, замещенный одним или несколькими атомами галогена, и R2 и R3 образуют оксазолидиновый цикл, монозамещенный или гем-дизамещенный в положении 2, путем обработки с помощью цинка в уксусной кислоте или электрохимическим путем.
обозначает атом водорода, могут быть получены из продукта общей формулы (I), в которой R1 обозначает радикал R4-O-CO-, в котором R4 обозначает алкильный радикал, замещенный одним или несколькими атомами галогена, и R2 и R3 образуют оксазолидиновый цикл, монозамещенный или гем-дизамещенный в положении 2, путем обработки с помощью цинка в уксусной кислоте или электрохимическим путем.
Продукт общей формулы (VII), в которой 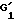 обозначает ацетильный радикал или защитную для гидроксильной функции группу и
обозначает ацетильный радикал или защитную для гидроксильной функции группу и 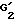 обозначает защитную для гидроксильной функции группу, может быть получен из продукта общей формулы (I), в которой R1 обозначает атом водорода и R2 и R3 вместе образуют оксазолидиновый цикл, замещенный в положении 2 тригалогенметильным радикалом или фенильным радикалом, замещенным тригалогенметильным радикалом, путем обработки с помощью цинка в уксусной кислоте.
обозначает защитную для гидроксильной функции группу, может быть получен из продукта общей формулы (I), в которой R1 обозначает атом водорода и R2 и R3 вместе образуют оксазолидиновый цикл, замещенный в положении 2 тригалогенметильным радикалом или фенильным радикалом, замещенным тригалогенметильным радикалом, путем обработки с помощью цинка в уксусной кислоте.
Следующие примеры иллюстрируют настоящее изобретение.
Пример 1
В реактор емкостью 50 см3 вводят, в инертной атмосфере и при температуре около 20oC, 0,321 г 5-карбокси-2,2-диметил-4-фенил-3-(трет.-бутоксикарбонил)-1,3(4S, 5R) -оксазолидина, 0,244 г 2,4,6-трихлор-бензоилхлорида, 8 см3 безводного толуола и 0,101 г триэтиламина. Реакционную смесь выдерживают в течение 2-х часов при перемешивании при температуре около 20oC. Затем добавляют 0,896 г 4-ацетокси-2-бензоилокси -5β, 20-эпокси- 1β,13α -дигидрокси-9-оксо-бис- 7β,10β -(2,2,2-трихлор-этоксикарбонилокси)-таксена-11 и 0,122 г 4-диметиламино-пиридина. После перемешивания в течение 20 часов при температуре около 20oC, образовавшийся триэтиламин-хлоргидрат отфильтровывают и промывают толуолом. Толуольную фазу промывают 2 раза по 10 см3 воды, сушат над сульфатом натрия, затем концентрируют досуха при пониженном давлении. Анализ путем высокоэффективной жидкостной хроматографии показывает, что выход 4-ацетокси -2α- бензоилокси -5β, 20-эпокси -1β- -гидрокси-9-оксо-бис -7β,10β- (2,2,2-трихлор-этоксикарбонилокси)-такс-11ен -13α- ил-2,2-диметил-4-фенил-3-(трет.-бутоксикарбонил)-1,3-(4S,5R)-оксазолидин-5- карбоксилата составляет 77% в расчете на превращенный спирт и 63% в расчете на используемый спирт.
Пример 2
В колбу емкостью 50 см3, снабженную системой магнитного перемешивания, вводят, в атмосфере аргона, 275 мг (0,78 ммоль) 3-фенил-3-трет.-бутоксикарбониламино-2-(1-этокси-этокси)-(2R, 3S)- пропионовой кислоты в виде раствора в 13 см3 безводного толуола. Затем последовательно добавляют 108,5 мкмл триэтиламина (0,78 ммоль) и 189,5 мг (0,78 ммоль) 1-хлоркарбонил-2,4,6-трихлор-бензола. Реакционную смесь перемешивают в течение 54-х часов при температуре около 25o. К бесцветной гетерогенной среде добавляют 190,6 мг 4-диметиламинопиридина (1,56 ммоль). Оставляют реагировать в течение 5 минут при температуре около 25oC, затем вводят 116 мг (0,13 ммоль) 4-ацетокси -2α- бензоилокси -5β-, 20-эпокси -1β,13α- дигидрокси-9-оксо-бис -7β,10β- (2,2,2-трихлор-этоксикарбонилокси)-таксена-11. Оставляют реагировать в течение 5 минут при температуре около 25oC, затем реакционную смесь нагревают при 72 - 73oC. Оставляют реагировать, при хорошем перемешивании, в течение 64-х часов при этой температуре. После охлаждения реакционную смесь желто-оранжевого цвета разбавляют 60 см3 этилацетата. Полученную органическую фазу промывают 3 раза по 5 см3 водного насыщенного раствора бикарбоната натрия, 5 раз по 5 см3 водой и 2 раза по 5 см3 водного насыщенного раствора хлорида натрия, затем сушат над сульфатом натрия.
После отфильтровывания и удаления растворителей при пониженном давлении (2,7 кПа), получают остаток (488 мг), который очищают путем препаративной тонкослойной хроматографии на диоксиде кремния, элюируя смесью диэтилового эфира с дихлорметаном (5:95 по объему) и осуществляя 2 пропускания.
Таким образом получают 46 мг исходного производного баккатина-III и 69 мг 4-ацетокси -2α- бензоилокси -5β, 20-эпокси -1β- гидрокси-9-оксо-бис -7β,10β- (2,2,2-трихлор-этоксикарбонилокси)-такс-11-ен -13α- ил - 2-(1-этокси-этокси)-3-фенил-3-трет.-бутоксикарбониламино-(2R,3S)- пропионата, структура которого подтверждена ИК-спектром и спектром протонного ядерного магнитного резонанса. Выход составляет 72% в расчете на используемый спирт.
Пример 3
Следуя той же методике, что и в примере 1, но заменяя 2,4,6-трихлор-бензоил-хлорид на 0,120 г пивалоилхлорида, получают 1,16 г сырого продукта, анализ с помощью высокоэффективной жидкостной хроматографии которого показывает, что выход 4-ацетокси -2α- бензоилокси -5β, 20-эпокси -1β- гидрокси-9-оксо-бис -7β,10β- (2,2,2-трихлор-этоксикарбонилокси)-такс-11-ен -13α- ил- 2,2-диметил-4-фенил-3-(трет.-бутоксикарбонил)-1,3(4S,5R)- оксазолидин-5-карбоксилата составляет 98% в расчете на превращенный спирт и 71% в расчете на используемый спирт.
Пример 4
Следуя той же методике, что и в примере 1, но заменяя 2,4,6-трихлор-бензоил-хлорид на 0,119 г тионилхлорида и используя 0,202 г триэтиламина, получают 1,36 г сырого продукта, анализ с помощью высокоэффективной жидкостной хроматографии которого показывает, что выход 4-ацетокси -2α- -бензоилокси -5β, 20-эпокси -1β- гидрокси-9-оксо-бис -7β,10β- (2,2,2-трихлор-этоксикарбонилокси)-такс-11-ен -13α- ил -2,2-диметил-4-фенил-3-(трет.-бутоксикарбонил)-1,3- -(4S,5R)-оксазолидин-5-карбоксилата составляет 93% в расчете на превращенный спирт и 31% в расчете на используемый спирт.
Пример 5
К перемешиваемому раствору 0,353 г 2-(1-этокси-этокси)-3-фенил-3-трет. -бутоксикарбониламино-(2R, 3S) -пропионовой кислоты и 0,122 г 4-диметиламино-пиридина в 4 см3 толуола в течение 15 минут и при температуре около 20oC добавляют 0,244 г 2,4,6-трихлор-бензоил-хлорида. Реакционную смесь выдерживают в течение 16 часов при перемешивании и при температуре около 20oC. Добавляют 0,448 г 4-ацетокси -2α- бензоилокси -5β, 20-эпокси -1β,13α- дигидрокси-9-оксо-бис -7β,10β- 2,2,2-трихлор-этоксикарбонилокси)- таксена-1 и 0,122 г 4-диметиламино-пиридина. Выдерживают в течение 20 часов при перемешивании. Анализ с помощью высокоэффективной жидкостной хроматографии показывает, что выход 4-ацетокси -2α- бензоилокси -5β, 20-эпокси -1β- гидрокси-9-оксо-бис -7β,10β- (2,2,2-трихлор-этоксикарбонилокси)-такс-11-ен-2(1-этокси-этокси)-3- фенил-3-трет. -бутоксикарбониламино-(2R, 3S)- и (2S,3S)-пропионата составляет 58% в расчете на используемый спирт и 100% в расчете на превращенный спирт.
Соотношение двух эпимеров (2R,3S)/(2S,3S) равно 84/16.
Способ получения сложных эфиров баккатина-III или 10-дезацетилбакнатина-III формулы I заключается в этерификации до сложного эфира защищенного баккатина-III или 10-дезацетил-баккатина-III формулы II с помощью антивированной кислоты формулы III. В формулах I, II и III Аr - фенил, или а) R1-ароильный радикал, где арильная часть - фенил или радикал формулы R4-O-СО-, в которой R4 - линейный или разветвленный C1-8 алкил; R2 - Н, R3 - защитная группа функциональной ОН группы; или б) R1 имеет вышеуказанные значения и атом водорода; R2 и R3 вместе образуют оксазолидинил; G1 - защитная для гидроксильной функции группа или ацетил; G2 - защитная для гидроксильной функции группа. Сложные эфиры формулы I пригодны для получения произвольных таксана, обладающих замечательными антилейкемическими и противоопухолевыми свойствами. 2 c. и 17 з. п. ф-лы.


 O
O
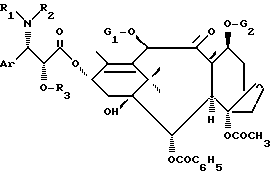
в которой Ar обозначает фенил, или
(а) R1 обозначает ароильный радикал, где арильная часть является фенилом, или радикал формулы R4-O-CO-, в которой R4 обозначает линейный или разветвленный алкильный радикал с C1-C8;
R2 обозначает атом водорода;
R3 обозначает защитную группу функциональной OH группы;
или
(б) R1 имеет вышеуказанное значение и, кроме того, может обозначать атом водорода;
R2 и R3 вместе образуют оксазолидинил;
G1 обозначает защитную для гидроксильной функции группу или ацетил;
G2 обозначает защитную для гидроксильной функции группу, отличающийся тем, что защищенный баккатин-III или 10-дезацетил-баккатин-III общей формулы II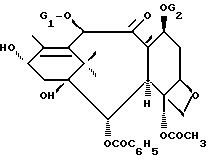
в которой G1 и G2 имеют вышеуказанное значение,
этерифицируют до сложного эфира с помощью активированной кислоты общей формулы III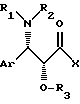
в случае необходимости получаемой in situ, в которой Ar, R1, R2 и R3 имеют вышеуказанное значение и X обозначает ацилоксирадикал с 1 - 5 атомами углерода в линейной или разветвленной цепи, или ароилоксирадикал, в котором арильная часть обозначает фенильный радикал, в случае необходимости замещенный 1 - 5 одинаковыми или разными заместителями, выбираемыми среди атомов галогена и нитрогруппы, метильного или метоксирадикалов, или X - атом галогена, и полученный продукт выделяют.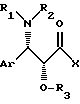
отличающийся тем, что Ar, R1, R2, R3 и R4 имеют указанное в п.1 значение.
| Автоматический огнетушитель | 0 |
|
SU92A1 |
| МАССА ДЛЯ ИЗГОТОВЛЕНИЯ ЭЛЕКТРОДОВ | 0 |
|
SU336840A1 |
Авторы
Даты
1998-12-20—Публикация
1993-10-04—Подача