Изобретение относится к новым ангидридам формулы (1):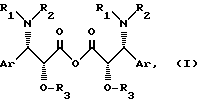
где А r обозначает фенил, возможно замещенный атомом галогена, C1-C4 алкилом или C1-C4 алкоксилом, или R1 обозначает бензоильный или трет-бутоксикарбонильный радикал, R2 обозначает атом водорода и R3 обозначает защитную группу для гидроксильной функции, или R1 обозначает трет-бутоксикарбонильный радикал и R2 и R3 вместе образуют 5- или 6-членный насыщенный гетероцикл, содержащий в качестве гетероатома азот или кислород,
их получению и использованию.
Согласно изобретению новые ангидриды общей формулы (1) могут быть получены путем воздействия дегидратирующего агента, такого, как имид, например, дициклогексилкарбодиимид, на кислоту общей формулы (II):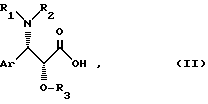
где Ar, R1, R2 и R3 имеют указанные значения.
Обычно используют 0,5-1 моль дегидратирующего агента на моль применяемой кислоты.
Обычно реакцию осуществляют в органическом растворителе, выбираемом среди алифатических галогенированных углеводородов, таких, как дихлорметан или хлороформ и ароматических углеводородов, таких как бензол, толуол или ксилолы.
Обычно реакцию осуществляют при 0-30oC.
Полученный ангидрид может быть отделен от полученной смеси обычными способами. Однако может быть предпочтительным использование полученного ангидрида, приготовленного перед самым его применением, без предварительного выделения, в особенности в реакциях этерификации (для получения сложных эфиров).
Ангидриды общей формулы (1) обычно более стабильны, чем кислоты, из которых они образуются, в реакциях этерификации, и они могут приводить к более легко воспроизводимым реакциям.
Новые ангидриды общей формулы (1) особенно пригодны для получения таксола или таксотера или их производных общей формулы (III):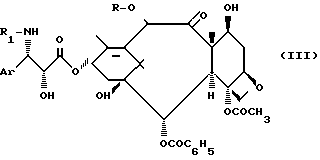
в которой R обозначает атом водорода или ацетильный радикал и R1 и Ar имеют указанное значение, которые обладают особенно интересными противоопухолевыми свойствами.
Согласно изобретению продукты общей формулы (III) могут быть получены:
а) либо путем воздействия ангидрида общей формулы (I), в которой Ar имеет указанное значение, R1 обозначает бензоильный или трет-бутоксикарбонильный радикал, R2 обозначает атом водорода и R3 обозначает защитную группу для гидроксильной функции, на производное баккатина III или 10-дезацетил-баккатина III общей формулы /IV/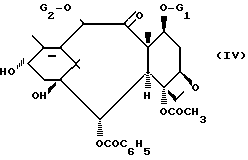
где G1 обозначает защитную группу для гидроксильной функции, такую, как 2,2,2-трихлор-этоксикарбонильный или триалкилсилильный радикал, каждая алкильная часть которого содержит 1-4 атома углерода и G2 обозначает ацетильный радикал или защитную группу для гидроксильной функции, такую как 2,2,2-трихлорэтоксикарбонильный радикал с получением соединения общей формулы (V):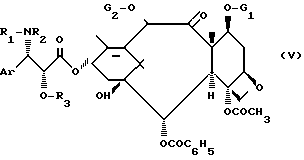
где Ar, R1, R2, R3, G1 и G2 имеют указанное значение, с последующей заменой радикалов G1, R3 и в случае необходимости G2 на атомы водорода для получения соединения общей формулы (III).
Получение сложного эфира спирта общей формулы (IV) обычно осуществляют в присутствии активирующего агента, такого, как аминопиридин, как 4-диметиламинопиридин, работая в органическом растворителе, таком, как бензол, толуол, ксилолы, этилбензол, изопропилбензол или хлорбензол, при 0-90oC.
Обычно используют 0,6-1,6 моль ангидрида общей формулы (I) на моль спирта общей формулы (IV).
Обычно используют 0,1-1 моль активирующего агента на моль спирта общей формулы (I).
Особенно предпочтительно работать в среде, в которой концентрация спирта общей формулы (IV) в растворителе составляет 1-30% (мас./об.).
В зависимости от природы защитных групп G1, G2 и R3 их замена атомами водорода может быть осуществлена с помощью цинка в присутствии уксусной кислоты или неорганической или органической кислоты, такой, как соляная кислота или уксусная кислота, в виде раствора в алифатическом спирте с 1-3 атомами углерода, в присутствии цинка, если защитные группы обозначают по крайней мере один 2,2,2-трихлорэтоксикарбонильный радикал, либо с помощью кислоты, такой, как соляная кислота, в алифатическом спирте с 1-3 атомами углерода, при температуре, близкой к 0oC, если защитные группы обозначают по крайней мере один триалкилсилильный радикал.
Если защитная группа R3 обозначает метоксиметильный, 1-этоксиэтильный, бензилоксиметильный, ( β-триметилсилилэтокси)-метильный или тетрагидропиранильный радикал, то эту защитную группу можно заменять атомом водорода путем обработки в кислой среде при 0-30oC с получением соединения общей формулы (VI):
который может быть предварительно очищен до замены защитных групп G1 и G2 атомами водорода в описанных условиях,
б) либо путем воздействия ангидрида общей формулы (I), в которой Ar имеет указанное значение, R1 обозначает трет-бутоксикарбонильный радикал и R2 и R3 вместе образуют насыщенный 5- или 6-членный гетероцикл, на соединение общей формулы (IV) с получением соединения общей формулы (V), в которой Ar имеет указанное значение, R1 обозначает трет-бутоксикарбонильный радикал и R2 и R3 вместе образуют насыщенный 5- или 6-членный гетероцикл, который обрабатывают неорганической или органической кислотой, в случае необходимости в спирте в условиях, которые не оказывают влияния на защитные группы G1 и G2 c получением соединения общей формулы (VII):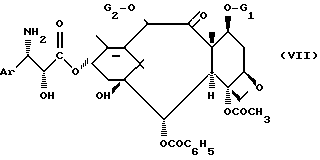
в которой Ar имеет указанное значение, G1 обозначает защитную группу для гидроксильной функции, предпочтительно 2,2,2-трихлор-этоксикарбонильный радикал, и G2 обозначает ацетильный радикал или защитную группу для гидроксильной функции, такую, как 2,2,2-трихлорэтоксикарбонильный радикал, которое обрабатывают соединением, позволяющим вводить в амино-функцию бензоильный или трет-бутоксикарбонильный радикал, с получением соединения общей формулы (VI), в которой Ar, G1 и G2 имеют указанные значения, после чего в этом соединении защитную группу G1 и G2 заменяют атомами водорода в описанных условиях.
Обычно этерификацию (получение сложного эфира) продукта общей формулы (V) осуществляют в присутствии активирующего агента, такого, как аминопиридин, как 4-диметиламинопиридин, работая в органическом растворителе, таком, как бензол, толуол, этилбензол, изопропилбензол или хлорбензол, при 0-90oC.
Обычно используют 0,6-1,6 моль ангидрида общей формулы (I) на моль спирта общей формулы (IV).
Обычно используют 0,1-1 моль активирующего агента на моль спирта общей формулы (IV).
Особенно предпочтительно работать в среде, в которой концентрация спирта общей формулы (IV) составляет 0-30% (мас./об.).
Обычно продукт общей формулы (VII) получают путем обработки продукта общей формулы (I), в которой Ar имеет указанное значение, R1 обозначает трет-бутоксикарбонильный радикал и R2 и R3 вместе образуют насыщенный 5- или 6-членный гетероцикл, с помощью муравьиной кислоты, в случае необходимости в спирте, таком, как этанол, или с помощью газообразного хлороводорода в спирте, таком, как этанол.
Введение бензоильной или трет-бутоксикарбонильной группы осуществляют путем взаимодействия бензоилхлорида или ди-трет-бутил-дикарбоната с соединением общей формулы (VII), работая в органическом растворителе, таком как метиленхлорид, в присутствии неорганического основания, такого как бикарбонат натрия, или органического основания, такого, как третичный амин, как триэтиламин.
Соединения общей формулы (III), полученные согласно изобретению, могут быть очищены обычными способами.
Пример 1. К раствору 1,72 г (2R,3S)-3-фенил-3-трет-бутоксикарбонил-амино-2-(1-этокси-этокси)- пропионовой кислоты (4,87 ммоль) в 4 см3 безводного метиленхлорида, при -10oC и в атмосфере аргона добавляют 0,206 г дициклогексилкарбодиимида в виде раствора в 1 см3 безводного метиленхлорида.
Реакционную смесь перемешивают в течение 40 мин, давая температуре повышаться до значения около 20oC.
Образовавшуюся дициклогексилмочевину отделяют путем фильтрования в инертной атмосфере, и фильтрат концентрируют при пониженном давлении (20 мм рт.ст., 2,7 кПа) при 30oC.
Таким образом получают 1,72 г ангидрида (2R, 3S)-3-фенил-3-трет-бутоксикарбониламино-2-(1-этокси-этокси)-пропионовой кислоты, характеристики которого следующие:
температура плавления 43oC,
ИК-спектр (вазелиновое масло): характерные полосы абсорбции: 3450-3330, 1835, 1764 и 1722 см-1,
спектр протонного ядерного магнитного резонанса (смесь трех изомеров)) (360 мГц, CDCl3/ГМДС, хим. сдвиги в м.д., T=40oC):
изомер A: 0,93(6Н, т.), 1,37(16Н, с. уширенный), 3,27(4Н, мультиплет), 4,36(2Н, к.), 4,44(2Н, с. уширенный), 5,53(2Н, с. уширенный), 7,11((4Н, д.), 7,20(2Н, т.), 7,29(4Н, т.),
-изомер В: 0,93(6Н, т.), 0,99(6Н, д.), 1,37(18Н, с. уширенный), 3,27(4Н, мультиплет), 4,37(2Н, к.), 4,44(2Н, с. уширенный), 5,53(2Н, с. уширенный), 7,11(4Н, д.), 7,20(2Н, т.), 7,29(4Н, т.),
изомер C: 0,73(6Н, т.), 1,12(3Н, д.), 1,13(3Н, д.), 1,37(18Н, с. уширенный), 2,61(2Н, м. ), 3,08(2Н, м.), 4,58(2Н, с. уширенный), 4,72 (1Н, к.), 4,73(1Н, к. ), 5,53(2Н, с. уширенный), 7,11(4Н, д.), 7,20(2Н, т.), 7,29(4Н, т.).
Пример 2. В реактор емкостью 250 см3 вводят 22,16 г (2R,3S)-3-фенил-3-трет-бутоксикарбониламино-2-(1-этокси-этокси)- пропионовой кислоты (6,28•10-2 моль) и 12,43 г дициклогексилкарбодиимида (6,02•10-2 моль) в 85 см3 безводного толуола. Перемешивают в течение 30 мин.
После отфильтровывания образовавшейся дициклогексилмочевины, полученный раствор в течение 8 ч добавляют к раствору 21 г 4-ацетокси- 2α-бензоилокси-5β, 20эпокси- 1,13α-дигидрокси-9-оксо-7β, 10β-бис-(2,2,2-трихлорэтокси)-карбонилокси-11-таксена с титром 95% (2,24•10-2 моль) и 0,61 г 4-диметиламинопиридина в 84 см3 безводного толуола при 75oC.
Перемешивают еще в течение 2 ч после окончания добавления. После охлаждения до температуры около 20oC дициклогексилмочевину отделяют фильтрованием. Фильтрат концентрируют, и остаток обрабатывают с помощью 150 см3 циклогексана. После полного растворения при 60oC раствор выливают в 350 см3 гептана, охлажденного до 1-5oC. Образовавшийся осадок отделяют фильтрацией, промывают холодным гептаном, затем высушивают при пониженном давлении. Таким образом получают 38 г слегка коричневого продукта, анализ которого с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ) показывает, что он содержит 25,5 г (2R, 3S)-/4-ацетокси-2α-бензоилокси-5β, 20-эпокси-1-гидрокси-9-оксо-7β, 10β-бис(2,2,2-трихлорэтокси)-карбонилокси-11-таксен-13α-ил/-3-трет-бутоксикарбониламино-3-фенил-2-(1-этокси-этокси)-пропионата, содержащего 15% (2S, 3S)-эпимера.
Полученный продукт, обработанный в условиях, описанных в патенте США 4924011, представляет собой (2R,3S)-/4-ацетокси-2α-бензоилокси-5β,20-эпокси-1, 7β, 10β-тригидрокси-9-оксо-11-таксен-13α-ил/-3-трет-бутоксикарбониламино-3-фенил-2-гидрокси-пропионат.
Пример 3. К раствору 1,6 г (4S,5R)-3-трет-бутоксикарбонил-2, 2-диметил-4-фенил-5-оксазолидинкарбоновой кислоты в 5 см3 безводного метиленхлорида при температуре около 20oC и в атмосфере аргона добавляют 0,206 г дициклогексилкарбодиимида.
Реакционную смесь перемешивают в течение 30 мин.
Образовавшуюся дициклогексилмочевину отделяют фильтрованием и фильтрат концентрируют досуха при пониженном давлении (20 мм рт.ст., 2,7 кПа) при 30oC.
Таким образом получают 1,5 г ангидрида (4S, 5R)-3-трет-бутоксикарбонил-2,2-диметил-4-фенил-5-оксазолидинкарбоновой кислоты, характеристики которого следующие:
температуре плавления 46oC,
ИК-спектр (вазелиновое масло): основные характерные полосы абсорбции: 1836, 1764, 1703 см-1,
спектр протонного ядерного магнитного резонанса (360 мГц, ДМСО/ГМДС, хим. сдвиги в м.д.): 1,15 (C. уширенный, 9Н), 1,57(с., 3Н), 1,64(с., 3Н), 4,52(д. 1Н), 5.03(с. уширенный, 1Н), 7,28(м. 5Н).
Пример 4. Работая, как в примере 2, но используя ангидрид (4S, 5R)-3-трет-бутоксикарбонил-2,2-диметил-4-арил-5-оксазолидинкарбоновой кислоты, полученный в условиях примера 3, через промежуточный продукт общей формулы (YII), с которым вводят во взаимодействие ди-трет-бутил-дикарбонат или бензоилхлорид, получают следующие продукты:
(2R, 3S)-/4-ацетокси-2α-бензоилокси-5β, 20-эпокси-1,7β, 10β-тригидрокси-9-оксо-11-таксен-13α-ил/-3-трет-бутоксикарбонил-амино-3-(4-метил-фенил)-2-гидроксипропионат, вращательная способность которого (α)
(2R, 3S)/-4-ацетокси-2α-бензоилокси-5β, 20-эпокси-1,7β, 10β-тригидрокси-9-оксо-11-таксен-13α-ил-/-3-трет-бутоксикарбониламино-3-(3-фторфенил)-2-гидроксипропионат, вращательная способность которого (α)
(2R, 3S)-/4-ацетокси-2α-бензоилокси-5β, 20-эпокси-1,7β, 10β-тригидрокси-9-оксо-11-таксен-13α-ил/-3-трет-бутоксикарбониламино-3-(2-фторфенил)-2-гидроксипропионат, вращательная способность которого (α)
(2R, 3S)-/2-ацетокси-2α-бензоилокси-5β, 20-эпокси-1,7β, 10β-тригидрокси-9-оксо-11-таксен-13α-ил/-3-трет-бутоксикарбониламино-3-(4-хлорфенил)-2-гидроксипропионат, вращательная способность которого (α)
(2R, 3S)-/4-ацетокси-2α-бензоилокси-5β, 20-эпокси-1,7β, 10β-тригидрокси-9-оксо-11-таксен-13α-ил/-3-трет-бутоксикарбониламино- 3-(4-метокси-фенил)-2-гидроксипропионат, вращательная способность которого (α)
(2R, 3S)-/4-ацетокси-2α-бензоилокси-5β, 20-эпокси-1,7β, 10β-тригидрокси-9-оксо-11-таксен-13α-ил/-3-трет-бутоксикарбониламино-3-(4-фторфенил)-2-гидроксипропионат, вращательная способность которого (α)
(2R,3S)-/4,10β-диацетокси-2α-бензоилокси-5β,20-эпокси-1,7β-дигидрокси-9-оксо-11-таксен-13α-ил/-3-бензоиламино-2-гидрокси-3-фенил-пропионат (или таксол).
Изобретение также относится к соединениям общей формулы (III), полученным по способу с использованием ангидрида общей формулы (I).
Изобретение относится также к противоопухолевым композициям, которые содержат соединения общей формулы (III), полученные по способу с использованием ангидрида общей формулы (I).
Объектом изобретения являются новые ангидриды общей формулы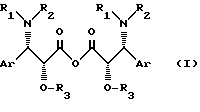
где Ar - арильный радикал
или R1 - C6H5-CO или (CH3)3C-O-CO, R2 - атом водорода и R3 - защитная группа для гидроксильной функции;
или R1 - (CH3)3C-O-CO и R2 и R3 вместе образуют насыщенный 5- или 6-членный гетероцикл,
способ их получения и их использование для получения производных таксана общей формулы: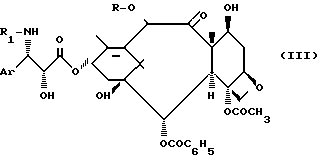
где R - H, ацетил, R1 - C6H5-CO или (CH3)3C-O-CO,
которые обладают противоопухолевыми свойствами. 4 с. и 5 з.п. ф-лы.
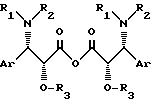
где Ar фенил, возможно замещенный атомом галогена или радикалом алкил с 1 4 атомами углерода или радикалом алкокси с 1 4 атомами углерода;
R1 бензоил или трет-бутоксикарбонил;
R2 водород;
R3 защитная группа для гидроксила,
или
R1 трет-бутоксикарбонил;
R2 и R3 образуют вместе 5- или 6-членный насыщенный гетероцикл, содержащий в качестве гетероатома азот или кислород.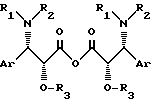
где Ar фенил, возможно замещенный атомом галогена, алкилом C1 - C4, алкоксилом C1 C4;
R1 бензоил или трет-бутоксикарбонил;
R2 водород;
R3 защитная группа для гидроксила,
или
R1 трет-бутоксикарбонил;
R2 и R3 вместе образуют 5- или 6-членный насыщенный гетероцикл, содержащий в качестве гетероатома азот или кислород,
отличающийся тем, что дегидратирующий агент вводят во взаимодействие с кислотой общей формулы II
в которой Ar, R1, R2 и R3 имеют указанные значения.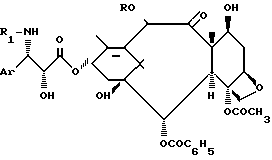
где R водород или ацетильный радикал;
R1 бензоильный или трет-бутоксикарбонильный радикал;
Ar фенил, возможно замещенный атомом галогена, алкилом C1 - C4, алкоксилом C1 C4,
путем этерификации производного баккатина III или 10-дезацетилбаккатина III, отличающийся тем, что в качестве производного баккатина III или 10-дезацетилбаккатина III используют соединение общей формулы IV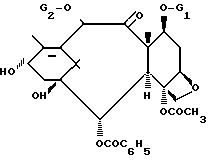
где G1 защитная группа для гидроксила;
G2 ацетильный радикал или защитная группа для гидроксила,
и этерификацию осуществляют с помощью ангидрида общей формулы I по пп.1 и 2, полученного по пп.4 7, возможно ин ситу, до получения соединения общей формулы V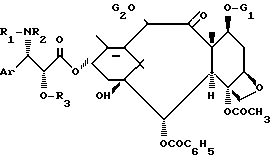
где Ar, R1, R2, R3, G1 и G2 имеют указанные значения,
и заменяют защитные группы R3, G1 и G2 на атомы водорода.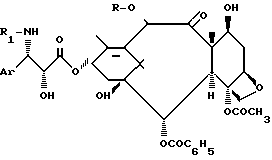
где Ar и R имеют значения, указанные в п.8;
R1 трет-бутоксикарбонильный радикал,
путем этерификации производного баккатина III или 10-дезацетилбаккатина III, отличающийся тем, что в качестве производного беккатина III или 10-дезацетилбаккатина III используют соединение общей формулы IV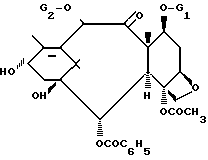
где G1 защитная группа для гидроксила;
G2 ацетильный радикал или защитная группа для гидроксила,
и этерификацию осуществляют с помощью ангидрида общей формулы I по пп.1
3, полученного по пп.4 7 возможно ин ситу, до получения соединения общей формулы V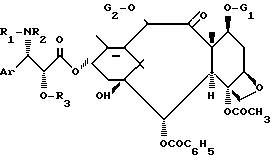
где R1 трет-бутоксикарбонил;
R2 и R3 вместе образуют насыщенный 5-6-членный гетероцикл;
Ar имеет значение, указанное в п.1;
G1 защитная группа для гидроксила;
G2 ацетильный радикал или защитная группа для гидроксила,
которое обрабатывают в кислой среде в условиях, не оказывающих влияния на защитные группы G1 и G2, с получением соединения общей формулы VI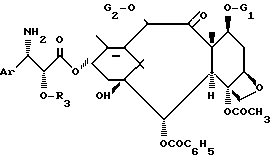
в которой Ar, G1 и G2 имеют указанные значения,
которое затем обрабатывают соединением, позволяющим вводить трет-бутоксикарбонильный радикал в аминную функцию, после чего защитные группы G1 и G2 заменяют атомом водорода согласно известным способам.
| EP, патент, 0253738, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| EP, патент, 0400971, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1998-02-10—Публикация
1993-02-04—Подача