Настоящее изобретение относится к способу каталитического частичного окисления (который в данной заявке на патент будет кратко обозначаться как "КЧО") природного газа с целью получения синтез-газа и формальдегида; более конкретно оно относится к получению синтез-газа для процесса Фишера-Тропша (Ф-Т), к способам синтеза метанола и смесей метанола с диметиловым эфиром в условиях высокой скорости конверсии на проход.
В настоящее время синтез-газ производят способами конверсии с водяным паром, автотермального риформинга, некаталитического частичного окисления углеводородов. Процессы конверсии с водяным паром каталитически превращают смеси углеводородов и водяного пара (H2O/C = 2.5 - 3.5 (объем/объем)) в смеси CO и H2 с отношением H2/CO обычно около 3 в том случае, когда исходным веществом является природный газ. Основные реакции, которые описывают этот процесс, следующие:
CnHm + n•H2O ---> n•CO + (m+n/2)•H2 [1]
H2O + CO ---> CO2 + H2 [2]
Отношение H2O/C в реакционной смеси определяется условиями температуры и давления, при которых проводят реакцию, а также необходимостью ингибирования реакций образования угля [3] и [4]:
CnHm ---> Cn + m/2 H2 [3]
2CO ---> C + CO2 [4]
Обычно используемые в этом процессе катализаторы основаны на Ni, нанесенном на носители - оксиды Al, Mg и Si. Применяемые носители проявляют высокие термостабильность и механические прочностные характеристики. Реакции проходят внутри трубчатых реакторов, находящихся в камере сгорания. Давления в трубах в типичных случаях лежат в диапазоне от 1 до 5 МПа, а температура на выходе из труб обычно выше 850oC (см., например, "Catalysis Science and Technology, " vol.5, Chapter I, J.R. Rostrup-Nilsen). Время пребывания газовых потоков внутри слоев катализатора составляет около 5 секунд. Вдоль труб для риформинга (приблизительно 15-метровой длины), которые полностью заполнены катализатором, возникают большие градиенты в составе газовой смеси.
Способы некаталитического частичного окисления используются менее широко и применяются для конверсии смесей углеводородов, кислорода, водяного пара и воздуха в синтез-газ с отношениями H2/CO обычно около 2, если исходным веществом является природный газ. Химия этого процесса может быть представлена уравнениями [5] и [2].
CnHm + n/2O2 ---> nCO + m/2H2 [5]
Оборудование, установленное в настоящее время в компаниях Texaco и Shell (см. Hydrocarbon Processing; April 1990, p. 99), оснащено адиабатическими реакторами, внутри которых начинают реакции с применением форсунки, где в основном проходят реакции полного сгорания углеводородов [6]:
CnHm + (n+m/2)O2 ---> nCO2 + m/2 H2O [6]
В результате этих реакций выделяются большие количества тепла, водяного пара и CO2. Теплота вызывает протекание реакций крекинга несожженных углеводородов и способствует реакции конверсии водяного пара и CO2 [1], [7].
nCO2 + CnHm ---> 2nCO + m/2 H2 [7]
Температуры процесса в типичных случаях лежат в диапазоне от 1250 до 1500oC, а давление устанавливается в диапазоне от 3 до 12 МПа. Для процесса требуется очень малое время пребывания смеси реагент/продукт внутри реактора (около 0.5 секунд). Поскольку в реакционной смеси используются отношения O2: CH4 обычно более 0.6 (объем/объем), получаемый синтез-газ содержит большие количества CO2.
Процессы автотермального риформинга осуществляют внутри адиабатических реакторов, в которые вводят смеси углеводородов, кислорода и водяного пара; кроме того, в этом случае отношения O2:CH4 превышают стехиометрическую величину 0.5. В первой реакционной зоне с помощью форсунки начинаются реакции полного сгорания углеводородов [6], во второй реакционной зоне внутри слоя катализатора происходят реакции конверсии водяного пара [1] и CO2 [7]. В каталитическом слое используются катализаторы, проявляющие такие же характеристики, как катализаторы, описанные выше для процессов конверсии водяного пара. В результате автотермального риформинга получаются смеси синтез-газа с отношениями H2: CO, промежуточными между отношениями, обнаруженными для синтез-газа, полученного при конверсии водяного пара, и некаталитическом частичном окислении соответственно. Температура на выходе реактора в типичных случаях лежит в диапазоне от 900 до 1000oC, но температура в зоне, где установлена форсунка, значительно выше. Давление внутри реактора лежит в диапазоне от 2 до 4 МПа. Время пребывания внутри каталитического слоя составляет около 0.7 секунд.
Синтез-газ в основном используется в синтезе Ф-Т для получения углеводородных смесей, в синтезе метанола и в синтезе аммиака.
Процессы Ф-Т в основном реализованы Sasol в Южной Африке и используют синтез-газ, полученный из угля путем его газификации или в результате процесса конверсии метана. Инвестиционные затраты для оборудования Sasol подразделяются следующим образом (см. M.E. Dry "The Fischer-Tropsch synthesis - Commercial aspects" Catal. Today, 1990, 6, 183):
- добыча угля, производство водяного пара и O2 - 47%
- производство синтез-газа - 23%
- синтез Ф-Т - 30%
Как можно видеть, стоимость добычи угля и конверсии и стоимость производства синтез-газа составляют примерно 70% общей стоимости процесса, и производство топлива из угля экономически выгодно, если имеется доступный уголь по цене гораздо ниже цены нефти. Смеси синтез-газа, полученные по процессу Sasol, содержат отношения H2:CO в диапазоне от 1.7 до 2.
Синтез Ф-Т приводит в основном к получению углеводородов по уравнению [8]:
2nH2 + nCO ---> CnH2n + nH2O [8]
В действительности синтез Ф-Т является процессом полимеризации C1-единиц, в котором образуются насыщенные и ненасыщенные, линейные и разветвленные углеводороды.
В основном, в доступных в настоящее время технологиях гидрирования потока окиси углерода, образующегося в процессах конверсии водяного пара, автотермального риформинга и частичного окисления, требуется содержание метана менее 5%.
Реакции гидрирования окиси углерода в смесях чистых CO и H2 обнаруживают производительность конверсии менее 70%. Низкое содержание метана в синтез-газе необходимо для увеличения парциальных давлений CO и H2 и предотвращения уменьшения производительностей конверсии, обусловленного кинетическими и термодинамическими ограничениями, как это имеет место в реакциях гидрирования CO. Уменьшение производительности конверсии обуславливает увеличение количеств реагентов, которые нужно возвращать на повторную переработку, и CH4, накапливающегося во время рециклов.
В соответствии с приведенными доводами, целью является достижение величин производительности конверсии метана более 95%. Начиная с 1985 года разрабатываются способы синтеза дизельных топлив из природного газа, которые основаны на промежуточном производстве синтез-газа, синтезе Ф-Т углеводородов с длинной цепью и гидрокрекинге последних. В этом случае стоимость стадии производства синтез-газа также составляет примерно 60% от общей стоимости производства.
Стоимость производства синтез-газа вносит аналогичный процентный вклад также в общую стоимость обычного процесса получения метанола при температурах от 220 до 300oC.
Следовательно, в синтезах Ф-Т и синтезах метанола, осуществляемых обычными способами, используют смеси синтез-газа с пренебрежимо малым содержанием метана для того, чтобы предотвратить как уменьшение скоростей реакций и, следовательно, производительностей конверсии на проход, так и накопление метана в рециркулированном газе к стадии синтеза, что может быть обусловлено уменьшением парциальных давлений H2 и CO.
В противоположность этому, в синтезах метанола с высокими производительностями конверсии на проход, проводимых при низких температурах, можно конвертировать приблизительно 90% синтез-газа в метанол даже в присутствии больших количеств инертных газов. Однако в данном случае в реакционных смесях недопустимы примеси CO2 и H2O.
Этот способ в основном исследован в работах Shell (EP-285 228; EP-287 151; EP-289 067; EP-306 113; EP-306 114; EP-309 047; EP-317 035), Brookhaven National Laboratories (US-4935395; US-4614749; US-4 623 634; US-4 613 623), Mitsui (JP-81/169 934; JP -82/I28 642), Sintef (WO-86/3190), Snamprogetti (IT 20,028 A/88; IT 23,101 A/88; IT 23,102 A/88; IT 22,352 A/89; EP 357 071, EP-504 981).
Каталитические системы, используемые в этих синтезах, включают никель [Ni(CO)4/MeONa] или медь (CuCl/NeONa, хромит меди/MeONa), и синтезы осуществляют в шламовых реакторах. Реакции проходят в диапазоне температур от 90 до 120oC и в диапазоне давлений от 5 до 50 атм. В этих условиях достигаются производительности конверсии около 90% и селективности свыше 95% при использовании смесей CO и H2 (с отношениями H2:CO, равными 2 (объем/объем)) с высоким содержанием инертных молекул, таких как азот и метан (в типичных случаях исследовались реакции с содержанием инертных веществ около 40%).
Кроме того, синтез смесей метанол-диметиловый эфир может быть проведен с высокими значениями производительности конверсии на проход, поскольку образование диметилового эфира с последующей конверсией метанола благоприятствует достижению полной конверсии смеси CO/H2 [J. Bogild Hansen, F. Joensen - Stud. Surf. Sk. Catal., 61 (1991), 457]. Поэтому в данном случае реакция также может быть проведена в присутствии такого инертного газа, как неконвертированный метанол.
В данной работе найден способ каталитического частичного окисления (КЧО) природного газа для получения синтез-газа, в котором используется катализатор, содержащий благородный металл, и который осуществляется при сверхвысокой объемной скорости (СВОС), при температурах значительно более низких, чем применяемые в современных способах, а также при даже особенно низких мольных отношениях O2: C и H2O:CH4; при этом данный способ может быть эффективно объединен с процессами гидрирования окиси углерода, такими как синтезы Ф-Т и синтезы метанола или смесей метанол-диметиловый эфир.
Побочным продуктом настоящего способа является формальдегид, который отделяют перед использованием синтез-газа, если он образуется в относительно больших количествах, например превышающих около 3% по весу.
Возможность проведения процесса при объемных скоростях (1500000 > СЧСПГ > 20000 ч-1, СЧСПГ - среднечасовая скорость подачи газа) более высоких, чем используемые в настоящее время (СЧСПГ < 10000 ч-1) позволяет применять малогабаритные реакторы, что позволяет достичь экономии в инвестиционной стоимости. Возможность работы с потоками реагентов с мольными отношениями O2: CH4<0,5 (объем/объем) позволяет уменьшить потребление энергии и инвестиционные стоимости устройств для получения кислорода.
Способ каталитического частичного окисления метана [12], осуществляемый при объемных скоростях менее 15000 ч-1, может быть описан как сумма реакций полного сгорания углеводородов [9] и конверсии водяного пара и CO2 [10]-[11] .
CH4 + 2O2 ---> CO2 + 2H2O [9]
CO2 + CH4 ---> 2CO + 2H2 [10]
H2O + CH4 ---> CO + 3H2O [11]
CH4 + 1/2O2 ---> CO +2H2 [12]
При температурах ниже 600oC сильно экзотермичная реакция полного окисления [9] является в значительной степени выгодной, в то время, как протекание сильно эндотермичных реакций конверсии водяного пара и CO2 [10]-[11] невыгодно. Наоборот, при температурах выше 750oC обе эти последние реакции могут приводить к конверсии CO2 и H2O в синтез-газ.
Катализаторы, используемые в стадии КЧО по данному изобретению, дают возможность проведения реакций с отношениями O2:CH4 менее 0.5 также в отсутствие водяного пара, в условиях, которые нельзя осуществить в настоящее время с использованием известных в прототипах катализаторов вследствие реакций образования угля [3] и [4]. Синтез-газ, полученный в данных условиях, может содержать даже большие количества (до 50%) непрореагировавшего метана и может использоваться в реакциях синтеза с высокими величинами производительности конверсии на проход.
О влиянии высоких значений объемной скорости сообщается в опубликованных исследованиях D.A. Hickman and L.D. Schmidt (Science 1993, 259, 343), которые проводили эксперименты при температурах выше 1000oC с катализаторами на основе родия, и исследованиях V. R. Choudari, A.S. Mamman, S.D. Sansare (Angew. Chem. Int. Ed. Eng 1. 1992, 31, 1189), которые выполнили опытные испытания при температурах в диапазоне от 300 до 900oC с катализаторами, в состав которых не входили благородные металлы (Fe, Co, Ni). Опытные испытания, приведенные в настоящей заявке на патент, отличаются от описанных в опубликованных статьях. Вышеупомянутые авторы использовали катализаторы, отличающиеся от исследованных нами, и, следовательно, не могли работать с отношениями O2:CH4 < 5 (объем/объем) для того, чтобы избежать реакций образования угля [3], [4] и не допустить получения HCHO; более того, способ КЧО по настоящему изобретению позволяет получить синтез-газ в условиях СВОС даже в присутствии больших количеств CO2. Возможность использования CO2 в реакционной смеси дает возможность получения значительных преимуществ во всех случаях, когда требуется получить смесь синтез-газа с отношением H2:CO менее 2 (объем/объем). Такие низкие значения этого отношения выгодны для получения углеводородов с длинной цепью и высоким молекулярным весом в процессе синтеза Ф-Т. Как мы уже кратко заметили, углеводородные продукты с длинной цепью могут быть превращены в дизельные топлива для двигателей автомобилей.
При высоких значениях объемных скоростей, используемых в предлагаемом способе КЧО, значительно изменяются характеристики селективности реакций КЧО. Окись углерода и водород образуются с чрезвычайно высокими величинами селективности даже при низких температурах. Катализаторы, использованные в экспериментальных исследованиях КЧО по предлагаемому способу, значительно отличаются от описанных в технических статьях, поскольку они содержат очень малые количества благородного металла (до 0.1%).
Полагают, что реакции получения синтез-газа могут быть представлены в следующем виде: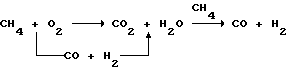
В соответствии с современными представлениями полагается, что в условиях высокой объемной скорости могут быть получены первичные продукты реакций окисления CO и H2, которые затем быстро удаляются с поверхности катализатора перед вступлением в реакции с образованием вторичных продуктов.
Первый предмет настоящего изобретения, способ каталитического частичного окисления природного газа с целью получения синтез-газа и формальдегида отличается тем, что такое окисление осуществляют с помощью катализатора, образуемого одним или более соединением металлов платиновой группы, которые имеют форму проволочных сеток или нанесены на носитель из неорганических соединений таким образом, что процентное содержание по весу металла или металлов платиновой группы лежит в диапазоне от 0.1 до 20%, предпочтительно от 0.1 до 5% общего веса катализатора и носителя, путем проведения процесса при температурах в диапазоне от 300 до 950oC, предпочтительно от 350 до 850oC, при давлениях в диапазоне от 0.5 до 50 атмосфер, предпочтительно от 1 до 40 атмосфер, при объемных скоростях в диапазоне от 20000 до 1500000 ч-1, предпочтительно от 100000 до 600000 ч-1.
Используемые катализаторы особенно активны по отношению к реакциям КЧО и особенно инертны по отношению к реакциям образования угля [3], [4], а также даже обладают способностью работать с отношениями O2:CH4 менее 0.5 (объем/объем) и в присутствии CO2 без потери активности. В тех случаях, когда отношение O2: CH4 меньше 0.5, потоки, выходящие из реактора КЧО, будут содержать большие количества непрореагировавшего метана.
Если реакции КЧО проводятся при использовании смесей реагентов с отношениями O2/CH4, равными 0.65 (объем/объем), содержание метана в выходящих потоках может быть уменьшено до уровней даже ниже 5%.
Как уже было кратко указано, используются катализаторы КЧО, содержащие металлы платиновой группы, в форме таблеток, которые получены по процедурам, описанным в патентной литературе (UK Patent N 2 240 284, UK Publ, N 2 247 465, IT-M192A 001 953, UK Publ. N 2 274 284). Кроме того, на стадии КЧО могут использоваться сетки из проволок благородных металлов, аналогично применяемым при производстве азотной кислоты, но с содержанием Rh более 9% по весу, или монолитные катализаторы. В частности, для последнего случая по предлагаемому способу описан оригинальный метод приготовления монолитных катализаторов, позволяющий быстро наносить благородные металлы с высокой степенью дисперсности на поверхность монолитного тела путем погружения последнего в раствор металлоорганических кластеров Rh, Ru и Ir в органическом растворителе. Металлы фиксируются на поверхностях монолитного тела путем твердофазно-жидкофазной реакции между реакционноспособными центрами на поверхности и металлоорганическими кластерами, которые затем разлагаются с образованием моноатомных частиц в крайне высокодисперсном состоянии. Эта процедура существенно отличается от способа импрегнации, поскольку содержание благородного металла, закрепленного на носителе, определяется числом активных центров на его поверхности.
Дальнейшим предметом настоящего изобретения являются объединенные способы синтезов метанола или смесей метанол/диметиловый эфир, а также синтезов Ф-Т.
Объединенный способ синтеза метанола из синтез-газа в основном заключается в проведении реакции синтез-газа, полученного с помощью вышеописанного способа, после возможного предварительного отделения образовавшегося формальдегида с помощью подходящего катализатора путем проведения процесса в случае синтезов с высокой конверсией на проход (после дополнительного отделения CO2 и H2O от указанного синтез-газа) при температуре выше 40oC и ниже 200oC и при давлении выше 1 МПа, или, в случае синтезов, осуществляемых обычным способом, при температуре выше 200oC и ниже 350oC и при давлении выше 0.3 МПа.
Объединенный способ синтеза смесей метанол-диметиловый эфир заключается в проведении реакции смеси синтез-газа и метана, полученной как было описано выше, после возможного предварительного отделения, возможно, образовавшегося формальдегида, в присутствии катализаторов, способных производить метанол и превращать полученный таким образом метанол в диметиловый эфир путем проведения процесса при температуре выше 150oC и ниже 400oC и при давлении выше 0.1 МПа и ниже 10 МПа.
Объединенный способ синтезов Ф-Т из синтез-газа в основном заключается в проведении реакции синтез-газа, полученного вышеописанным способом, после предварительного отделения, возможно, образовавшегося формальдегида, если это желательно, в присутствии подходящего катализатора путем проведения процесса при температуре выше 200 и ниже 400oC и при давлении выше 1 МПа.
Присутствие метана в реакционной смеси в настоящем случае допустимо только если используются способы с высокой производительностью конверсии на проход.
Значительное уменьшение стоимости, которое может быть достигнуто в способе получения синтез-газа, позволяет определить обладающие преимуществами объединенные способы конверсии природного газа в жидкий углеводород и/или кислородсодержащие продукты через синтез-газ, содержащий более 5% метана по объему.
Вышеупомянутые объединенные способы схематически показаны на фиг. 1 - 3.
На фиг.1 схематически показан объединенный способ синтезов Ф-Т из природного газа через синтез-газ, полученный с помощью способа по настоящему изобретению.
Природный газ (1) и кислород (2) вводят в реактор (3), где происходит каталитическое частичное окисление природного газа и образуются синтез-газ и формальдегид.
Формальдегид (4) может быть отделен от синтез-газов (5), которые поступают в реактор (10), где осуществляются синтезы Ф-Т.
Выходящий продукт (11) направляется в разделяющее устройство (12), из которого выходят поток (13), содержащий углеводороды с двумя или более атомами углерода и воду, и поток (14), содержащий метан и углеводороды с двумя или менее атомами углерода, причем последний поток направляется на повторную обработку в реактор (3).
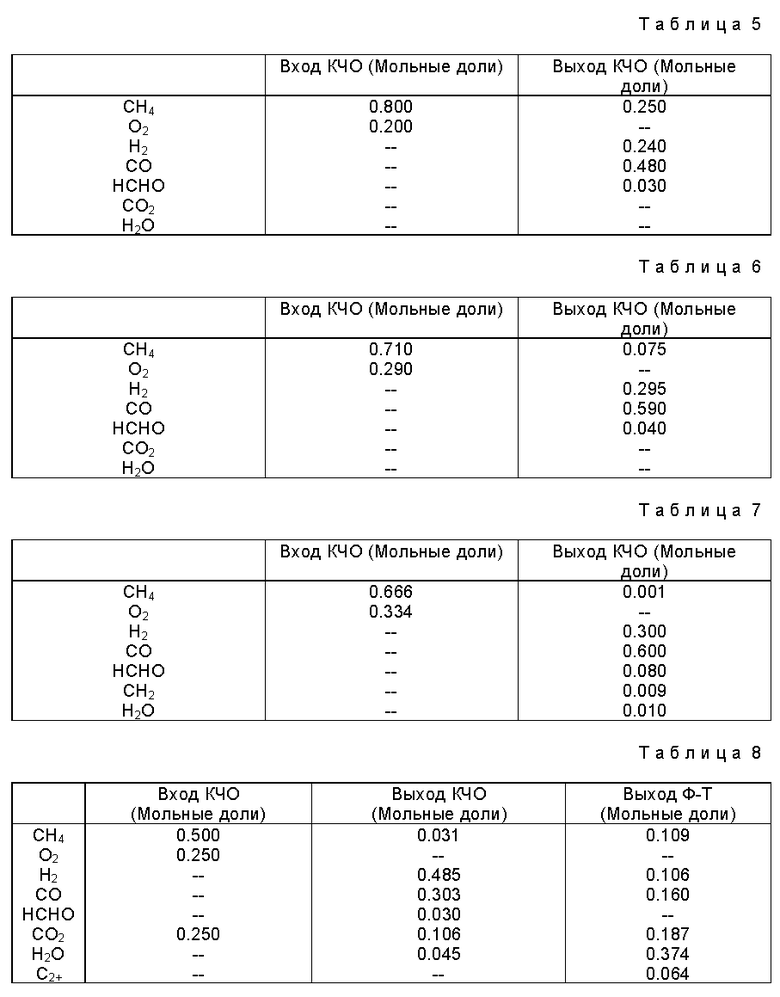
На фиг. 2 схематически показан объединенный способ синтеза метанола или смесей метанол-диметиловый эфир из природного газа через синтез-газ.
Природный газ (1) и кислород (2) поступают в реактор (3), в котором осуществляется каталитическое частичное окисление природного газа и образуются синтез-газ и формальдегид.
Формальдегид (4) может быть отделен от синтез-газов (5), которые поступают в реактор (20), где осуществляются синтезы метанола или смесей метанол-диметиловый эфир.
Выходящий продукт (21) направляется в разделяющее устройство (22), из которого выходят поток (23), содержащий метанол и кислородсодержащие продукты, и поток (24), содержащий метан и углеводороды с двумя или менее атомами углерода, причем последний поток направляется на повторную обработку в реактор (3).
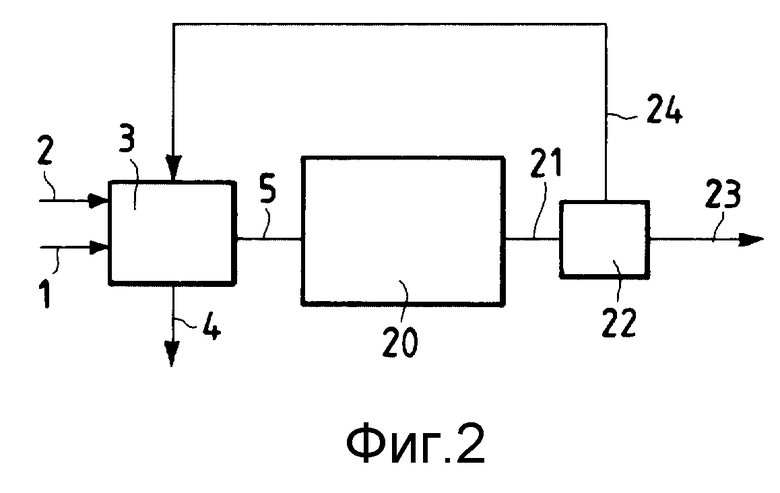
На фиг. 3 схематически показан объединенный способ синтеза метанола из природного газа через синтез-газ в условиях высокой производительности конверсии на проход.
Природный газ (1) и кислород (2) поступают в реактор (3), в котором осуществляется каталитическое частичное окисление природного газа и образуются синтез-газ и формальдегид.
Формальдегид (4) может быть отделен от синтез-газов (5), которые после отделения CO2 и H2O (7) в устройстве (6) поступают в реактор (30), в котором осуществляется синтез метанола.
Выходящий продукт (31) направляется в разделяющее устройство (32), из которого выходят поток (33), содержащий в основном метанол, и поток (34), содержащий метан, который направляется на повторную обработку в реактор (3).
Дешевизне этих способов способствует возможность отделения от конечных продуктов реакции непрореагировавших легких (C1 и C2) углеводородов и повторное их направление в устройство для КЧО.
Более подробно, в объединенном способе получения и использования синтез-газа в устройстве для КЧО можно применять смеси природного газа и кислорода или обогащенного воздуха, в которых мольные отношения O2/CH4 могут быть даже ниже 0.5, даже в отсутствие водяного пара. В способе КЧО по настоящему изобретению можно также использовать в условиях СВОС (сверхвысоких объемных скоростей) смеси CH4/O2/CO2, не содержащие водяной пар. Условия процесса таковы, что в устройстве для получения синтез-газа кислород подвергнется полной конверсии, в то время как в выходящем из реактора КЧО потоке могут оставаться значительные количества метана, в частности при отношении O2:CH4 менее 0.5.
Продукты реакции КЧО в основном состоят из смесей H2, CO и CH4 с малыми количествами H2O и CO2, при этом, побочным продуктом реакции является HCHO. После отделения формальдегида, который может быть возвращен на стадию каталитического частичного окисления, смеси, содержащие CO и H2, используются для синтеза метанола и/или диметилового эфира (ДИЭ) и/или углеводородов.
В том случае, когда в потоках, выходящих из устройства для получения синтез-газа, остаются большие количества непрореагировавшего метана, последний остается в качестве инертного вещества во время последующей стации синтеза углеводородов и/или кислородсодержащих продуктов, его легче отделить от более тяжелых продуктов реакции и возвратить на повторную переработку в устройство для КЧО.
Такие результаты очень трудно достичь в условиях высокого давления; напротив, удивительно, что было обнаружено то, что с помощью таких описанных выше способов можно добиться реакций и изменений в селективности при давлениях выше атмосферных. Если получение синтез-газа в условиях СВОС предназначено для синтеза метанола с высокими значениями производительности конверсии на проход, будут использованы условия реакции, при которых весь кислород расходуется, а присутствующие в синтез-газе CO2 и H2O будут удалены перед стадией гидрирования.
Результаты, полученные из опытных испытаний, описанных в последующих примерах, показывают, что в широком диапазоне условий эксперимента каталитическая система для реакции КЧО может быть описана уравнением [12] без образования воды и двуокиси углерода в качестве промежуточных продуктов по реакции [9] . Таким образом, высокие производительности конверсии могут быть достигнуты при низких температурах и в условиях высокой объемной скорости потому, что реакция [12] очень быстрая и является термодинамически выгодной в широком температурном диапазоне (в диапазоне температур от 25 до 800oC ее константа равновесия составляет около 1016) в то время, как реакции [10] и [11] медленные и термодинамически невыгодны при температурах ниже 750oC. Высокие выходы синтез-газа, достигаемые даже при низких температурах при использовании смесей CH4 и O2 с отношениями O2:CH4 < 0.5 (объем/объем), дают особые преимущества проведению реакций получения метанола или смесей метанол-диметиловый эфир с использованием способов с высокой производительностью конверсии на проход.
С целью лучшего иллюстрирования изобретения ниже приводятся несколько примеров, хотя понятно, что оно не ограничивается ими.
Пример 1.
Реакции КЧО и синтеза метанола при высоких значениях производительности конверсии на проход из полученных смесей синтез-газа и метанола проводили в двух реакторах при давлении 1.5 МПа.
В реакторе "А" осуществляли реакции КЧО при температуре 750oC и с величиной СЧСПГ 300000 ч-1. Поток горячих газов, выходящих из первого реактора с температурой 750oC, охлаждали с применением змеевика с протекающей внутри водой и направляли (после удаления небольших количеств водяного пара и CO2, образовавшихся во время синтеза с КЧО) в реактор "Б" с температурой 100oC, в котором проходит синтез метанола.
Смесь продуктов реакции анализировали как на выходе первого, так и на выходе второго реакторов, в обоих случаях с использованием газовой хроматографии.
Реактор, внутри которого проводят реакции КЧО, представляет собой керамическую глиноземную трубу, окруженную стальным цилиндром. Глиноземная труба обеспечивает химическую инертность стенок реактора, а стальная труба образует прочное тело, позволяющее проводить опытные испытания при давлениях выше атмосферных.
Реакционный газ, состоящий из CH4 и O2 (O2:CH4 = 0.2:0.8 объем/объем) проходит через каталитический слой (А), содержащий 0.5 г катализатора на основе Rh и Ru с временем контакта 10-2 секунд (СЧСПГ 300000 ч-1).
Благородные металлы нанесены на носитель, образованный альфа-глиноземом, привитым окисью кремния. Содержание Ph и Ru составляет соответственно 0.5% и 1% (по весу) материала. Носитель (глинозем, привитый двуокисью кремния) получали реакциями конденсации между реакционноспособными группами на поверхности глинозема и тетраэтилсиликатом (ТЭС) с последующим гидролизом и прокаливанием. Благородные металлы наносили с использованием углеводородных растворов Rh4(CO)12 и Ru3(CO)12 в соответствии с процедурами, описанными в UK Patent N 2240284, UK Publ. N 2247465, IT-M192 A 001 953, UK Publ. N 2274284.
Смесь продуктов, полученных на стадии КЧО, входит в шламовый реактор "Б" для синтеза метанола. Каталитическая система в шламовом реакторе была приготовлена с использованием в качестве исходных веществ CuCl и MeONa путем проведения процесса в соответствии с процедурами, описанными в EP-375,071. Соль меди и алкоксид щелочного металла помещали в реактор с покрывающим слоем атмосферы азота. Затем добавляли растворитель (90 мл тщательно осушенного анизола) в присутствии метанола (40 ммоль). Молярную концентрацию алкоксида поддерживали на уровне примерно 2 М, концентрация соли меди составляла 0.06 М. Во время стадии начала процесса реактор был герметизирован и заполнен при 15 атм смесью CO и H2 (H2:CO = 2:1 объем/объем), а температура повышена до 100oC перед тем, как в него поступала реакционная смесь из реактора КЧО. В таблице 1 приведены данные по составу смесей продуктов на обеих стадиях реакции.
Производительность конверсии синтез-газа на стадии синтеза метанола составляет 90%, а селективность по метанолу - 98%. Производительность системы лимитируется стадией синтеза метанола и поэтому в результате составляет 65 г MeOH /ч-л объема реактора.
Пример 2.
В этом случае стадию получения синтез-газа осуществляли в реакторе "А" при 1.5 МПа, при температуре 750oC на монолитном катализаторе, содержащем Rh и Ru. Смесь реагентов (СЧСПГ = 300000 ч-1) содержала метан и кислород во взаимном отношении O2:CH4 = 0.29:0.71. Стадию гидрирования окиси углерода с целью получения метанола в присутствии непрореагировавшего метана осуществляли путем пропускания прореагировавшего потока через шламовый реактор при 1.0 МПа и температуре 95oC.
Монолитный катализатор получали путем опускания монолитного куска глинозема в раствор гидроксида алюминия. Слой гидроксида покрывает монолитный кусок, и после высушивания и прокаливания он превращается в пористый гидроксидный слой. После такой обработки площадь поверхности монолитного куска составляет 12 м2/г (этот способ называется в соответствующей технической литературе "wach-coating" process - способ "промывного покрытия"). Монолитный кусок пропитывали в углеводородном растворе Rh4(CO)12 и Ru3(CO)12 (гексан, Rh: Ru:Ir = 0.1:0.5:0.5 моль/моль) в течение 2 часов. В этих условиях происходят реакции диссоциативной хемосорбции кластеров, приводящие к покрытию поверхности монолитного куска монослоем благородных металлов, что было подтверждено количественным анализом конечного содержания металлов (0.08% Rh, 0.4% Ru, 0.3% Ir).
Катализатор для реакций синтезов метанола был приготовлен смешиванием CuCl (6 ммоль), CH3ONa (80 ммоль), метилформиата (50 ммоль) с 90 мл анизола. Эксперименты проводились в соответствии с теми же рабочими процедурами, что были описаны в вышеприведенном примере 1; полученные результаты приводятся в таблице 2.
Конверсия синтез-газа в стадии синтеза метанола составляла 92%, а селективность по метанолу - 98%.
Пример 3.
Реакции получения синтез-газа проводили в реакторе "А" над каталитическим слоем при давлении 3.0 МПа (СЧСПГ = 400000 ч-1), температура на выходе 750oC, O2:CH4 = 0.41 (объем/объем). Полученный синтез-газ, содержащий более 10% непрореагировавшего метана, был использован во втором реакторе "Б" для осуществления реакций Ф-Т синтеза углеводородов. Давление в реакторе "Б" поддерживалось на уровне 3 МПа, а температура - 300oC.
В синтезе с КЧО использовался монолитный катализатор, приготовленный по процедуре, описанной в примере 2. Катализатор для синтеза Ф-Т был приготовлен путем последовательных импрегнаций гамма-глинозема (площадь поверхности 150 м2/г) до появления признаков влажности. Первая импрегнация осуществлялась водным раствором нитрата кобальта. После высушивания при 115oC катализатор подвергали второй импрегнации водным раствором нитрата рутения, и затем - второй процедуре высушивания. Третью стадию импрегнации осуществляли водным раствором карбоната калия. После дальнейшего высушивания катализатор прокаливали до 350oC. Конечный катализатор содержал 18% кобальта, 2.5% рутения и 1% калия. Каталитическому испытанию предшествовала термическая восстанавливающая обработка при 350oC, во время которой через реакторы "А" и "Б" продували поток азота, содержащий 25% водорода. Составы реакционных смесей и продуктов обеих стадий реакции приведены в таблице 3.
Пример 4.
Повторялись процедуры, описанные в примере 3, с использованием того же катализатора для реакций КЧО и соответственно того же катализатора для реакций синтеза Ф-Т; однако, в данном случае, смесь метана и кислорода, подаваемая на вход реактора "А" для КЧО, имела отношение O2:CH4 = 0.55. Полученные результаты приведены в таблице 4.
Примеры 5-7.
Повторяли эксперименты, описанные в примерах 1, 2 и 4, с использованием в первом реакторе КЧО в качестве катализатора сетки из платино-родиевой проволоки, содержащей 10% родия по весу. Указанная сетка имеет такие же характеристики, как и проволочные сетки, применяемые при окислении аммиака в азотную кислоту, и изготовлена из металлических проволок диаметром 0.076 мм. Поскольку оказалось, что родий особенно активен в реакциях КЧО и особенно инертен в реакциях образования угля, сетки модифицировали путем электрохимического нанесения на их поверхность слоя металлического родия из водных растворов нитрата родия. Обнаружилась активность полученного материала в реакциях КЧО, проводимых в условиях СВОС, с селективностями по CO и H2 более 95% в условиях реакции, описанных в примерах 1-4, но с более низкой селективностью по формальдегиду. В следующих таблицах 5, 6 и 7 приведены результаты, относящиеся к первой стадии реакции, в которой получают смеси синтез-газа.
Пример 8.
В этом случае во время первого прохода получения синтез-газа использовались катализаторы из примера 2, но смеси реагентов составляли CH4:O2:CO2 = 1: 0.5:0.5; в то же время, на следующей стадии синтеза Ф-Т использовался катализатор, описанный в примере 3. На стадии КЧО использовались следующие условия процесса: СЧСПГ = 400000 ч-1, P = 3 МПа, на выходе реактора Т = 750oC. Для реактора синтеза Ф-Т использовались следующие условия: СЧСПГ = 1500 ч-1, P = 3 МПа, T = 300oC. Полученные результаты приведены в таблице 8.

Способ каталитического частичного окисления природного газа с целью получения синтез-газа и формальдегида, объединенный с процессами гидрирования образующегося CO, такими как синтезы Фишера-Тропша и метанола. Такое окисление осуществляют с помощью катализатора, образованного одним или более соединением металлов платиновой группы, который имеет форму проволочных сеток или нанесен на носитель, изготовленный из неорганических соединений, таким образом, что содержание металла или металлов платиновой группы в весовых процентах лежит в диапазоне 0.1 - 20% от общего веса катализатора и носителя, путем проведения процесса при температурах в диапазоне 300 - 950oC, при давлениях в диапазоне 0,05 -5 МПа, при объемных скоростях в диапазоне 20000 -150000 ч-1. 3 с. и 4 з.п. ф-лы, 3 ил., 8 табл.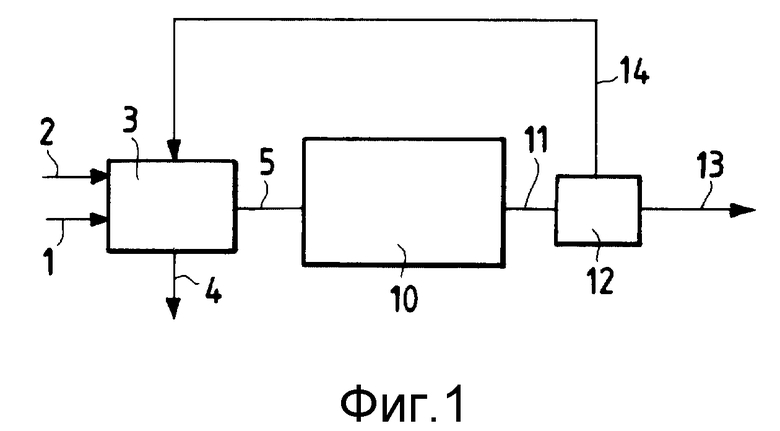
| СПОСОБ ВЫДЕЛЕНИЯ КРИСТАЛЛОГИДРАТА НИТРАТА КАЛЬЦИЯ | 2003 |
|
RU2240284C1 |
| КАТАЛИТИЧЕСКАЯ СИСТЕМА ДЛЯ ЖИДКОФАЗНОГО ПОЛУЧЕНИЯ МЕТАНОЛА ИЗ СИНТЕЗ-ГАЗА И СПОСОБ ПОЛУЧЕНИЯ МЕТАНОЛА | 1992 |
|
RU2060820C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОПИТОЧНЫХ РАСТВОРОВ для ИЗГОТОВЛЕНИЯ СЛОИСТЫХ ПЛАСТИКОВ | 0 |
|
SU285228A1 |
| Аналого-цифровой преобразователь поразрядного уравновешивания | 1974 |
|
SU504981A1 |
| US 4935395 A, 19.06.90 | |||
| СХЕМА РЕГУЛИРОВАНИЯ НАПРЯЖЕНИЯ ДЛЯ ИНТЕГРАЛЬНЫХ СХЕМ ЧИП-КАРТ | 2001 |
|
RU2247465C1 |
| УСТРОЙСТВО для ТРЕНИРОВКИ мышц КУЛЬТЕЙ БЕДЕР | 0 |
|
SU375071A1 |
| J.R.Rostrup - Nilson, Catalysis Science and Technology, T.5, Chapter 1 | |||
| Hydrocarben Processing, 1990, c.99; J.Bogild Hansen, F.Joensen, Stud | |||
| Surf | |||
| Sc | |||
| Catal., 1991, t.61, c.457 | |||
| D.A.Hickman and L.D.Schmidt | |||
| Science, 1993, c.259, 343. | |||
Авторы
Даты
1999-02-20—Публикация
1994-08-26—Подача