Изобретение относится к биотехнологии, в частности к использованию аминокислотных и дипептидных производных фуллерена в качестве стимуляторов иммунного ответа - адъювантов, и может быть использовано в научно-исследовательской практике, а также в биологической промышленности при разработке и производстве вакцин.
Известно, что в качестве адъювантов применяются микроорганизмы, продукты их метаболизма, их суспензии в минеральных маслах (адъювант Фрейнда), гидроокись алюминия, нерастворимые неорганические соли, сапонины, а также экстракты растительного происхождения гидрофобной природы.
Однако известно также, что иммунизация с адъювантами, представляющими собой водно-масляные эмульсии и суспензии, часто приводит к нежелательным осложнениям, таким как местные инфильтрации, изъязвления и аллергические реакции [1 - 3].
Описано использование низкомолекулярного растворимого адъюванта, синтетического фрагмента пептидогликана из стенки микобактерий - N-ацетил-мурамил-Л-аланил-Д-изо-глутамина (МДП) [4].
Использование водорастворимого адъюванта, МДП, исключает те нежелательные последствия, которые проявляются при иммунизации адъювантами на основе водно-масляных эмульсий и суспензий, однако имеет ряд недостатков иного характера, а именно наблюдается пирогенность [5] и нейрофармакологический эффект [3], стимулирующая активность проявляется лишь при относительно высоких дозах, причем для некоторых антигенов требуется ковалентное присоединение МДП к молекуле антигена. Кроме того, этот адъювант лишь заменяет бактериальный компонент в адъюванте Фрейнда, но не отменяет применение масляного компонента, и для ряда антигенов его применение неэффективно [6].
Предлагаемое изобретение относится к использованию описанных ранее соединений, фуллереновых производных аминокислот и дипептидов общей формулы I в качестве адъювантов
C60-X,
где С60 - фуллереновое ядро;
X = NH-СHR-COOH, NH-(CH2)n-COOH,
NH-CHR-CO-NH-CHR-COOH,
где n = от 2 до 6, R - боковой радикал природной аминокислоты.
Производные фуллерена общей формулы I представляют собой относительно новый класс органических соединений. Иx синтезируют непосредственно присоединением остатков аминокислот или дипептидов к фуллереновому ядру [7]. Они представляют собой твердые порошкообразные вещества темно-коричневого цвета, растворимые в воде. Их биологические свойства в настоящее время широко изучаются.
Оценку адъювантных свойств соединений I осуществляют в две стадии. На 1-й стадии оценивают их антигенные свойства. Для этого получают гипериммунную сыворотку, иммунизируя кроликов и мышей препаратами различных производных фуллерена совместно с сильным адъювантом Фрейнда. Анализ сывороток проводят по стандартной методике методом ИФА.
На 2-й стадии определяют адъювантные свойства соединений I. Для этого одну группу мышей иммунизируют модельным антигеном - яичным альбумином (Ova), другие несколько групп - смесью Ova с различными соединениями I (Ova-I).
Для выявления IgG - антител используют меченый пероксидазой анти-IgG мыши (Sigma). За титр принимается величина, обратная разведению образца, оптическая плотность (ОП) которого равна ОП образца нормальной сыворотки (перед иммунизацией), разведенного в 50 раз (ОП нормальной сыворотки ≤ 0.2, что достигается подбором условий ИФА). Эффективность адъюванта определяют как отношение титра анти-Ova-I-сыворотки к титру анти-Ova-сыворотки.
Изобретение иллюстрируется нижеследующими примерами.
I. Определение иммуногенности.
Получение сывороток.
Пример 1.
Для приготовления гипериммунной сыворотки 100 мкг препарата C60-Ser растворяют в 0.5 мл 0.05 М фосфатного буфера с pH 7.4. Первую иммунизацию проводят в полном адъюванте Фрейнда (Gibco, 1:1 об/об), последующие три иммунизации проводят в неполном адъюванте Фрейнда. Кролику породы шиншилла подкожно вводят препараты с двухнедельным интервалом. Забор крови осуществляют в те же интервалы, и полученные из крови образцы сывороток анализируют на антитела к C60-Ser иммуноферментным методом.
Пример 2.
Способ осуществляют как указано в примере 1, но в качестве антигена используют C60-Ala.
Пример 3.
Способ осуществляют как указано в примерах 1 и 2, но в качестве антигена для получения антисыворотки используют дипептидное производное C60-Ala-Ala.
II. Проведение иммуноферментного анализа.
Для проведения ИФА производные фуллерена, указанные в примерах 1 - 3, растворяют в 60 мМ карбонат-бикарбонатном буфере (pH 9.6) и наносят на планшеты GREINER в концентрации 20 мкг/мл. После инкубации в течение 1.5 ч при 37oC планшеты отмывают от несвязавшихся компонентов фосфатно-солевым буфером (ФСБ) pH 7.4 с 0.05% твин-20. Тестируемые сыворотки, полученные соответственно по примерам 1 - 3, разводят в 50 раз раствором 0.5% бычьего сывороточного альбумина (Sigma) с 0.05% твин-20 в ФСБ и инкубируют с адсорбированными на планшете препаратами в течение 30 мин при 37oC. После инкубации планшеты 4 раза отмывают раствором ФСБ/0.05% твин-20. Раствор конъюгата анти-lgG кролика с пероксидазой (Sigma) в рабочем разведении инкубируют в лунках планшета 30 мин при 37oC и проводят аналогичную отмывку. Для выявления иммунных комплексов используют проявляющую смесь: 4 мг о-фенилендиамина/10 мл 0.1 М цитратфосфатного буфера/80 мкл 3% H2O2. Реакцию останавливают 2N H2SO4, и оптическую плотность в лунках измеряют при 492 нм, используя автоматический сканер Multiscan Plus (Flow Laboratories, Швейцария). Величину фонового поглощения (Cut off) оценивают как среднее значение величины оптической плотности для нормальных кроличьих сывороток (n=5)+3SD. Титр сывороток оценивали при двоичном разведении сывороток, первичное разведение составляло 1:50. Данные приведены в таблице 1.
Как показывают 4 серии иммунизаций, приведенных в таблице 1, аминокислотные и дипептидные производные фуллерена не обладают антигенными свойствами, что, вероятно, обусловлено его особой чужеродностью, т.е. резким отличием их структур от структур природных антигенов и отсутствием подходящих клонов лимфоцитов в природном репертуаре.
III. Определение адъювантных свойств.
1. Получение сывороток.
Пример 1.
Одну группу мышей (7 животных) породы Fl (CBA/BALB/c) иммунизируют внутрибрюшинно 3-кратно через 3-недельные интервалы, вводя в каждую мышь 30 μг Ova в 0.5 мл 0.05 М фосфатного буфера с pH 7.4.
Другую группу мышей (7 животных) иммунизируют аналогичным способом, однако используя на каждую мышь 10 μг Ova с 330 μг C60-Ser /соотношение 3: 100 (в/в)/.
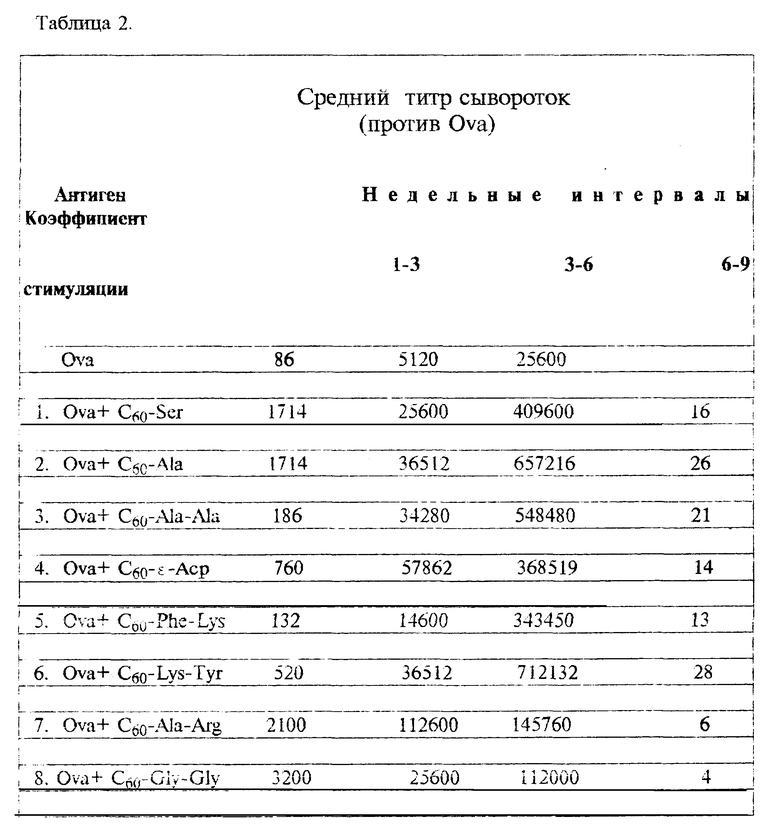
Забор крови осуществляют в те же 3-недельные интервалы, и полученные из крови образцы сывороток анализируют в ИФА, как описано в п. II. Для выявления IgG-антител используют меченый пероксилазой анти-IgG мыши (Sigma). Полученные результаты приведены в таблице 2.
Пример 2.
Способ осуществляют как описано в примере III.1, но в качестве антигена используют смесь 10 μг Ova с 30 μг C60-Ala /весовое соотношение 1:3/.
Пример 3.
Способ осуществляют как описано в примере III.1, но в качестве антигена используют смесь 15 μг Ova с 105 μг C60-Ala-Ala /весовое соотношение 1:7/.
Пример 4.
Способ осуществляют как описано в примере III.1, но в качестве антигена используют смесь 10 μг Ova с 200 μг C60- ε -аминокапроновая кислота (C60-ε-Acp) /весовое соотношение 1:20/.
Пример 5.
Способ осуществляют как описано в примере III.1, 2, но в качестве антигена используют смесь 20 μг Ova с 260 μг C60-Phe-Lys /соотношение 1:13/.
Пример 6.
Способ осуществляют как описано в примере III.1, 2, но в качестве антигена используют смесь 20 μг Ova с 60 μг C60-Lys-Tyr /соотношение 1:3/.
Пример 7.
Способ осуществляют как описано в примере III.1, 2, но в качестве антигена используют смесь 45 μг Ova с 300 μг C60-Ala-Arg /соотношение 3:20/.
Пример 8.
Способ осуществляют как описано в примере III.1, 2, но в качестве антигена используют смесь 20 μг Ova с 100 μг C60-Lys-Ala /соотношение 1:5/.
Пример 9.
Способ осуществляют как описано в примерах III.1, 2, но в качестве антигена используют смесь 20 μг Ova с 120 μг C60-Ala-Thr при соотношении 1:6.
Определение токсичности.
Эксперименты с эритроцитами человека показали, что даже в высоких дозах - 400 мкМ - они не обладают гемолитическими свойствами, клетки в процессе инкубации не агглюцинируют и их морфология не изменяется. Введение мышам высокой дозы этих соединений (80 мг/кг) не влияет на жизнеспособность и поведение мышей в течение 6 месяцев.
Таким образом, заявляемые в качестве адъювантов фуллереновые производные аминокислот и дипептидов, как видно из таблицы 2, хорошо стимулируют иммунный ответ на белковый антиген. Как показало тестированиеб указанные производные не обладают собственной иммуногеностью, гемолитическими свойствами, они нетоксичны при введении в высоких дозах.
Cписок литературы
1. Иммунологические адъюванты. Доклад научной группы ВОЗ. М., 1978.
2. Murhay R., Cohen P. and Hardegree M.C.//Ann. Allergy, 1972, 30, 146.
3. Chedid L. //Ann. Inst. Pasteur/Lmmunol., 1985, 136 D, 283 - 291.
4. Merser C. , Sinay P. and Adam A.// Biochem. Biophys. Res. Commun., 1975, 66, 1316 - 1322.
5. Kotani S., Watanabe Y., Shimono T., Harada K., Shiba T., Kusumoto S., Yokogawa K, and Taniguchi M.//Biken J., 1976, 19, 9 - 13.
6. Иванов Б.Б. Создание иммунопотенциирующих систем для пептидных экспериментальных вакцин. Канд. диссертация, 1992.
7. В.С.Романова, В.А.Цыряпкин, Ю.А.Ляховецкий, З.Н.Парнес, М.Е.Вольпин// Изв. РАН, сер. Xим., 1994, 1151.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФУЛЛЕРЕНОВОЕ ПРОИЗВОДНОЕ ГЛИКОПЕПТИДА, ОБЛАДАЮЩЕЕ АДЪЮВАНТНОЙ АКТИВНОСТЬЮ | 1997 |
|
RU2124022C1 |
| СРЕДСТВО ДЛЯ ИНГИБИРОВАНИЯ ВИЧ И ЦМВ-ИНФЕКЦИЙ И СПОСОБ ИХ ИНГИБИРОВАНИЯ | 2002 |
|
RU2196602C1 |
| ИММУНОГЕН ДЛЯ ПРЕДОТВРАЩЕНИЯ ИЛИ ЛЕЧЕНИЯ СЕМЕЙНОЙ ЛОБНО-ВИСОЧНОЙ ДЕМЕНЦИИ (ЛВД) И/ИЛИ БОКОВОГО АМИОТРОФИЧЕСКОГО СКЛЕРОЗА (БАС) | 2020 |
|
RU2833931C2 |
| СПОСОБ КОНЦЕНТРИРОВАНИЯ ВИРУСА | 1997 |
|
RU2130069C1 |
| АНТИГЕННАЯ КОМПОЗИЦИЯ ДЛЯ ИНДУЦИРОВАНИЯ ОТВЕТА ЦИТОТОКСИЧЕСКИХ Т-ЛИМФОЦИТОВ, СПОСОБ ИНДУЦИРОВАНИЯ И СПОСОБ ЛЕЧЕНИЯ БОЛЕЗНИ | 1992 |
|
RU2129439C1 |
| ВАКЦИНА ПРОТИВ ГРИППА | 2014 |
|
RU2546861C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ И СПОСОБ ЛЕЧЕНИЯ ОНКОЛОГИЧЕСКОГО ЗАБОЛЕВАНИЯ С ЕЕ ИСПОЛЬЗОВАНИЕМ | 2005 |
|
RU2323722C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПРЕДЕЛЬНО ДОПУСТИМОЙ АНТИГЕННОЙ НАГРУЗКИ, СТИМУЛИРУЮЩЕЙ ПРОДУКЦИЮ ГУМОРАЛЬНЫХ АНТИТЕЛ | 2008 |
|
RU2371196C1 |
| ИММУНОСТИМУЛИРУЮЩИЕ КОМПОЗИЦИИ | 2016 |
|
RU2732118C2 |
| ПРИМЕНЕНИЕ ПЕПТИДА, УСИЛИВАЮЩЕГО СЕКРЕЦИЮ СОМАТОТРОПНОГО ГОРМОНА, В КАЧЕСТВЕ АДЪЮВАНТА ВАКЦИНЫ | 2017 |
|
RU2768134C2 |


Изобретение относится к биотехнологии, в частности к использованию аминокислотных и дипептидных производных фуллерена в качестве стимуляторов иммунного ответа - адъювантов, и может быть использовано в биологической промышленности при разработке и производстве вакцин. Изобретение относится к использованию описанных ранее соединений, фуллереновых производных аминокислот и дипептидов общей формулы I в качестве адъювантов: С60-X, где С60 - фуллереновое ядро; X=NH-CHR-COOH, NH-(CH2)n-COOH, NH-CHR-CO-NH-CHR-COOH, где n = 2 - 6; R - боковой радикал природной аминокислоты. Изобретение обеспечивает при экспериментах с эритроцитами человека возможность использовать высокие дозы - 400 мкМ, но даже они не обладают гемолитическими свойствами, клетки в процессе инкубации не агглюцинируют и их морфология не изменяется. Введение мышам высокой дозы этих соединений - 80 мг/кг - не влияет на жизнеспособность и поведение мышей в течение 6 месяцев. 2 табл.
Применение фуллереновых производных аминокислот и дипептидов общей формулы
C60-X,
где C60 - фуллереновое ядро,
X = NH - CHR - COOH, NH - (CH2)nCOOH, NH - CHR - CO - NH - CHR - COOH;
n = от 2 до 6;
R - боковой радикал природной аминокислоты,
в качестве адъювантов.
| Иммунологические адъюванты | |||
| Доклад научной группы | |||
| BОЗ М., 1978, с.3 и далее | |||
| Романова В.С., Цыряпкин В.А., Ляховецкий Ю.А., Парнес З.Н., Вольпин М.Е | |||
| Изв | |||
| РАН, сер.Химия, 1994, 1151 | |||
| US 4501733 A, 26.02.85. |
Авторы
Даты
1999-04-27—Публикация
1997-04-10—Подача