Изобретение относится к комплексам платины, обладающим противоопухолевой активностью, к способам их получения и к фармацевтическим композициям, содержащим указанные комплексы.
Использование комплексов патины, таких как цисплатин и карбоплатин, в противораковой химиотерапии хорошо известно специалистам. Так, например, ряд комплексов пластины, таких как цисплатин, используют для лечения рака яичка, рака яичника, опухолях головы и шеи и плоскоклеточного рака легких. Однако лечение цисплатином может приводить к тяжелой нефротоксичности. Другим недостатком этого средства является приобретение устойчивости к нему, в результате чего опухоль становится невосприимчивой к лечению данным лекарственным препаратом.
Полагают, что, в основном, биологическая активность комплексных соединений патины, таких как цисплатин, обусловлена ковалентным взаимодействием с ДНК. В частности, цисплатин индуцирует образование на ДНК аддуктов, включая моноденатные аддукты и бидентатные аддукты, такие как внутрицепочечные перекрестные сшивки GG или AG, и GG (Reedijk et al., Structure and Bonding, (1987) 67, 53-89). В меньшей степени, цисплатин также приводит к образованию внутрицепочечных перекрестных сшивок GG и перекрестных сшивок ДНК-белок (Rahmouni et al., Biochemistry, (1987) 26, 7229-7234). Такие повреждения ДНК проводят к конформационным изменениям, которые отражаются на скручивании и локальном "расплетании" ДНК. Имеется мнение, что такие повреждения ДНК ингибируют активность различных ДНК-полимеров (Vallan et al., Nuel. Acids.Res. , (1988) 16, 4407-4418; Pinto et al., Proc, Natl. Acad.Sci., (1985) 82, 4616-4619 и Gralla et al., Cancer Res., (1987) 47, 5092-5096). Было также показано, что внутрицепочечные перекрестные сшивки между двумя соседними гуаниновыми основаниями также ингибируют действие РНК-полимеразы (Lemaire et al. , Proc. Natl. Acad. Sci. (1991) 88, 1982-1985). Отсюда можно сделать вывод, что цитотоксическое действие цисплатина, по всей вероятности, обусловлено комплексным эффектом указанных повреждений ДНК и не является результатом какого-либо конкретного повреждения.
Комплексы моно(платины) и бис(платины), содержащие, соответственно, один или два атома платины, известны специалистам и описаны в патентах США NN 4225529, 4250189, 4533502, 4565884, 4571335 и 4797393. Так, например, комплексы моно(платины) представляют собой мономерные хлораминовые соединения платины (11) с плоско-квадратной конфигурацией и координационным числом 4. Относительное число хлоридных и аммиачных групп в таких соединениях может варьироваться, а поэтому указанные соединения могут быть представлены общей формулой.
[PtClm(NH3)4-m](2-m)+
Таким образом, структура этих соединений может варьироваться от [Pt(NH3)4] 2+, где m= 0, до PtCl2- 4, где m=4. Поскольку Cl является более лабильным в отношении замещения, чем аммиак, то комплексы [PtCl2(NH3)2] и [PtCl2(NH3)3] Cl считаются бифункциональными и монофункциональными, соответственно, где префиксы "би" и "моно" относятся к числу уходящих лигандов. Заряд комплекса определяют исходя из того, что катион Pt(11) имеет формальный заряд +2, а поэтому для нейтрализации заряда требует отрицательного заряда -2. Так, например, если m=0, то нейтрализация обеспечивается присутствием двух хлорид-анионов во внешней координационной сфере.
Образование связи между платиной и аммиаком, который является нейтральным лигандом, модно описать как передачу электронной пары от NH3 на свободные орбитали атома (Pt(11). Таким образом, обобщения электронной пары между Pt и NH3-группой не происходит. Поскольку такое обобщение электронов отсутствует, число нейтральных лигандов не влияет на полный заряд в координационной сфере Pt. Таким образом, формально [Pt(NH3)4]2+ представляет собой двухзарядный катион, который для нейтрализации комплекса требует присутствия некоординирующего аниона, либо анионов, или противоионов, имеющих полный отрицательный заряд 2-. Например, нейтрализация комплекса может обеспечиваться двумя однозарядными анионами (например, NO- 3, Cl-, PF- 6, BF- 4 и монокарбоксилатами общей формулы RCoo-) или одним двухзарядным анионом (например, SO2- 4, дикарбоксилатами, имеющими общую формулу [R(COO)2]-2). Исходя из этих соображений, [PtCl2(NH3)2] является нейтральным комплексом.
Этот же самый принцип может быть применен не только к аммиаку, но и также к нейтральным лигандам, таким как первичные или вторичные амины.
Следует отметить, что отрицательно заряженные лиганды, такие как Cl-, либо могут образовывать координационную связь (т.е., связь Pt-Cl), либо могут действовать как противоион без какой-либо необходимости образовать ковалентную связь. Точная форма, которую имеют анионы, такие как CL-, в данном комплексе платины зависит как от конкретно рассматриваемой теории (кинетической или термодинамической), так и от конкретного метода синтеза, используемого для получения данного комплекса (например, от степени реакции, кислотности и концентрации определенного аниона, такого как CI-, содержащегося в реакционной смеси). Аналогичные рассуждения могут быть также отнесены и к другим отрицательно заряженным или нейтральным лигандам.
Тот факт, что полный заряд моноплатиновых комплексов зависит от относительного числа нейтральных лигандов и лигандов-анионов, связанных с металлом Pt(11), в равной степени относится как к многоядерным комплексам (которые содержат более, чем одну координационную сферу Pt(11)), так и к Pt(IV)-содержащим комплексам, где степень окисленности атома платины составляет +4. Так, например, двухъядерные комплексы, где две эквивалентные координационные сферы Pt(11) связаны диаминовой мостиковой группой, могут быть представлены общей формулой
[PtClm(NH3)3-m)2 (диамин)]2(2-m)+.
Таким образом, если m=2 и имеются две бифункциональные координационные сферы, то соединение является нейтральным. В противоположность этому, если m= 1, то отсутствуют монофункциональные координационные сферы, а атом платины, который имеет формальный заряд 2+, должен быть уравновешен одним или несколькими противоионами, имеющими суммарный заряд -2.
Примеры трехъядерных комплексов платины (называемых также комплексами три-платины) были недавно описаны в литературе (Yun Qu et al., Inorg.Chem., 32, 2591-2593 (1993)). Эти соединения, в которых лиганды имеют цис-конфигурацию, являются нейтральными комплексами или комплексами, имеющими суммарный заряд +2, и могут быть представлены следующими общими формулами: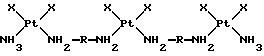
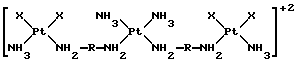
где X представляет собой лабильный лиганд (такой, как атом хлора);
R представляет собой алкиленовую цепь.
Исходя из вышеуказанного очевидно, что в случае, если комплексы имеют суммарный заряд +2, то этот заряд локализуется на центральном атоме платины, связанном с четырьмя нейтральными лигандами, тогда как два периферических атома платины являются формально нейтральными и, как описано выше, бифункциональными. Было высказано предположение, что указанные комплексы обладают противоопухолевой активностью, однако, это предположение не было подтверждено экспериментально.
Настоящее изобретение относится к три-платиновым комплексам, где три атома платины связаны диамоновыми цепями и где вокруг центрального атома платины координировано четыре нейтральных лиганда, а вокруг каждого из двух периферических атомов платины координировано три нейтральных лиганда и один лиганд, имеющий заряд -1.
Поэтому, соединения настоящего изобретения отличаются от соединений прототипа тем, что их полный заряд составляет +4, а в частности, центральный атом платины имеет формальный заряд +2, а каждый из двух периферических атомов платины имеет формальный заряд +1.
Кроме того, как видно из вышеуказанного, оба периферических атома платины являются монофункциональными.
Другое отличие от три-платиновых комплексов прототипов заключается в том, что лиганды в соединениях настоящего изобретения присутствуют в транс-конфигурации.
Более конкретно, настоящее изобретение относится к триплатиновым комплексам формулы 1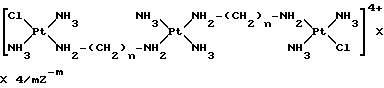
где n является целым числом от 2 до 7 включительно;
Z-m представляет собой анион, выбранный из хлорида, бромида, иодида, нитрата и сульфата (m=2);
m= 1 или 2.
Предпочтительными соединениями формулы 1 являются соединения, в которых n=6.
Особенно предпочтительными соединениями формулы 1 являются соединения, в которых n=6, Z-m представляет собой анион, такой как хлорид или нитрат, а m = 1.
Настоящее изобретение также относится к способам получения соединений формулы 1.
Способ получения соединений формулы 1 предусматривает синтез промежуточного соединения III исходя из транс-платины (предварительно активированной путем замещения атома хлора диметилформамидом) посредством реакции с амином формулы II, как показано на следующей схеме: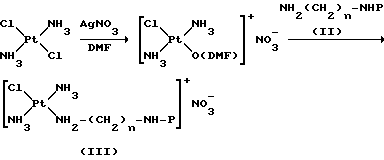
где P является подходящей стандартной защитной группой, такой как трет-бутоксикарбонил или п-метоксибензилоксикарбонил;
n определено выше.
Из промежуточного соединения формулы III после отщепления защитной группы P получают промежуточное соединение формулы IV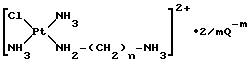
где n определено выше;
Q-m представляет собой противоион, тип которого зависит от условий отщепления группы P. Например, если P является трет-бутоксикарбонильной группой, то Q-m может быть хлорид-анионом или трифторацетатанионом.
Затем промежуточное соединение (IV) превращают в промежуточное соединение (V)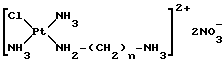
где n определено выше,
посредством обменной реакции между ионом Q-m и нитрат-ионом.
Указанная обменная реакция, в том случае, когда Q-m является хлорид-анионом, может быть осуществлена в присутствии нитрата серебра и в растворителе, таком как вода или спирты (метанол, этанол).
Затем, промежуточное соединение (V) подвергают реакции с 0,5 моль транс-платины, предварительно активированной путем замещения обоих атомов хлора двумя молекулами диметилформамида, в результате чего получают соединения формулы 1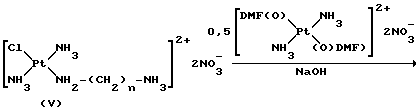
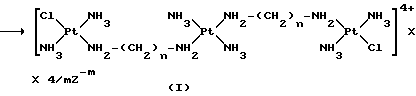
где Z-m представляет собой нитрат-анион.
Указанные соединения могут быть затем превращены в соединения формулы 1, где Z-m представляет собой галогенид или сульфат, с помощью стандартных обменных реакций, широко описанных в литературе, таких как обработка галогенидом или сульфатом щелочного или щелочноземельного металла. Альтернативно соединения формулы 1, в которых Z-m является сульфат-анионом, могут быть получены из соответствующих соединений формулы 1, где Z-m является галогенидом, путем обработки сульфатом серебра.
Предпочтительный способ получения соединений формулы 1, где Z-m является хлоридом, из соединений формулы 1, где Z-m является нитратом, предусматривает реакцию этих соединений с молярным избытком соляной кислоты при температуре в пределах от 0 до 50oC.
Другой способ получения соединений формулы I заключается в том, что сначала два моль амина формулы II подвергают реакции с транс-платиной, предварительно активированной путем замещения двух атомов хлора двумя молекулами диметилформамида, в результате чего получают промежуточное соединение формулы VI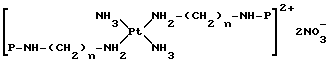
где P имеет значения, определенные выше.
После отщепления группы P получают промежуточное соединение формулы VII, где Q-m определен выше, которое затем превращают в промежуточное соединение формулы VIII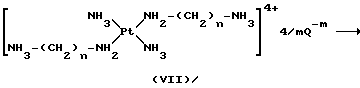
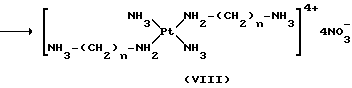
Такое превращение осуществляют с помощью обменной реакции между ионом Q-m и нитрат-ионом. Если Q-m является хлорид-анионом, то эта реакция может быть проведена в присутствии нитрата серебра и в растворителях, таких как вода или спирты (метанол, этанол).
Затем промежуточное соединение (VIII) подвергают реакции с двумя моль транс-платины, предварительно активированной путем замещения атома хлора молекулой диметилформамида, в результате чего получают соединение формулы I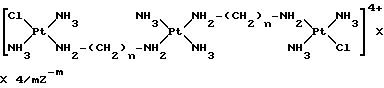
где Z-m является нитрат-анионом.
Указанные соединения могут быть затем превращены в соединения формулы I, где Z-m является галогенидом или сульфатом, с помощью стандартных обменных реакций, широко описанных в литературе, например, таких как обработка галогенидом или сульфатом щелочного или щелочноземельного металла. Альтернативно соединения формулы I, в которых Z-m является сульфат-анионом, могут быть получены из соответствующих соединений формулы I, в которых Z-m является галогенидом, путем обработки сульфатом серебра.
Предпочтительный способ получения соединений формулы I, где Z-m является хлоридом, предусматривает осуществление реакции соединений формулы I, где Z-m является нитратом, с молярным избытком соляной кислоты при температуре в пределах от 0 до 50oC.
Подходящим способом удаления группы P может быть обработка неорганической кислотой (такой как водный, спиртовой или эфирный раствор соляной кислоты) или органической кислотой (такой как трифторуксусная кислота). Если P является третбутоксикарбонильной группой, то предпочтительными условиями ее отщепления является использование хлористого водорода в спиртовом растворе. В этом случае, как указывалось выше, противоион Q-m будет представлять собой хлорид-ион.
Соединения настоящего изобретения хорошо растворяются в воде, в физиологическом растворе и в смешивающихся с водой растворителях.
Соединения настоящего изобретения обладают не только заметной противоопухолевой активностью, но и также низкой токсичностью, а поэтому их терапевтический индекс является особенно благоприятным.
Кроме того, высокая водорастворимость три-платиновых комплексов настоящего изобретения значительно облегчает получение парентеральных и пероральных фармацевтических форм.
Соединения настоящего изобретения были подвергнуты испытанию на их цитотоксическое действие in vitro с использованием различных опухолевых клеточных линий, включая клеточную линию мышиного лейкоза L-1210, клеточную линию карциномы яичника человека А2780, или соответствующие резистентные к цисплатину сублинии L-1210/CDDP и A2780/CDDP. Испытание на клеточной линии А2780 является традиционным методом оценки комплексов платины на их противоопухолевую активность. Кроме того, было проведено in vivo-испытание соединений настоящего изобретения, в котором мышам внутрибрюшинно инокулировали опухолевые клетки L-1210, а затем, через 24, 120 и 216 часов после инокуляции опухоли, внутрибрюшинно вводили соединение. Соединения настоящего изобретения обнаруживали высокое противоопухолевое действие в вышеописанных экспериментальных моделях.
Если соединения формулы I вводить человеку или животным, страдающим опухолями, восприимчивыми к лечению платиновыми комплексами, в дозах, составляющих в пределах от 0,1 мг до 1,2 г на один квадратный метр поверхности тела, то эти соединения способны вызвать регрессию указанных опухолей.
Поэтому, другой целю настоящего изобретения является использование соединений формулы I в целях изготовления лекарственного препарата для лечения опухолей.
Эффективная доза соединений настоящего изобретения может быть определена лечащим врачом в соответствии со стандартной техникой. Величины доз, используемых для введения животным различных видов, а также для введения человеку (в миллиграммах на один квадратный метр поверхности тела) описаны Freirech, E. J. и др. (Quantitative Comparison of Toxicity of Anticancer Agents in Mouse, Rat, Hamster, Dog, Monkey and Man, Cancer Chemother. Rep., 50, N4, 219-244 (1966)).
Однако, в основном, доза комплекса, которая может быть введена пациенту, составляет от 0,1 до 1200 мг на кг веса тела, а схема введения этой дозы может варьироваться в зависимости от различных факторов, хорошо известных специалистам.
Иногда может оказаться предпочтительным вводить платиновые комплексы настоящего изобретения вместе с одним или несколькими агентами, способствующими усилению противоопухолевой активности или устранению нежелательных побочных эффектов указанных комплексов.
Так, например, платиновые комплексы настоящего изобретения могут быть введены вместе с восстановленным глутатионом, как описано в патенте Великобритании 214905 и патенте США 4871528.
Кроме того, может оказаться предпочтительным вводить платиновые комплексы настоящего изобретения в комбинации с другими платиновыми комплексами, обладающими противоопухолевой активностью.
Поэтому, другой целью настоящего изобретения является получение фармацевтической композиции, содержащей по крайней мере одно соединение формулы I в комбинации с платиновым комплексом, обладающим противоопухолевой активностью.
Платиновые комплексы настоящего изобретения могут быть использованы для лечения таких опухолевых заболеваний, которые, как известно, являются восприимчивыми к терапии с применением цис-платины. Комплексы настоящего изобретения обладают также активностью против некоторых опухолей, которые являются резистентными к цис-платине.
Вообще говоря, соединения настоящего изобретения могут быть использованы для лечения тех же самых патологических состояний, которые лечат с применением цис-платины. Такими состояниями являются опухоли, сенсибилизация организма или облучение повышенными дозами радиации (Douple et al., Cisplatin Current Status and Development, Ed. A.W. Prestayk et al., Academic Press, 125(1980); Douple et al. , Platinum Metals Res., 29, 118 (1985)), а также паразитарные инвазии, такие как африканская сонная болезнь (Farrel et al., Biochem. Pharmacol., 33, 961 (1984)).
Как хорошо известно специалистам, схема лечения может соответствующим образом варьироваться в зависимости от типа опухоли и состояния пациента.
Еще одной целью настоящего изобретения является получение фармацевтических композиций, содержащих терапевтически эффективное количество по крайней мере одного соединения формулы I в сочетании со стандартными носителями и наполнителями.
Предпочтительно, если соединения настоящего изобретения вводят в виде стерильных водных растворов, необязательно содержащих хлорид натрия в соответствующей концентрации (0,1 - 0,9 мг/мл). Указанные растворы вводят предпочтительно внутривенно или внутриартериально, хотя в некоторых случаях могут быть использованы и другие способы введения.
Фармацевтические композиции для парентерального введения представляют собой стерильные физиологические растворы, описанные выше, либо стерильные порошки, которые могут быть затем использованы для приготовления растворов, а также масляные препараты для внутримышечного или внутрибрюшинного введения.
Другие фармацевтические композиции могут быть изготовлены в виде сиропов или аналогичных жидких форм, а также в виде твердых форм, таких как таблетки, капсулы и т.п.
Фармацевтические композиции настоящего изобретения могут быть получены хорошо известными методами, например методами, описанными в "Remington's Pharmaceutical Sciences Handbook, XVII Ed., Mack. Pub., N.Y., USA.
Настоящее изобретение, кроме того, проиллюстрировано нижеприведенными примерами.
Получение 1.
N- BOC-гександиамин получали из его гидрохлоридной соли, которая является коммерческим продуктом.
2,1 г гидрохлорида N- BOC-гександиамина растворяли в диэтиловом эфире (20 мл), и полученный раствор обрабатывали, перемешивая при этом 16 миллилитрами 1 н водного раствора гидроксида натрия.
Органическую фазу промывали солевым раствором, осушали сульфатом натрия, а растворитель выпаривали при пониженном давлении, в результате чего получали N- BOC-гександиамин в виде свободного основания с теоретическим выходом.
Пример 1. Получение т-[PtCl(NH3)2H2N- (CH2)6 - NH-BOC]+ + NO- 3.
2 г Транс-платины растворяли в 133 мл безводного диметилформамида (ДМФ), а затем, одной порцией, добавляли 1,13 г нитрата серебра. Полученную реакционную смесь, перемешивая и защищая от воздействия света, выдерживали в течение 18 часов. После этого, осажденный хлорид серебра отфильтровывали, прозрачный фильтрат охлаждали до температуры -20oC, и добавляли раствор N-BOC-1,6-гександиамина (1,36 г) в 40 мл безводного диметилформамида. Добавление продолжали приблизительно в течение 30 минут. Полученный раствор выдерживали при перемешивании и при температуре -20oC в течение 3 часов, а затем в течение еще одного часа при константной температуре. Растворитель выпаривали при пониженном давлении, поддерживая при этом температуру раствора не выше 40oC, после чего полученный остаток растворяли в 200 миллилитрах этилового эфира при перемешивании в течение 20 минут и фильтровали. Полученное твердое вещество растворяли в 200 мл метанола и оставляли на 15 часов при перемешивании для осаждения имеющихся следовых количеств транс-платины. Выделенную транс-платину отфильтровывали, а раствор обрабатывали активированным углем (1 г), снова фильтровали и, наконец, растворитель выпаривали при пониженном давлении. Остаток очищали путем суспендирования его в 100 мл ацетона при перемешивании в течение 30 минут. После фильтрования получали 2,3 г продукта.
Элементный анализ (%):
Вычислено: C 24,33; H 5,57; N 12,90; Cl 6,53; Pt 35,93;
Найдено: C 24,05; H 5,64; N 12,84; Cl 6,40; Pt 36,06.
195Pt-ЯМР в ДМФ/d7-ДМФ: - 2433 млн.д.
Пример 2. Получение т-[PtCl(NH3)2H2N-(CH2)6- NH3]2+ 2NO- 3.
К раствору, содержащему 1,5 г т-[PtCl(NH3)2H2N-(CH2)6- NH-BOC]+ NO- 3 и 150 мл метанола, добавляли 21 мл (6,5 моль) раствора хлористого водорода в этаноле. Полученную реакционную смесь перемешивали в течение 24 часов при комнатной температуре, а затем твердый остаток фильтровали, промывали на фильтре и этиловым эфиром и, наконец, осушали.
Полученное твердое вещество растворяли в 180 мл метанола, а затем добавляли раствор нитрата серебра (0,825 г) в 45 мл метанола. Эту реакционную смесь перемешивали в течение 30 минут при комнатной температуре, после чего осажденный хлорид серебра отфильтровывали и прозрачный фильтрат выпаривали досуха. Остаток растворяли в ацетоне, перемешивали в течение 15 минут, фильтровали и осушали, в результате чего получали 0,925 г продукта.
Элементный анализ (%):
Вычислено: C 14,65; H 4,71; N 14,24; Cl 7,21; Pt 39,67;
Найдено: C 14,19; H 4,66; N 16,62; Cl 6,91; Pt 36,10.
195Pt-ЯМР в ДМФ/d7-ДМФ: -2433 млн.д.
Пример 3. Получение т. т. т -[PtCl(NH3)2H2N-(CH2)6- NH2-Pt(NH3)2H2-(CH2)6-NH2 PtCl(NH3)2]4+ 4NO- 3.
61 мг Транс-платины суспендировали в 2 мл безводного диметилформамида, а затем добавляли 69,1 мг нитрата серебра. Полученную реакционную смесь перемешивали в течение шести часов при температуре 65oC, охлаждали до комнатной температуры и осажденный хлорид серебра отфильтровывали. К фильтрату добавляли раствор и- [PtCl(NH3)2H2N-(CH2)6NH3]+2 2NO3 (200 мг) в 2 мл диметилформамида и 0,4 мл раствора 1н гидроксида натрия в метаноле. Полученную реакционную смесь оставляли на ночь при комнатной температуре, а затем разводили этиловым эфиром до тех пор, пока не было выделено твердое вещество, после чего это вещество фильтровали, промывали этиловым эфиром и ацетоном и, наконец, осушали, в результате чего получали 220 мг продукта.
Полученный продукт суспендировали в диметилформамиде (5 мл) и перемешивали в течение 10 минут, а затем выделяли путем фильтрации и ресуспендировали в ацетоне (10 мл), перемешивая в течение еще 30 минут. После фильтрации и осушки было получено 150 мг продукта.
Элементный анализ (%):
Вычислено: C 11,63; H 4,07; N 15,83; Cl 5,72; Pt 47,24;
Найдено: C 11,70; H 3,95; N 15,20; Cl 4,60; Pt 47,10.
195Pt-ЯМР в NaCl (0,35% в воде): - 2416 млн.д.; - 2667 млн.д.
1H-ЯМР (200 МГц) в D2O: 1,35 млн.д.(м, 8H), 1,68 млн.д.(м, 8H), 2,65 млн. д.(шир.м.,8H).
Пример 4. Получение т- [BOC-NH-(CH2)6NH2Pt(NH3)2H2N- (CH2)6-NH-BOC]+2 - 2NO- 3.
К суспензии, содержащей 1,028 г транс-платины в 35 мл безводного диметилформамида, добавляли 1,16 г нитрата серебра. Полученную реакционную смесь нагревали до температуры 60oC в темноте в течение 5 часов, а затем осажденный хлорид серебра отфильтровывали. После добавления раствора N-BOC-1,6-гександиамина (1,48 г) в 5 мл диметилформамида, полученную реакционную смесь выдерживали в течение ночи при комнатной температуре. Эту смесь разводили 300 миллилитрами этилового эфира до тех пор, пока не было выделено белое твердое вещество, после чего это вещество фильтровали, повторно растворяли в метаноле и, наконец, фильтровали через фильтр Millex в 0,2 микрон для удаления имеющихся следовых количеств солей серебра. Метаноловый раствор разводили этиловым эфиром. Белое твердое вещество кристаллизовали, а затем фильтровали и осушали, в результате чего получали 1,94 г продукта.
Элементный анализ (%):
Вычислено: C 33,63; H 6,93; N 14,26; Pt 24,83;
Найдено: C 33,44; H 7,00; N 14,30; Pt 25,06.
195Pt-ЯМР в ДМФ/d7-ДМФ: - 2687 млн.д.
Пример 5. Получение и-[NH3-(CH2)6-NH2-Pt(NH3)2H2N- (CH2)6-NH3] +4 4Cl-.
500 мг т-[BOC-NH-(CH2)6-NH2-Pt(NH3)2H2N- (CH2)6-NH-BOC] 2+ 2NO- 3 растворяли в 50 мл метанола, а затем добавляли 5 мл (6,5 моль) раствора хлористого водорода в этаноле. Полученную реакционную смесь оставляли при перемешивании на 42 часа при комнатной температуре и образовавшееся твердое вещество фильтровали и промывали этиловым эфиром, в результате чего получали 340 мг продукта.
Элементный анализ (%):
Вычислено: C 23,81; H 6,66; N 13,88; Cl 23,42; Pt 32,23;
Найдено: C 23,14; H 6,73; N 13,51; Cl 22,03; Pt 31,68.
195Pt-ЯМР в воде: - 2674 млн.д.
Пример 6. Получение т. т. т. -[PtCl(NH3)2H2N- (CH2)6-NH2-Pt(NH3)2H2N- (CH2)6- NH2PtCl(NH3)2]4+ 4NO- 3.
220 мг т-[NH3-(CH2)6-NH2- Pt(NH3)2H2H-(CH2)6-BH3] 4+ -4Cl- растворяли в 10 мл дистиллированной воды и этот раствор обрабатывали 224 миллиграммами нитрата серебра. Полученную суспензию выдерживали при комнатной температуре при перемешивании в течение 10 минут, а затем осажденный хлорид серебра удаляли путем фильтрации. Фильтрат концентрировали почти досуха, а затем разводили ацетоном. Выделенное белое твердое вещество фильтровали, промывали ацетоном и осушали, в результате чего получали 204 мг т-[NH3-(CH2)6-NH2- Pt(NH3)2H2N-(CH2)6-NH3]4+ 4NO- 3
Раствор, содержащий 172 мг транс-платины и 21,5 мл безводного диметилформамида, обрабатывали 98 миллиграммами нитрата серебра. Полученную суспензию перемешивали при комнатной температуре в течение ночи, после чего осажденный хлорид серебра отфильтровывали. Раствор, содержащий 204 мг т-[NH3-(CH2)6-NH2--Pt (NH3)2H2N(CH2)6-NH3] +4 4NO- 3 в 7 мл диметилформамида, обрабатывали 0,57 миллилитрами раствора 1 н гидроксида натрия в метаноле, а затем этот раствор при комнатной температуре добавляли к вышеуказанному фильтрату, содержащему транс-платину, активированную диметилформамидом. Через 6 часов раствор фильтровали через фильтр Millex в 0,2 микрон для удаления имеющихся следовых количеств солей серебра и полученный фильтрат разводили этиловым эфиром. Осажденное твердое вещество выделяли путем фильтрации, в результате чего получали 326 мг продукта.
195Pt-ЯМР в NaCl (0,3% в воде): - 2416 млн.д.; - 2667 млн.д.
195H-ЯМР (200 МГц) в D2O (млн.д.): 1,35 (м, 8H), 1,68 (м, 8H), 2,65 (шир.м., 8H).
Пример 7. Получение т. т. т. -[PtCl(NH3)2H2N- (CH2)6NH2-Pt(NH3)2H2N- (CH2)6)6-NH2PtCl(NH3)2]4+ 4Cl-.
326 мг т.т.т -[PtCl(NH3)2H2N-(CH2)6-NH2-Pt (NH3)2H2-(CH2)6-NH2 PtCl(NH3)2] 4+ 4NO- 3 растворяли в солевом растворе (0,9%-ном хлориде натрия) и этот раствор фильтровали через фильтр Millex 90,2 микрон), а затем концентрировали до выделения белого твердого вещества. Полученное вещество фильтровали и получали 187 мг продукта. Элементный анализ (%):
Вычислено: C 12,73; H 4,45; N 12,37; Cl 18,78; Pt 51,68;
Найдено: C 12,60; H 4,45; N 12,85; Cl 14,77; Pt 48,33.
195Pt-ЯМР в NaCl (0,3% в воде): - 2416 млн.д.; - 2671 млн.д.
1H-ЯМР (200 МГц) в D2O (млн.д.): 1,40 (м,8H); 1,70 (м, 8H), 2,70 (шир.м. , 8H).
Пример 8. В соответствии со способами, описанными в примерах 1, 2 и 3, или альтернативно способами, описанными в примерах 4, 5 и 6, и с использованием соответствующего монозащищенного диамина были получены следующие транс-три-платиновые комплексы:
[PtCl(NH3)2H2N-(CH2)5-NH2- Pt(NH3)2H2N-(CH2)5-NH2PtCl- (NH3)2]4+ 4NO- 3;
[PtCl(NH3)2H2N-(CH2)4-NH2- Pt(NH3)2H2N-(CH2)4-NH2PtCl- (NH3)2]4+ 4NO- 3;
[PtCl(NH3)2H2N-(CH2)3-NH2- Pt(NH3)2H2N-(CH2)3-NH2PtCl- (NH3)2]4+ 4NO- 3;
[PtCl(NH3)2H2N-(CH2)2-NH2- Pt(NH3)2H2N-(CH2)2-NH2PtCl- (NH3)2]4+ 4NO- 3;
[PtCl(NH3)2H2N-(CH2)7-NH2- Pt(NH3)2H2N-(CH2)7-NH2PtCl- (NH3)2]4+ 4NO- 3;
195Pt-ЯМР в NaCl (0,3% в воде): - 2422 млн.д; - 2670 млн.д.
Пример 9. В соответствии со способом, описанным в примере 7, и с использованием указанных в примере 8 транс-три-платиновых комплексов были получены следующие соединения:
[PtCl(NH3)2H2N-(CH2)5-NH2- Pt(NH3)2H2N-(CH2)5-NH2Pt Cl-(NH3)2] 4+ 4Cl-;
[PtCl(NH3)2H2N(CH2)4-NH2- Pt(NH3)2H2N-(CH2)4-NH2PtCl- (NH3)2] 4+ 4Cl- ;
[PtCl(NH3)2H2N(CH2)3-NH2- Pt(NH3)H2H2N-(CH2)3-NH2PtCl- (CH3)2]4+ 4Cl- ;
[PtCl(NH3)2H2N(CH2)2-NH2- Pt(NH3)2H2N-(CH2)2-NH2PtCl- (NH3)2] 4+ 4Cl- ;
[PtCl(NH3)2H2N(CH2)7-NH2- Pt(NH3)2H2N-(CH2)7-NH2-Pt (NH3)2] 4+ 4Cl-;
1H-ЯМР (200 МГц) в D2O (млн.д.); 1,39 (с, 12H), 1,68 (шир. м., 8H), 2,67 (шир. м., 8H).
Пример 10. Получение т.т.т.-[PtCl(NH3)2-N-(CH2)6-NH2- Pt(NH3)2H2N-(CH2)6-NH2- PtCl(NH3)2]4+ 4Cl-.
Суспензию, содержащую т.т.т.[PtCl(NH3)2H2N- (CH2)6 - NH2-Pt(NH3)2H2N-(CH2)6- NH2-PtCl(NH3)2] 4+ 4NO3 (1,3 г) и 65 мл водного раствора 0,1 н соляной кислоты, получали в атмосфере азота, а затем солюбилизировали при 54oC. После выдерживания в течение одного часа при той же температуре раствор охлаждали при 20oC, а затем фильтровали на стекловолоконном фильтре для удаления механических примесей; к прозрачному раствору добавляли 7,8 мл водного раствора 4 н соляной кислоты и через несколько минут начиналось осаждение. Полученную суспензию перемешивали в течение 30 минут при температуре 20oC, а затем еще 30 минут при температуре 10oC. Осадок фильтровали с помощью воронки Бюхнера, а затем промывали раствором 0,4 н соляной кислоты (0,5 мл) и ацетоном. Собранное белое твердое вещество осушали в течение ночи в вакууме при температуре 40oC, в результате чего получали 1,03 г продукта.
Элементный анализ (вычислено/найдено, %) • 2H2O: C 12,33/-12:34: H 4,65/4,73; N 11,98/12,05; C 18,21/17,55; Pt 50,07/49,97.
Пример 11. Раствор для инъекций, содержащий соединение примера 7.
Смешивают 0,250 г указанного соединения с 4,5 г хлористого натрия, доводят pH примерно до 4 (3,5 - 4,2) с помощью 0,1 н раствора соляной кислоты и добавляют волу для инъекций до объема 500 мл. Раствор хранят в прозрачных стеклянных ампулах на 1 мл, предпочтительно цвета янтаря.
Трехъядерные катионные комплексы платины формулы I, где n = 2 -7, целое число; Z-m- анион хлора, брома, иода, нитрата или сульфата; m = 1 или 2, обладают противоопухолевой активностью. 3 с. и 19 з.п.ф-лы.
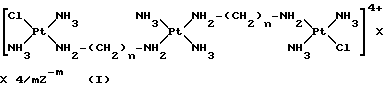
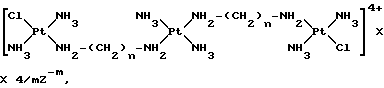
где n = 2 - 7, целое число;
Z-m является анионом, выбранным из хлорида, бромида, иодида, нитрата и сульфата;
m = 1 или 2.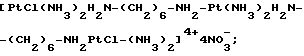
[PtCl(NH3)2H2N-(CH2)6-NH2-Pt(NH3)2H2N-(CH2)6-NH2PtCl-(NH3)2] 4+4Cl-;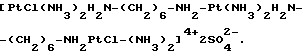
5. Способ получения соединений по пп.1 - 4, включающий в себя следующие стадии:
а) активацию транс-платины путем замещения атома хлора молекулой диметилформамида в присутствии нитрата серебра;
b) взаимодействие активированного промежуточного соединения с диамином формулы II
H2N-(CH2)n-NH-P,
где n = 2 - 7, целое число;
P представляет собой подходящую стандартную защитную группу;
с получением после отщепления защитной группы P промежуточного соединения формулы IV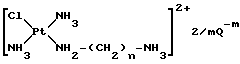
где n является таким, как он был определен выше;
m = 1 или 2, целое число;
Q-m - противоион, тип которого зависит от условий отщепления группы P;
с) реакцию обмена между анионом Q-m и анионом NO- 3 в растворителе, таком как вода или спирт, с получением промежуточного соединения формулы V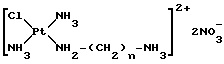
где n является таким, как он был определен выше;
d) взаимодействие промежуточного соединения (V) с транс-платиной, предварительно активированной путем замещения двух атомов хлора на две молекулы диметилформамида в присутствии нитрата серебра, в молярном соотношении 1 : 0,5 с получением соединения формулы I, где n является таким, как он был определен выше, m = 1, а Z-m - нитрат-анион, и, если это необходимо,
е) реакцию обмена указанного нитрат-аниона и другого аниона Z-m, где Z-m является таким, как он был определен выше.
а) взаимодействие амина формулы II
H2N-(CH2)n-NH-P,
где n = 2 - 7, целое число;
P представляет собой подходящую стандартную защитную группу;
с транс-платиной, предварительно активированной путем замещения двух атомов хлора двумя молекулами диметилформамида в присутствии нитрата серебра в молярном соотношении 2 : 1 с получением промежуточного соединения формулы VI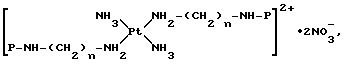
где n и P являются такими, как они были определены выше;
b) отщепление защитной группы P с получением промежуточного соединения формулы VII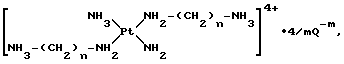
где n является таким, как он был определен выше;
Q-m - анион, тип которого зависит от условий реакции отщепления;
с) реакцию обмена между анионом Q-m и анионом NO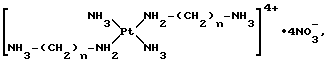
d) взаимодействие промежуточного соединения формулы VIII с транс-платиной, предварительно активированной путем замещения атома хлора молекулой диметилформамида, в присутствии нитрата серебра в молярном соотношении 1 : 2 с получением соединения формулы I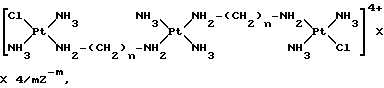
где n является таким, как он был определен выше;
m = 1;
Z-m - нитрат анион;
и если это необходимо, е) реакцию обмена между указанным нитрат-анионом и другим анионом Z-m, где Z-m является таким, как он был определен выше.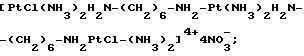
[PtCl(NH3)2H2N-(CH2)6-NH2-Pt(NH3)2H2N-(CH2)6-NH2PtCl-(NH3)2] 4+ • 4Cl-;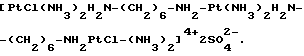
20. Композиции по пп.16 - 19, отличающиеся тем, что указанное терапевтически активное количество является таким, что введенная доза составляет 0,1 - 1200 мг активного ингредиента на 1 кг массы тела.
| US 4871528 A1, 1989 | |||
| Магнезиальный цемент | 1974 |
|
SU503830A1 |
| Способ получения комплексных соединений платины | 1985 |
|
SU1570649A3 |
| US 5091521 A1, 1992 | |||
| US 4504847 A1, 1985. | |||
Авторы
Даты
1999-05-27—Публикация
1995-03-22—Подача