Изобретение относится к производным индола, промежуточным соединениям для их получения, содержащим их фармацевтическим композициям и к их применению в медицине. Активные соединения настоящего изобретения пригодны для лечения мигреней и других расстройств.
Патенты США 4839377 и 4855314 и Европейская патентная заявка 313397 относятся к 5-замещенным 3-аминоалкилиндолам. Указывается, что эти соединения пригодны для лечения мигрени.
Патентная заявка Великобритании 040279 относится к 3-аминоалкил-1Н-индол-5-тиоамидам и карбоксамидам. Указано, что эти соединения можно использовать для лечения гипертензии, болезни Реймонда и мигреней.
Европейская патентная заявка N 303506 относится к 3-поли: гидропиридил-5-замещенным-1Н-индолам. Указано, что эти соединения обладают активностью в качестве 5-НТ1рецепторных агонистов и вазоконстрикторных агентов, а также могут быть использованы для лечения мигреней.
Европейская патентная публикация N 354777 относится к производным N-пиперидинил : индолил - этил-алкансульфонамидам. Указано, что эти соединения обладают активностью в качестве 5-НТ1-рецепторных агонистов и вазоконстрикторных агентов, и могут быть использованы для лечения головной боли.
Европейская патентная публикация N 438230 относится к индол-замещенным пятичленным гетероароматическим соединениям. Указано, что эти соединения обладают активностью в качестве 5-НТ1-подобных рецепторных агонистов, и могут быть использованы для лечения мигреней и других расстройств, для которых показаны селективные агонисты этих рецепторов.
Европейская патентная публикация заявки N 313397 относится к производным 5-гетероциклического индола. Указано, что эти соединения обладают исключительными свойствами для лечения и профилактики мигреней, "гистаминовых" головных болей и головных болей, связанных с сосудистыми нарушениями. Указано, также, что эти соединения обладают исключительным 5-НТ1-подобным" рецепторным агонизмом.
Международная патентная заявка WO- 91-18897 относится к производным 5-гетероциклического индола. Указано татке, что эти соединения обладают исключительными свойствами для лечения и профилактики мигрени, "гистаминовых" головных болей и головных болей, связанных с сосудистыми нарушениями. Указано также, что эти соединения обладают исключительным "5-НТ1-подобным" рецепторным агонизмом.
Европейская патентная публикация заявки 457701 относится к производным арилоксиамина, как имеющим высокое сродство с 5-НТ1D серотониновыми рецепторами. Указано, что эти соединения пригодны для лечения заболеваний, связанных с дисфункцией серотониновых рецепторов, например, мигреней.
Европейская патентная публикация заявки N 497512 А2 относится к классу производных имидазола, триазола и тетразола, которые селективны по отношению к 5-НТ1-подобным рецепторам. Указано, что эти соединения пригодны для лечения мигреней и связанных с ними расстройств.
В "New Trends in Benzodiazepin Research" in Drugs of Today, vol. 24, 649-663 /1987/ обсуждаются применение лигандов рецепторов бензодиазепин для лечения состояний тревог и других расстройств.
Европейская патентная заявка ЕР-499527-А1 относится к новым производным β-карболина, которые обладают сродством к рецепторам бензодиазепина, и которые можно использовать для лечения дегенеративных расстройств центральной нервной системы, например болезни Альцгеймера.
Краткое содержание изобретения
Настоящее изобретение относится к соединениям формулы: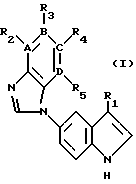
где R1 представляет: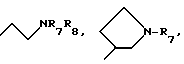
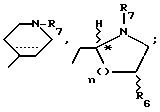
n равно 0, 1 или 2;
A, B, C и D - каждый независимо представляет азот или углерод;
каждый из R2, R3, R4 и R5 независимо представляет водород; C1-C6алкил, арил, C1-C3алкиларил, галоид /например, фтор, хлор, бром или иод/, циано, нитро, -/CH2/mNR14R15, - /CH2/m OR9, -SR9, -SO2NR14R15, N/CH2/m NR14SO2R15, -/CH2/m NR14CO2R9, -/CH2/mNR14COR9, -/CH2/mNR14CONHR9, -CONR14R15 или -CO2R9;
R2 и R3, R3 и R4 или R4 и R5 взятые вместе, могут представлять пяти-семичленное алкильное кольцо, шестичленное арильное кольцо, пяти-семичленное гетероалкильное кольцо, содержащее 1 гетероатом, выбранный из N, O или S, или пяти-шестичленное гетероарильное кольцо, содержащее 1 или 2 гетероатома, выбранные из N, O или S; R6 представляет водород, -OR10, или -NHCOR10;
каждый из R7, R8, R14 и R15 каждый независимо представляет водород, C1-C6алкил, -/CH2/xOR11 C1-C3алкиларил, арил;
R7 и R8 или R14 и R15 взятые вместе, образуют трех-шестичленное кольцо; R9 представляет водород, C1-C6алкил, C1-C3алкиларил или арил;
R10 представляет водород, C1-C6алкил или C1-C3алкиларил;
R11 представляет водород, C1-C6алкил, или C1-C3алкиларил;
m равно 0, 1, 2 или 3;
x представляет 2 или 3;
пунктирная линия представляет необязательную двойную связь, а вышеуказанные арильные группы и арильные фрагменты вышеуказанных алкиларильных групп независимо представляют фенил или замещенный фенил, причем указанный фенил может быть замещен одним-тремя C1-C4алкилом, галоидом /например, фтором, хлором, бромом или иодом/, гидрокси, циано, карбоксамидо, нитро или C1-C4алкокси; и их фармацевтически приемлемые соли.
Эти соединения являются эффективными агонистами 5-НТ1 рецепторов и агонистами и антагонистами бензодиазепиновых рецепторов, и могут использоваться при лечении мигреней и других расстройств.
Соединения настоящего изобретения включают оптические изомеры формулы I /т. е. R и S стереоизомеры у любого хирального сайта/ и их рацемические, диастереоизомерные или эпимерные смеси. Если R6 представляет водород, эпимеры с абсолютной конфигурацией R у хирального углерода, обозначенного звездочкой в формуле I, наиболее предпочтительны. Если R6 представляет -OR10 или NHCOR10, а n равно 0 или 1, предпочтительны эпимеры с абсолютной конфигурацией S у хирального углерода, обозначенного звездочкой в формуле I. Если R6 представляет -OR10 или -NHCOR10, а n = 2, предпочтительны эпимеры с абсолютной конфигурацией R у хирального углерода, обозначенного звездочкой в формуле I. Если R6 представляет -OR10 или -NHCOR10, а n = 0, наиболее предпочтительны цис-эпимеры //2S, 3S / абсолютная конфигурация в азетидиновом кольце/. Если R6 представляет -OR10 или -NHCOR10, а n = 1, наиболее предпочтительны цис-эпимеры //2S, 4R/ абсолютная конфигурация в пирролидиновом кольце/. Если R6 представляет -OR10 или -NHCOR10, а n = 2, наиболее предпочтительны цис-эпимеры //2R, 5R/ абсолютная конфигурация в пиперидиновом кольце/.
Если нет другие указаний, алкильные и алкенильные группы, указанные здесь, а также алкильные фрагменты других групп, указанных здесь /например, алкоксильных/, могут быть линейными или разветвленными, и могут быть циклическими /например, циклопропилом, циклопентилом или циклогексилом/, или могут быть линейными или разветвленными и содержать циклические фрагменты.
Предпочтительными соединениями изобретения являются соединения формулы I, в которых R1 представляет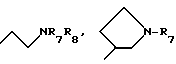
или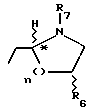
n = 1;
А, B и С каждый представляет углерод;
R6 представляет водород или -OCH3;
R7 представляет водород, C1-C3алкил или -CH2CH2OCH3.
Из вышеперечисленных соединений, наиболее предпочтительны R энантиомеры с хиральным углеродом) помеченным звездочкой в формуле I. Из указанных соединений особенно предпочтительны цис-эпимеры.
Наиболее предпочтительны следующие соединения:
5-циано-1-/3-/N-/2-метоксиэтил/пирролидин-2R-илметил/индол- 5-ил/-1Н-бензимидазол;
5-метоксикарбонил-1-/3-/N-/2-метоксиэтил/пирролидин-2R- илметил/индол-5-ил/-1Н-бензимидазол;
5-циано-1-/3-/4R-метоксипирролидин-2R-илметил/индол-5-ил/-1Н- бензимидазол;
5-циано-1-/3-/N-/2-метоксиэтил/-4R-метоксипирролидин-2R- илметил/индол-5-ил/-2Н-бензимидазол;
5-гидроксиметил-1-/3-/N-/2-метоксиэтил/пирролидин-2R-илметил/- индол-5-ил/-1Н-бензимидазол;
5-циано-1-/3-/пирролидин-2R-илметил/индол-5-ил/-1Н-бензимидазол 1-/3-/N-циклопропилметил/пирролидин-2R-илметил/индол- 5-ил/-3Н-имидазоло[4,5-b] пиридин;
1-/3-/пирролидин-2R-илметил/индол-5-ил/-3Н-имидазо[4,5-b] пиридин 5-циано-1-/3-/N-метилпирролидин-2R-илметил/индол-5- ил/-1Н-бензимидазол;
5-циано-1-/3-/N-циклопропилметил/пирролидин-2R-илметил/ индол-5-ил/-1Н-бензимидазол;
1-/3-/N-метилпирролидин-2R-илметил/индол-5-ил/-1Н- бензимидазол; 5-метил-1-/3-/N-метилпирролидин-2R-илметил/индол-5-ил/- 1Н-бензимидазол;
1-/3-/N-мeтилпиppoлидин-2R-илмeтил/индoл-5-ил/-3H-имидaзo- [4,5-b]пиридин;
6-метокси-1-/3-/N-метилпирролидин-2R-илметил/индол-5-ил/-3Н- имидазо[4,5-b]пиридин;
1-/3-/N-метилпирролидин-2R-илметил/индол-5-ил/-5-трифторметил- 1Н-бензимидазол;
1-/3-/2-N,N-диметиламиноэтил/индол-5-ил/-3Н-имидазо[4,5-b]- пиридин;
1-/3-/2-аминоэтил/индол-5-ил/-3Н-имидазо[4,5-b]пиридин;
1-/3-/N-метилпирролидин-2R-илметил/индол-5-ил/-5-фенил-1Н- бензимидазол;
6,7-дихлор-1-/3-/N-метилпирролидин-2R-илметил/индол-5-ил/- 1H-бензимидазол;
1-/3-/пиперид-4-ил/индол-5-ил/-3Н-имидазо[4,5-b]пиридин;
1-/3-/N-мeтилпиppoлидин-3-ил/индoл-5-ил/-3H-имидaзo [4,5-b]-пиридин;
5-хлор-1-/3-/N-мeтилпирролидин-2R-илметил/индoл-5-ил/-1Н- бензимидазол;
6-хлор-1-/3-/N-метилпирролидин-2R-илметил/индол-5-ил/-1Н- бензимидазол;
7-хлор-1-/3-/N-мeтилпиppолидин-2R-илмeтил/индoл-5-ил/- 1H-бензимидазол;
5-aминомeтил-1-/3-/N-/2-мeтoкcиэтил/пиppолидин-2R-илмeтил/- индол-5-ил/-1Н-бензимидазол;
5-ацетиламинометил-1-/3-/N-/2-мeтoкcиэтил/пиppoлидин-2R- илметил/индол-5-ил/-1Н-бензимидазол;
5-циано-1-/3-/пиперид-4-ил/индол-5-ил/-1Н-бензимидазол;
5-циано-1-/3-/1,2,5,6-тетрагидропирид-4-ил/индол-5-ил/-1Н- бензимидазол;
N-фенил-N'-/3-/N-/2-мeтoкcиэтил/пирролидин-2R-илметил/индол- 5-ил/-1H-бенз[b]имидазилметилмочевина;
5-циано-1-/3-/N-метилпирролидин-3-ил/индол-5-ил/-1Н- бензимидазол; 5-бензоиламинометил-1-/3-/N-/2-метоксиэтил/ пирролидин-2R-илметил/индол-5-ил/-1Н-бензимидазол;
5-аминометил-1-/3-N-метилпирролидин-2R-илметил/индол- 5-ил/-1H-бензимидазол;
5-циано-1-/3-/N-метилпирролидин-2R-илметил/индол-5-ил/-1Н- пиридо[4,5-b] имидазол; и
4-мeтил-1-/3-/N-метилпиppoлидин-2R-илмeтил/индoл-5-ил/-1H- пиридо[4,5-b] имидазол.
Настоящее изобретете относится также к соединению формулы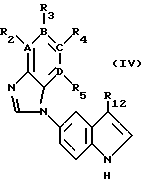
где R12 представляет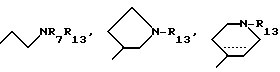
или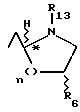
n = 0, 1 или 2;
A, B, C и D каждый независимо представляет азот или углерод;
R2, R3, R4 и R5 каждый независимо представляет водород, C1-C6алкил, арил, C1-C3алкиларил, галоид /например, фтор, хлор, бром или иод/, циано, нитро, -/CH2/m NR14R15, -/CH2/mOR9, -SR9, -SO2NR14R15, -/CH2/mNR14SO2R15,
-/CH2/mNR14CO2R9, -/CH2/mNR14R15 или -CO2R9;
R2 и R3, R3 и R4, или R4 и R5 взятые вместе, образуют пяти-семичленное алкильное кольцо,
шестичленное арильное кольцо, пяти-семичленное гетероалкильное кольцо, содержащее 1 гетероатом, выбранный из N, O или S, или пяти-шестичленное гетероарильное кольцо, содержащее 1 или 2 гетероатома, выбранные из N, O или S;
R6 представляет водород, -OR10 или -NHCOR10; R7, R14 и R15 каждый независимый представляет водород, C1-C6алкил, -/CH2/xOR11, C1-C3алкиларил или арил;
R14 и R15 взятые вместе, могут образовывать трех-шестичленное кольцо;
R9 представляет водород, C1-C6алкил, C1-C3алкиларил или арил;
R10 представляет водород, C1-C6алкил, или C1-C3алкиларил;
R11 представляет водород, C1-C6алкил или C1-C3алкиларил;
R13 представляет -COR16, -CO2R16 или -CH2Ph;
R16 представляет C1-C6алкил; C1-C3алкиларил или арил;
m = 0, 1, 2 или 3;
x представляет 2 или 3;
пунктир представляет необязательную двойную связь; указанные ранее арильные группы и арильные фрагменты вышеуказанных алкиларильных групп представляют независимо фенил и замещенный фенил, причем указанный замещенный фенил может быть замещен одним-тремя C1-C4алкилом, галоидом /например, фтором, хлором, бромом или иодом/, гидрокси, циано, карбоксамидо, нитро и C1-C4алкокси.
Эти соединения можно использовать в качестве промежуточных при получении соединений формулы I.
Настоящее изобретение относится также к фармацевтической композиции, для лечения таких состояний, как гипертензия, депрессия, беспокойство, нарушения аппетита, тучность, токсикомания, охватывающие головные боли, мигрень, боль и хроническая пароксимальная гемикрания и головная боль, связанные с сосудистыми нарушениями, содержащей такое количество соединения формулы I или его фармацевтически приемлемей соли, которого достаточно для эффективного лечения таких состояний, и фармацевтически приемлемый носитель.
Настоящее изобретение относится также к способу лечения таких состояний, как гипертензия, депрессия, беспокойство, нарушении аппетита, тучность, токсикомания, охватывающие головные боли, мигрень, боль и хроническая пароксимальная гемикрания и головная боль, связанные с сосудистыми нарушениями, который включает введение млекопитающему /например, человеку/ необходимого для такого лечения количества соединения формулы I, или его фармацевтически приемлемой соли, эффективных при лечении такого состояния.
Настоящее изобретение относится также к способу лечения расстройств, возникающих за счет дефицита серотонергической нейротрансмиссии /например, депрессии, беспокойства, нарушения аппетита, тучности, токсикомании, охватывающих головных болей, мигрени, боли и хронической пароксимальной гемикрании и головной боли, связанных с сосудистыми нарушениями/, включающий введение млекопитающему /например, человеку/, нуждающемуся в таком лечении, такого количества соединения формулы 1 или его фармацевтически приемлемой соли, которое эффективно при лечении такого состояния.
Соединения формулы I можно получить в соответствии со следующей схемой реакции (см. в конце описания).
Соединения формулы III можно получить при взаимодействии соединения формулы VI, где R1 имеет указанные для формулы I знамения, с соединением формулы V, где А, В, С, D, R2, R3, R4 и R5 имеют указанные для формулы I значения, и где Z представляет такую подходящую отщепляемую группу, как, например, F, Cl, Br, J, -SCH3, -SO2CH3, -SO2CH3, -SPh, или -SO2Ph /Ph = фенил/, в кислотных, нейтральных или щелочных условиях в инертном растворителе. Предпочтительны щелочные условия. Подходящие основания включают карбонат натрия, карбонат натрия, триалкиламины /включая, например, триэтиламин/, натрий и гидрид натрия. Предпочтительным основанием являются триэтиламин. Подходящие растворители включают C1-C4 спирты, диоксан, диэтиловый эфир, тетрагидрофуран, ацетонитрил, N,N-диметилформамид и N-метил- пирролидин. Предпочтительным растворителем является этанол. Реакцию обычно ведут при температуре от около 25oC до около 154oC, предпочтительно от около 70oC до около 80oC.
Соединения формулы II можно получить за счет восстановления соединений формулы III, где A, B, C, D, R1, R2, R3, R4 и R5 имеют указанные для формулы I значения, в инертном растворителе. Такое восстановление можно осуществить либо за счет переходных металлов, либо металлических восстанавливающих агентов. Если для восстановления используют переходные металлы, используют также источник водорода. Подходящие переходные металлы включают палладий на угле, гидроксид палладия на угле и оксид платины. Предпочтителен палладий на угле. Подходящие источники водорода включают газообразный водород, аммонийформат и муравьиную кислоту. В качестве источника водорода предпочтительно использовать газообразный водород при давлении от около 1 до около 3 атмосфер. Предпочтительным давлением является давление газообразного водорода в три атмосферы. Подходящие растворители включают C1-C4 спирты, ацетонитрил, N,N-диметилформамид и N-метилпирролидин. Предпочтительным растворителем является этанол. Другие металлические восстанавливающие агенты включают FeSO4, Zn /металл/ в водной соляной кислоте, а также Sn /металл/ в водной соляной кислоте. Из этих групп предпочтительна FeSO4. Подходящие растворители включают водный гидроксид аммония /в смеси с этанолом или концентрированную водную соляную кислоту. Предпочтительным растворителем является водный гидроксид аммония /в смеси с этанолом/. Все перечисленные восстановительные реакции обычно ведут при температуре от около 25oC до около 100oC, предпочтительно, от около 25oC до около 50oC. Следует отметить, что соединения формулы II используют далее непосредственно из реакции восстановления, без дополнительной очистки.
Соединения формулы I получают в реакции соединения II, где A, B, C, D, R1, R2, R3, R4 и R5 имеют указанные для формулы I значения, с синтоном муравьиной кислоты в нейтральных или кислотных условиях в инертном растворителе. Подходящие синтоны муравьиной кислоты включают диметилформамиддиметилацеталь, триметилортоформат, триэтилортоформат, этоксиметиленмалононитрил и диэтилэтоксиметиленмалонат. Предпочтительным синтоном муравьиной кислоты является этоксиметиленмалононитрил. Для этоксиметиленмалононитрила предпочтительно использовать нейтральные условия. Подходящие кислотные катализаторы, которые можно использовать с вышеуказанными синтонами муравьиной кислоты, включают пара-толуолсульфокислоту, соляную кислоту, муравьиную кислоту или уксусную кислоту. Подходящие растворители включают C1-C4спирты) диоксан, диэтиловый эфир, тетрагидрофуран, ацетонитрил, N,N-диметилформамид и N-метилпирролидин. Предпочтительным растворителем является 2-пропанол. Реакцию обычно ведут при температуре от около 25oC до около 154oC, предпочтительно, при температуре от около 75oC до около 85oC.
Соединения формулы I можно также получить альтернативным способом, представленным схемой (см. в конце описания).
Соединения формулы VIII можно получить при взаимодействии соединения формулы VII, где R12 имеет указанные для формулы IV значения, с соединением формулы V, где A, B, C, D, R2 R3, R4 и R5 имеют указанные для формулы I знамения и где ZG представляет такую подходящую отщепляемую группу, как, например, F, Cl, Br, J, -SCH3, -SO2CH3, -SPh или -SO2Ph, в кислотных нейтральных иди щелочных условиях в инертном растворителе. Предпочтительны щелочные условия. Подходящие основания включают бикарбонат натрия, карбонат натрия, триалкиламины /например, триэтиламин/, натрий и гидрид натрия. Предпочтительным основанием является триэтиламин. Подходящие растворители включают C1-C1 спирты, диоксан, диэтиловый эфир, тетрагидрофуран, ацетонитрил, N,N-диметилформамид и N-метилморфолин. Предпочтительным растворителем является этанол. Реакцию обычно ведут при температуре от около 26 до около 154oC, предпочтительно, от около 70oC до около 80oC.
Соединения формулы IX можно получить за счет восстановления соединений формулы VIII, где A, B, C, D, R1, R2, R3, R4 и R5 имеют указанные для формулы IV значения, в инертном растворителе. Такое восстановление можно осуществить за счет переходных металлов или других металлических восстанавливающих агентов. Если при восстановлении используют переходный металл, используют также источник водорода. Подходящие переходные металлы включают платину на угле, гидроксид палладия на угле и оксид платины. Предпочтителен палладий на угле. Подходящие источники водорода включают газообразный водород, аммонийформат и муравьиную кислоту. В качестве источника водорода используют газообразный водород под давлением от около одной до трех атмосфер. Предпочтительным давлением газообразного водорода является давление в три атмосферы. Подходящие растворители включают C1-C4спирты, ацетонитрил, N,N-диметилформамид и N-метилпирролидин. Предпочтительным растворителем является этанол. Другие металлические восстанавливающие агенты включают FeSO4, Zn /металл/ в водной соляной кислоте, и Sn /металл/ в водной соляной кислоте. Предпочтительной из этих групп является FeSO4. Подходящие растворители включают водный гидроксид аммония / в смеси с этанолом/ или концентрированную водную соляную кислоту. Предпочтителен водный гидроксид аммония /в смеси с этанолом/. Все вышеперечисленные реакции восстановления обычно ведут при температуре от около 25oC до около 100oC, предпочтительно, от около 25oC до около 50oC. Следует заметить, что соединения формулы IX используют непосредственно из реакции восстановления без дополнительной очистки.
Соединения формулы IV получают в результате реакции соединения формулы IX, где A, B, C, D, R2, R3, R4, R5 и R12 имеют указанные в формуле IV значения, с синтоном муравьиной кислоты в нейтральных или кислотных условиях в инертном растворителе. Подходящие синтоны муравьиной кислоты включают диметилформамиддиметилацеталь, триметилорформат, триэтилортоформат, этоксиметиленмалононитрил и диэтилэтоксиметиленмалонат. Предпочтительным синтоном муравьиной кислоты является этокоиметиленмалонитрил. Хотя предпочтительны нейтральные условия, подходящие кислотные катализаторы включают паратолуолсульфокислоту, соляную кислоту, муравьиную кислоту или уксусную кислоту. Подходящие растворители включают C1-C4 спирты, диоксан, диэтиловый эфир, тетрагидрофуран, ацетонитрил, N,N-диметилформамид и N-метилпирролидин. 2-пропанол является предпочтительным растворителем. Реакцию обычно ведут при температуре от около 25oC до около 154oC, предпочтительно, при температуре от около 75oC до около 85oC.
Соединения формулы IA, где R7 представляет водород, можно получить, удаляя защиту у основного азота в соединениях формулы IV, где B, A, C, D, R2, R3, R4, R5 и R12 имеют указанные для формулы IV значения, в инертном растворителе. Характер такого удаления защитных групп, зависит от природы R13. Если R13 представляет -CH2Ph или -CO2CH2Ph, такое удаление можно осуществить за счет каталитического гидрирования, используя источник водорода и катализатор-переходный металл в инертном растворителе. Подходящие переходные металлы включают палладий на угле, гидроксид палладия на угле и оксид платины. Предпочтителен палладий на угле. Подходящие источники водорода включают газообразный водород, аммонийформат и муравьиную кислоту. Предпочтительным источником водорода является газообразный водород под давлением от одной до около трех атмосфер, причем предпочтительно давление около трех атмосфер. Подходящие растворители включают C1-C4спирты, ацетонитрил, N,N-диметилформамид и N-метилпирролидин. Предпочтительным растворителем является этанол. Реакцию обычно ведут при температуре от около 25oC до около 100oC, предпочтительно, от около 25oC до около 50oC. Если R13 представляет -COR16 или -CO2R16, где R16 имеет указанные для формулы IV значения, удаление защиты можно осуществить щелочным или кислотным гидролизом. Подходящие основания включают гидроксид натрия, алкоксиды натрия и трет.-бутоксид калия. Подходящие кислоты включают минеральные кислоты и серную кислоту. Подходящие растворители включают воду и C1-C3спирты. Реакцию обычно ведут при температуре от около 25oC до около 100oC, предпочтительно, от около 70oC до около 80oC.
Соединения формулы IB, где R7 не является водородом, можно получить за счет алкилирования соединения формулы IA, где R7 представляет водород, а A, B, C, D, R1, R2, R3, R4 и R5 имеют указанные для формулы I значения, алкилирующим агентом формулы R7-G, где G представляет подходящую отщепляемую группу, и основанием в инертном растворителе. Подходящие алкилирующие агенты включают галоиды /хлориды, бромиды, или иодиды/, алкилтозилаты, алкилмезилаты, алкилтрифлаты, α,β- ненасыщенные кетоны, α,β- ненасыщенные сложные эфиры, α,β- ненасыщенные альдегиды, α,β- ненасыщенные амиды и α,β- ненасыщенные нитрилы. Предпочтительны алкилгалоиды /иодиды/. Подходящие основания включают бикарбонат натрия, карбонат натрия, триалкиламины /например, триэтиламин/, натрий и гидрид натрия. Предпочтительным основанием является триэтиламин. Подходящие растворители включают метиленхлорид, хлороформ, четыреххлористый углерод, ацетонитрил, тетрагидрофуран, диэтиловый эфир, диоксан, N, N-диметилформамид, этанол, пропанол, метанол. Предпочтительным растворителем служит ацетонитрил. Реакцию ведут при температуре от около 0oC до около 150oC, предпочтительно, от около 25oC до около 65oC.
Соединения формулы I, в которых R3 представляет -CH3NH2 можно получить, восстанавливая соединение формулы I, где R3 представляет -CN, в инертном растворителе. Подходящие условия восстановления включают литийалюминийгидрид и никель Ренея вместе с водородом. Предпочтительными восстановительными условиями являются никель Ренея с водородом, предпочтительно, при давлении водорода три атмосферы. Подходящий инертный растворитель включает диэтиловый эфир, тетрагидрофуран, C1-C3спирты и N,N-диметилформамид. Предпочтительным растворителем является этанол. Реакцию ведут при температуре от около 0oC до около 100oC, предпочтительно, около 25oC.
Соединения формулы I, в которых R3 представляет -Ch2NH/C=O/R9, а R9 имеет значения, указанные для формулы I, можно получить за счет ацилирования соединения формулы I, где R3 представляет -CH2NH2, с активным производным сложного эфира карбоновой кислоты формулы R9CO2H, где R9 имеет указанные ранее значения, в инертном растворителе, обычно в присутствии основания. Подходящие активные сложные эфиры включают хлорангидриды, имидазилкарбоксамиды, ангидриды и пара-нитрофениловые сложные эфиры. Предпочтительными активными сложноэфирными производными являются, хлорангидриды. Подходящие основания включают триалкиламины, карбонат натрия и бикарбонат натрия. Предпочтительным основанием является триэтиламин. Подходящие инертные растворители включают диэтиловый эфир, тетрагидрофуран, 1,4-диоксан, метиленхлорид, 1,2-дихлорэтан, C1-C3спирты и N,N-диметилформамид. Предпочтительным инертным растворителем является этанол. Реакцию ведут при температуре от около 0oC до около 100oC, предпочтительно, при температуре около 25oC.
Соединения формулы I, в которых R3 представляет -CH2NH/C=O/NHR9, а R9 имеет указанные для формулы I значения, можно получить при взаимодействии соединения формулы I, где R3 представляет -CH2NH2, с изоцианатом формулы O= C=NR9, где R9 имеет указанные ранее значения, в инертном растворителе, обычно в присутствии основания. Подходящие основания включают триалкиламины, карбонат натрия и бикарбонат натрия. Предпочтительным основанием является триэтиламин. Подходящие инертные растворители включают диэтиловый эфир, тетрагидрофуран, 1,4-диоксан, метиленхлорид, 1,2-дихлорэтан, C1-C3спирты и N, N-диметилформамид. Предпочтительным инертным растворителем является этанол. Реакцию ведут при температуре от около 0oC до около 100oC, предпочтительно, около 25oC.
Соединения формулы V либо коммерчески доступны, либо их можно получить известными специалистам способами.
Соединения формулы VI и VII можно получить в соответствии со следующей схемой реакции (см. в конце описания).
Соединения формулы XI, где R18 представляет -N/R20/2, -NHCOR20 или 2,5-диметил-1Н-пиррол, а R20 представляет бензил или замещенный бензил, получают за счет алкилирования или ацилирования соединения формулы X, где R17 представляет -NH2, бензилом или замещенными бензилгалоидами /предпочтительно, бензилбромидом/, бензоилом или замещенными бензоилгалоидами /предпочтительно бензоилхлоридом/ в присутствии основания в инертном растворителе, или за счет конденсирования с 1,4-дикарбонильными соединениями в дегидративных условиях в инертном растворителе. Для реакции алкилирования подходящие основания включают бикарбонат натрия, карбонат натрия, гидрид натрия и триалкиламины. Предпочтительным основанием является триэтиламин. Подходящие растворители включают диметилформамид, простые эфиры /включая тетрагидрофуран/, и C1-C3спирты. Предпочтительным растворителем является тетрагидрофуран. Реакцию обычно ведут при температуре от около 25oC до около 100oC, предпочтительно, при температуре около 25oC. Для дегидративной конденсации предпочтительным 1,4-дикарбонильным соединением является ацетониилацетон. Подходящие растворители включают бензол, толуол и ксилолы. Предпочтительным растворителем является толуол. Дегидратацию можно осуществить, используя молекулярные сита, осушающие агенты или ловушку Дина-Старка. Предпочтительна ловушка Дина-Старка. Реакцию обычно ведут при температуре от около 70oC до около 150oC, предпочтительно при температуре от около 70oC до около 80oC.
Соединения формулы XII, где R19 представляет: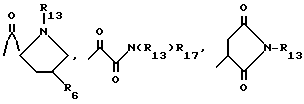
или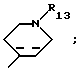
R6 и R7 имеют указанные для формулы I значения, а R13 имеет указанные для формулы IV значения, можно получить при взаимодействии соединения формулы XI, где R18 представляет -N/R20/2, -N/R20/2, -NHCOR20, или 2,5-диметил-1Н-пиррол, а R20 представляет бензил или замещенный бензил, с подходящим электрофильным соединением, в кислотных, щелочных или нейтральных условиях. Подходящие электрофильные соединения включают N-защищенные хлорангидриды пролина, N-защищенные-4-пиперидоны, оксалилхлорид или малеимиды. В случае оксалилхлорида, образующийся хлорид индол-3-гликосаминовой кислоты подвергают далее взаимодействию с вторичным амином формулы HNR7R8, где R7 и R8 имеют указанные для формулы I знамения. Подходящие кислоты включают минеральные кислоты, уксусную кислоту или муравьиную кислоту. Подходящие основания включают реагенты Гриньяра, включая этилмагний-бромид, первичные, вторичные или третичные амины, металлический натрий или калий, или гидрид натрия. Подходящие растворители включают простые эфиры /включая тетрагидрофуран и диэтиловый эфир/, бензол, толуол, уксусную кислому, муравьиную кислоту или C1-C4спирты. Реакцию обычно ведут при температуре от около 0oC до 150oC, предпочтительно, в интервале от около 0oC до около 120oC. Так например, в случае, если электрофильным соединением является N-защищенный хлорангидрид пролина, предпочтительным растворителем является бензол, реакцию предпочтительно, ведут в основных условиях, используя этилмагнийбромид, как предпочтительное основание, и реакцию ведут при температуре, предпочтительно, около 0oC; в том случае, если электрофильным соединением является N-защищенный-4-пиперидон, предпочтительным растворителем является метанол, реакцию ведут, предпочтительно, в основных условиях, используя метоксид натрия в качестве предпочтительного основания, и реакцию ведут при температуре, предпочтительно, около 65oC; в том случае, если электрофильным соединением является оксалилхлорид, предпочтительных растворителем является эфир, реакцию предпочтительно ведут в основных условиях, используя HNR7R8 в качестве предпочтительного основания, и реакцию ведут при температуре, предпочтительно около 0oC, а в том случае, если предпочтительным электрофильным соединением является малеимид, предпочтительным растворителем является уксусная кислота, реакцию, предпочтительно, ведут в кислотных условиях, используя уксусную кислоту в качестве предпочтительной кислоты, и реакцию ведут при температуре около 101oC.
Соединения формулы XII, где R1 имеет указанные для формулы I значения, и формулы XIV, где R12 имеют указанные для формулы IV значения, можно получить за счет восстановления соединения формулы XII, где R19 представляет: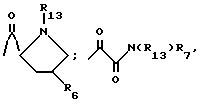
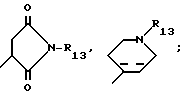
R6 и R7 имеют указанные для формулы I значения, R13 имеет указанные для формулы IV значения, a R18 имеет указанные для формулы XI значения, в инертном растворителе. Подходящие восстанавливающие агенты включают литийалюминийгидрид, литийборгидрид и диборан. Литийалюминийгидрид предпочтителен для получения соединений формулы XIII. Литийборгидрид предпочтителен для получения соединений формулы XIV. Подходящие инертные растворители включают тетрагидрофуран, диоксан и другие простые эфиры. Тетрагидрофуран является предпочтительным растворителем. Реакцию обычно ведут при температуре от около 25oC до около 100oC, предпочтительно, при температуре около 65oC.
Соединения формулы VII, где R12 имеет указанные для формулы IV значения, можно получить за счет удаления защиты у C5-индольного азота соединения формулы XIV, где R12 имеет указанные для формулы IV значения, a R18 имеет указанные для формулы XI значения, используя в качестве катализатора переходный металл и источник водорода, или полугидрохлорид гидроксиамина. Подходящие растворители включают C1-C4 спирты, этилацетат, ацетон и диметилформамид. Предпочтительным растворителем является этанол. Подходящие катализаторы - переходные металлы включают палладий на угле, гидроксид палладия на угле, и оксид платины. Предпочтительным катализатором является гидроксид палладия на угле. Подходящие источники водорода включают газообразный водород, аммонийформат и муравьиную кислоту. Предпочтителен газообразный водород, обычно при давлении от около 1 до около 3 атмосфер, предпочтительно, при давлении 3 атмосферы. Реакцию обычно ведут при температуре от около 25oC до около 100oC, предпочтительно, при температуре около 40oC. Если для удаления защиты у индольного азота используют полугидрохлорид гидроксиламина, предпочтительным растворителем является этанол, а предпочтительной температурой реакции температура от около 70oC до около 80oC.
Соединения формулы VI можно получить, удаляя защиту у C5-индольного азота соединения формулы XIII, где R1 имеет указанные для формулы I значения, а R18 имеет указанные для формулы XI значения, используя катализатор - переходный металл и источник водорода или полугидрохлорид гидроксиламина. Подходящие растворители включают C1-C4спирты, этилацетат, ацетон и диметилформамид. Предпочтительным растворителем является этанол. Подходящие катализаторы-переходные металлы включают палладий на угле, гидроксид палладия на угле и оксид платины. Предпочтительным катализатором является гидроксид палладия на угле. Подходящие источники водорода включают газообразный водород, аммонийформат и муравьиную кислоту. Предпочтителен газообразный водород, обычно при давлении от около 1 до около 3 атмосфер, предпочтительно при давлении 3 атмосферы. Реакцию обычно ведут при температуре от около 25oC до около 100oC предпочтительно около 40oC. Если для удаления защиты у индольного азота используют полугидрохлорид гидроксиламина, предпочтительным растворителем является этанол, а предпочтительной температурой реакции температура от около 70oC до около 80oC.
Соединения формулы X, где R17 представляет -NH2 или -NO2, либо коммерчески доступны, либо их можно получить известными специалистам способами.
Соединения формулы I, основные по природе, способны образовывать широкий круг различных солей с различными неорганическими и органическими кислотами. Хотя такие соли должны быть фармацевтически приемлемыми для введения животным, часто оказывается желательным /на практике/ вначале выделить соединение формулы I из реакционной смеси в виде фармацевтически неприемлемой соли, а затем просто превратить соединение в свободное основание за счет обработки его щелочным реагентом, и затем превратить это свободное основанием в фармацевтически приемлемую соль присоединения кислоты. Соли присоединения кислот основных соединений настоящего изобретения легко получить за счет обработки основного соединения практически эквивалентным количеством выбранной органической или минеральной кислоты в водном растворителе или в подходящем органическом растворителе, таком, как метанол или этанол. После осторожного выпаривания растворителя получают целевую твердую соль.
Кислоты, которые используют для получения фармацевтически приемлемых солей присоединения кислот основных соединений настоящего изобретения, являются такими кислотами, которые образуют нетоксичные соли присоединения кислот, то есть соли, которые содержат фармакологически приемлемые анионы, такие, как гидрохлорид, гидробромид, гидроиодид, нитрат, сульфат или бисульфат, фосфат или кислый фосфат, ацетат, лактат, цитрат или кислый цитрат, тартрат или битартрат, сукцинат, малеат, фумарат, глюконат, сахарат, бензоат, метансульфонат и памоат /то есть 1,1'-метилен-бис-/2 гидрокси-3- нафтоат//.
Соединения формулы I, которые также являются по своей природе кислыми, например, такие, в которых R2 содержит карбоксилат, способны образовывать основные соли с различными фармакологическими приемлемыми катионами. Примеры таких солей включают соли щелочных металлов или щелочноземельных металлов, и, в частности, соли нутрия и калия. Эти соли получают обычными способами. Химические основания, которые используют в качестве реагентов для получения фармацевтически приемлемых основных солей настоящего изобретения, являются такими основаниями, которые образуют нетоксичные основные соли с описанными кислыми соединениями формулы I. Такие нетоксичные основные соли включают соли, полученные из таких фармакологически приемлемых катионов, как натрий, кальций, калий и магний и т.д. Эти соли легко получить, обрабатывая соответствующие кислотные соединения водным раствором, содержащим целевые фармакологически приемлемые катионы, а затем выпаривая полученный раствор досуха, предпочтительно, при пониженном давлении. В другом варианте их можно получить, смещая слабощелочные растворы кислотных соединений и алкоксиды щелевых щелочных металлов вместе, а затем выпаривая полученные растворы досуха указанным ранее способом. В любом случае используют, предпочтительно, стехиометрические количества реагентов для того, чтобы обеспечить полноту реакции с максимальным выходом целевого окончательного продукта.
Соединения формулы I и их фармацевтически приемлемые соли /здесь и далее именуемые активными соединениями изобретения/ обладают психотерапевтическими активностями и являются сильными агонистами серотонина /5-НТ1/ и агонистами и антагонистами бензодиазепина, и могут быть использованы при лечении депрессий, беспокойства, нарушений аппетита, тучности, токсикомании, охватывающих головных болей, мигреней, хронической пароксимальной гемикрании и головных болей, связанных с сосудистыми нарушениями, болей, и других расстройств, связанных с дефицитом серотонергической нейротрансмиссии. Эти соединения можно также использовать как центрального действия антигипертензивные и вазодиляторные агенты. Активные соединения настоящего изобретения оценены как противомигреневые агенты за счет тестирования степени, до которой они имитируют суматриптан при контрактации выделенных у собак полосок подкожной вены ног /P.P.A.Humphrey et al., Br. J. Pharmacol., 94, 1128 /1988//. Этот эффект можно блокировать метиотепином, известным антагонистом серотонина. Известно, что суматриптан можно использовать при лечении мигреней и он приводит к селективному повышению сопротивляемости каротидных сосудов у анестезированных собак. Было выдвинуто предположение /W. Fenwick et al., Br. J. Pharmacol., 96, 83 /1989// что это является основой его эффективности.
Активные соединения настоящего изобретения можно также оценить за счет реакции транссудации плазменного протеина внутри мозгового вещества морских свинок с последующей электростимуляцией тригеминальных ганглий по способу Markowitz et al. , J. Neuro Sci., 7/12/, 4129-4136 /1967/. В этом анализе определяют степень имитации суматриптана как с точки зрения силы, так и эффективности.
Активность агониста серотонина 5-НТIA определяют ин витро рецепторным связывающим анализом, как описано для 5-НТIA рецептора, используя в качестве источника рецепторов кору головного мозга крыс и /3H/-8-ОН-DРАТ в качестве радиолиганда /D. Hoyer et al., Eur. J. Pharm., vol. 118, 13/1985// и как указано для 5-НТ1D рецептора, используя в качестве источника рецепторов бычий хвост и 3H серотонин в качестве радиолиганда /R.E. Heuring and S.J. Peroutka, J. Neuroscience, vol. 7, 894 /1987//. Сродство к бензодиазепиновым рецепторам определяют ин витро в рецепторном связывающем анализе, с использованием в качестве источника рецепторов мозжечок морских свинок и 3H флунитразепам в качестве радиолиганда /P. Supavilai and M. Karobath Eur., J. Pharm., vol. 70, 183 /1981//.
Композиции настоящего изобретения можно получить обычным способом, используя один или более из фармацевтически приемлемых носителей. Так, активные соединения настоящего изобретения могут быть подготовлены для перорального, буккального, через нос, парентерального /например, внутривенного, внутримышечного или подкожного/ или ректального введения, или в форме, пригодной для введения с помощью ингаляции или вдувания.
Для перорального введения фармацевтические композиции могут принимать форму, например, таблеток или капсул, полученных обычными способами, с такими фармацевтически приемлемыми эксципиентами, как связующие агенты /например, прежелатизированным кукурузным крахмалом, поливинилпирролидоном или гидроксипропилметилцеллюлозой/; наполнителями /например, лактозой, микрокристаллической целлюлозой или фосфатом кальция/; скользящими /например, стеаратом магния, тальком или двуокисью кремния/; разрыхляющими /например, картофельным крахмалом или натрийкрахмалгликолятом/; или смачивающими агентами /например, натрийлаурилсульфатом/. Таблетки могут быть покрыты оболочкой способами известными специалистам. Жидкие препараты для перорального введения могут принимать форму, например, растворов, сиропов или суспензий, или они могут быть представлены в виде сухих продуктов для растворения в воде или в другом подходящем растворителе перед применением. Такие жидкие препараты можно приготовить обычными способами с фармацевтически приемлемыми добавками, такими, как суспендирующие агенты /например, сироп, метилцеллюлоза или гидрированные пищевые жиры/; эмульгирующими агентами /например, лецитином или акацией/; неводными носителями /например, миндальным малом, сложными масляными эфирами или этиловым спиртом/; и консервантами /например, метил или пропил р-гидроксибензоатами или сорбиновой кислотой/.
Для буккального введения композиции могут иметь форму таблеток или пастилок, приготовленных обычными способами.
Активные соединения настоящего изобретения могут быть приготовлены для парентерального введения за счет инъекций, включая использование обычных способов катетеризации или за счет вливаний. Композиции для инъекций могут быть представлены в единичной дозированной форме, например, в ампулах или контейнерах для многих доз, с добавлением консервантов. Композиции могут иметь такие формы, как суспензии, растворы или эмульсии в масле или водных носителях, и могут содержать такие агенты, композиций, как суспендирующие, стабилизирующие и/или диспергирующие агенты. В другом варианте активный ингредиент может быть в виде порошка для смешивания с подходящим носителем, стерильной водой, не содержащей пиролена, перед применением.
Активные соединения настоящего изобретения могут быть приготовлены в виде ректальных композиций, таких как суппозитории или удерживаемые клизмы, содержащие, например, такие обычные основы для суппозиториев, как масло какао или другие глицериды.
Для введения через нос и или за счет ингаляций активные соединения настоящего изобретения обычно поставляют в форме раствором или суспензий в контейнерах под давлением, которые пациент вдыхает или впрыскивает, или в виде аэрозольных спреев в контейнерах под давлением или распылителях, с использованием подходящих пропеллентов, например, дихлордифторметана, трихлорфторметана, дихлортетрафтор этана, двуокиси углерода или других подходящих газов. В случае аэрозолей под давлением единичную дозу можно определить, если предусмотреть клапан для получения отмеренного количества. Контейнер под давлением или распылитель может содержать раствор или суспензию активного соединения. Капсулы и картриджи /изготовленные, например, из желатина/ для использования в ингаляторах или распылителях могут содержать смесь порошков соединения настоящего изобретения и подходящей основы, например, лактозы или крахмала.
Предполагаемая доза активных соединений настоящего изобретения для перорального, парентерального или буккального введения взрослым людям для лечения состояний перечисленных ранее /например, мигреней/ составляет от 0,1 до 200 мг активного ингредиента в единичной дозе, которую можно вводить, например, от 1 до 4 раз в день.
Аэрозольные композиции для лечения указанных ранее состояний /например, мигреней/ для взрослых приготавливают таким образом, чтобы каждая мерная доза или "распыл" аэрозоля содержала бы от 20 мкг до 1000 мкг соединения настоящего изобретения. Полная дневная доза с аэрозолем достигает величины в интервале от 100 мкг до 10 мг. Вводить можно несколько раз в день, например, 2, 3, 4 или 8 раз, используя каждый раз 1, 2 или 3 дозы.
Нижеследующие нелимитирующие примеры иллюстрируют получение соединений настоящего изобретения. Коммерческие реагенты используют без дополнительной очистки. Т. плавления даны без поправок. Данные ЯМР приведены в частях на миллион /мл/ и отнесены к доковому сигналу дейтерия того же растворителя. Удельное вращение определяют при комнатной температуре, используя линию натрия Д /589 нм/. Если нет других указаний, все масс-спектры получены в условиях электронного удара /Е1, 70 эВ/. Хроматографические данные получены на хроматографической колонке с силикагелем 32 - 63 мкм и под давлением азота /флеш- хроматография/. Комнатная температура соответствует 20 - 25oC.
Пример 1
Синтез 1-индолил-1Н-бензимидазолов и 1-индолил-3Н-имидазо- [4,5-b]пиридинов
Смесь 5-/2-нитроариламино/-1Н-индола /2,00 ммоля/ и Pd) на угле /20 вес. %/ в абсолютном этаноле встряхивают в атмосфере водорода /3 атм/ при комнатной температуре в течение 8 часов. Полученную реакционную смесь фильтруют через ЦелитR и полученный фильтрат выпаривают при пониженном давлении до получения неочищенного 5-/2-аминоариламино/-1Н-индола, который используют без дополнительной очистки. В другом варианте, смесь 5-/2-нитроариламино/-1Н-индола /2,00 ммоля/ и FeSO4 /5,5 г, 20 ммолей, 10 экв./ в смеси гидроксид аммония/вода/этанол /1:5:3, соответственно, полный объем 27 мл/ перемешивают при комнатной температуре в течение 24 часов. Полученную реакционную смесь фильтруют через Целит, и этанол удаляют из фильтрата выпаривая его при пониженном давлении. Оставшуюся водную смесь экстрагируют метиленхлоридом /3 х 26 мл/ и органические экстракты объединяют, сушат над сульфатом магния и выпаривают при пониженном давлении до получения неочищенного 5-/2-аминоариламино/-1Н-индола, который используют непосредственно.
Затем 5-/2-аминоариламино/-1Н-индол и либо диметилформамиддиметилацеталь /10 мл/, триэтилортоформат /муравьиную кислоту /5 мл/5 мл/, либо этоксиметиленмалононитрил /0,49 г, 4,01 ммоля 2,0 экв/. в 10 мл пропанола нагревают при кипячении с обратным холодильником в атмосфере азота в течение 1 - 24 часов, в зависимости от субстрата. Если используют диметилформамиддиметилацеталь, растворитель реакции меняют на толуол через 1 час, добавляют каталитическое количество /5 мг/ паратолуолсульфоновой кислоты и реакционный раствор нагревают при кипячении с обратным холодильником в атмосфере азота в течение 12 - 24 часов в зависимости от субстрата. Затем полученный реакционный раствор выпаривают при пониженном давлении, а остаток обрабатывают на хроматографической колонке, используя силикагель /примерно 50 г/ и соответствующую систему растворителей до получения соответствующего 1-индолил-1Н-бензимидазола или 1-индолил-3Н- имидазо[4,5-b]пиридина.
Этим же способом получают следующие соединения.
А. 5-циано-1-/3-/N-/2-метоксиэтил/пирролидин-2R-илметил/индол- 5-ил/-1Н-бензимидазол
5-/4-циано-2-нитрофениламино/-3-/N-/2-метоксиэтил/пирролидин- 2Н-илметил/1Н-индол используют. Восстанавливают каталитическим гидрированием, в реакции циклизации используют этоксиметиленмалононитрил в пропаноле) и реакционную смесь для циклизации нагревают в течение 2 часов. После хроматографической обработки 18: 1: 1 /этилацетат/метанол/триэтиламин/ получают указанное в заглавии соединение /83%/ в виде белой пены: 13C ЯМР /CD3OD/ δ: : 146,4, 142,4, 137,3, 136,4, 128,2, 126,6, 126,3, 125,0, 124,1, 119,0; 117,7, 114,9, 113,3, 112,2, 112,1, 105,6, 70,9, 65,6, 57,5, 54,4, 53,6, 30,2, 29,1 21,4; (α)25 = +33o /метиленхлорид, с = 1/. Масс-спектр высокого разрешения: рассчитано для C24 H25N5O 399,2054, найдено 399,2050.
Элементный анализ для C24H25N5O • 1,2 H2O:
Рассчитано: C 68,45 H 6,56 N 16,63
Найдено: C 68,21 H 6,18 N 16,82
В. 5-метоксикарбонил-1-/3-/N-/2-метоксиэтил/-пирролидин-2R- илметил/индол-5-ил/-1Н-бензимидазол
5-/4-метоксикарбонил-2-нитрофениламино/-3-(N-(2-метоксиэтил) пирролидин-2R-илметил)-1Н-индол используют. Восстанавливают каталитическим гидрированием, в реакции циклизации используют этоксиметиленмалононитрил в пропаноле) и реакционную смесь циклизации нагревают в точение 14 часов. После хроматографической обработки 38:1:1/этилацетат/метанол/триэтиламином получают указанное в заглавии соединение /75%/ в виде пены бледно-желтого цвета. 13C ЯМР /CD3OD/ δ: : 167,4, 145,5, 142,3, 137,7, 136,3, 128,1, 126,8, 124,9, 124,7, 124,6, 121,2, 117,7, 114,7, 113,0, 112,2, 110,5, 70,6, 65,8, 57,5, 54,4, 53,5, 51,2, 30,1, 28,9, 21,4; (α)25 = +63o /метиленхлорид, с = 1/. Масс-спектр высокого разрешения /МСВР/: Рассчитано для C25H28N4O3: 432,2163, найдено 432,2167.
C. 1-/3-/N-бензилоксикарбонил-4R-метоксипирролидин-2R- илметил/-индол-5-ил/-5-циано-1Н-бензимидазол
Используют 3-/N-бензилоксикарбонил-4R-метоксипирролидин-2R- илметил/-5-/4-циано-2-нитрофениламино/-1Н-индол. Восстанавливают FeSO4 • 7H2O, в реакции циклизации используют этоксиметиленмалонитрил в пропаноле, реакционную смесь циклизации нагревают в течение 2 часов. После хроматографической обработки используя градиент этилацетата в гексанах /1:2 до 1:1 до 1,0, соответственно/ получают указанное в заглавии соединение /47%/ в виде бледно-желтой пены. Rf = 0,15 в смеси этилацетат/гексаны /1:1/.
D. 5-циано-1-/3-/N-трет.-бутоксикарбонилпирролидин-2R- илметил/-индол-5-ил/-1Н-бензимидазол
Используют 3-/N-/трет. -бутоксикарбонил/пирролидин-2R илметил/-5-/4-циано-2-нитрофениламино/-1Н-индол. Восстанавливают каталитическим гидрированием, в реакции циклизации используют диметилформамиддиметилацеталь, реакционную смесь циклизации нагревают в течение 24 часов. После хроматографической обработки 25% гексанами в эфире получают указанное в заглавии соединение /71% в виде твердого белого вещества: Т. плавления с разложением 215,0oC; (α)25 = + 71o /метиленхлорид, с = 1/; МСВР: рассчитано для C26H27N5O2 441,2167, найдено, 441,2189.
Элементный анализ для C26H27N5O2 • 0,7C6H14 /гексаны/: 0,25 H2O:
Рассчитано: C 71,74 H 7,50 N 13,71
Найдено: C 72,10 H 7,10 N 13,60
Е. 1-/3-/N-циклопропилметилпирролидин-2R-илметил/индол- 5-ил/-3Н-имидазо[4,5-b]пиридин
Используют 3-/N-циклопропилметилпирролидин-2R-илметил/-5-/3- нитропирид-2-иламино/-1Н-индол. Восстанавливают каталитическим гидрированием, в реакции циклизации используют триэтилортоформат /муравьиную кислоту, реакционную смесь реакции циклизации нагревают в течение 2,6 часа. В результате хроматографической обработки смесью 9:1:0,1 /метиленхлорид : метанол : гидроксидаммония/ получают указанное в заглавии соединение в виде бледно-желтой пены: Rf = 0,55 в смеси метиленхлорид/метанол/гидроксидаммония /9:1:0,1/; 1H ЯМР /CDCl3/ δ: 8,44 /дд, J = 1,5 и 4,7 Гц, 1Н/, 8,39 /шир. с, NH/, 8,33 /с, 1Н/, 8,16 /дд, J = 1,5 и 8,1 Гц/1Н/, 7,80 /д, J = 1,9 Гц, 1Н/, 7,50-7,42 /м, 2Н/, 7,30 /дд, J = 4,7 и 8,0 Гц, 1Н/, 7,12 /д, J = 2,1 Гц, 1Н/, 3,43-3,35 /м, 1Н/, 3,22-3,12 /м, 1Н/, 2,94 /дд, J = 6,1 и 12,3 Гц/, 1Н/, 2,69-2,61 /м, 2Н/, 2,22-2,16 /м, 1Н/, 1,98 /дд, J = 7,2 и 18,3 Гц, 1Н/, 1,81-1,51 /3м, 6Н/, 0,99-0,888 /м, 1Н/, 0,58-0,43 /м, 2Н/; 13C ЯМР /CDCl3/ δ: 147,8, 144,3, 135,7, 128,4, 128,2, 127,0, 123,9, 118,8, 118,6, 115,3, 114,9, 112,0, 64,8, 59,9, 54,9, 30,9, 30,3, 22,2, 15,1. 10,1.
F. 5-циано-1-/3-/N-метидпирролидин-2R-илметил/индол-5-ил/-1Н- бензимидазол
Используют 5-/4-циано-2-нитрофениламино/-3-/N-метилпирролидин -2R-илметил/-1Н-индол. Восстанавливают каталитическим гидрированием, в реакции циклизации используют этоксиметиленмалонитрил в пропаноле, реакционную смесь реакции циклизации нагревают в течение 14 часов. В результате хроматографической обработки смесью этилацетат/метанол/триэтиламин /18:1:1/ получают указанное в заглавии соединение /85%/ в виде грязно-белой пены: 13C ЯМР /ДМСО-d6/ δ: : 146,9. 143,1, 137,1, 135,6, 128,1, 126,5, 126,3, 125,4, 124,4, 124,9, 119,8, 117,6, 114,8, 113,1, 112,5, 112,1, 104,4, 66,1, 57,0, 40,5, 30,8, 29,1, 21,7.
Элементный анализ для C22H21N5:
Рассчитано: C 74,34, H 5,96 N 19,70
Найдено: C 74,18 H 5,61 N 19,84
Масс-спектр высокого разрешения FAB* рассчитано 355,1999, найдено 355, 1889 (α)25 = +111o /метиленхлорид, с = 1.
G. 1-/3-/N-метилпирролидин-2R-илметил/индол-5-ил/-1Н- бензимидазол
Используют 3-/N-метилпирролидин-2R-илметил/-5-/2- нитрофениламино/-1Н-индол. Восстанавливают каталитическим гидрированием, в реакции циклизации используют триэтилортоформат/муравьиную кислоту, реакционную смесь нагревают в течение 12 часов. В результате хроматографической обработки смесью метиленхлорид/метанол/гидроксид аммония /9:1:0,1/ получают указанное в заглавии соединение /43%/ в виде бледно-желтой пены: 13C ЯМР /CDCl3/ δ: : 143,7, 143,2, 135,9, 134,9, 128,5, 128,0, 124,6, 123,5, 122,6, 120,2, 118,6, 115,1, 114,2, 112,4, 110,8, 66,7, 57,5, 40,9, 31,5, 29,9, 21,9 (α)25 = +59o /метиленхлорид, с = 0,4/;
Масс-спектр высокого разрешения FAB рассчитано для [C21H22N4 • H] 331,1925, Найдено: 331,1906.
* Здесь и далее FAB сокращения для бомбардировки быстрыми атомами
H. 4-метил-1-/3-/N-метилпирролидин-2R-илметил/индол-5/ил/- 3Н-имидазо[4,5-b]пиридин
Используют 5-/4-метил-3-нитропирид-2-иламино/-3-/N- метилпирролидин-2R-илметил/-1Н-индол. Восстанавливают каталитическим гидрированием, в реакции циклизации используют триэтилортоформат/муравьиную кислоту, реакционную смесь нагревают в течение 12 часов. В результате хроматографической обработки смесью метиленхлорид/метанол/гидроксид аммония /12:1:0,04/ получают указанное в заглавии соединение /29%/ в виде бледно-желтой пены: 13C ЯМР /CDCl3/ δ: 147.2, 144,6, 143,3, 139,8, 135,9, 135,4, 128,2, 126,8, 124,2, 119,6, 118,6, 115,2, 114,1, 112,1, 66,5, 57,4, 40,8, 31,5, 29,8, 21,8, 16,4(α)25 = 55o /метиленхлорид, с = 1, 2/. Масс-спектр высокого разрешения FAB для /C21H23N5 • H/ 346,2034, найдено 346,2039.
1. 1-/3-/N-метилпирролидин-2R-илметил/индол-5-ил/-3Н- имидазо[4,5-b]пиридин
Используют 3-/N-метилпирролидин-2R-илметил/-5-/3-нитропирид -2-иламино/-1Н-индол. Восстанавливают каталитическим гидрированием, в реакции циклизации используют смесь триэтилортоформат/ муравьиная кислота, реакционную смесь нагревают в течение 1,5 часа. В результате хроматографической обработки смесью метиленхлорид/метанол/гидроксидаммония /9:1:0,1/ получают указанное в заглавии соединение /30%/ в виде белой пены. 13C ЯМР /CDCl3/ δ 147,7, 144,8, 144,3, 135,8, 135,7, 128,3, 128,2, 127,0, 124,1, 118,8, 118,6, 115,3, 114,4, 112,1, 66,6, 57,5, 40,8, 31,4, 29,7, 21,8 (α)25 = +40o /метиленхлорид, c = 1,8/. Масс-спектр высокого разрешения рассчитано для C20H21N5 331,1799 найдено 331,1786.
J. 6-метокси-1-/3-/N-метилпирролидин-2R-илметил/индол-5- ил/-3Н-имидазо[4,5-b]пиридин
Используют 5-/6-метокси-3-нитропирид-2-иламино/-3-N- метилпирролидин-2R-идметил/-1Н-индол. Восстанавливают каталитическим гидрированием, реакционную смесь реакции циклизации нагревают в течение 4 часов. После хроматографической очистки смесью метиленхлорид/метанол/гидроксид аммония /12:1 : 0,04/ получают указанное в заглавии соединение /38%/ в виде желто-коричневой пены: Rf = 0,35 /в смеси метанолхлорид/метанол/гидроксид аммония /6:1:0,1/; 13C ЯМР /CDCl3/ δ 161,7, 144,3, 141,2, 135,4, 130,8, 130,4, 128,0, 127,5, 124,1, 117,9, 114,2, 111,9, 106,7, 66,8, 57,5, 53,7, 40,8, 31,4, 30,0, 21,8. Масс-спектр высокого разрешения рассчитано для C20H21N5: 361,1905. Найдено 361,1881.
K. 1-/3-/N-метилпирролидин-2R-илметил/индол-5-ил/-5- трифторметил-1H-бензимидазол
Используют 3-/N-метилпирролидин-2R-илметил/-5-/4- трифторметил-2-нитрофениламино/-1Н-индол. Восстанавливают каталитическим гидрированием, в реакции циклизации используют диметилформамиддиметилацеталь, реакционную смесь нагревают в течение 3 часов. После хроматографической обработки смесью метиленхлорид/метанол/гидроксид аммония /18:1:0,1/ получают указанное в заглавии соединение /49%/ в виде желтой пены: 13C ЯМР /CDCl3/ δ: 145,0, 143,3, 136,8, 135,8, 128,5, 127,7, 124,8, 124,5, 120,3, 118,2, 115,3, 114,5, 112,4, 111,1, 66,7, 57,5, 40,8, 31,4, 29,6, 21,9 (α)25 = +64o /метиленхлорид, с = 1/; Масс-спектр высокого разрешения рассчитано для C22H21F3N4: 398,1720, найдено: 398,1643. Элементный анализ для C22H21F3N4 • 0,1 H2O:
Рассчитано: C 66,02 H 5,34 N 13,99
Найдено: C 65,97 H 5,27 N 13,61
Z. 1-/3-/2-N,N-диметиламиноэтил/индол-5-ил/-3Н-имидазо[4,5- b]-пиридин
Используют 3-/2-N, N-диметиламиноэтил/-5-/3-нитропирид-2- иламино/-1Н-индол. Восстанавливают каталитическим гидрированием. В реакции циклизации используют диметилформамиддиметилацеталь, реакционную смесь реакции циклизации нагревают в течение 2,5 часа. В результате хроматографической обработки смесью метиленхлорид/метанол/гидроксид аммония /9: 1:0,1/ получают указанное в заглавии соединение /63%/ в виде белой пены:
1H ЯМР /CDCl3/ δ: 9,97 /шир. с, NH/, 8,44 /дд, J = 1,4 и 4,7 Гц/ 1Н/, 8,35 /с, 1Н/, 8,15 /дд, J = 1,4 и 8,1 Гц, 1Н/, 7,76 /шир. с/, 1Н/, 7,35-7,25 /м, 3H/, 6,98 /д, J = 2,0 Гц, 1Н/, 2,95-1,88 /м, 2Н/, 2,66-2,60 /м, 2Н/, 2,31 /с, 6Н/; 13C ЯМР /CDCl3/ δ: 146,6, 144,8, 144,4, 135,9, 135,7, 128,2, 127,9, 126,8, 123,8, 118,6, 115,0, 114,4, 112,2 60,0, 45,3; 23,5: FAB Масс-спектр низкого разрешения /м/Z/, относительная интенсивность /306 ///MH+, 19/, 155/67/, 135/32/, 119/100/ 103/44/.
M. 1-/3-/N-метилпирролидин-2R-илметил/индол-5-ил/-5-ил/-5- фенил-1Н-бензимидазол
Используют 3-/N-метилпирролидин-2R-илметил/-5-/4-фенил- нитрофениламино/-1Н-индол. Восстанавливают каталитическим гидрированием, в реакции циклизации используют смесь триэтилортоформат/муравьиная кислота, реакционную смесь нагревают в течение 3 часов. После хроматографической обработки смесью метиленхлорид/метанол/гидроксидаммоний /12:1:0,44/ получают указанное в заглавии соединение /75%/ в виде желто-коричневой пены.
13C ЯМР /CDCl3/ δ: 143,8, 141,8, 136,3, 135,7, 134,3, 128,8, 128,2, 127,5, 126,8, 124,2, 123,2, 122,1, 120,7, 118,8, 118,7, 115,2, 114,7, 112,3, 110,8, 66,5, 57,5, 40,9, 31,5, 29,8, 21,9. Масс-спектр низкого разрешения /м/z/, относительные интенсивности /407 //MH/+, 100/, 391/9/, 350/7/, 336/14/, 323/29/, 310/7/, 298/37/; FAB Масс-спектр высокого разрешения рассчитано для C27H26N4 • H 407,2238, Найдено 407,2198.
N. 6,7-дихлор-1-/3-/N-метилпирролидин-2R-илметил/индол-5-ил/- 1Н-бензимидазол
Используют 5-/5,6-дихлор-2-нитрофениламино/-3-/N- метилпирролидин-2R-илметил/-1Н-индол. Восстанавливают каталитическим гидрированием, в реакции циклизации используют смесь триэтилортоформат/муравьиная кислота, реакцию ведут при нагревании в течение 2,5 часа. После хроматографической обработки смесью метиленхлорид/метанол/гидроксид аммония /12: 1:0,04/ получают указанное в заглавии соединение /27%/ в виде грязно-белой пены:
13C ЯМР /CDCl3/ δ: 146,4, 143,6, 136,3, 132,5, 128,3, 127,6, 124,7, 124,3, 121,7, 119,3, 118,5, 116,9, 114,6, 111,1, 66,5, 57,5, 40,9, 31,5, 29,9, 21,9: Масс-спектр низкого разрешения /м/z, относительная интенсивность/ 398 /M+, 1/, 314 /4/, 216/2/, 84/100/, Масс-спектр высокого разрешения: рассчитано для C21H20Cl2N4 398,1066, найдено 398,1063.
O. 1-/3-/N-трет. -бутоксикарбонилпиперид-4-ил/индол-5-ил/-3Н- имидазо[4,5-b]пиридин
Используют 3-/N-трет.-бутоксикарбонилпиперид-4-ил/-5-/3- нитропирид-2-иламино/-1Н-индол. Восстанавливают каталитическим гидрированием, в реакции циклизации используют диметилформамиддиметилацеталь, реакционную смесь нагревают в течение 12 часов. После хроматографической обработки 5% метанолом в этилацетате с последующей перекристаллизацией из метиленхлорида получают указанное в заглавии соединение /39%/ в виде белого твердого вещества: т. пл. 212-218oC; Rf = 0,60 /5% метанол в этилацетате, FAB масс-спектр низкого разрешения /м/z, относительная интенсивность /418 / /MH+, 94/, 362/100/, 318/65/, 261/38/, 235/35/,
Элементный анализ для C24H27N5O2:
Рассчитано: C 69,04 H 6,52 N 16,77
Найдено: C 68,72 H 6,90 N 16,59
P. 1-/3-/N-метилпирролидин-3-ил/индол-5-ил/-3Н-имидазо [4,5-b]пиридин
Используют 3-/N-метилпирролидин-3-ил/-5-/3/нитропирид-2- иламино/-1Н-индол. Восстанавливают каталитическим гидрированием. В реакции циклизации используют диметилформамиддиметилацеталь, реакционную смесь нагревают в течение 24 часов. После хроматографической обработки смесью этилацетат/метанол/триэтиламин /9: 1: 1/ получают указанное в заглавии соединение /24%/ в виде белого твердого вещества; т. плавления 110,0-112,0oC;
13C ЯМР /CDCl3/ δ: 147,7, 144,8, 144,3, 136,2, 135,7, 128,3, 127,3, 126,8, 122,4, 119,0, 118,7, 115,6, 112,4, 62,3, 56,2, 42,2, 34,9, 32,1.
Масс-спектр высокого разрешения, рассчитано для C19H19N5 317,1643, найдено 317, 1665. Элементный анализ для C19H19N5 • 0,5 C4H8O4 /этилацетат/:
Рассчитано: C 68,08 H 6,53 N 18,90
Найдено: C 67,93 H 6,51 N 19,17
Q. 1-/3-/N-/2,2,2-трихлорэтоксикарбонил/пирролидин-2R- илметил/-индол-5-ил/-3Н-имидазо[4,5-b]пиридин
Используют 5-/3-нитропирид-2-иламино/-3-/N-/2,2,2- трихлорэтоксикарбонил/пирролидин-2R-илметил/-1Н-индол. Восстанавливают каталитическим гидрированием, в реакции циклизации используют смесь триэтилортоформат/муравьиная кислота, реакционную смесь нагревают в течение 3,5 часа. После хроматографической обработки 10% метанолом в метиленхлориде получают указанное в заглавии соединение /17%/ в виде желто-коричневой пены: Rf = 0,50 /5% метанол в метиленхлориде/.
R. 5-хлор-1-/3-/N-метилпирролидин-2R-илметил/индол-5-ил/-1Н- бензимидазол
Используют 5-хлор/4-хлор-2-нитрофенил/амино-3/N-метил- пирролидин-2R-илметил/-1Н-индол. Восстанавливают каталитическим гидрированием, в реакции циклизации используют смесь триэтилортоформат/муравьиная кислота, реакционную смесь нагревают в течение 4,5 часа. После хроматографической обработки смесью метиленхлорид/метанол/гидроксид аммония /12: 1:0,4 / получают указанное в заглавии соединение /34%/ в виде грязно-белого твердого вещества: Rf = 0,35 /метиленхлорид/метанол/гидроксидаммония 9:1:0,1/. FAB масс-спектр высокого разрешения, рассчитано для [C21H21ClN4H] + 365,1535, Найдено 365,1535 (α)25 = +61o метиленхлорид, с = 0,29/.
S. 6-Хлор-1-/3-/N-метилпирролидин-2R-илметил/индол-5-ил/-1Н- бензимидазол
Используют 5-/5-хлор-2-нитрофенил/амино-3-/N-метилпирролидин- 2R-илметил/-1Н-индол. Восстанавливают каталитическим гидрированием, в реакции циклизации используют смесь триэтилортоформат/муравьиная кислота, реакционную смесь нагревают в течение 4,5 часа. После хроматографической обработки смесью метиленхлорид/метанол/гидроксид аммония /12:1:0,4/ получают указанное в заглавии соединение /28%/ в виде бледно-желтого твердого вещества; Rf = 0,35 /метиленхлорид/метанол/гидроксид аммония 9: 1: 0,1/. FAB масс-спектр высокого разрешения, рассчитано для [C21H21ClN4 • H]+ 365,1535, найдено 366,1513; (α)25 = +57o /метиленхлорид, с = 0,27/.
T. 7-хлор-1-/3-/N-метилпирролидин-2R-илметил/индол-5-ил/-1Н- бензиимидазол
Используют 5-/6-хлор-2-нитрофенил/амино-3-/N- метилпирролидин-2R-илметил/-1Н-индол. Восстанавливают каталитическим гидрированием. В реакции циклизации используют смесь триэтилортоформат/ муравьиная кислота, реакционную смесь нагревают в течение 4,6 часа. В результате хроматографической обработки смесью метиленхлорид/метанол/гидроксид аммония /12:1:0,4 / получают указанное в заглавии соединение /28%/ в виде светло-желтого твердого вещества: Rf = 0,35 /метиленхлорид/метанол/гидроксид аммония 9:1:0,1/; FAB масс-спектр высокого разрешения, рассчитано для [C21H21ClN4 • H]+ 365,1535, найдено 365,1504 (α)25 = +45o /метиленхлорид, с = 1,36/.
U. 5-циано-1-/3-/N-трет.-бутоксикарбонилпиперид-4-ил/-индол- 5-ил/-1Н-бензимидазол
Используют 5-/4-циано-2-нитрофенил/амино-3-/N-трет- бутоксикарбонил-1,2,5,6-тетрагидропирид-4-ил/-1Н-индол. Восстанавливают каталитическим гидрированием. В реакции циклизации используют этоксиметиленмалонитрил, реакционную смесь нагревают в течение 48 часов. В результате хроматографической обработки 10% этилацетатом в метиленхлориде получают указанное в заглавии соединение /10%/ в виде коричневой пены: Rf = 0,2 /10% этилацетат в метиленхлориде/. Масс-спектр высокого разрешения, рассчитано для /C26H27N5O2/ 441,2167, Найдено 441,2169.
Y. 5-циано-1-/3-/N-трет. -бутиксикарбонил-1,2,5,6- тетрагидропирид-4-ил/индол-5-ил/-1Н-бензимидазол
Используют 5-/4-циано-2-нитрофенил/амино-3-/N-трет. - бутоксикарбонил-1,2,5,6-тетрагидропирид-4-ил/-1Н-индол. Восстанавливают водным FeSO4 в этаноле. В реакции циклизации используют этоксиметиленмалонитрил, реакционную смесь нагревают в течение 56 часов. В результате хроматографической обработки 8% ацетонитрилом в метиленхлориде получают указанное в заглавии соединение /10%/ в виде коричневой пены; Rf = 0,5 в 5% ацетоне в метиленхлориде; Масс-спектр высокого разрешения для C26H26N5O2 Рассчитано 439,2011, найдено 439,1999.
W. 5-циано-1-/3-/N-метилпирролидин-3-ил/индол-5-ил/-1Н- бензимидазол
Используют 5-/4-циано-2-нитрофенил/амино-3-/N- метилпирролидин-3-ил/индол-5-ил/-1Н-бензимидазол. Восстанавливают каталитическим гидрированием. В реакции циклизации используют триэтилортоформат/муравьиную кислоту, реакционную смесь нагревают в течение 2 часов. В результате хроматографической обработки смесью метиленхлорид/метанол/ гидроксидаммония 9:1;0,5 /получают указанное в заглавии соединение /22%/ в виде светло-желтого твердого вещества; Rf = 0,35 /метиленхлорид/метанол/гидроксид аммония 9:1:0,1/; 13C ЯМР /CDCl3/ δ 145,7, 143,3, 137,5, 136,5, 127,5, 126,8, 126,7, 125,4, 123,0, 120,3, 119,9, 118,5, 115,8 112,7, 111,9, 105,7, 62,8, 56,3, 42,3, 35,0, 32,3. FAB масс-спектр низкого разрешения /м/z, относительная интенсивность /342/MH+/.
X. 5-циано-1-/3-/-N-метилпирролидин-2R-илметил/индол-5-ил/- 1Н-пиридо[4,5-b]имидазол
Используют 5-/5-циано-3-нитропирид-2-ид/амино-3-/N- метилпирролидин-2R-илметил/-1Н-индол. Восстанавливают каталитическим гидрированием. В реакции циклизации используют триэтилортоформат/муравьиную кислоту, реакционную смесь нагревают в течение 2,5 часа. В результате хроматографической обработки смесью метиленхлорид/метанол/гидроксид аммония /12:1:0,4/ получают указанное в заглавии соединение /50%/ в виде светло-желтого твердого вещества: Rf = 0,2 /метиленхлорид/метанол/гидроксидаммония 12:1:0,4/:
13C ЯМР /CDCl3/ δ: 149,3, 147,7, 147,0, 136,0, 134,8, 131,9, 128,4, 125,8, 124,4, 118,4, 117,7, 115,3, 114,6, 112,3, 104,1, 66,6, 57,5, 40,8, 31,4, 29,7, 21,9; Масс-спектр высокого разрешения, рассчитано для C21H20N6 356,1752, найдено 356,1784; (α)25 = +78o /метиленхлорид, с = 0,48/. Элементный анализ для C21H20N6 • 0,5 H2O
Рассчитано: C 69,07 H 5,80 N 23,01
Найдено: C 69,11 H 5,82 N 22,62
Y. 5-метил-1-/3-/N-метилпирролидин-2R-илметил/индол-5-ил/-1Н- бензимидазол Используют 5-/4-метил-2-нитрофенил/амино-3-/N-метилпирролидин -2R-илметил/-1Н-индол. Восстанавливают каталитическим гидрированием. В реакции циклизации используют этоксиметиленмалонитрил, реакционную смесь нагревают в течение 24 часов. В результате хроматографической обработки смесью этилацетат/метанол/триэтиламин /8: 1: 1/ получают указанное в заглавии соединение /21%/ в виде пены коричневого цвета: Rf = 0,3 /этилацетат метанол/триэтиламин 8:1:1/;
3C ЯМР /CDCl3/ δ: 143,1, 143,0, 136,1, 132,6, 132,4, 127,9, 127,6, 124,9, 124,8, 118,5, 117,8, 114,2, 112,4, 110,1, 67,3, 56,8, 39,4, 30,7, 28,3, 21,0, 20,1. Масс-спектр низкого разрешения /м/z относительная интенсивность /344 /M+, 38/, 334 /10/, 318 /100/, 289 /18/. Масс-спектр высокого разрешения рассчитано для C22H24N4 344,2003, найдено 344,2030.
Пример 2
Общий способ алкилирования пирролидинов
К перемешиваемому раствору производного пирролидина /1,00 ммоля/ и триэтиламина /0,126 г, 1,25 ммоля/ или карбоната натрия /0,132 г, 1,25 ммоля, 1,25 эквив./ либо в безводном метиленхлориде, безводном ацетонитриле, абсолютированном этаноле, либо в изо-пропаноле /10 мл/ при комнатной температуре в атмосфере азота прикапывают алкилирующий агент /1,25 ммоля, 1,25 эквив./. Полученный реакционный раствор перемешивают затем в атмосфере азота при комнатной температуре или нагревают при кипении с обратным холодильником в течение 1 - 20 часов, в зависимости от субстрата. Полученную реакционную смесь обрабатывают на хроматографической колонке с силикагелем /примерно 25 г/, элюируя смесью метиленхлорид : метанол : гидроксид аммония /9:1:0,1/ до получения соответствующего алкилированного пирролидина. Таким способом получают:
А. 3-/N-циклопропилметилпирролидин-2R-илметил/-5-/3- нитропирид-2-ил-амино/-1Н-индол
Используют 3-/пирролидин-2R-илметил/-5-/3-нитропирид-2 иламино/-1Н-индол и бромметилциклопропан в качестве алкилирующего агента. В качестве основания используют триэтиламин, в качестве растворителя - метиленхлорид, реакционный раствор нагревают при кипении с обратным холодильником в течение 4 часов. В результате хроматографической обработки получают указанное в заглавии соединение /34%/ в виде пены темно-красного цвета:
1C ЯМР /CDCl3/ δ: 155,7, 151,4, 135,5, 134,3, 129,4, 128,2, 123,1, 119,3, 114,4, 114,3, 113,0, 111,4, 65,0, 59,9, 55,0, 30,9, 30,3, 22,2, 10,0. FAB масс-спектр низкого разрешения /м/z, относительная интенсивность /392 /MH+, 33/, 374/3/, 307/3/, 267/7/, 220/7/, 154/10/, 124/100/; Масс-спектр высокого разрешения рассчитано для C22H25N5O2 391,2011, найдено 391,1988.
В. 5-/2,5-диметил-1Н-пиррол-1-ил/-3-/N-/2-метоксиэтил/ пирролидин-2R-илметил/-1Н-индол
Используют 5-/2,5-диметил-1Н-пиррол-1-ил/-3-/пирролидин-2R- илметил/-1Н-индол. В качестве алкилирующего агента используют бромэтилметиловый эфир и иодид натрия. В качестве основания используют карбонат натрия, в качестве растворителя N, N-диметилформамид, реакционный раствор нагревают при температуре 120oC в течение 2 часов. В результате хроматографической обработки получают указанное в заглавии соединение /54%/ в виде грязно-белой пены: Rf = 0,75 в смеси метиленхлорид/метанол/гидроксидаммония /9:1:1/; масс-спектр низкого разрешения /м/z относительная интенсивность/ 351/M+, 48/, 304/10/, 210/57/, 128/100/; Масс-спектр высокого разрешения, рассчитано для C22H29N3O: 351,2313, найдено 351,2262.
C. 5-циано-1-/3-/N-/2-метоксиэтил/-4R-метоксипирролидин- 2R-илметил/индол-5-ил/-1Н-бензимидазол
Используют 5-циано-1-/3-(4R-метоксипирролидин-2R-илметил- индол-5-ил/-1Н-бензимидазол. В качестве алкилирующего агента используют бромэтилметиловый эфир и иодид натрия. В качестве основания используют карбонат натрия, а в качестве растворителя используют N,N-диметилформамид. Реакционный раствор нагревают при 130oC в течение 2 часов. В результате хроматографической обработки получают указанное в заглавии соединение /60%/ в виде грязно-белой пены: Rf = 0,60 /метиленхлорид/метанол/гидроксид аммония 9:1:1/;
13C ЯМР /CDCl3/ δ: 145,6, 143,3, 137,5, 135,8, 128,6, 127,2, 126,7, 125,6, 124,7, 119,8, 118,6, 115,5, 114,3, 112,5, 111,9, 105,8, 78,8, 71,6, 64,5, 60,0, 58,8, 56,5, 53,5, 37,9, 29,4; (α)25 = +61o /метанол, с = 0,53/. FAB Масс-спектр высокого разрешения, рассчитано для /C25H27N5O2 • H/ 430,2246, найдено 430,2222.
D. 5-циано-1-/3-(N-циклопропилметил)пирролидин-2R-илметил/- индол-6-ил/-1Н-бензимидазол
Используют 5-циано-1-/3-(пирролижин-2R-илметил)индол-5-ил/- 1Н-бензимидазол. В качестве алкилирующего агента используют (бромметил)циклопропан и иодид натрия. В качестве основания используют карбонат натрия, в качестве растворителя -N,N-диметилформамид, реакционный раствор нагревают при кипячении с обратным холодильником в течение 2 часов. В результате хроматографической обработки получают указанное в заглавии соединение /59%/ в виде бледно-желтой пены: Rf = 0,40 /метиленхлорид/метанол/гидроксид аммония /9:1:1/;
13C ЯМР /CDCl3/ δ: 146,4, 142,4, 137,2, 136,5, 127,4, 126,7, 126,0, 124,1, 119,0, 118,4, 114,7, 112,2, 112,7, 109,9, 105,6, 67,8, 58,8, 54,1, 29,5, 26,7, 21,3, 6,7 (α)25 = -29o /метиленхлорид, с = 0,5/; FAB масс-спектр низкого разрешения /м/z, относительная интенсивность /396 //MH+/, /100/, 309/21/, 273/9/; Полевой масс-спектр высокого разрешения рассчитано для [C25H25N5 • H] 396,2191, найдено 396,2191
Пример 3
Общий способ превращения N-бензилоксикарбонилпирролидинов в NH-пирролидины
Смесь N-бензилоксикарбонилпирролидина /10,0 ммоля/ и 20% гидроксида палладия на угле /1,0 г/ в абсолютированном этаноле /50 мл/ встряхивают в атмосфере азота /3 атмосферы/ при комнатной температуре в течение времени, зависящего от субстрата. Полученную реакционную смесь фильтруют через Целит и полученный фильтрат выпаривают при пониженном давлении. Остаток либо используют непосредственно в качестве соответствующего NH-пирролидина, либо остаток очищают на хроматографической колонке с силикагелем /примерно 100 г/, элюируя соответствующей системой растворителей до получения целевого NH-пирролидина.
Таким способом получают следующие соединения:
А. 5-/2,5-диметил-1Н-пиррол-1-ил/-3- /пирролидин-2R-илметил/-1Н-индол
Используют 5-(2,5-диметил-1Н-пиррол-1-ил)-3-(N- бензилоксикарбонилпирролидин-2R-илметил)-1Н-индол; время реакции составляет 18 часов. Полученный фильтрат выпаривают при пониженном давлении до получения указанного в заглавии соединения /100%/ в виде бледно-желтой пены: Rf = 0,36 в смеси метиленхлорид/метанол/ гидроксид аммония /9:1:0,1/;
13C ЯМР /CDCl3/ δ 135,8, 130,6, 129,4, 128,5, 127,8, 127,0, 124,6, 122,0, 118,1, 112,7, 111,9, 105,2, 59,8, 45,7, 31,5, 30,6, 24,9, 23,3.
B. 5-циано-1-/3-(4R-метоксипирролидин-2R-илметил)индол-5-ил /-1H-бензимидазол
Используют 1-/3-(N-бензилоксикарбонил-4R-метоксипирролидин- 2R-илметил)индол-5-ил/-5-циано-1Н-бензимидазол, и реакцию ведут в течение 24 часов. После хроматографической обработки, элюируя смесью метиленхлорид/метанол/гидроксид аммония /12: 1: 0,04/ получают указанное в заглавии соединение /44%/ в виде бледно-желтого аморфного вещества, Rf = 0,35 /метиленхлорид/-метанол/гидроксид аммония 9:1:0,1/;
13C ЯМР /CDCl3/ δ 145,7, 143,3, 137,6, 136,1, 128,3, 127,0, 126,7, 125,4, 125,0, 119,8, 118,4, 115,3, 114,1, 112,6, 111,9, 105,7, 82,1, 59,1, 56,5, 52,4, 38,7, 31,6. Масс-спектр высокого разрешения рассчитано для /C22H21N5O • H/ 372,1827, найдено 372,1825
Пример 4
Общий способ превращения N-трет.-бутоксикарбониламинов в NH-амины
К перемешиваемому раствор N-трет.-бутоксикарбониламина /2,00 ммоля/ в соответствующем безводном растворителе /10 мл/ при 0oC прикапывают раствор хлористого водорода в диоксане /4,0 М, 2 мл, 8,0 ммоля, 4 эквив./. Полученную реакционную смесь перемешивают при комнатной температуре в атмосфере азота в течение 12 часов, выпавший в осадок твердый продукт фильтруют до получения соответствующих NH-аминов в виде гидрохлоридной соли. Этим же способом получают следующие соединения:
А. 5-циано-1-/3-(пирролидин-2R-илметил)индол-5-ил/-1Н- бензимидазол
Используют 5-циано-1-/3-(N-трет. -бутоксикарбонилпирролидин- 2R-илметил/индол-6-ил/-1Н-бензимидазол, а в качестве растворителя используют метиленхлорид. После фильтрования получают указанное в заглавии соединение /83%/ в виде твердого вещества белого цвета; Т. плавления с разложением 185oМ. Масс-спектр низкого разрешения /м/z) относительная интенсивность /341/M+, 4/, 339/60/, 272/73/, 70/100/; Масс-спектр высокого разрешения, рассчитано для /C21H19N5/ 341,1643, найдено 341,1649.
В. 1-/3-(пиперид-4-ил)индол-8-ил/-3Н-имидазо[4,5-b]пиридин
Используют 1-/3-(N-трет.-бутоксикарбонилпиперид-4-ил)индол- 5-ил/-3Н-имидазо[4,5-b] пиридин, а в качестве растворителя используют метиленхлорид. После фильтрования получают указанное в заглавии соединение /100%/ в виде твердого продукта желтого цвета, Т. плавления 260-268oC /с бурным выделением газа/;
13C ЯМР /CD3OD/ δ 149,7, 145,6, 144,0, 138,5, 127,7, 126,0, 125,8, 125,6, 124,6, 123,9, 120,6, 119,7, 117,4, 113,7, 45,7, 32,6, 30,7; FAB масс-спектр /м/z, относительная интенсивность /318 /M+, 22/, 277/12/, 261/4/, 235/5/, 185/100/.
С. 5-циано-1-/3-(пиперид-4-ил)индол-5-ил/-1H-бензимидазол
Используют 5-циано-1-/3-(N-трет.-бутоксикарбонилпиперид-4- ил)индол-5-ил/-1Н-бензимидазол, а в качестве растворителя используют метиленхлорид. В результате фильтрования приучают указанное в заглавии соединение /64%/ в виде твердого продукта желтого цвета; ИК /KBr/ 2229 см-1; 13C ЯМР /CDOD/ δ: 137,4, 129,6, 126,6, 124,7, 123,6, 120,6, 119,2, 117,9, 116,4, 114,8, 112,8, 109,9, 44,6, 31,3, 29,4. Элементный анализ для C21H19N5 • 3HCl. • 1,25 H2O. Рассчитано: C 53,29 H 5,22 N 14,80
Найдено: C 53,63 H 5,34 N 14,68
D. 5-циано-1-/3-(1,2,5,6-тетрагидропирид-4-ил)-индол-5-ил/-1Н- бензимидазол
Используют 5-циано-1-/3-(N-трет.бутоксикарбонил-1,2,5,6- тетрагидропирид-4-ил)индол-5-ил/-1Н-бензимидазол, а в качестве растворителя используют метиленхлорид. В результате фильтрования получают указанное в заглавии соединение /75%/ в виде твердого продукта желтого цвета; Т. плавления с разложением 240oC; ИК /KBr/ 2228 см-1; 13C ЯМР /CD3OD/ δ: 144,4, 137,9, 133,6, 131,1, 129,9, 126,0, 125,3, 125,2, 120,1, 118,4, 118,3, 117,6, 117,3, 116,1, 114,8, 113,2, 112,9, 110,4, 66,7, 42,0, 40,9.
Элементный анализ для C21H17N5 • 1,1 C4H8O2 /диоксан/ • 1,1 HCl:
Рассчитано: C 64,03 H 5,69 N 14,70
Найдено: C 64,20 H 5,54 N 14,47
Пример 5
5-гидроксиметил-1-/3-(N-(-метоксиэтил)пирролидин-2R-илметил)- индол-5-ил/-1Н-бензимидазол
К перемешиваемому раствору литийалюминийгидрида /0,081г, 2,13 ммоля, 3 экв. / в безводном тетрагидрофуране /6 мл/ добавляют раствор 5-метоксикарбонил-1-/3-(N-(2-метоксиэтил) пирролидин-2R- илметил)индол-5-ил/-1H-бензимидазола /0,31 г, 0,72 ммоля/ в безводном тетрагидрофуране /4 мл/. Полученную реакционную смесь перемешивают при комнатной температуре в атмосфере азота в течение 1 часа. Затем добавляют декагидрат сульфата натрия /5 г/ осторожно, затем 0,1 мл воды и 10 мл этилацетата. Полученную смесь перемешивают при комнатной температуре в течение 1 часа. Затем смесь фильтруют через Целит, а полученный фильтрат выпаривают при пониженном давлении до получения указанного в заглавии соединения /0,19 г, 65%/ в виде бледно-коричневой пены; Rf = 0,40 /этилацетат/метанол/триэтиламин 18:1:1/;
13C ЯМР /CD3OD/ δ: 143,6, 142,8, 136,4, 136,1, 133,8, 128,1, 127,3, 124,7, 123,0, 117,7, 117,4, 114,5, 113,1, 112,1, 110,4, 70,8, 65,6, 64,1, 57,5, 54,4, 53,5, 30,2, 29,1, 21,4; Масс-спектр высокого разрешения, рассчитано для /C24H28N4O2/ 404,2214, Найдено 404,2121.
Пример 6
1-/3-(2-аминоэтил)индол-5-ил/-3Н-имидазо[4,5-b]пиридин
К перемешиваемой смеси литийалюминийгидрида /0,22 г, 5,80 ммоля, 5 экв./ в 10 мл безводного тетрагидрофурана добавляют 5-/3- (2-нитроэтенил)индол-5-ил/-1Н-бензимидазол /0,35 г, 1,14 ммоля/ быстро, но порциями в твердом виде. Полученную реакционную смесь перемешивают при комнатной температуре в атмосфере азота в течение 12 часов. Затем к реакционной смеси осторожно добавляют 10 г декагидрата сульфата натрия, затем 0,5 мл воды и 25 мл этилацетата. Полученную реакционную смесь интенсивно перемешивают при комнатной температуре в атмосфере азота в течение 1 часа. Затем реакционную смесь фильтруют через Целит, а полученный фильтрат выпаривают при пониженном давлении. Остаток обрабатывают на хроматографической колонке с силикагелем /примерно 30 г/) и элюируют смесью этилацетат/метанол/триэтиламин/ гидроксид аммония /8: 1: 1:0,1/ до получения указанного в заглавии соединения /41%/ в виде прозрачного бесцветного масла: Rf = 0,10 /этилацетат/метанол/триэтиламин/гидроксид аммония 8:1:1:0,1 /. Это масло растворяют в смеси метанол/метиленхлорид /0,5 мо/ 4 мл соответственно/, и к этому раствору добавляют малеиновую кислоту /0,050 г, 0,43 ммоля/. Полученный твердый продукт фильтруют до получения указанного в заглавии соединения в виде его малеатной соли /0,085 г/; Т. плавления 195,0 - 196,0oC с интенсивным газовыделением
1H ЯМР /ДМСО-d6/ δ: 11,3 /шир.с, NH/, 8,81 /с, 1Н/, 8,42 /дд J = 1,40 4,7 Гц/, 1Н/, 8,22 /дд, J = 1,4 и 8,0 Гц, 1Н/, 7,97 /д, J = 1,7 Гц, 1Н/, 7,78 /шир. с, 2Н/, 7,61-7,52 /м, 2Н/, 7,43-7,36 /м, 2Н/, 6,04 /с, 2Н/, 3,37 /шир. с, 2Н/, 3,16-3,01 /м, 4H/. Элементный анализ для C16H15N5 • C4H4O4 /малеиновая кислота/ • 0,1 H2O:
Рассчитано: C 60,78 H 4,89 N 17,72
Найдено: C 60,58 H 4,53 N 17,50
Пример 7
1-/3-(пирролидин-2R-илметил)индол-5-ил/-3Н-имидазо[4,5-b] пиридин
Смесь 1-/3-(N-2,2,2-трихлорэтоксикарбонил)пирролидин-2R- илметил)индол-5-ил/-3Н-имидазо[4,5-b] пиридина /0,090 г, 0,18 ммоля/ в цинковый пыли /0,45 г/ в растворе тетрагидрофурана /2 мл/ и водного KH2PO2 /1,0 М, 1 мл/ перемешивают при комнатной температуре в течение 12 часов. Затем к реакционной смеси добавляют карбонат натрия /0,35 г/ и полученную смесь фильтруют через Целит, обильно промывая этанолом. Объединенные фильтраты выпаривают при пониженном давлении, а остаток обрабатывают на хроматографической колонке с силикагелем /примерно 1 г/ и элюируют смесью метиленхлорид/метанол/гидроксидаммония /6:1:0,1 до получения указанного в заглавии соединения /0,022 г, 40%/ в виде аморфного твердого белого вещества:
1H ЯМР /CDCl3/ δ: 9,20 /шир.с, NH/, 8,44 /дд, J = 1,4 и 4,8 Гц, 1Н/, 8,31 /с, 1Н/, 8,15 /дд, J = 1,4 и 8,1 Гц, 1Н/, 7,80 /д, J = 1,7 Гц, 1Н/, 7,44/д, J = 8,5 Гц, 1Н/, 7,38 /дд, J = 1,9 и 8,6 Гц, 1Н/, 7,29 /дд, J = 4,8 и 8,1 Гц, 1Н/, 7,07 /с, 1Н/, 3,38-3,30 /м, 1Н/, 3,06-2,80 /м, 4Н/, 2,48 /шир. с, NH/, 1,95-1,64 /м, 3Н/, 1,49-1,40 /м, 1Н/, Масс-спектр низкого разрешения /м/z, относительная интенсивность /317 /M+, 1/, 315/25/, 248 /100/, 129/39/, 70/80, Масс-спектр высокого разрешения рассчитано для /C19H19N5/ 317,1643, найдено 317,1659.
Пример 8
Общий способ получения 5-(2-нитроариламино)-1Н-индолов
Раствор 5-амино-1Н-индола /2,00 ммоля/, 2 нитрогалоидарена /3,00 ммоля, 1,5 экв/ и основания / при необходимости 3,00 ммоля/ в подходящем безводном растворителе /10 мл/ в зависимости от субстрата либо нагревают при кипячении с обратным холодильником в атмосфере азота в течение 1-18 часов, либо перемешивают при комнатной температуре 1 час. Реакционную смесь выпаривают при пониженном давлении, остаток обрабатывают на хроматографической колонке с силикагелем /примерно 50 г/, элюируя метиленхлоридом : метанолом : гидроксидом аммония /9: 1:0,1/ или другой подходящей системой растворителей до получения 5-арил-1Н-индольного производного. В некоторых случаях для получения аналитически чистых образцов соответствующих 5-/2-нитроариламино/-1Н-индолов после хроматографической обработки проводят перекристаллизацию твердых образцов. В соответствии с этим способом получают следующие соединения:
A. 5-(4-циано-2 нитрофениламино)-3-(N-(2-метоксиэтил) пирролидин-2R-илметил)-1Н-индол
Используют 5-амино-3-(К-(2 метоксиэтил)пирролидин-2R- илметил)-1Н-индол и 4-хлор-3-нитробенэонитрил. В качестве основания используют триэтиламин, в качестве растворителя - абсолютированный этанол, реакционную смесь кипятят с обратным холодильником в течение 2 часов. В результате хроматографической обработки используя в качестве элюента смесь этилацетат/метанол/триэтиламин /18:1:1/ получают указанное в заглавии соединение /74%/ в виде пены красного цвета: Rf = 0,55 /Этилацетат/метанол/триэтиламин 18:1:1/;
13C ЯМР /CD3OD/ δ: 148,8, 138,0, 137,1, 132,9, 132,7, 129,8, 129,6, 125,6, 121,0, 119,1, 118,3, 117,6, 114,2, 113,6, 99,4, 72,2, 67,2, 59,0, 55,9, 55,0, 31,6, 30,5, 22,9.
Элементный анализ для C23H25N5O3 • 0,5 H2O:
Рассчитано: C 64,47 H 6,11 N 16,34
Найдено: C 64,33 H 5,94 N 16,19
В. 5-(4-метоксикарбонил-2-нитрофениламино)-3-(N-(2- метоксиэтил)-пирролидин-2R-ил-метил)-1Н-индол
Используют 5-амино-3-(1-(2-метоксиэтил)пирролидин-2R- илметил-1Н-индол и метил-4-хлор-3-нитробензоат. В качестве основания используют триэтиламин, в качестве растворителя используют абсолютированный этанол, реакционную смесь кипятят с обратным холодильником в течение 2 часов. В результате хроматографической обработки, используя смесь этилацетат/метанол/триэтиламин/ /34:1: 1/ получают указанное в заглавии соединение /88%/ в виде пены красного цвета: Rf = 0,60 /этилацетат/метанол/триэтиламин 18:1:1/:
13C ЯМР /CD3OD/ δ: 165,5, 147,7, 135,5, 134,9, 131,1, 128,6, 128,5, 128,3, 124,1, 119,7, 117,3, 116,0, 115,6, 112,7, 112,1, 70,7, 65,8, 57,5, 54,4, 53,6, 51,2, 30,2, 29,1, 21,4. Масс-спектр высокого разрешения для C24H27N4 O5 рассчитано 452,2061, найдено 452,1965.
Элементный анализ для C24H27N4O5:
Рассчитано; C 63,08 H 6,29 N 12,26
Найдено: C 63,12 H 6,38 N 12,16
C. 3-(N-бензилоксикарбонил-4R-метоксипирролидин-2R-илметил- -5-(4-циано-2-нитрофениламино)-1H-индол
Используют 5-амино-3-(N-бензилоксикарбонил-4R-метокси- пирролидин-2R-илметил)-1Н-индол и 4-хлор-3-нитробензонитрил. В качестве основания используют триэтиламин, а в качестве растворителя - абсолютированный этанол, реакционную смесь кипятят с обратным холодильником в течение 3,5 часа. В результате хроматографической обработки, используя этилацетат/гексаны /1:3/ получают указанное в заглавии соединение /70%/ в виде пены красного цвета: Rf = 0,45 /этилацетат/гексаны 1:1/.
D. 3-(N-трет. -бутоксикарбонилпирролидин-2R-илметил/)-5-(4- циано-2-нитрофениламино)-1Н-индол
Используют 5-амино-3-(N-трет. -бутоксикарбонилпирролидин- 2R-илметил)-1Н-индол и 4-хлор-3-нитробензонитрил. В качестве основания используют триэтиламин, в качестве растворителя используют абсолютированный этанол, реакционную смесь нагревают при кипении с обратным холодильником в течение 3 часов. В результате обработки на хроматографической колонке, элюируя смесью метиленхлорид/метанол/гидроксид аммония /18:1:0,1/, получают указанное в заглавии соединение /82%/ в виде пены красного цвета: Т. плавления с разложением 60oC; ИК /KBr/ 2226, 1688, 1681, 1671, 1621 см-1; Масс-спектр низкого разрешения /м/z относительная интенсивность / 461/ M+, 23/, 431/27/, 388/13/, 291/50/; 244/43/, 170/53/, 114/75/, 70/100/; Масс-спектр высокого разрешении, рассчитано для /C25H27N5O4/ 461,2065, найдено 461,2071.
E. (R)-5-(3-нитропирид-2-иламино)-3-(пирролидин-2-илметил)- 1H-индол
Используют (R)-5-амино-3-(пирролидин-2-илметил)индол и 2-хлор-3-нитропиридин. В качестве основания используют ацетат натрия, а в качестве растворителя используют уксусную кислоту, реакционную смесь нагревают при кипении с обратным холодильником /116oC/ в течение 2 часов. После хроматографической обработки получают указанное в заглавии соединение /23%/ в виде пены темно-красного цвета:
1H ЯМР /CDCl3/ δ: 10,05 /шир, с, 1Н/, 9,23 /шир, с., 1Н/, 8,49 /дд, J = 1,8 и 8,3 Гц, 1Н/, 8,39 /1,8 и 4,5 Гц, 1Н/, 7,70 /д, J = 1,7 Гц, 1H/, 7,33-7,22 /м, 2Н/, 6,98 /с, 1Н/, 6,73 /дд, J = 4,5 и 8,3 Гц, 1Н/, 3,47-3,34 /м, 1Н/, 3,10-2,97 /м, 1Н/ 2,97-2,78 /м, 3Н/, 1,99-1,64 /м, 3Н/, 1,56-1,42 /м, 1Н/;
13C ЯМР /CDCl3/ δ: 155,7, 151,5, 135,5, 134,5, 129,2, 128,1, 127,8, 123,8, 119,4, 114,3, 113,0, 111,6, 59,5, 45,7, 31,3, 30,6, 24,7; FAB масс-спектр низкого разрешения /м/z, относительная интенсивность /338/6/ /MH+/, З09 /12/, 155/49/, 135/38/, 119/100/.
Элементный анализ для C18H19N5O2 • 0,67 C2H4O2 /уксусная кислота/:
Рассчитано: C 61,53 H 5,79 N 18,56
Найдено: C 61,57 H 5,74 N 18,82
F. 5-(4-циaнo-2-нитpфенилaминo)-3-(N-мeтилпиppoлидин-2- илметил)-1Н-индол
Используют (R)-5-амино-3-(N-метилпирролидин-2-илметил)-1H- индол и 4-хлор-3-нитробензонитрил. В качестве основания используют триэтиламин, а в качестве растворителя - абсолютированный этанол, реакционную смесь нагревают при кипении с обратным холодильником в течение 4 часов. После хроматографической обработки получают указанное в заглавии соединения /80%/ с виде твердого вещества красного цвета; Т. плавления 170-171,0oC:
13C ЯМР /CDCl3/ δ: 147,3, 137,1, 135,4, 132,0, 131,4, 128,6, 128,0, 125,3, 120,6, 117,9, 118,1, 116,3, 113,1, 111,9, 99,1, 68,1, 57,3, 40,6, 31,2, 28,1, 21,9. Элементный анализ для C21H21N5O2 • 0,05 CH2Cl2:
Рассчитано: C 66,59 H 5,60 N 18,44
Найдено: C 66,56 H 5,26 N 18,42
G. 3-(N-метилпирролидин-2-илметил)-5-(2 нитрофениламино)-1H- индол
Используют (R)-5-амино-3-(N-метилпирролидин-2-илметил)-1H- индол и о-нитрофторбензол. В качестве основания используют триэтиламин, а в качестве растворителя используют о-нитрофторбензол, реакционную смесь кипятят с обратным холодильником в течение 24 часов. После хроматографической обработки получают указанное в заглавии соединение /48%/ в виде аморфного твердого вещества красного цвета:
1H ЯМР /CDCl3/ δ: 9,62 /шир. с, NH/, 8,77 /шир.с, NH/, 8,19 /дд J = 8,7 и 1,5 Гц, 1Н/, 7,47 /д, J = 1,6 Гц, 1Н/, 7,38 /д, J = 8,5 Гц, 1Н/, 7,29-7,23 /м, 1H/, 7,09-7,00 /м, 3Н/, 6,69-6,64 /м, 1H/, 3,20-3,12 /м, 2Н/, 2,63 /дд, J = 14,0 и 9,5 Гц, 1Н/, 2,54-2,45 /с, 3Н/, 2,25 /дд, J = 17,1 и 9,2 Гц, 1Н/, 1,91-1,54 /м, 4Н/,
13C ЯМР /CDCl3/ δ: 145,4, 135,7, 134,8, 132,1, 130,1, 128,6, 126, 123,6, 120,7, 116,4, 116,1, 114,1, 112,2, 66,7, 57,5, 40,8, 31,5, 29,8, 21,9. FAB масс-спектр высокого разрешения рассчитано для /C20H22N4O2 • H/ 351,1823, найдено 351,1797.
Н. 5-(4-метил-3-нитропирид-2-иламино)-3-(1-метилпирролидин-2- илметил)-1Н-индол
Используют (R)-5-aминo-3-(N-мeтилпирpoлидин-2-илмeтил)-1H- индол и 2-хлор-4-метил-3-нитропиридин. В качестве основания используют триэтиламин, а в качестве растворителя используют абсолютированный этанол, реакционную смесь кипятят с обратным холодильником в течение 24 часов. В результате хроматографической обработки получают указанное в заглавии соединение /34%/ в виде аморфного твердого продукта красного цвета: 1H ЯМР /CDCl3/ δ: 9,26 /шир. с, NH/, 8,79 /шир. с, NH/, 8,10 /д, J = 4,8 Гц, 1Н/, 7,64 /д, J = 1,7 Гц, 1Н/, 7,29 /д, J = 8,5 Гц, 1Н/, 7,17 /дд, J = 8,5 и 1,9 Гц, 1Н/, 6,97 /д, J = 2,2 Гц, 1Н/, 6,56 /д, J = 4,8 Гц, 1Н/, 3,25-3,16 /м, 2Н/, 2,67 /дд, J = 13,2 и 9,4 Гц, 1Н/, 2,64-2,56 /м, 1Н/, 2,56 /с, 3Н/, 2,46 /с, 3Н/, 2,30 /дд, J = 17,7 и 9,4 Гц, 1Н/, 1,90-1,60 /м, 4Н/;
13C ЯМР /CDCl3/ δ: 152,2, 151,5, 146,6, 134,3, 131,0, 130,0, 127,9, 123,4, 119,4, 117,1, 114,0, 113,3, 111,3, 111,6, 67,0, 57,4, 40,7, 31,4, 29,5, 21,8, 21,7;
FAB масс-спектр высокого разрешения, рассчитано для /C20H23N5O2 • H/ 366,1932, найдено 366,1957.
1. (R)-3-(N-метилпирролидин-2-илметил)-5-(3-нитропирид-2- иламино)-1Н-индол
Используют (R)-3-(N-метилпирролидин-2-илметил)индол и 2-хлор-3-нитропиридин. В качестве основания используют триэтиламин, а в качестве растворителя используют ацетонитрил. Реакционную смесь кипятят с обратным холодильником в течение 3,5 часа. После хроматографической обработки получают указанное в заглавии соединение /81%/ в виде пены темно-красного цвета: 1H ЯМР /CDCl3/ δ: 10,11 /шир. с, 1Н/, 8,52 /дд, J = 1,8 и 8,4 Гц, 1Н/, 8,43 /1,8 и 4,5 Гц, 1Н/ 8,33 /шир, с, 1Н/, 7,77 /д, J = 1,7 Гц, 1Н/, 7,35 /д, J = 8,7 Гц, 1Н/, 7,26 /дд, J = 2,0 и 8,6 Гц, 1Н/, 7,03/д, J = 2,1 Гц, 1Н/, 6,74 /дд, J = 4,4 и 8,4 Гц, 1Н/, 3,21 - 3,12 /м, 2Н/, 2,68- 2,58 /м, 1Н/, 2,54 - 2,46 /м, 1Н/, 2,47 /с, 3Н/, 2,28-2,18 /м, 1Н/, 1,89-1,73 /м, 2Н/, 1,73-1,54 /м, 2Н/;
13C ЯМР /CDCl3/ δ: 155,7, 151,5, 135,5, 134,3, 129,8, 128,2, 128,1, 123,1, 119,4, 114,3, 113,0, 111,4, 66,7, 57,5, 40,8, 31,5, 29,9, 21,9. Элементный анализ для C19H21N5O2 • 1/3H2O:
Рассчитано: C 63,85, H 6,11 N 19,59
Найдено: C 63,86 H 5,86 N 19,31
J. 5-(6-метокси-3-нитропирид-2-иламино)-3-(N-метилпирролидин -2-илметил)-1Н-индол
Используют (R)-5-амино-3-(N-метилпирролидин-2-илметил)-1H- индол и 2-хлор-5-метокси-3-нитропиридин. В качестве основания используют триэтиламин, а в качестве растворителя используют абсолютированный этанол, реакционную смесь нагревают при кипении с обратным холодильником в течение 5,5 часа. В результате хроматографической обработки получают указанное в заглавии соединение /54%/ в виде аморфного вещества красного цвета:
1H ЯМР /CDCl3/ δ: 8,80 /шир, с, NH/, 8,37 /д, J = 9,1 Гц, 1Н/, 7,85 /с, 1Н/, 7,34-7,28 /м, 2H/, 7,03 /д, J = 2,0 Гц, 1Н/, 6,14 /д, J = 9,1 Гц 1Н/, 3,85 /с, 3Н/, 3,19-3,11 /м, 2Н/, 2,61 /дд, J = 13,8 и 9,5 Гц, 1Н/, 2,54-2,45 /м, 1Н/, 2,45 /с, 3Н/, 2,24 /дд, J = 17,1 и 9,3 Гц, 1Н/, 1,91-1,54 /м, 4Н/;
13C ЯМР /CDCl3/ δ: 166,9, 151,3, 138,2, 134,0, 129,6, 127,8, 123,3, 122,0, 118,6, 114,1, 113,3, 111,1, 102,0, 66,5, 57,5, 54,7, 40,8, 31,6, 29,9, 21,9. Масс-спектр высокого разрешения, рассчитано для /C20H23N5O3/ 381,1803, найдено 381,1299.
К. 3-(N-метилпирролидин-2-илметил)-5-(4-трифторметил-2- нитрофениламино)-1Н-индол
Используют (R)-5-амино-3-(N-метилпирролидин-2-илметил)-1H- индол и 4-хлор-3-нитробензотрифторид. В качестве основания используют триэтиламин, в качестве растворителя используют абсолютированный этанол, реакционную смесь кипятят с обратным холодильником в течение 4,5 часа. В результате хроматографической обработки получают указанное в заглавии соединение /38%/ в виде пены красного цвета: Rf = 0,30 /метиленхлорид/метанол/гидроксид аммония 9:1: 0,1/.
13C ЯМР /CDCl3/ δ: 147,0, 139,7, 135,1, 131,6, 131,0, 129,2, 128,5, 124,7, 124,2, 120,7, 118,6, 116,8, 113,6, 112,6, 67,1, 57,4, 40,8, 31,3, 29,2, 21,9. FAB масс-спектр низкого разрешения 419 /MH+/. Элементный анализ рассчитано для C21H21F3N4O2 • 0,6 CH2Cl2:
Рассчитано: C 55,27 H 4,77 N 11,94
Найдено: C 55,44 H 4,58 N 11,52
L. 3-(2-диметиламиноэтил)-6-(3-нитропирид-2-иламино)-1Н-индол
Используют 5-амино-3-(2-диметидаминоэтил)индол- и 2-хлор-3- нитропиридин. В качестве основания используют триэтиламин, в качестве растворителя используют р-диоксан, реакционную смесь кипятят с обратным холодильником в течение 3 часов. В результате хроматографической обработки получают указанное в заглавии соединение /67%/ в виде пены темно-красного цвета; Т. плавления 59,0-61,0oC;
1H-ЯМР /CDCl3/ δ: 8,66 /шир. с., 1Н/, 8,61 /дд, J = 8,3 и 1,8 Гц, 1Н/, 8,41 /дд, J = 4,4 и 1,8 Гц, 1Н/, 7,76 /шир, с, 1Н/, 7,30-7,24 /м, 2Н/, 6,97 /д, J = 2,1 Гц, 1Н/, 6,73 /дд, J = 8,3 и 4,4 Гц, 1Н/, 2,97-2,91 /м, 2Н/, 2,70-2,63 /м, 2Н/, 2,36 /с, 6Н/;
13C ЯМР /CDCl3/ δ: 155,7, 151,5, 135,5, 134,5, 129,4, 128,2, 127,9, 122,8, 119,3, 114,4, 114,3, 113,0, 111,5, 60,3, 45,4, 23,7. Элементный анализ для C17H19N5O2 • 1/3 H2O:
Рассчитано: C 61,62 H 5,98 N 21,13
Найдено: C 61,58 H 5,65 N 20,80
М. 3-(N-метилпирролидин-2-илметил)-5-(4-фенил-2- нитрофениламино)-1Н-индол
Используют (R)-5-амино-3-(N-метилпирролидин-2-илметил)-1H- индол и 4-бром-3-нитробифенил. В качестве основания используют триэтиламин, в качестве растворителя используют N,N-диметилформамид, реакционную смесь нагревают при 110oC в течение 12 часов. В результате хроматографической обработки получают указанное в заглавии соединение /24%/ в виде твердого аморфного вещества красного цвета.
1H ЯМР /CDCl3/ δ: 9,63 /шир. с, NH/, 8,97 /шир. с, NH/, 8,42 /д J = 2,2 Гц, 1Н/, 7,56-7,25 /м, 9Н/, 7,08 /д, J = 9,0 Гц, 2Н/, 3,50-3,32 /м, 2Н/, 2,59-2,52 /м, 1Н/, 2,53 /с, 3Н/, 2,05-1,71 /м, 4Н/; 13C ЯМР /CDCl3/ δ: 144,4, 138,8, 134,9, 132,4, 131,1, 130,2, 129,7, 129,0, 127,3, 126,2, 124,7, 124,1, 120,8, 116,7, 115,9, 112,7, 112,0, 67,9, 57,4, 40,6, 31,2, 28,6, 21,9. FAB масс-спектр высокого разрешения, рассчитано для /C26H26N4O2 • H/ 427,2136, найдено 427,2099.
N. 5-(5,6-дихлор-2-нитрофениламино)-3-(N-метилпирролидин-2- илметил)-1H-индол
Используют (R)-5-амино-3-(N-метилпирролидин-2-илметил)-1H-индол и 1,2,3-дихлорнитробензол. В качестве основания используют карбонат натрия, в качестве растворителя используют N, N-диметилформамид, реакционную смесь нагревают при 125oC в течение 3 часов. В результате хроматографической обработки получают указанное в заглавии соединение /60%/ в виде твердого вещества красного цвета, Rf = 0,4 /метиленхлорид/метанол/гидроксид аммония, (9:1:0,1).
1H ЯМР /CDCl3/ δ: 8,59 /шир. с, NH/, 8,36 /шир. с, NH/, 7,96 /д, J = 9,1 Гц, 1Н/, 7,23 Д, J = 8,6 Гц, 1Н/, 7,09 /с, 1Н/, 7,07 /д, J = 9,1 Гц, 1Н/, 6,99 /д, J = 1,9 Гц, 1Н/, 6,81 /дд, J = 8,6 и 2,1 Гц, 1Н/, 3,15-3,05 /м, 2Н/, 2,54 /дд, 13,8 и 9,6 Гц, 1Н/, 2,46-2,33 /м, 1Н/, 2,40 /с, 3Н/, 2,22 /дд, J = 17,4 и 9,3 Гц, 1H/, 1,84-1,48 /м, 4Н/; Полевой масс-спектр высокого разрешения, рассчитано для /C20H20Cl2N4O2 • H/ 419,1044, найдено 419,1046.
O. 3-(N-трет-бутоксикарбонилпиперид-4-ил)-5-(3-нитропирид-2 иламино)-1Н-индол
Используют 5-амино-3-(N-трет. -бутоксикарбонилпиперид-4-ил)- 1Н-индол и 2-хлор-3-нитропиридин. В качестве основания используют триэтиламин, в качестве растворителя используют диоксан, реакционную смесь нагревают при кипении с обратным холодильником /101oC/ в течение 6 часов. В результате хроматографической обработки, используя этилацетат /30 - 40%/ в гексанах в качестве элюента, получают указанное в заглавии соединение /70%/ в виде пены темно-красного цвета: 1H ЯМР /CDCl3/ δ: 155,8, 155,0, 151,6, 135,5, 134,6, 129,4, 126,9, 121,3, 120,8, 119,8, 114,8, 113,1, 111,5, 79,4, 44,5, 33,6, 32,8, 28,5. Элементный анализ для C23H27N5O4 • 1/4 C4H8O2 /этилацетат/:
Рассчитано: C 62,73 H 6,36 N 15,24
Найдено: C 62,51 H 6,08 N 15,21
P. (R,S)-3-(N-метилпирролидин-3-ил)-5-(3-нитропирид-2 иламино)-1Н-индол
Используют (R, S)-3-(N-метилпирролидин-3-ил)индол и 2-хлор-3- нитропиридин. В качестве основания используют ацетат натрия, в качестве растворителя используют уксусную кислоту, реакционную смесь кипятят с обратным холодильником в течение 4 часов. В результате хроматографической обработки получают указанное в заглавии соединение /44%/ в виде пены темно-красного цвета; Т. плавления 55,0-57,0oC
13С ЯМР /CDCl3/ δ: 155,7, 151,5, 135,5, 135,0, 129,0, 128,1, 127,1, 121,7, 119,3, 119,2, 114,7, 113,0, 111,6, 62,8, 56,2, 42,4, 35,1, 32,1. FAB масс-спектр высокого разрешения /м/z, относительная интенсивность /306 /MH+, 100/, 155/38/. Элементный анализ для C18H19N5O2 • 0,5C4H4O2 /этилацетат/
Рассчитано: C 62,98 H 6,08 N 18,36
Найдено: C 62,71 H 5,80 N 18,51
Q. 5-(3-нитропирид-2-ил)-1Н-индол
Используют 5-аминоиндол и 2-хлор-3-нитропиридин. В качестве основания используют триэтиламин, в качестве растворителя используют абсолютированный этанол, реакционную смесь перемешивают при комнатной температуре в течение 4 дней. Полученную реакционную смесь фильтруют до получения угаданного в заглавии соединения /69%/ в виде твердого вещества оранжевого цвета; Т. плавления 162-163,5oC;
13C ЯМР /CDCl3/ δ: 155,6, 150,5, 135,5, 129,7, 127,9, 125,9, 127,6, 118,5, 115,0, 113,4, 111,2, 101,2, Элементный анализ для C13H10N4O2:
Рассчитано: C 61,41 H 3,96 N 22,04
Найдено: C 61,22 H 3,80 N 22,08
R. 5-(4-хлор-2-нитрофенил)-амино-3-(N-метилпирролидин- 2R-илметил)-1Н-индол
Используют (R)-5-амино-3-(N-метилпирролидин-2-илметил)-1Н- индол и 2,5-дихлорнитробензол. В качестве основания используют карбонат натрия, в качестве растворителя используют N, N-диметилформамид, реакционную смесь нагревают при 110oC в течение 5 часов. В результате хроматографической обработки, используя метиленхлорид/метанол/гидроксид аммония в качестве элюента /12: 1: 0,4, соответственно/, получают указанное в заглавии соединение /35%/ в виде твердого вещества красного цвета: Rf = 0,5 /метиленхлорид/метанол/гидроксид аммония 9: 1:0,1/; 1H ЯМР /CDCl3/ δ: 9,58 /с, 1Н/, 8,21 /д, J = 2,5 Гц, 1Н/, 8,14 /шир. с., 1Н/, 7,46 /д, J = прибл. 2 Гц/, 7,40 /д, у = 8,5 Гц, 1Н/, 7,21 /дд, J = 2,5 и 9,3 Гц, 1Н/, 7,11 /д, J = прибл. 2 Гц/, 7,05 /дд, J = 2,0 и 8,5 Гц, 1Н/, 6,98 /д, J = 9,3 Гц, 1Н/. 3,18-3,08 /м, 2Н/, 2,57 /дд, J = 9,5 и 14,2 Гц, 1Н/, 2,50-2,40; /м, 1Н/, 2,28-2,17 /м, 1Н/, 2,44 /с, 3Н/, 1,85-1,50 /м, 4Н/,
S. 5-(5-хлор-2-нитрофенил)амино-3-(N-метилпирролидин-2R- илметил)-1Н-индол
Используют (R)-5-амино-3-(N-метилпирролидин-2-илметил)-1H- индол и 2,4-дихлорнитробензол. В качестве основания используют карбонат натрия, в качестве растворителя используют N, N-диметилформамид, реакционную смесь нагревают при 110oC в течение 5 часов. В результате хроматографической обработки, используя в качестве элюента метиленхлорид/метанол/гидроксид аммония /12,1,0,4/, получают указанное в заглавии соединение /51%/ в виде твердого вещества красного цвета; Rf = 0,5 метиленхлоридметанол/гидроксид аммония 9: 1: 0,1/; FAB масс-спектр высокого разрешения, рассчитано для /C20H21N4ClO2 • H/ 385,1434, найдено 385,1451.
Т. 5-(6-хлор-2-нитрофенил)амино-3-(N-метилпирролидин-2R- илметил)-1Н-индол
Используют (R)-5-амино-3-(N-метилпиррилидин-2-илмитил)-1H- индол и 2,3-дихлорнитробензол. В качестве основания используют карбонат натрия, в качестве растворителя используют N, N-диметилформамид, реакционную смесь нагревают при 110oC в течение 6 часов. В результате хроматографической обработки, используя в качестве элюента метиленхлорид/метанол/ гидроксид аммония /12: 1: 0,4/, получают указанное в заглавии соединение /62%/ в виде твердого вещества красного цвета; Rf = 0,5 /метиленхлорид/метанол гидроксид аммония 9: 1: 0,1/. 1H ЯМР /CDCl3/ δ: 8,33 /с, 1Н/, 8,21 /шир. с, 1Н/, 7,99 /дд, J = 1,5 и 8,5 Гц, 1Н/, 7,56 /дд, J = 1,6 и 7,8 Гц, 1Н/, 7,25 /д, J = 8,5 Гц, 1Н/, 7,08 /д, J= 1,8 Гц, 1Н/, 7,05 /д, J. 2,1 Гц, 1Н/, 6,92 /дд, J = 7,8 и 8,4 Гц, 1Н/, 6,82 /дд, J = 2,1 и 8,6 Гц, 1Н/, 3,22-3,10 /м, 2Н/, 2,65-2,50 /м, 2Н/, 2,41 /с, 3Н/, 2,29 /дд, J = 17,2 и 9,4 Гц, 1Н/, 1,90-1,55 /м, 4Н/.
U. 5-(4-циано-2-нитрофенил)амино-3-(N-трет. - бутоксикарбонил-1,2,5,6-тетрагидропирид-4-ил)-1H-индол
Используют 5-амино-3-(N-трет. -бутоксикарбонил-1,2,5,6- тетрагидропирид-4-ил)-1Н-индол и 4-хлор-3-нитробензонитрил. В качестве основания используют триэтиламин, в качестве растворителя используют абсолютированный этанол, реакционную смесь кипятят с обратным холодильником в течение 2 часов В результате обработки на хроматографической колонке, используя в качестве элюента 1% метанол в метиленхлориде, получают указанное в заглавии соединение /40%/ в виде пены красного цвета; Т. плавления с разложением 85oC. Rf = 0,35 (1% метанол в метиленхлориде/; Масс-спектр высокого разрешения рассчитано для C25H25N5O4 459,1909, найдено 459,1853.
V. 5-(4-циано-2-нитрофенил)амино-3-(N-метилпирролидин-3-ил)- 1Н-индол
Используют 5-амино-3-(N-метилпирролидин-3-ил)-1Н-индол и 4-хлор-3-нитробензонитрил. В качестве основания используют ацетат натрия, в качестве растворителя используют уксусную кислоту, реакционную смесь кипятят с обратным холодильником в течение 5 часов. После обработки на хроматографической колонке получают указанное в заглавии соединение /16%/ в виде твердого аморфного вещества красного цвета, Rf = 0,35 /метиленхлорид/метанол/гидроксид аммония 9: 1: 0,1 /; 13C ЯМР /CDCl3/ δ: 147,4, 137,0, 135,8, 132,1, 131,4, 128,2, 127,8, 122,2, 120,4, 120,3, 118,2, 117,2, 112,7, 98,9, 62,7, 56,3, 42,4, 35,0, 32,3. Масс-спектр высокого разрешения, рассчитано для [C20H19N5O2]: 361,1541, найдено 361,1500.
W. 5-(5-циано-3-нитропирид-2-ил)амино-3-(N-метилпирролидин- 3-илметил)-1Н-индол
Используют (R)-5-амино-3-(N-метилпирродидин-2-илметил)-1H- индол и 2-хлор-5-циано-3-нитропиридин. В качестве основания используют триэтиламин, в качестве растворителя используют абсолютированный этанол, реакционную смесь нагревают при кипении с обратным холодильником в течение 2 часов. В результате хроматографической обработки, используя метиленхлорид/метанол/гидроксид аммония /9:1:0,1/, получают указанное в заглавии соединение /53%/ в виде пены красного цвета; Rf = 0,2 /20% метанол в метиленхлориде; 13C ЯМР /CD3OD/ δ: 158,3, 140,3, 136,5, 130,0, 128,4, 125,9, 122,2, 120,4, 115,2, 112,8, 111,1, 96,4, 70,1, 57,9, 40,4, 31,3, 28,2, 22,4. Масс-спектр высокого разрешения рассчитано для [C20H20N6O2] 376,1650, найдено 376,1653.
X. 5-(4-метил-2-нитрофенил)амино-3-(N-метилпирролидин-2R- илметил)-1H-индол
Используют (R)-5-амино-3-(N-метилпирролидин-2-илметил)-1H- индол и 4-хлор-3-нитротолуол. Не используют никаких оснований. В качестве растворителя используют 4-хлор-3-нитро-толуол, реакционную смесь нагревают при 150oC в течение 18 часов. После обработки на хроматографической колонке с использованием в качестве элюента смеси метиленхлорид/метанол/гидроксид аммония /18: 1: 0,1/, получают указанное в заглавии соединение /63%/ в виде пены красного цвета; Rf = 0,6 /метиленхлорид/метанол/гидроксид аммония 18:1:0,1/;
13C ЯМР /CD3OD/ δ: 144,8, 138,2, 136,6, 132,9, 131,3, 129,6, 127,2, 126,3, 125,1, 121,2, 117,3, 116,8, 113,8, 113,3, 68,4, 58,3, 41,0, 32,3, 30,2, 22,4, 20,0.
Элементный анализ для C21H24N4O2 • 0,5 H2O:
Рассчитано: C 67,54 H 6,75 N 15,00
Найдено: C 67,58 H 6,90 N 14,66
Пример 9
Общий способ превращения 5-(2,5-диметил-1Н-пиррол-1-ил)-1Н- индолов в 5-амино-1Н-индолы
Смесь 5-(2,5-диметил-1Н-пиррол-1-ил)-1Н-индола /10,00 ммоля/ гидроксиламингидрохлорида /6,95 г, 100 ммоля, 10 экв./ и триэтиламина /6,97 мл, 50 ммолей, 5 экв./ в 35 мл 2-пропанола и 5 мл воды нагревают при кипении с обратным холодильником в атмосфере азота в течение промежутка времени, который зависит от субстрата. Полученную реакционную смесь охлаждают, добавляют гидроксид натрия /4,00 г, 100 ммолей, 10 экв./, и полученную реакционную смесь перемешивают при комнатной температуре в атмосфере азота в течение 24 часов. Затем реакционную смесь фильтруют через Целит, а полученный фильтрат выпаривают при пониженном давлении. Остаток обрабатывают на хроматографической колонке с силикагелем /примерно 100 г/, элюируя соответствующей системой растворителей до получения соответствующего 5-амино-1Н-индола. Таким способом получают следующие соединения:
А. 5-амино-3-(N-(2-метоксиэтил)пирролидин-2R-илметил)-1H-индол.
Используют 5-(2,5-диметил-1Н-пиррол-1-ил)-3-(N-(2- метоксиэтил)-пирролидин-2R-илметил)-1Н-индол) и кипятят с обратным холодильником в течение 4,5 часа. В результате хроматографической обработки, используя в качестве элюента этилацетат/метанол/триэтиламин /18: 1: 1/ получают указанное в заглавии соединение /71%/ в виде пены коричневого цвета; Rf = 0,70 /этилацетат/метанол/триэтиламин /8: 1; 1/; 13C ЯМР /CD3OD/ δ: 146,0, 138,0, 132,0, 128,2, 122,7, 112,8, 111,2, 104,4, 70,9, 65,9, 57,6, 54,6, 53,7, 30,2, 29,4, 21,4; FAB масс-спектр высокого разрешения, рассчитано для [C16H22N3O • H] 273,1661, найдено 273,1838.
Элементный анализ для C16H22N3O • 0,9 H2O:
Рассчитано: C 66,59 H 6,31 N 14,56
Найдено: C 06,59 H 8,15 N 14,34
В. 5-амино-3-(N-бензилоксикарбонил-4R-метоксипирролидин-2R- илметил)-1Н-индол
Используют 5-(2,5-диметил-1Н-ииррол-1-ил)-3-(N- бензилоксикарбонил-4R-метоксипирролидин-2R-илметил)-1Н-индол, реакционную смесь кипятят с обратным холодильником в течение 4 часов. В результате хроматографической обработки при элюировании смесью этилацетат/метанол/триэтиламин/18:1:1/ получают указанное в заглавии соединение /92%/ в виде прозрачного бледно-коричневого масла; Rf = 0,80 /метиленхлорид/метанол/гидроксид аммония 6:1:1/.
C. 5-амино-3-(1-трет.-бутоксикарбонилпирролидин-2R-илметил)- 1Н-индол
Используют 3-(N-трет.-бутоксикарбонилпирролидин-2R-илметил)- 5-(2,5-диметил-1Н-пиррол-1-ил)-1Н-индол, реакционную смесь кипятят с обратным холодильником в течение 12 часов. В результате хроматографической обработки смесью этилацетат/гексаны /1: 1/ получают указанное в заглавии соединение /78%/ в виде пены бледно-коричневого цвета; Т. плавления с разложением 50oC; Rf = 0,30 /этилацетат/гексаны 1:1/, ИК /KBr/ 1673, 1405 см-1; Масс-спектр высокого разрешения, рассчитано для C18H25N3O2 315,1949, найдено 315, 1914.
D. 5-амино-3-(N-метилпирролидин-2R-илметил)-1Н-индол
Используют 5-(2,5-диметил-1Н-пиррол-1-ил)-3-(N-метил-пирролидин- 2R-илметил)-1Н-индол, реакционную смесь кипятят с обратным холодильником в течение 4,5 часа. В результате хроматографической обработки, используя в качестве элюента смесь этилацетат/метанол/триэтиламин /8:1:1/ получают указанное в заглавии соединение /83%/ в виде коричневой пены; Rf = 0,4 /этилацетат/метанол/триэтиламин /8: 1: 1/; Т. плавления 43 - 47oC; 13C ЯМР /CDCl3/ δ: 138,9, 131,2, 128,5, 122,7, 112,8, 112,7, 111,7, 104,0, 66,7, 57,5, 40,7, 31,5, 29,8, 21,8. Масс-спектр высокого разрешения рассчитано для C14H19N3 найдено 229,1560
Пример 10
Общий способ превращения 3-(N-бензилоксикарбонилпирролидин- 2-илкарбонил)-1Н-индолов в 3-(N-метилпирролидин-2-илметил)-1Н- индолы
К перемешиваемой смеси литийалюминийгидрида /1,71 г, 45,1 ммоля, 4,5 экв. / в безводном тетрагидрофуране /40 мл/ при 0oC прикапывают раствор 3-(N-бензилоксикарбонилпирролидин-2- илкарбонил)-1Н-индола /10,0 ммоля/ в 20 мл безводного тетрагидрофурана. Полученную реакционную смесь кипятят с обратным холодильником в атмосфере азота в течение 6 часов. Реакционную смесь охлаждают, очень осторожно, порциями добавляют декагидрат сульфата натрия /50 г/, затем 1 мл воды и 100 мл этилацетата. Полученную смесь перемешивают при комнатной температуре в атмосфере азота в течение 24 часов. Реакционную смесь фильтруют через Целит, полученный фильтрат выпаривают при пониженном давлении. Остаток обрабатывают на хроматографической колонке с силикагелем /примерно 100 г/ элюируя соответствующей системой растворителей до получения целевого 3-(N-метилпирролидин-2-илметил)-1Н-индола. Таким способом получают следующие соединения:
А. 5-(2,5-диметил-1Н-пиррол-1-ил)-3-(N-метилпирролидин-2R- илметил)-1Н-индол
Используют 5-(2,5-диметил-1Н-пиррол-1-ил) (3-N- бензилоксикарбонилпирролидин-2R-илкарбонил)-1Н-индол. После хроматографической обработки, используя в качестве элюента этилацетат/метанол/триэтиламин /8:1:1/ получают указанное в заглавии соединение /92%/ в виде белой пены; Т. плавления 52-58oC; 13C ЯМР /CD3OD/ δ: 137,2, 131,7, 129,9, 129,1, 125,2, 122,6, 119,0, 114,0, 112,6, 105,9, 68,5, 58,3, 41,0, 32,4, 30,2, 22,4, 13,2; (α)25 = +81o /метиленхлорид, с = 1/. Элементный анализ для C20H25N3 • 0,5 H2O:
Рассчитано: C 75,92 H 8,28 N 13,27
Найдено: C 75,88 H 8,43 N 13,24
В. (R)-5-дибензиламино-3-(N-метилпирролидин-2-илметил)-1H-индол
Используют 3-(N-бензилоксикарбонилпирролидин-2R-илкарбонил)- 5-дибензиламино-1H-индол. В результате хроматографической обработки, элюируя смесью метиленхлорид/метанол/гидроксид аммония /9:1:0,1/ получают указанное в заглавии соединение /89%/ в виде пены бледно-зеленого цвета:
1H ЯМР /CDCl3/ δ: 7,82 /шир. с., NH/, 7,35-7,19 /м, 10Н/, 7,20 /д, J = 8,6 Гц, 1Н/, 6,95 / д, J = 2,1 Гц, 1Н/, 6,85 /дд, J = 2,3 и 8,7 Гц, 1Н/, 6,80 /д, J = 2,2 Гц, 1Н/, 4,65 /с, 4Н/, 3,25-3,02 /м, 2Н/, 2,52 /дд, J = 9,5 и 13,9 Гц, 1Н/, 2,39-2,15 /м, 2Н/, 2,30 /с, 3Н/, 1,85-1,40 /м, 4Н/; 13C ЯМР /CDCl3/ δ 143,2, 139,7, 130,5, 128,5, 127,3, 126,8, 122,9, 112,5, 112,2, 111,8, 103,4, 67,0, 57,4, 56,4, 40,6, 31,4, 29,7, 21,9. FAB Масс-спектр высокого разрешения, рассчитано для C28H31N3 409,2520, найдено 409,2475.
Пример 11
Общий способ превращения 3-(пирролидин-2-илкарбонил)-1H- индолов в 3-(пирролидин-2-илметил)-1Н-индолы
К перемешиваемому раствору литийборогидрида /0,33 г, 15,2 ммоля, 3,0 экв. / в 10 мл безводного тетрагидрофурана в атмосфере азота прикапывают раствор 3-пирролидин-2-илкарбонил)-1Н-индола /10 мл/ в 40 мл безводного тетрагидрофурана. Полученный реакционный раствор кипятят с обратным холодильником в атмосфере азота в течение промежутка времени, который зависит от субстрата. Реакционную смесь охлаждают, медленно и осторожно добавляют декагидрат сульфата натрия /примерно 25 г/, затем 1 мл воды и 50 мл этилацетата. Полученную реакционную смесь перемешивают при комнатной температуре в атмосфере азота в течение 4 часов. Затем реакционную смесь фильтруют через Целит, а полученный фильтрат выпаривают при пониженном давлении. Остаток обрабатывают на хроматографической колонке с силикагелем /примерно 200 г/, элюируя соответствующей системой растворителей до получения 3-/пирролидин-2-илметил/-1Н-индола. Указанным способом получают следующие соединения:
А. 5-(2,5-диметил-1Н-пиррол-1-ил)-3-(N- бензилоксикарбонилпирролидин-2R-илметил)-1Н-индол
Используют 5-(2,5-диметил-1Н-пиррол-1-ил)-3-(N- бензилоксикарбонилпирролидин-2R-илкарбонил)-1Н-индол, реакционную смесь кипятят с обратным холодильником в течение 1,5 часа. В результате хроматографической обработки при элюировании смесью этилацетат/гексаны /1:3/ получают указанное в заглавии соединение /59%/ в виде бесцветной смеси масла и пены. Rf = 0,45 в эфире. ИК /KBr/ 3340-3300, 1686, 1680, 1451, 1415 см-1; Полевой масс-спектр низкого разрешения /м/z относительная интенсивность/: 488/M+, 100/, 294/14/, 224/32/; FAB масс-спектр высокого разрешения, рассчитано для [C27H29N3O2 • H] 428,2340, найдено 428,2303.
Элементный анализ для C27H29N3O2 • 0,75 H2O:
Рассчитано: C 73,53 H 6,97 N 9,53
Найдено: C 73,49 H 6,71 N 9,17
В. 5-(2,5-диметил-1Н-пиррол-1-ил)-3-(N-бензилоксикарбонил-4R- метоксипирролидин-2R-илметил)-1Н-индол
3-(N-бензилоксикарбонил-4-метоксипирролидин-2R-илкарбонил)- 5-(2,5-диметил-1Н-пирролил)-1Н-индол используют, реакционную смесь кипятят с обратным холодильником в течение 12 часов. В результате хроматографической обработки, используя в качестве элюента 30% метиленхлорид в гексанах, получают указанное в заглавии соединение /57%/ в виде прозрачного бесцветного масла, которое кристаллизуется при стоянии; Rf = 0,80 /метанол/этилацетат 1:9/; Полевой масс- спектр низкого разрешения /м/z, относительная интенсивность /458 /MH+, 100/, 367/7/ 350/5/, 324/17/, 239/10/; FAB масс-спектр высокого разрешения, рассчитано для [C28H31N3O3 • H] 458,2446, найдено 458,2468.
C. 3-(N-бензилоксикарбонилпирролидин-2R-илметил)-5- дибензиламино-1Н-индол
Используют 3-(N-бензилоксикарбонилпирролидин-2R-илкарбонил)- 5-дибензиламино-1Н-индол) и реакционную смесь кипятят с обратным холодильником в течение 4 часов. В результате хроматографической обработки, используя в качестве элюента этилацетат в гексанах /1:3/ получают указанное в заглавии соединение /70%/ в виде пены белого цвета; FAB масс-спектр низкого разрешения /м/z, относительная интенсивность /530/ MH+, 87/, 529 /М+, 100/, 439/10/, 409/10/, 325/32/, 235/20/.
Пример 12
Общий способ получения 3-(N-бензилоксикарбонилпирролидин-2- илкарбонил)-1Н-индолов.
К перемешиваемому раствору N-бензилоксикарбонилпролина /10 ммолей/ в 25 мл безводного метиленхлорида со следами N,N-диметилформамида /0,1 мл/ добавляют оксалилхлорид /1,31 мл, 15,02 ммоля, 1,5 экв/. В результате получают реакционный раствор с интенсивным газообразованием, который перемешивают при комнатной температуре в атмосфере азота в течение 3 часов. Затем реакционный раствор выпаривают при пониженном давлении, добавляют 50 мл безводных гексанов, и полученный раствор снова выпаривают при пониженном давлении до получения N-бензилоксикарбонилпролинового хлорангидрида, который растворяют в безводном бензоле /25 мл/.
Параллельно, раствор этилмагнийбромида /3,0 М в эфире 6,8 мл, 20,4 ммоля, 2,0 экв. / прикапывают к перемешиваемому раствору 3-незамещенного-1Н-индола /20,0 ммоля, 2,0 экв/ в 50 мл бензола при 0oC в атмосфере азота. Полученный реакционный раствор перемешивают при 0oC в атмосфере азота в течение 15 минут. Затем при интенсивном перемешивании прикапывают полученный ранее раствор N-бензилоксикарбонилпролинового хлорангидрида. Полученный реакционный раствор интенсивно перемешивают при 0oC в атмосфере азота в течение 1 часа. Затем добавляют 75 мл насыщенного раствор бикарбоната натрия и эту водную смесь экстрагируют трижды этилацетатом порциями по 75 мл. Органические экстракты объединяют, сушат над сульфатом магния и выпаривают при пониженным давлении. Оставшуюся пену перекристаллизовывают из смеси этилацетата в диэтиловом эфире /общий объем 25 мл/ до получения соответствующего 3-/N-бензилоксикарбонилпирролидин-2-илкарбонил/-1Н-индола. Этим способом получают следующие соединения:
A. 5-(2,5-диметил-1Н-пиррол-1-ил)-3-(N- бензилоксикарбонилпирролидин-2R-илкарбонил)-1Н-индол
Используют (R)-N-бензилоксикарбонилпролин и 5-(2,5-диметил- 1Н-пиррол-1-ил)-1Н-индол. В результате кристаллизации экстракционного остатка из диэтилового эфира получают указанное в заглавии соединение /75%/ в виде грязно-белого твердого вещества. Т. плавления 155,0 - 157,0oC / с интенсивным газовыделением/; (α)25 = +101o /метиленхлорид, с = 1/. Элементный анализ для C27H27N3O3:
Рассчитано: C 73,45 H 6,16 N 9,52
Найдено: C 73,41 H 6,02 N 9,52
В. 3-(N-бензилоксикарбонил-4-метоксипирролидин-2R-илкарбонил) -5-(2,5-диметил-1Н-пирролил)-1Н-индол
Используют (R)-цис-N-бензилоксикарбонил-4-метоксипролин /Krapcho, et. al, Med, Chem. 1148/1988// и 5-(2,5-диметил-1Н- пиррол-1-ил/-1Н-индол. В результате кристаллизации экстракционного остатка, используя диэтиловый эфир, получают указанное в заглавии соединение 54% в виде грязно-белого твердого вещества: Т плавления 189,0-191,0oC. Rf = 0,4 в смеси этилацетат/гексаны /2:1/; (α)25 = +89o /метиленхлорид, с = 1/; FAB масс-спектр высокого разрешения, рассчитано для [C28H29N3O4 • H] 472,2238, найдено 472,2281.
Элементный анализ для C28H29N3O4:
Рассчитано: C 71,32 H 6,20 N 8,91
Найдено: C 71,56 H 6,28 N 8,92
C. 3-(N-бензилоксикарбонилпирролидин-2R-илкарбонил)-5- дибензиламино-1Н-индол
Используют (R)-N-бензилоксикарбонилпролин и 5-дибензиламино- 1H-индол. В результате кристаллизации экстракционного остатка, используя диэтиловый эфир, получают указанное в заглавии соединение /24%/ в виде белого твердого вещества; Т. плавления 176-177,0oC. Масс-спектр низкого разрешения /м/z, относительная интенсивность /543/100; М+/, 453 /10/, 407/7/, 339/40/, 307/10/, 247/10/, 154/36/; (α)25 = +112o ТГФ, с = 1/.
Элементный анализ для C35H33N3O3:
Рассчитано: C 77,32 H 6,12 N 7,73
Найдено: C 77,35 H 6,30 N 7,66
Пример 13
(R)-5-амино-3-(N-метилпирролидин-2-илметил)-1Н-индол
Смесь (R)-5-дибензиламино-3-(N-метилпирролидин-2-илметил)- 1Н-индола /1,08 г, 2,64 ммоля/ и 20% гидроксида палладия на угле /0,6 г/ в 25 мл абсолютированного этанола встряхивают в атмосфере водорода /3 атм/ при 40oC в течение 4 часов. Полученную смесь фильтруют через диатомовую землю, а полученный фильтрат выпаривают при пониженном давлении до получения указанного в заглавии соединения /0,60 г, 2,62 моля, 99%/ в виде белой пены: 1H ЯМР /ДМСО-d6/ δ: 10,65 /шир. с, NH/, 7,14 /д, J = 2,2 Гц, 1Н/, 7,12 /д, J = 8,6 Гц, 1Н/, 6,85 /д, J = 1,6 Гц, 1Н/ 6,60 /дд, J = 2,0 и 8,6 Гц, 1Н/, 3,63-2,63 /м, 7Н/, 2,78 /с, 3Н/, 2,06-1,67 /м, 4Н/; (α)25 = +9o /MeOH, с = 1,0/. Масс-спектр высокого разрешения, рассчитано для C14H19N3 22,1575, найдено 229,1593.
Пример 14
5-(2,5-диметил-1Н-пиррол-1-ил)-1Н-индол
Смесь 5-аминоиндола /1,32 г, 10,0 ммоля/, ацетилацетона 4,0 мл, 34 ммоля, 3,4 экв./ и 25 мл толуола кипятят с обратным холодильником в атмосфере азота, используя ловушку Дина-Старка в течение 24 часов. Реакционную смесь охлаждают, а затем выливают через силикагельный фильтр /примерно 200 г/, промывая его затем 10% эфиром в гексанах до получения указанного в заглавии соединения /1,52 г, 72%/ в виде грязно-белого твердого вещества, Rf = 0,75 в диэтиловом эфире; 13C ЯМР /CDCl3/ δ: 135,0, 131,4, 129,5, 128,1, 125,6, 122,4, 120,3, 111,3, 105,0, 103,0, 13,2. Элементный анализ для C14H14N2:
Рассчитано: C 79,97 H 6,71 N 13,52
Найдено: C 79,72 H 6,75 N 13,13
Пример 15
5-дибензиламино-1H-индол
К перемешиваемой смеси 5-аминоиндола /3,00 г, 22,7 ммоля/ и триэтиламина /10,5 мл, 74,9 ммоля, 3,3 экв./ в 30 мл ацетонитрила при комнатной температуре в атмосфере азота добавляют бензилбромид /8,2 мл, 68,9 ммоля, 3,0 экв. / по каплям. Полученную реакционную смесь кипятят с обратным холодильником в атмосфере азота в течение 3 часов. Полученную реакционную смесь фильтруют, полученный фильтрат выпаривают при пониженном давлении. После обработки полученного остатка на хроматографической колонке с силикагелем /примерно 200 г/, элюируя смесью этилацетат/гексаны /от 1:9 до 1:1, получают указанное в заглавии соединение в виде грязно-белого твердого вещества; Т. плавления 124,0-126,0oC 13C ЯМР /ацетон-d6/ δ: 144,3, 140,8, 131,8, 129,9, 129,2, 128,3, 127,5, 125,5, 113,5, 112,4, 106,4, 101,9, 57,0; TCX /15% этилацетат в гексанах/: Rf = 0,3
Пример 16
5-амино-3-(N-метилпирролидин-3-ил)-1Н-индол
Смесь 5-бензиламино-3-(N-метилпирролидин-3-ил)-1H-индола /7,80 г, 25,5 ммоля/, формата аммония /16,10 г, 255 ммолей, 10 экв./ и 10% Pd на угле /0,78 г/ в 250 мл абсолютированного этанола кипятят с обратным холодильником в атмосфере азота в течение 1 часа. Реакционную смесь фильтруют, а полученный фильтрат выпаривают при пониженном давлении. Оставшееся масло обрабатывают на хроматографической колонке с силикагелем /примерно 200 г/, элюируя 0,3% триэтиламина в метаноле до получения указанного в заглавии соединения /0,90 г, 16%/ в виде бледно-желтого масла; 1H ЯМР /CD3OD/ δ: 7,13 /д, J = 8,5 Гц, 1Н/, 6,94 /шир.с, 2Н/, 6,65 /дд, J = 2,0 и 8,5 Гц, 1Н/, 4,91 /с, 2-NH/, 3,66-3,50 /м, 1Н/, 3,17-3,08 /шир. т, 1Н/, 2,96-2,85 /м, 1Н/, 2,67-2,50 /м, 2Н/, 2,40 /с, 3Н/, 2,37-2,24 /м, 1Н/, 2,08-1,93 /м, 1Н/; FAB масс-спектр низкого разрешения /м/z, относительная интенсивность /216/MH+, 100/.
Пример 17
5-бензиламино-3-(N-метилпирролидин-3-ил)-1Н-индол
К перемешиваемому раствору N-метил-3-/5- фенилкарбониламиноиндол-3-ил/сукцинамида /18,31 г, 52,71 ммоля/ в безводном тетрагидрофуране /270 мл/ при 0oC добавляют литийалюминийгидрид /20,01 г, 527 ммолей, 10 экв.) в твердом виде, порциями в течение 45 минут. Полученную реакционную смесь перемешивают при комнатной температуре в атмосфере азота в течение 24 часов. Затем осторожно добавляют декагидрат сульфата натрия /50 г/ к этой реакционной смеси, затем добавляют 5 мл воды и 100 мл этилацетата. Полученную смесь перемешивают при комнатной температуре в течение часа. Реакционную смесь фильтруют, а полученный фильтрат выпаривают при пониженном давлении. Оставшееся масло обрабатывают на хроматографической колонке с силикагелем /примерно 500 г, элюируя смесью этилацетат:метанол:триэтиламин /от 9:0:1, до 8:1:1/ до получения указанного в заглавии соединения /7,90 г, 49%/ в виде бледножелтого масла, 13C ЯМР /ацетон-d6/ δ: 142,9, 142,1, 132,3, 129,3, 128,6, 127,5, 121,9, 119,6, 112,8, 112,5, 102,0, 63,6, 57,1, 49,9, 42,6, 36,5, 33,0. FAB масс-спектр низкого разрешения /м/z, относительная интенсивность /306 /MH+, 100/, 263/4/, 248/4/, 223/8/.
Пример 18
N-метил-3-(5-фенилкарбониламиноиндол-3-ил)сукцинамид
Раствор 5-фенилкарбониламино-1Н-индола /2,50 г, 10,58 ммоля,/ Chem. Abctracts, 10991g /1954// и N-метилмалеимида /2,94 г, 26,46 ммоля, 2,5 экв./ в 75 мл ледяной уксусной кислоты кипятят с обратным холодильником в атмосфере азота в течение 24 часов. Полученный реакционный раствор выпаривают при пониженном давлении, а оставшееся масло растворяют в 50 мл этилацетата. Этот раствор промывают насыщенным водным раствором бикарбоната натрия /2 х 25 мл/ сушат над сульфатом магния и выпаривают при пониженном давлении. Оставшееся масло обрабатывают на хроматографической колонке примерно 100 г /силикагеля/, используя в качестве элюента смесь этилацетат/гексаны/ от 1:3 до 1: 1/ до получения указанного в заглавии соединения /1,06 г, 29%/ в виде твердого вещества белого цвета. Т. плавления 226,5- 227,5oC. FAB масс-спектр низкого разрешения /м/z, относительная интенсивность /348/ MH+, 100/, 332 /2/, 275/4/, 263/5/. Элементный анализ для C20H17N3O3 • 1/8 H2O:
Рассчитано: C 68,71 H 4,97 N 12,02
Найдено: C 68,68 H 4,74 N 11,91
Пример 19
5-амино-3-(2-диметиламиноэтил)индол
Смесь 3-(2-диметиламиноэтил)-5-нитроиндола /1,85 г, 7,93 ммоля/ и 10% палладия на угле /0,40 г, 20 вес.%/ в 30 мл абсолютированного этанола встряхивают в атмосфере водорода /3 атм./ в течение 6 часов. Полученную смесь фильтруют через Целит и целитную лепешку промывают интенсивно абсолютированным этанолом. Объединенные фильтраты выпаривают при пониженном давлении до получения указанного в заглавии соединения /1,60 г, 7,87 ммоля, 99%/ в виде прозрачного, слегка темноватого гигроскопического масла: ИК /CHCl3/ 3480, 1610, 1585. 1640, 1335 см-1:
1H ЯМР /CDCl3/ δ: 8,10 /шир. м. NH/, 7,12 /д, J = 8,5 Гц, 1Н/, 6,91 /д, J = 2,3 Гц, 1Н/, 6,88 /д, J = 2,2 Гц, 1Н/, 6,64 /дд. J = 2,2 и 8,5 Гц, 1Н/, 2,89-2,84 /м, 2Н/, 2,64-2,58 /м, 2Н/, 2,34 /с, 6Н/; 13C ЯМР /CDCl3/ δ: 139,1, 131,2, 128,3, 122,2, 113,1, 112,9, 111,7, 103,8, 60,3, 45,4, 23,7; Масс-спектр низкого разрешения /м/z, относительная интенсивность /203 /9, М+/, 158/2/, 145/6/, 83/66/, 58/100/. Масс-спектр высокого разрешения, рассчитано для C12H17N3 203,1424, найдено 203, 1418. Элементный анализ для C12H17N3 • 1/2 H2O:
Рассчитано: C 67,89 H 8,55 N 19,79
Найдено: C 67,71 H 8,60 N 19,41
Пример 20
3-/2-диметиламиноэтил/-5-нитроиндол
К перемешиваемому раствору 5-нитроиндол-3-N,N- диметилглиоксамида /5,36, 20,52 ммоля/ в 55 мл безводного тетрагидрофурана добавляют боран в тетрагидрофуране /1,0 М, 78,8 мл, 78,8 ммоля, 3,8 экв./ медленно по каплям. Полученный реакционный раствор перемешивают при комнатной температуре в атмосфере азота в течение 16 часов. Осторожно добавляют к реакционному раствору насыщенный раствор бикарбоната натрия /200 мл/ и полученную водную смесь экстрагируют трижды диэтиловым эфиром порциями по 150 мл. Эфирные экстракты объединяют, сушат над сульфатом магния, выпаривают при пониженном давлении до получения 3-/2-диметиламиноэтил/-5- нитроиндол боранового комплекса в виде аморфного твердого вещества оранжевого цвета /6,9 г/. 1H ЯМР /ДМСО-d6/ δ: 11,7 /шир. м, NH/, 8,58 /д, J = 2,2 Гц, 1Н/, 8,00 /дд, J = 2,3 и 9,0 Гц, 1Н/, 7,52 /д, J = 8,8 Гц, 1Н/, 7,49 /шир, с, 1Н/, 3,23-3,17 /м, 2Н/, 3,02-2,97 /м, 2Н/, 2,63 /с, 6Н/. Это твердое вещество помещают в абсолютированный этанол /150 мл/ вместе с цезийфторидом /6,9 г/ и карбонатом натрия /6,9 г/ и полученную смесь кипятят с обратным холодильником в атмосфере азота в течение 16 часов. Полученную реакционную смесь фильтруют через целит, и полученный фильтрат выпаривают при пониженном давлении. Оставшееся масло обрабатывают хроматографически на силикагеле /примерно 450 г/, элюируя смесью метиленхлорид/метанол/гидроксид аммония /8:2:0,1/ до получения указанного в заглавии соединения /2,58 г, 11,06 ммоля, 54%/ в виде твердого вещества желтого цвета; Т. плавления 133,0, 135,0oC. ИК /KBr/ 1625, 1575, 1550, 1520, 1480, 1470, 1460, 1445, 1380, 1370, 1330 см-1; 1H ЯМР /ДМСО-d6/ δ: 11,55 /шир. м, NH/, 8,48 /д, J = 2,2 Гц, 1Н/, 7,94 /дд, J = 2,3 и 9,0 Гц, 1Н/ 7,47 /д, J = 9,0 Гц, 1Н/, 7,40 /шир. с, 1Н/, 2,88-2,83 /м, 2Н/, 2,53-2,48 /м, 2Н/, 2,19 /с, 6Н/; 13С ЯМР /ДМСО-d6/ δ: 140,2, 139,3, 126,6, 126,5, 116,3, 116,0, 115,6, 111,7, 59,8, 45,1, 22,7; Масс-спектр низкого разрешения /м/z, относительная интенсивность /233 /7,M+/, 189/7/, 188/8/, 143/10/, 129/23/, 115/14/, 59/36/, 58/100/. Масс-спектр высокого разрешения, рассчитано для C12H15N3O2: 233,1166, найдено: 233,1155.
Элементный анализ для C12H15N3O2:
Рассчитано: C 61,79 H 6,48 N 18,01
Найдено: C 61,39 H 6,45 N 17,68
Пример 21
5-нитроиндол-3-N,N-диметилглиоксамид
К перемешиваемому раствору 5-нитроиндола /10,00 г, 61,7 ммоля и фталимида /4,00 г, 40 вес.%/ в безводном эфире /250 мл/ добавляют оксалилхлорид /17,0 мл, 0,194 моля, 3,1 экв./ по каплям. Полученную реакционную смесь перемешивают при комнатной температуре в атмосфере азота в течение 72 часов. Полученную реакционную смесь охлаждают в ледяной бане /0oC/, и осторожно добавляют раствор эфира /80 мл/ и диметиламина /80 мл, конденсированный при -78oC/ при интенсивном перемешивании. Полученную смесь интенсивно перемешивают при комнатной температуре в течение часа. Эфир из реакционной смеси выпаривают при пониженном давлении, а остаток разделяют между водой /500 мл/ и метиленхлоридом /500 мл/. pH водного слоя устанавливают 3, используя концентрированную HCl. Метиленхлоридный слой удаляют, а водный слой экстрагируют трижды метиленхлоридом /порциями по 500 мл/. Метиленхлоридные экстракты объединяют, сушат над сульфатом магния, выпаривают при пониженном давлении. В результате перекристаллизации оставшейся твердой части в кипящем с обратным холодильником метаноле, при охлаждении получают указанное в заглавии соединение /Rf = 0,15 в 10% ацетоне в метиленхлориде, 5,74/, 22,0 ммоля, 36%/ в виде бледно-желтого твердого вещества. Т. плавления 248,0-249oC. ИК /KBr/ 1755, 1740, 1730, 1650, 1620, 1585, 1530 см-1; 1H ЯМР /ДМСО-d6/ δ: 12,9 /шир. c, NH/, 3,97 /д, J = 2,3 Гц, 1H/, 8,43 /с, 1Н/, 8,18 /дд, J = 2,3 и 9,0 Гц, 1H/, 7,74 /д, J = 9,0 Гц, 1H/, 3,02 /с, 3Н/, 2,95 /с, 3Н/; 13C ЯМР /ДМСО-d6/ δ: 166,6, 143,2, 140,4, 140,2, 124,5, 118,9, 117,2, 114,2, 113,6, 36,8, 33,6. Масс-спектр низкого разрешения /м/z, относительная интенсивность /261 /24, M+/, 190/29/, 189/100/, 173/15/, 143/83/ 115/23/; Масс-спектр высокого разрешения, рассчитано для C12H11N3O4: 261,0750, найдено 261,0746. Элементный анализ для C12H11N3O4:
Рассчитано: C 55,17 H 4,24 N 16,08
Найдено: C 55,15 H 3,96 N 15,96
Пример 22.
5-амино-3-(N-трет.-бутоксикарбонилпиперид-4-ил)-1Н-индол.
Смесь 3-(N-трет. -бутоксикарбонил-1,2,5,6-тетрагиропирид-4- ил)-5-нитро-1Н-индола /3,55 г, 10,34 ммоля/ и 10% палладий на угле /0,55 г/ в 60 мл абсолютированного этанола встряхивают в атмосфере водорода /3 атм/ в течение 7 часов при комнатной температуре. Полученную реакционную смесь фильтруют через диатомовую землю и полученный фильтрат выпаривают при пониженном давлении. Оставшуюся твердую часть тщательно растирают с диэтиловым эфиром до получения указанного в заглавии соединения /2,56 г, 78%/ в виде твердого вещества бледно-розового цвета. Т. плавления с разложением, 215oC. 13С ЯМР /CDCl3/ δ: 155,0, 139,0, 131,3, 127,3, 120,4, 119,8, 112,9, 111,8, 104,1, 79,4, 44,5, 33,8, 32,7, 28,5. Элементный анализ для C18H25N3O2 • 1/2 H2O:
Рассчитано: C 67,57 H 8,03 N 13,13
Найдено: C 67,20 H 8,07 N 13,44.
Пример 23
3-(N-трет. -бутоксикарбонил-1,2,5,6-тетрагидропирид-4-ил)-5- нитро-1Н-индол
К перемешиваемому раствору натрия /2,51 г, 105 ммолей, 7 экв. в 50 мл абсолютированного метанола добавляют 5-нитроиндол /2,43 г 15,0 ммоля/ и N-трет. -бутоксикарбонил-4-пиперидон /8,96 г, 45 ммолей, 3,0 экв./. Полученный реакционный раствор выпаривают при пониженном давлении, а остаток разделяют между насыщенным раствором бикарбоната натрия /50 мл/ и этилацетатом /50 мл/. Органический слой удаляют, а водный слой экстрагируют этилацетатом /2 х 50 мл/. Органические экстракты объединяют, сушат над сульфатом магния и выпаривают при пониженном давлении. В результате обработки экстракционного остатка на колонке с силикагелем /примерно 100 г/ при элюировании этилацетатом в гексанах / градиентное элюирование от 1:2 до 1:1 / получают указанное в заглавии соединение /72%/ в виде твердого вещества желтого цвета. Т. плавления с разложением 230oC; 1H ЯМР /CDCl3/ δ: 9,24 /шир. с, 1Н/, 8,78 /д, J = 1,3 Гц, 1Н/, 8,09 /дд, J = 1,4 и 9,4 Гц, 1Н/, 7,40 /д, J = 9,3 Гц, 1Н/, 7,30 /д, J = 1,8 Гц, 1Н/, 6,17-6,15 /м, 1Н/, 4,16-4,13 /м, 2Н/, 3,68 /т, J = 5,8 Гц, 2Н/, 2,58-2,48 /м, 2Н/, 1,50 /с, 9Н/,
Элементный анализ для C15H21N3O4 • 0,1 H2O
Рассчитано: C 62,62 H 6,19 N 12,17
Найдено: C 62,71 H 6,09 N 11,81
Пример 24
3-(N-трет-бутоксикарбонилпирролидин-2R-илметил)-5-(2,5- диметил-1Н-пиррол-1-ил)-1Н-индол
Смесь 3-(N-бензилоксикарбонил-4-метоксипирролидин-2R- илкарбонил)-5-(2,5-диметил-1Н-пирролил)-1Н-индола /6,16 г, 14,41 ммоля/ и 10% палладия на угле /3,32 г/ в абсолютированном этаноле /75 мл/ встряхивают в атмосфере водорода в течение 20 часов при комнатной температуре. Полученную реакционную смесь фильтруют через Целит, а полученный фильтрат выпаривают при пониженном давлении. Оставшуюся пену растворяют в безводном тетрагидрофуране /50 мл/ и прикапывают ди-трет.-бутилдикарбонат /3,45 г, 15,88 ммоля, 1,1 экв./ к перемешиваемому раствору при комнатной температуре. Этот реакционный раствор перемешивают при комнатной температуре в атмосфере азота в течение 30 минут, затем раствор выпаривают при пониженном давлении. Остаток обрабатывают на хроматографической колонке с силикагелем /примерно 200 г/, элюируя смесью этилацетат/гексаны /1:2/ до получения указанного в заглавии соединения /91%/ в виде белого твердого вещества; (α)25 = -1,3o /метиленхлорид, с = 1/; Масс-спектр высокого разрешения, рассчитано для C24H31N3O2 393,2418, найдено 393,2461.
Элементный анализ для C24H31N3O2:
Рассчитано: C 73,25 H 7,94 N 10,68
Найдено: C 73,28 H 7,76 N 10,51
Пример 25
5-(3-формилиндол-5-ил)-1Н-бензимидазол
Смесь 5-амино-3-(N-метилпирролидин-2R-илметил)-1Н-индола /5,50 г, 21,63 ммоля/ и 10% палладия на угле /1,00 г/ в 75 мл абсолютированного этанола встряхивают в атмосферу водорода /3 атм/ в течение 5 часов. Полученную смесь фильтруют через Целит, полученный фильтрат выпаривают при пониженном давлении. Остаток /4,95 г/ растворяют в диметилформамиддиметилацетале /25 мл/ и полученный раствор кипятят с обратным холодильником в атмосфере азота в течение 12 часов. Затем реакционный раствор выпаривают при пониженном давлении, а остаток помещают в раствор /75 мл/ 10% водный гидроксид натрия/этанол /5: 1/. Полученную смесь кипятят с обратным холодильником в атмосфере азота в течение 3 часов. Затем добавляют концентрированную соляную кислоту для установления pH 3 и эту водную смесь экстрагируют этилацетатом /3 х 75 мл/. Органические экстракты объединяют, сушат над сульфатом магния и концентрируют до примерно 20 мл объема. Осевшую твердую часть фильтруют до получения указанного в заглавии соединения /1,54 г, 29%/ в виде твердого вещества белого цвета. Т. плавления более 280oC; 1H ЯМР /ДМСО-d6/ δ: 12,4 /шир. с, NH/, 9,99 /с, CHO/, 8,86 /с, 1Н/, 8,51-8,50 /м, 1Н/, 8,44-8,41 /м, 1H/, 8,22 /дд, J = 1,5 и 8,0 Гц, 1Н/, 7,76-7,67 /м, 2Н/, 7,39 /дд, J=4,7 и 8,0 Гц, 1Н/. Элементный анализ для C14H10N4 • 0,26 H2O:
Рассчитано: C 67,54 H 3,97 N 21,00
Найдено: C 67,82 H 3,99 N 20,68
Пример 26
5-/3-(2-нитроэтенил)индол-5-ил/-1Н-бензимидазол
Смесь 5-/3-формилиндол-5-ил/-1Н-бензимидазола /0,40 г, 1,53 ммоля/ и ацетата аммония /50 мг/ в растворе нитрометана /10 мл/, N,N-диметилформамида /5 мл/ и диметилсульфоксида /1 мл/ кипятят с обратным холодильником в атмосфере азота в течение 4 часов. Полученную реакционную смесь охлаждают до комнатной температуры и фильтруют до получения указанного в заглавии соединения /0,40 г, 86%/ в виде твердого вещества желтого цвета. Т. плавления более 280oC: 13C ЯМР /ДМСО-d6/ δ: 146,9, 145,3, 144,3, 137,4, 136,6, 135,5, 134,2, 132,1, 129,8, 127,8, 125,0, 119,9, 118,7, 115,9, 113,4, 108,7. Элементный анализ для C16H11N5O2 • 0,125 H2O:
Рассчитано: C 62,49 H 3,69 N 22,77
Найдено: С 62,34 H 3,51 N 22,45
Пример 27
5-(3-нитропирид-2-иламино)-3-(N-(2,2,2- трихлорэтоксикарбонил)-пирролидин-2R-илметил)-1Н-индол
К перемешиваемому раствору (R)-5-(3-нитропирид-2-иламино/-3- (пирролидин-2-илметил/-1Н-индола /0,42 г, 1,24 ммоля/ и пиридина /0,11 мл, 1,36 ммоля, 1,1 экв./ в безводном дихлорэтане /6 мл/ при комнатной температуре добавляют 2,2,2-трихлорэтилхлорформат /0,18 мл, 1,30 ммолей, 1,05 экв./ Полученный реакционный раствор перемешивают при комнатной температуре в атмосфере азота в течение 1,5 часа. Метиленхлорид добавляют к полученной реакционной смеси и полученную смесь промывают насыщенным раствором бикарбоната натрия /20 мл/. Органический слой сушат над сульфатом магния и выпаривают при пониженном давлении до получения указанного в заглавии соединения /0,62 г, 100%/ в виде аморфного твердого вещества красного цвета. FAB масс-спектр низкого разрешения /м/z, относительная интенсивность /516 /MH+, с двумя 37Cl и одним 35Cl, 36/, 515/41/, 514//MH+ с одним 37Cl и двумя 35Cl, 100/, 513/66/, 512//MH+ с тремя 35Cl/, 99/, 511/36/, 498/7/, 478/14/, 391/8/.
Пример 28
5-аминометил-1-/3-(N-(2-метоксиэтил)пирролидин-2R- илметил)-индол-5-ил/-1Н-бензимидазол
К перемешиваемой смеси литийалюминийгидрида /0,200 г, 5,27 ммоля, 3,0 экв. / в безводном тетрагидрофуране /9 мл/ добавляют 5-циано-1-/3-(N-(2-метоксиэтил)пирролидин-2R-илметил)индол-5-ил/-1Н- бензимидазол /0,700 г, 1,75 ммоля/ и полученную реакционную смесь кипятят с обратным холодильником в атмосфере азота в течение 24 часов. Затем осторожно добавляют декагидрат сульфата натрия /примерно 10 г/, затем воду /2 мл/, а затем этилацетат /20 мл/. Полученную смесь перемешивают при комнатной температуре в течение 1 часа. Смесь фильтруют через Целит, и полученный фильтрат выпаривают при пониженном давлении. Остаток обрабатывают на хроматографической колонке с силикагелем /примерно 50 г/ элюируя смесью этилацетат/метанол/триэтиламин /18:1:1 / до получения указанного в заглавии соединения /0,358 г, 51%/ в виде пены бледно-желтого цвета. Rf = 0,15 /метиленхлорид/ метанол/гидроксид аммония 9:1; 0,1/ 13C ЯМР /CD3OD/ δ: 145,2, 144,3, 137,6, 137,2, 135,2, 129,6, 128,7, 126,2, 125,0, 119,3, 119,1, 115,9, 114,5, 113,5, 112,1, 72,3, 67,1, 58,9, 55,8, 55,0, 46,6, 31,6, 30,5, 22,9; (α)25 = +61o /метиленхлорид, с = 1/.
Элементный анализ для C24H29N5O • 0,25 этилацетат C4H8O2 • 0,8
Рассчитано: C 68,30, H 7,47 N 15,93
Найдено: C 67,97 H 7,19 N 15,95
Пример 29
5-аминометил-1-/3-(N-метилпирролидин-2R-илметил)индол-5-ил/- 12-бензимидазол
Смесь никеля Ренея /примерно 0,25 г/ и 5-циано-1-/3-(N- мeтилпиppoлидин-2R-илмeтил)индoл-6-ил/-1H-бeнзимидaзoлa /1,00 г, 2,81 ммоля/ в абсолютированном этаноле, насыщенном аммиаком, встряхивают в атмосфере водорода /3 атм/ в течение 5 часов. Полученную смесь фильтруют через Целит, полученный фильтрат выпаривают при пониженном давлении до получения указанного в заглавии соединения /0,900 г, 89%/ в виде грязно-белой пены, Rf = 0,2 /этилацетат/метанол/триэтиламин /6: 2: 2/; 13С ЯМР (CD3OD) δ: 143,5, 142,9, 137,5, 136,1, 136,0, 133,5, 128,1, 127,4, 124,7, 123,4, 117,7, 117,5, 114,2, 113,0, 112,1, 110,5, 66,9, 56,9, 45,6; 39,6, 30,9, 28,8, 21,0. Элементный анализ для C22H25N5 • 1,5 H2O:
Рассчитано: C 68,36 H 7,30 N 18,12
Найдено: C 68,26 H 7,38 N 17,88
Пример 30
Общий способ ацилирования 5-аминометил-1-/3-(N-(2-метоксиэтил)- пирролидин-2R-илметил)индол-5-ил/-1Н-бензимидазола
К перемешиваемому раствору 5-аминометил-1-/3-(N-(2- метоксиэтил)пирролидин-2R-илметил)индол-5-ил/-1Н-бензимидазола /0,100 г 0,25 ммоля/ и триэтиламина /0,04 мл, 0,3 моля, 1,1 экв./ в абсолютированном этаноле /3 мл/ при комнатной температуре прикапывают соответствующий ацилирующий агент /0,27 ммоля, 1,1 экв. /. Полученный реакционный раствор перемешивают при комнатной температуре в атмосфере азота в течение ночи, затем его выпаривают при пониженном давлении. Остаток обрабатывают на хроматографической колонке с силикагелем/примерно 10 г/, элюируя соответствующей системой растворителей, до получения соответствующего 5-ациламинометил-1-/3-(N-(2-метоксиэтил) пирролидин-2R-илметил)индол-5-ил/-1Н-бензимидазола. Указанным способом получают следующие соединения:
А. 5-ацетиламинометил-1-/3-(N-(2-метоксиэтил)пирролидин-2R - илметил)индол-5-ил/-1Н-бензимидазол
В качестве ацилирующего агента используют ацетилхлорид, реакционный остаток обрабатывают хроматографически, элюируя 5% метанолом в метиленхлориде до получения указанного в заглавии соединения /68%/ в виде бледно-коричневого твердого вещества: Rf = 0,35 в 10% метаноле в метиленхлориде. 13С ЯМР /CD3OD/ δ: 173,6, 142,5, 140,6, 138,5, 132,8, 132,4, 128,8, 128,3, 128,2, 126,6, 119,4, 117,0, 114,7, 114,5, 114,4, 111,7, 70,3, 68,2, 59,3, 56,3, 55,4, 43,9, 30,9, 27,8, 22,7. Масс-спектр высокого разрешения, рассчитано для C26H31N5O2 445,2480, найдено 445,2439, (α)25 = +71o /метиленхлорид, c = 1/.
В. N-фенил-N'-/3-(N-(2-метоксиэтил)пирролидин-2R-илметил) индол-5-ил/-1Н-бенз[b]имидазилметилмочевина
В качестве ацилирующего агента используют фенилизоцианат, реакционный остаток обрабатывают хроматографически, элюируя смесью этилацетат/метанол/триэтиламин /36:1:1/ до получения указанного в заглавии соединения /57%/ в виде белого аморфного вещества; Rf = 0,3 /этилацетат/метанол/триэтиламин /18:1:1/; FAB масс-спектр высокого разрешения, рассчитано для [C31H34N6O2 • H] 523,2825, найдено 523,2866 (α)25 = 169o /метиленхлорид, с = 1/.
С. 5-бензоиламинометил-1-/3-(N-(2-метоксиэтил)пирролидин-2R- илметил)индол-5-ил/-1Н-бензимидазол
В качестве ацилирующего агента используют бензоилхлорид, а реакционный остаток обрабатывают хроматографически, элюируя смесью этилацетат/метанол/триэтиламин /18:1:1/ до получения указанного в заглавии соединения /20%/ в виде белого аморфного вещества; Rf = 0,5 /этилацетат/метанол/триэтиламин 16: 1:1/; FAB масс-спектр высокого разрешения, рассчитано для [C31H33N5O2 • H] 508,2715, найдено 508,2722; (α)25 = +75o /метиленхлорид, с = 1/.
Пример 31
5-амино-3-(N-трет. бутоксикарбонил-1,2,5,6-тетрагидропирид-4- ил)-1Н-индол
К перемешиваемому раствору натрия /2,61 г, 0,114 моля/ в 50 мл абсолютированного метанола добавляют 5-аминоиндол/ 2,50 г, 18,9 ммоля/ и 4-N-трет. -бутоксикарбонилпиперидон /9,42 г, 47,3 ммоля, 2,5) кв/. Полученный реакционный раствор кипятят с обратным холодильником в атмосфере азота в течение 6 часов. Затем реакционный раствор выпаривают при пониженном давлении, а остаток разделяют между этилацетатом и насыщенным раствором бикарбоната натрия /100 мл каждого/. Органический слой удаляют, а водный слой экстрагируют этилацетатом /2 х 100 мл/. Органические экстракты объединяют, сушат над сульфатом магния и выпаривают при пониженном давлении. Остаток обрабатывают на хроматографической колонке с силикагелем /150 г/, элюируя диэтиловым эфиром до получения указанного в заглавии соединения /4,10 г, 70%/ в виде грязно-белой пены. Rf = 0,1 /диэтиловый эфир/ 1H ЯМР /CD3OD/ δ: 7,26 /д, J = 1,8 Гц, 1Н/, 7,17 /с, 1Н/ 7,16 /д, J = 6,8 Гц, 1Н/, 6,70 /дд, J= 2,0 и 8,5 Гц, 1Н/, 6,06 /шир. м, 1Н/, 4,88 / в обмене H/, 4,09 /шир. м, 2Н/, 3,65 /шир. т, J = 5,7 Гц, 2Н/, 2,52 /шир. м, 2Н/, 1,49 /с, 9Н/
Пример 32
6-гидрокси-5-нитроникотиновая кислота
Смесь 6-гидроксиникотиновой кислоты /16,60 г, 0,119 моля/ и дымящейся азотной кислоты /166 мл/ нагревают при 50oC в течение 4 часов. Полученный реакционный раствор охлаждают до комнатной температуру, а затем осторожно добавляют ко льду /300 г/. Полученную смесь хранят при 10oC в течение ночи, а затем твердый осадок фильтруют и сушат в вакууме до получения указанного в заглавии соединения /5,50 г, 0,027 моля, 23%/ в виде твердого вещества желтого цвета. 1H ЯМР /ДМСО-d6/ δ: 13,4 /шир. с, 2Н/, 8,64 /д, J = 2,2 Гц, 1Н/, 8,37 /д, J = 2,2 Гц, 1Н/, 13С ЯМР /ДМСО-d6/ δ: 164,1, 154,4, 138,5, 137,2, 107,9. Масс-спектр высокого разрешения, рассчитано для C6H4N2O5 184,0120, найдено 184,0134.
Элементный анализ для C6H4N2O5
Рассчитано: C 39,14 H 2,19 N 15,21
Найдено: C 39,21 H 2,33 N 15,56
Пример 33
6-хлор-5-нитроникотинамид
Смесь 6-гидрокси-5-нитроникотиновой кислоты /1,33 г, 7,22 ммоля/ пятихлористого фосфора /1,5 г, 7,20 ммолей, 1,0 экв./ и хлорокиси фосфора /2,7 мл/ нагревают при 130oC в атмосфере азота в течение 4 часов. Полученный раствор концентрируют, выпаривая при понижением давлении. Оставшееся масло /предположительно 6-хлор-5- нитроникотиновой кислоты хлорангидрид/ растворяют в растворе тетрагидрофурана и метиленхлорида /1:1, 20 мл/ и этот раствор охлаждают до -78oC. Прикапывают раствор аммиака в ТГФ /2,7 М, 15 мл, 40 ммолей, 5 экв. / и полученный реакционный раствор оставляют нагреваться до комнатной температуры. Затем добавляют 50 мл воды, и водную смесь экстрагируют метиленхлоридом /2 х 50 мл/. Полученные экстракты объединяют, сушат над сульфатом натрия и выпаривают при пониженном давлении до получения указанного в заглавии соединения /0,72 г, 3,57 ммоля, 49%/ в виде твердого вещества желтого цвета. 1H ЯМР /CD3OD/ δ: 9,05 /д, J = 2,2 Гц, 1Н/, 8,81 /д, J = 2,2 Гц, 1Н/, 4,88 /с, 2Н в обмене/ 13C ЯМР /CD3OD/ δ: 166,7, 152,5, 146,1, 135,0, 131,37 Масс-спектр высокого разрешения для C6H4ClN3O3 рассчитано 200,9942, найдено 200,9938. Элементный анализ для C6H4ClN3O3:
Рассчитано: C 35,75 H 2,00 N 20,85
Найдено: C 35,41 H 2,14 N 20,29
Пример 34
2-хлор-5-циано-3-нитропиридин
Смесь 6-хлор-5-нитроникотинамида /0,60 г, 2,98 ммоля/ и хлорокиси фосфора /9 мл/ нагревают при кипячении с обратным холодильником в атмосфере азота в течение 3 часов. Затем реакционный раствор выпаривают при пониженном давлении, а оставшееся масло разделяют между насыщенным раствором бикарбоната натрия и этилацетатом /по 10 мл каждого/. Органический слой удаляют, сушат над сульфатом натрия, и выпаривают при пониженном давлении до получения указанного в заглавии соединения /0,38 г, 2,07 ммоля, 69%/ в виде твердого вещества желтого цвета.
1H ЯМР /CD3OD/ δ: 9,00 /д, J = 2,0 Гц, 1Н/, 8,91 /д, J = 1,9, Гц, 1Н/. 13C ЯМР /CD3OD/ δ: 156,1, 147,7, 139,4, 115,3, 111,3; Масс-спектр высокого разрешения, рассчитано для C6H2ClN3O2 182,9837, найдено 182,9834. Элементный анализ для C6H2ClN3O2 • 0,08 C4H8O2 /этилацетат/:
Рассчитано: C 39,82 H 1,40 N 22,05
Найдено: C 39,47 N 1,48 N 21,99
Все соединения относятся к низкотоксичным продуктам.
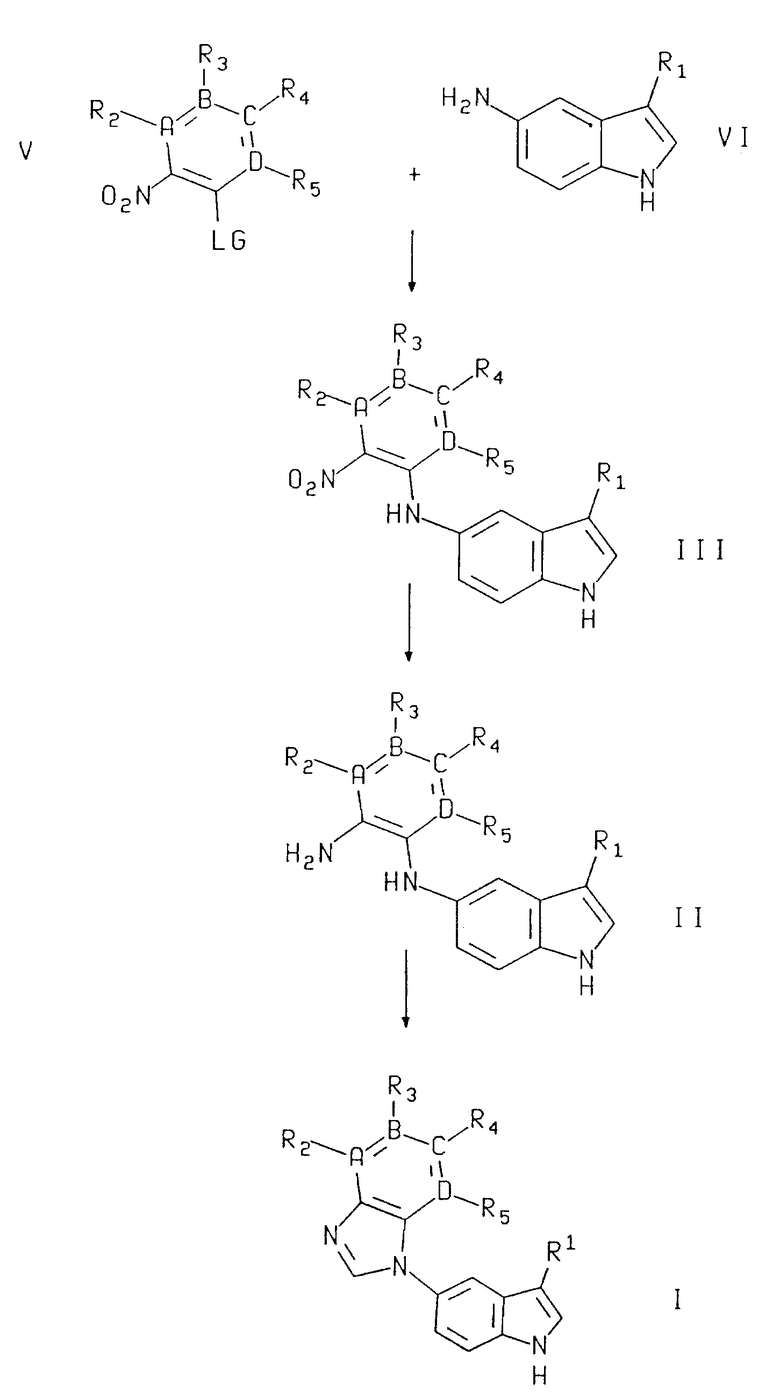
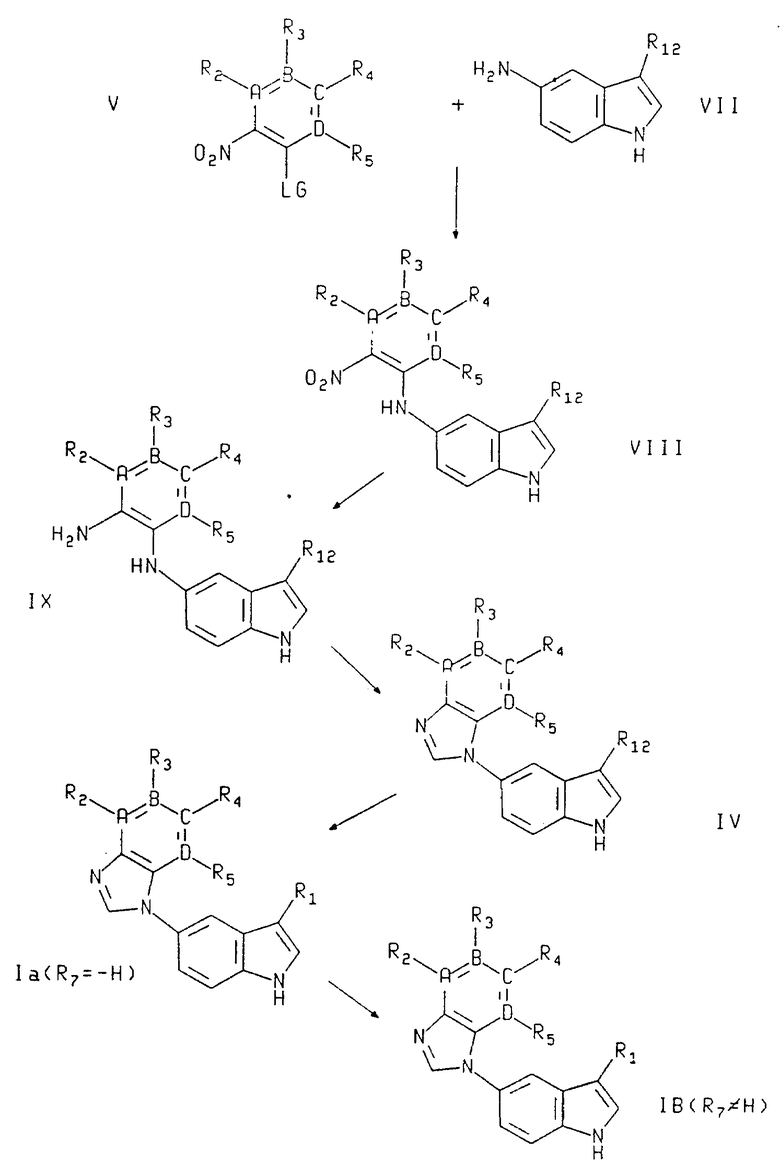
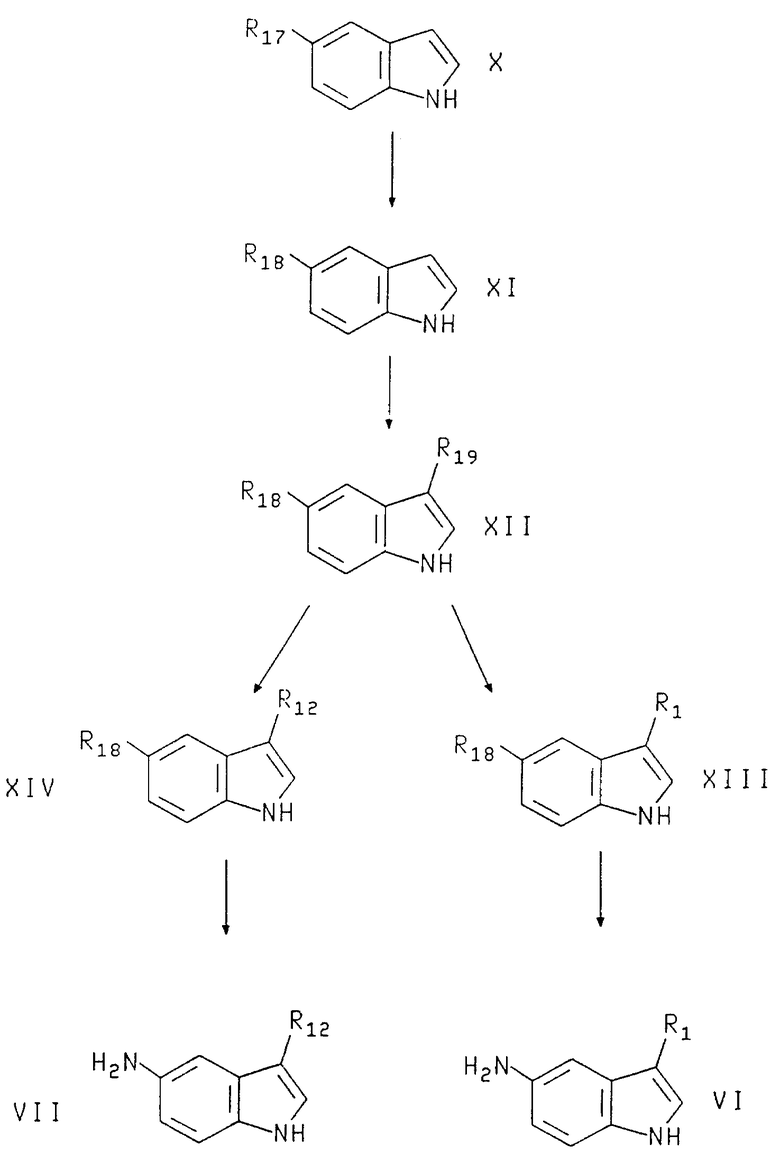
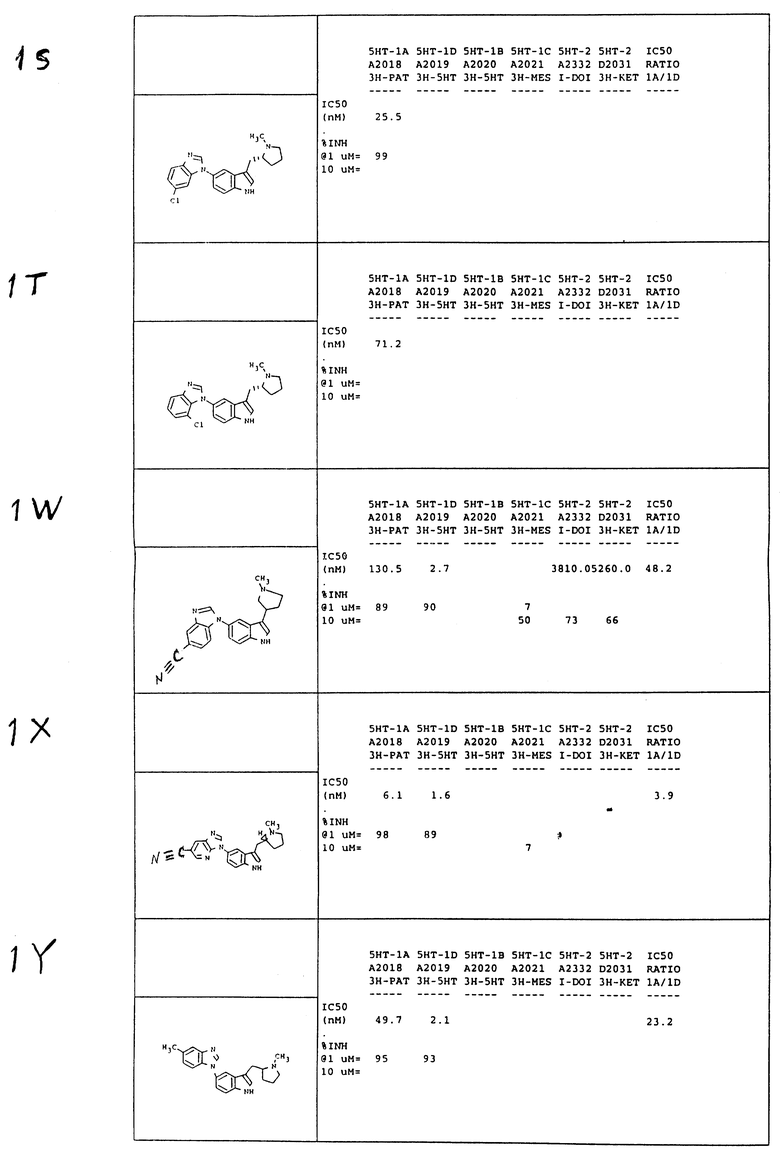

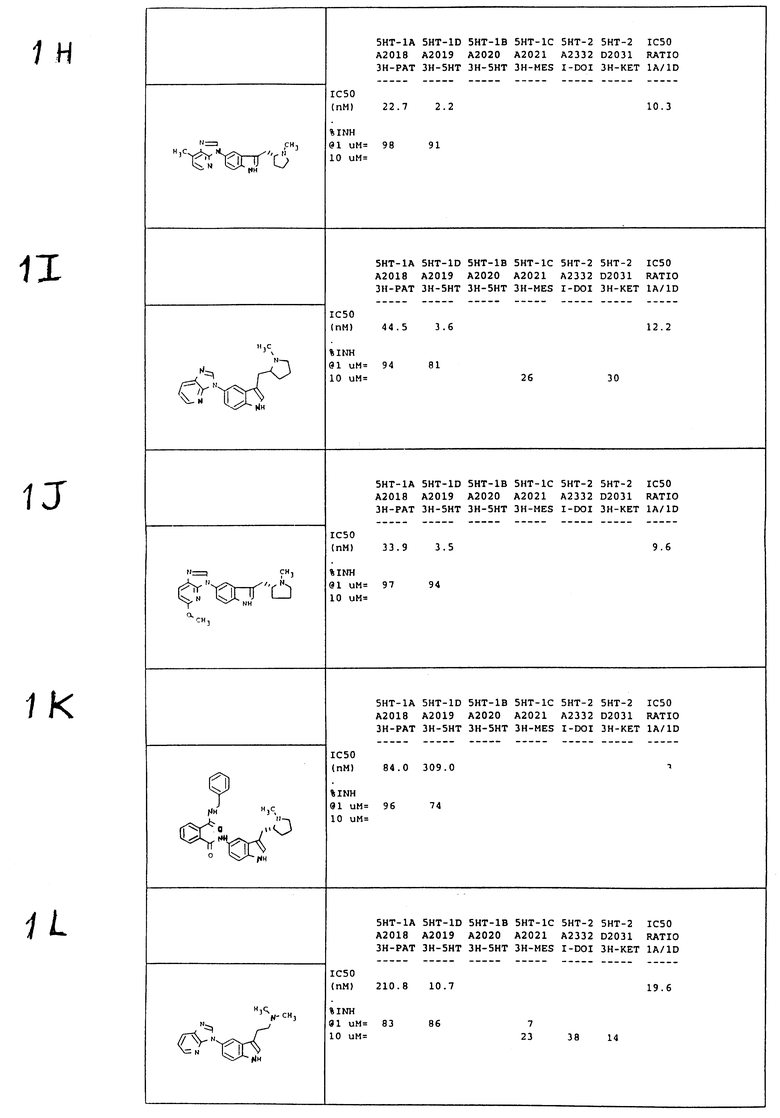
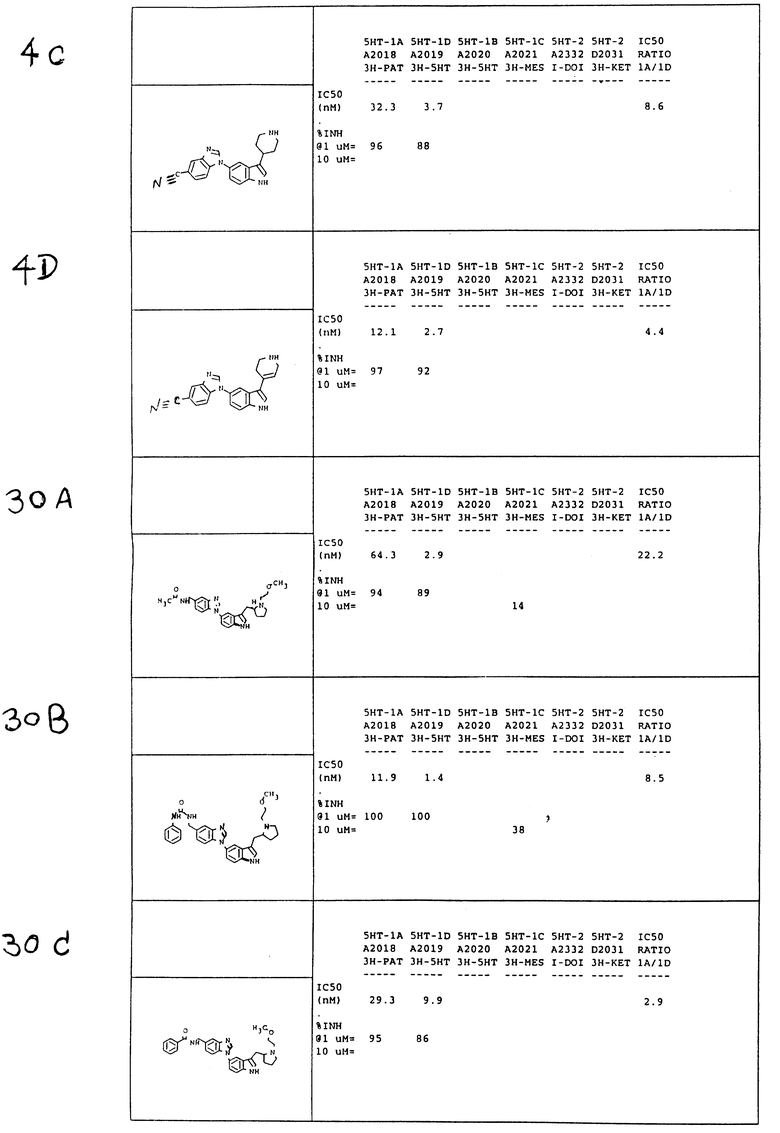
Изобретение относится к новым производным 5-арилиндола формулы I, где R1 имеет значения указанные в описании, A, B, C, D - каждый представляет углерод или один из них представляет азот; R2, R3, R4, R5 - каждый независимо представляет водород, С1 - C6-алкил, фенил, галоид циано-, -(CH2)mNR14R15, -(CH2)mOR9, -(CH2)mNR14COR9, -(CH2)mNR14CONHR9, -CO2R9; R6 представляет водород, -OR10; R7, R8, R14, R15 - каждый независимо представляет водород, С1 - C6-алкил, (CH2)xOR11; R9 представляет водород, С1 - C6-алкил, фенил; R10 представляет С1 - C10-алкил; R11 представляет С1 - C6-алкил; n = 0,1 или 2; m = 0, 1, 2 или 3; x = 2 или 3; пунктирная линия означает необязательно одинарную связь или их фармацевтически приемлемые соли. Описывается фармацевтическая композиция на основе соединений формулы I, связывающая рецепторы 5НТ-1А и 5НТ-1 при лечении состояний, выбираемых из гипертензии, депрессии, мигрени, а также способ связывания рецепторов. 4 с. и 15 з.п.ф-лы, 1 табл.
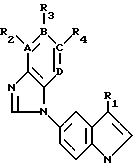
R1 представляет собой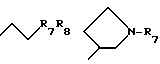
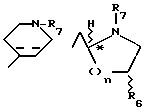
А, В, С, D - каждый представляет углерод или один из них представляет азот;
R2, R3, R4, R5 - каждый независимо представляет водород, С1-С6-алкил, фенил, галоид, циано-, -(СН2)m NR14R15, -(CH2)mOR9, -(СН2)mNR14СОR9, - (СН2)mNR14CONHR9, -СО2R9;
R6 представляет водород, ОR10;
R7, R8, R14, R15 - каждый независимо представляет водород, С1-С6-алкил, -(СН2)хОR11;
R9 представляет водород, С1-С6-алкил, фенил;
R10 представляет С1-С10-алкил;
R11 представляет С1-С6-алкил;
n = 0, 1 или 2;
m = 0, 1, 2 или 3;
х = 2 или 3;
пунктирная линия означает необязательно одинарную связь,
или их фармацевтически приемлемые соли.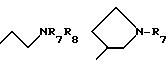
или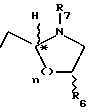
3. Соединение по п.2, где R1 представляет собой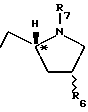
4. Соединение по п.3, которое является цис-эпимером.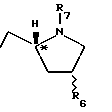
9. Соединение по п.8, которое является цис-эпимером.
5-циано-1-/3-(N-(2-метоксиэтил)пирролидин-2R-илметил)индол-5-ил/-1Н-бензимидазола,
1-/3-(2-N,N-диметиламиноэтил)индол-5-ил/-3Н-имидазо [4, 5-b]-пиридина,
1-/3-(2-аминоэтил)индол-5-ил/-3Н-имидазо [4, 5-b]пиридина,
1-/3-(N-метилпирролидин-2R-илметил)индол-5-ил)/-5-фенил-1Н-бензимидазола,
6,7-дихлор-1-/3-(N-метилпирролидин-2R-илметил)индол-5-ил/-1Н-бензимидазола,
1-/3-(пиперид-4-ил)индол-5-ил/-3Н-имидазо [4, 5-b]пиридина,
5-хлор-1-/3-(N-метилпирролидин-2R-илметил)индол-5-ил/-1Н-бензимидазола,
6-хлор-1-/3-(N-метилпирролидин-2R-илметил)индол-5-ил/-1Н-бензимидазола,
5-аминометил-1-/3-(N-(2-метоксиэтил)пирролидин-2R-илметил)-индол-5-ил/-1Н-бензимидазола,
5-ацетиламинометил-1-/3-(N-(2-метоксиэтил)пирролидин-2R-илметил)индол-5-ил/-1Н-бензимидазола,
5-циано-1-/3-(пиперид-4-ил)индол-5-ил/-1Н-бензимидазола,
5-циано-1-/3-(1,2,5,6-тетрагидропирид-4-ил/-1Н-бензимида-5-циано-1-/3-(N-метилпирролидин-3-ил)индол-5-ил/-1Н-бензимидазола,
5-бензоиламинометил-1-/3-(N-(2-метоксиэтил)пирролидин-2R-илметил)индол-5-ил/-1Н-бензимидазола,
5-аминометил-1-/3-(N-метилпирролидин-2R-илметил)индол-5-ил/-1Н-бензимидазола,
5-циано-1-/3-(N-метилпирролидин-2R-илметил)индол-5-ил/-1Н-пиридо [4, 5 b] имидазола, и
4-метил-1-/3-(N-метилпирролидин-2R-илметил)индол-5-ил/-1Н-пиридо [4, 5 b]-имидазола.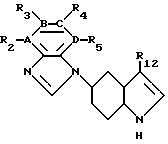
где А, В, С, D - каждый представляет углерод или один из них представляет азот;
R2, R3, R4, R5 - каждый независимо представляет водород, С1-С6-алкил, фенил, галоид, циано-, -(СН2)m NR14CONHR9, -СО2R9,
R6 представляет водород, ОR10;
R7, R14, R15 - каждый независимо представляет водород, С1-С6-алкил, (СН2)хОR11;
R9 представляет водород, С1-С6-алкил, фенил;
R10 представляет С1-С6-алкил;
R11 представляет С1-С6-алкил;
R12 представляет собой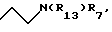
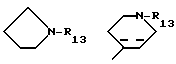
или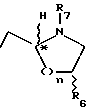
R13 - представляет -СО2R16;
R16 представляет С1-С6-алкил, С1-С3-алкилфенил,
пунктирная линия представляет необязательно одинарную связь.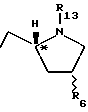
17. Соединение по п.16, которое является цис-эпимером.
| EP 438230, 1991 | |||
| Справочник практического врача | |||
| - М.: Медицина, ч.2, 1990, с.94, 117. |
Авторы
Даты
1999-08-10—Публикация
1993-10-19—Подача