Изобретение относится к области органического синтеза, в частности к получению пропионовой кислоты. Пропионовая кислота и ее производные находят широкое применение в промышленности органического синтеза, в пищевой, парфюмерной, фармацевтической, лакокрасочной, лесохимической промышленности, а также в сельском хозяйстве для консервации кормов и предохранения зерна от порчи и слеживания.
В настоящее время установлено, что наиболее перспективный метод получения пропионовой кислоты основан на реакции каталитического гидроксикарбонилирования этилена моноксидом углерода и водой:
C2H2 + CO + H2O ---> CH3CH2COOH.
Известен способ получения пропионовой кислоты гидроксикарбонилированием этилена моноксидом углерода и водой в присутствии катализатора - карбонила никеля [K. Weissermel, H.J.Arpe "Industrielle Organische Chemie", 1978, 2. Auflage, Verlag chemie, S. 132]. Из-за низкой активности катализатора процесс ведут в очень жестких условиях (200-240 атм, 270-320oC). Селективность по целевому продукту - 95%.
Известен более селективный способ получения пропионовой кислоты гидроксикарбонилированием этилена моноксидом углерода и водой в присутствии каталитической системы, содержащей дихлоро-бис-(трифенилфосфин)палладий (2+) в среде диоксана [А.С. СССР, N 1237659, кл. C 07 C 51/14, Б.И. N 22, 1986 г.]. Процесс характеризуется невысокими выходом целевого продукта и скоростью.
Более высокие показатели достигнуты в способе получения пропионовой кислоты (далее ПК) [ЕР 0759420 A1, кл. C 07 C 51/14, 1996 г.], заключающемся в проведении реакции гидроксикарбонилирования этилена моноксидом углерода и водой в присутствии соединений родия и больших количеств (лучше 10 мас.%) пиридина или его производных и в растворе пропионовой кислоты. Максимальная селективность по ПК 96 мас.% достигнута при 90oC и 100 атм при скорости 585 моль ПК/моль Rh•час. Кроме того, наряду с ПК образуются значительные количества пропионового альдегида, диэтилкетона, 4-кетокапроновой кислоты и др., что усложняет технологию выделения целевого продукта.
Наиболее близким к заявляемому является способ получения пропионовой кислоты гидроксикарбонилированием этилена моноксидом углерода и водой в среде органической карбоновой кислоты в присутствии каталитической системы, содержащей безгалоидное соединение палладия и третичный органический фосфин [А. С. СССР, N 1696422, кл. C 07 C 53/122, Б.И. N 45, 1991 г.]. Данный способ характеризуется высокой селективностью (не менее 99 мас.%), но недостаточно высоким выходом целевого продукта в расчете на палладий.
Задачей изобретения является усовершенствование способа получения пропионовой кислоты с высоким выходом при сохранении высокой селективности.
Задача изобретения достигается тем, что способ получения пропионовой кислоты включает:
- гидроксикарбонилирование этилена моноксидом углерода и водой в среде органической карбоновой кислоты C1-C10, преимущественно пропионовой кислоты при повышенных давлении и температуре;
- в присутствии каталитической системы, включающей безгалоидное соединение палладия и третичный органический фосфин. В качестве безгалоидного соединения палладия используют по крайней мере одно соединение из ряда, включающего соединения, не содержащие связь палладий-галоид, например ацетат, пропионат, ацетилацетонат, сульфат, нитрат, перхлорат палладия (2+), при этом преимущественно используют ацетат, пропионат, ацетилацетонат палладия (2+). В качестве безгалоидного соединения палладия используют также по крайней мере одно соединение из его комплексных соединений с третичным органическим фосфином, в частности комплексное соединение палладия (O), преимущественно тетракис(трифенилфосфин)палладий (O); комплексное соединение палладия (1+), преимущественно μ-гидридо-μ-карбонил-тетракис (трифенилфосфин) палладий (1+), - перхлорат; комплексное соединение палладия (2+), преимущественно диацетато- бис(трифенилфосфин)палладий (2+).
В качестве третичного органического фосфина используют по крайней мере одно соединение из ряда, включающего третичные органические фосфины, содержащие по крайней мере один заместитель, связанный с атомом фосфора через ароматический атом углерода, например диалкиларилфосфин, алкилдиарилфосфин, триарилфосфин, при этом из ряда диалкиларилфосфинов преимущественно используют диизопропилфенилфосфин; из ряда алкилдифенилфосфинов преимущественно используют изопропилдифенилфосфин; из ряда триарилфосфинов преимущественно используют трифенилфосфин, три(п-толил)фосфин, дифенил-м-сульфофенилфосфин (Na, К соль);
- в присутствии добавки основного характера, в качестве которой используют по крайней мере одно соединение из ряда: оксид щелочного, щелочноземельного металла, гидроксид щелочного, щелочноземельного металла, карбонат щелочного, щелочноземельного металла, бикарбонат щелочного, щелочноземельного металла, карбоксилат щелочного, щелочноземельного металла в количестве не менее 0,05 мас.%, при этом в качестве карбоксилата щелочного, щелочноземельного металла используют соль органической карбоновой одно-, двух-, многоосновной кислоты C1-C12 со щелочным, щелочноземельным металлом, например соль алифатической карбоновой кислоты C1-C10 со щелочным, щелочноземельным металлом, преимущественно формиат, ацетат, пропионат натрия.
Установлено, что при взаимодействии безгалоидного соединения палладия (2+) с третичным органическим фосфином как в реакционной среде, так и в других растворителях образуются комплексные соединения L4Pd(O), L2Pd(2+)A2, LnPd2A2, где L - третичный органический фосфин, A - анион, не образующий связи палладий-галоид. Поэтому в качестве безгалоидных соединений палладия можно использовать комплексы палладия с третичными органическими фосфинами, причем степень окисления палладия может быть от 0 до 2.
Роль добавки основного характера согласно имеющимся данным заключается в повышении концентрации карбоксилат-ионов, стабилизирующих каталитическую частицу. Каталитически активная частица предположительно содержит димер одновалентного палладия. Стабилизация может осуществляться за счет бидентантности карбоксилата, как показано ниже: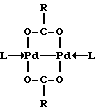
где RCOO- - анион используемой органической карбоновой кислоты, L - третичный органический фосфин.
Оксиды, гидроксиды, карбонаты щелочных, щелочноземельных металлов в реакционной среде превращаются в карбоксилаты.
Процесс гидроксикарбонилирования этилена моноксидом углерода и водой ведут при давлении выше атмосферного, преимущественно при 7-100 атм, причем соотношение давления моноксида углерода к давлению этилена от 3 до 0,5, преимущественно от 2 до 1.
Температурный режим определяется условиями контролируемой скорости реакции, стабильной работы каталитической системы, стойкостью материала реактора к реакционной среде и выбирается в интервале преимущественно 90-165oC.
Изобретение иллюстрируется следующими примерами.
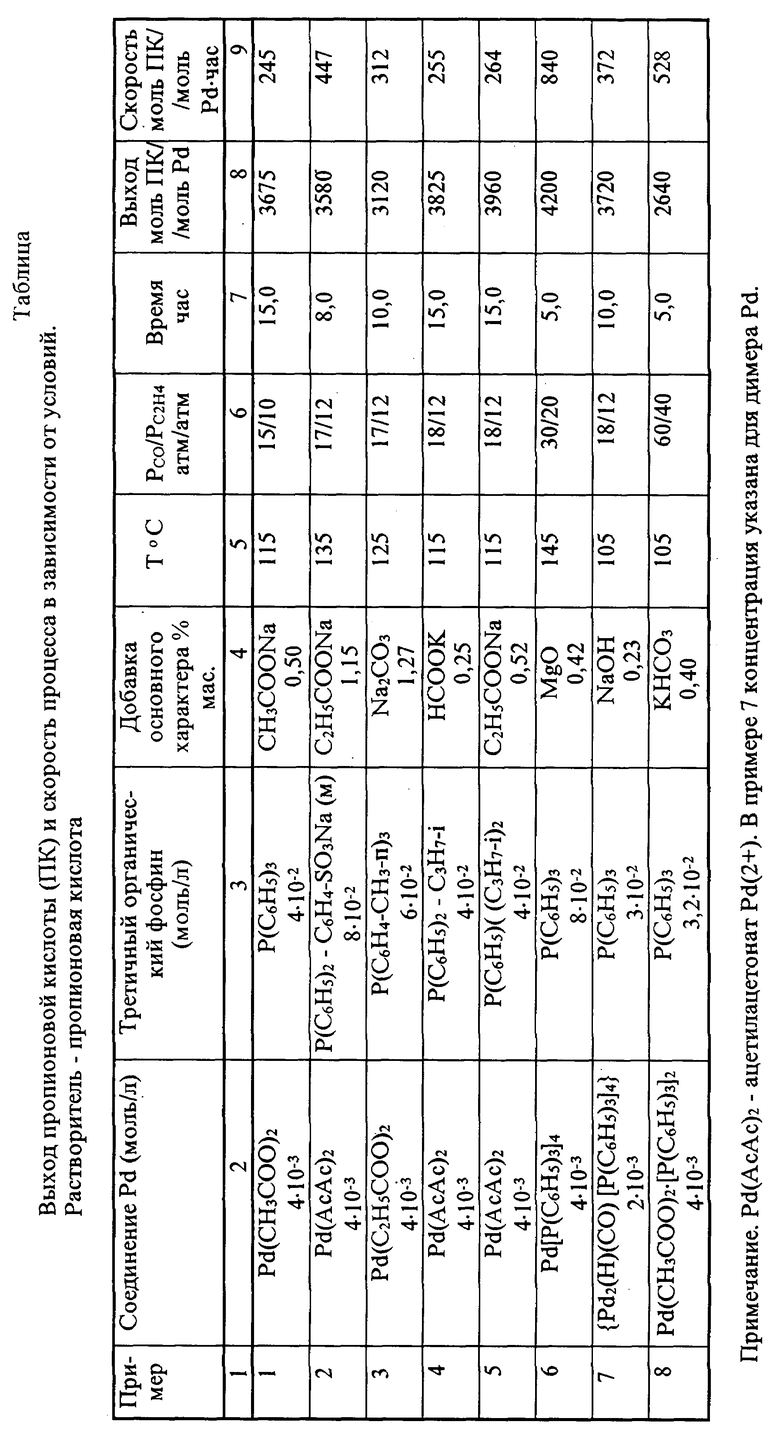
Пример 1. В реактор из нержавеющей стали загружают 11,2 мг (0,05 ммоль) ацетата палладия (2+), 131 мг (0,5 ммоль) трифенилфосфина, 11,5 г пропионовой кислоты, 1,0 г воды и 63 мг (0,5 мас.%) ацетата натрия. Реактор откачивают, подают 5 атм моноксида углерода и нагревают при перемешивании до 125oC. Затем давление доводят до 25 атм эквимолярной смесью моноксида углерода и этилена и процесс ведут при постоянном давлении, добавляя в реактор реагенты (моноксид углерода, этилен и воду) по мере их расхода. Через 10 часов процесс заканчивают, реактор охлаждают, газ собирают для ГЖХ-анализа, измеряют вес жидкой фазы (26,1 г). Жидкую фазу анализируют ГЖХ, определяют содержание ПК и воды и наличие побочных продуктов. Теоретически возможные побочные продукты: этиловый и н-пропиловый спирт, уксусный и пропионовый альдегид, диэтилкетон, этилпропионат, н-пропилпропионат, 4-кетокапроновая кислота. В данном опыте анализ газа показал кроме исходных газов наличие следов этана, диоксида углерода и кислорода, которые накопились из исходных газов. Анализ жидкой фазы показал отсутствие вышеуказанных побочных продуктов. По результатам взвешивания и ГЖХ анализа вычисляют количество полученной пропионовой кислоты (13,6 г), выход и скорость образования ПК, которые в данном опыте составили 3675 моль/моль Pd и 245 моль ПК/моль Pd-час (см. таблицу).
Примеры 2-8. Опыты проводят как в примере 1, берут указанные в таблице компоненты каталитической системы в указанных концентрациях и процесс ведут в указанных в таблице условиях. Ни в одном из примеров побочных продуктов не обнаружено.
Поставленная задача достигается также при всех других заявленных компонентах каталитической системы.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОЧИСТКИ ВЫХЛОПНЫХ ГАЗОВ ДВИГАТЕЛЯ ВНУТРЕННЕГО СГОРАНИЯ | 1999 |
|
RU2159344C1 |
| Способ получения пропионовой кислоты | 1990 |
|
SU1696422A1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРИДА ТИТАНА | 2002 |
|
RU2208573C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГРАФИТОПОДОБНОГО НИТРИДА БОРА | 1999 |
|
RU2163562C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРИСТОГО МАТЕРИАЛА И МАТЕРИАЛ, ПОЛУЧЕННЫЙ ЭТИМ СПОСОБОМ | 2000 |
|
RU2175904C2 |
| Двухстадийный способ получения пропионовой кислоты | 2016 |
|
RU2616623C1 |
| СПОСОБ ПЕРЕРАБОТКИ ТВЕРДЫХ ВЫСОКОАКТИВНЫХ ОТХОДОВ | 1999 |
|
RU2176830C2 |
| МОСТОВОЕ УСТРОЙСТВО | 2000 |
|
RU2175137C1 |
| МОСТОВОЕ УСТРОЙСТВО МАШКИНОВА | 1998 |
|
RU2138056C1 |
| СТАБИЛИЗИРОВАННЫЙ ИСТОЧНИК ПИТАНИЯ | 1999 |
|
RU2159460C1 |

Изобретение относится к способу получения пропионовой кислоты путем гидроксикарбонилирования этилена моноксидом углерода в среде воды и органической каробоновой кислоты С2-С4. Процесс ведут при повышенных давлении и температуре в присутствии каталитической системы, включающей безгалоидное соединение палладия и третичный органический фосфин с добавкой основного характера. В качестве добавки используют по крайней мере одно соединение из ряда: оксид, гидроксид, карбонат, бикарбонат или карбоксилат щелочного либо щелочноземельного металла в количестве не менее 0,05 мас.% В качестве карбоксилата щелочного или щелочноземельного металла используют соль органической карбоновой одно-, двух-, многоосновной кислоты С1-С12, например соль алифатической карбоновой кислоты C1-C10, преимущественно пропионат натрия. В результате повышается выход пропионовой кислоты. 14 з.п.ф-лы, 1 табл.
| Способ получения пропионовой кислоты | 1990 |
|
SU1696422A1 |
| Способ получения пропионовой кислоты | 1984 |
|
SU1237659A1 |
| EP 0759420 A1, 26.02.97. | |||
Авторы
Даты
1999-08-20—Публикация
1997-11-19—Подача