Изобретение обеспечивает гомогенную реакционную среду и способ использования гомогенного комплексного катализатора на основе кислоты Льюиса-углеводорода для получения алкилатного продукта, смешиваемого с моторными бензинами.
Кроме того, изобретение обеспечивает способ использования гомогенного катализатора для превращения нормальных алканов в изоалканы и α-олефинов во внутренние олефины. Изоалканы и олефины можно затем подвергнуть реакции алкилирования для образования алкилатов, подходящих для вмешивания в моторные бензины.
Типичные моторные бензины, не содержащие свинец, с различными сортами октана, продаваемые в наши дни в США, получают путем смешивания потоков различных компонентов, которые являются конечными продуктами ряда процессов очистки углеводородов. Например, типичная бензиновая смесь может содержать в качестве своих компонентов гидрокрекинговый бензин, получаемый путем каталитической гидрогенизации в "гидрокрекинговой" установке, крекинг-бензины, получаемые путем псевдоожиженного каталитического крекинга, реформат, полученный каталитической реформацией нафты, алкилат, полученный путем кислотного алкилирования изобутанов и олефинов, нормальный бутан, полученный от перегонки сырого масла или природного газа и т.д. Для того чтобы получить бензины, имеющие определенное октановое число и другие конкретные свойства, например, давление пара, регулируют относительные количества этих компонентных потоков в бензиновой смеси. Например, если желательно получить бензин с повышенным значением октанового числа, тогда следует добавить большую долю компонентов с повышенным значением октанового числа, в то время как количество низкооктановых компонентов следует уменьшить или удалить из смеси.
В качестве предпосылки принятия во внимание октановых чисел долгое время признавали, что сильноразветвленные углеводороды и ароматические углеводороды, например, бензол, толуол и ксилол, имеют высокие октановые числа. Это означает, что когда эти углеводороды смешивают с воздухом при температуре и давлении, достаточных для допущения полного испарения и воспламенения смеси, они сгорают с равномерной скоростью сгорания и не сгорают со взрывом. Взрывчатое сгорание или "детонирование" причиняет ущерб моторам внутреннего сгорания, если это продолжается в течение длительного периода времени.
Нефтеперерабатывающая промышленность имеет разработанные стандарты и способы сравнения сгорания различных углеводородов и смесей углеводородов 2,2,4-триметилпентану (обычно называемому "изооктаном") произвольно приписывают значение октанового числа, равное 100, и все другие бензиновые компоненты смешения сравнивают с этим стандартом.
Алкилаты получают путем реакции алкена с изоалканом, катализируемой кислотой. Поток алкилатного продукта содержит смесь сильноразветвленных углеводородных соединений с увеличенным углеродным числом. Сильноразветвленные углеводородные соединения, например, триметилпентаны, весьма ценятся в качестве компонентов бензиновых смесей для увеличения "октанового" числа бензина или же модифицирования других свойств бензинового топлива. Во время 1930-х годов летательные аппараты с улучшенными летными данными требовали производства авиационных топлив с улучшенными качествами, одним из важнейших свойств которых было повышенное октановое число. Сильноразветвленные углеводородные соединения с высоким "октановым" числом, например, 2,2,4-триметилпентан, обычно известный как "изооктан", которому приписано октановое число, равное 100, не содержатся по природе в достаточно богатом количестве в сыром масле, для того чтобы их можно было получить в количествах, необходимых для смешивания с бензином, соответствующих количественным потребностям в высокооктановом авиационном топливе.
Это вызвало во время этого раннего периода интенсивное изучение способов получения сильноразветвленных алканов в температурных пределах кипения бензиновой фракции, имеющей высокооктановые свойства, путем взаимодействия низших олефинов с низшими изоалканами. В 1930 - 1940-е годы это имело небольшое экономическое значение для этилена или низших изоалканов, например, изобутана, которое затем послужило побудительным мотивом для попытки превращения их в высокоценные углеводородные продукты, например, высокооктановые соединения смешения для бензиновых топлив.
Один из способов получения углеводородов с высоким значением октанового числа, который был разработан во время этого периода, включал подверждение этилена и изобутана составу кислотной пары, содержащему кислоту Льюиса типа галогенид металла и протонную кислоту Бренстеда, наиболее обычно кислотой Льюиса является AlCl3, а протонной кислотой Бренстеда - HCl. При таких условиях этилен и изобутан взаимодействуют в присутствии состава кислотной пары с образованием многоразветвленных углеводородных соединений C6-C8 и с более высоким углеродным числом, известных как "алкилатный" продукт (патент США 3873635 кл. C 07 C 3156, 1975).
В литературе периода 1930 - 1960-х годов существует много сообщений об "алкилировании" катализатором типа кислота Льюиса - кислота Бренстеда. Смотри, например, R.C. Alden et al., Diisopopyl, The Oil and Gas Journal, cc. 70-73, 103-107 (Feb. 1946); Clark Hollaway et al., "Pilot Plant Production of 2-3 Dimethylbutane", Industrial and Engineering Chemistry, т.38, N 12, cc. 1231-1238 (декабрь 1946); R.R. Thompson et al., "Production of 2;3-Dimethylbutane by Alkylation", т.40. N 7, cc.1265-1269 (июль 1948), R.S. Manne, патент США N 2674637 (1954), и L.F. Mayhue, патент США N 3470264 (1969); и G.F. Prescott et al., патент США N 38736 (1975). Типичным во всех этих способах было то, что состав катализатора на основе кислотной пары, комплекса хлорид алюминия - углеводород, образованный в виде "красного масла" или пульпы, не смешивался с этилен-изоалкан-алкилатной углеводородной жидкой фазой. Типично объемное отношение углеводородного сырья к объему катализатора в виде красного масла составляет от 1:1 до 1:3, при этом реакцию осуществляют в условиях сильного перемешивания. Кроме того, активность состава катализатора на основе кислотной пары нарушается с течением времени и когда содержание красного масла или кислотной пульпы увеличивалось. Это привело к необходимости непрерывной подачи свежеприготовленного состава катализатора в реакционную зону при удалении затем отработанной каталитической пульпы.
Со временем произошли определенные события, которые позволили вытеснить способ производства алкилата с использованием кислотной пары из коммерческого применения. Были изобретены неалкилатные октановые усилители, - например, тетраэтилсвинец "свинцового" бензина, - а также были изобретены другие способы производства алкилатных потоков, например, посредством алкилирования HF и/или H2SO4. Кроме того, когда полимерная промышленность начала развиваться, потребность в полиэтилене значительно увеличилась и этилен стал высокозначимым продуктом как мономер, стало нежелательным с экономической точки зрения использовать этилен для производства алкилата.
Еще недавно с открытием опасностей для здоровья, связанных со свинцом, тетраэтилсвинец получил дурную славу как усилитель октана и производство "свинцовых" бензинов было запрещено. Это привело к использованию ароматических углеводородов в качестве бензиновых добавок, усиливающих октан, - например, комбинации бензол-толуол-ксилол - для производства бензина, не содержащего свинец, пользующегося большим спросом.
Коммерческие установки, на которых осуществляют алкилирование в настоящее время, можно разделить на две категории, такие, в которых используют серную кислоту в качестве катализатора, и другие, в которых в качестве катализатора для реакции алкилирования используют фтороводород (HF).
Хотя способ, в котором используют серную кислоту, является способом более раннего периода из этих двух способов, в последние годы в значительной мере возросла относительная важность способа, в котором используют фтороводород, таким образом HF-установки теперь производят около 47% всего алкилата. Было подсчитано, что к концу 1990 г. около 11% всего бензинового фонда состоит из алкилатов, полученных алкилированием изобутана C3-C5-олефинами.
Кроме того, производительность алкилирования в США равняется приблизительно 960.000 в/d алкилата.
Способы алкилирования как HF, так и серной кислотой, требуют протекания одинаковой суммарной реакции:
(1) CH3-CH=CHCH3+H+ (от кислоты) ---> CH3CH2CHCH3 [C4H9 (+)]
(2) C4H9 (+) + (CH3)3CH ---> C4H10 + (CH3)3C(+)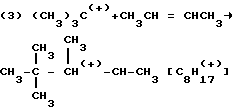
(4) C8H17 (+) + (CH3)3CH ---> (CH3)3C(+) + 2,2,3-триметиллентан (и другие).
Таким образом, требуемый изобутиловый катион взаимодействует с олефином (здесь 2-бутен) с образованием разветвленного C8-катиона, который в свою очередь взаимодействует с другой изобутановой молекулой с образованием нейтрального C8-углеводорода (2,2-триметилпентана) при регенерировании другого изобутилового катиона. Однако также происходят одновременно протекающие побочные реакции, наиболее нежелательные из которых дают полимеризованные олефины ("связанные полимеры" (сополимеры) или "смолы"), которые более растворимы в кислотной фазе, чем в изобутановой фазе. Кислотный катализатор не смешивается с углеводородной фазой (изобутан)-2-бутен-(алкилатный углеводород) и реакцию осуществляют при сильном перемешивании. Нежелательная реакция полимеризации происходит в кислотной фазе. В противоположность, желательная реакция алкилирования в основном происходит на поверхности раздела кислота/масло. Чтобы свести к минимуму образование этих полимеров или смол и довести до максимума выход алкилата, регулируют несколько действующих переменных величин: сводят до минимального в реакторе отношение кислоты к маслу, поверхность раздела кислота/масло увеличивают посредством высокой турбулентности; олефин разбавляют посредством высокого отношения изобутана к олефину, а температуру в реакторе поддерживают настолько низкой, насколько это возможно.
Во время алкилирования изобутана C3-C5-олефинами расходуется часть кислотного катализатора. Например, при алкилировании, катализируемом серной кислотой, для получения около 1 галлона алкилата обычно необходимо около 0,4-0,6 фунтов серной кислоты, но при предпочтительных условиях можно реализовать гораздо более низкий расход, например, 0,1-0,25 фунта на галлон (ppg). Стоимость расходов на кислоту обычно составляет одну третью часть от общих расходов по эксплуатации установок алкилирования, катализируемых серной кислотой.
При алкилировании, катализируемом фтороводородом, расход HF часто находится в диапазоне 0,08-0,25 ppg, а регенерация используемого HF осуществляется легко и является дешевой. Кроме того, так как большую часть HF извлекают и рециркулируют, количество требуемого свежеприготовленного HF незначительно и составляет обычно около 0,15-0,2 фунтов/барель алкилата. Однако связанные полимеры (сополимеры), полученные при алкилировании HF, могут содержать некоторое остаточное количество HF, и, следовательно, возникает проблема приемлемого в отношении окружающей среды устранения.
Таким образом, явствует, что ароматические углеводородные октановые усилители создают опасность для здоровья, поскольку возможно являются канцерогенами, а также содействуют образованию озона. Удаление фазы ароматических соединений в виде октановых усилителей значительно увеличивает потребность в высокооктановых алкилатах, при этом способ их производства, существующий на сегодняшний день, вызывает другие заботы.
За исключением проблемы безопасного удаления связанных полимеров, полученных в установках HF алкилирования, существует усиливающееся беспокойство о сохранности установок алкилирования, в которых используют HF. Когда HF выделяется в атмосферу, он образует аэрозоль, который возникает на уровне земли и затем переносится ветром. В случае выделения HF в воздух концентрация в диапазоне 2-10 ppm (част. на миллион) вызывает раздражение глаз, кожи и носовых ходов. Концентрации около 20 ppm приводят к прямой угрозе для жизни и здоровья. В результате опасности, возникшей в результате неумышленного выделения HF из установок алкилирования с использованием HF, существует необходимость создания других технологий производства алкилата, которые не имеют этих сопутствующих рисков.
В A. K. Roebuch et al. , "Icobutane-Olefin Alkylation with Inhibited Aluminum Chloride Catalyst", Ind. Eng. Chem. Prod. Res. Develop, т. 9, N 1 (март 1970) катализатор типа хлорид алюминия рассмотрен с другой точки зрения, согласно которой следует больше растворять изобутана, свести к минимуму производство тяжелых конечных продуктов по сравнению с методиками алкилирования с помощью HF или H3SO4, при сведении также к минимуму неподходящего побочного продукта, который является обычным при использовании катализатора, основанного на AlCl3. Описан катализатор на основе комплекса хлорид алюминия - эфир, который вместе с другими ингибиторами дает возможность получить желательные результаты при определенных условиях.
К тому же, что является типичным при использовании катализатора типа хлорид алюминия, каталитическая фаза не смешивается с углеводородной фазой, и реакционная среда является негомогенной эмульсией, полученной при сильном перемешивании.
Существует потребность в высокооктановом бензиновом компоненте смешения, который является неопасным для здоровья или окружающей среды для замещения ароматических компонентов в бензиновом резерве. Хотя эта потребность может быть удовлетворена посредством алкилатных компонентов смешения, кроме того, существует потребность в способе алкилирования, который не имеет осознанного риска для здоровья и жизни человека, связанного с использованием способа алкилирования, в котором применяют HF, с проблемой удаления смолы, возникающей в способе алкилирования с помощью как серной кислоты, так и HF, и с проблемами красного масла, связанными с применением катализатора типа AlCl3.
Кроме того, желательно разработать способ алкилирования, при котором в реакторах используют меньшее количество катализатора, и внести его в изобретение.
Изобретение обеспечивает образование гомогенной реакционной среды, содержащей растворенный катализатор, и способ изомеризации алканов и α-олефинов и алкилирования алканов олефинами в гомогенной реакционной среде. Желательно, чтобы алканы и α-олефины, подлежащие изомеризации, имели от 4 до 12 углеродных атомов.
Способ, в котором используют эту гомогенную среду, осуществляют в условиях текучей среды, при которых катализатор растворяют в текучей среде, содержащей углеводород парафинового ряда. В результате создания гомогенной фазы реакции алкилирования протекают быстро при температурах, по крайней мере, около 24oC с высокой селективностью и при высокой степени превращения в присутствии каталитического комплекса на основе кислоты Льюиса, который находится в среде в растворе в количествах, которые обеспечивают концентрацию кислоты Льюиса от 3•10-3 до ~ 20•10-3 ммоль растворенной кислоты Льюиса на г среды. По отношению к предпочтительной кислоте Льюиса, хлориду алюминия, каталитический комплекс находится в растворе в количествах от 80 до 550 мас. частей на миллион (wppm). В способе сведено к минимуму производство связанных полимеров (сополимеров) и нежелательных или токсических отходов производства, которые ставят проблемы, связанные с их безопасным удалением относительно окружающей среды. Кроме того, в способе этого изобретения обычно не используют фтористоводородную кислоту таким образом и в таком количестве, в котором ее используют во фтористоводородных способах алкилирования, посредством чего устраняется потенциальный риск для здоровья людей путем устранения риска образования аэрозоля фтористоводородной кислоты в случае непреднамеренных частичных потерь содержимого реактора.
Каталитический состав содержит кислоту Льюиса типа галогенид металла и протонную кислоту Бренстеда в качестве неотъемлемой части комплексного катализатора на основе кислоты Льюиса/углеводорода. Желательно, чтобы протонная кислота имела анион, соответствующий анионному компоненту кислоты Льюиса. Комплексный каталитический состав на основе кислоты Льюиса-углеводорода может также содержать катион переходного металла, полученный из металла, выбранного из групп 1b, 6b, 7b Периодической таблицы элементов, который способен подвергаться окислительно-восстановительным реакциям. Кислотная пара связана с, по крайней мере, одной углеводородной "цепью" или "лигандом", который является гидрокарбильным радикалом, имеющим формулу CnH2n+1, где n составляет не более 12, или который является простым эфиром. Наиболее предпочтительной кислотой Льюиса для образования катализатора является ди- или трихлорид алюминия.
Изобретение включает образование гомогенной реакционной среды, содержащей комплексный катализатор на основе кислоты Льюиса/углеводорода, растворенный в жидкости, содержащей углеводород парафинового ряда, и применения гомогенной реакционной среды, содержащей растворенный катализатор, для катализирования взаимодействия изоалканов с олефинами при гомогенном состоянии текучей среды для получения потока алкилатного продукта. Гомогенную реакционную среду, содержащую растворенный катализатор, можно получить в виде жидкофазного раствора или сверхкритического текучего раствора и использовать в таком текучем состоянии для катализирования желательной реакции алкилирования в гомогенной жидкой фазе или при сверхкритическом состоянии текучей фазы. Для проведения процесса в сверхкритическом режиме текучей фазы желательную реакцию можно осуществить и предпочтительно осуществляют при непрерывном поршневом движении потока в реакционном сосуде, предназначенном для сведения к минимуму турбулентности в реакционной среде.
При завершении желательной реакции можно легко осуществить отделение катализатора от углеводородного содержимого текучей среды. Если реакцию проводят при сверхкритическом состоянии текучей среды, отделение катализатора осаждением легко выполняется путем незначительного увеличения температуры или снижения давления реакционной среды; тогда как, если реакцию осуществляют в жидкофазных условиях, углеводородное содержимое среды можно отделить от катализатора однократным равновесным испарением или альтернативно путем подвержения жидкой среды абсорбенту катализатора. Извлеченный катализатор можно рециркулировать для повторного использования с исходными материалами свежеприготовленного состава реагентов для образования свежих загрузок гомогенной реакционной среды для дальнейшей реакции.
Состав катализатора содержит углеводородный растворимый комплекс, который образуется при взаимодействии кислоты Льюиса типа галогенид металла и протонной кислоты Бренстеда с парафином, олефином или эфиром углеводорода.
Природа углеводорода для гомогенной реакционной среды будет зависеть от типа желательной реакции, которую осуществляют внутри среды. Там, где осуществляют алкилирование, изоалкановый реагент можно использовать в качестве текучего компонента среды. Там, где реакцию проводят при сверхкритическом состоянии текучей среды, помимо углеводородного реагента для достижения жидкой смесью критической температуры, которая ниже таковой только одного алканового реагента, может быть использован растворитель. "Растворитель", который может быть использован в качестве компонента в сверхкритической жидкой смеси, может быть любым известным полярным или неполярным, инертным растворителем, имеющим критическую температуру между около -110oC и 400oF (-79 до 204oC). Эти растворители включают метан, этан, пропан, двуокись серы, двуокись углерода, окислы азота (например, N2O3, NO, NO2), низкомолекулярные фторированные углеводороды, или галоидзамещенные углеводороды, редкие металлы в виде газа (аргон или ксенон) и т.п.
Получение гомогенной реакционной среды, содержащей растворенный катализатор, можно осуществить множеством способов. Текучий компонент среды можно привести в контакт с источником твердой кислоты Льюиса одновременно с контактированием его с кислотой Бренстеда, затем текучую среду устраняют от дальнейшего контакта с твердой кислотой Льюиса и получают гомогенный текучий раствор из 2-х компонентов. Более предпочтительно текучий компонент среды приводят в контакт, а затем устраняют от контакта с твердой кислотой Льюиса перед тем, как к жидкости добавляют кислоту Бренстеда. Альтернативно растворимый катализатор можно получить путем взаимодействия кислоты Льюиса с алкилгалогенидом, который при реакции алкилирования разлагается на алкен и галоидоводородную кислоту.
Фиг. 1 представляет упрощенную схему технологического процесса варианта изобретения, иллюстрирующую способ алкилирования изобретения, который осуществляют при сверхкритическом состоянии текучей фазы.
Фиг. 2 представляет схематическое изображение варианта реактора, пригодного в способе изобретения.
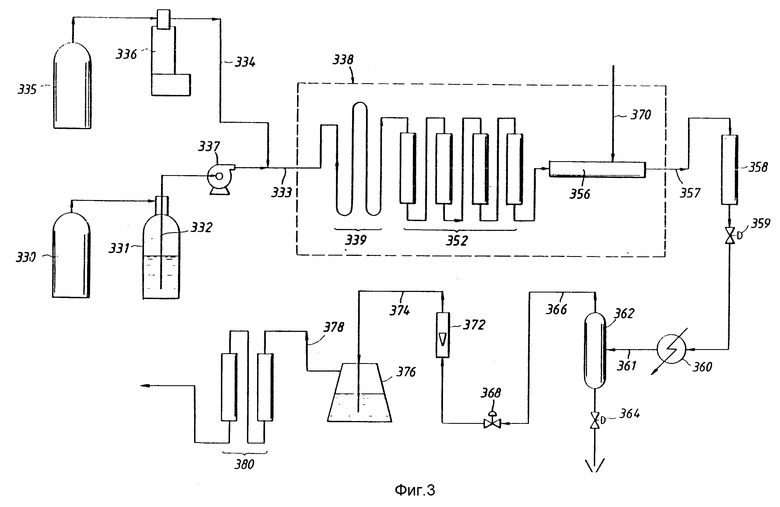
Фиг. 3 показывает схему аппаратуры, используемую в нескольких примерах.
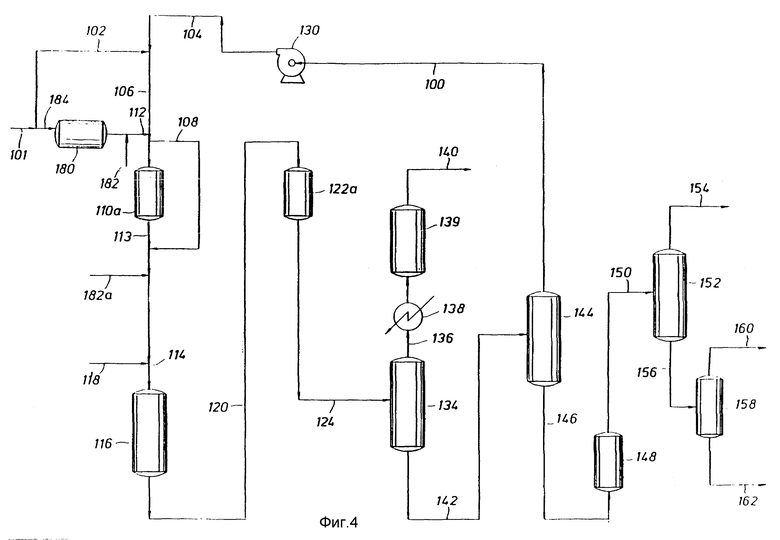
Фиг. 4 показывает схему технологического процесса варианта изобретения, в которой способ осуществляют в жидкофазных условиях.
Изобретение обеспечивает катализатор, способ получения этого катализатора и способы применения катализатора в реакции алкилирования, проводимой в гомогенной реакционной среде. Способ алкилирования соединяет изоалканы, имеющие от 4 до 12 углеродных атомов с олефинами, имеющим от 2 до 9 углеродных атомов.
Наиболее предпочтительным α-олефином является 1-бутен. Поскольку 1,2 и 1,3-бутадиены составляют каталитические яды в коммерческих процессах алкилирования, способ этого изобретения можно подвергнуть их алкилированию изопарафином.
Алкан в способе этого изобретения выполняет множество функций. Он является реагентом, который претерпевает желательную реакцию алкилирования в присутствии растворенного комплексного катализатора на основе кислоты Льюиса-углеводорода. Однако часть алкана также служит в качестве реагента при образовании растворенного каталитического комплекса, который катализирует желательную реакцию алкилирования. Кроме того, алкан также служит в качестве компонента текучей среды, в которой растворим каталитический комплекс. Таким образом, алкан образует часть гомогенной текучей среды, в которой осуществляют реакцию, посредством которой углеводородный реагент реагирует для получения углеводородного продукта различной молекулярной структуры.
Текучая среда реакционной среды.
В соответствии с этим изобретением желательную реакцию алкилирования осуществляют в гомогенной текучей среде. Текучей средой реакционной среды может быть жидкий углеводород или сверхкристаллическая текучая среда, содержащая парафин.
Жидкофазные текучие среды.
Когда для практики этого способа выбирают жидкофазные реакционные условия, текучей средой для реакционной среды предпочтительно является ожиженный углеводород, который также является реагирующим углеводородом в способе.
Для реакции алкилирования текучую среду реакционной среды предпочтительно выбирают из изоалкана, который является реагентом для олефинового реагента процесса алкилирования. Опять же в этом случае изоалкан выполняет функцию текучей среды для образования гомогенной реакционной среды и также служит в качестве углеводородного реагента в этой среде. В предпочтительном варианте реакции жидкофазного алкилирования в соответствии с изобретением текучей средой реакционной среды является изобутан.
В случае жидкофазной реакции углеводород, выбранный в качестве текучей среды для реакционной среды, следует поддерживать при температуре ниже его критической температуры и при давлении, достаточном для поддержания углеводорода в жидком состоянии при образовании комплексного катализатора на основе кислоты Льюиса-углеводорода и во время проведения выбранной реакции алкилирования.
Для реакции алкилирования в качестве текучей среды для гомогенной реакционной среды выбирают изоалкан, который участвует в реакции. Во время реакции алкилирования изоалкан обычно присутствует в среде в молярном отношении к олефиновому реагенту, составляющему, по крайней мере, 5:1 и выше. Соответственно для жидкофазной реакции температура изоалкановой текучей среды не должна превосходить критическую температуру выбранного изоалкана.
Для алкилирования предпочтительным является изобутан, а температура текучей среды не должна превосходить 275oF (135oC).
При алкилировании гомогенную реакционную среду следует сохранять при температуре, по крайней мере, около 24oC, тогда как для изомеризации предпочтительной является температура, по крайней мере, около 93oC. Для жидкофазного алкилирования, когда катализатор содержит хлорид алюминия, температуру текучей среды следует поддерживать при 24 - 105oC, более предпочтительно 44 - 83oC и наиболее предпочтительно 49 - 71oC.
Сверхкритические текучие среды.
В качестве альтернативного варианта гомогенная реакционная среда может быть образована в виде сверхкритической текучей среды. Сверхкритическая текучая среда не является жидкостью и не проявляет свойства газа; вместо этого она проявляет свойства растворимости, более возможные для жидкости, чем для газа, и молекулярные диффузионные свойства, более характерные для газа, чем для жидкости; следовательно, ее можно отнести в данной области к "сверхкритической текучей среде".
Для целей этого изобретения сверхкритическая текучая среда может состоять из компонентов, которые при обычных условиях температуры и давления будут обычными жидкими компонентами или смесью обычных жидких и обычных газообразных компонентов.
В первом случае, в котором компонентом сверхкритической текучей среды является обычный жидкий компонент, этот компонент поднимают до температуры выше его критической температуры и сохраняют под давлением, достаточным для создания текучей фазы плотностью, составляющей по крайней мере, 0,1 от плотности чистого компонента, насыщенного в жидком состоянии при 20oC. Во втором случае компоненты являются смесью обычной жидкости и обычного газа, при этом функции газового компонента как "растворителя" жидкости такие, что смесь имеет более низкую критическую температуру, чем температура одного жидкого компонента. Как следствие, жидкостно-газовая смесь может быть преобразована в сверхкритическую текучую среду при более низких температурах, чем та температура, при которой может быть преобразован только жидкий компонент.
"Растворитель" или "со-растворитель", который может стать компонентом в сверхкритической жидкой смеси, может быть любым известным полярным или неполярным, инертным растворителем, имеющим критическую температуру между -79 и 204oC. Эти растворители включают метан, этан, пропан, двуокись серы, двуокись углерода, окислы азота (например, N2O3, NO, NO2), низкомолекулярные фторированные углеводороды или галоидзамещенные углеводороды, редкие металлы в виде газа (аргон или ксенон) и т.п.
Термин "инертный" означает, что растворитель химически активно не вмешивается в образование катализатора, реакции алкилирования для получения отдельного продукта. Предпочтительные растворители включают этан и пропан, а наиболее предпочтительным растворителем является этан.
В контексте этого изобретения растворитель первоначально служит в качестве компонента сверхкритической смеси, который обеспечивает смесь свойствами давления и температуры, наиболее предпочтительными для реакции в сверхкритическом состоянии. Это сверхкритическое состояние допускает как образование, так и растворение комплексного катализатора на основе кислоты Льюиса-углеводорода.
"Сверхкритические условия" относятся к условиям, когда температуры находятся выше критической температуры смеси растворитель - углеводород, а давление является достаточным для придания смеси плотности, которая составляет по крайней мере, 0,1 от плотности чистого растворителя, когда он насыщен в жидком состоянии при 20oC. Предпочтительно плотность смеси составляет более 0,25 от плотности чистого растворителя, насыщенного в жидком состоянии при 20oC. В общем сверхкритическое абсолютное давление будет находиться в интервале от 600 до ~ 5000 фунтов/дюйм2, предпочтительно от 700 до 2500 фунтов/дюйм2.
Выбор вида текучей среды.
Выбор текучей среды в качестве жидкой фазы или в качестве сверхкритической текущей среды приводит к различным текущим затратам.
Обычно в сверхкритической текучей среде реакция алкилирования протекает с более высокой скоростью, чем в жидкофазных текучих средах. После реакции каталитический комплекс можно легко отделить от углеводородных компонентов сверхкритической текучей среды путем изменения плотности сверхкритической текучей среды. Уменьшение плотности приводит к осаждению катализатора из раствора. Плотность может быть уменьшена или путем увеличения температуры, или путем снижения давления сверхкритической текущей среды, или путем сочетания того и другого. Это приводит к необходимости повторного нагрева и/или повторного сжатия непрореагировавшего избытка алкана и растворителя, используемого для рециркулирования, затраты на которые могут привести к предпочтению методики жидкофазной реакции. При жидкофазной методике реакционная среда может быть допущена подвержению однократному испарению для отделения углеводородных компонентов от каталитического комплекса. Опять же непрореагировавший избыток алкана следует извлечь и подвергнуть сжатию - но до меньшей степени, чем это необходимо для сверхкритического процесса - при уменьшенной стоимости повторного сжатия. Альтернативно жидкую среду, содержащую непрореагировавший алкан, более тяжелый алкилатный продукт и катализатор можно распределить по слою абсорбента катализатора, чтобы отделить его от алкилатного продукта.
Катализатор.
Изобретение обеспечивает гомогенный катализатор для алкилирования олефинов и алканов. Катализатор содержит кислоту Льюиса типа галогенид металла, протонную кислоту Бренстеда и углеводородный компонент.
Комплексный катализатор на основе кислоты Льюиса - углеводорода является продуктом реакции, по крайней мере:
(a) кислоты Льюиса формулы R(m-2-z)MX2+z, в которой M представляет металл группы 3a, 5a или 5b, X является галогенидом, R - гидрокарбильный радикал, имеющий от 1 до 12 углеродных атомов, m - целое число, равное самой большой степени окисления M, a z - целое число, равное 0, 1 или m-2;
(b) галогенида водорода; и (с) органического соединения, выбранного из (1) парафинов, имеющих 12 или меньшее количество углеродных атомов, (2) олефинов, имеющих 12 или меньшее количество углеродных атомов, или (3) простых эфиров, имеющих 6 или меньшее количество углеродных атомов. Все ссылки приведены по отношению к Периодической таблице элементов, которая опубликована в CRC Handbook of Chemistry and Phisics, 51-ое издание (1970-1971), опубл. The Chemical Rubbeu Co. пригодные кислоты Льюиса включают, например, тригалогениды алюминия, дигалогениды алкилалюминия, оксихлориды алюминия, тригалогениды галлия, дигалогениды алкилгаллия, тригалогениды бора, пентагалогениды сурьмы, пентагалогениды тантала и пентагалогениды ниобия и т. п. Из них предпочтительными являются фториды сурьмы, тантала, ниобия и бора, при этом для алюминия и галлия предпочтительными являются хлориды. Наиболее предпочтительными в качестве компонента кислоты Льюиса для катализаторов являются хлориды алюминия, например, трихлорид алкилалюминия или дихлорид алкилалюминия, где алкильная группа имеет от 1 до 12 углеродных атомов. В особенности предпочтительными кислотами Льюиса являются трихлорид алюминия и дихлорид изобутилалюминия.
Кислоты Бренстеда включают протонные кислоты Бренстеда, которые имеют анион, соответствующий аниону используемой кислоты Льюиса. Таким образом, кислота Бренстеда может быть выбрана из фтороводорода, хлороводорода, бромоводорода и йодоводорода. Предпочтительными кислотами Бренстеда являются HCl и HBr.
Поскольку наиболее предпочтительной кислотой Льюиса является хлорид алюминия, наиболее предпочтительной кислотой Бренстеда является хлористоводородная кислота. Кислоту Бренстеда можно подать в виде донора кислоты Бренстеда, а именно соединения, которое при температурных условиях для реакции алкилирования разлагается до образования кислоты Бренстеда. Такими донорами кислоты Бренстеда являются алкилхлориды, подобные бутилхлориду, которые разлагаются на бутен и хлороводород.
Органическими соединениями, которые можно использовать при образовании катализатора, являются алканы и/или олефины, которые используют в качестве реагентов для реакции алкилирования алкана. При образовании катализатора органическим соединением может быть простой эфир, например, диметиловый, диэтиловый или метилэтиловый эфир, или их сочетания. В этом случае катализатор лучше всего получают путем добавления простого эфира к перемешиваемой суспензии трихлорида алюминия в углеводородном растворителе.
После взаимодействия трихлорида алюминия и простого эфира образованный комплекс хлорид алюминия - простой эфир можно затем растворить в текучей среде, содержащей углеводород, и к такой текучей среде для образования каталитического комплекса добавляют кислоту Бренстеда или донор кислоты Бренстеда.
Гомогенную среду, содержащую растворенный комплексный катализатор на основе кислоты Льюиса-углеводорода, можно образовать рядом способов. Текучую среду, содержащую углеводород, можно пропустить через слой твердой кислоты Льюиса, например, AlCl3, чтобы вызвать растворение кислоты Льюиса в текучей среде, затем предотвратить ее от дальнейшего контакта с твердой кислотой Льюиса. Впоследствии к текучей среде, содержащей растворенную кислоту Льюиса, можно добавить кислоту Бренстеда или донор кислоты Бренстеда.
Когда добавляют кислоту Бренстеда, катализатор образуется при добавлении кислоты Бренстеда. Когда добавляют донор кислоты Бренстеда, например, бутилхлорид, каталитический комплекс образуется, когда текучая среда достигает температуры, при которой алкилхлорид ионизируется в присутствии кислоты Льюиса.
Предпочтительно кислоту Льюиса растворить перед добавлением кислоты Бренстеда или донора кислоты Бренстеда. Предпочтительное соотношение кислоты Бренстеда или донора кислоты Бренстеда к галогенангидриду (кислоте) Льюиса находится между 0,5 и 2,5 на молярной основе. По желанию активность комплексного катализатора на основе кислоты Льюиса - углеводорода может быть модифицирована путем образования его в присутствии галогенида переходного металла, где переходный металл выбирают из групп 1b, 6b, 8b и 8 Периодической таблицы элементов, при этом он является металлом, который способен подвергаться окислительно-восстановительным реакциям. Примерами предпочтительных галогенидов переходного металла являются хлорид серебра, хлорид меди и хлорид железа, которые пригодны для изменения активности катализатора.
Когда используют в качестве модификатора галогенид переходного металла, предпочтительно добавить его к растворенной кислоте Льюиса в количестве, которое обеспечивает молярное отношение галогенида переходного металла к растворенной кислоте Льюиса от 0,5 до 1,0.
Комплексный катализатор на основе кислоты Льюиса включает продукт реакции по меньшей мере кислоты Льюиса формулы
R(m-1-z)MX(2+z),
где R является гидрокарбильным радикалом, имеющим от 1 до 12 углеродных атомов, М является металлом и/или металлом группы 3a, 5a или 5b, X является галогенидом, m - целое число, равное самой большой степени окисления М, z является 0, 1 или m-2. Соответственно при образовании этого катализатора кислоту Бренстеда (HX) следует добавить к растворенной кислоте Льюиса (Rm-2-zMX2+z) в количестве, которое обеспечивает молярное отношение кислоты Бренстеда к кислоте Льюиса от 1:2 до 5:2. Катализатор, который образуется в виде комплекса кислота Льюиса - простой эфир, может быть представлен следующей формулой:
R'2OM'X3 • sM'X3 • rHX,
где каждый R' является алкильным радикалом, содержащим от одного до 3-х углеродных атомов, и каждый радикал R' может быть одинаковым или различным, M' является трехвалентным металлом или металлоидом групп 3a, 5a или 5b, X является галогенидом, s и r - более 0,05 и менее 0,1.
Образование гомогенной реакционной среды.
Природа текучей фазы в виде жидкой фазы или в виде сверхкритической текучей среды требует различных способов образования гомогенной реакционной среды. Когда выбирают жидкофазный процесс, катализатор может быть образован большим разнообразием способов, чем когда выбирают процесс, в котором используют сверхкритическую текучую среду. Содержание катализатора в среде, выраженное в виде содержания кислоты Льюиса, может находиться в интервале 3 - 30 ммоль кислоты Льюиса/1000 г среды, предпочтительно 3,0 - 22,5 ммоль/1000 г среды и более предпочтительно 3,1 - 20,0 ммоль/1000 г среды.
Процесс с использованием сверхкритической текучей среды.
Кислоту Бренстеда можно выбрать из фтороводорода, хлороводорода, бромоводорода и йодоводорода. Предпочтительными кислотами Бренстеда являются HCl и HBr. Так как наиболее предпочтительной кислотой Льюиса является AlCl3, то наиболее предпочтительной кислотой Бренстеда является HCl. Кислота Бренстеда является неотъемлемой частью разновидностей дискретного катализатора, таким образом для получения разновидностей активного катализатора в пригодных количествах должна присутствовать, по крайней мере, часть ее. Дискретный катализатор желательно получать в такой концентрации, чтобы он оставался растворимым в алкане или сверхкритической текучей среде, растворяющей алкан. Таким образом, катализатор можно получить в интервале от 400 до 4000 ppm/част. на миллион/, предпочтительно от 1000 до 3000, наиболее предпочтительно около 2000 ppm. относительно массы текучей среды при пересчете на AlCl3.
Желательно, чтобы молярное отношение кислоты Бренстеда к кислоте Льюиса составляло от 0,5 до 2,5, предпочтительно от 0,9 до 1,5 и наиболее предпочтительно от 1,0 до 1,5.
Как объяснялось выше, пригодными алканами являются такие, которые содержат от 4 до 12 углеродных атомов, предпочтительно от 4 до 8 углеродных атомов и более предпочтительно от 4 до 6 углеродных атомов. Желательно, чтобы алкан в своем сверхкритическом текучем состоянии присутствовал в растворителе при молярном отношении алкана к растворителю от ~ 1:99 до ~ 50:50; предпочтительно от 10:90 до 40:60 и наиболее предпочтительно от 20:80 до 40: 60. Алканы можно также использовать без растворителя. Процесс сдерживается критической температурой и давлением алкана или изоалкана.
Для получения катализатора изобретения соединяют кислоту Льюиса, по желанию переходный металл, кислоту Бренстеда, растворитель и алкан при сверхкритических условиях и в вышеприведенном интервале концентраций в реакторе образования катализатора. Таким образом, катализатор может быть получен путем контактирования предпочтительной кислоты Льюиса, AlCl3, предпочтительного переходного металла (железа или меди), сверхкритической текучей среды, содержащей алкан, предпочтительно нормальный бутан, при соотношении от 20: 80 до 30:70 по отношению к растворителю, предпочтительно этану или пропану, наиболее предпочтительно пропану, и кислоты Бренстеда, предпочтительно HCl, при абсолютном давлении 1000 фунтов-дюйм2 и 200oF (93oC). Кислоту Бренстеда добавляют предпочтительно после того, как поток уже содержит кислоту Льюиса.
Если во время контактирования алкана с твердой кислотой Льюиса присутствует кислота Бренстеда, время контактирования с твердой кислотой Льюиса следует ограничить до времени, достаточного для получения дискретного каталитического состава.
Таким образом, желательно, чтобы в предпочтительном непрерывном способе образования катализатора смесь алкана и растворителя протекала по поверхности, которую представляет кислота Льюиса и переходный металл, к текучей сверхкритической жидкой смеси в реакторе образования катализатора. Затем скорость потока смеси регулируют таким образом, чтобы жидкость не находилась в контакте с кислотой Льюиса в течение времени более чем 10 минут, предпочтительно она должна находиться в контакте с кислотой в течение около 5 минут, и наиболее предпочтительно менее, чем около 3 минут. Оптимальный диапазон времени пребывания материала в реакторе будет зависеть от конкретных кислот Льюиса и Бренстеда, алкана и температуры, и давления. Затем добавляют кислоту Бренстеда.
Следует отметить, что пока сверхкритическая смесь алкана, кислоты Бренстеда и сорастворителя находится в контакте с твердой кислотой Льюиса типа галогенид металла, олигомеризация углеводородных цепей катализатора будет продолжаться. При выводе сверхкритической текучей среды из контакта с твердой кислотой Льюиса желаемый каталитический состав может быть получен в виде дискретного катализатора, который является активным и селективным для алкилирования алканов олефинами. "Дискретная форма" означает, что реакцию, генерирующую катализатор, проводят таким образом, чтобы подавить или устранить получение комплекса кислотная пара - углеводород нерегулируемой молекулярной массы в диапазоне полимерной или смолистой смеси. Полученный "дискретный" катализатор является катализатором с регулируемым диапазоном молекулярной массы и он растворим в сверхкритической среде, в которой его сначала производят или, если осаждают и извлекают, затем вновь растворяют в такой среде.
Жидкофазный процесс.
При жидкофазном процессе катализатор может быть подходяще получен путем растворения кислоты Льюиса в углеводородной жидкости и впоследствии, основываясь на содержании растворенной кислоты Льюиса, добавления к жидкости соответствующих количеств кислоты Бренстеда или донора кислоты Бренстеда.
Альтернативно кислоту или донор кислоты Бренстеда можно добавить в реактор алкилирования с углеводородной жидкостью, имеющей растворенную кислоту Льюиса, которую отдельно добавляют в реактор. Катализатор образуется в реакторе в гомогенной смеси.
Образованный каталитический комплекс растворяется в гомогенной текучей среде в количестве, которое обеспечивает концентрацию катализатора 3 - 20 ммоль на 1000 г среды в пересчете на MXm, где M представляет металл или металлоид группы 3a, 5a или 5b, X является галогенидом, а m - целое число, равное самой высокой степени окисления M. Гомогенную текучую среду поддерживают при температуре, достаточной для предотвращения осаждения из раствора
каталитического комплекса.
Катализатор изобретения может быть использован при алкилировании изомеризованных алканов олефинами.
Процесс алкилирования.
Процесс алкилирования можно осуществить с катализатором изобретения в том же самом реакторе. Реакция алкилирования является экзотермической. При выборе конструкции реактора теплоудаляющая способность является фактором. Может быть также желательным осуществить реакцию алкилирования при двух различных температурах.
Подходящая конструкция реактора алкилирования представляет пустой сосуд, имеющий приблизительно тот же самый или слегка больший диаметр, чем реактор изомеризации, с тем, чтобы при выгрузке продукта реактора изомеризации в реактор алкилирования происходил небольшой перепад давления. По одному варианту как реактор изомеризации, так и реактор алкилирования могут содержаться в одном трубопроводе. Реакция алкилирования осуществляется в двух отдельных реакторах.
Олефиновое сырье, когда олефин содержит от 3 до 9 углеродных атомов, загружают во множество точек вдоль длины реактора алкилирования. Дозирование олефина к подаваемому алкановому сырью должно быть в соотношении от 1:2 до 1:20 при загрузке в реактор алкилирования. Предпочтительно отношение олефина к алкану должно быть от 1:5 до 1:15, наиболее предпочтительно около 1:10.
При добавлении олефина происходит алкилирование и получается алкилат, который имеет низкое содержание связанного полимера (сополимера) или смолы относительно типичных алкилатов, получаемых от процессов со фтористоводородной кислотой или серной кислотой. Для того чтобы достигнуть этого, дискретный катализатор должен присутствовать при концентрации от 3 до около 30 ммоль кислоты Льюиса на 1000 г среды, предпочтительно 15 ммоль относительно массы изоалкана и растворителя. Кроме того, для того чтобы свести к минимуму галогенирование алкилата, следует свести к минимуму, насколько это возможно, избыток кислоты Бренстеда.
Время пребывания среды с добавленным олефином в реакторе алкилирования для достижения пригодной степени превращения в алкилат составит по крайней мере, около 1 минуты, предпочтительно, по крайней мере, около 2 минут.
Степень превращения олефина в алкилат является высокой и в зависимости от особенностей используемого катализатора и от особенностей изоалканов и олефинов, составляет 95-100% за одно прохождение. Таким образом для предпочтительного изобутана, реагирующего с олефинами, имеющими от 3 до 9 углеродных атомов, в присутствии катализатора, полученного из кислотной пары AlCl3/HCl и нормального бутана, растворителя этана, можно обеспечить степень превращения олефина до ~ 100% за одно прохождение.
Гомогенная реакционная среда образуется смесью изоалкана и растворителя, которую приводят в сверхкритическое состояние и делают так, чтобы она содержала растворенную кислоту Льюиса, к которой одновременно или последовательно добавляют кислоту Бренстеда или донор кислоты Бренстеда. Затем эту реакционную среду подают в реактор алкилирования, к которой добавляют олефин в таком количестве, чтобы получить молярное отношение изоалкана к олефину от ~ 1 до ~ 10. Контактирование олефина с гомогенной средой предпочтительно осуществляют через неподвижную поверхность раздела. Олефин поступает в гомогенную среду посредством молекулярной диффузии, и алкилирование происходит внутри среды. Одновременно протекающие реакции, которые будут давать нежелательный полимер, и смолистый побочный продукт, которые будут происходить в олефиновой фазе, сводят к минимуму или устраняют, так как олефиновая фаза не содержит ощутимого содержания катализатора, поскольку он остается растворенным в гомогенной реакционной среде. Очень высокое отношение изоалкана к олефину, существующее в гомогенной смеси по причине молекулярной диффузии олефина в гомогенную среду, ускоряет алкилирование и, кроме того, сводит к минимуму получение нежелательных побочных продуктов.
Процесс с использованием сверхкритической текучей среды.
Каталитическая система изобретения может быть использована в любой из широкого многообразия схем потока процесса для того, чтобы получить алкилатный продукт. Для иллюстрации разнообразия потоков процесса на фиг. 1 представлена упрощенная схема потока. На этой схеме потока свежий алкан 102 смешивают со сжатой загрузкой (загрузкой, находящейся под давлением) 104, включающей рециркулированный бутан, сжатый рециркулированный поток растворителя 128 и поток свежеприготовленного растворителя 103, для получения сырья, растворяющего катализатор 106, которое загружают в чан для растворения катализатора 110, который поддерживают при сверхкритических условиях. Через трубопровод 112 в чан для растворения 110 загружают также регулируемое количество свежеприготовленного катализатора.
Свежеприготовленный катализатор получают в реакторе "образования катализатора" или получения "свежеприготовленного катализатора" 180, в котором обеспечивается контактирование между потоком алкана растворителя 184 (показан в виде исчезающего потока, взятого из всей свежей загрузки алкана 101) с твердой кислотой Льюиса и, по желанию, с модификатором-галогенидом переходного металла.
К потоку 112 выпускного реактора 180 добавляют через линию 182 загрузку кислоты Бренстеда. На стадии контактирования получают катализатор изобретения, который растворим в растворителе при сверхкритических условиях. Кроме того, реактор 180 является проточным реактором непрерывного действия, в котором реагенты и продукты протекают через реактор при минимальном перепаде давления и который сконструирован так, чтобы время пребывания в нем составило менее 5 минут, предпочтительно менее 3 минут. В пределах этих ограничений реактор может иметь множество конструкций. По одному из предпочтительных вариантов конструкций реактор может быть сконструирован подобно обычным, при этом кожухотрубный переходный аппарат и трубчатый теплообменник с кислотой Льюиса и переходным металлом упакованы внутри труб таким образом, что перепад давления через трубы был бы минимальным, с тем, чтобы сверхкритические условия можно было поддерживать по всей длине трубы. Таким образом реагенты будут перетекать в трубную зону реактора, протекая вдоль труб для обеспечения реакции с кислотой Льюиса и переходным металлом. Непрореагировавший алкан, растворитель и катализатор перетекают от выходного конца труб в коллектор, где добавляют кислоту Бренстеда, и из него в чан для растворения 110. На внетрубную зону реактора образования катализатора 180 можно подать жидкий теплоноситель для поддержания температуры в пределах желательного рабочего диапазона, так как реакция образования катализатора является экзотермической.
Свежеприготовленный катализатор, обеспеченный через трубопровод 112 из реактора образования катализатора 180, является достаточным для возмещения потерь в процессе, и реактор образования катализатора может работать по необходимости непрерывно или только прерывисто.
Чан для растворения катализатора 110 содержит дискретный катализатор, который ранее был извлечен в виде осадка. Этот катализатор растворяют в загрузке, растворяющей сверхкритическую текучую среду, которая содержит текучие среды на линиях 106 и 112, до желательной концентрации дискретного катализатора относительно алкана и растворителя. Это может быть легко достигнуто путем перепускания части загрузки через линию 108 около чана для растворения 110. Поток, вытекающий из чана для растворения 110, содержащий теперь пригодное количество растворенного дискретного катализатора, перетекает через трубопровод 113 в реактор алкилирования 116. В технологической линии имеется также реактор 115, который используется в случае проведения дополнительной реакции изомеризации и предназначен для облегчения отвода тепла, так как реакция является экзотермической и, кроме того, для сведения к минимуму перепада давления, чтобы сохранить сверхкритические условия текучей среды. В пределах этих ограничений может быть много конструкций. Самой простой конструкцией является трубопровод, образующий реактор с поршневым потоком, окруженный средствами переноса тепла из трубопровода.
Таким образом, может быть использована конструкция кожуха и трубы, в которой реакция происходит на трубной зоне и тепло отводят посредством охлажденной среды во внетрубную зону. Время пребывания в реакторе должно быть достаточным для обеспечения значительной степени превращения алканов в изоалканы. Катализатор изобретения обеспечивает степень превращения, приближающуюся к термодинамическому равновесному превращению.
Реактор алкилирования 116 сконструирован на минимальный перепад давления и обеспечивает достаточное время пребывания для осуществления реакции алкилирования до желательной степени реакции изоалкана. При этих ограничениях реактор алкилирования может иметь любые виды конструкций. Одним из примеров такой конструкции является простой реактор с поршневым потоком, который имеет соответствующий объем для обеспечения желаемого времени пребывания и который имеет средства для отвода тепла реакции. Поступление сырья следует производить путем добавления олефина в несколько точек, предпочтительно 3-5, вдоль длины реактора. Таким образом, реактор может содержать трубопровод, рассчитанный на обеспечение соответствующего времени пребывания при задуманных скоростях потока.
Поток, вытекающий из реактора алкилирования 116, увлекается трубопроводом 120 во входное отверстие "осадителя" катализатора 122. Желательно, чтобы этот сосуд имел ту же самую конфигурацию, какую имеет растворитель (чан для растворения) катализатора 110. Таким образом, загрузку в осадитель пропускают через трубы при снижении давления ниже сверхкритических условий. При этих условиях катализатор осаждается в осадителе 122.
Таким образом, катализатор, содержащийся в "растворителе" 110, постепенно переносится в "осадитель" 122. Когда катализатор в значительной степени извлечен из растворителя 110, поток через систему процесса может быть переключен посредством соответствующей системы трубопроводов, клапана переключения и регулятора с тем, чтобы сосуд 122 стал "растворителем", в то время как сосуд 110 стал "осадителем".
Поток, вытекающий из осадителя 122, который по существу не содержит катализатор, при давлении ниже критического загружают в колонну вторичной перегонки растворителя 126. В колонне вторичной перегонки 126 растворитель, например, этан, и остаточную кислоту Бренстеда отделяют от непрореагировавшего олефинового и алканового сырья и алкилатного продукта. Растворитель удаляют в виде продукта, отбираемого сверху колонны на линии 128, и загружают во входное отверстие насоса 130 для рециркулирования через линию 104 на вход растворителя 110. Остаточный продукт колонны вторичной перегонки 126, содержащий алкилат, непрореагировавшие алканы или олефины и незначительное количество остаточной кислоты Бренстеда, загружают через линию 132 в этанизатор 134. Дистилляционная колонна (этанизатор) 134 отделяет легкие фракции от алкилата и непрореагировавших алканов и олефинов. Пропан-пропеновый поток удаляют через линию 136 в верхние погоны депропанизатора, охлаждают и конденсируют в холодильнике-конденсаторе 138 и затем он перетекает в щелочной скруббер 139 для удаления остаточных следовых количеств кислоты. Поток, вытекающий через линию 140 из щелочного скруббера, не содержащий теперь остаточной кислоты, может быть использован в других химических процессах или в качестве источника топлива. Остаточный продукт 142 депропанизатора 134 загружают в дебутанизатор 144, который удаляет бутан в виде продукта, отбираемого сверху колонны на линии 100, для загрузки во всасывающий насос, откуда его рециркулируют на лицевую сторону реактора изомеризации 110. Остаточный продукт 146 дебутанизатора 144 обрабатывают в скруббере 148 для удаления остаточной кислоты Бренстеда или алкилхлоридов. Поток, вытекающий из щелочного скруббера 148, по существу не содержащий кислоты, загружают по линии 150 в алкилатный делитель 152. Алкилатный делитель делит алкилатный поток на легкий алкилатный продукт, отбираемый сверху колонны 154, и тяжелый алкилатный остаточный продукт 156. Затем тяжелый алкилатный продукт 156 необязательно загружают в алкилатный испарительный барабан 158 для разделения на тяжелый алкилат, отбираемый сверху колонны 160, и тяжелый колонный остаточный продукт 162.
Легкий алкилатный поток 154 и тяжелый алкилатный продукт 160 легко вмешивают в бензин, обеспечивая высокооктановый компонент смешения, который может быть замещен ароматическими компонентами.
Хотя упрощенная схема технологического процесса (фиг. 1) показывает основную схему потока, специалисты в данной области без труда поймут, что на практике может быть необходимым дополнительное оборудование и модификации.
Как объяснялось выше, катализатор изобретения и способ можно осуществить в одной любой из множества конструкций реактора. Конструкция реактора ограничивается по существу только теми функциями, которые необходимо выполнить. Например, реактор должен быть способен выдерживать сверхкритические реакционные условия. Кроме того, реактор должен быть такой конструкции, которая свела бы к минимуму перепад давления с тем, чтобы сохранить сверхкритическую текучую среду, содержащую активный катализатор, выше критического давления во избежание осаждения катализатора. Кроме того, желательно, чтобы конструкция была такого типа, который дает возможность легкого удаления тепла реакции. Следовательно предпочтительным является кожухотрубный вариант.
Фиг. 2 схематически изображает реактор конструкции типа кожух и труба (кожухотрубный реактор). Реактор 200 имеет цилиндрический кожух 202 с фланцами 204 на каждом конце. Кроме того, кожух снабжен входным отверстием 206 и выходным отверстием 208 для обеспечения возможности жидкому теплоносителю перемещаться через кожух реактора 200. Таким образом, пространство внутри кожуха, окружающего трубы, обеспечивает средства для теплообмена труб. Впускная крышка 210 снабжена входным отверстием 212 для принятия загрузки реагентов, а фланец 214 прикреплен болтами к фланцу 204. Подобно, выходная крышка 216 прикреплена болтами к фланцу 204 на выходном конце кожуха и снабжена выходным отверстием 218 для выгрузки продуктов реакции из реактора. Кожух 202 содержит пучок труб 220. Пучок труб имеет входную коллекторную пластину 222, сквозь которую протянуты трубы 224, которые связаны с выходным коллектором. Коллекторы внутри кожуха установлены плотно, с тем, чтобы сверхкритическая текучая среда не могла пройти от трубной зоны к внетрубной зоне или наоборот.
На практике для получения реактора образования катализатора трубы наполняют кислотой Льюиса и переходным металлом или насадку, состоящую из кислоты Льюиса и переходного металла, распределяют по их поверхности. Реакторная загрузка поступает во входное отверстие, протекает через пучок труб, вследствие чего перед выходом через выходное отверстие 218 происходит контактирование кислоты Льюиса и переходного металла. В то же самое время охлаждающая жидкость, подаваемая через входное отверстие 206, перетекает по пучку труб, вследствие чего осуществляются удаление экзотермического тепла реакции образования катализатора и выход через выходное отверстие 208.
Как объяснялось, реактор может быть также использован для растворения катализатора в потоке сверхкритической текучей среды или осаждения катализатора из алкилата на внутреннюю поверхность труб или на насадку, размещенную внутри труб. В этом смысле сосуд функционирует или как "растворительный", или как "осадительный" сосуд.
Для создания реактора алкилирования трубы не следует наполнять кислотой Льюиса, переходным металлом или насадкой, а предпочтительно следует оставлять пустыми для сведения к минимуму перепада давления.
Жидкофазные процессы.
Процессы следует осуществлять в подобном потоке, но при температуре и давлении, сохраняющих алкан в жидком состоянии. Фиг. 4 иллюстрирует схему потока для жидкофазного процесса алкилирования. Во многих отношениях схема потока подобна таковой для суперкритического режима текучей среды на фиг. 1, отличаясь от нее главным образом вычеркиванием предметов оборудования, которые необходимы только для процесса, в котором используют сверхкритическую жидкую среду, и изменением режимов работы других сосудов. Соответственно на фиг. 4 предметы оборудования, которые выполняют одинаковые функции, пронумерованы идентично, оборудование, которое выполняет измененную функцию, нумеруют с помощью суффикса "а". Следуя реакции алкилирования в реакторе 116, поток алкилатного продукта 120 подают в сосуд 122a, в котором расположен абсорбент для удаления катализатора, после этого алкилатный продукт подают посредством линии 124 в остаток процесса, режим работы которого такой, который был описан ранее.
Последующие примеры поясняют изобретение и ни в коей мере не ограничивают или не определяют объем изобретения.
Все примеры 1-3 процессов, в которых использовали сверхкритическую текучую среду, выполняли на аппаратуре, схематически изображенной на фиг. 3. На фиг. 3 изомеризованный алкан, содержащийся в автоклаве 331, и растворитель в газообразном состоянии из автоклава 330 добавляют в автоклав 331 путем барботажа в алкан через погружную трубку 332 до тех пор, пока давление в автоклаве 331 достигнет значения около 200 psi (фунтов/дюйм2). Стадия барботажа происходит в течение 48 часов, затем образованную жидкую смесь загружают во всасывание загрузочного насоса 337. Протонную кислоту Бренстеда держат в сосуде 335 и всасывают в шприцевидный насос 336 с объемом поршня около 500 мл, когда он полностью растянут. Когда поршень поднимают, кислота Бренстеда сжимается и разжижается в объем около 50 мл при давлении около 1300 фунтов/дюйм2. Сжатая кислота Бренстеда перетекает через трубу 334 в трубу 333, разгрузку загрузочного насоса 337, которая увлекает смесь растворителя и алкана в систему реактора, которую содержат в бане постоянной температуры 338, через которую циркулируют этиленгликоль для поддержания желательного уровня температуры в системе реактора.
В системе реактора исходное сырье 333, подаваемое в систему реактора, сначала проходит через предварительно нагретую систему труб длиной около 20 футов (20 х 30,5 см) для доведения его до рабочей температуры. Затем исходная смесь поступает в серию из 4 труб 352, где две средние трубы содержат кислоту Льюиса типа галогенид металла и, по желанию, переходный металл.
В средних трубах реактора протонная кислота Бренстеда, алкан, кислота Льюиса, по желанию переходный металл и растворитель взаимодействуют при сверхкритических условиях текучей среды для получения дискретного катализатора изобретения, растворенного в гомогенной среде, предназначенного для алкилирования алканов и олефинов. Первую и последнюю из труб 352 заполняют оксидом алюминия для образования первой и последней "предохранительной камеры". Из предохранительных труб 352 сверхкритическая жидкая смесь протекает на вход реактора 356, где происходит алкилирование. При этом через линию 370, расположенную на 2/3 длины реактора 356 от его входа, добавляют олефины. Изомеризованные алканы, остаточные непрореагировавшие алканы, растворитель, катализатор и остаточная кислота Бренстеда выходят из реактора 356 через линию 357 и входят в трубу 358, наполненную окисью магния для удаления из выходного потока остаточной кислоты Льюиса.
Вытекающий поток, по существу не содержащий кислоту Льюиса, протекает из трубы 358 через нагнетательный редукционный клапан 359 и частично сжижается. Частично жидкофазный вытекающий поток затем поступает в конденсатор 360, который сжижает, по крайней мере, алкилаты (C5 и выше) в вытекающем потоке. Частично сжиженный вытекающий поток поступает в конденсатор по линии 361 и разделяется в сепараторе 362 на жидкий и паровой продукт.
Жидкий продукт можно периодически удалять открытием клапана 364. Паровой продукт протекает через линию 366 через клапан 368 к ротаметру 372, который измеряет скорость его потока. Паровой продукт входит в ротаметр 372 по линии 374 и протекает в скруббер 376, содержащий 10 мас.% каустической соды, для удаления остаточных кислот Бренстеда. Из скруббера 376 вытекающий поток, по существу не содержащий кислоту, перетекает через линию 378 в сушильные камеры 380 и из них - в пробосборник.
Пример 1. Методика жидкофазного алкилирования.
Все стадии получения катализатора осуществляли под атмосферой сухого азота.
250 мл Трехгорлую колбу с круглым дном при азотной атмосфере снабдили магнитным перемешивающим брусом, капельной воронкой, конденсатором, охлаждаемым водой, и термометром. В капельную воронку поместили 9,7 г диизобутилалюминийхлорида. В круглодонную колбу поместили 7,9 г хлорида алюминия и 200 мл (132 г) высушенного н-гексана. В колбу при перемешивании медленно добавили диизобутилалюминий хлорид. Смесь оставили для перемешивания в течение 24 часов. Затем ее фильтровали фильтром, работающим под давлением, фильтрат анализировали на содержание алюминия. Анализ алюминия: экспериментально - 1,8%, теоретически - 1,9%. Раствор н-гексана содержал около 10,3% моноизобутилалюминийдихлорида (MIBAD) - предшественника катализатора.
i-Бутановое сырье, состоящее из 0,14 вес.% 1-хлорбутана, подали в реакторную установку со скоростью 96 см3/час.
Подали отдельную i-бутановую смесь, состоящую из 2,5 вес.% i-бутилалюминийдихлорида и 22,5 вес. % н-гексана, со скоростью 7,8 см3/час, которую смешали с другим потоком при рабочих условиях 220oF (104oC) и 650 фунтов/дюйм2.
К этому потоку со скоростью 4,5 см3/час добавили 2-бутен. Перед понижением давления через дозирующий клапан весь поток поступающего материала пропустили через трубу реактора OD длиной 4 фута 1/4 дюйма. Время пребывания в реакторе равно 10 минутам. Концентрация катализатора во всем потоке составила 1550 ppm (мас. частей на миллион) в пересчете на AlCl3. Анализ выходящего потока показал 100%-ную степень превращения олефина. Выходящий поток перетекает в охлаждающую ловушку при -110oF (-70oC). Затем обеспечили нагрев жидкости, собранной в охлаждающей ловушке, до температуры смеси воды со льдом и жидкость анализировали. Анализ GC/MS (газовой хроматографией/спектрометрией) жидкости, показал следующее:
Состав - Вес.%
Пропан - 1,1
Изобутан - 8,7
н-Бутан - 0,3
Изопентан - 3,4
2,3-Диметилбутан - 4,6
2-Метилпентан - 3,6
3-Метилпентан - 0,4
н-Гексан - 14,9
(из каталитической смеси)
2,4-Диметилпентан - 4,3
2,3-Диметилпентан - 2,1
2,2,4-Триметилпентан - 11,5
2,5-Диметилгексан - 6,0
2,4-Диметилгексан - 4,8
2,3,4-Триметилпентан - 6,9
2,3,3-Триметилпентан - 4,0
2,3-Диметилгексан - 3,1
2-Метилгептан - 1,6
3-Метилгептан - 1,0
2,2,5-Триметилгексан - 4,0
2,3,5-Триметилгексан - 1,5
н-Нонан (внутренний стандарт) - 10,4
Неустановленный углеводород - Баланс
Пример 2. Алкилирование в сверхкритической текучей среде.
В реакторную установку со скоростью 165 см3/час подавали этан. К этану со скоростью 2,5 см3/час добавили отдельный поток поступающего материала, состоящий из 96,3 об.% этана и 3,7 об.% HCl. К этому потоку этана со скоростью 50 см3/час также добавили i-бутановое исходное сырье. Рабочими условиями были температура 180oF (82oC) и давление 1000 фунтов/дюйм2. Этот поток пропустили через слой AlCl3. К потоку этана, i-бутана, HCl и AlCl3 добавили со скоростью 3,4 см3/час 2-бутен. Весь поток имел рассчитанную критическую температуру (Li, C. C. Can Y. ChE 19:709 (1972)) приблизительно 130oF и рассчитанное критическое абсолютное давление (Reid, Prausnitz, and Poling, The Properties of Gases and Liquids (Свойства газов и жидкостей), с. 131, 1987 (820 psia/фунтов/дюйм2). Перед выходом через дозирующий клапан этот поток пропустили через систему труб (реактор) OD длиной 11 1/4 дюйма. Время пребывания в реакторе составило 30 секунд. Концентрация катализатора в потоке была приблизительно 1090 мас. частей на миллион в пересчете на AlCl3. Выходящий поток пропустили через разделительную систему газа и жидкости, при этом газ удалили, а жидкость собрали в сборнике, погруженном в баню со льдом. Анализ газа показал 100% степень превращения. Анализ жидкости газовой хроматографией/масс-спектрометрией показал следующее:
Состав - Вес.%
Изобутан - 2,7
Изопентан - 2,6
2,3-Диметилбутан - 3,6
2-Метилпентан - 2,4
2,4-Диметилбутан - 1,2
2-Метилгексан - 2,0
2,3-Диметилпентан - 3,4
3-Метилгексан - 1,3
2,2,4-Триметилпентан - 11,5
2,5-Диметилгексан - 8,4
2,4-Диметилгексан - 6,9
2,3,4-Триметилпентан - 6,5
2,3,3-Триметилпентан - 5,0
2,3-Диметилгексан - 2,3
2-Метилгептан - 1,2
3-Метилгептан - 1,2
2,2,5-Триметилгексан - 10,7
2,3,5-Триметилгексан - 0,8
2,6-Диметилгептан - 0,6
2,5-Диметилгептан - 0,9
Неустановленный углеводород - Баланс
Пример 3. Алкилирование в сверхкритической текучей фазе.
Рабочими условиями были температура 200oF (93oC) и давление 750 фунтов/дюйм2, в установку со скоростью 165 см3/час подали пропановое сырье, содержащее 0,27 вес.% 1-хлорбутана. Поток i-бутана смешали с потоком пропана при скорости 40 см3/час. Перед смешиванием с пропаном и потоком бутана через слой AlCl3 пропустили отдельный поток i-бутана. В общий поток со скоростью 4,5 см3/час подали 2-бутен. Поток имел рассчитанную критическую температуру 220oF (104oC) и рассчитанное критическое давление 620 фунтов/дюйм2. Критическую температуру и критическое давление рассчитывали, используя тот же самый метод, что и в примере 1.
Этот поток перед снижением давления в дозирующем клапане пропустили через систему труб (реактор) длиной 1 фут 1/4 дюйма. Время пребывания в реакторе было около 45 секунд. Концентрация катализатора составляла приблизительно 700 мас. частей на миллион в пересчете на AlCl3. Газовый анализ выходного потока показал, что степень превращения олефина составила около 80%. Разделительная система газа и жидкости была той же самой, которую использовали в примере 1. Анализ газовой хроматографией/масс-спектрометрией показал следующее:
Состав - Вес.%
Изобутан - 3,5
н-Бутан - 0,4
транс-2-Бутен - 1,2
цис-2-Бутен - 1,2
Изопентан - 2,1
н-Пентан - 0,3
2,3-диметилбутан - 1,0
2-Метилпентан - 1,7
3-Метилпентан - 0,9
н-Гексан - 0,5
2-Хлорбутан - 0,8
2,4-Диметилбутан - 4,9
2-Метилгексан - 3,1
2,3-Диметилпентан - 5,3
3-Метилгексан - 2,2
2,2,4-Триметилпентан - 2,8
2,5-Диметилгексан - 4,5
2,4-Диметилгексан - 2,8
2,3,4-Триметилпентан - 1,5
2,3,3-Триметилпентан - 1,1
C8 - ан - 1,7
2-Метилгептан - 0,2
3-Метилгептан - 1,3
2,2,5-Триметилгексан - 1,1
C9 - ан - 0,9
Неустановленные углеводороды - Баланс
Пример 4. Жидкофазное алкилирование с использованием трубчатого реактора (120oF).
Методика эксперимента была такой, которая описана в примере 1, за исключением того, что для изучения влияния температуры на распределение продукта реакцию осуществляли вместо 220oF при 120oF. Рабочие условия были следующими: T=120oF, P=649 фунтов/дюйм2, исходное сырье - 2 бутен, молярное отношение i-бутана к 2-бутену = 43, молярное отношение 2-бутена к моноизобутилалюминийдихлориду (MIBAD)= 1,4; время пребывания в реакторе составило 8,2 минуты. Наблюдали 100%-ную степень превращения олефина. Продукт анализировали газовой хроматографией, результаты следующие:
Состав - Вес.%
i-Пентан - 3,2
2,3-Диметилбутан (DMB) - 5,1
2-Метилпентан (MP) - 9
3-Метилпентан - 4
2,4-Диметилпентан (DMP) - 4,1
2,2,3-Триметилбутан (TMB) - 6
2,3-Диметилпентан - 1,8
3-Метилгексан (MH) - 3
2,2,4-Триметилпентан (TMP) - 26,9
2,5-Диметилгексан (DMH) - 3,9
2,2,3-TMP - 3,3
2,4-DMH - 3,3
2,3,4-TMP - 14,8
2,3,3-TMP - 9,8
2,3-DMH - 5,9
2-Метилгептан (MHEP) - 9
3,4-DMH - 1,0
3-MHEP - 7
4-MHEP - 5
2,2,5-Триметилгексан (TMH) - 4,2
Другие C9 - 3,3
C10+ - 4,2
Исследовательское октановое число вычисляли посредством стандартного промышленного подхода, созданного по образцу метода Hutson и Logan Hydrocarbon Processing (Обработка углеводородов) сентябрь, 1975. В этом подходе используют весовой процент каждого компонента для вычисления распределения такого компонента к рассчитанному количеству октана (не молярного процента, как использовались Logan и Hutson). Предполагали, что содержание остаточного октана всех неустановленных соединений было равно 87 (по сравнению с 74 это значение было получено при вычислении по методу Logan и Hutson). Исследовательское октановое число, вычисленное этим способом, было равно 92,3. Установили, что значение бромного числа было равно 2,7, что указывало на то, что продукт был высокопарафинистым. Было ясно, что продукт примера 4 является продуктом более высокого качества, чем продукт примера 1, что доказывалось присутствием большого количества желательных TMP и уменьшенного количества C10+. Это иллюстрирует выгоду от использования низкотемпературного процесса.
Пример 5. Жидкофазное алкилирование с использованием трубчатого реактора (110 и 100oF).
Получив улучшенный продукт при 120oF, были сделаны попытки осуществления алкилирования при 110oF и при 100oF.
Методика эксперимента была такой, которая описана в примере 1. Рабочие условия для двух испытаний показаны в табл. 1.
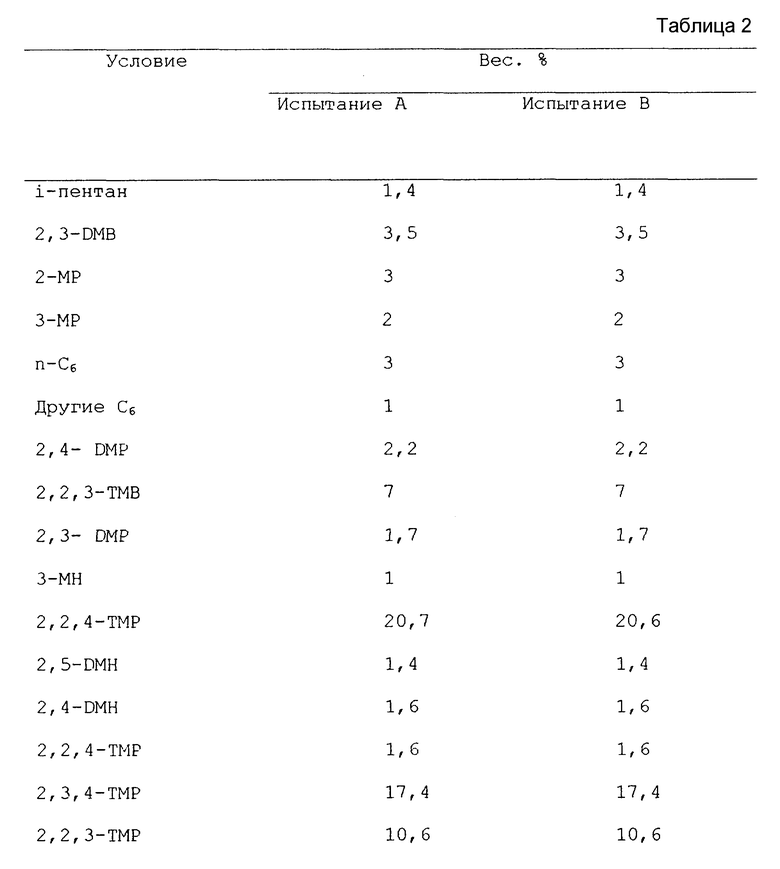
В испытании A наблюдали 100%-ную степень превращения олефина. В испытании B степень превращения олефина составила 81%. Продукт собрали в охлаждающей ловушке в бане со смесью сухого льда с ацетоном. Непревращенный i-бутан удалили, а алкилат анализировали газовой хроматографией. Анализ представлен в табл. 2.
Для обоих испытаний вычислили октановые числа, используя методику, описанную в примере 4. В соответствии с подобием при анализе продукта рассчитанное октановое число для испытания A было равно 93,9 а для испытания B оно составило 94,0. Для испытания A бромное число было равно 19, а для испытания В оно равнялось 28, что указывало на значительные количества ненасыщенности во фракции C10. При сравнении примеров 4 и 5 видно, что полученный октан улучшают путем снижения температуры ниже 120oF. Однако выход C10+ увеличивается и продукт становится более олефиновым.
Пример 6. Влияние бутадиена на производительность трубчатого реактора (120oF).
Бутадиен является обычной примесью при алкилировании сырья, который получают в виде побочного продукта при каталитическом крекинге. При обычных процессах алкилирования концентрация бутадиена обычно ограничивается значениями 1000-2000 част. на миллион (относительно общего содержания олефинов), потому что он полимеризуется и взаимодействует с катализатором алкилирования с образованием кислоторастворимого масла (Hydrocarbon Processing, ноябрь, 1991, cc. 89-92).
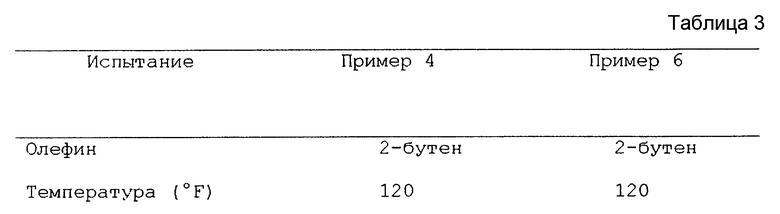
Для изучения влияния бутадиена на производительность реактора при использовании растворимых катализаторов этого способа 6600 част. на миллион 1,3-бутадиена смешивали с 2-бутеном. Полученное сырье испытывали в трубчатом реакторе при условиях, подобных тем, которые использовали в примере 4. Рабочие условия, анализы полученного продукта газовой хроматографией и рассчитанные октановые числа представлены в табл. 3. Октановые числа вычисляли посредством методики, обрисованной в общих чертах в примере 4. В обоих испытаниях наблюдали 100% степень превращения олефина. Бутадиен увеличивал вычисленное октановое число продукта за счет разрастания количества триметилпентанов и уменьшения количества диметилгексанов.
Бутадиен также образовывался при увеличении ненасыщенного C10+, что показано увеличением бромного числа и C10+ в продукте примера 6 относительно примера 4 (см. табл. 3).
Пример 7. Жидкофазное алкилирование с использованием реактора полного перемешивания (120oF).
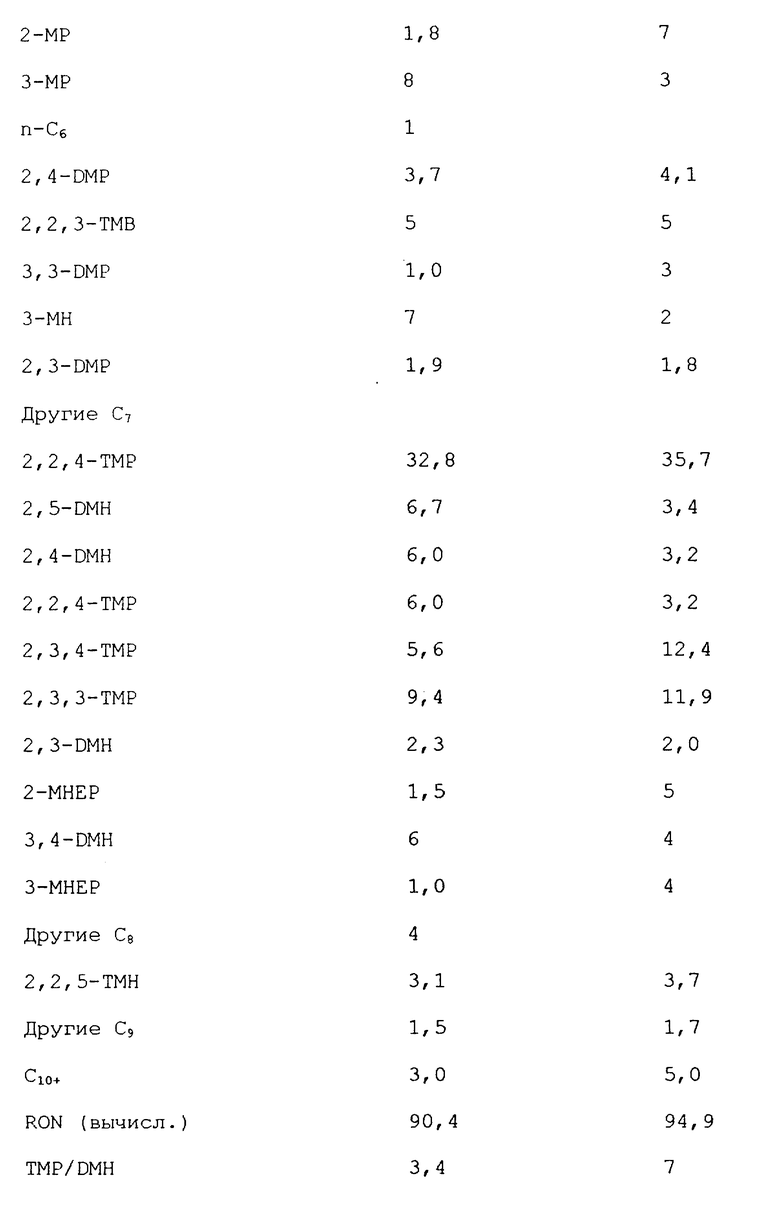
Использовали стадию получения катализатора и методику эксперимента, подобную таковым примера 1, за исключением того, что трубчатый реактор заменили плоскодонным реактором полного перемешивания общим объемом 75 см3. Алкилирование осуществляли путем подачи на основание реактора i-бутана, катализатора и 2-бутена. Продукт удаляли в верхнюю часть реактора и собирали в охлаждающей ловушке, охлажденной смесью сухого льда с ацетоном. Непрореагировавший i-бутан удалили, а алкилат анализировали газовой хроматографией. Рабочие условия, анализы продукта и рассчитанное значение октанового числа представлены в табл. 4. Исследовательское октановое число (RON) вычисляли методикой, описанной в общих чертах в примере 4. В испытании наблюдали 100%-ную степень превращения олефина (см. табл. 4).
Значение октанового числа отражает процентное содержание в продукте С8, а также относительные количества ТМР и DМН. Низкое бромное число указывает, что продукт является высокопарафинистым.
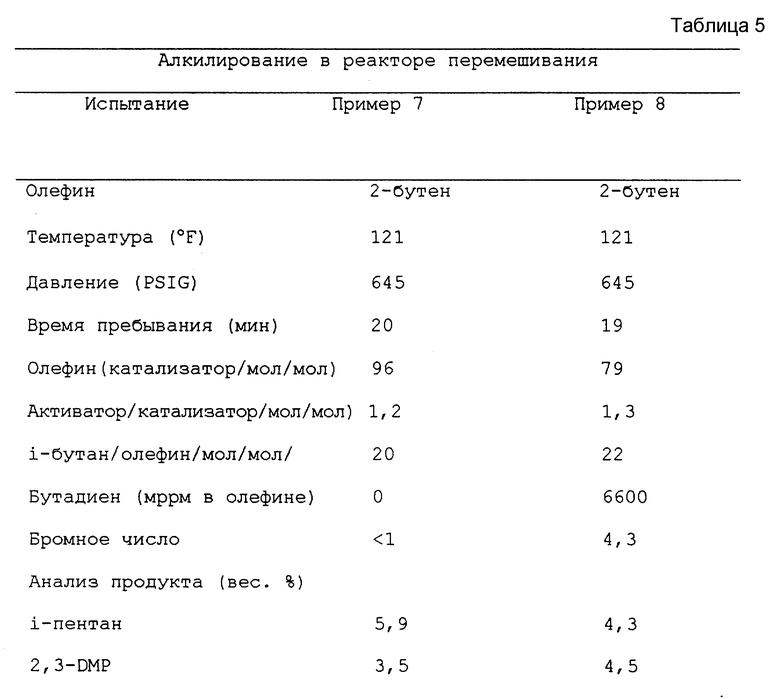
Пример 8. Влияние бутадиена на аклилирование в реакторе полного перемешивания (120oF). Осуществляли опыт, подобный примеру 7, в реакторе полного перемешивания, имеющем чашеобразное дно вместо плоского дна примера 7. Алкилирование проводили при условиях, показанных в табл. 5. Второе испытание проводили при добавлении к исходному 2-бутену 6600 молярных част. на миллион 1/3-бутадиена. В обоих случаях продукт удалили с верхней части реактора и собрали в охлаждающей ловушке, охлажденной смесью сухого льда с ацетоном. Непрореагировавший i-бутан удалили, а алкилат анализировали газовой хроматографией. Рабочие условия, анализ продукта и рассчитанное значение октанового числа представлены в табл. 5. Исследовательское октановое число вычисляли методикой, описанной в общих чертах в примере 4. В испытании наблюдали 100%-ную степень превращения олефина.
В испытании с добавлением бутадиена октановое число было выше. Это происходило в результате увеличения C8 в продукте, а также в результате увеличения количества полученного TMP относительно DMH. Во время испытания бутадиена отмечали также незначительное увеличение C10+ и ненасыщенности, что отражалось незначительным возрастанием бромного числа.
Пример 9. Жидкофазное алкилирование с использованием реактора полного перемешивания (77oF).
После того, как было доказано, что алкилирование можно осуществить при 100-120oF, была сделана попытка провести алкилирование при комнатной температуре.
Аппаратура, условия процесса и методика вычисления октанового числа были такими, как это описано в примере 7. Рабочие условия, анализ продукта и рассчитанное октановое число представлены ниже. На всем протяжении опыта наблюдали 100%-ную степень превращения олефина.
Алкилирование в реакторе перемешивания
Олефин - 2-Бутен
Температура (Fo) - 77
Давление (PSIG) - 647
Время пребывания (мин) - 19,3
Олефин/катализатор /мол/мол/ - 49,6
1-Хлорбутан (MIBAD/молярн.) - 8
i-Бутан/олефин /мол/мол/ - 19,3
Бромное число
Анализ продукта (вес.%)
i-Пентан - 3,6
2,3-DMB - 2,8
2-MP - 8
3-MP - 2
n-C6 - 8
2,4-DMP - 2,0
2,2,3-TMB - 1,4
2,3-DMP - 5
3-MH - 3
2,3-DMP - 9
Другие C7
2,2,4-TMP - 20,3
2,5-DMH - 3,1
2,4-DMH - 3,0
2,2,3-TMP - 3,0
2,3,4-TMP - 10,7
2,3,3-TMP - 6,9
2,3-DMH - 11,6
2-MHEP - 1,1
3,4-DMH - 1,2
3-MHEP - 9
Другие C8 - 2
2,2,5-TMH - 3,9
Другие C9 - 4,3
C10+ - 16,5
RON (вычисл.) - 88,8
TMP/DMH - 2,2
Вышеприведенное демонстрирует, что алкилирование можно проводить при комнатной температуре. Хотя изобретение было описано со ссылкой на его предпочтительные варианты, обычные специалисты в данной области при прочтении этого описания поймут те изменения и модификации, которые не отклоняются от области и сущности изобретения, которые описаны выше или которые будут изложены далее в формуле изобретения.







Описывается способ алкилирования олефина, имеющего по меньшей мере 3 атома углерода, изоалканом, имеющим по меньшей мере 4 атома углерода, в присутствии углеводородного комплексного катализатора на основе кислоты Льюиса, отличающийся тем, что используют комплексный катализатор, включающий продукт реакции по меньшей мере кислоты Льюиса
R(m-2-z)MX(2+z),
где М - металл групп 3а, 5а или 5в Периодической системы элементов; Х - галогенид; R - гидрокарбильный радикал, имеющий от 1 до 12 атомов углерода; m - целое число, равное наибольшей степени окисления M; z - целое число, равное 0, 1 или m-2; галогенида водорода и органического соединения, выбранного из парафинов или олефинов, имеющих 12 или меньшее количество атомов углерода, растворяют указанный продукт реакции во втором жидком углеводороде парафинового ряда, являющемся изоалканом C4-C12, при этом концентрация указанного продукта реакции составляет 3-30 ммоль на 1000 г полученного раствора, поддерживают полученный раствор, содержащий продукт реакции, растворенный во втором жидком углеводороде парафинового ряда, при температуре, при которой не происходит осаждение катализатора в течение процесса алкилирования, добавляют алкилируемый углеводород, являющийся олефином С3-С5, при этом указанный раствор и олефин поддерживают в условиях температуры и давления, достаточных для поддержания их в жидком состоянии, и алкилирование ведут до того, как начнется существенное осаждение катализатора; полученный алкилированный изопарафин, включающий углеводородные соединения с разветвленной структурой, имеющие число атомов углерода большее, чем изоалкан или олефин, отделяют от углеводородного комплексного катализатора на основе кислоты Льюиса. Технический результат - упрощение процесса. 14 з.п.ф-лы, 4 ил., 5 табл.
R(m-2-z)MX(2+z),
где М - металл групп 3а, 5а или 5в Периодической системы элементов;
Х - галогенид;
R - гидрокарбильный радикал, имеющий от 1 до 12 атомов углерода;
m - целое число, равное наибольшей степени окисления М;
z - целое число, равное 0, 1 или m-2,
галогенида водорода и органического соединения, выбранного из парафинов, имеющих 12 или меньшее количество атомов углерода, или олефинов, имеющих 12 или меньшее количество атомов углерода, растворяют указанный продукт реакции во втором жидком углеводороде парафинового ряда, являющемся изоалканом С4-С12, при этом концентрация указанного продукта реакции составляет 3-30 ммоль на 1000 г полученного раствора, поддерживают полученный раствор, содержащий продукт реакции, растворенный во втором жидком углеводороде парафинового ряда, при температуре, при которой не происходит осаждение катализатора в течение процесса алкилирования, добавляют углеводород для алкилирования, являющийся олефином С3-С5, при этом указанный раствор и олефин поддерживают в условиях температуры и давления, достаточных для поддержания их в жидком состоянии, и алкилирование ведут до того, как начнется существенное осаждение катализатора, полученный алкилированный изопарафин, включающий углеводородные соединения с разветвленной структурой, имеющие число атомов углерода, больше, чем изоалкан или олефин, отделяют от углеводородного комплексного катализатора на основе кислоты Льюиса.
R(m-2-z)AlX(2+z),
где Х - хлорид, R - гидрокарбильный радикал, имеющий от 1 до 12 атомов углерода, m - целое число, равное наибольшей степени окисления алюминия, z - целое число, равное 0, 1 или m-2, галогенид водорода, которым является HCl.
Приоритет по пунктам:
21.12.92 - по пп.1-15,
19.07.93 - по п.1.
| US 3873635 A, 25.03.75 | |||
| ВПТБ | 0 |
|
SU400075A1 |
| Способ получения высокооктанового алкилата | 1981 |
|
SU1172916A1 |
Авторы
Даты
1999-09-27—Публикация
1993-12-13—Подача