Изобретение относится к иммунной системе, в частности к вакцине для профилактики или лечения опосредованной Т-клетками патологии или нерегулируемой репликации клонами Т-клеток, способу выделения вакцины, способу диагностирования или прогнозирования восприимчивости к ревматоидному артриту или рассеянному склерозу, способу профилактики или лечения ревматоидного артрита или рассеянного склероза и содержащему последовательность SGDQGGNE пептиду, являющемуся агентом для обнаружения, профилактики или лечения рассеянного склероза.
Высшие организмы отличаются иммунной системой, защищающей их от инвазии возможно вредных веществ или микроорганизмов. Если вещество, обозначаемое как антиген, проникает в тело и если оно узнавается как чужое, то иммунная система вызывает и опосредованную антителами реакцию, и клеточно-опосредованную реакцию. Клетки иммунной системы, обозначаемые как Б-лимфоциты, или Б-клетки, производят антитела, специфически узнающие чужое вещество и связывающиеся с ними. Другие лимфоциты, обозначаемые как Т-лимфоциты, или Т-клетки, и вызывают, и регулируют клеточно-опосредованную реакцию, в конечном счете приводящую к уничтожению антигена.
В клеточно-опосредованной реакции участвуют разные виды Т-клеток. Некоторые из них индуцируют определенные клоны Б-клеток к пролиферации и производству антител, специфических для соответствующего антигена. Другие узнают и уничтожают клетки, представляющие собой чужие антигены на своей поверхности. Определенные Т-клетки регулируют реакцию или путем стимуляции, или путем супрессии других клеток.
Нормальная иммунная система точно регулируется, однако отклонения не редки. В некоторых случаях иммунная система работает неправильно и реагирует на компонент хозяина, как будто он являлся чужим. Такая реакция приводит к аутоиммунной болезни, которая выражается в том, что иммунная система организма атакует ткань хозяина. Т-клетки, являясь основными регуляторами иммунной системы, непосредственно или косвенно вызывают такие аутоиммунные патологии.
Предполагают, что многочисленные болезни являются результатом аутоиммунных механизмов. Самые известные из этих болезней - ревматоидный артрит, системная красная волчанка, рассеянный склероз, диабет типа I, миастения gravis и обыкновенная пузырчатка. Миллионы людей во всем мире страдают от аутоиммунных болезней, и связанные с этими болезнями расходы, включающие и само лечение, побочные расходы и потери трудовой производительности составляют миллиарды долларов каждый год. В настоящее время нет средств для эффективного лечения таких аутоиммунных патологий. Обычно можно лечить лишь симптомы, причем сама болезнь прогрессирует, часто приводя к серьезному ослаблению больного или его смерти.
В других случаях лимфоциты умножаются чрезмерно и неконтролируемым образом. Такое умножение приводит к раковому состоянию, т.н. лимфоме. В том случае, если нерегулируемые лимфоциты являются Т-клетками, то данные опухоли обозначают как лимфомы Т-клеток. Также как и другие злокачественные опухоли и лимфомы Т-клеток эффективно лечить трудно.
Таким образом, уже давно нуждаются в эффективном средстве для лечения или уменьшения интенсивности патологий, опосредованных Т-клетками. В идеальном случае такое лечение включало бы скорее контроль неподходящей реакции Т-клеток чем лишь уменьшение интенсивности симптомов. Настоящее изобретение удовлетворяет это требование и одновременно имеет побочные преимущества.
Первым объектом настоящего изобретения является вакцина для профилактики или лечения опосредованной Т-клетками патологии или нерегулируемой репликации клонами Т-клеток в млекопитающих, содержащая фармацевтически переносимую среду и активное вещество, представляющее собой рецептор Т-клеток или его фрагмент, соответствующий рецептору опосредующих данную патологию Т-клеток, находящемуся на их поверхности, или антиидиотипические антитела, являющиеся внутренним изображением данного рецептора Т-клеток или его упомянутого фрагмента, причем активное вещество взято в иммуногенно эффективном количестве.
Под понятием "опосредованная Т-клетками патология" в данном тексте понимается любое состояние, в котором неуместная реакция Т-клеток является компонентом патологии. Данное понятие здесь охватывает и болезни, непосредственно опосредованные Т-клетками, и болезни, напр. миастению gravis, которые прежде всего проявляются в нарушении, вызываемом связыванием антител, а также болезни, вызванные неуместной реакцией Т-клеток, приводящей к производству таких антител. Т.е., данное понятие охватывает и аутоиммунные болезни, опосредованные Т-клетками, и нерегулируемую репликацию клонами Т-клеток.
В нижеследующем обороте "в основном последовательность" в связи с последовательностью аминокислот следует понимать в смысле или описываемой последовательности, или другой последовательности, в которой добавлены, пропущены или заменены отдельные звенья, причем данные изменения не существенно влияют на способность последовательности вызывать иммунную реакцию против желаемой последовательности рецептора Т-клеток. Таким образом, участок описываемой иммунизирующей последовательности можно использовать всегда тогда, когда он в достаточной степени является характерным для желаемого рецептора Т-клеток с тем, чтобы вызывать эффективную иммунную реакцию против желаемых рецепторов Т-клеток, а не против нежелаемых рецепторов Т-клеток. Таких вариаций последовательности можно достичь простыми методами, напр., путем синтеза другой последовательности, и их эффективность можно проверять, напр., путем иммунизации млекопитающих.
Понятие "фрагмент" в нижеследующем охватывает фрагменты в сочетании с дополнительными последовательностями или частями, в которых, напр., пептид связан с другими последовательностями аминокислот или с носителем, или фрагменты, связанные с ними. Понятия "фрагмент" и "пептид" поэтому могут быть использованы в данном тексте как взаимозаменимые понятия, т.к. пептид будет являться самым распространенным фрагментом рецептора Т-клеток. Каждый фрагмент согласно изобретению может иметь измененную последовательность, как описано выше в разделе "в основном последовательность".
Когда в нижеследующем речь идет о "фрагменте или участке рецептора Т-клеток", тогда это не означает, что они должны быть производными неповрежденных рецепторов Т-клеток. Такие "фрагменты или участки" можно производить с помощью разных известных методов, напр., путем ручного или автоматического синтеза пептида или путем клонирования.
В нижеследующем в связи с отношением между фрагментом предлагаемого пептида и последовательностями рецепторов Т-клеток слово "соответствующий" означает, что фрагмент пептида имеет последовательность аминокислот, которая в достаточной степени гомологична последовательности рецептора Т-клеток с тем, чтобы возбуждать регулирующую реакцию в индивидууме. Однако последовательности не обязательно тождественны с последовательностью рецептора Т-клеток, как видно в примерах II и III.
Под словами "иммуногенно эффективный" здесь понимается количество рецептора Т-клеток или его фрагмента, которое эффективно вызывает иммунную реакцию для профилактики или лечения опосредованной Т-клетками патологии или нерегулируемой репликации клонами Т-клеток в индивидууме. Само собой разумеется, что такое количество может колебаться в зависимости от существа и индивидуума и многих других факторов. Например, в общем у человека для эффективной иммунной реакции необходима большая доза, чем у мыши.
В качестве наличия вакцины в жидком состоянии концентрация активного вещества составляет примерно 1 мкг - 100 мг на мл. В случае использования предлагаемой вакцины в твердом состоянии активное вещество берут с соответствующей концентрацией.
В нижеследующем под "Vβ17" понимается определенный вариабельный участок β-цепи рецептора Т-клеток. Vβ17 имеет следующую последовательность аминокислот: MSNQVLCCVVLCFLGANTVDGGITQSPKYLFRKEGQNVTLSCEQNLNHD AMYWYRQDPGQGLRLIYYSQIVNDFQKGDIAEGYSVSREKKESFPLTVTSAQK NPTAFYLCASS. Гипервариабельные и связывающие участки являются наиболее полезными для вакцин. Один из гипервариабельных участков Vβ17, а именно участок CDR2, имеющий последовательность аминокислот SQIVNDFQK, является особенно полезным. Модификации данной последовательности, не затрагивающие способность рецептора к действию в качестве иммуногена, вызывая желаемую иммунную реакцию, также охватываются данным термином. Вариабельный участок может быть сявзан с любым D- или J-сегментом рецептора Т-клеток. Кроме того, иммуногенно действующие фрагменты Vβ17 также охватываются определением "Vβ17".
В нижеследующем под "партнером (для связывания)" понимается состав, способный к взаимодействию с рецептором Т-клеток. В общем данный состав представляет собой главный антиген тканевой совместимости (МНС), но он может быть любым составом, при обычном связывании рецептора Т-клеток приводящим к активации или пролиферации Т-клеток.
Под понятием "лиганд" в нижеследующем понимается любая молекула, которая реагирует с другой молекулой с образованием комплекса.
Слова "избирательно связывается с" в нижеследующем следует понимать так, что молекула связывается с одним видом молекул, но в основном не с другими. В отношении Vβ17 "избирательно связывается с" включает связывание с рецепторами Т-клеток, содержащими Vβ17 , но в основном не с рецепторами Т-клеток, не содержащими Vβ17.
Иммунная система является главной биологической защитой хозяина (собственного организма) от возможно вредных (чужих) агентов. Такими вредными агентами могут быть, напр., патогенные факторы, напр., бактерии или вирусы, а также модифицированные собственные клетки, включая инфицированные вирусами клетки, опухолевые клетки и другие анормальные клетки хозяина. Все эти цели иммунной системы обобщенно называют антигенами. При узнавании антигена иммунной системой сразу же включается иммунный механизм для уничтожения антигена, защищая таким образом здоровье хозяина.
Главными типами специфической для определенного антигена иммунной реакции являются гуморальный (опосредованный антителами) и клеточный (клеточно-опосредованный) иммунитет. Каждый из этих иммуннологических механизмов пускается активацией вспомогательными (CD4+) Т-клетками. Данные CD4+ Т-клетки стимулируют Б-клетки, способные к синтезу антител путем связывания антигенов, в результате чего они пролиферируют и секретируют антитела. Секретированные антитела связываются с антигенами и облегчают их уничтожение путем других иммунных механизмов. Подобным образом CD4+ Т-клетки отдают стимулирующие сигналы цитотоксическим (CD8+) Т-клеткам, которые узнают и уничтожают соответствующие клетки (напр., инфицированные вирусами клетки хозяина). Таким образом, активация CD4+ Т-клеток является решающим фактором при стимуляции иммунной реакции. Поэтому ознакомление с механизмами, приводящими к специфической для определенного антигена активации CD4+ Т-клеток, важно при любой попытке избирательной модификации иммунологического действия.
Специфичность Т-клеток относительно определенных антигенов обеспечивается рецептором Т-клеток, выраженным на поверхности клетки. Рецептор Т-клеток является гетеродимерным гликопротеином, состоящим из двух полипептидных нитей, каждая из которых имеет молекулярный вес примерно 45 пар оснований (п.о.). Известны две формы рецепторов Т-клеток. Одна состоит из альфа-нити и бета-нити, а другая - из гамма-нити и дельта-нити. Каждая из данных полипептидных нитей рецепторов Т-клеток кодирована определенным генетическим локусом, содержащим сложные прерывистые сегменты генов, представляющее собой, напр., вариабельные (В), связывающие (J) или неменяющиеся (С) участки. Бета- и дельта-нити содержат дополнительный элемент, обозначаемый как диверзиционный (D) сегмент. (Т.к. диверзиционные сегменты (D) и элементы содержатся лишь в некоторых генетических локусах рецепторов Т-клеток и полипептидах, в нижеследующем они приведены в скобках с тем, чтобы показать, что данные участки имеются лишь в соответствующих нитях рецепторов Т-клеток. Таким образом, V(D)J относится или к последовательности VDJ нитей, имеющих D-участок, или к последовательности VJ, в которых не имеется D-участка.)
Во время мейозы лимфоцитов отдельные V-, (D-) и J-сегменты перегруппируются и формируют функциональный ген, определяющий последовательность аминокислот рецептора Т-клеток, выраженного данной клеткой. Т.к. запас V-, (D-) и J-генов, который может перегруппироваться, содержит много членов и благодаря тому, что отдельные элементы данного запаса могут перегруппироваться с любой комбинацией, общий запас рецепторов Т-клеток является в высокой степени диверзиционным и способным к связыванию бесчисленных партнеров, которые могут наступать на организм. Однако каждая отдельная Т-клетка имеет лишь одну молекулу Т-рецептора, которая в основном, если не полностью, предопределяет специфичность данной Т-клетки относительно его партнера.
Модели на животных значительно способствовали пониманию иммунологических механизмов аутоиммунных болезней. Одной моделей является экспериментальный аллергический энцефаломиелит (ЕАЕ), представляющий собой аутоиммунную болезнь центральной нервной системы, которую можно вызывать в мышах и крысах путем иммунизации с основным протеином миелина (МБР). Характеристика упомянутой болезни следующая: клинически - паралич и легкая гипотрофия, а гистологически - периваскулярная мононуклеарная инфильтрация клеток паренхимы центральной нервной системы. Патогенез болезни опосредуется Т-клетками, специфическими в отношении основного протеина миелина. Разнообразные клоны специфических в отношении основного протеина миелина Т-клеток выделяли из животных, страдающих от экспериментального аллергического энцефаломиелита, и их амплифицировали путем последовательной культивации. После стимуляции in vitro основным протеином миелина данные Т-клетки сражу же вызывают экспериментальный аллергический энцефаломиелит, когда их адаптивно переносят в здорового хозяина. Важно при этом, что данные вызывающие экспериментальный аллергический энцефаломиелит Т-клетки специфические не только в отношении именно этого антигена (основного протеина миелина), но обычно в отношении одного единственного эпитопа на данном антигене. Все это означает, что малые количества аутоагрессивных Т-клеток ответственны за патогенез экспериментального аллергического энцефаломиелита.
В результате анализа рецепторов Т-клеток, вызывающих экспериментальный аллергический энцефаломиелит, выявилось, что структура данных связанных с болезнью рецепторов имеет уменьшенную разнородность. В ходе анализа, в котором исследовали 33 взаимодействующие с основным протеином миелина Т-клетки, обнаружили лишь два содержащих вариабельные участки сегмента альфа-нитей и один единственный сегмент альфа-нити, содержащий связывающий участок. В этой совокупности Т-клеток также обнаружили одинаково ограниченное использование генов рецепторов Т-клеток в бета-нитях. Имелись лишь два содержащих вариабельные участки сегмента бета-нитей и два сегмента, содержащих связывающие участки. Еще важнее, примерно 80% клонов Т-клеток на V-D-J-участках бета-нити имели идентичные последовательности аминокислот. Эти результаты подтверждают, что рецепторы Т-клеток с похожей специфичностью относительно антигенов также имеют одинаковую структуру, и показывают, что рецептор Т-клеток является подходящей целью для иммунотерапевтичесих стратегий при борьбе с патогенезом экспериментального аллергического энцефаломиелита.
Разнообразными методами пытались использовать специфичность аутоагрессивных Т-клеток относительно антигенов для выработки стратегий для лечения экспериментального аллергического энцефаломиелита. Например, использовали пассивную дачу моноклональных антител, специфических для рецепторов, имеющихся на поверхности вызывающих экспериментальный аллергический энцефаломиелит Т-клеток. В случае мышиной модели экспериментального аллергического энцефаломиелита в результате инфузии моноклонального антитела, специфического для V,β8, представляющего собой больший вариабельный участок бета-нити, использованный в специфических относительно основного протеина миелина Т-клетках, восприимчивость мышей к последующей индукции экспериментального аллергического энцефаломиелита снизилась (см. Аха-Орбеа и др., Cell, N 54, стр. 263 - 273, 1988 г., и Урбан и др., Cell, N 54, стр. 577 - 592, 1988 г.). Подобная защита достигалась в случае экспериментального аллергического энцефаломиелита у крыс с помощью моноклонального антитела, способного к взаимодействию с неидентифицированной идиотипической детерминантой рецептора Т-клеток на специфических относительно основного протеина миелина Т-клетках (см. Бэрнс и др., J. Exp. Med., N 169, стр. 27 - 39, 1989 г. ). Хотя терапия пассивными антителами по всей видимости положительно сказывается на восприимчивость к экспериментальному аллергическому энцефаломиелиту, она связана с потенциальными проблемами. Достигаемая защита исчезает, в связи с чем требуется повторная дача антитела. При многократной инфузии антител, однако, повышается вероятность того, что хозяин развивает иммунную реакцию против подаваемых антител, в частности тогда, если их получили в ксеногенном животном. Кроме того, реакция антител на патогенный клон Т-клеток представляет собой лишь одно звено всей иммунной реакции и пренебрежает возможную роль клеточного иммунитета при преодолении аутореактивности.
Роль клеточного иммунитета при снижении активности аутоагрессивных Т-клеток при экспериментальном аллергическом энцефаломиелите явилась предметом исследований, и предложены возможные терапии. Подобно методу пассивных антител ex vivo получили регулирующие Т-клетки, которые затем вновь дали хозяину в рамках иммунотерапии. Напр., недавно выделили клон CD8+ Т-клеток из выздоравливающих крыс, в которых путем адоптивного переноса специфической относительно основного протеина миелина линии CD4+ Т-клетки вызвали экспериментальный аллергический энцефаломиелит (см. Сан и др., Nature, N 332, стр. 843 - 845, 1988 г.). Данный клон CD8+ Т-клетки in vitro проявил цитолитическую активность в отношении содержащей CD4+ Т-клетки, использованной для индукции болезни. Кроме того, адоптивный перенос данного клона CTL снизил восприимчивость соответствующих крыс при последующей подаче основного протеина миелина. Лидер и др. (см. Science, N 239, стр. 181 -183, 1988 г.) также выделили клоны CD8+ Т-клеток, обладающие супрессивной активностью относительно вызывающих экспериментальный аллергический энцефаломиелит Т-клеток. Данный клон CD8+ Т-клеток выделили из крыс, вакцинированных аттенуированными клонами Т-клеток, вызывающими болезнь, и, хотя он не проявлял ситолитической активности in vitro, он был способен к супрессии зависимой от основного протеина миелина пролиферации Т-клеток, вызывающих экспериментальный аллергический энцефаломиелит. Хотя данные анализы показывают, что содержащие CD8+ Т-клетки способны к сдерживанию экспериментального аллергического энцефаломиелита, все-таки невероятно, что данные определенные CD8+ CTL будут играть важную роль для долгосрочной резистентности выздоровевших крыс, т.к. Седжвик и др. (Eur. J. Immunol., N 18, стр. 495 - 502) ясно показали, что удаление содержащих CD8+ клеток с моноклональными антителами не влияет на протекание болезни или выздоровление.
В вышеописанных опытах Сана и др. и Лидера и др. дача регулирующих Т-клеток приводит к преодолению важной проблемы пассивной терапии антителами, т.к. она позволяет достичь долгосрочной регулирующей реакции in vivo. Однако она требует культивации in vitro с использованием аттенуированных Т-клеток, вызывающих болезнь, с тем, чтобы развивать клоны таких регулирующих Т-клеток, что представляет собой дорогостоящий и трудоемкий процесс. Кроме того, в случае человека из-за неидентичности главного антигена тканевой совместимости это требует в высокой степени индивидуализованную терапевтическую стратегию, т.к. для каждого отдельного больного необходимо получение регулирующих клонов, которые затем дают исключительно этому больному с тем, чтобы исключить возможную реакцию "трансплантат против хозяина".
Непосредственную вакцинацию аттенуированными клонами Т-клеток, вызывающих болезнь, использовали для терапии экспериментального аллергического энцефаломиелита. Т-клетки, специфические относительно основного протеина миелина и способные к передаче болезни, аттенуировали путем облучения гамма-лучами или химической фиксации и затем их использовали для вакцинации неинфицированных крыс. В некоторых случаях вакцинированные животные развивали резистентность относительно последующих попыток вызвать у них экспериментальный аллергический энцефаломиелит (Лидер и др., см. выше, а также у Кохена и Вайнера, Immunol. Today, N 9, стр. 332 - 335, 1988 г.). Однако эффективность такой вакцинации изменчивая, и степень защиты также значительно колеблется. Т-клетки содержат много разнообразных антигенов, которые вызывают иммунную реакцию, когда целую Т-клетку применяют в качестве вакцины. Это показали Оффнер и др. (J. NeuroimmunoL, N 21, стр. 13 - 22, 1989 г.), кто доказали, что иммунизация применением целой Т-клетки способствует аллергической реакции замедленного типа, определяемой на набухании уха, на данные Т-клетки, которая возрастает с увеличением числа вакцинаций. Однако четкие аллергические реакции замедленного типа устанавливали и в защищенных, и в незащищенных животных. Крысы показывали похожую реакцию при вакцинации и вызывающих энцефалит Т-клеток, и контрольных Т-клеток. И наоборот, вакцинация специфическими относительно очищенного деривата протеина Т-клетками из специфической относительно очищенного деривата протеина линии вызвала аллергическую реакцию замедленного типа и на клетки вакцины, и на вызывающий энцефалит клон, хотя не обнаруживалось никакой защиты. Похожая реакция вакцинированных крыс на вызывающие болезнь клетки и на контрольные клетки, определяемая на аллергической реакции замедленного типа (которая является мерой для клеточно-опосредованного иммунитета), указывает на то, что многочисленные антигены данных Т-клеток вызывают иммунную реакцию. Таким образом, недостатками вакцинации аттенуированными Т-клетками, вызывающими болезнь, являются недостаточная специфичность относительно защитного антигена на поверхности данной Т-клетки, а также непостоянные результаты относительно иммунитета против данного антигена. Что касается применения данного метода для лечения людей, то он является таким же трудоемким, как и вышеописанная инфузия CD8+ клеток, и также как и последняя данный метод требует индивидуализованной терапии.
Настоящее изобретение предлагает эффективный способ иммунотерапии патологий, опосредованных Т-клетками, включая аутоиммунных болезней, не связанный с теми проблемами, с которыми связаны вышеописанные известные методы лечения. Путем вакцинации, а не путем пассивной дачи гетерологических антител мобилизуется собственная иммунная система хозяина к супрессии аутоагрессивных Т-клеток. Таким образом, супрессия является постоянной и может охватывать любые и все иммунологические механизмы, приводящие к этой супрессии. Такая многосторонняя реакция является более эффективной, чем односторонняя супрессия, достигаемая путем пассивного применения моноклональных антител или клонов регулирующих Т-клеток.
Т. к. предлагаемые вакцины служат для борьбы с аутоиммунными болезнями, они содержат рецепторы Т-клеток, опосредующих аутоиммунные болезни. Вакцины могут являться или целыми рецепторами Т-клеток, в основном очищенными от клонов Т-клеток, или отдельными нитями рецепторов Т-клеток (напр., альфа- бета-, гамма-нитями), или частями таких нитей, или отдельно или в сочетании друг с другом. Вакцина может быть или гомогенной, напр., включать лишь один пептид, или содержать более одного типа пептида, причем каждый пептид относится к разной части рецептора. Кроме того, данные пептиды могут происходить от разных рецепторов, когда оба рецептора способствуют опосредованной Т-клетками патологии.
Согласно особенной форме выполнения изобретения иммунизирующий пептид может иметь последовательность аминокислот SGDQGGNE, если он призван служить для лечения рассеянного склероза. Любая иммуногенная часть данного пептида может быть эффективной. Таким образом, возможна замена аминокислот без потери иммуногенности пептида. Кроме того, данный пептид может быть связанным с носителем с тем, чтобы дальше повышать его иммуногенность.
Согласно дальнейшему развитию изобретения для иммунизации человека, страдающего от ревматоидного артрита, можно использовать рецепторы Т-клеток или фрагменты рецепторов, содержащие Vβ17 , для лечения или профилактики данной болезни. Вызываемая в человеке иммунная реакция может обезвреживать или уничтожать Т-клетки, имеющие Vβ17, и таким образом предотвращать или лечить их вредное действие. Кроме того, в той степени, в которой Vβ17 имеется также в рецепторах на патогенных Т-клетках, опосредующих аутоиммунные болезни в общем, предлагаемые вакцины можно использовать и для борьбы с такими другими аутоиммунными болезнями.
Слова "в основном чистый" означают, что рецептор Т-клеток в основном свободен от других биохимических компонентов, с которыми он обычно связан в природе. Альтернативно вакцины содержат пептиды разной длины, соответствующей рецептору Т-клеток или его частям. Пептиды можно получать или путем синтеза, или путем рекомбинации с помощью известных для специалиста методов. Предпочтительно пептидные вакцины соответствуют участкам рецепторов Т-клеток, которыми данный рецептор отличается от других, непатогенных рецепторов. Такие специфические участки могут находиться на отдельных(ом) участках(е) соответствующих полипептидных нитей рецептора, в частности на небольшой последовательности, включающей V(D)J-участок, ограничивая таким образом иммунную реакцию на Т-клетки, содержащие данную детерминанту.
Вакцины дают в том случае, если хозяин показывает аутоиммунную реакцию или находится в такой опасности. Точный клинический диагноз определенной аутоиммунной болезни оправдывает дачу необходимых специфических для данной болезни вакцин, содержащих рецепторы Т-клеток. Профилактическая дача оправдана там, где аутоиммунные механизмы предшествуют началу открытой клинической болезни (напр., диабета типа I). Таким образом, данные вакцины можно до начала болезни профилактически применять у людей, у которых в семейном анамнезе имеется соответствующая болезнь и которые, судя по надежным показателям, находятся в опасности заболевания.
Содержащие рецепторы Т-клеток вакцины можно применять с многими возможными составами, с фармацевтически переносимой средой. В случае короткого пептида последний может быть связан с носителем, напр., выделенным из блюдечка гемоцианином, с тем, чтобы повысить его иммуногенность. Вакцину можно давать в сочетании с адъювантом (имеется несколько известных адъювантов). После начальной иммунизации вакциной можно подавать усилитель. Вакцины апплицируют известными методами в дозах, которые достаточны для индукции иммунной реакции и легко могут быть определены любым специалистом.
Пригодные для иммунизации пептиды можно находить следующим образом. Клоны вызывающих болезнь Т-клеток, взаимодействующие с антигенами, с которыми хотят бороться, выделяют из зараженных индивидуумов. Такие Т-клетки получают предпочтительно в месте, где проявляется сильная аутоагрессивная активность, т. е. в месте патологического изменения в случае обыкновенной пузырчатки, из центральной нервной системы в случае рассеянного склероза, из синовиальной жидкости или ткани в случае ревматоидного артрита или же из крови соответствующего зараженного индивидуума. Затем определяют последовательность аминокислот генов рецепторов аутоагрессивных Т-клеток. После этого для вакцинов, используемых вышеописанным образом, можно выбирать полипептиды, соответствующие рецепторам Т-клеток или частям рецепторов, имеющимся, в частности, в вызывающих болезнь Т-клетках (по сравнению с непатогенными Т-клетками).
Вместо этого вакцина может содержать антиидиотипические антитела, являющиеся внутренними изображениями вышеописанных пептидов. Методы получения, отбора и применения таких антиидиотипических вакцин известны (см., напр., Айхманн и др., CRC Critical Reviews в Immunology, N 7, стр. 193 - 227, 1987 г.).
Опосредованные Т-клетками патологии со злокачественной этиологией
Полезность вакцинации рецепторами Т-клеток выше пояснилась на примере аутоиммунных болезней. Кроме того, и вызванная Т-клетками лимфома является патологией, поддающейся такому лечению. Применение данной технологии при лечении Т-лимфомы можно осуществлять в основном идентичным методом. Однако данная технология применяется скорее при Т-клеточной пролиферативной болезни, т. к. легче осуществлять выделение патогенных Т-клеток. После выделения клонов технологию осуществляют нижеописанным образом. В частности, определяют последовательность аминокислот генов рецепторов Т-клеток Т-лимфомов и определяют подходящие участки данных рецепторов, которые используют в качестве вакцин. Вакцины могут содержать или простые, или сложные пептиды, и их можно применять известным образом в фармакологически переносимом составе с адъювантом или без него.
Рассеянный склероз
Вызывающие рассеянный склероз Т-клетки до сих пор еще не идентифицировали, хотя из-за клинических и гистологических сходств рассеянного склероза и экспериментального аллергического энцефаломиелита предполагали, что Т-клетки, взаимодействующие с основным протеином миелина, при этом играют некоторую роль. При экспериментальном аллергическом энцефаломиелите на крысах и мышах энцефалогенные Т-клетки, взаимодействующие с основным протеином миелина, показывают поразительное сохранение последовательности аминокислот на VDJ-участке β-нити, несмотря на известные различия по рестрикции главного антигена тканевой совместимости и антигенной специфичности основного протеина миелина. Настоящее изобретение основывается на обнаружении того, что линия Т-клетки человека, взаимодействующая с основным протеином миелина и полученная из больного рассеянным склерозом, имеет β-нить рецептора Т-клеток с VDJ-последовательностью аминокислот, соответствующей последовательности на β-нитях Т-клеток, взаимодействующих с основным протеином миелина и вызывающих патогенез у экспериментального аллергического энцефаломиелита, представляющего собой модель рассеянного склероза у животных. Данная линия является специфической для другого эпитопа основного протеина миелина. Это открытие показывает, что взаимодействующие с основным протеином миелина Т-клетки участвуют в патогенезе рассеянного склероза и что рецепторные пептиды, подобные описанным для профилактики экспериментального аллергического энцефаломиелита, можно использовать для лечения рассеянного склероза.
Ревматоидный артрит
Ревматоидный артрит является аутоиммунной болезнью, опосредованной Т-клетками. Изобретение описывает олигоклональные инфильтраты активированных Т-клеток, содержащих Vβ17, в синовиальный слой больных ревматоидным артритом. Наличие данных Т-клеток в больной ткани всех осмотренных больных, их олигоклональность и цитотоксическая активность одной из этих Т-клеток для синовиальных присоединенных клеток показывают центральную роль содержащих Vβ17 T-клеток в патогенезе ревматоидного артрита.
Активированные популяции Т-клеток в синовиальной ткани больных ревматоидным артритом исследовали путем анализа мРНК рецепторов Т-клеток, выделенных из синовиальных Т-клеток, положительных относительно рецептора IL-2 (IL-2R+). мРНК рецепторов Т-клеток амплифицировали известным образом путем цепной реакции с помощью полимеразы (PCR). В этом анализе выявилось, что олигоклональные Vβ17 перегруппировки обогащены в популяции IL2-R+, что указывает на вероятность участия содержащих Vβ17 Т-клеток в патогенезе ревматоидного артрита. Из пробы синовиальной ткани выделяли клон Т-клетки, содержащий CD4+, Vβ17 и тот факт, что он обладает цитотоксичностью in vitro относительно синовиальных присоединенных клеток, подтверждает непосредственное участие содержащих Vβ17 Т-клеток в ревматоидном артрите.
Как уже указывалось, настоящее изобретение содержит чрезвычайно важное открытие, заключающееся в том, что специфический вариабельный участок β-нити рецептора Т-клеток, обозначаемый как Vβ17, тесно связан с ревматоидным артритом у человека. Данное открытие делает возможными обнаружение, профилактику и лечение ревматоидного артрита с использованием описанного в данном изобретении способа. Специалист будет способен применять в отношении ревматоидного артрита терапевтические методы, подобные описанным выше в связи с экспериментальным аллергическим энцефаломиелитом методам.
Таким образом, вторым объектом изобретения является способ диагностирования или прогнозирования восприимчивости к ревматоидному артриту или рассеянному склерозу индивидуума. В случае ревматоидного артрита способ включает обнаружение Т-клеток, содержащих обозначаемый как Vβ17 вариабельный участок β-нити в пробе индивидуума, причем наличие анормального количества содержащих Vβ17 Т-клеток указывает на ревматоидный артрит или восприимчивость к ревматоидному артриту. Содержащую Vβ17 Т-клетку можно качественно или количественно сравнивать с клеткой нормального индивидуума. Такое диагностирование можно осуществлять путем обнаружения части Vβ17, которая не имеется на вариабельном участке β-нити рецепторов Т-клеток, не связанных с ревматоидным артритом. Vβ17 можно обнаруживать, напр., путем приведения Vβ17 в контакт с детекторным лигандом, способным к специфическому связыванию с Vβ17. Известны многочисленные детекторные лиганды, напр., связанное с ферментом антитело. Вместо этого для обнаружения содержащих Vβ17 Т-клеток также можно использовать нуклеотидные пробы, комплементарные с кодирующими Vβ17 последовательностями нуклеиновых кислот (см. пример IX).
В случае диагностирования или прогнозирования восприимчивости к рассеянному склерозу предлагаемый способ включает обнаружение в пробе индивидуума Т-клеток, имеющих в основном последовательность SGDQGGNE, причем наличие данной последовательности указывает на рассеянный склероз или восприимчивость к рассеянному склерозу. Последовательность можно обнаруживать, напр., путем приведения в контакт с детекторным лигандом. Известны многочисленные детекторные лиганды, напр. связанное с ферментом антитело. Вместо этого для обнаружении Т-клеток также можно использовать нуклеотидные пробы, комплементарные с кодирующей последовательностью нуклеиновой кислоте (см. пример IX).
Третьим объектом изобретения является способ профилактики или лечения ревматоидного артрита или рассеянного склероза. В случае ревматоидного артрита способ включает предотвращение связывания содержащей Vβ17 Т-клетки с ее партнером. Согласно одной форме выполнения изобретения связывание предотвращается путем связывания лиганда с Vβ17. Согласно другой форме выполнения изобретения связывание предотвращается путем связывания лиганда с партнером Vβ17. Связывание можно предотвращать известными методами, напр. путем связывания антитела с Vβ17 или связывающей частью для физического блокирования связывания.
Согласно другой возможности выполнения изобретения профилактику или лечение ревматоидного артрита можно также осуществлять путем цитотоксической или цитостатической обработки содержащих Vβ17 Т-клеток в индивидууме. Согласно одному варианту содержащие Vβ17 Т-клетки обрабатывают цитотоксическим или цитостатическим агентом, избирательно связывающим Vβ17. Агент может представлять собой радиоактивное или хемотерапевтическое вещество. Такое связывание и пригодные для этой цели агенты широко известны (см., напр., Харлоу Э. и Лейн Antibodies, a Laboratory Manual, Коульд спринг Харбор Лэборатори, 1988 г.).
В случае профилактики или лечения рассеянного склероза способ включает предотвращение связывания содержащей в основном последовательность SGDQGGNE Т-клетки с ее партнером. Согласно одной форме выполнения изобретения связывание предотвращается путем связывания лиганда с последовательностью. Согласно другой форме выполнения изобретения связывание предотвращается путем связывания лиганда с партнером. Связывание можно предотвращать известными методами, напр. путем связывания антитела с последовательностью для физического блокирования связывания.
Согласно другой возможности профилактику или лечение рассеянного склероза можно осуществлять путем цитотоксической или цитостатической обработки содержащих в основном последовательность SGDQGGNE Т-клеток в индивидууме. Согласно одному варианту Т-клетки обрабатывают цитотоксическим или цитостатическим агентом, избирательно связывающим последовательность. Агент может представлять собой радиоактивное или хемотерапевтическое вещество.
Четвертым объектом настоящего изобретения является способ выделения вакцины для лечения опосредованной Т-клетками патологии, включающий получение клонов Т-клеток, вызывающих данное состояние, определение последовательности аминокислот рецепторов Т-клеток клонов Т-клеток, связанных с данным состоянием, отбор сегментов данных рецепторов Т-клеток, характерных для упомянутых рецепторов Т-клеток, а не для рецепторов Т-клеток, не связанных с данным состоянием, и отбор из упомянутых последовательностей тех последовательностей, которые способны к индукции иммуногенной реакции относительно упомянутого рецептора Т-клеток, таким образом отбирая вакцину.
Пятым объектом настоящего изобретения является содержащий последовательность SGDQGGNE пептид, являющийся агентом для обнаружения, профилактики или лечения рассеянного склероза.
Шестым объектом изобретения является способ согласно пп. 25-27 формулы изобретения.
Изобретение поясняется нижеследующими примерами.
Пример I
Экспериментальный аллергический энцефаломиелит на крысах
Крыс-самок разновидности Льюиса (Чарлз Ривер Лабораториз, Ралей-Дэрхам, США) иммунизировали подачей в лапу каждой задней ноги 50 мкл основного протеина миелина морской свинки в виде эмульсии в полном стимуляторе Фрейнда. Первые симптомы болезни обычно обнаруживали за 9-11 дней после иммунизации. Степень болезни оценивали с помощью шкалы с тремя разделами: 1 - хромой хвост, 2 - слабость задних ног, 3 - паралич задних ног. После продолжительности болезни примерно 4 - 6 дней большинство крыс спонтанно выздоровело и было резистентным к последующему вызыванию экспериментального аллергического энцефаломиелита.
Пример II
Выделение вакцины
Вакцинации осуществляли пептидом рецептора Т-клеток, последовательность которого вывели из последовательности ДНК бета-гена рецептора Т-клеток, преобладающем среди вызывающих экспериментальный аллергический энцефаломиелит Т-клеток мышей разновидности B10.PL/L. Последовательность ДНК соответствует указаниям Урбана и др. (см. выше). Пептид, содержащий девять аминокислот и имеющий последовательность VDJ β-нити рецептора Т-клеток из мыши, синтезировали известным методом. Последовательность данного пептида следующая: SGDAGGGYE. Соответствующая последовательность в крысах гласит: SSD-SSNTE (Бэрнс и др., J. Exp. Med., N 169, стр. 27 - 39, 1989 г.). Пептид обессоливали путем колоночной хроматографии на колонне на Сефадекс Г-25 (Фармасия Фаин Кемикэлс, Пискатавей, Нью Джерсей, США) с использованием в качестве элюента 0,1 М уксусной кислоты, и растворитель затем удаляли лиофилизацией в двух циклах. Часть пептида с помощью глутаральдегида конъюгировали с выделенным из блюдечка гемоцианином (LH) в соотношении 7,5 мг пептида на мг гемоцианина. Конъюгат подвергали диализу с применением солевого фосфатного буфера (РВС).
Пример III
Вакцинация против экспериментального аллергического энцефаломиелита
Используемые в данных опытах вакцины состоят из свободного пептида с VDJ-участком, а также из пептида с VDJ-участком, конъюгированного с выделенным из блюдечка гемоцианином. Их разбавляли в солевом фосфатном буфере и эмульгировали равными частями или (1) неполного стимулятора Фрейнда или (2) полного стимулятора Фрейнда, полученного путем суспендирования 10 мг/мл убитых термообработкой высушенных Mycobacterium tuberculosis H37ra (Дифко Лабораториз, Дитройт, США) в неполном стимуляторе Фрейнда. Эмульсии дали крысам-самкам разновидности Льюиса возрастом 8 - 12 недель в общем количестве 100 мкл на животное (50 мкл в лапу каждой задней ноги). Каждой крысе дали 5 мкг неконъюгированного VDJ пептида. Конъюгат выделенного из блюдечка гемоцианина и VDJ дали в количестве, соответствующем 10 мкг выделенного из блюдечка гемоцианина на животное. За 29 дней после этого каждой крысе дали 50 мкг основного протеина миелина морской свинки в полном стимуляторе Фрейнда в передние лапы. Животных наблюдали каждый день, начиная с 9-го дня, чтобы обнаруживать клинические симптомы экспериментального аллергического энцефаломиелита, и их оценивали вышеописанным образом. Результаты опыта приведены в таблице I (см. в конце описания). Они показывают не только то, что у вакцинированных животных болезнь выявилась меньше, но и то, что в заболевших животных болезнь протекала менее тяжело и/или ее начало было замедлено. Степени защиты были разными, как и составы вакцин, причем вакцины, содержащие полный стимулятор Фрейнда, показывали наибольшую степень защиты.
Пример IV
Вакцинация против экспериментального аллергического энцефаломиелита с VDJ пептидами, полученными из крыс разновидности Льюиса
VDJ пептид, используемый в предыдущих примерах, синтезировали согласно последовательности молекул в β-цепи рецептора Т-клеток, найденной в вызывающих экспериментальный аллергический энцефаломиелит Т-клетках мышей разновидности B10.PL. Данные VDJ последовательности являются гомологичными, а не идентичными, с последовательностями, найденными в Т-клетках мышей разновидности B10. PL. Пептиды крыс синтезировали согласно последовательностям ДНК, названным Бэрнсом и др. и Клуба и др. (Eur. J. Immunol., N 19, стр. 279 - 284, 1989 г. ). Последовательности данных трех пептидов, обозначаемые как IR1, IR2 и IR3, приведены ниже, вместе с последовательностью мыши разновидности B10.PL, использованной в примерах I и III (VDJ).

Получение, дачу и оценку данных вакцин осуществляли описанным в примерах I - III образом, за следующими исключениями. В составах вакцин, содержащих полный стимулятор Фрейнда, использовали 50 мкг отдельных VDJ пептидов; не использовали ни вакцины в неполном стимуляторе Фрейнда, ни вакцины, содержащие конъюгированные с выделенным из блюдечка гемоцианином (LH). Контрольным животным перед подачей основного протеина миелина (МБР) ничего не дали или их вакцинировали эмульсией солевого фосфатного раствора (PBS) и полного стимулятора Фрейнда (CFA) с тем, чтобы оценивать защитное действие одного адъюванта. Результаты приведены в табл. II (см. в конце описания).
Приведенные в таблице II результаты показывают, что в невакцинированных контрольных животных обнаружили болезнь уже в 10-ый день. Болезнь проявилась в тяжелом параличе и ослаблении, продолжалась в течение 4 - 6 дней и затем спонтанно прекратилась. У крыс, вакцинированных PBS-CFA, болезнь протекала в основном таким же образом, как и в невакцинированных контрольных животных. В отличие от этого на некоторых животных, вакцинированных IR1, IR2 и IR3, обнаруживали замедленное начало, а на других - и замедленное начало, и уменьшенную интенсивность и/или продолжительность болезни. Однако в общем вакцинация VDJ пептидами крыс (IR1-3) была немного менее эффективной, чем вакцинация VDJ пептидом мыши (см. пример III). Однако вакцинация IR9b привела к полной защите во всех четырех животных, на которых его исследовали. Важное значение имеет тот факт, что ни в одном из четырех животных, вакцинированных IR9b, не обнаруживали ни одного гистологического изменения, характерного для болезни, что указывает на то, что были предотвращены также субклинические симптомы болезни.
Пример V
Вакцинация пептидами, специфическими относительно вариабельного участка
Специфический для семейства Vβ8 генов пептид исследовали в качестве вакцины против экспериментального аллергического энцефаломиелита. Vβ8 является наиболее распространенным семейством β-нити, и он используется в энцефалитогенных Т-клетках крыс и мышей. Пептид синтезировали согласно уникальной последовательности ДНК, которую нашли в гене Vβ8 , а не в других генах крысы, последовательности которых приведены у Морриса и др. (Immunogenetics, N 27, стр. 174 - 179, 1988 г.). Последовательность данного Vβ8 пептида, обозначаемого как IR7, следующая:
IR7 DMGHGLRLIHYSYDVNSTEК.
Эффективность данного пептида исследовали в экспериментальном аллергическом энцефаломиелите на крыс (пример I) описанным в примерах II и III образом. 50 мкг пептида исследовали с полном стимуляторе Фрейнда (CFA). Вакцинацию с неполным стимулятором Фрейнда (IFA) или с конъюгатом пептида с выделенным из блюдечка гемоцианином (IFA) не осуществляли. Результаты данных опытов приведены в табл. III (см. в конце описания).
Результат вакцинаций, осуществляемых 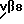 пептидом крысы, похож на результаты вакцинаций IR1, IR2 и IRS пептидами мышей и крыс. На одном животном обнаруживали уменьшенную интенсивность и продолжительность болезни, а одно животное защищалось полностью.
пептидом крысы, похож на результаты вакцинаций IR1, IR2 и IRS пептидами мышей и крыс. На одном животном обнаруживали уменьшенную интенсивность и продолжительность болезни, а одно животное защищалось полностью.
Пример VI
Вакцинация содержащими J-участки пептидами
Пептид синтезировали согласно сегменту J на α-нити, ТА39, нашли среди рецепторов энцефалитогенных Т-клеток и в крысах, и в мышах. Последовательность данного пептида, обозначаемого как IR5, следующая:
IR5 RFGAGTRLTVX.
Эффективность JαTA39 пептида исследовали в экспериментальном аллергическом энцефаломиелите на крыс разновидности Льюиса (пример I) описанным в примерах II и III образом. 50 мкг пептида исследовали в полном стимуляторе Фрейнда (CFA). Вакцинацию с неполным стимулятором Фрейнда (IFA) или с конъюгатом пептида с выделенным из блюдечка гемоцианином (IFA) не осуществляли. Результаты данных опытов приведены в табл. IV (см. в конце описания).
Результаты вакцинации JαТА39 пептидом крысы являются более эффективными, чем результаты вакцинации VDJ пептидом мыши или Vβ8 пептидом. Два из трех животных полностью защищались, а в третьем животном начало болезни было значительно замедлено. Кроме того, в этом животном интенсивность болезни также была снижена, несмотря на то, что болезнь имела нормальную продолжительность 5 дней. Важное значение имеет тот факт, что на обоих полностью защищенных животных не обнаруживали ни одного гистологического симптома инфильтрации Т-клеток в центральную нервную систему. Этот результат показывает, что вакцинация JαTA39 очень эффективно вызывает регулятивную реакцию, нацеленную на энцефалитогенные Т-клетки. Даже не обнаруживалось субклинических симптомов болезни.
Пример VII
Вакцинация смесями пептидов рецепторов Т-клеток
Вакцинации осуществляли со смесью пептидов рецептора Т-клеток. Данная смесь содержала по 50 мкг пептидов IR1, IR2 и IR3 (VDJ пептидами трех крыс и пептидом JαТА39 крысы).
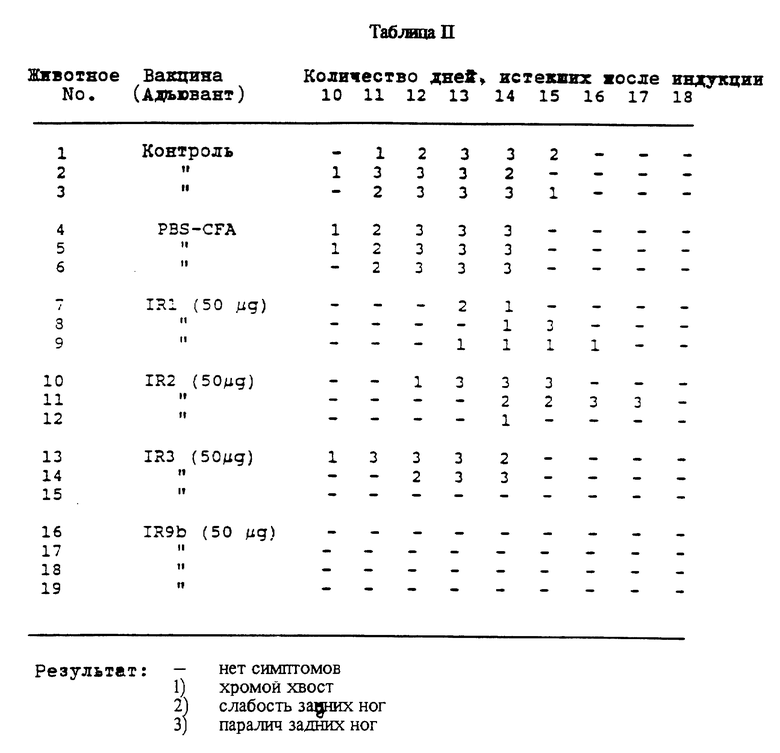
Эффективность данной смеси пептидов исследовали в экспериментальном аллергическом энцефаломиелите на крыс разновидности Льюиса (пример I) описанным в примерах II и III образом. Пептиды исследовали в полном стимуляторе Фрейнда (CFA). Вакцинацию с неполным стимулятором Фрейнда (IFA) или с конъюгатом пептида с выделенным из блюдечка гемоцианином (IFA) не осуществляли. Результаты данных опытов приведены в табл. V (см. в конце описания).
Результаты вакцинаций, осуществленных с использованием JαТА39 пептидом крысы и тремя VDJ пептидами, являются почти столь эффективными, сколь результаты вакцинации IR9b, приведенные в таблице II. Все три животных полностью защищались. Наряду с отсутствием клинических симптомов экспериментального аллергического энцефаломиелита два из трех животных были полностью свободными от гистологических симптомов инфильтрации Т-клеток в центральную нервную систему, причем на третьем наблюдали лишь два маленьких очага лимфоцитарной инфильтрации на основании спинного мозга.
Пример VIII
Вакцина против рассеянного склероза
Взаимодействующие с основным протеином миелина Т-клетки человека
Линии взаимодействующих с основным протеином миелина Т-клеток человека получили из периферийных одноядерных клеток крови (РВМС) девяти больных хроническим прогрессирующим рассеянным склерозом и двух здоровых контрольных людей. Клетки в течение 3 дней держали в культуре при регулярной стимуляции очищенного основного протеина миелина человека и облученной аутологическими периферийными одноядерными клетками крови, а затем в течение 4 дней в содержащей IL-2 среде.
Амплификация путем цепной реакции с помощью полимеразы (PCR) генов β-нити рецептора Т-клеток из линий взаимодействующих с основным протеином миелина Т-клеток
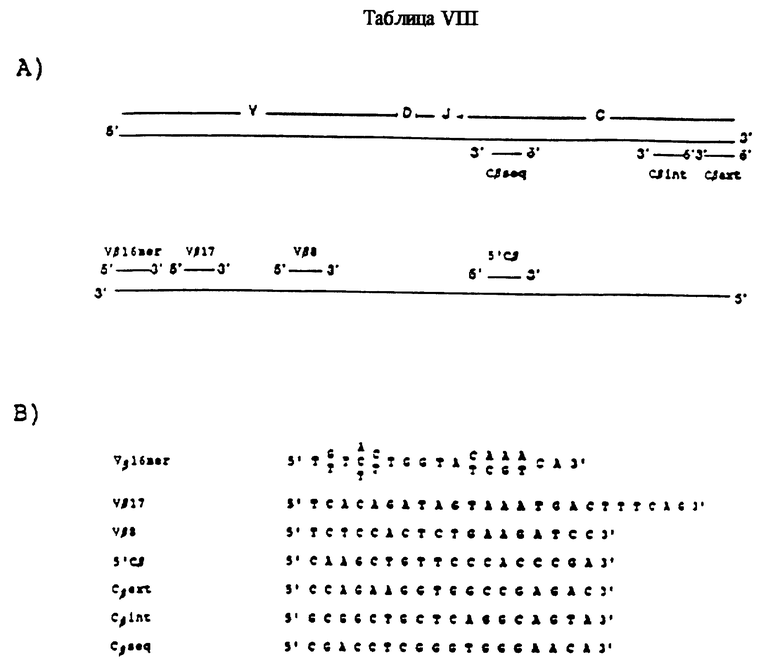
Т-клетки выделяли из культур, получаемых после логарифмической фазы роста, и получили РНК, амплифицированную Vβ16-мерным примером и примером Cβ для осуществления 55 циклов согласно примеру IX.
Последовательности β-нитей рецептора Т-клеток человека, взаимодействующих с основным протеином миелина
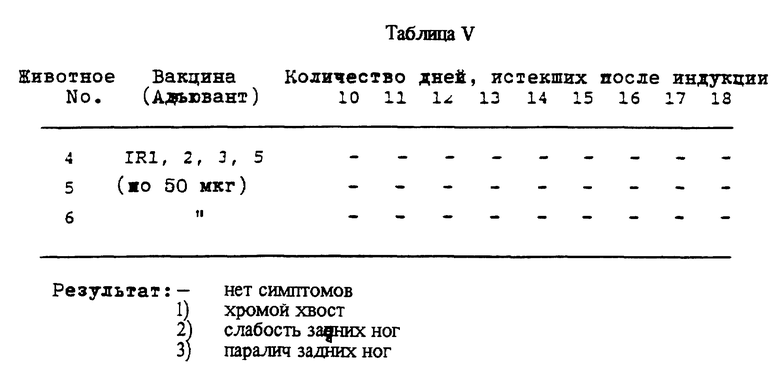
С использованием примера Cβseq определяли последовательность амплифицированных Vβ16-мером генов β-нити рецептора линий Т-клеток человека, взаимодействующих с основным протеином миелина. Продукт амплификации очищали с помощью геля, денатурировали основания и с помощью примера Cβseq определяли его последовательности. Из пяти линий получили способные к считыванию последовательности ДНК, которые показывали, что доминирующие клоны Т-клеток получили путем длительного переноса in vitro. Одна из данных последовательностей, из клеточной линии Re (см. табл. VI в конце описания), имела VDJ последовательность аминокислот β-нити, в которой пять из первых шести и шесть из девяти в общем остатков идентичны с соответствующими остатками VDJ последовательности аминокислот β-нити, сохраняемых в энцефалогенных Т-клетках, взаимодействующих с основным протеином миелина, в экспериментальном аллергическом энцефаломиелите на мышах разновидности B10.PL. Данная последовательность не имелась в численно преобладающих перегруппировках рецептора Т-клеток, найденных в остальных четырех линиях Т-клеток человека, взаимодействующих с основным протеином миелина.
Для выяснения возможного наличия похожих последовательностей в β-нитях линий Т-клеток, взаимодействующих с основным протеином миелина, других больных рассеянным склерозом осуществляли амплификацию PCR с дегенерированным (n = 1024) 21-нуклеотидным примером (VβRe), соответствующим семи аминокислотам данной последовательности (см. таблицу VI). Осуществляли обратную транскрипцию РНК, которые Vβ16-мерным примером и примером Cβext амплифицировали реакцией в 20 циклах (стадия I). 1 мкл аликвотной пробы продукта данных реакций стадии I реамплифицировали в 35 циклах примерами VβRe и Cβint. 1 мкл аликвотной пробы продукта данных реакций исследовали путем гибридизации по Саутерну маркированной 32P пробы Cβ человека. Данное исследование показало амплифицированный продукт с 300 п.о. в клеточной линии Re и в линии одного другого больного рассеянным склерозом, но не в Т-клетках, взаимодействующих с основным протеином миелина, контрольных индивидуумов или линиях и клонах не взаимодействующих с основным протеином миелина Т-клетках человека. Наличие данной последовательности в двух из девяти исследованных линий клеток больных рассеянным склерозом имеет важное значение. Т.к. данная последовательность, как известно, сохраняется среди энцефалогенных Т-клеток при экспериментальном аллергическом энцефаломиелите, ее обнаружение в Т-клетках, взаимодействующих с основным протеином миелина, больных рассеянным склерозом показывает, что имеющие этот детерминант Т-клетки играют некоторую роль в патогенезе рассеянного склероза.
Иммуногенные пептиды, имеющие последовательность SGDQGGNE, можно получить путем синтеза описанным в примере II образом, и их можно использовать для иммунизации людей описанным в примере III методом. Такая иммунизация может приводить к эффективной иммунной реакции.
Пример IX
Выделение олигоклональных инфильтратов II активированных Т-клеток, содержащих Vβ17, в синовии больных ревматоидным артритом
Получение Т-клеток из синовиальной ткани
Пробы синовиальной ткани получили из больных, на которых ревматоидный артрит подтверждался радиографией и которых лечили протезированием суставов. С использованием магнитных жемчужин и антител, взаимодействующих с IL2-R (α IL2-R) человека, следующим образом получили активированные Т-клетки. Синовиальную ткань переваривали при температуре 37oC в течение 4 ч в среде RPMI с 10% сыворотки плода коровы (FBS), содержащей 4 мг/мл коллагеназы (Вортингтон Биокемикэл, Фрихольд, Нью Джерсей, США) и 0,15 мг/мл ДНКазы (Зигма, Ст. Луис, США). Продукт переваривания подали через 80-меш сито, и отдельные клетки собрали путем центрифугирования в градиенте плотности согласно Фиколлу. Клетки на поверхности раздела промывали и инкубировали в солевом фосфатном буфере (PBS), содержащем 2% FBS (PBS-FBS), 5 мкг/мл иммуноглобулина IgG контрольных мышей (Соултер Иммунолоджи, Хайали, Флорида, США) в концентрации 106/мл при температуре 0oC в течение 30 минут. Клетки три раза промывали и инкубировали с магнитными шариками, конъюгированными с анти-мышинным IgG козы (Адвансд Магнетикс, Кембридж, Массачюсетс, США). Шарики магнитно отделяли, и их трижды промывали PBS-FBS. Данный предварительный отбор с помощью IgG мыши (mIgG) и магнитными шариками использовали для контроля не- специфической адсорбции Т-клеток. Оставшиеся в исходной суспензии клетки дополнительно инкубировали с 5 мкг/мл моноклонального IgG мыши, взаимодействующего с IL2-R Т-клетки человека при температуре 0oC в течение 30 минут (Коултер Иммунолоджи, Хайали, Флорида, США). Клетки промывали и отбирали вышеописанным образом с помощью магнитных шариков. Шарики предварительной адсорбции IgG и отобранные антитела IL2-R сразу же ресуспендировали в подкисленной смеси гуанидиния, фенола и хлороформа и РНК, полученной согласно Хонецынски и Саки (Anal. Biochem. N 162, стр. 156, 1987 г). Т.к. РНК получили без культивации клеток in vitro и возможно вызванного отклонения, они должны точно отражать количество Т-клеток в синовиальной ткани в момент ее оперативного удаления. Лишь половина mIgG и шариков с α IL2-R больного 1012 сразу же обрабатывали для получения РНК. Остальную часть культивировали в среде RPMI 1640 с 5% FBS, 20% HL-1 (Вентрекс Лабораториз Инк. , Портлэнд, США), 25 мМ HEPES, глутамином, антибиотиками и в качестве источника IL-2 20% надосадочной жидкости LAK (Аллегретта и др., Science, N 247, стр. 718, 1990 г.) в течение 5 дней. РНК экстрагировали из культур шариков αIL2-R (1012IL2.d5), а не из пробы 1012mIgG, т.к. не имелось жизнеспособных клеток в конце 5-дневной культивации.
Клон Т-клетки выделяли из центрифугата из больного 1008. Имеющиеся в центрифугате клетки культивировали с концентрацией 2 • 106/мл в среде, не содержащей IL-2, в течение двух недель. Неприсоединенные клетки данной культуры клонировали с использованием метода лимитирующего разбавления на аутологические монослои синовиальных клеток. Получили клон 1008.8 CD4+ клетки, который приспосабливали к культивации путем регулярной стимуляции аутологическими синовиальными монослоями в течение 3 дней в среде, не содержащей IL-2, а затем культивировали в течение 4 дней в среде, содержащей надосадочную жидкость LAK.
Лизис синовиальных присоединенных к 1008.8 клеток
Лизис синовиальных присоединенных клеток 1008.8 демонстрировали следующим образом. Монослои синовиальных слоев маркировали согласно Стэдмэн и Кэмпбелл (J. Immunol Meth.., N 119, стр. 219, 1989 г.) с помощью 35S в качестве маркера в опытах CTL. Клетки обрабатывали трипсином, промывали и нанесли на круглодонную микротитровую пластину с 96 углублениями, причем в каждое углубление подали 2000 клеток. Клетки 1008.8, культивированные за 3 дня до исследования вместе с синовиальными присоединенными клетками и содержащей надосадочную жидкость средой, добавляли к маркерам с нижеприведенным соотношением эффекторов и маркеров. Культуры инкубировали при температуре 37oC в течение ночи, их центрифугировали при 300 • g в течение 2 минут и определяли радиоактивность в 50 мкл надосадочной жидкости. Специфический лизис высчитывали с помощью известных формул на основе лизированных в поверхностно-активном веществе маркеров. Данный клон является цитотоксическим относительно синовиальных присоединенных клеток в опытах CTL (см. табл. VII в конце описания).
Амплификация генов β-нити рецептора Т-клеток путем цепной реакции с помощью полимеразы
Гены β-нити рецептора Т-клеток амплифицировали с помощью примеров в разных комбинациях, приведенных в табл. VIII (см. в конце описания). Vβ16-мерный пример является дегенерированным Vβ примером (n = 256), который предположительно связывается с 85% генов β-нити рецептора Т-клеток человека на всех 16 остатках и с 95% на 15 остатках. Данный пример использовали для амплификации β-нитей рецептора Т-клеток более 25 разных клонов, линий или препаратов первичной ткани человека. Определяли продолжительность многих разных генов Vβ данных амплифицированных ДНК, несмотря на значительное отклонение примера относительно некоторых групп Vβ. Таким образом, амплификация PCR с использованием Vβ16-мерного примера облегчает исследование популяций Т-клеток, использование генов Vβ которых специалисту неизвестно.
Гены β-нити рецептора Т-клеток амплифицировали путем двухстадийных реакций с парами примеров, приведенными в таблице VIII. РНК подвергали обратной транскрипции при температуре 42oC 40 пмоль с использованием Cβext примера в 12 мгл в условиях, описанных Хартом и др., The Lancet, стр. 596 (1988). Продукт реакций разбавляли смесью, содержащей 40 пмоль Vβ16-мерного примера, нуклеотиды и буфер, как выше описано, но без MgCl2 с тем, чтобы достичь конечной концентрации 3,6 мМ. Пробы денатурировали при температуре 95oC в течение 15 минут, добавляли 1 единицу теплостойкой рекомбинантной ДНК полимеразы (фирмы Ситэс Корпорейшн, Эмеривилль, Калифорния, США, название: АмплитакTM) и осуществляли 20 циклов PCR. Каждый цикл состоял из денатурации при температуре 95oС в течение 1 минуты, ренатурации в течение 2 минут и распространения при температуре 72oC в течение 2 минут. Продукт первых двух циклов ренатурировали при температуре 37oC и 45oC, а остаток - при температуре 50oС. Один мкг аликвотной пробы результата данных реакций I стадии добавляли к 100 мкг амплифицирующей стадии II (см. Ситус, Gene Amp, KitIM), содержащей 100 пмоль Cβint примера и 100 пмоль примеров Vβ8,Vβ17 или 5′Cβ или 100 пмоль примеров Vβ мерный пример. Амплификацию стадии II осуществляли вышеописанным образом при температуре ренатурации 50oC и без обработки при температуре 37oC и 45oC.
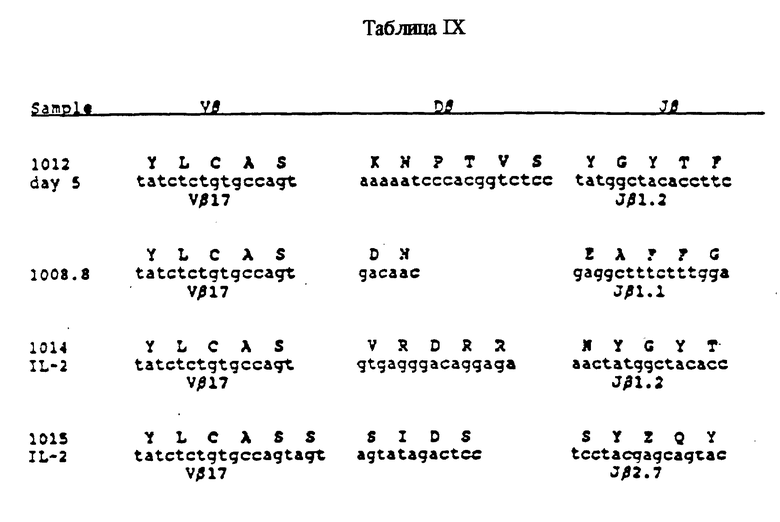
Пробы РНК из культур 1012IL2. d5 и 1008.8 амплифицировали с помощью Vβ16-мерного примера и примера Cβext в реакциях стадии I и с помощью Vβ16-мерного примера и примера Cβint в реакциях в 35 циклах стадии II. Продукт реакций с помощью стеклянных шариков (Биолол, Сан Дьего, Калифорния, США) очищали от агарозного геля с низкой точкой плавления, его основания денатуризировали, и его последовательность определяли Т7 полимеразой (Секвенейз, Юнайтед Стейтс Байохем, Кливлэнд, Охайо, США) с использованием Cβseq примера. Численно преобладающая последовательность Vβ, соответствующая отдельной перегруппировке Vβ17 (см. таблицу IX), в пробе 1012IL2.d5 легко подавалась считыванию. Другие, менее распространенные перегруппировки являлись слабыми, не поддающимися считыванию фоновыми полосами в гелях, служащих для определения последовательности. По всей вероятности культура данных 1012.IL2 шариков в содержащей IL2 среде без добавления дополнительных клеток или антигена не приводит к повторной активации Т-клеток. Таким образом, преобладание одной единственной перегруппировки Vβ17 в данной пробе отражает клональную экспансию in vivo содержащих Vβ17 Т-клеток в этом больном. Определение последовательности ДНК β-нити рецептора Т-клеток, амплифицированной с применением цитотоксического клона Т-клеток, 1008.8, также указывает на перегруппировку Vβ17 (см. табл. IX в конце описания). Наличие данных двух видов проб синовиальных Т-клеток, полученных из двух больных ревматоидным артритом, предполагает участие содержащих Vβ17 Т-клеток в патогенезе ревматоидного артрита.
Наличие перегруппировок Vβ17 в остальных пробах синовиальной РНК определяли путем амплификации путем PCR с применением специфического относительно Vβ17 примера (см. таблицу VIII). ДНК содержащего Vβ17 рецептора Т-клеток амплифицировали с применением проб на магнитных шариках, полученных из семи больных ревматоидным артритом. С помощью обработки продуктов электорфореза бромидом этидия обнаруживали большую амплификацию Vβ17 в четырех из проб, содержащих αIL2-R, чем в соответствующих контрольных пробах, содержащих mIgG. Данное обогащение являлось результатом не процесса выделения, т. к. при амплификации содержащих Vβ8 рецепторов Т-клеток не обнаруживалась разница между пробами, содержащими mIgG, и пробами, содержащими IL2-R.
Перегруппировки Vβ17 двух из препаратов, содержащих РНК αIL2-R, амплифицировали примерами Vβ17 и Cβint, а последовательность продукта реакций определяли с использованием примера Cβseq. Пробы 1014 и 1015 содержали отдельные последовательности (см. таблицу IX), которые, также как и проба 1012IL2. d5, указывают на клональную экспансию содержащих Vβ17 Т-клеток in vivo. В отличие от этого, непосредственное определение последовательности перегруппировок, амплифицированных с помощью специфического относительно Vβ8 примера, было невозможным из-за значительной разнородности β -нити продукта.
Vβ17 имеет последовательность аминокислот MSNQVLCCVVLCFLGANTVDGGI- TQSPKYLFRKEGQNVTLSCEQNLNHDAMYWYRQDPGQGLRLIYYSQIVNDFQ- KGDIAEGYSVSREKKESFPLTVTSAQKNPTAFYLCASS.
HLA-DR-анализ ДНК больных ревматоидным артритом
HLA-DR-анализ ДНК больных ревматоидным артритом осуществляли следующим образом. ДНК из каждого больного препарировали путем кипения 105 синовиальных клеток в 200 мкл dH2O. 10 мкл амплифицировали в 35 циклах в 100 мкл среды (Ситус, Джин Амп КитИМ), содержащей 100 пмоль каждого примера для осуществления цепной реакции DRβ при помощи полимеразы (см. таблицу X). 1/10 мкл данной среды реамплифицировали в 10 циклах в 10 мкл, содержащих лишь пример DRβ2 и 17 пмоль α32P-dCTP в качестве единственного источника dCTP. Добавляли 200 мкМ dCTP и осуществляли 2 цикла. Получаемые пробы (отрицательный тяж) в условиях, описанных Амором и др. (J. Immunol., N 138, стр. 1947, 1987 г.), гибридизировали с получением следов, содержащих 10 пмоль HLA-DR аллель-специфических олиго (положительные тяжи). Следы два раза промывали хлоридом тетраметиламмония (Вуд и др., Proc. Natl. Acad. Sd USA, N 82, стр. 1585, 1985 г.) при температуре 65 - 68oC в течение 20 минут, и затем их обрабатывали рентгеновскими лучами.
Каждый больной в данном анализе имел по крайней мере один аллель генов HLA-DR, а именно DR4w4, DR1, DR4w14 или DR4w15, известные как вызывающие восприимчивость к ревматоидному артриту факторы (см. таблицу X в конце описания).
Содержащие Vβ17 рецепторы Т-клеток или их фрагменты, которые являются иммуногенными или которым можно придавать иммуногенность, можно использовать для иммунизации людей с помощью способов, описанных в примере VII. Такая иммунизация может привести к эффективной иммунной реакции.
Хотя в данном тексте изобретение описано на одном предпочтительном примере его выполнения, следует указать на то, что возможны разные модификации без выхода за рамки изобретательского замысла. Поэтому изобретение не ограничивается раскрытым в тексте описанием, а лишь формулой изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| Т-КЛЕТОЧНАЯ ВАКЦИНА ДЛЯ ЛЕЧЕНИЯ РАССЕЯННОГО СКЛЕРОЗА | 1998 |
|
RU2209633C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИКЛОНАЛЬНОЙ Т-КЛЕТОЧНОЙ ВАКЦИНЫ ДЛЯ ЛЕЧЕНИЯ ИММУНОЛОГИЧЕСКИХ РАССТРОЙСТВ | 2004 |
|
RU2277422C2 |
| ПЕПТИД ИЗ СОСТАВА ТЯЖЕЛОЙ ЦЕПИ ИММУНОГЛОБУЛИНА ЧЕЛОВЕКА, ПРИГОДНЫЙ ДЛЯ ЛЕЧЕНИЯ РАССЕЯННОГО СКЛЕРОЗА | 2016 |
|
RU2646817C1 |
| МАТЕРИАЛЫ И СПОСОБЫ, ОТНОСЯЩИЕСЯ К АУТОЛОГИЧНЫМ Т-КЛЕТОЧНЫМ ВАКЦИНАМ | 2002 |
|
RU2302257C2 |
| ВЫДЕЛЕНИЕ И ИДЕНТИФИКАЦИЯ Т-КЛЕТОК | 2003 |
|
RU2327487C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ РАССЕЯННОГО СКЛЕРОЗА | 1992 |
|
RU2121850C1 |
| КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ РАССЕЯННОГО СКЛЕРОЗА | 2008 |
|
RU2492234C2 |
| ПЕПТОИДНЫЕ ЛИГАНДЫ ДЛЯ ВЫДЕЛЕНИЯ И ОБРАБОТКИ АУТОИММУННЫХ Т-КЛЕТОК | 2010 |
|
RU2563822C2 |
| ЛЕЧЕНИЕ РАССЕЯННОГО СКЛЕРОЗА | 2010 |
|
RU2539034C2 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ РЕВМАТОИДНОГО АРТРИТА | 2010 |
|
RU2524152C2 |





Изобретение относится к медицине, в частности к иммунологии. Предложенная вакцина для профилактики или лечения опосредованной Т-клетками патологии или нерегулируемой репликации клонами Т-клеток в млекопитающих содержит активное вещество и фармацевтически переносимую среду, при этом в качестве активного вещества она содержит рецептор Т-клеток или его фрагмент, соответствующий рецептору Т-клеток, находящемуся на поверхности опосредующих данную патологию Т-клеток, или антиидиотипические антитела, являющиеся внутренним изображением данного рецептора или его упомянутого фрагмента, причем активное вещество взято в иммуногенно эффективном количестве. Ее готовят путем получения клонов Т-клеток, вызывающих опосредованную Т-клетками патологию, определения последовательности аминокислот рецепторов Т-клеток клонов Т-клеток, связанных с данной патологией, отбора сегментов данных рецепторов Т-клеток, характерных для упомянутых рецепторов Т-клеток, а не для рецепторов Т-клеток, не связанных с данной патологией, и отбора из упомянутых последовательностей тех последовательностей, которые способны к индукции иммуногенной реакции относительно упомянутого рецептора Т-клеток, таким образом отбирая вакцину. Также предложены способ диагностирования или прогнозирования восприимчивости индивидуума к ревматоидному артриту, который заключается в том, что он включает обнаружение Т-клеток, содержащих вариабельный участок β-нити MSNQVLCCVVLCFLGANTVDGGITQSPKYLFRKEGQNVTLSCEQNLNHDAMYWYRQDPGQGLRLIYYSQIVNDFQKGDIAEGYSVSREKKESFPLTVTSAQKNPTAFYLCASS или его фрагмент в пробе индивидуума, причем анормальная экспрессия Т-клеток, содержащих такой участок, указывает на ревматоидный артрит или восприимчивость к ревматоидному артриту, а также способ профилактики или лечения ревматоидного артрита, который заключается в том, что он включает предотвращение связывания рецептора Т-клеток, содержащего последовательность MSNQVLCCVVLCFLGANTVDGGITQSPKYLFRKEGQNVTLSCEQNLNHDAMYWYRQDPGQGLRLIYYSQIVNDFQKGDIAEGYSVSREKKESFPLTVTSAQKNPTAFYLCASS, или рецептора Т-клеток, содержащего в основном последовательность SGDQGGNE, с его партнером, и способ профилактики или лечения ревматоидного артрита в индивидууме, который заключается в том, что он включает цитотоксическую или цитостатическую обработку Т-клеток, MSNQVLCCVVLCFLGANTVDGGITQSPKYLFRKEGQNVTLSCEQNLNHDAMYWYRQDPGQGLRLIYYSQIVNDFQKGDIAEGYSVSREKKESFPLTVTSAQKNPTAFYLCASS, или Т-клеток, содержащих в основном последовательность SGDQGGNE в индивидууме. 5 с. и 16 з.п.ф-лы, 10 табл.
Приоритет по пунктам и признакам:
21.03.89 п. 1 в части активного вещества рецептора Т-клеток или его фрагмента, соответствующего рецептору Т-клеток, находящемуся на поверхности опосредующих ревматоидный артрит Т-клеток, пп.3, 4, 7, 9 - 13 также в части активного вещества, указанного в п.1;
18.07.89 п.1 в части активного вещества, касающегося антиидиотипических антител, являющихся внутренним изображением рецептора Т-клеток или его фрагмента, соответствующего рецептору Т-клеток, находящемуся на поверхности опосредующих ревматоидный артрит Т-клеток, пп.3, 4, 7, 9 - 12 в части указанного в п.1 активного вещества и п.8, относящийся к вакцине, содержащий в качестве активного вещества фрагмент рецептора Т-клеток.
| WO 8606413 A, 06.11.86 | |||
| ШИРОКОУГОЛЬНАЯ ТЕЛЕСКОПИЧЕСКАЯ ГАЛИЛЕЕВСКАЯ ОПТИЧЕСКАЯ СИСТЕМА | 0 |
|
SU175270A1 |
| US 4587222 A, 06.05.86 | |||
| Harlow E | |||
| fnd Lane Antibodies, A Laboratory Manual, Cald Spring Harbor Laboratory, 1988. | |||
Авторы
Даты
1999-09-27—Публикация
1990-03-21—Подача