Изобретение относится к области медицинской техники, в частности к средствам, предназначенным для очистки, дезинфекции, промывания и хранения контактных линз.
В настоящее время производят и выпускают на рынок для пользователей мягкие и жесткие контактные линзы. Как те, так и другие со временем загрязняются вследствие осаждения на них глазных выделений, белковых веществ, неорганических веществ, микроорганизмов.
Удаление имеющихся на контактных линзах загрязнений является необходимым условием при их использовании, так как позволяет предупредить возможные повреждения глаза.
В настоящее время известен целый ряд очищающих растворов для контактных линз, обеспечивающих различную степень очистки.
Требования, предъявляемые к таким растворам, достаточно высоки:
- отсутствие вредного воздействия на глаза и материал линзы,
- удаление загрязнений разного типа и происхождения,
- стабильность растворов,
- простота в использовании,
- универсальность (возможность использования для линз разного типа).
Известные в настоящее время композиции для обработки контактных линз состоят преимущественно из следующих компонентов - бактерицидный активный агент, поверхностно-активные вещества, консервант и физиологический раствор.
Композиция, описанная в (I), в качестве активного начала содержит бендазан, в качестве поверхностно-активных веществ - очистителей - гидроксиэтилцеллюлозу, поливиниловый спирт, октилфеноксиэтанол, полисорбат-80 или их смеси, в качестве консервантов - тиомерсал, хлоргексидин глюконат и натриевую соль этилендиаминотетрауксусной кислоты, которая кроме этого удаляет кальций, и изотонический физиологический раствор на основе хлорида натрия и боратной буферной системы.
Основным недостатком указанной композиции является необходимость использования тиомерсала. Все примеры конкретных композиций содержат тиомерсал или тиомерсал в сочетании с хлоргексидин глюконатом. Оба вещества являются высокотоксичными, тиомерсал содержит ртуть - 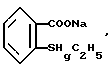 вызывает сильное раздражение слизистых оболочек глаз у пациентов. При длительном использовании композиций с тиомерсалом у многих пациентов развивается стойкая непереносимость этих компонентов.
вызывает сильное раздражение слизистых оболочек глаз у пациентов. При длительном использовании композиций с тиомерсалом у многих пациентов развивается стойкая непереносимость этих компонентов.
Что касается свойств бендазана, который, являясь активным началом, в соответствии с описанием устраняет седиментацию белков и увеличивает активность.
Известно, что эффективность активного начала и композиции в целом оценивается не только удалением белковых отложений, но и дезинфицирующими свойствами, т.е. антимикробной активностью.
Последнюю не представляется возможным оценить как в виду отсутствия каких-либо сведений в материалах описания к патенту, так и из-за неидентифицируемости структуры вещества, названного бандазаном, поскольку оно не является ни общеизвестным в данной области и не соответствующим номенклатуре органических соединений.
В настоящее время известен ряд композиций, использующих в качестве активного антимикробного начала соединения из класса солей четвертичных аммониевых оснований (2).
Показано, что многие из указанного типа соединений, в частности бензалконий хлорид - алкилдиметилбензиламмоний хлорид структурной формулы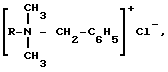
обладая эффективным антимикробным действием, токсичны и повреждают клетки тканей глаза, вызывая раздражение.
Одним из современных методов снижения токсичности четвертичных аммониевых оснований является их модификация полимерами, на котором основано и техническое решение, описанное в (3) и являющееся ближайшим аналогом предложенного решения по технической сущности и достигаемому эффекту.
В патенте (3) описан способ обработки контактных линз с использованием раствора, содержащего в качестве антимикробного активного начала четвертичное аммониевое основание структурной формулы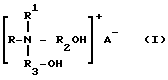
где R - насыщенный или ненасыщенный остаток жирных кислот или их смесей, состоящий из 12-18 атомов углерода,
A- - Cl-, NO3 -, SO4 -,
R1, R2, R3 - одинаковые или различные алкил-группы, предпочтительно - этил в количестве 0,01 - 0,1%, предпочтительно 0,03 - 0,06%; конкретно в примерах представлен алкилтриэтаноламмоний хлорид, где алкил - остаток природной смеси олеиновых, стеариновых и пальмовых кислот, который имеет торговое название "мирамин" или "миранол".
Для снижения токсичности берут полимеры из группы: полигидроксиэтилметакрилат, карбоксиметилцеллюлоза, поливинилпирролидон и их смеси. В формуле изобретения указан только полигидроксиэтилметакрилат в количестве 0,04%, в качестве поверхностно-активных очистителей - полисорбат-80 (0,2%), пропиленгликоль, в качестве консерванта - тиомерсал - 0,002% и изотонический физиологический раствор, содержащий бикарбонат натрия, фосфат натрия двухосновной безводный, фосфат натрия одноосновной моногидрат.
В соответствии с описанием приведенные растворы проявляют антимикробную активность по отношению к следующим микроорганизмам: Staphylococcus aureus, Pseudomonas aeruginosa, Escherichia coli, Candida albicans - за 6 часов контакта менее 102 микроорганизмов
Дополнительно S. marcescens требует 8 часов контакта.
Приведены сравнительные эксперименты с известным антимикробным веществом бензалконий хлоридом (катамин АБ, БАК) с добавкой полигидроксиметилметакрилата и показано, что последний не снижает токсичность катамина АБ, а значительная концентрация полимера приводит к снижению антимикробной активности.
На основании примеров с одним полигидроксиметилметакрилатом сделаны выводы о том, что при высокой концентрации БАК полимеры не снижают его токсичность.
Все испытанные композиции, в том числе и с новым антимикробным веществом, содержали в качестве консерванта тимеросал, хотя в описании без экспериментальных подтверждений указано на возможность использования вместо тимеросала (мертиолат, тиомеррал) динатриевой соли этилендиаминотетрауксусной кислоты (трилон Б, ЭДТА).
Недостатками прототипа являются ограниченный спектр антимикробного действия при длительном времени обезвреживания и использование тимеросала.
Тимеросал - очень эффективный консервант, однако он содержит ртуть (структурная формула тимеросала -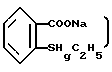
и его применение отрицательно сказывается на тканях глаза.
В настоящее время показателем качества композиций для очистки контактных линз является отсутствие именно этого компонента, что указывается на этикетках и в рекламах.
Предлагаемым изобретением решается задача увеличения эффективности очистки за счет расширения спектра антимикробного действия и сокращения времени обезвреживания, а также исключение высокотоксичного компонента.
Цель достигается предложенной композицией для обработки контактных линз, которая включает в качестве активного антимикробного вещества - мирамистин (миристамидопропилдиметилбензиламмоний хлорид) структурной формулы: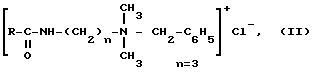
где R ≈ CH3(CH2)12,
в качестве полимера, снижающего токсичность при сохранении антимикробной активности - натриевую соль карбоксиметилцеллюлозы (Na - КМЦ); который образует комплекс с мирамистином, в качестве поверхностно-активных очистителей - полисорбит-80 (твин-80) и полиэтиленоксид (ПЭО - 400), в качестве консерванта и для удаления кальция - динатриевую соль этилендиаминотетрауксусной кислоты (трилон Б), и в качестве изотонического физиологического раствора
- хлорид натрия,
- натрия гидрофосфат 12-водный,
- калия дигидрофосфат
в воде при следующих соотношениях ингредиентов:
мирамистин - 0,01-0,05,
Na - КМЦ - 0,015 - 0,2,
полисорбат-80 - 0,015-0,05,
ПЭО - 400 - 0,015 - 0,2,
трилон Б - 0,01-0,05,
раствора - до 100 мл.
Изотонический физиологический раствор может иметь следующий состав (на 100 мл воды):
хлорид натрия - 0,5 - 0,6,
натрий гидрофосфат 12-водный - 0,465 - 1,47,
калий дигидрофосфат - 0,03 - 0,42
и должен обеспечивать pH = 6,7 - 8,0
и осмолярность 280 - 300 мосм/л.
Предложенное техническое решение отличается от прототипа тем, что в качестве антимикробного активного вещества используют мирамистин в комбинации с Na - КМЦ и трилон Б. Мирамистин известен как антисептик, его регистрационный номер - 91/146/2, и он производится отечественной промышленностью.
Однако известные антимикробные свойства мирамистина не предопределяют очевидную возможность его использования в композициях для обработки контактных линз, поскольку последнее требует знания таких специфических свойств, как воздействие на материал, из которого изготовлены линзы.
Большинство катионных поверхностно-активных веществ, к которым относится и мирамистин, не пригодны для использования в композициях для очистки линз, вследствие взаимодействия их с полимерной матрицей линз.
Важную роль в достижении эффективности играет тот факт, что мирамистин образует комплекс с Na - КМЦ, позволяющий при сохранении антимикробной активности снизить токсичность.
Несмотря на то, что в прототипе Na - КМЦ для снижения токсичности описана, однако, во-первых, не ясно как она влияет на антимикробную активность (отсутствуют данные), во-вторых, как следует из того же описания, не удалось получить снижение токсичности на БАК, который по структуре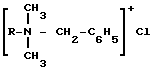
близок к мирамистину (структура 11), а потому можно было бы ожидать одинакового эффекта, т. е. его отсутствия. Однако нами в результате эксперимента было показано, что сочетание Na - КМЦ с трилоном Б позволяет снизить токсичность и сохранить бактерицидную активность и на БАК (катамин АБ), что не было достигнуто в прототипе и что свидетельствует об избирательности влияния типа полимера на определенные антимикробные соли четвертичных аммониевых оснований (сравнительные примеры с катамином АБ в таблице под NN 4, 5).
Na - КМЦ с мирамистином образует комплекс, который позволяет сохранить антимикробную активность и снизить токсичность использования комплекса совместно с трилоном Б, позволяет исключить токсичный тиомерсал.
Сказанное позволяет сделать вывод, что новая комбинация признаков приводит к результату, который не мог быть предсказан, исходя из известного творчества.
Мирамистин сравнительно с мертиолатом (прототип) обладает более широким спектром антимикробного действия при малых концентрациях, обладает специфической активностью и низкой токсичностью.
Мирамистин активен в отношении грамположительных микроорганизмов: Стафилококки, Стрептококки, Bacillus anthracoides;
против грибов: Candida albicans, C. tropicalis, Trichophiton rubrum, Microsporum lansum, Aspergillus niger (в концентрации 0,0001% - 0,002%).
Диапазон антимикробного влияния на грамотрицательные бактерии: гонококки (дикие и музейные штаммы), эшерихии (патогенные и непатогенные серотипы), шигеллы (Зонне, Флекснера и др.), сальмонеллы, спирохеты (Treponema pallidum и др.) в концентрации 0,005%.
Влияние на простейшие (Trichomonas vaginalis) находится в пределах 0,002% - 0,02%. Специфическая активность - прекращает подвижность трихомонад при концентрации 0,01% в течение 1-10 мин.
Мирамистин активен в отношении вирусов герпеса, гриппа, аденовируса, ВИЧ-1. По токсичности мирамистин относится к 4 классу вредности (малотоксичен), в концентрации 0,01 - 0,1 - 1% - не раздражает кожу, в концентрации 0,01 - не раздражает слизистые (глаза, внутренних органов).
Пример (основной).
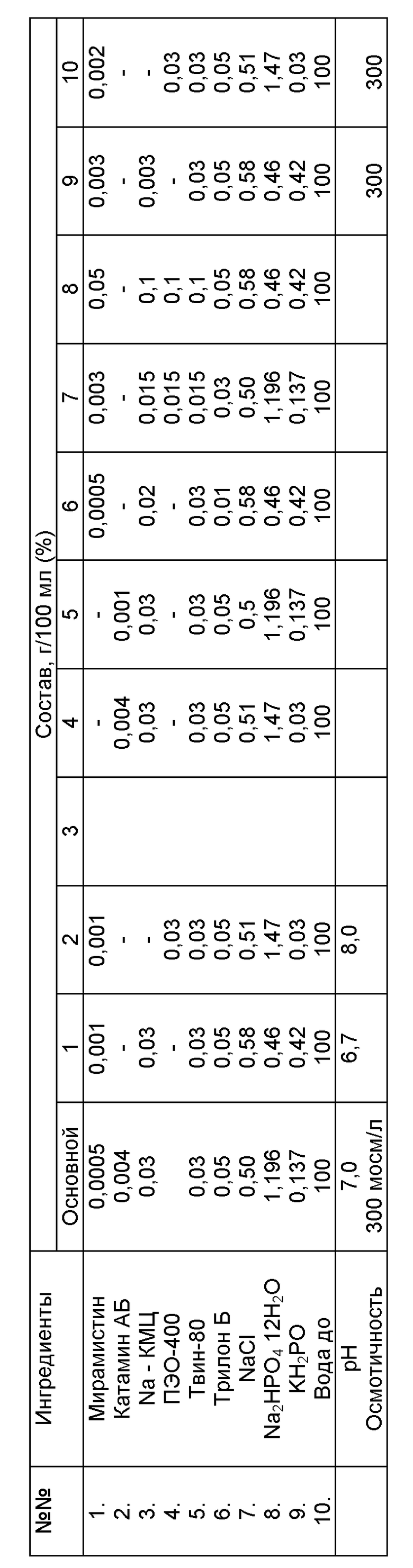
Изотонический раствор, содержащий 0,5 г NaCl, 1,196 г Na2HPO4 • 12H2O, 0,137 г KH2PO4 в 100 мл воды, смешивают с 0,005 г мирамистина, 0,03 г Na - КМЦ, 0,03 г твина - 80 и 0,05 г трилона Б.
Полученный раствор имеет pH 7,0 и осмотичность 300 мосм/л.
Раствор представляет собой прозрачную, бесцветную, слегка опалесцирующую без цвета и запаха жидкость, предназначенную для промывки, хранения и дезинфекции контактных линз в клинических, амбулаторных и бытовых условиях.
Проводилась проверка прозрачности (оптической плотности) раствора с помощью спектрофотометра КФК-2 в оптических кюветах 10,070 при длине волны от 315 нм до 750 нм. Показатели оптической плотности (Д), полученные при указанных условиях для разных значений λ, следующие:
λ нм : 315 400 440 490 540 590 670 750
Д: 0,25 0,18 0,16 0,15 0,15 0,23 0,20 0,16
Таким образом, оптическая плотность раствора отличается от оптической плотности чистой воды, принятой за 0, что характерно для многокомпонентных солевых растворов. Второй пик оптической плотности при λ = 590 нм, что связано с присутствием в растворе фракции стабилизирующих высокомолекулярных органических соединений. Это обеспечивает соответствие характеристик раствора показателем назначения.
Проверка цветности раствора.
Цветность раствора определялась путем сравнения с эталоном чистой воды в химических стаканчиках одинакового диаметра при дневном освещении на матово-белом фоне.
В указанных условиях цвет раствора и эталона воды неразличим.
Проверка модифицирующего действия раствора на жидкие белковые среды.
После погружения линз в раствор следы белковых субстратов на поверхности линзы (серозная жидкость, экссудат, слущившиеся и мигрировавшие клетки) взаимодействуют с раствором. При этом белковые загрязнения должны подвергаться денатурации (или лизису), не должны сорбироваться на поверхности контактных линз.
Для проверки действия раствора на белковый субстрат его смешивали с белковым препаратом "Желатиноль" в соотношении 1:1 в химических стаканчиках.
Затем с помощью спектрофотоколориметра КФК-2 измеряли оптическую плотность полученной смеси относительно контроля. В качестве контрольного образца использовали препарат "Желатиноль", разведенный дистиллированной водой в соотношении 1:1. Оптическую плотность определяли в оптических кюветах калибра 10,070 при значении λ = 315 нм. Использовались кюветы из различного материала (кварцевое стекло, оргстекло, лавсан, полиэтилен низкого давления).
Свежеполученные смеси "Желатиноля" с раствором и с водой заливали в оптические кюветы и экспонировали в этих кюветах в течение 2 часов. Показатель Д свежеприготовленной смеси "Желатиноля" с водой принимали за исходный. Последующие определения Д в смесях "Желатиноля" с раствором и "Желатиноля" с водой производили каждые 20 мин. Получены следующие результаты:
Исходные средние значения Д контрольных образцов = 0,70.
Исходные средние значения испытуемых образцов Д = 0,82.
Средние значения Д контрольных образцов после 2-часовой экспозиции = 0,73.
Средние значения Д испытуемых образцов после 2-часовой экспозиции = 2,0 (при дальнейшей экспозиции Д _→ ∞.
Интенсивное и необратимое помутнение "Желатиноля" при смешении с раствором связано с образованием микрокоагулянтов белка. При фильтрации полученной коагулированной взвеси через бумажный беззольный фильтр по ТУ 6-09-1678-86 ("красная полоса") селективность пропускания коагулированных частиц 0,69.
Следовательно, раствор вызывает необратимую денатурацию (образование взвеси скоагулированных хлопьев) жидких белковых загрязнений, что соответствует показателям назначения.
Проверка качества удаления белковых загрязнений со стеклянных и полимерных поверхностей после действия раствора.
Скоагулированная взвесь белковых частиц "Желатиноля" после смешения с раствором экспонировалась в течение суток в закрытых крышками оптических кюветах из различного материала (всего 10 кювет) и в тонком слое в открытых стеклянных и полиэтиленовых чашках Петри (20 образцов). После 24-часового экспонирования при комнатной температуре белковая взвесь в кюветах сохранялась в жидком виде. Затем оптические кюветы после удаления белковой взвеси на слив промывались однократным объемом дистиллированной воды, а затем заполнялись новым объемом дистиллированной воды и тестировались на оптическую прозрачность относительно эталона чистой воды.
Во всех наблюдениях фотометрический контроль не обнаружил следов загрязнения в кюветах, в которых скоагулированная смесь "Желатиноля" и раствора экспонировалась в течение суток. Таким образом, белковые загрязнения после обработки раствором не сорбировались на материале оптических кювет, что соответствует показателям назначения испытуемого раствора.
В открытых чашках Петри при суточном экспонировании происходило высыхание белковой скоагулированной взвеси, которая полностью смывалась после 30-минутного замачивания в дистиллированной воде. После этого на отмытых поверхностях чашек Петри оставались крайне незначительные очаги загрязнений. В целом коэффициент чистоты отмываний поверхности чашек Петри от засохшего коагулята по данным планиметрического исследования составил 99,0 - 99,5%.
Таким образом, предложенный раствор для очистки, промывки, дезинфекции и хранения контактных линз исключает момент их подсыхания (или любого другого отмываемого изделия) в процессе цикла обработки.
Клинические испытания раствора для очистки, промывки, дезинфекции и хранения контактных линз проводились в клинике глазных болезней РГМУ (кафедра глазных болезней лечебного факультета).
Для испытаний были представлены образцы в количестве 50 штук.
Медицинские исследования проводились в соответствии с программой и методикой клинических испытаний.
Среди 30 пациентов-больных, использующих для коррекции зрения мягкие контактные линзы, были пациенты, которые коррегированны линзами с различной степенью гидрофильности (от 38 до 70%).
В результате были сделаны следующие выводы:
- растворы хорошо переносимы больными,
- применение растворов не требует дополнительной отмывки контактных линз после их использования (растворов),
- растворы обладают высокой эффективностью чистящих и дезинфицирующих свойств.
Составы композиции, подтверждающие объем предложенной формулы изобретения, представлены в таблице (примеры 1-10).
Растворы получали и испытывали так же, как в основном примере.
Было изучено также местно-раздражающее действие интерполимерного комплекса мирамистина с Na-карбоксиметилцеллюлозой in vivo в экспериментах на кроликах и морских свинках. Показано, что ежедневное в течение 30 дней нанесение на кожу (обезволошенную) кроликам (18 штук) и морским свинкам (15 штук) препарата не вызывало никаких явлений раздражения и воспаления кожи, не отражалось на общем состоянии и поведении животных, не сказывалось на динамике их массы тела, содержании гемоглобина, эритроцитов, лейкоцитов, не приводило к патоморфологическим изменением кожи, печени, почек, селезенки, сердца и надпочечников.
Кожно-резорбтивное действие комплекса изучали в экспериментах на белых крысах (по 15 штук в группе). Комплекс применяли в концентрации 0,2% и в 5 раз превышающей таковую.
Препарат наносили на депилированный участок кожи в течение 30 дней, контрольной группе животных наносили только раствор Na - КМЦ, без антисептика.
Аппликацию проводили по 4 ч в сутки.
В результате проведенных исследований показано, что нанесение препарата на неповрежденную поверхность кожи не выявило кожно-резорбтивного действия, о чем свидетельствовали результаты анализа крови и подопытных и контрольных животных, биохимические показатели у которых были практически одинаковыми.
Изучены аллергенные и иммунотоксические свойства комплекса. Показано, что препарат в концентрации не вызывает сенсибилизацию организма и не оказывает иммунотоксического действия. Многократное введение в различных дозах не сказывалось на количестве иммунокомпетентных клеток, не влияет на массу и клеточность центральных и периферических органов иммунной системы.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЭНЗИМАТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ОЧИСТКИ КОНТАКТНЫХ ЛИНЗ | 1998 |
|
RU2139095C1 |
| КОМПОЗИЦИЯ ДЛЯ ОБРАБОТКИ И ХРАНЕНИЯ МЯГКИХ КОНТАКТНЫХ ЛИНЗ | 2004 |
|
RU2262342C1 |
| Раствор для ухода за контактными линзами | 2020 |
|
RU2755298C1 |
| МНОГОФУНКЦИОНАЛЬНЫЙ РАСТВОР ДЛЯ УХОДА ЗА КОНТАКТНЫМИ ЛИНЗАМИ | 2011 |
|
RU2468823C2 |
| АНТИСЕПТИЧЕСКОЕ СРЕДСТВО "КАТАЦЕЛ" | 1998 |
|
RU2146136C1 |
| СПОСОБ ДЕЗИНФЕКЦИИ КОНТАКТНЫХ ЛИНЗ И КОМПОЗИЦИЯ ДЛЯ ДЕЗИНФЕКЦИИ КОНТАКТНЫХ ЛИНЗ | 1991 |
|
RU2067456C1 |
| Фармацевтическая комбинированная композиция для лечения гнойных ран на основе фторхинолонов (варианты) | 2016 |
|
RU2682171C2 |
| Фармацевтическая комбинированная композиция для местного и наружного применения на основе диоксидина | 2016 |
|
RU2667974C2 |
| ГЛАЗНЫЕ КАПЛИ ДЛЯ ЛЕЧЕНИЯ АЛЛЕРГИЧЕСКИХ КОНЪЮНКТИВИТОВ И КЕРАТОКОНЪЮНКТИВИТОВ | 2001 |
|
RU2193403C1 |
| Фармацевтическая комбинированная композиция для местного и наружного применения на основе бактериолитического и протеолитического комплекса ферментов | 2016 |
|
RU2655808C2 |
Изобретение относится к средствам, предназначенным для очистки, дезинфекции, промывания контактных линз. Композиция для обработки контактных линз содержит в качестве активного антимикробного вещества - мирамистин в комбинации с натриевой солью карбоксиметилцеллюлозы, образующих комплекс, и динатриевой солью этилендиаминотетрауксусной кислоты в качестве консерванта и для удаления кальция. Композиция также содержит поверхностно-активные очистители - полисорбат-80 и полиэтиленоксид и изотонический физиологический раствор на основе хлорида натрия и фосфатной буферной системы. Компоненты берут в определенных количественных соотношениях. Композиция не вызывает сенсибилизацию организма и не оказывает иммунотоксического действия, не влияет на массу и клеточность центральных и периферических органов иммунной системы. 1 з. п. ф-лы, 1 табл.
Мирамистин - 0,001 - 0,05
Na-КМЦ - 0,015 - 0,05
Трилон Б - 0,01 - 0,08
Изотонический физиологический раствор - До 100 мл
2. Композиция по п.1, отличающаяся тем, что изотонический физиологический раствор содержит
Хлорид натрия - 0,5 - 0,58
Натрия гидрофосфат 12-водный - 0,465 - 1,47
Калий дигидрофосфат - 0,03 - 0,42
Вода - До 100 мл
| RU 2001631, 31.07.87 | |||
| АППАРАТ ДЛЯ ОСУЩЕСТВЛЕНИЯ ХИМИЧЕСКИХ ПРОЦЕССОВВ «КИПЯЩЕМ» | 0 |
|
SU175490A1 |
| Пюпитр для работы на пишущих машинах | 1922 |
|
SU86A1 |
| ДЕТАЛЬ, СОДЕРЖАЩАЯ КЕРАМИЧЕСКИЙ ЭЛЕМЕНТ | 2013 |
|
RU2619013C2 |
Авторы
Даты
1999-10-10—Публикация
1998-04-23—Подача