Данное изобретение касается соединений с антивирусной активностью и более конкретно конъюгированных соединений антивирусного лекарственного средства с носителями, имеющими гепатотропную активность.
В лечении инфекции, вызываемой вирусами, побочные действия антивирусных лекарственных средств можно уменьшить с применением химиотерапевтического лизосомотропного подхода /Balboni PG, Minia A, Grossi MP, Barbanti - Brodano G, Mattioli A, Fiume L., Activity of albumin conjugates of 5-fluorodeoxyuridine and cytosine arabinoside on poxviruses as a lysosomotropic appraach to antiviral chemotherapy, Nature 1976; 264: 181-183/.
Этот подход состоит в конъгировании лекарственного средства с макромолекулой, которая избирательно захватывается из инфицированных клеток и транспортируется из них в лизосомы.
Если, как и требуется, ферменты лизосом расщепляют связь между носителем и лекарственным средством, то лекарственное средство концентрируется в фармакологически активной форме внутри инфицированных клеток.
Хронический гепатит, вызываемый вирусом B /HBV/ и хронический гепатит, вызываемый вирусом C /HCV/, является подходящей мишенью для такого химиотерапевтического подхода, поскольку: (a) эти вирусы растут в основном в печеночных клетках, в гепатоцитах; (b) гепатоциты специфически вносят и транспортируют в лизосомы некоторые гликопротеины с остаткам галактозы, которые, следовательно, могут функционировать в качестве гепатотропных векторов лекарственных средств; (c) конъюгаты - лекарственное средство/гликопротеины - могут легко входить в контакт с поверхностью гепатоцитов, т.к. печеночный синусоид не является барьером для белков.
Согласно этому подходу и для уменьшения нейротоксических побочных действий антивирусное лекарственное средство арабинозидаденинмонофосфат /ara-AMP/, активное против HBV /Jacyna MR, Thomas HC., Antiviral therapy: Hepatitis B. , Brit Med Bull 1990; 46: 369-382/ было конъюгировано с азиалофетуином (AF) / Fiume L, Mattioli A, Busi C, Balboni PG, Barbanti - Brodano G, De Vries J, Altman R, Wieland Th., Selective inhibition of Ectromelia virus DNA synthesis in hepatocytes by adenine-9- β -D-arabinofuranoside (ara-A) и adenine- β -D-arabinofuranoside 5'-monophosphate (ara-AMP) conjugated to asialofetuin, FEBS Letters 1980; 116: 185-188/ и с лактозаминированным альбумином (L-SA) / (Fiume L, Busi C, Mattioli A, Balboni PG, Barbanty-Brodano G. , Hepatocyte targeting of adenine-9- β -D-arabinofuranoside 5'-monophosphate (ara-AMP) coupled to lactosaminated albumin, FEBS Lett 1981; 129: 261-264; Fiume L, Bassi B, Busi C, Mattioli A, Spinosa G., Drugtargeting in antiviral chemotherapy./ A chemically stable conjugate of 9- β -D-arabinofuranosyladenine 5'-monophosphate with lactosaminated albumin accomplishes a selective delivery of the drugto liver cells, Biochem Pharmacol 1986; 55: 967-972/. В мышах оба этих носителя приводят к направлению лекарственного средства в печень.
L-SA имеет большое преимущество по сравнению с AF: фактически конъюгаты, приготовленные с гомогологичным лактозаминированным альбумином /т.е. альбумином из того же вида/ при внутривенном введении не индуцируют образование антител /Fiume L, Mattioli A, Busi C, Spinosa G, Wieland Th., Conjugates of adenine-9- β D-arabinofuranoside monophosphate (ara-AMP) with lactosaminated homologous albumin are not immunogenic in the mouse, Experientia 1982; 38: 1087-1089; Fiume L, Busi C, Preti P., Spinosa G. Conjugates of a a-AMP with lactosaminated albumin: a study on their immunogeneti citu in mouse and rat. Cancer Drug Delivery 1987; 4: 145-150/.
У лесного сурка с гепатитом, вызываемым WHV /Ponzetto A Fiume L, Forzani B, Song SY, Busi C, Mattioli A, Spinelli C, Marinelli M, Smedile A, Shialberge E, Bonio F, Gervasi GB, Rapicetta M, Verme G., Adenine arabinoside monophosphate and acyclovir monophosphate coupled to lactosaminated albumin reduce wooduck hepatitis virus viremia doses lower than do the unconjugated drugs, Hapatology 1991; 14: 16-24/ и у больных с хроническим HBV /Fiume L, Torrani Cerenzia MR, Bonino F, Busi C, Mattioli A, Brunetto MR, Chiaberge E, Verme G. Inhibition of hepatitis B virus replication by viadabine monophosphate conjugated with lactosaminated serum albumin, Lancet 1988; 2: 13-15. Torrani Cerenzia MR, Fiume L, Busi C, Mattioli A, Di Stefano G, Gervasi GB, Brunetto MR, Piantino P, Verme G, Bonino F. Inhibition of hepatitis B virus replication by adenine arabinoside monophosphate coupled to lactosaminated albumin. Efficacy, minimal effecti ve dose and plasma clearance of conjugate. J. Hepatol-1994; 20: 307-309/ ara-AMP, конъюгированный с L-SA, ингибировал репликацию вируса в дозах, в 2 раза меньших, чем дозы свободного лекарственного средства.
Конъюгат с L-sa должен вводиться внутривенно из-за большого объема, требуемого для инъекции, а также потому, что при введении его иными путями образуются антитела, что ведет к плохому соблюдению больным режима и схемы лечения при долгосрочной терапии.
Поэтому гепатотропный носитель ara-AMP и других антивирусных лекарственных средств, делающий возможным внутримышечное ведение соответствующих конъюгатов, представлял бы собой значительное усовершенствование с терапевтической точки зрения.
Известно также, что основная полиаминокислота, поли-L-лизин, с 1/3 аминогрупп, замещенных остатками галактозы, при внутривенном введении осуществляет направленную доставку в печень ara-AMP /Fiume L, Bassi B, Busi C, Mattioli A, Spinosa G, Faulstich H, Galactosylated poly (L-лизин) asa hepatotropie carrier of 9- β -D-arabinofuranoside 5'-monophosphate, FEBS hetters 1986; 203: 203-206/. Кроме того, поли-L-лизин, в котором все или большая часть его ε -аминогрупп замещены, не вызывает образования антител даже при введении иными путями, чем внутривенная инъекция /Levine BB, studies on antigenicity. The effect of succinylation of ε -aminogroups on antigenicity of benzylpenicilloyl-poli-L-lysine conjugates in random and in strain 2 Guinea pig, Proc Soc Exptl Biol Med 1964; 116: 1127-1131; Sela M. Immunological studies with synthetic polyptides, Adran Immunol, 1966; 5: 29-129/.
В настоящее время обнаружено, что если в поли-L-лизине большая часть ε -аминогрупп замещена галактозой и одним из антивирусных лекарственных средств, активных против вирусов гепатита, то можно получить на мышах три очень важных терапевтических эффекта:
(i) этот конъюгат теряет высокую токсичность поли-L-лизина, которая отличала прежние галактозилированные конъюгаты поли-L-лизин-ara-AMP /Fiume et al, FEBS Letters 1986, 203: 203-206/, в которых большая часть ε -аминогрупп оставалась незамещенной;
(ii) направленная доставка антивирусного лекарственного средства к печени осуществляется даже в том случае, если конъюгат вводится не внутривенно и, в частности, путем внутримышечной инъекции;
(iii) повторное введение конъюгата внутримышечной или внутривенной инъекцией не приводит к образованию антител.
Терапевтическое значение этого свойства будет очевидным, если иметь ввиду, что возможность направленной доставки в печень лекарственного средства при помощи внутримышечной инъекции не только участвует в использовании интересных особых свойств, уже упоминавшихся ранее в отношении лизосомотропного подхода /т.е. значительное уменьшение побочных действий, обусловленных токсичностью антивирусных лекарственных средств/, но также важна для того, чтобы сделать химиотерапию более удобной /комфортной/ для больного, поскольку химиотерапевтическое лечение в случае вирусного хронического гепатита является длительным.
В предпочтительном варианте в качестве основной полиаминокислоты выбирают поли-L-лизин или поли-L-орнитин, а в качестве лекарственных средств, известных как лекарства, обладающие активностью против вирусов гепатита, применяют ara-AMP, ацикловир, рибавирин, азидотимидин и т.п.
Данное изобретение касается поэтому применения в качестве носителя антивирусных лекарственных средств основной галактозилированной полиамикислоты, характеризующейся тем, что большая часть аминогрупп замещена молекулами лекарственного средства и молекулами галактозы.
Высокая степень замещения исключает острую токсичность как основных полиаминокислот, так и конъюгатов поли-L-лизина, описанных в литературе ранее /Fiume et al. FEBS Letters 1986; 203: 203-206/, в которых менее 50% ε -аминогрупп были замещены лекарственным средством и галактизольными остатками.
Получение конюъгированных соединений в соответствии с данным изобретением предусматривает двухступенчатую процедуру:
(a) конъюгирование основной полиаминокислоты с антивирусным лекарственным средством или с остатками галактозы и
(b) последующее конъюгирование полученного в стадии (a) конъгата с остатками галактозы или остатками антивирусного лекарственного средства соответственно. В предварительном основном определении можно отметить, что эти две стадии конъюгирования могут быть переставлены местами.
Как правило, выбор последовательности стадий определяется молекулярной массой полиаминокислоты, в том смысле, что в случае низких молекулярных масс предпочтительно проводить сначала конъюгирование с лекарственным средством, а затем конъюгирование с галактозой.
В предпочтительном варианте способа, согласно данному изобретению, конъюгирование лекарственного средства проводят известным per se путем через имидазолат антивирусного лекарственного средства в его монофосфатной форме и при щелочном pH /Fiume L, Busi C, Di Stefano G, Mattioli A, Goupling of antiviral nucleoside aralogs to lactosaminated human albumin by using the imidazolides of their phoshoric esters - Analyt Biochem 1993; 212: 407-411/.
Галактозные остатки предпочтительно конъюгируют /стадия b/ путем восстановительного лактозаминирования в присутствии цианоборгидрида натрия /Schwartz BA, Gray GR, Proteins containing reductively aminated disaccharides Synthesis and chemical characterization - Arch Biochem Biophys 1977; 181: 542-549/.
В качестве нелимитирующих примеров приведены примеры получения конъюгатов с использованием поли-L-лизина и поли-L-орнитина в качестве носителя и ara-AMP, ацикловира, рибавирина и азидотимидина в качестве антивирусных лекарственных средств. При этом должно быть понятно, что подобные способы пригодны для получения конъюгатов с другими известными антивирусными лекарственными средствами.
Были получены конъюгаты основных полиаминокислот как с низкой молекулярной массой, так и с высокой молекулярной массой.
1. Конъюгаты с низкой молекулярной массой
A. Конъюгат с поли-L-лизином
A.1. Получение
В коммерческой композиции /Simga/ поли-L-лизина с молекулярной массой 1000-4000 Да и средней степенью полимеризации 14 полимеры с молекулярной массой ниже 1800 удаляли гель-фильтрацией на P2 BiO Gel колонке, элюированной 0,2 MNH4HCO3. Полимеры, полученные из колонки, после лиофилизации использовали для получения соединений, показанных в таблице 1.
Во всех конъюгатах галактозные остатки соединялись с ε -аминогруппами путем восстановительного лактозаминирования в присутствии цианоборгидрида натрия /Schwartz BA, Gray GR., Arch. Biochem Biophys 1977; 181: 542-549/.
Соединение 1
Поли-L-лизин метили [H3] формальдегидом по способу Jentoft и Dearborn/Jentoft N, Deaborn DG. , Protein labelling by reductive alkylation, Methods Enzymol 1983; 91: 570-579/. Реакционная смесь содержала 44 мкКи [3H] фольмальдегида/мл. [3H]-поли-L-лизин выделяли гель-фильтрацией на P2 BiO Gel колонке с последующей лиофилизацией.
Соединение 2
Галактозу соединили с полилизином восстановительным лактозаминированием в присутствии цианоборгидрида натрия. 20 мг поли-L-лизина растворили в 2 мл буфера 0,1 М борная кислота/бура (pH 8,5) и добавили 80 мг L-лактозы, содержащей 50 мкКи [D-глюкозо-1-14C] лактозы /Amersham/ и 50 мг NaBH3CN. Смесь инкубировали при 37oC в течение 48 часов и [14C]Lat-поли-L-лизин выделяли в качестве соединения 1. Содержание лактозы измеряли по способу Duboiset al. /Dubois M, Gilles KA, Hamilton JK, Rebers PA, Smith F, Colorimetric method for determination of sugar and related substances Anal Chem 1956; 28: 350-356/ и относили к сухому весу соединения.
Соединения 3 и 4
Ara-AMP конъюгировали при помощи его имидазолата /Fiume L, Busi C, Di Stefano G, Mattioli A., Analyt Biochem - 1993; 212: 407-411/.
Этот способ более эффективен, чем применение водорастворимых карбодиимидов, и не имеет химических побочных реакций, продуцируемых этими веществами.
Имидазолат ara-AMP получали по способу Lormann и Orgel/Lohrmann R, Orgel LE, Preferential formation of (2'-5')-linked internucleotide bonds in non-enzymatic reactions, Tetrahedron 1978; 34: 853-855/. Поли-L-лизин растворяли (50 мг/мл) в буфере 0,1 M NaHCO3, Na2CO3 pH 9,5. После добавления имидазолата ara-AMP (75 мг/мл) pH доводили до pH 9,5 при помощи HCl и смесь инкубировали в течение 48 часов при 37oC. Конъюгаты выделяли, как соединение 1; содержание ara-AMP определяли спектрофотометрически и относили к сухому весу конъюгатов, которые затем лактозаминировали (для соединения 4 применяли немеченную лактозу).
Соединение 5
Конъюгат поли-L-лизин/ara-AMP, полученный, как указано для соединений 3 и 4, метили [3H]формальдегидом (100 мКи/ммоль).
Реакционную смесь содержала 2800 мкКи 3H формальдегида на мл. Меченый конъюгат затем лактозаминировали, как описано выше. Этот конъюгат применяли в качестве антигена в определении антител по способу Minden и Farr /Minden P, Farr RS, The ammonium sulphate method to measure antigen-binding capacity, Weir DM ed., Handbook of Experimental Immunology, Blackwell, Oxford 1973; 15.1-15-21/.
Соединение 6
Конъюгирование тритированного ara-AMP в этом соединении проводили с применением 1-этил-3-(диметиламинопропил)карбодиимида /ECD 1/, так как превращение ara-[3H]AMP в его имидазолат приводит почти к полной потере трития. Поли-L-лизин сначала лактозаминировали, как описано выше /соединение 2/, но с уменьшением периода реакции с 48 часов до 24 часов для замещения сахаром только 2/3 ε -аминогрупп.
После этого ara-[3H] AMP конъюгирировали по описанному выше способу /Fiume L, Bassi B, Busi C, Mattioli A, Spinosa G, Faulfstich H, FEBS Letters 1986; 203: 203-206/. При получении этого конъюгата первой стадией было лактозаминирование для уменьшения числа свободных ε -аминогрупп ко времени использования ECD 1, что позволяло полимеризовать молекулы поли-L-лизина при помощи этого соединения.
Соединение 7
[3H]ACVMP, примененный для получения этого конъюгата, получали при помощи фосфорилирования /Yoshikawa M, Kato T, Takenishi T., A novel method for phosphorylation of nucleosides to 5'-nucleotides, Tetrahedron Lett 1967; 50: 5065-5068/ [3H]АС /трициат в положении 2 боковой цепи/ (NEN). Конъюгат получали, как в случае соединений 3 и 4, с той разницей, что инкубирование поли-L-лизина [3H]ACVMP продолжали только 6 часов. Имидазолат [3H]ACVMP получали по описанному выше способу Лормана и Оргеля.
Конъюгированный продукт данного изобретения, полученный в предшествующих примерах, подвергали физико-химическим определениям и биологическим тестам с целью обнаружения экспериментального подтверждения терапевтических свойств этих соединений.
Следующие определения относятся к прилагаемым фиг. 1 - 6, в которых:
- Фиг. 1 изображает хроматографический график на BioGel P 10 Lat-поли-L-лизин-ara-AMP /соединение 4 таблицы 1/.
- Фиг. 2A-2C показывают распределение радиоактивности в печени 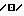 , в селезенке /•/, в кишечнике /°/ и в мозгу /□/ самок швейцарских /Swiss/ мышей (28-30 г), которым соединения данного изобретения /таблица 1/ и неконъюгированные соединения для сравнению вводили при помощи внутримышечной инъекции.
, в селезенке /•/, в кишечнике /°/ и в мозгу /□/ самок швейцарских /Swiss/ мышей (28-30 г), которым соединения данного изобретения /таблица 1/ и неконъюгированные соединения для сравнению вводили при помощи внутримышечной инъекции.
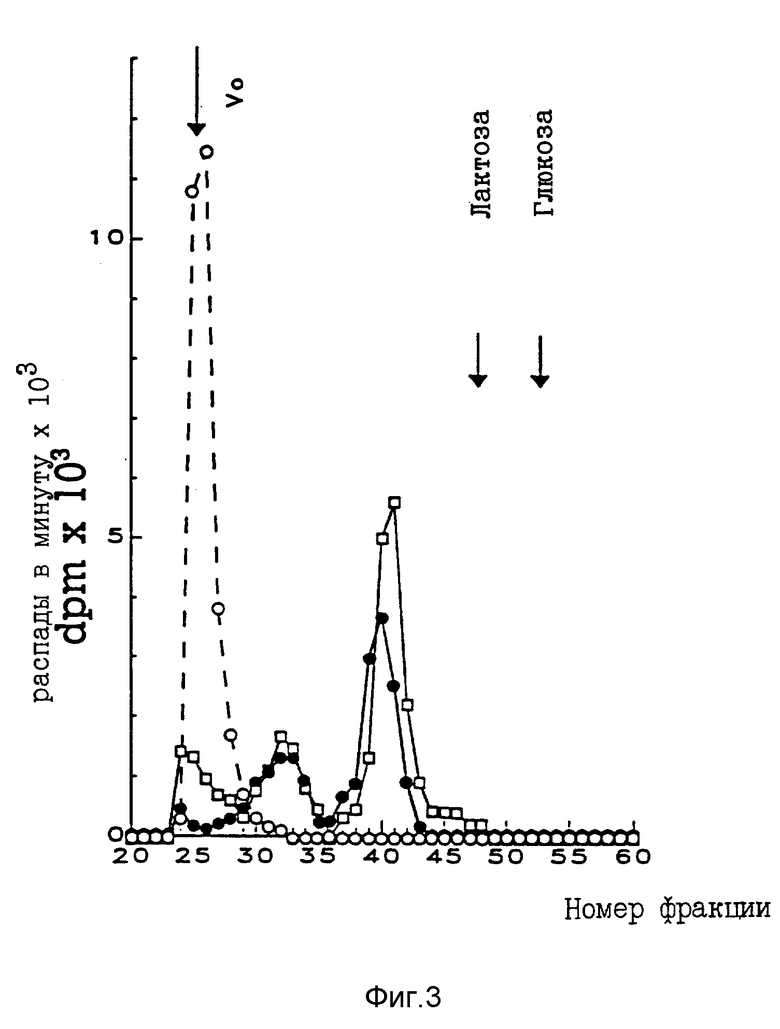
- Фиг. 3 изображает хроматографический график на BioGel P 2 экстрактов печени мышей, инъецированных соединением 3 таблицы 1.
A.2. ЭКСПЕРИМЕНТАЛЬНЫЕ НАБЛЮДЕНИЯ
a/ Средняя мол. масса соединения 4
Фиг. 1 изображает хроматографию Lat-поли-L-лизин-ara-AMP /соединение 4 таблицы 1/ на Bio Gel P 10 /1,6 х 92/ колонке, калиброванной декстраном синим 2000 /свободный объем/, рибонуклеазой /мол. масса 13700/ и апротинином /мол. масса 6500/.
25 мг конъюгата наносили на 1,6 х 92 см колонку, уравновешенную и элюированную 0,2 M NH4HCO3. Собирали фракции по 2 мл. Объемы элюции как конъюгата, так и маркеров /последние указаны стрелками/ определяли.
По способу Whitaker/Whitaker JR, Determination of molecular weights of proteins by gel filtration on sephadex, Analy Chem 1963; 35: 1950-1953/ было расчитано, что средняя мол. масса конъюгата равна 9100, что соответствует носителю с 19 остатками лизина и средней мол. массе 2400.
о/ Распределение соединений в органах.
Как уже упоминалось, Фиг. 2A-2G показывают распределение радиоактивности в органах мышей после внутримышечной инъекции A. [3H]поли-L-лизина (24 мкг/г); B. [14C] a - поли-L-лизина (24 мкг/г); C. ara-[3H] AMP (5 мкг/г);
D. [14C]Lat-поли-L-лизин-ara-AMP (24 мкг/г);
E. Lat-поли-L-лизин-ara-[3H] AMP (28 мкг/г), что соответствует 5 мкг/г ara-[3H] AMP; F. [3H]ACVMP (4 мкг/г); G. Lat-поли-L-лизин-ara-[3H] ACVMP (50 мкг/г), что соответствует 4 мкг/г [3H]ACVMP). Все соединения инъецировали в объеме 10 мкл на 1 животное в мышцы задних ног при помощи микрошприца Hamilton на 25 мкл.
Был рассчитан вклад радиоактивности, даваемый плазмой, содержащейся в органах /Fiume L, Busi C, Mattioli A, Lactosaminated human serum albumin as hepatotropicdrug carrier - Rafe of uptake by mouse liver, FEBS Letters 1982; 146: 42-46/. Эта часть радиоактивности вычиталась.
Каждый результат обозначает среднее из результатов, полученных для 2-3 животных.
Стандартная ошибка варьировалась от 0,1 до 2% от среднего.
Как показано, после введения [3H]поли-L-лизина /2A/, ara-[3H]AMP /2C/ и [3H] ACVMP /2F/ количества радиоактивности в печени, селезенке, кишечнике и мозгу практически эквивалентны. И напротив, после инъекции [14H]Lat-поли-L-лизина /2B/ и конъюгатов Lat-поли-L-лизина с ara-AMP и AMVMP, меченых в лактозе /2D/ или в лекарственных средствах /2E, 2G/, уровни радиоактивности в печени выше уровней радиоактивности других органов.
Проценты радиоактивности, измеренной на 1 г печени, после введения ara-[3H] AMP и [3H]ACVMP /2C, 2F/ были подобны процентам, рассчитанным после инъекции равной дозы этих лекарственных средств, конъюгированных с Lat-поли-L-лизином /2E, 2G/.
В почках уровни радиоактивности достигают тех же величин, что и в печени, через час после инъекции меченых конъюгатов /соединение 3 таблице 1/ или они в 1,5-2 раза выше /соединения 6 и 7/. В последующие точки времени уровни радиоактивности в почках равны или ниже, по сравнению с уровнями в печени. Высокие уровни радиоактивности в почках могут объясняться тем, что различные полипептиды, после гломерулярной фильтрации, включаются клетками проксимальных почечных канальцев /Maack Th, Johnson, V, Kau ST, Figueiredo J, Sigulem D. , Renal filtration. tran sport and metabolism of low molecular weight proteins, Kidney Int 1979; 16: 251-270/. Проникновение в почечные клетки не должно действовать на химиотерапевтический индекс конъюгатов Lat-поли-L-лизина с антивирусными лекарственными средствами. В действительности, за исключением ацикловира, который имеет тенденцию к соединению в почечных канальцах /Balfour Hh, Acyclovir and other chemotherapy for herpes group viral infection, Ann Rev Med 1984; 35: 279-291/, антивирусные нуклеозиды не очень токсичны для клеток этого органа.
c/ Биологическая переработка соединения 3 в печени.
Разрушение связи между ara-AMP и ε -аминогруппами галактозилированного поли-L-лизина внутри клеток печени было показано прежними исследованиями /Fiume L, Bassi B, Bongini A., Conjugates of 9-β-arabinofuranosyladenine 5'-monophosphate (ara-AMP) with lactosaminated albumin: characterization of the drug-carrier bonds, Pharm Acta Helv 1988; 63: 137-139/. Фиг. 3 показывает хроматографические профили на Bio Gel P 2 экстрактов печени мышей через 2 и 6 часов после внутримышечной инъекции [14C]Lat-поли-L-лизин-ara-AMP /24 мкг/г/.
Самки швейцарских мышей 28-30 г получили путем внутримышечной инъекции конъюгат (24 мкг/г в общем объеме 10 мкл).
После 3 β или 6 /□/ часов мышей убивали (каждый раз по два животных) и печени гомогенизировали с 4 объемами холодной воды; сразу же добавляли 5 объемов перхлорной кислоты и после центрифугирования супернатанты нейтрализовали при помощи KOH.
Через два часа выдерживания на холоде перхлорат калия осаждали центрифугированием и спернатанты лиофилизировали.
Лиофилизированный материал перераcтворяли в 2 мл H2O и после центрифугирования для осветления раствора 1 мл хроматографировали на Bio Gel P 2 (1,6 х 92) колонке и элюировали при помощи 0,2 M NH4HCO3.
Радиоактивность, присутствующая во фракциях, в которых элюировались молекулы, включенные в гель и имеющие размеры, большие, чем размеры молекул лактозы, показывает, что поли-L-лизин в печени распадался на фрагменты, хотя его /•/ -аминогруппы все еще были связаны с сахаром.
Символ ε○ в рисунке относится к хроматографическому профилю экстракта гомогенизированной печени, полученной из двух необработанных мышей, к которому конъюгат (14 мкг/мл) добавляли непосредственно перед осаждением перхлорной кислотой.
d/ Получение антител в мышах, обработанных соединением A.
12 самок швейцарских мышей (вес 28-30 г в начале теста) получали конъюгат N 4 (таблица 1), введенный в мышцы задней ноги 5 дней в неделю в течение 4 недель (одна дневная доза = 700 мкг/животное в 10 мкл 0,9% NaCl).
Кровоизвлечение проводили из заглазничного сосудистого сплетения при эфирной анестезии через неделю после последней инъекции.
Антитела измеряли в 50 мкл сыворотки в трех повторностях при помощи способа осаждения сульфатом аммония по Миндену и Фарру.
В качестве антигена применяли конъюгат 5 (таблица 1).
В присутствии 50 мкл сыворотки из 5 необработанных мышей количество распадов в минуту /dpm/ было 78±11 (стандартная ошибка, SE). В присутствии 10 мкл сыворотки мышей, способной соединяться либо с ara-A (938 пикомолей ara-A, вязанных 1 мл сыворотки), либо с ara-AMP, конъюгированным с L-HSA [Fiume h, Bassi B, Busi C, Mattidi A, Wieland Th., A study on the pharmacolineties in mouse of adenine -9- β-D-arabin ofuranoside 5-monophosphate conjug ated with lactosaminated albumin, Experientia 1985; 41, 1326-1328/ количество распадов в минуту в осадке было 1599±21.
В присутствии сывороток из 12 мышей, обработанных конъюгатом Lat-поли-L-лизин-ara-AMP, осажденные dpm были в диапазоне от 41±5 (минимум) до 80±6 (максимум).
Этот результат показал, что ни одна из обработанных мышей не образовала антитела, количество которых измеримо при помощи примененного способа, чувствительность которого была приблизительно 0,5 мкг IgG/мл сыворотки.
e/ Острая токсичность соединения 4
Конъюгат Lat-поли-L-лизин-ara-AMP /N 4/, растворенный в 0,9% NaCl, вводили внутривенно 5-ти самкам швейцарских мышей или подкожно (5-ти животным) в виде одной инъекции 0,4 мл/животное и в дозе 1,3 мг/г.
Токсичность не была обнаружена.
Инъецированная доза была в 50 раз выше по сравнению с дозой, вводимой внутримышечной инъекцией в опытах по изучению распределения конъюгата в органах /фиг. 2/.
Было показано, что летальная доза LD50 для самок мышей поли-L-лизина, примененного для получения этого конъюгата, инъецированного внутривенно в виде соли соляной кислоты, находилась в диапазоне 30-60 мкг/г.
f/. Растворимость соединения 4.
Больным с хроническим гепатитом B неконъюгированный а a-AMP вводили в дозах 2,5 или 5 мг/кг при помощи двух инъекций в день.
Конъюгат Lat-поли-L-лизин-ara-AMP /N 4/ легко растворяется в физиологическом растворе при концентрации 400 мг/мл.
Следовательно, доза 24 мг/кг, соответствующая 5 мг/кг ara-AMP, может быть введена больному весом 70 кг в объеме меньшем 5 мл.
B. КОНЪЮГАТ С ПОЛИ-L-ОРНИТИНОМ
B.1. Получение
Соединение 8
Это соединение получали с применением поли-L-орнитина-HBr/Sigma/ с мол. массой 5300-7600. Поли-L-орнитин /25 мг/ метили [3H] формальдегидом (100 мКи/ммоль) /NEN/ согласно Jentoft и Dearbon/Methods Enzymol 1983, 91: 570-579/. Реакционная смесь содержала 98 мкКи [3H] формальдегида/мл. [3H]поли-L-орнитин выделяли из реакционной смеси гельфильтрацией на Bio Gel P 2 колонке с элюцией при помощи 0,5 М NH4HCO3 и затем лиофилизировали. Ara-AMP-имидазолат соединяли с меченым полимером по способу, примененному для соединений 3 и 4.
Для последующего лактозаминирования 10 мг [3H] поли-L-орнитин-ara-AMP растворяли в 1 мл 0,1 М бура/NaOH буфере, pH вместе с 80 мг L-лактозы и 50 мг NaBH3Cl. Раствор инкубировали в течение 72 ч при 37oC. Лактозиминированный конъюгат (Lat- [3H]поли-L-орнитин ara-AMP) извлекали гель-фильтрацией на Bio Gel P2 колонке, элюированной при помощи 0,5 NH4HCO3, и затем лиофилизировали 1 мг соединения (удельная активность 668 распадов в минуту /dpm/на мкг) содержал 134 мкг a a-AMP (определено спектрофотометрически) и 604 мкг лактозы/измерено по Dubois et al. Anal Chem. 1956; 28: 350-356/. Приблизительно 90% ε\-аминогрупп полимера были замещены: 17% лекарственным средством, 73% лактозой.
B2. Экспериментальные наблюдения
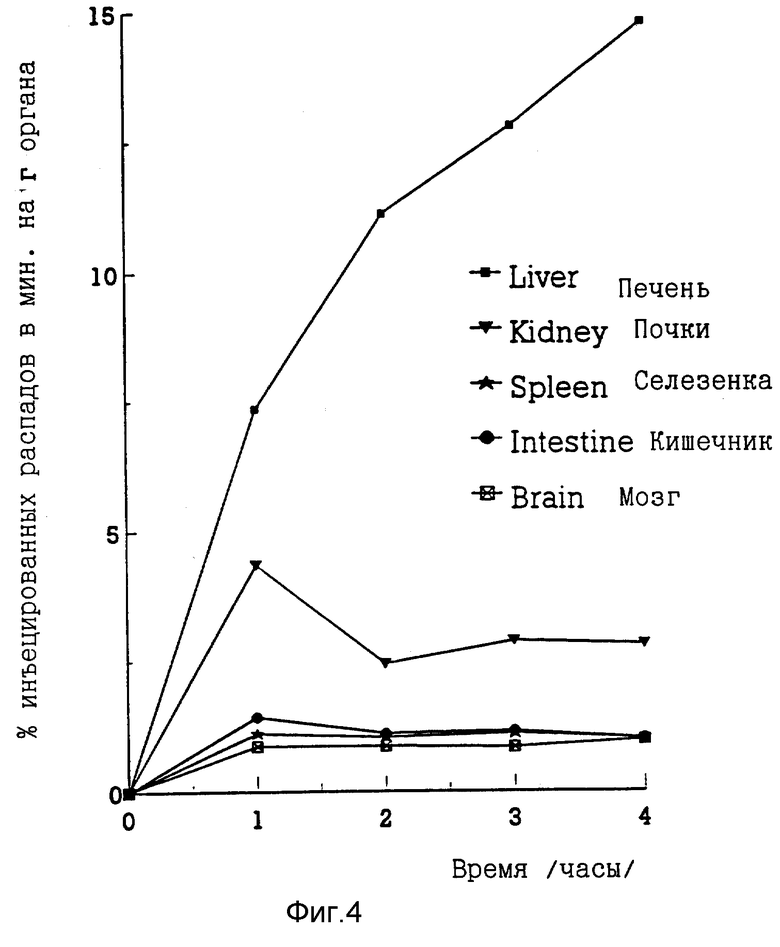
a/ - Распределение по органам соединения 8.
Фиг. 4 показывает распределение по органам радиоактивности в мышах после внутримышечной инъекции конъюгата Lat-[3H] -поли-L-орнитин-ara-AMP (36,5 мкг/г, что соответствует 5 мкг/г ara-AMP). Экспериментальная процедура была такой же, как в подобных экспериментах с конъюгатами Lat-поли-L-лизина. Уровни радиоактивности в печени выше, чем в других органах. Величины радиоактивности в почках были в 3-4 раза выше, чем в селезенке, кишечнике и мозгу.
II. Конъюгаты с высокой молекулярной массой
У больных с вирусным гепатитом введение из организма макромолекул, имеющих на конце галактозил, гораздо медленнее, чем у мышей, крыс и здоровых людей, возможно, вследствие более медленного проникновения в гепатоциты /Marshall Js, Williams S, Jones P. Seru de sialylated glycoproteins in patients with hepatobiliary dysfunctions. J. Lab Clin Med 1978; 92: 30-37; Torrani Cerenzia MR et al. J. Hepatol 1994; 20: 307-309/. Вследствие этого у этих больных можно ожидать даже более высокое почечное выведение конъюгатов, полученных с полиаминокислотами низкой мол. массы, чем измерено у мышей.
Для преодоления этого недостатка мы получили конъюгаты с применением поли-L-лизина с высокой мол. массой. В этих конъюгатах также большая часть ε -аминогрупп поли-L-лизина была замещена молекулами лекарственного средства и галактозы.
Мы наблюдали, что:
1/ Конъюгаты с высокой мол. массой также специфически проникают в клетки печени после внутримышечного введения.
2/ Почечное выведение этих конъюгатов очень низко, и вследствие этого процент инъецированной дозы, входящей в гепатоциты, выше процента, измеренного после введения конъюгатов с низкой мол. масс.
3/ Конъюгаты с высокой мол. массой лишены высокой точности и после повторного внутримышечного и внутривенного введения не индуцируют образование антител.
4/ Благодаря их высокой растворимости (более 150 мг/мл) и высокой загрузки лекарственным средством фармакологически активная доза может вводиться в малом объеме, хорошо совместимом с внутримышечным путем введения.
II. 1.Получение
Эти конъюгаты получали с применением поли-L-лизина-HBr с мол. массой 30-70000 и степенью полимеризации 145-335 (Sigma). Как и при получении конъюгатов поли-L-лизина с низкой мол. массой, лекарственные средства соединяли через имидазолат их фосфорных эфиров, а лактозу соединяли при помощи восстановительного аминирования в присутствии NaBH3CN. Однако процедура была модифицирована: pH, температура, продолжительность времени реакции, а также концентрация имидазолата увеличивалась на стадии конъюгирования лекарственного средства. Кроме того, лактозаминирование проводили перед соединением с лекарственным средством, т.к. при высоком pH поли-L-лизин высокой мол. массы осаждается, если часть ε -NH2-групп не замещена галактозными остатками.
Соединение 9
Восстановительное лактозаминирование ε -NH2-групп проводили растворением 200 мг поли-L-лизина в 20 мл 0,4 М K-фосфатного буфера с pH 7 вместе с 800 мг -лактозы и 500 мг NaBH3CN. После инкубирования при 37oC в течение 24 ч pH повышали до 8 с помощью 5 М KOH и раствор оставляли при 37oC еще на 6 ч. Lat-поли-L-лизин диафильтровали с 0,9% NaCl и концентрировали до 100 мг/мл. Лактозу измеряли способом фенол-серная кислота 1956; 28: 350-356/ с применением галактозы в качестве стандарта; полилизин определяли путем измерения азота по Къельдалю. 2 мл раствора Lat-поли-L-лизина (= 200 мг) разбавляли 2 мл 1М Na-карбонатным буфером, pH 11. 800 мг имидазолата ara-AMP, синтезированного по Лорману и Оргелю /Tetrahedron, 1978; 34: 853-855/, растворяли и pH доводили до 11 5 М NaOH.
После инкубирования при 50oC в течение 96 ч конъюгат диафильтровали с 0,9% NaCl. Химические характеристики комплекса получали спектрофотометрическим определением связавшегося лекарственного средства и измерением лактозы. Вклад ara-AMP при проведении колориметрического анализа вычитали. Содержание поли-L-лизина конъюгата рассчитывали из количества лактозы по известному отношению лактоза/поли-L-лизин, определенному перед связыванием лекарственного средства (см. выше). Это было возможно, поскольку связь между сахаром и ε -NH2-группами лизина не разрывалась во время конъюгирования лекарственного средства, как было проверено экспериментально. Конъюгат концентрировали в солевом растворе (0,9% NaCl) до 150 мг/мл и лиофилизировали после замораживания приблизительно до -80oC. Концентрацию конъюгата рассчитывали, не принимая во внимание противоионы.
Перед применением конъюгат Lat-поли-L-лизин-ara-AMP разбавляли водой при концентрации 150 мг/мл. Он легко растворялся при условии, что замораживание было быстрым. При необходимости конъюгат разбавляли 0,9% NaCl.
Соединение 10
Перед соединением с ara-AMP Lat-поли-L-лизин метили [3H]формальдегидом /NEN/ согласно Jentoft и Dearbon/Methods Enzymol 1983; 91: 570-579/. Реакционная смесь содержала 78 мкКи [3H]формальдегида/мл. После диафильтрования с 0,9% NaCl Lat-[3H]поли- -лизин конъюгировали с a a-AMP, как описано выше.
Соединение 11
Рибаварин (RIBV) (1- β -D-рибофуранозил-1,2,4-триазол-3- карбоксамид) сначала фосфорилировали (RIBVMP) согласно /Allen LB, Boswell KH, Khwaja TA, Meyer RB, Sidwell RW, Witkowski JT. Synthesis and antiviral achivity of some phosphates of the broad-spectrum antiviral nucleoside I β-D-Ribofuranosyl-1,2,4-triazole-3-carboxamide /Ribavarin/. J. Med Chim 1978; 21: 742-746/.
Затем соль пиридиния этого фосфорилированного производного превращали в имидазолат /Lormann and Orgel Tetrahedron 1978; 853-855/, который соединяли с Lat-[3H] поли-L-лизином, как описано для конъюгата с ara-AMP. В этом конъюгате количество соединенного RIBVMP измеряли по органическому фосфату согласно /Ames BN, Assay of inorganic phosphate. Total phosphate and phosphatases. Methods Enzymol 1966; 8: 115-118/.
Вследствие сильных помех, вызываемых RIBV при колориметрическом определении сахара, невозможно было измерить лактозу, как описано для Lat-поли-L-лизин-ara-AMP, и потому определяли содержание Lat[3H]поли-L-лизина конъюгата подсчетом радиоактивности.
Соединение 12
3'-азидо-3-[2-14С] деокситимидин ([14C] AT) (Moravek) фосфорилировали согласно Yoshikawa et al./Tetrahedron Lett 1967; 50: 5065-5068/. Соль пиридиния фосфорилированного производного превращали в имидозалат и затем соединяли с Lat-поли-L-лизином. Соединение проводили, как описано для соединения 9, но в реакционной среде отношение количества имидазолата лекарственного средства к количеству полимера было 2,7 вместо 4. Химическую характеристику этого конъюгата выполняли, как описано для соединения 9.
Соединение 13
Этот конъюгат получали, как соединение 9, но лактозаминирование поли-L-лизина прерывали после первых 24 ч. Кроме того, отношение количества имидазолата ara-AMH к количеству полимера было 4,6 вместо 4. 30% ε -аминогрупп этого полимера были замещены галактозильными остатками и 64% были замещены ara-AMP.
11.2. Экспериментальные наблюдения.
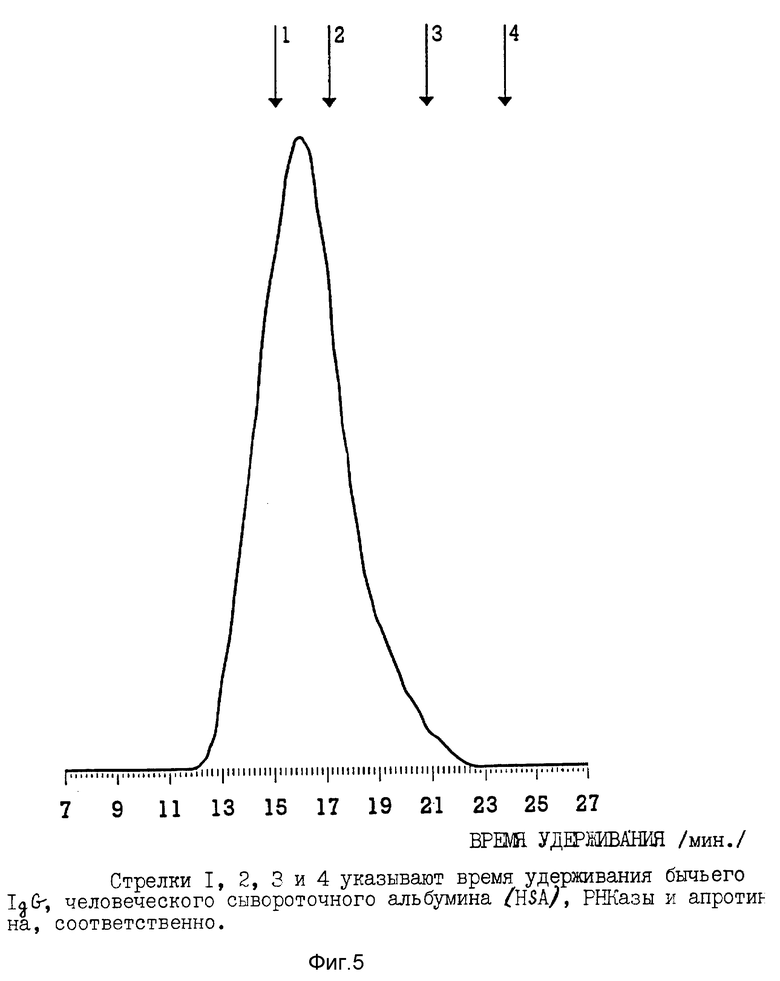
a/ - Средние мол. массы соединения 9.
Их определяли при помощи проникающей хроматографии с применением оборудования HPLC (ЖХВР) (Waters) с двумя соединенными колонками Protein-Pak (125 и 300 SW). Соединения 9 (80 мкг) растворяли в 20 мкл подвижной фазы (125 мМ Na2SO4 + 2 мМ NaH2PO4 • H2O, доводили до pH 6,0 0,1N NaOH, фильтровали и дегазировали) и хроматографировали при следующих условиях. Скорость потока: 0,9 мл/мин; детектирование: УФ при 260 нм, 0,1 единиц поглощения на всю шкалу (AUFS). Колонки калибровали апротинином (Mr 6500), РНКазо (Mr 13700), HSA (человеческий сывороточный альбумин) /Mr 69000/ и IgG (Mr 158000). Среднемассовую молекулярную массу и среднечисловую молекулярную массу определяли с применением GPC 745/745B Waters Software. Они были равны 140339 и 72419 соответственно. Гель-проникающая хроматография соединения 9 показана на фиг. 5.
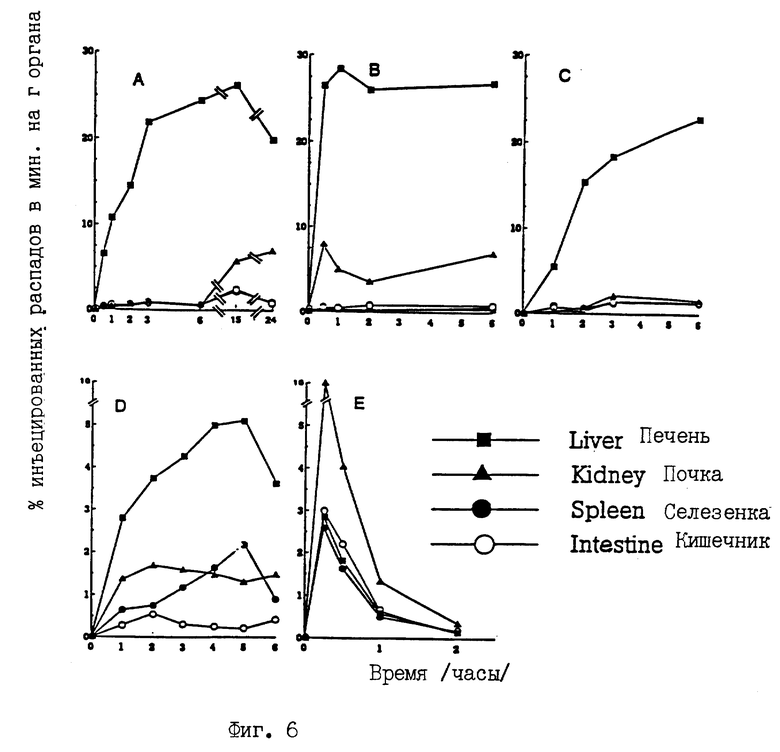
b/ - Распределение соединений по органам.
Применяли экспериментальную процедуру, описанную для подобных экспериментов с конъюгатами низкой мол. массы. Результаты представлены на фиг. 6.
Конъюгаты ara-AMP и RIBVMP были радиоактивны в носителе, в то время как конъюгат AZTMP был меченым в молекуле лекарственного средства.
После внутримышечного введения конъюгатов, меченых в носителе (фиг. 6, A, C), радиоактивность была высокой в печени и низкой в селезенке, кишечнике и почках. Проценты инъецированной радиоактивности (dpm), извлеченной в почках, были в 10-20 раз ниже, чем измеренные после внутримышечного введения комплексов, полученных с поли-L-лизином низкой мол. массы. Поскольку почечное накопление белков является следствием их гломерулярной фильтрации /Maack TH, Johnson V, Kau ST, Figuereido J, Sigulem D. Renal filtration, transport, and metabolism of lew-moleculra weigt proteins: A review. Kidney Int 1979; 16: 251-270/, данный результат показывает, что, как и ожидалось, только малые количества конъюгатов высокой мол. массы проходили через почечные клубочки, по меньшей мере после внутримышечного введения (см. ниже).
У мышей, инъецированных внутримышечно конъюгатом Lat-поли-L-лизин-[14C] AZTMP, уровень радиоактивности в печени был в 2,5-6 раз выше, чем в почках, селезенке и кишечнике (фиг. 6, 1). Различие между количеством радиоактивности в печени и в других органах было менее заметным, чем у животных, которым вводили конъюгаты, меченые в носителе (фиг. 6, A, C). Этот результат, возможно, обусловлен частичным выделением лекарственного средства (и (или) его метаболитов/ из клеток печени в кровоток после внутриклеточного расщепления связи между лекарственным средством и носителем. Подобное выделение лекарственного средства из клеток печени в кровоток наблюдали после введения других гепатотропных конъюгатов лекарство/носитель /Fiume L, Busi C, Corzani S, Di Stefano G, Gervasi GB, Mattioli A. Organ distribution of a conjugate of adenine arabinos de monophos-Phate with lactosaminated albumin in the rat. J. Hepatol 1994, in press; Fiume L, Mattioli A, Balboni A, Tognon M, Barbanti-Bradano G, De Vries J and Wiel and Th. Enhanced inhibition of virus DNA synthesis by hepatocytes by trifluorothymidine coupled to asialofetuin. FEBS Lett 1979; 103: 47-51/.
При внутримышечной инъекции свободного [14C]AZTMP мышам радиоактивность одинаково распределялась в печени, селезенке и кишечнике с более высокими величинами в почках (фиг. 6, E). Скорость накопления и снижения радиоактивности после введения свободного или связанного [14C]AZTMP была различной. После инъекции свободного лекарственного средства радиоактивность накаливалась в тканях в течение первых 15 минут и затем быстро снижалась; после инъекции конъюгированного лекарственного средства радиоактивность в печени увеличивалась до 4-5 ч. При 1-2 ч количества радиоактивности в печени были выше в животных, инъекцированных конъюгированным [14C] A TMP при дозе 2 мкг/г, чем в животных, которым вводили 5 мкг/г свободного лекарственного средства.
У мышей, инъецированных внутривенно Lat-[3H]поли-L-лизин-ara-AMP (фиг. 6, B), конъюгат быстро накапливался в печени; у этих животных радиоактивность в почках была выше, чем у тех, которые получили тот же самый конъюгат внутримышечно (фиг. 6, A). Это можно объяснить с учетом того,
что:
/i/ часть молекул конъюгата имела мол. массу более низкую, чем мол. масса HSA (человеческого сывороточного альбумина) /фиг. 5/;
/ii/ существует прямая зависимость между концентрацией плазмы и гломерулярной фильтрацией малых белков /Maack TH al Kidney Int 1979; 16: 251-270/;
/iii/ концентрация конъюгата в плазме, которая постоянно низка (менее 0,9 мкг/мл) после внутримышечного введения, достигает высоких величин после внутривенной инъекции (104 мкг/мл при 3 мин).
c/ - Эксперименты по толерантности к лекарственному средству и иммуногенности.
Эксперименты проводили с применением соединения 9. Конъюгат, введенный внутривенно (i. v.) 5 мышам в дозе 1,5 г/кг, не вызвал какого-либо признака страдания. 1,5 г Lat-поли-L-лизин-ara-AMP содержали 480 мг лекарственного средства (см. таблицу 2), дозу в 300 раз более высокую, чем доза, при которой ara-AMP, конъюгированный с L-HSA, ингибирует рост вируса у инфицированных HB больных. У мышей LD50 поли-L-лизина, примененного для получения конъюгата, при внутривенном введении в виде соли HCl была между 15 и 30 мг/кг. Для выяснения, может ли Lat-поли-L-лизин-ara-AMP, растворенный в солевом растворе в концентрации 150 мг/мл, разрушать ткани в месте введения, проводили эксперимент по первичному раздражению глаз у 6 кроликов путем помещения 0,1 мл этого раствора в конъютивальный мешочек. Ни у одного животного не наблюдали изменений в глазах.
Полутонкие срезы печени из мышей и крыс, которые получили Lat-поли-L-лизин-ara-AMP, введенный по различным схемам (см. таблицу 3), наблюдали под световым микроскопом, ни в одном из этих животных не обнаружили изменений ни в паренхимных, ни в синусоидальных печеночных клетках. Накопление во вторичных лизосомах неполностью расщепленных молекулах (дисахаридов, пептидов), которые не могут проходить через мембрану лизосом, приводит к быстрому набуханию этих органелл, которые в световом микроскопе выглядят как цитоплазматические вакуоли. Такие вакуоли наблюдали в печеночных клетках мышей и крыс через 24 ч после одного введения L-HSA-ara-AMP при дозах в 5-10 раз более высоких, чем дозы, которые активны в инфицированных HBV больных /Fiume L, Betts CM, Busi C, Corzani S, Derenzini M, Di Stefano G, Mattioli A. The pathogenesis of vacuoles produced in rat and mouse liver cell by a conjucate of adenine arabinoside monophosphate with lactosaminat albumin. J. Hepatol 1992; 15: 314-322/. Отсутствие вакуолей в печеночных клетках мышей и крыс после введения высоких доз Lat-поли-L-лизин-ara-AMP дало косвеннное доказательство быстрого расщепления этого конъюгата до продуктов, способных проходить через мембрану лизосом.
Для исследования иммуногенности Lat-поли-L-лизин-ara-AMP 24 мыши получали конъюгат 5 дней в неделю в течение 4 последовательных недель (одна дневная доза - 200 мкг/животное). Двенадцать мышей инъецировали внутримышечно и двенадцать внутривенно. Через неделю после последней инъекции проводили кровоизвлечение и антитела против конъюгата измеряли, как описано для конъюгатов низкой мол. массы. Ни одно из животных не образовывало антител в количествах, детектируемых в нашем анализе (чувствительность приблизительно 0,5 мкг IgG/мл сыворотки).
Из предшествующих экспериментальных данных можно считать наиболее вероятно доказанным, что конъюгаты антивирусных нуклеозидов с галактозилированным поли-L-лизином, в которых большая часть ε-аминогрупп гомополимера замещена галактозными остатками и лекарственными средствами, при внутримышечной инъекции осуществляют доставку лекарственных средств в печень без образования антител.
Конъюгаты не обладают сильной токсичностью поли-L-лизина, применяемого для их приготовления. По сравнению с конъюгатами с лактозаминированным альбумином, которые нужно вводить внутривенным инъецированием, поскольку при ином введении они иммуногенны, конъюгаты, полученные с использованием галактозилированного поли-L-лизина, потенциально способны, при инфекции печеночными вирусами, улучшить соблюдение больными режима и схемы лечения с длительным введением антивирусного состава.
Как уже упоминалось, все вышесказанное касается конъюгатов, в которых носителем был поли-L-лизин или поли-L-орнитин экспериментально проверенные физико-химические свойства и биологическое поведение делают приемлемым идентичное использование в качестве носителей других полиаминокислот.
Поэтому подобные другие конъюгаты попадают в сферу действия данного изобретения так же, как применение таких полиаминокислот в качестве носителей для приготовления гепатотропных конъюгатов с антивирусными соединениями, введение которых иным путем было бы серьезно затруднено неблагоприятными побочными явлениями, вызываемыми высокой токсичностью для других органов, иных чем печень.
Животных убивали через 24 часа после последней инъекции. Пробы печени фиксировали и полутонкие срезы окрашивали, как описано в /Fiume L., Betts M. C. , Busi C., Corzani S., Derenzini M., Di Stefano G.,Mattioli A., J./ Hepatol 1992; 15: 314-322/.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ РАСТВОРИМЫХ КОВАЛЕНТНЫХ КОНЪЮГАТОВ | 1994 |
|
RU2127606C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОКОНЪЮГАТОВ НА ОСНОВЕ ПОЛИКАТИОНОВ, ПРИГОДНЫХ ДЛЯ ТРАНСПОРТИРОВКИ В ОРГАНИЗМ РАЗЛИЧНЫХ ВИДОВ АКТИВНЫХ ВЕЩЕСТВ | 2000 |
|
RU2250782C2 |
| БИОЛОГИЧЕСКИ АКТИВНЫЕ ПРОИЗВОДНЫЕ ПЕПТИДА VAPEEHPTLLTEAPLNPK | 2005 |
|
RU2377249C2 |
| Гибридные белки и белковые конъюгаты на основе белка теплового шока-70 (БТШ70) и способы их применения (варианты) | 2012 |
|
RU2685867C2 |
| САЙТ-СПЕЦИФИЧЕСКАЯ КОНЪЮГАЦИЯ АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО ПОСРЕДСТВОМ ГЛИКОИНЖЕНЕРИИ | 2014 |
|
RU2711935C2 |
| ЛИГАНДНЫЕ СОЕДИНЕНИЯ, КОНЪЮГАТЫ И ИХ ПРИМЕНЕНИЕ | 2021 |
|
RU2819894C1 |
| КОНЪЮГАТЫ ИНТЕРФЕРОНА | 1997 |
|
RU2180595C2 |
| КОНЪЮГАТЫ ЭТОПОЗИДА И ДОКСОРУБИЦИНА ДЛЯ ДОСТАВКИ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2009 |
|
RU2531591C2 |
| Композиция системы доставки на основе конъюгата для доставки полинуклеотида РНК-интерференции в клетку печени и способ ее получения | 2011 |
|
RU2623160C9 |
| КОНЪЮГАТ АНТИ-TROP2 АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2014 |
|
RU2705367C2 |
Изобретение относится к медицине, а именно к способу получения гепатотропных конъюгатов, которые осуществляют доставку лекарственных веществ в печень и фармацевтической композиции, содержащей конъюгаты. Антивирусные лекарства, такие как ara-АМФ, ацикловир и т.п., конъюгированы с носителем, выбранным из полиаминокислот и, в частности с поли-L-лизином или поли-L-орнитином, в которых большая часть аминогрупп, которые не замещены антивирусными лекарствами, замещена галактозными молекулами, используются при лечении гепатита. Конъюгат и фармацевтическая композиция, содержащая его, обеспечивают снижение токсичности и отсутствие образования антител при внутримышечном введении. 4 с. и 11 з.п.ф-лы, 6 ил., 3 табл.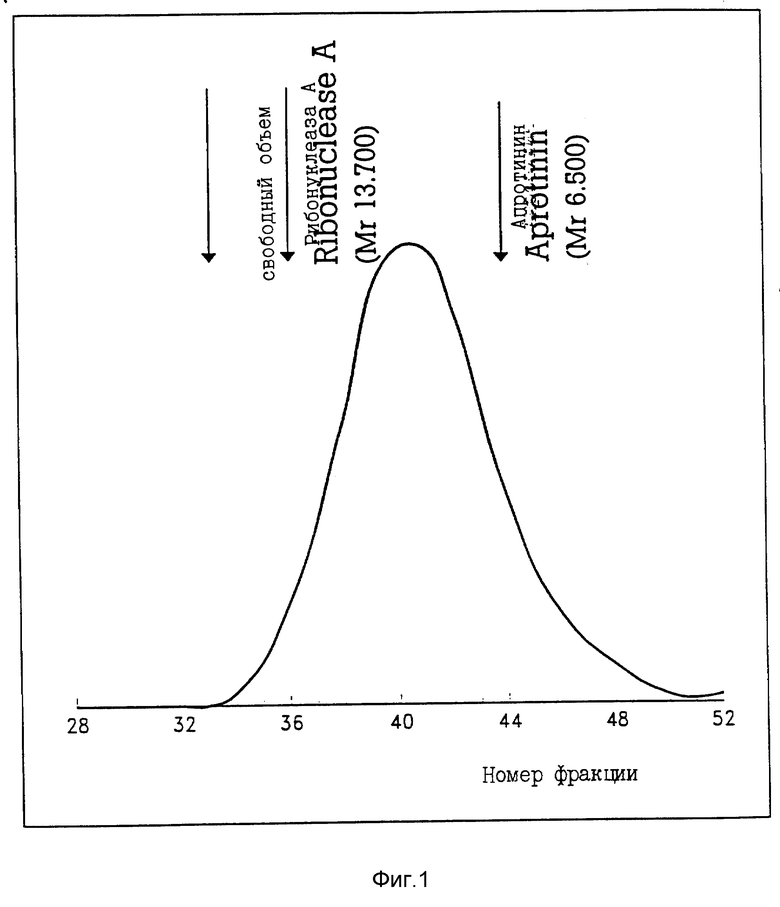
| J.Fiume et al - FEBS LETTERS, 1986, v.203, N 2, p.203 - 206 | |||
| RU 94016158 A1, 27.09.95 | |||
| Автоматический огнетушитель | 0 |
|
SU92A1 |
Авторы
Даты
1999-10-27—Публикация
1994-05-24—Подача