Изобретение относится к области биологических окислителей, т.е. к биокатализаторам, которые могут быть использованы для окислительной деструкции вредных органических соединений, например тиодигликоля.
Наиболее близким из уровня техники аналогом являются клетки уксуснокислых бактерий Gluconobacter oxydans, используемые в качестве биокатализаторов для микробиологической деструкции тиодигликоля [1] . Для этого в водные растворы тиодигликоля объемом 50 мл с концентрацией от 0,2 мас.% до 10 мас.% вносили биомассу бактерий Gluconbacter oxydans, количество которой варьировали от 0,8 до 5,0 г АСБ/л (абсолютно сухих бактерий) (вес абсолютно сухих бактерий определяют с помощью высушивания до постоянной массы при температуре 105oC). Измерение окислительной деструкции проводили периодически через 3, 5, 9, 15, 20, 24, 72 ч. В результате происходит окислительная трансформация тиодигликоля на 98+2% в течение 3 ч при концентрации тиодигликоля в растворе 0,2%, в течение 9 ч при концентрации тиодигликоля в растворе 1,5%, на 85% через 24 ч при концентрации тиодигликоля в растворе 3% и на 46% за 72 ч при концентрации тиодигликоля в растворе 10%. Жизнеспособность клеток Gluconobacter oxydans в суспензии снижается через 24 ч до 80-85% при исходной концентрации тиодигликоля в растворе 0,2 мас.% до 70-75% при исходной концентрации тиодигликоля в растворе 1,5 мас.% и до 25-30% при исходной концентрации тиодигликоля в растворе 10 мас.%.
Состав кислых продуктов трансформации тиодигликоля изучали методом тонкослойной хроматографии на пластинках "Silufol" в системе растворителей пропанол: аммиак (80: 20 по объему) в качестве индикатора использовали 0,8% спиртовой раствор бромкрезолового зеленого [2], а также методом ЯМР13 спектроскопии на Brueer AC-200 ЯМР-спектроскопе. Наличие тиодигликоля в растворе определяли на пластинках "Silufol" в системе растворителей хлороформ: метанол (10: 1 по объему), индикатор 1% раствор KMnO4 в 6% растворе Na2CO3 [3]; количественное содержание определяли на хроматографе "Хром - 104" с плазменно-ионизационным детектором при следующих условиях: температура испарителя 250oC; температура термостата колонок 200oC; колонка кварцевая капиллярная длиной 25 м и внутренним диаметром 0,2 мм с неподвижной жидкой фазой E-30; скорость потока газа носителя (азота) через колонку 1 см3/мин, в линии поддува детектора 30 см3/мин; скорость потока воздуха 300 см3/мин. Для обсчета полученных хроматограмм использовали систему автоматизации анализа CAA-05-01 [1].
Основным недостатком известного биокатализатора является низкая до 25-30% окислительная способность при высоких концентрациях тиодигликоля в растворе. (Часто в производственных условиях возможны выбросы в окружающую среду тиодигликоля с высокой концентрацией, т.к. он является основным продуктом гидролиза в водной среде высокотоксичного вещества иприта, что приводит к загрязнению окружающей среды и экологической нестабильности, кроме того, повышение концентрации тиодигликоля может появится в окружающей среде на отделочно-красильных производствах).
Вторым существенным недостатком известного биокатализатора является малая продолжительность жизнедеятельности клеток в соответствии с этим неудобства проведения технологического процесса. Через 24 ч содержание жизнеспособных клеток Gluconobacter oxydans в суспензии снижается до 25-30 % при концентрации тиодигликоля 10% в растворе.
Техническим результатом заявляемого изобретения является повышение каталитической активности с одновременным увеличением срока службы.
Технический результат достигается тем, что биокатализатор на основе клеток Gluconobacter oxydans дополнительно содержит в качестве носителя мезопористое углеродное волокно, насыщенное соединениями серебра или меди по всей глубине волокна при содержании соединений металла 3-6 мас.%, а содержание клеток на волокне, находящееся в зависимости от содержания металла в волокне, определяют по формуле
Cк = -0,025 Cм 2 + 0,235 Cм - 0,38,
где Cк - содержание клеток на волокне, г АСБ/1 г волокна,
Cм - содержание металла в слое волокна, %.
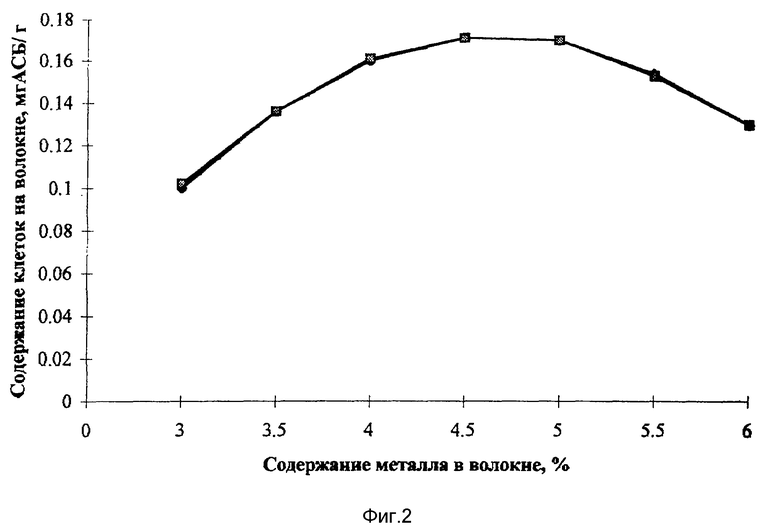
В отличие от прототипа в заявленном изобретении, используя в качестве дополнительного носителя углеродное волокно со специфическими свойствами с закрепленными на нем клетками Gluconobacter oxydans, достигается повышенная окислительная способность не только при незначительных концентрациях тиодигликоля, но и при более высоких концентрациях (10%). Это происходит за счет того, что при взаимодействии мезопористого углеродного волокна с металлом образуются особые микрообласти во всем объеме волокна, что подтверждается данными рентгеноструктурного анализа [4], а также данными РЭС [4] и данными электронной микроскопии [5] (фиг. 1). Эти микрообласти обладают электрофизическими свойствами, в частности способностью образовывать донорно-акцепторные связи с поверхностью биоклеток и легко вступать в окислительно-восстановительные реакции с органическими молекулами белков, что подтверждается данными. Экспериментальные данные показали (фиг. 2), что содержание клеток на волокне зависит от содержания металла в волокне и определяется формулой
Cк= -0,025 Cм 2 + 0,235 Cм - 0,38,
где Cк - содержание клеток на волокне, г АСБ/1 г волокна,
Cм - содержание металла в слое волокна, %.
Экспериментально подтверждено, что эта структура обеспечивает связь с клетками Gluconobacter oxydans, что проявляется в их повышенной окислительной активности, т.е. происходит инициирование окислительно-восстановительной активности клетки.
Кроме этого, вся система сохраняет не только повышенную каталитическую активность, но и обеспечивает длительную жизнеспособность клетки, что приводит к увеличению срока службы биокатализатора.
Использование биокатализатора в форме "носитель-клетка" обеспечивает удобную технологическую эксплуатацию в производственных условиях, например, в виде фильтрующего материала.
Способ получения биокатализатора заключается в следующем: мезопористое углеродное волокно, полученное на основе вискозы с удельной поверхностью 1500-1800 м2г (Содержание мезопор определяли по методике [6]), обрабатывают солями металлов (серебро или медь). Для этого берут 1% раствор AgNO3, или 1% раствор CuSO4, или CuCl2. Обработку ведут при pH 5,8-6,2 в течение 2 ч, при комнатной температуре, а затем сушат при температуре 150oC. Полученный материал содержит 3-6 мас.% металла, распределенного по всему объему волокна. При обработке металл распределяется по всей глубине слоя волокна, что подтверждается данными рентгено-структурного анализа, РЭС и электронной микроскопии.
Сорбцию клеток проводили из суспензий с концентрацией 1,5 г АСБ/л в статических условиях при перемешивании на качалке 230 об/мин, при pH 5,8-6,2, при температуре 28oC в течение 24 ч. Для этого навеску волокна массой 100 мг погружали в суспензию клеток объемом 30 мл. Полученный биокатализатор содержит 0,1-0,17 г АСБ на 1 г носителя. Содержание Gluconobacter oxydans на волокне определяли по весу абсолютно сухой биомассы. Полученный по такому способу биокатализатор использовали для окислительной трансформации тиодигликоля. Для этого 0,1 г биокатализатора погружали в раствор тиодигликоля объемом 50 мл с концентрацией от 0,2% до 10% при температуре 28oC, pH 5,8-6,2. Определяли степень трансформации тиодигликоля по методике [2, 3] через 3, 5, 9, 15, 20, 24, 72 ч.
Полученные результаты представлены в таблице.
Уменьшение содержания металла в волокне (< 3 мас.%) нецелесообразно, т. к. уменьшается степень окисления тиодигликоля.
Увеличение содержания металла в волокне (> 6 мас.%) также нецелесообразно, т. к. не приводит к улучшению технического результата, а кроме того, это связано с увеличением расхода соли металла.
Формула дает соотношение содержания металла в волокне и клеток на волокне, при котором достигается оптимальное содержание клеток на волокне, обеспечивающее высокую степень окисления тиодигликоля, что и подтверждается примерами таблицы. Изменение соотношения, представленного в формуле, т.е. когда содержание клеток Gluconobacter oxudans на волокне не отвечает приведенной зависимости, приводит к снижению каталитической активности получаемого биокатализатора.
| название | год | авторы | номер документа |
|---|---|---|---|
| КАТАЛИЗАТОР ДЕСТРУКЦИИ ОРГАНИЧЕСКИХ РАСТВОРИТЕЛЕЙ | 1998 |
|
RU2141381C1 |
| СПОСОБ ПОЛУЧЕНИЯ МЕТАЛЛСОДЕРЖАЩЕГО УГЛЕРОДНОГО СОРБЕНТА | 1998 |
|
RU2142336C1 |
| СПОСОБ КАРБОНИЗАЦИИ ШЕРСТЯНОГО МАТЕРИАЛА | 2000 |
|
RU2178020C2 |
| СПОСОБ ПОЛУЧЕНИЯ РАСТВОРА СВЕРХВЫСОКОМОЛЕКУЛЯРНОГО ПОЛИЭТИЛЕНА | 1997 |
|
RU2121483C1 |
| ТЕКСТИЛЬНЫЙ ОБЪЕМНЫЙ ВОЛОКНИСТЫЙ КАТАЛИЗАТОР | 1997 |
|
RU2118908C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ТЕКСТИЛЬНОГО КАТАЛИЗАТОРА НА ПОДЛОЖКЕ ИЗ СТЕКЛОВОЛОКОН | 1998 |
|
RU2134613C1 |
| СПОСОБ ПОЛУЧЕНИЯ РАСТВОРОВ ЦЕЛЛЮЛОЗЫ | 1999 |
|
RU2156265C1 |
| СПОСОБ ВЫДЕЛКИ КОЖИ ИЗ ШКУР РЫБ | 2000 |
|
RU2172778C1 |
| СПОСОБ ОЧИСТКИ ПРИРОДНЫХ И СТОЧНЫХ ВОД ОТ НЕФТЕПРОДУКТОВ | 1993 |
|
RU2063386C1 |
| СПОСОБ ПОЛУЧЕНИЯ РАСТВОРОВ ЦЕЛЛЮЛОЗЫ | 2000 |
|
RU2184750C2 |



Изобретение относится к биокатализаторам, которые могут быть использованы для окислительной деструкции вредных органических соединений, например тиодигликоля. Биокатализатор на основе клеток Gluconоbacter oxydans содержит в качестве носителя мезопористое углеродное волокно, насыщенное соединениями серебра или меди по всей глубине волокна. Содержание соединений металла 3-6 мас. %, а содержание клеток на волокне находится в зависимости от содержания металла в волокне, которые определяют по формуле Ск = -0,025 См 2+0,235 См -0,38, где Ск - содержание клеток на волокне, г АСБ/1 г волокна; См - содержание металла в слое волокна, %. Преимуществом изобретения является повышение каталитической активности с одновременным увеличением срока службы. 2 ил., 1 табл.
Биокатализатор для окислительной деструкции тиодигликоля на основе клеток Gluconobacter oxydans, отличающийся тем, что он дополнительно содержит в качестве носителя мезопористое углеродное волокно, насыщенное соединениями металлов - серебра или меди по всей глубине слоя волокна, при содержании металла 3 - 6 мас.% и содержании клеток на волокне, определяемом по формуле в зависимости от содержания металла в волокне
Cк = - 0,025 Cм 2 + 0,235хСм - 0,38,
где Cк - содержание клеток на волокне, г АСБ/1 г волокна;
См - содержание металла в слое волокна, %.
| Медведева Н.Г., Сухаревич В.И., Федорова Н.В., Гриднева Ю.А | |||
| Трансформация тиодигликоля уксуснокислыми бактериями | |||
| - Биотехнология, 1996, N 2, с.44-47 | |||
| Kersters K., De Ley J | |||
| - Biochim | |||
| et Biophys | |||
| Acta, 1963, V.71, N 2, p.311-331 | |||
| Munavalli S., Panella M.J | |||
| of Chromotographi, 1988, N 437, p.423-428 | |||
| Уманский Я.С., Спаков Ю.А., Иванов А.Н | |||
| и др | |||
| Кристаллография, рентгенография и электронная микроскопия | |||
| - М.: Металлургия, 1982, с.631 | |||
| Шимель Г | |||
| Методика электронной микроскопии | |||
| - М.: Мир, 1972, 300 с | |||
| Кельцев Н.В | |||
| Основы адсорбционной технологии | |||
| - М.: Химия, 1967, 511 с. |
Авторы
Даты
1999-11-27—Публикация
1998-07-29—Подача