Изобретение относится к медицине, а именно к токсикологии, и может быть, в частности, использовано для лечения острых отравлений.
Из практики медицины известен способ лечения острых отравлений эссенциале ("Бюллетень экспериментальной биологии", Влияние гепатопротектеров на метаболизм липидов при CCl4-гепатите. А.И.Вегнеровский, В.С.Чучалин, О.В.Пауль, А.С.Саратиков. N 4, 1987), состоящий во введении экспериментальным животным ампульного раствора эссенциале после отравления CCl4. Однако этот способ имеет существенные недостатки: не влияет на реологические свойства крови, не участвует в транспорте кислорода к ишемизированным тканям, не обладает сорбционным, антитоксическим и дезагрегирующим действием, не купирует явления ДВС-синдрома, "сладжа" эритроцитов, требует длительного применения (более 4-х раз).
Известен, также, способ лечения острых отравлений, состоящий в парэнтеральном применении реополиглюкина (Е. А. Лужников.Клиническая токсикология. 1994, М. : Медицина), состоящий в парэнтеральном применении реополиглюкина после отравлений различной этиологии. Однако этот способ имеет следующие недостатки: препарат не обладает газотранспортной функцией, имеет противопоказания при патологии, часто встречающейся при отравлениях прижигающими жидкостями (кровотечения), опасен возникновением осложнений - осмотический нефроз - при использовании в качестве лечебного средства более 3-х суток подряд, выводится почками, а следовательно, ограничено его использование при олигоанурии.
Наиболее близким прототипом к предлагаемому способу является применение при острых отравлениях гипербарической оксигенации (Кашуба Э.А. Влияние гипербарической оксигенации на течение острого и подострого поражения печени четыреххлористым углеродом в эксперименте. Воронежский государственный медицинский институт, автореферат на соискание ученой степени кандидата мед. наук, 1976 г.), состоящий в том, что экспериментальных животных после затравки 50%-ным раствором четыреххлористого углерода (CCl4), подвергали оксигенобаротерапии в барокамере при давлении 3 атм, через день в течение 15 дней. На 5-е сутки (2 сеанса) авторами отмечено лишь восстановление массы печеночной паренхимы, и только на 15-е сутки (7 сеансов) не определялось зон некроза, но сохранялась дистрофия гепатоцитов, проявляющаяся вакуолизацией цитоплазмы, изменением ее тинкториальных свойств, пикнозом ядер; указывается, что дистрофические изменения сохраняются и к 30-м суткам опыта (15 сеансов оксигенации).
Однако известный способ имеет следующие недостатки:
- не позволяет насыщать кислородом сосуды микроциркуляторного русла, не увеличивая доставку кислорода к ишемизированным тканям через спавшиеся, спазмированные, закупоренные эритроцитарными "пробками" сосуды;
- имеет прямую зависимость от количества эритроцитов в кровяносном русле, в которых происходит химическое растворение кислорода;
- не улучшает реологии крови,
- не купирует явления "сладжа" эритроцитов, ДВС синдрома;
- имеется возможность возникновения осложнений, связанных с передозировкой кислорода;
- длительность проведения самой процедуры, необходимость ее многократного применения для получения лечебного эффекта (более 5 раз), таким образом положительный эффект достигается в срок не менее 15 суток;
- требует применения дорогостоящего стационарного, сложного в обслуживании оборудования, специально обученного персонала.
Целью предлагаемого изобретения является повышение эффективности лечения токсического поражения организма путем насыщения микроциркуляторного русла кислородом, увеличения полезной площади капиллярного массообмена, улучшения реологических свойств крови за счет снижения ее вязкости, уменьшения агрегации тромбоцитов и эритроцитов, повышения устойчивости клеточных мембран к действиям химических, механических и термических факторов, активации дезинтоксикационной функции печени.
Поставленная цель достигается в изобретении тем, что после отравления CCl4 экспериментальным животным вводят парэнтерально перфторуглеродную эмульсию (Перфторан) двухкратно через день в дозе 6-12 мл/кг.
Предлагаемый способ введения разработан в эксперименте на мышах - 200 шт. Эмульсия Перфторан взята авторами в качестве лечебного средства при острых токсических поражениях в связи с тем, что она обладает рядом уникальных свойств и, в первую очередь, способна переносить кислород, а т.к. ишемия и гипоксия внутренних органов играет важную роль в патогенезе острых отравлений это свойство препарата оказалось перспективным в плане терапии токсических поражений; эмульсия также способна повышать устойчивость клеточных мембран к действию повреждающих химических, механических и термических факторов, обладает антигемолитическим действием, улучшает реологические свойства крови в результате снижения вязкости, уменьшения агрегации тромбоцитов и эритроцитов. Способ введения эмульсии - внутрибрюшинный - выбран в связи с малыми размерами экспериментальных животных и возможностью всасывания Перфторана из брюшной полости в кровеносное русло, местным воздействием на органы брюшной полости, в частности, на печень - выполняющую дезинтоксикационную функцию. Способ отравления экспериментальных животных выбран в связи с тем, что модель токсического поражения четыреххлористым углеродом общеизвестна и принята во всем мире по литературным данным. Отравление животных сероводородом выбрано из тех соображений, что Астраханская область входит в сеть газоперерабатывающих предприятий страны и промышленный газ Астраханского месторождения характеризуется высоким содержанием сероводорода, а также в связи с тем, что до настоящего времени не существует сколько-нибудь эффективной методики терапии острых отравлений сероводородом. Доза и кратность введения препарата Перфторан (6-12 мл/кг дважды через день, после отравления) была выбрана опытным путем - животных разбили на 12 групп, различавшихся по дозе и кратности введения: на введение меньшего количества (менее 6 мл/кг) препарата достоверного эффекта от терапии выявлено не было, наиболее выраженный эффект, как по клиническим (осмотр животных) и биохимическим (определение аланиновой и аспаргиновой трансаминаз) данным, так и но данным патоморфологического исследования выявлен на дозу препарата от 6 до 12 мл/кг, при этом отмечено, что увеличение дозы свыше 12 мл/кг не ведет за собой улучшения всех показателей, т.е. доза 12 мл/кг является своеобразным пределом насыщения организма Перфтораном, за которым не наблюдается дальнейшего улучшения клинических, биохимических и патоморфологических показателей. Экспериментальным же путем выявлена неэффективность предварительного введения препарата перед отравлением.
Предлагаемый способ позволяет: насыщать кислородом не только общий кровоток, но и микроциркуляторное русло; увеличивает доставку кислорода к ишемизированным тканям через спавшиеся и спазмированные сосуды за счет меньшего размера частиц эмульсии по сравнению с эритроцитом, насыщение кровеносного русла кислородом не зависит от количества эритроцитов, т.к. происходит не химическое, а физическое растворение этого газа; улучшает реологию крови; купирует явления "сладжа" эритроцитов, ДВС-синдрома; длительность проведения самой процедуры не превышает по длительности обычное внутривенное введение растворов, для получения лечебного эффекта достаточно двукратного введения эмульсии; препарат выводится, в основном, через легкие и небольшое количество через желудочно-кишечный тракт, таким образом не обладает токсическим действием на почки и не имеет противопоказаний при токсической нефропатии, не ограничен в применении при кровотечениях; не требует применения дорогостоящего стационарного, сложного в обслуживании оборудования и специально обученного персонала, легко дозируется, что позволяет индивидуально подобрать дозу препарата и избежать побочных явлений, связанных с передозировкой кислорода.
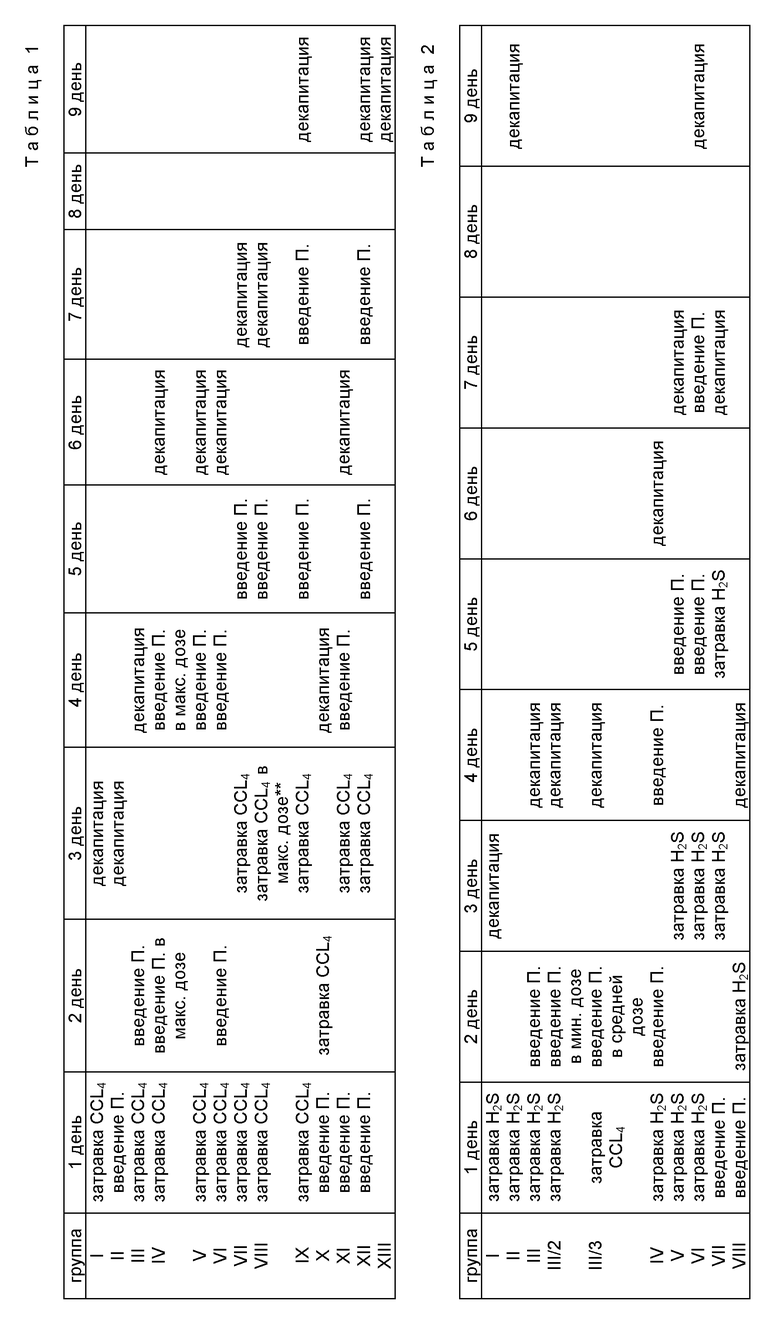
Изложенная сущность изобретения пояснена таблицей N 1, где:
- первая строка последовательность дней опыта;
- первый столбец - разбивка животных на группы;
- "затравка" - ингаляционное отравление животных CCl4 в закрытом эксикаторе 20 мин;
- "введение эмульсии" - впутрибрюшинная инъекция Перфторана в дозе 6 мл/кг;
- "введение эмульсии в максимальной дозе" - внутрибрюшинная инъекция Перфторана в дозе 14 мл/кг;
- "декапитация" - забивка животных с последующим извлечением внутренних органов и патологоанатомическим исследованием;
- "группа N 1" - контрольная группа животных, подвергнутая только воздействию CCl4 с последующей декапитацией;
- "группа N 2" - контрольная группа животных, получивших только инъекцию П, с последующей декапитацией;
- "группа N 13" - интактные животные.
и таблицей N 2, где:
- первая строка - последовательность дней опыта,
- первый столбец - разбивка животных на группы,
- "затравка" - ингаляционное отравление животных сероводородсодержащим газом;
- "введение эмульсии" - внутрибрюшинная инъекция Перфторана в дозе 12 мл/кг;
- "введение эмульсии в мин. дозе" - внутрибрюшинная инъекция Перфторана в дозе 4 мл/кг;
- "введение эмульсии в средней дозе" - внутрибрюшинная инъекция Перфторана в дозе 10 мл/кг;
- "декапитация" - забивка животных с последующим извлечением внутренних органов и патологоанатомическим исследованием;
- "группа I" - контрольная группа животных, подвергнутая только воздействию сероводородсодержащего газа с последующей декапитацией;
- "группа II" - контрольная группа животных, подвергнутая только воздействию сероводородсодержащего газа с последующей отсроченной декапитацией.
Предлагаемый способ прошел успешную апробацию на 200 мышах линии СВА на базе кафедры факультетской терапии Астраханской медицинской академии в течение 1994-95 годов.
Ниже проводятся результаты апробации.
Пример N 1
Исследования выполнены на мышах линии СВА (24 шт.), массой 10-12 г, подвергнутых воздействию четыреххлористого углерода. Затравка производилась в закрытом эксикаторе емкостью 4 литра, в центре которого на решетке помещали по 6 мышей, на дно эксикатора ставили бюкс с 0,05 мл препарата, что создавало концентрацию CCl4, равную 1,225 мг%. Время экспозиции 20 мин - 6 мышей (IV группа) и 20 мин дважды через день - 6 мышей (VI группа) в табл. N 1. Инъекции Перфторана осуществлялись интрабрюшинно в дозе 6 мл/кг дважды с интервалом в один день, на следующий день после затравки. Контроль составили интактные мыши, которым вводился Перфторан (6 шт.) и экспериментальные животные, подвергнутые воздействию CCl4 в течение 10 мин без Перфторана (6 шт. ). Было выделено 2 группы мышей, различавшиеся по условиям затравки (см. выше). Животные содержались в условиях вивария на стандартном рационе, составленного по нормам МЗ РФ. Перед взятием в опыт они проходили карантин в специальном помещении вивария. Животные с подозрением на спонтанную патологию выбраковывались. Оценивались: внешний вид и общее состояние животного, блеск и гладкость шерсти, наличие кожных изъязвлений и покусов, выделение из носа, глаз, заднего прохода. В опытах использовали контрольных и экспериментальных животных из одной партии. После эксперимента животных забивали путем декапитации и проводили патолого-анатомическое вскрытие с извлечением печени, сердца, почек и легких, с последующим описанием их внешнего вида, кровенаполнения. Для дальнейшего исследования часть материала фиксировалась в 10%-ном растворе нейтрального формалина. После фиксации из органов методом случайного отбора выбирались кусочки размером 5х5х3 мм, которые обезвоживались в спиртах восходящей концентрации до 100o этанола и заливали для световой микроскопии в парафин. Блоки резали на отечественном санном микротоме, получая срезы толщиной 5-8 мкм. Материал, исследуемый на содержание липидов, после формалиновой фиксации резался на криостатном микротоме на срезы толщиной 10 мкм. Полученные срезы окрашивали гематоксилинзозином, проводили ШИК-реакцию с контролем амилазой по методу Мак-Мануса, для выявления нуклеиновых кислот и нуклеопротеидов срезы окрашивали метиловым зеленым-пиронином по Брашо в модификации Курника, суммарный белок в срезах печени определяли прочным зеленым "FCF" по методу Альферта и Гешвинда. Нейтральные жиры окрашивали на срезах суданом III по методу Ромейса. Элективную окраску коллагеновых волокон проводили пикрофусцином по методу Ван-Гизона. Оценку эффективности гистохимической реакции на рибонуклеопротеиды производили по методу Г.А.Чекаревой и соавт. (1982) в условных единицах с градацией на четыре степени: отрицательную (0), низкую (1), умеренную (2), высокую (3), очень высокую (4). Результаты оценивались методами медицинской статистики (Г. Г. Автандилов, 1973, 1974) с оценкой достоверности признаков по критерию Стъюдена. При отравлении CCl4 - контроль с затравкой - у животных развивалось тяжелое поражение печени: множество перипортальных и мостовидных порта-портальных некрозов со слабой воспалительной реакцией, у некоторых животных наблюдалась вакуольная или зернистая дистрофия гепатоцитов, полнокровие сосудов; сердца - зернистая и гиалиновокапельная дистрофия кардиомиоцитов, очаговые некрозы, в сосудах выраженные расстройства кровообращения по типу "сладж" феномена и ДВС-синдрома; почек - явления зернистой, гиалиновокапельной, иногда вакуольной дистрофии эпителия извитых каиальцев и проксимального отдела нефрона, расстройство кровообращения в системе микроциркуляции (клубочковые и паренхиматозные капилляры). В контрольной группе с введением перфторана - изменений в органах не выявлено, печень содержит диффузные включения П в цитоплазме гепатоцитов. В группе IV в печени на фоне умеренно выраженной гиалиновокапельной дистрофии гепатоцитов перипортальных отделов дольки и одиночных гепатоцитов других отделов выражена от умеренной до сильной картина продуктивного агрессивного гепатита с зональными некрозами. В гепатоцитах центральных долек включения П. В почках очаговая вакуольная дистрофия канальцевого эпителия и выражены в различной степени расстройства кровообращения. В сердце очаговая зернистая и гиалиновокапельная дистрофия, нерезко выражены расстройства кровообращения. В группе VI выявлена сохранность структура печени, единичные гепатоциты по краю портальных трактов в состоянии гиалиновокапельной дистрофии. Практически все гепатоциты содержат вакуоли П, сосуды полнокровны. В почках и сердце структура сохранена.
Таким образом, на полученной модели токсического поражения организма CCl4-ом прослеживается лечебное действие Перфторана в дозе 6 мл/кг, что выражается в снижение количества, а в IX группе и в исчезновении некрозов, уменьшением интенсивности дистрофических явлений, расстройств кровообращения в печени, нормализации структуры почек и сердца, более значительное улучшение морфологической картины несмотря на двукратную затравку наблюдается в IX группе, что можно объяснить отсроченным по времени патологоанатомическим вскрытием и более длительным воздействием препарата на организм.
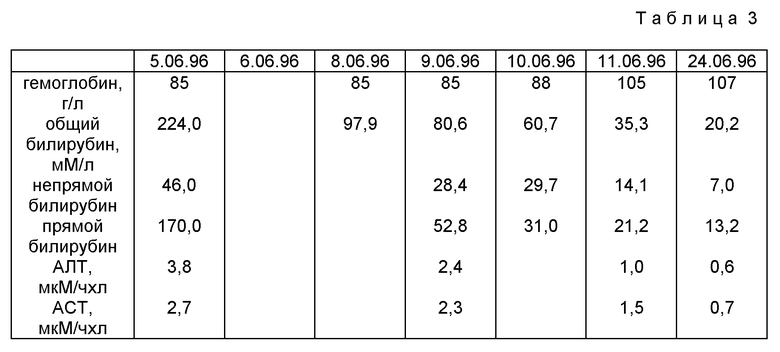
Приводится выписка из истории болезни больного С., 1969 г. р. с отравлением хлорсодержащим соединением, который поступил в токсикологическое отделение медсанчасти АГПК 1.01.96 с диагнозом: острое отравление ланиментом хлороформным тяжелой степени, токсическая гепатонефропатия тяжелой степени, острая печеночнопочечная недостаточность. В клинической картине доминировали следующие признаки: лихорадка до 39 - 40oC, желтуха, боль в животе диффузного характера, вздутие живота, тошнота, слабость, геморрагические проявления в виде высыпаний на коже и мелены. Наряду с традиционной комплексной терапией больному вводилась внутривенно капельно эмульсия Перфторан на 6 день после отравления (6.01.96) в количестве 400 мл, одновременно с ингаляцией увлажненной кислородо-воздушной смеси. Улучшение самочувствия произошло на следующий день после инфузии препарата и проявлялось уменьшением слабости, снижением температуры тела до нормальной, уменьшением болевого синдрома и метеоризма, купированием головной боли, уменьшением интенсивности желтухи и геморрагического синдрома. Динамика некоторых показателей лабораторного исследования представлена в виде табл. 3, где наиболее наглядны положительные изменения холестатического синдрома - снижение билирубина и его фракций с 224.0 мМ/л до нормы в течение 19 дней, причем в первые 3 дня он снизился более чем в 2 раза; цитолитического синдрома - снижение АЛТ с 3,8 мкМ/ч х л, до нормы в течение 6 дней, АСТ с 2,7 мкМ/ч х л до нормы в течение 19 дней:
Таким образом, анализируя историю болезни больного С., можно говорить о высокой эффективности Перфторана в лечении токсической гепатопатии, что выражается в быстром купировании клинических проявлений токсического поражения печени и нормализации лабораторных данных - показателей холестатического и цитолитического синдромов.
Пример N 2
Исследования выполнены на мышах линии СВА (24 шт.), массой 10-12 г., подвергнутых воздействию сероводородсодержащего газа. Затравка производилась в специальной затравочной камере производства Московского института профзаболеваний и гигиены труда им. Эрисмана объемом 200 литров. Для исследования использовался природный газ Астраханского месторождения. Эксперименты проводились на интактных животных с составлением газовых смесей воздуха с сероводородсодержащим газом в концентрации 300 мг/м3 по сероводороду, который является наиболее агрессивным компонентом природного газа Астраханского месторождения, время экспозиции 1 час. Отбор природного газа производился в контейнеры пробоотборники типа ПГО-50 по ГОСТ 149-69 из замерного узла установки "Y-171" Астраханского газоперерабатывающего завода. Состав проб газа определялся в центральной заводской лаборатории методом газохроматографического анализа на хроматографе "GC - 121 VL". В экспериментах использовался промышленный газ Астраханского месторождения следующего состава (данные приведены в об.%):
Метан - 57,23 ± 1,24
Этан - 2,26 ± 0,17
Пропан - 0,94 ± 0,06
Изо-бутан - 0,28 ± 0,04
Углекислый газ - 13,78 ± 1,21
Азот - 0,52 ± 0,02
Сероводород - 24,03 ± 1,33
Определение концентрации сероводорода в используемых воздушно-газовых смесях проводилась по ГОСТ 22387.2-83 (СТС 7В 3763-82). Метод основан на связывании сероводорода из газов растворами уксуснокислого или хлористого кадмия с последующим иодметрическим титрованием. Использовались также индикаторные трубки для определения сероводорода.
Инъекции Перфторана осуществлялись интрабрюшинно в дозе 12 мл/кг. Контроль составили интактные мыши, которым вводился Перфторан и экспериментальные животные, подвергнутые воздействию сероводородсодержащего газа без Перфторана. Было выделено 2 группы (IV и VI) мышей, различавшихся по условиям экспозиции, табл. N 2.
После эксперимента животных забивали путем декапитации и проводили патолого-анатомическое вскрытие с последующим гистологическим исследованием печени, сердца, почек и легких, забиралась кровь для исследования цитолитических ферментов - аланиновой и аспаргиновой трансаминаз (методом Reitman, Frankel, 1957). Последующая обработка срезов из извлеченных органов производилась по методике, описанной в примере N 1.
В контрольной группе с затравкой при патологоанатомическом исследовании выявлены значительные изменения в органах, в легких - большая часть легочной ткани в состоянии дис- и ателектаза с явлениями нарушения сосудистой проницаемости, а местами массивные интраальвеолярные гаморрагии со скоплениями гамосидерофагов. Крупные и средние бронхи с явлениями тяжелой гиалиновокапельной дистрофии и десквамации эпителия. Начальные явления острого эндобронхита и бронхиолита. В окружающей легочной ткани картина начинающейся очаговой гнойно-десквамативной пневмонии. В печени - выраженная дискомплексация печеночных долек. Выражена диффузная гиалиновокапельной дистрофия, очаговые /групповые/ некрозы гепатоцитов. При этом в гепатоцитах выражены явления дискариоза /изменение формы и размеров ядер, глыбчатая конденсация хроматина, фенестрация/, а вокруг некрозов гиперплазия звездчатых эндотелиоцитов. В строме портальных трактов отек, венозное полнокровие, диффузная инфильтрация гранулоцитами и пролиферация фибробластов. В почках - нерезко выраженная очаговая зернистая и гиалиново-капельная дистрофия эпителия канальцев проксимальной части нефрона. Сердце - умеренно выраженная гиалиново-капельная дистрофия мышечных волокон, нарушение кровообращения в капиллярах по "типу" сладжа эритроцитов. Отмечалось повышение цитолитических ферментов - АЛТ до 2,34 мМ/л, АСТ до 2,21 мМ/л. В контрольной группе с введением перфторана - контроль N 2 - изменений в органах не выявлено, печень содержит диффузные включения П в цитоплазме гепатоцитов. Патоморфологическая картина внутренних органов животных IV группы наиболее наглядно показывает лечебное действие П. - у большинства животных в легких ткань воздушна, встречаются небольшие участки дистелектазов. Мелкие бронхи в зоне их с явлениями бронхоспазма, а в просвете альвеол отечные массы. В печени - легкая дискомплексация долек, гепатоциты не изменены, в клетках Купфера небольшие вакуоли П; в сердце - структура нормальных мышечных волокон; почки - строение не изменено. Отмечено снижение аланиновой и аспаргиновой трансаминаз - 1,75 и 1,7 мМ/л соответственно. Во XI группе также отмечено улучшение патоморфологической картины по сравнению с контролем, хотя и в меньшей степени, чем в IV группе: легкие - основная ткань легочной ткани воздушна, без признаков патологии, однако примерно 1/3 ткани в состоянии дистелектазов с явлениями бронхоспазма и нарушения сосудистой проницаемости; печень - на фоне дискомплексации долек картина диффузной зернистой и гиалиновохапельной дистрофии гепатоцитов с явлениями дискариоза; почки - зернистая и гиалиновокапельная дистрофия эпителия канальцев; сердце - очаговая гиалиново-капельная дистрофия мышечных волокон. Цитолитические ферменты также имеют тенденцию к снижению АЛТ - 1.7 мМ/л, АСТ - 1.7 мМ/л.
Таким образом, при лечении Перфтораном экспериментальных животных в дозе 12 мл/кг после ингаляционного отравления сероводородсодержащим газом прослеживается отчетливый лечебный эффект, который выражается в купировании процессов гнойно-десквамативной пневмонии, дистрофических и воспалительных явлений в бронхах, нарушения проницаемости сосудов в легочной ткани, лечебный эффект отмечается в печеночной ткани, почках и сердце: исчезновение явлений дистрофии, нарушений микроциркуляции, некрозов гепатоцитов, явлений дискариоза в печеночных клетках, также наблюдается снижение уровня цитолитических ферментов, при этом наибольший лечебный эффект наблюдается в IV группе, что говорит о его прямой зависимости от интенсивности отравления (в VI группе затравка двукратная).
Пример N 3
Исследования выполнены на мышах линии СВА (6 шт.), массой 10-12 г., подвергнутых воздействию сероводородсодержащего газа. Методика затравки описана в примере N 2. Инъекции Перфторана осуществлялись интраорюшинно в дозе 10 мл/кг (группа III/3) табл. N 2. После эксперимента животных забивали путем декапитапии и проводили патологоанатомическое вскрытие с последующим гистологическим исследованием печени, сердца, почек и легких, забиралась кровь для исследования цитолитических ферментов - аланиновой и аспаргиновой трансаминаз (методом Reitman, Frankel, 1957). Последующая обработка срезов из извлеченных органов производилась по методике, описанной в примере N 1. При патологоанатомическом исследовании в легких - большая часть ткани воздушна и полнокровна. Капилляры межальвеолярных перегородок умеренного кровенаполнения, бронхи не изменены, в некоторых участках картина бронхоспазма с явлениями серозного эндобронхита. В зоне этих изменений очаговые дистелектазы с картиной нарушения сосудистой проницаемости, в некоторых альвеолах встречаются одиночные и группы перфторсодержащих макрофагов. В печени - структура долек сохранена, имеется нерезко выраженная зернистая дистрофия гепатоцитов III-й зоны ацинусов. В почках - картина нормального строения. В сердце - у одних животных вариант нормы, у других - нерезко выраженная зернистая дистрофия мышечных волокон. Уровень цитолитических ферментов был высок, но все же меньше, чем в контроле с затравкой сероводородсодержащим газом: АЛТ - 2,0 мМ/л, АСТ - 1,8 мМ/л.
Таким образом, прослеживается лечебный эффект Перфторана в дозе 10 мл/кг при токсическом поражении организма сероводородсодержащим газом, который заключается в уменьшении процессов дистрофии и нарушений в микроциркуляторном русле, но в некоторых органах (легкие) сохраняется явления воспалительного характера; снижается уровень цитолитических ферментов, хотя он более высок, чем на дозу Перфторана 12 мл/кг, что говорит о недостаточной дозе Перфторана 10 мл/кг при лечении токсического поражения сероводородсодержащим газом.
Пример N 4
Исследования выполнены на мышах линии СВА (6 шт.), массой 10-12 г, подвергнутых воздействию сероводородсодержащего газа. Методика затравки описана в примере N 2. Инъекции Перфторана осуществлялись интрабрюшинно в дозе 4 мл/кг (группа III/2) табл. N 2. После эксперимента животных забивали путем декапитации и проводили патологоанатомическое вскрытие с последующим гистологическим исследованием печени, сердца, почек и легких, забиралась кровь для исследования цитолитических ферментов - аланиновой и аспаргиновой трансаминаз (методом Reitman, Frankel, 1957). Последующая обработка срезов из извлеченных органов производилась по методике, описанной в примере N 1. При патологоанатомическом исследовании срезов органов выявлено, что большая часть легочной ткани в состоянии дистелектазов. Здесь же присутствует картина нарушения сосудистой проницаемости. В крупных и средних бронхах явления гиалиновокапельной дистрофии и десквамации эпителия. В мелких - картина бронхоспазма с явлениями серозного эндобронхита и мелкоочаговой пневмонии. В печени - дискомплексация долек и гиалиновокапельная диффузная дистрофия гепатоцитов с картиной дискариоза. В почках - выраженная зернистая дистрофия эпителия извитых канальцев, полнокровие капилляров, клубочки не изменены. В сердце - очаговая гиалиновокапельная дистрофия мышечных волокон. Зарегистрирован подъем трансаминаз: АЛТ - 1,75 мМ/л, АСТ - 1,95 мМ/л.
Таким образом, лечебная доза Перфторана 4 мл/кг при токсическом поражении организма сероводородсодержащим газом недостаточна, т.к. в органах сохраняются практически те же изменения, что и контроле с затравкой.
Пример N 5
Исследования выполнены на мышах линии СВА (6 шт), массой 10-12 г, подвергнутых воздействию четыреххлористого углерода. Методика затравки описана в примере N 1. Инъекции Перфторана осуществлялись интрабрюшинно в дозе 14 мл/кг дважды с интервалом в один день, после затравки (группа IV) табл. N 1. После эксперимента животных забивали путем декапитации и проводили патологоанатомическое вскрытие с извлечением печени, сердца, почек. Последующая обработка срезов из извлеченных органов производилась по методике, описанной в примере N 1. При патологоанатомическом исследовании срезов органов выявлено, что в печени структура сохранена, в перипортальных пространствах по краю пограничной пластинки единичные гепатоциты с явлениями гиалиновокапельной дистрофии и небольшой полиморфноклеточной инфильтрацией, встречаются единичные перфтросодержащие макрофаги, гепатоциты в центре долек содержат частицы Перфторана, сосуды полнокровны; почки и сердце обычного строения.
Таким образом, доза Перфторана 14 мл/кг не дает дальнейшего улучшения патологоанатомической картины токсического поражения организма, картина соответствует таковой в группе VI (табл. N 1) и в группе IV (табл. N 2), на дозу Перфторана 6-12 мл/кг. Дозу Перфторана 12 мл/кг можно считать пределом насыщения организма препаратом, превышение которого не дает дальнейшего улучшения показателей токсического поражения.
Предлагаемым способом достигается повышение эффективности лечения. Перфторан позволяет насыщать кислородом не только общий кровоток, но и микроциркуляторное русло; увеличивает отдачу кислорода ишемизированным тканям, которая достигает свыше 90%, легко проникает в спавшиеся, спазмированные и труднопроходимые сосуды за счет меньшего размера частиц эмульсии по сравнению с эритроцитом, что увеличивает полезную площадь капиллярного массообмена, обеспечивает снабжение кислородом участков ткани с обедненной сосудистой сетью и плохим кровообращением, при этом насыщение кровеносного русла кислородом не зависит от количества эритроцитов, т.к. происходит не химическое, а физическое растворение этого газа, что не уменьшает его эффективности при анемии различного генеза; снижает уровень молочной кислоты в крови более выражено, чем реополиглюкин; улучшает реологические свойства крови за счет снижения вязкости, уменьшения агрегации тромбоцитов и эритроцитов, увеличивает отрицательный заряд эритроцитов, что создает электрораспор между эритроцитами и стенками капилляров; купирует явления "сладжа" эритроцитов, ДВС-синдрома; повышает устойчивость клеточных мембран к действию повреждающих химических, механических и термических факторов за счет образования "вязкого" барьера на поверхности эритроцита, препятствующего проникновению гемолитика; изменяет функциональные свойства эритроцитов, повышая их устойчивость к механической травме, к гипо- и гиперосмии, к действию детергентов и ионофоров, увеличивает их термостабильную резистентность; уменьшает глубину ацидоза; активизирует дезинтоксикационную функцию печени; длительность проведения самой процедуры не превышает по длительности обычное внутривенное введение растворов, для получения лечебного эффекта достаточно двукратного введения эмульсии; препарат выводится, в основном, через легкие и небольшое количество через желудочно-кишечный тракт, таким образом не обладает токсическим действие на почки и не имеет противопоказаний при токсической нефропатии, не ограничен в применении при кровотечениях; не требует применения дорогостоящего стационарного, сложного в обслуживании оборудования и специально обученного персонала, легко дозируется, что позволяет индивидуально подобрать дозу препарата и избежать побочных явлений, связанных с передозировкой кислорода.
Предлагаемый способ может быть рекомендован в практику токсикологических отделений системы здравоохранения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРИМЕНЕНИЕ АЦИЗОЛА В КАЧЕСТВЕ ГЕПАТОПРОТЕКТОРА | 2004 |
|
RU2260427C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ПАТОЛОГИЧЕСКОГО РАЗРАСТАНИЯ СОЕДИНИТЕЛЬНОЙ ТКАНИ В ПАРЕНХИМАТОЗНЫХ ОРГАНАХ | 1996 |
|
RU2146133C1 |
| ЛЕЧЕБНОЕ СРЕДСТВО ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ХРОНИЧЕСКИХ ЗАБОЛЕВАНИЙ ПЕЧЕНИ | 2012 |
|
RU2526172C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИАРИТМИЧЕСКИМИ И ГЕПАТОПРОТЕКТОРНЫМИ СВОЙСТВАМИ | 2011 |
|
RU2469720C1 |
| 1,3- ДИ(3-ПИПЕРИДИНО-2-ГИДРОКСИПРОПИЛ)-6-МЕТИЛУРАЦИЛ ДЛЯ ПОВЫШЕНИЯ СОХРАННОСТИ И ПРОДУКТИВНОСТИ ПТИЦ | 2006 |
|
RU2334745C1 |
| АНТИОКСИДАНТНОЕ И МЕМБРАНОСТАБИЛИЗИРУЮЩЕЕ СРЕДСТВО | 2012 |
|
RU2540466C2 |
| СПОСОБ ПОЛУЧЕНИЯ НАСТОЙКИ СЕМЯН СОСНЫ КЕДРОВОЙ СИБИРСКОЙ И ГЕПАТОЗАЩИТНЫЙ ПРЕПАРАТ, ПОЛУЧЕННЫЙ ТАКИМ СПОСОБОМ | 2014 |
|
RU2545700C1 |
| СПОСОБ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ ПЕЧЕНИ РАЗЛИЧНОГО ГЕНЕЗА | 2009 |
|
RU2400233C1 |
| Применение суммарной рибонуклеиновой кислоты (РНК) из мультипотентных мезенхимальных стромальных клеток костного мозга млекопитающего в качестве средства для коррекции печеночной недостаточности | 2017 |
|
RU2655761C1 |
| СПОСОБ ЛЕЧЕНИЯ ОТРАВЛЕНИЙ, ВЫЗВАННЫХ ФОСФОРОРГАНИЧЕСКИМИ ВЕЩЕСТВАМИ | 1996 |
|
RU2155583C2 |
Изобретение относится к медицине, а именно к токсикологии, и может быть, в частности, использовано для лечении острых отравлений. Способ основан на насыщении микроциркуляциии органов, тканей кислородом. Для этого вводят парэнтерально перфторуглеродную эмульсию - перфторан двухкратно, через день в дозе 6 - 12 мл/кг после отравления. Способ позволяет повысить эффективность лечения токсичного поражения организма путем насыщения кислородом микроциркуляторного русла и проникновения в спавшиеся и спазмированные сосуды за счет меньшего размера частиц эмульсии. 3 табл.
Способ лечения острых отравлений, состоящий в насыщении микроциркуляции органов, тканей кислородом, отличающийся тем, что после отравления в организм внутривенно вводят перфторуглеродную эмульсию - перфторан двукратно, через день в дозе 6 - 12 мл/кг.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Лужников Е.А | |||
| Клиническая токсикология | |||
| Прибор для охлаждения жидкостей в зимнее время | 1921 |
|
SU1994A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Кашуба Э.А | |||
| Влияние гипербарической оксигенации на течение острого и подострого поражения печени четыреххлористым углеродом в эксперименте: Автореферат | |||
| - Воронеж, 1976, с.1 - 20. | |||
Авторы
Даты
2000-01-27—Публикация
1996-07-12—Подача