Предлагаемое изобретение относится к медицине, а именно к хирургии, и может использоваться для профилактики гнойно-септических осложнений после операций на открытом сердце.
Известен способ профилактики гнойно-септических осложнений путем создания у больных специфического иммунитета к возбудителям госпитальной инфекции. Для этого в предоперационном периоде проводится иммунизация различными моно- и поливакцинами, содержащими антигены наиболее часто встречающихся условно-патогенных микроорганизмов (Московцева Р.Л. // Состояние антибактериального иммунитета у больных раком пищевода и его стимуляция вакцинными препаратами // Автореферат дис. канд. мед. наук, М., 1988). Однако в первые 2-3 суток после операций на открытом сердце в условиях искусственного кровообращения происходит значительное снижение факторов приобретенного антибактериального иммунитета у вакцинированных больных, что уменьшает эффективность иммунопрофилактики и повышает риск возникновения инфекционных осложнений.
Для профилактики и лечения гнойно-септических процессов часто используются иммунные антибактериальные плазмы, получаемые от реконвалесцентов, перенесших хирургическую инфекцию, или от доноров, предварительно иммунизированных к одному из представителей патогенной микрофлоры (Попов С.Д., Рыжков С. В. и др. // Получение и применение плазмы против синегнойной инфекции // Военно-медицинский журнал. 1990, N 12, с. 30-31). Недостатком иммунной донорской плазмы является чужеродность по отношению к реципиенту. При использовании ее имеется опасность заражения больного возбудителями инфекционных заболеваний (трансфузионный гепатит, ВИЧ-инфекция и пр.), не исключаются посттрансфузионные реакции и осложнения, в значительной степени повышается стоимость лечения.
Известен способ получения и трансфузии аутогенной плазмы с целью возмещения операционной кровопотери и предупреждения синдрома гомологичной крови (Колесников И. С. , Лыткин М.И., Плешаков В.Т. // Аутотрансфузия крови и ее компонентов в хирургии. Л., 1979). Однако при этом не достигается повышения специфической антиинфекционной резистентности пациентов, так как переливаемая аутогенная плазма не является иммунной.
Цель изобретения - повышение иммунитета больных к основным возбудителям хирургической инфекции в раннем послеоперационном периоде.
Поставленная цель достигается дооперационной заготовкой плазмы больных, предварительно иммунизированных ассоциированной стафило-протейно-синегнойной (СПСА) вакциной, и трансфузией ее после оперативного вмешательства на сердце.
Способ осуществляется следующим образом. Через 10-30 суток после иммунизации СПСА-вакциной по стандартной методике (по 0,5 мл подкожно в подлопаточную область дважды с интервалом 7-30 дней) и не менее чем за 3 суток до операции больным производят забор плазмы методом одно- или двукратного плазмафереза. Интервал между сеансами процедур составляет 3-7 дней. Кровь в объеме 500-800 мл через вену локтевой области забирается одноразовыми системами в пластиковые контейнеры "Гемакон". Центрифугирование проводят на аппарате "Beckman" в течение 10 мин при режиме 3000 об/мин и снижении температуры до -5oC. Во время центрифугирования больному в канюлированную вену вливают 0,9%-ный раствор хлорида натрия или один из плазмозамещающих растворов (полиглюкин, желатиноль, реополиглюкин). После завершения центрифугирования отделенные форменные элементы крови разводят физиологическим раствором в соотношении 1:1 и возвращают в сосудистое русло. Объем заготовленной за один сеанс плазмы составляет 450±150 мл, после двойного плазмафереза - 900±300 мл. Аутогенная плазма хранится в морозильной камере при температуре -12oC. Срок хранения может достигать 1 мес.
Проведенные исследования титров специфических антител к стафилококку, протею, синегнойной палочке в полученной плазме показали возрастание их по сравнению с исходными в 4-7 раз, что позволяет охарактеризовать ее как полииммунную.
В раннем послеоперационном периоде на высоте нарушения гомеостаза и иммунодепрессии (первые 3 сут. после операции) больным производится трансфузия аутогенной полииммунной плазмы. Непосредственно перед применением плазма размораживается и согревается в воде до 37oC. Трансфузия в объеме 150-300 мл осуществляется через одноразовую систему и катетер, установленный в центральной вене. Скорость введения в среднем составляет 5 мл/мин. Количество трансфузий в зависимости от объема заготовленной плазмы колеблется от 2 до 4, интервал между введениями - от 12 до 24 ч. Вследствие трансфузий аутогенной полииммунной плазмы после операций в сыворотках пациентов изучаемой группы титры специфических антител возрастают быстрее и достигают более высоких значений по сравнению с больными, которым проводилась иммунизация без последующей заготовки и введения аутоплазмы (контрольная группа). Так, через 3 суток после операции у больных, которым применялся данный способ, титры антител более чем в 1,5 раза превышали значения таковых в контрольной группе. Результатом применения такой плазмы является усиление противоинфекционной защиты организма от трех наиболее вероятных возбудителей и снижение частоты послеоперационных гнойно-септических осложнений в изучаемой группе больных.
Пример 1. Больной Ш. , 42 года. Клинический диагноз: ревматизм, неактивная фаза; аортальный порок сердца с преобладанием недостаточности; недостаточность кровообращения 2А стадии; функциональный класс 4. Сопутствующий диагноз: хронический обструктивный бронхит. Исходные уровни плазменных антител, определенных в реакции пассивной гемагглютинации: к стафилококку - 1: 40, к протею - 1:20, к синегнойной палочке - 1:20, антистафилотоксин - 1 АЕ. Больному проведена иммунизация СПСА-вакциной: дважды по 0,5 мл подкожно в подлопаточную область с интервалом между инъекциями в 10 дней. Через 10 суток после ревакцинации произведен плазмаферез с заготовкой 600 мл аутогенной плазмы. Титры антител в ней: антистафилококковых - 1:160, антипротейных - 1: 80, антисинегнойных - 1: 80, антистафилотоксин - 4 АЕ. Аутогенная плазма хранилась в замороженном состоянии при температуре -12oC. Через неделю после плазмафереза больному произведена операция: протезирование аортального клапана в условиях искусственного кровообращения. Через сутки после операции выявлены титры антител: антистафилококковых - 1:40, антипротейных - 1:20, антисинегнойных - 1:40, антистафилотоксина - 1 АЕ. На вторые и третьи сутки послеоперационного периода больному производилась трансфузия аутоплазмы по 300 мл. Через 6 ч после второй плазмотрансфузии титры антител к стафилококку составляли 1: 160, к протею - 1:80, к синегнойной палочке - 1:80, уровень антистафилотоксина приблизился к дооперационному - 3 АЕ. На пятые сутки после операции произведено разведение нижней части раны, ревизия и санация переднего средостения по поводу гемоперикарда. Несмотря на значительный риск развития хирургической инфекции, обусловленный выраженными исходными нарушениями гемодинамики, вентиляционной функции легких, тяжелой операционной травмой, послеоперационным кровотечением и повторным оперативным вмешательством, заживление раны произошло первичным натяжением, инфекционных осложнений не было. В данном наблюдении функции аутогенной плазмы состояли прежде всего в повышении ранее созданного иммунитета к стафилококку, протею и синегнойной палочке, а также в возмещении операционной кровопотери и ограничении трансфузий гомологичных сред.
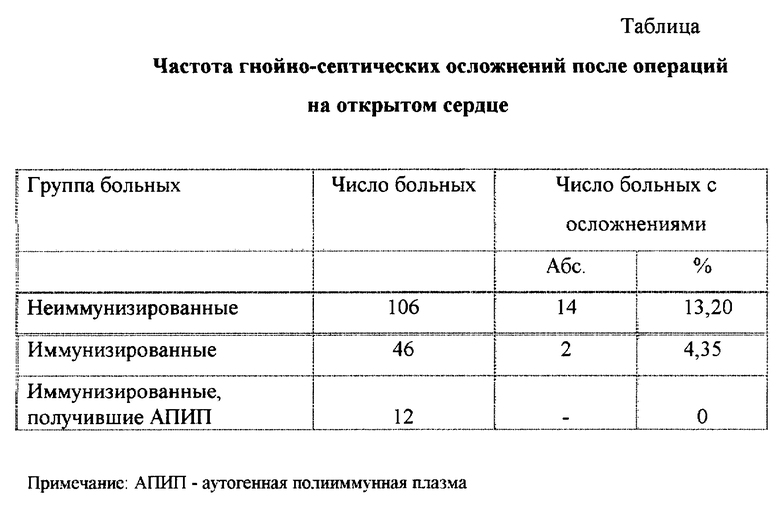
Предлагаемый способ апробирован у 12 больных. В таблице представлены клинические результаты заявляемого способа профилактики послеоперационных гнойно-септических осложнений.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОФИЛАКТИКИ ГНОЙНО-ВОСПАЛИТЕЛЬНЫХ ОСЛОЖНЕНИЙ СЛУЧАЙНЫХ ТРАВМАТИЧЕСКИХ И ОПЕРАЦИОННЫХ РАН | 2000 |
|
RU2193890C2 |
| СПОСОБ ЛЕЧЕНИЯ ПОСЛЕОПЕРАЦИОННЫХ ГНОЙНО-ВОСПАЛИТЕЛЬНЫХ ОСЛОЖНЕНИЙ, ОБУСЛОВЛЕННЫХ НОЗОКОМИАЛЬНОЙ ИНФЕКЦИЕЙ | 2003 |
|
RU2246273C2 |
| СПОСОБ ПРОФИЛАКТИКИ ПОСЛЕОПЕРАЦИОННЫХ ГНОЙНО-ВОСПАЛИТЕЛЬНЫХ ОСЛОЖНЕНИЙ | 2005 |
|
RU2286167C2 |
| СПОСОБ КОМПЛЕКСНОГО ПОСЛЕОПЕРАЦИОННОГО ЛЕЧЕНИЯ БОЛЬНЫХ, ПЕРЕНЕСШИХ ПЕРИТОНИТ | 2008 |
|
RU2371162C1 |
| ВАКЦИНА ПРОТИВ ИНФЕКЦИЙ, ВЫЗЫВАЕМЫХ УСЛОВНО-ПАТОГЕННЫМИ ВОЗБУДИТЕЛЯМИ | 2001 |
|
RU2204412C2 |
| СПОСОБ ЛЕЧЕНИЯ ПОСЛЕОПЕРАЦИОННЫХ АБСЦЕССОВ БРЮШНОЙ ПОЛОСТИ | 2004 |
|
RU2243780C1 |
| Способ отбора образцов крови доноров с повышенным содержанием дефензинов для получения моноиммунной плазмы крови | 2015 |
|
RU2606377C1 |
| РАНОЗАЖИВЛЯЮЩЕЕ СРЕДСТВО | 2000 |
|
RU2180241C2 |
| СПОСОБ ПОЛУЧЕНИЯ АССОЦИИРОВАННОЙ ВАКЦИНЫ ДЛЯ ПРОФИЛАКТИКИ ИНФЕКЦИЙ, ВЫЗЫВАЕМЫХ УСЛОВНО-ПАТОГЕННЫМИ БАКТЕРИЯМИ | 1986 |
|
RU2035189C1 |
| СПОСОБ ЛЕЧЕНИЯ ТОКСИКО-СЕПТИЧЕСКИХ СОСТОЯНИЙ У НОВОРОЖДЕННЫХ ДЕТЕЙ | 1997 |
|
RU2144837C1 |
Изобретение относится к медицине, в частности к хирургии, и может использоваться для профилактики гнойно-септических осложнений после операций. Предложено использовать аутогенную полииммунную плазму, полученную путем иммунизации больного ассоциированной стафило-протейно-синегнойной вакциной и последующего забора плазмы методом плазмафереза. Трансфузию плазмы проводят в первые трое суток после операции в 2 - 4 приема. Способ позволяет повысить титры специфических антител в 4 - 7 раз по сравнению с исходными. Это приводит к повышению иммунитета больных к основным возбудителям хирургической инфекции в раннем послеоперационном периоде. 1 табл.
Способ профилактики послеоперационных гнойно-септических осложнений, включающий использование аутогенной плазмы, отличающийся тем, что до предстоящей операции больного иммунизируют ассоциированной стафило-протейно-синегнойной вакциной, производят забор его плазмы методом плазмафереза, затем в первые трое суток после операции проводят трасфузию аутогенной полииммунной плазмы в 2 - 4 приема.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Применение вакцин и гипериммунной плазмы для профилактики и терапии гнойно-септических осложнений протейной этиологии | |||
| Методические рекомендации | |||
| Кузнечная нефтяная печь с форсункой | 1917 |
|
SU1987A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Способ лечения гнойно-воспалительного процесса | 1991 |
|
SU1790409A3 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Иммунология для хирургов | |||
| - М.: Медицина, 1974, с.108-110. | |||
Авторы
Даты
2000-02-20—Публикация
1997-05-06—Подача