Изобретение относится к области медицины, и в частности к трансфузиологии и может быть использовано при отборе доноров с повышенным содержанием дефензинов, с целью целенаправленного и эффективного лечения пациентов с осложнениями внутригоспитальными инфекциями.
Одной из перспективных задач Службы крови является обеспечение лечебных учреждений иммунными препаратами направленного действия, получаемыми из донорской крови. Терапевтическая необходимость данных препаратов при лечении гнойно-септических внутригоспитальных инфекций научно обоснованы и практически доказаны (С.С. Балаян, 1991 г. «Плазма иммунная», Е.А. Селиванов и соавт., 2003 г. - отраслевой классификатор «Консервированная кровь человека и ее компонентов».
Объем трансфузиологической помощи в лечебных учреждениях в последние годы характеризуется устойчивым ростом за счет увеличения трансфузий свежезамороженной, замороженной и иммунной плазмы. Применение иммунной плазмы основано на введении антител, которые в последующем связывают соответствующие антигены и способствуют устранению клинических проявлений бактериальной агрессии.
Переливание иммунной плазмы проводится не только с лечебной целью, но и с профилактической (Н.В. Демидова, М., «Медицина», 1987 г., В.Н. Цыган и соавт., С-Пб., 2011 г.).
В учреждениях Службы крови СССР имеется опыт выпуска антистафилоккоковой плазмы и иммуноглобулинов (противостолбнячной, противогриппозной, противооспенной и др.), которые получали из крови доноров, подвергаемых активной иммунизации. Однозначно объем и спектр выпускаемых иммунных препаратов не удовлетворял практическое здравоохранение.
Для увеличения необходимых специфических иммунных компонентов сотрудниками Ленинградского ордена Трудового Красного Знамени, ордена Дружбы народов научно-исследовательского института гематологии и переливания крови (проф. В.К. Мельникова, кандидаты медицинских наук А.И. Смирнова, Л.К. Николаева, кандидаты биологических наук Е.И. Кайтанджан и Р.Г. Файзулин), были подготовлены методические рекомендации «Организация новой формы иммунного донорства среди лиц с естественными антибактериальными антителами с целью получения иммунных препаратов направленного действия» и утверждены Заместителем Министра Здравоохранения СССР Э.А. Ноговицыным 15 сентября 1989 года. В соответствии с требованиями данных рекомендаций и положениями, представленными в работе А.В. Чечеткина и соавт., 2008 г. (Методические указания «Получение и клиническое применение иммунной плазмы в военно-медицинских учреждениях») до 2010 года в лечебных учреждениях РФ проводился отбор доноров крови путем скрининга определения бактериальных антител в «лечебном титре» в плазме крови (иммунная плазма) на наиболее часто встречаемые внутрибольничные инфекции:
- антистафилококковые;
- антиколибациллярные;
- антисинегнойные;
- антипротейные;
- антиклебсиеллезные.
Основным показателем отбора образцов крови доноров являлась величина или терапевтически значимый (и выше) титр антибактериальных антител для оказания трансфузиологической помощи. Процент обнаружения таковых у кадровых доноров варьировал от 12 до 73% и зависел от пола, возраста, времени года и сезонных работ.
С 2010 года производство диагностических препаратов в стране для тестирования на ранее указанные инфекции прекратилось, что побудило нас искать новый подход для поиска естественных антибактериальных белков в плазме крови доноров, что крайне необходимо для оказания медицинской помощи и целевого применения плазмы определенной категории больных (верифицированной внутригоспитальной инфекции, ожоговой болезни, осложненной присоединившейся вторичной гнойной инфекции и др). Патентный поиск по этим вопросам к успеху нас не привел.
Памятуя, что изыскание высокоэффективных средств терапии и профилактики различных инфекций для службы крови приобретает в настоящее время особую актуальность и неотложную задачу практического здравоохранения.
В настоящее время антимикробные пептиды представляют объект повышенного внимания широкого круга специалистов, в том числе рассматривающих такие соединения как альтернативу антибиотическим средствам. В настоящее время, чтобы противостоять патогенным микроорганизмам, появляются все новые и новые виды антибиотиков, которые по сути являются производными старых. Если мы не изменим методы производства, назначения и использования антибиотиков, нас ждут катастрофические последствия, а нам известно, что антимикробные пептиды уступают антибиотикам по эффективности, но действуют быстрее, разрушая бактерии, не восприимчивые к антибиотическим средствам (Garsia А.Е., Osapau G., Tran P.A. Selsted ME Infect Immun. 2008 Dec. 76 (12): 5883-91).
Антимикробные пептиды постоянно образуются даже в стабильном состоянии организма. А.Е. Абатуров (Журнал «Здоровье ребенка», 3 (38), 2012 г. ) указывает, что даже при низких концентрациях дефензины ингибируют аденовирусную инфекцию.
Антимикробные пептиды-дефензины - мультифункциональные катионные белки человека, представляющие собой короткие молекулы длиной от 12 до 50 аминокислот, имеющие среднюю молекулярную массу 4 кD, выполняющие сложную роль в поддержании и регулировании иммунного ответа на вирусную, микробную и иную антигенную агрессию на основе прямого воздействия на клеточную мембрану микроорганизма, вызывающего разрушение клетки, а также участие в регулировании процесса презентации антигена.
Показатели содержания дефензинов в плазме крови (белки нейтрофилов человека) рассматривается как индикатор наличия высокой иммунозащитной функции. Лекарственные препараты на основе антимикробных антител пока не созданы, но идет активная работа в этом направлении.
Б.П. Пинегин, А.С. Будихина в журнале «Иммунология», 2008 г., №5 отмечают, что антимикробные пептиды (дефензины) являются компонентами иммунной системы и обеспечивают первую линию защиты макроорганизма от различных патогенов.
Известен способ отбора доноров для получения плазмы крови путем исследования иммунологических показателей крови, в котором в плазме выявляют содержание антимикробных пептидов дефензинов и при титре дефензинов от 180 до 545 нг/мл - у мужчин и от 128 до 386 нг/мл - у женщин осуществляют забор крови (RU 2558114, G01N 33/53, опубл. 27.07.2015). Недостатком этого изобретения является то, что способ отбора не обеспечивает получения плазмы, направленной на подавление определенного вида инфекций.
В основу изобретения положена задача разработки способа получения плазмы крови доноров с содержанием дефензинов, обладающих наибольшей чувствительностью к бактериальной культуре, позволяющего определение в плазме крови доноров антимикробных пептидов (дефензинов - катионных белков нейтрофилов), которые обладают микробицидной, хемотаксической, иммуномодулирующей и цитотоксической активностью без проведения целевой иммунизации доноров, в результате чего вовлекаются в защиту организма и воспалительные процессы, а также дающего возможность расширить область их применения в клинической практике.
Решение поставленной задачи обеспечивается тем, что в способе получения плазмы крови доноров с содержанием дефензинов, обладающих наибольшей чувствительностью к бактериальной культуре, в плазме выявляют содержание антимикробных пептидов дефензинов и при титре дефензинов свыше 50 пг/мл осуществляют забор крови, выделяют бактериальную культуру от пациентов с осложненными инфекциями, вызванными протеем, синегнойной и кишечной палочками, стафилококком и клебсиеллой, определяют чувствительность данной культуры к полученным дефензинам, а затем для получения плазмы отбирают доноров с дефензинами, обладающими наибольшей чувствительностью к выделенной бактериальной культуре.
Поставленная нами цель достигается путем тестирования образцов крови кадровых доноров на выявление человеческого белка нейтрофилов трех из четырех HNP 1-3 дефензины (от англ. defense - защита), которые являются уникальными для нейтрофилов и составляют около 99% от общего содержания в этих клетках. Количество дефензинов 3-5 mg на 1000000 нейтрофилов, а в плазме - 50-100 ng/ml.
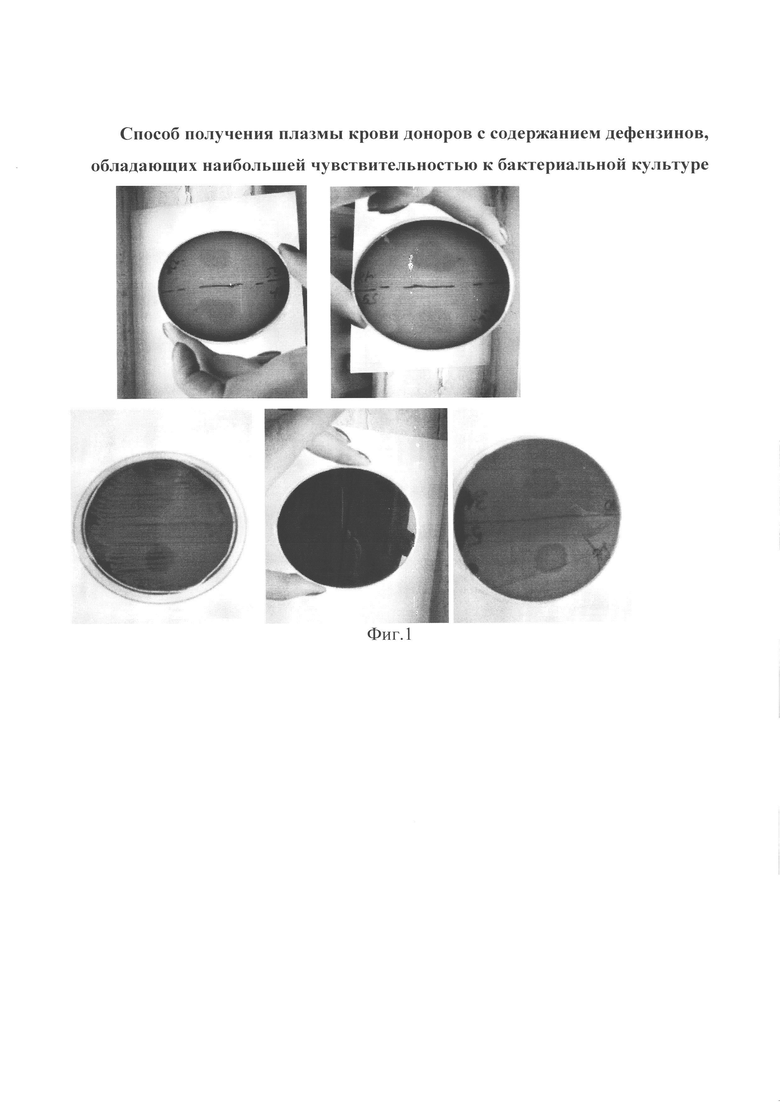
Изобретение поясняется фиг. 1, на которой представлены снимки результатов бактериологических исследований, полученных нами, характеризующих влияние дефензинов на литическую активность микроорганизмов, взятых для опыта.
Обследовались лица молодого возраста 19-26 лет, 98% мужского пола.
Способ количественного определения HNP 1-3 проводили на диагностической тест-системе фирмы HYCULT-biotech (Нидерланды) основанный на «сендвич»-методе твердофазного иммуноферментного анализа (дефензины нейтрофилов) ELISA. Подготовка образцов крови доноров к исследованию требовала строжайшего выполнения всех рекомендаций методической инструкции. После забора крови донора не позже 20 мин проводилось центрифугирование при 1500g, температуре +4°C в течение 15 мин. Плазму отбирали строго в полипропиленовые пробирки и вновь центрифугировали в прежнем режиме. Отобранную плазму до исследования хранили при -70°C. Хранение при других температурах отрицательно влияет на показатели дефензинов.
Исследование образцов донорской плазмы проводили через 24 часа после оттаивания.
После выполнения иммунологических исследований полученные нами показатели величины дефензинов условно были распределены на три группы: 1 - лица, у которых показатели были до 50 ng/ml, 2 - до 100 ng/ml и 3 - более 100 ng/ml (при нормальном их содержании 50-100 ng/ml).
Было обследовано 153 образца плазмы крови доноров, в которых выявили показатели дефензинов 1 группы до 50 ng/ml - 43 образцах (28,1%), 2 группа - до 100 ng/ml - 46 образцах (30%) и 3 группа - свыше 100 ng/ml - в 64 образцах (41,1%). Таким образом, мы получили исходную «универсальную» (поливалентную - полииммунную) плазму.
В интересах клинического, целевого применения целесообразно уточнить - против какого конкретно микроорганизма данная полииммунная плазма обладает наибольшей активностью.
Нами данная задача решалась следующим образом.
На стандартные питательные среды (кровяной агар, агар Мюллера-Хилтон, желточно-солевой агар), приготовленные заранее проводили посев общепринятым методом следующих культур, выделенных от больных лечебных отделений (гнойной хирургии и ожоговой) E.Coli, St.Aureus, Ps. Aeruginose, Kl. Pneumonia и Proteus vulgaris. Затем на поверхность засеянных чашек Петри наносили пастеровской пипеткой «полииммунную» плазму в количестве по 0,05 мл 2 и 3 группы (по содержанию дефензинов) помещали в термостат. Через 18-20 часов проводили учет влияния дефензинов на засеянную культуру.
Оценку литической активности проводили: « - » - отсутствие активности; «+» - низкая активность;
«++» - образование зоны лизиса с большим количеством колоний вторичного роста бактерий;
«+++» - зона лизиса с единичными колониями вторичного роста;
«++++» - прозрачная зона лизиса без колоний вторичного роста.
Было выяснено, что чем выше показатели дефензинов, тем отчетливее отмечалась литическая активность на засеянную культуру. В то же время показатели величины дефензинов по-разному оказывали влияние на рост использованных нами микробных культур. Так, 2 группа дефензинов (до 100 ng/ml) из 46 образцов плазмы проявилась литическая активность в 31 случаях (67,6%) на 2 и 3 креста на Е. Coli, Kl. Pneuvmonia. Из третьей группы (содержание дефензинов выше 100 ng/ml) литическая активность составила из 64 образцов плазмы крови в 48 (76,5%) случаях на 2 и 3 креста. Тогда как в первой группе отмечалась в единичных случаях - 4 образцах (0,93%).
Практический пример
1. (Донор мужчина) - показатель дефензинов - 83 ng/ml. Литическая активность - «++» - «+++» креста.
2. Донор мужчина с показателем дефензинов 112 ng/ml. Литическая активность «+++» креста.
На фиг. 1 представлены снимки результатов бактериологических исследований, полученных нами, характеризующих влияние дефензинов на литическую активность микроорганизмов, взятых для опыта.
В связи с отсутствием в настоящее время наличия сертифицированной иммунной плазмы на станциях (отделениях) переливания крови и отсутствием указаний руководящих документов получения специфичной иммунной плазмы и учитывая крайнюю необходимость в ней лечебных учреждений самого различного профиля, нами предлагается способ получения естественной, специфической иммунной плазмы.
Особенности ее получения:
- не требуется особой, специальной медицинской аппаратуры;
- выполнима на уровне районной больницы и в военном госпитале на 150 и выше коек;
- наличие в штате учреждения врача-бактериолога.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОТБОРА ДОНОРОВ ДЛЯ ПОЛУЧЕНИЯ ПЛАЗМЫ КРОВИ, ЭФФЕКТИВНОЙ ПРИ ЛЕЧЕНИИ ПАЦИЕНТОВ С ИНФЕКЦИОННЫМИ ЗАБОЛЕВАНИЯМИ И ОСЛОЖНЕНИЯМИ ПОСЛЕ ОПЕРАТИВНЫХ ВМЕШАТЕЛЬСТВ, ТРАВМ И ОЖОГОВ | 2014 |
|
RU2558114C1 |
| Способ лечения пациентов с осложнениями внутригоспитальными инфекциями | 2016 |
|
RU2665170C2 |
| СПОСОБ ОТБОРА ДОНОРОВ КРОВИ ДЛЯ ПОЛУЧЕНИЯ ПЛАЗМЫ С ЦЕЛЬЮ ЛЕЧЕНИЯ ПАЦИЕНТОВ С ИНФЕКЦИОННЫМИ ЗАБОЛЕВАНИЯМИ И ОСЛОЖНЕНИЯМИ ПОСЛЕ ОПЕРАТИВНЫХ ВМЕШАТЕЛЬСТВ, ТРАВМ И ОЖОГОВ | 2014 |
|
RU2601372C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ РЕЦИДИВА ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ КИШЕЧНИКА | 2012 |
|
RU2517069C1 |
| АНТИМИКРОБНОЕ ВЕЩЕСТВО | 2010 |
|
RU2447896C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПЛЕКСА АНТИМИКРОБНЫХ ПЕПТИДОВ НАСЕКОМОГО | 2013 |
|
RU2552157C1 |
| КОМПОЗИЦИЯ АНТИБАКТЕРИАЛЬНАЯ ДЛЯ ПРОФИЛАКТИКИ ИЛИ ЛЕЧЕНИЯ ГОСПИТАЛЬНЫХ ИНФЕКЦИЙ (ВАРИАНТЫ), ШТАММЫ БАКТЕРИОФАГОВ, ИСПОЛЬЗУЕМЫЕ ДЛЯ ПОЛУЧЕНИЯ ТАКОЙ КОМПОЗИЦИИ | 2015 |
|
RU2628312C2 |
| АНТИБАКТЕРИАЛЬНАЯ КОМПОЗИЦИЯ НА ОСНОВЕ ЭНДОЛИЗИНОВ И ЛЕКАРСТВЕННЫЕ СРЕДСТВА В ФОРМЕ ГЕЛЯ ИЛИ СПРЕЯ С ЕЕ ИСПОЛЬЗОВАНИЕМ | 2021 |
|
RU2790481C1 |
| АНТИБАКТЕРИАЛЬНАЯ КОМПОЗИЦИЯ В ВИДЕ СУППОЗИТОРИЯ И СПОСОБ ЕЕ ПРИГОТОВЛЕНИЯ | 2016 |
|
RU2622762C1 |
| Способ лечения бактериальных инфекций дыхательных путей | 2019 |
|
RU2707505C1 |
Изобретение относится к области медицины, в частности к трансфузиологии, и может быть использовано для получения плазмы крови доноров с содержанием дефензинов, обладающих наибольшей чувствительностью к бактериальной культуре. Для этого в плазме выявляют содержание антимикробных пептидов дефензинов и при титре дефензинов свыше 50 пг/мл осуществляют забор крови. Выделяют бактериальную культуру от пациентов с осложненными инфекциями, вызванными протеем, синегнойной и кишечной палочками, стафилококком и клебсиеллой, определяют чувствительность данной культуры к полученным дефензинам, а затем для получения плазмы отбирают доноров с дефензинами, обладающими наибольшей чувствительностью к выделенной бактериальной культуре. Использование данного способа позволяет получить плазму крови доноров с содержанием дефензинов, обладающих наибольшей чувствительностью к бактериальной культуре, для лечения внутрибольничной инфекции. 1 ил.
Способ получения плазмы крови доноров с содержанием дефензинов, обладающих наибольшей чувствительностью к бактериальной культуре, отличающийся тем, что в плазме выявляют содержание антимикробных пептидов дефензинов и при титре дефензинов свыше 50 пг/мл осуществляют забор крови, выделяют бактериальную культуру от пациентов с осложненными инфекциями, вызванными протеем, синегнойной и кишечной палочками, стафилококком и клебсиеллой, определяют чувствительность данной культуры к полученным дефензинам, а затем для получения плазмы отбирают доноров с дефензинами, обладающими наибольшей чувствительностью к выделенной бактериальной культуре.
| СПОСОБ ОТБОРА ДОНОРОВ ДЛЯ ПОЛУЧЕНИЯ ПЛАЗМЫ КРОВИ, ЭФФЕКТИВНОЙ ПРИ ЛЕЧЕНИИ ПАЦИЕНТОВ С ИНФЕКЦИОННЫМИ ЗАБОЛЕВАНИЯМИ И ОСЛОЖНЕНИЯМИ ПОСЛЕ ОПЕРАТИВНЫХ ВМЕШАТЕЛЬСТВ, ТРАВМ И ОЖОГОВ | 2014 |
|
RU2558114C1 |
| АНТИМИКРОБНОЕ ВЕЩЕСТВО | 2010 |
|
RU2447896C1 |
| WO 2000012132 A1, 09.03.2000 | |||
| ВИЛЬЯНИНОВ В.Н | |||
| И ДР | |||
| ПОЛИИММУННАЯ ПЛАЗМА С ПОВЫШЕННЫМИ УРОВНЯМИ ДЕФЕНЗИНОВ - ПЕРСПЕКТИВНЫЙ КОМПОНЕНТ ДОНОРСКОЙ КРОВИ // АКТУАЛЬНЫЕ ВОПРОСЫ МЕДИЦИНЫ В СОВРЕМЕННЫХ УСЛОВИЯХ, Сборник научных трудов по итогам международной научно-практической конференции, январь 2015, [он-лайн], [найдено 27.07 | |||
| Токарный резец | 1924 |
|
SU2016A1 |
| Найдено из Интернет: URL: http://elibrary.ru/item.asp?id=23355435&>. | |||
Авторы
Даты
2017-01-10—Публикация
2015-10-12—Подача