Изобретение относится к медицинской микробиологии, конкретно к получению препарата для специфической иммунопрофилактики смешанных условно-патогенных инфекций, вызываемых стафилококком, протеем, синегнойной палочкой. Необходимость создания такого препарата обусловлена природной и приобретенной устойчивостью возбудителей к воздействию известных антибактериальных препаратов, в том числе антибиотиков.
В литературе описана ассоциированная стафило-протейно-псевдомонас вакцина, содержащая поверхностные антигены одного штамма St. aureus, одного штамма мирабильного протея и шести штаммов синегнойной палочки [1,2] Известная вакцина индуцирует только антибактериальной стафилококковый и антибактериальный синегнойный иммунитет к поверхностным антигенам этих микробов, получаемым методом водной экстракции. Антипротейный иммунитет индуцируется также поверхностными антигенами из одного штамма только одного сероварианта.
Данные литературы свидетельствуют о серозависимости и фагозависимости при вышеназванных инфекциях. Кроме того, известно, что около 90% штаммов стафилококка и синегнойной палочки продуцируют экзотоксины, роль которых в патогенезе инфекций бесспорна, вследствие чего антигены экзотоксинов являются видовыми для этих возбудителей. Поэтому описанная ассоциированная вакцина имеет ограниченную протективную активность.
Целью изобретения является создание ассоциированной вакцины с высокими протективными свойствами для специфической профилактики смешанных условно-патогенных инфекций.
Способ получения ассоциированной вакцины для профилактики инфекций, вызываемых условно-патогенными бактериями, включает раздельное выделение протективных антигенов из штаммов Staphylococcus aureus, Ps. aеruginasa, Pr. mirabilis с последующим их смешиванием в физрастворе, при этом из штамма Staphylococcus aureus N Б-243 выделяют цитоплазматический антиген, из токсинпродуцирующего штамма Pseudomonas aeruginosa НИИЭМ РА-7 получают анатоксин синегнойной палочки, из клинических штаммов Proteus mirabilis 6,8,40,508,1115,4641 выделяют растворимые антигены путем контролируемого протеолиза, полученные антигены смешивают в физрастворе из расчета содержания их в 1 мл вакцины 0,15-0,2 мг белка, 15-30 мкг белка, 10-20 мкг белка соответственно и в смесь дополнительно добавляют коммерческий стафилококковый анатоксин и гидроокись алюминия в количестве 5-10 ЕС и 1-2 мг соответственно.
Для получения ассоциированной вакцины используют коммерческий стафилококковый анатоксин ФС 42-227 ВС-88; цитоплазматический антиген стафилококка (ЦПА), выделенный из штамма Б-243 (Ш-фагогруппа) путем механической дезинтеграции с помощью стеклянных бус с последующей очисткой двукратным кислотным осаждением и триптическим гидролизатом; очищенный концентрированный анатоксин синегнойной палочки, полученный путем формального обезвреживания экзотоксина А, продуцируемого штаммом РА-7 (из коллекции НИИЭМ им. Н.Ф.Гамалеи) с последующим осаждением сернокислым аммонием и очисткой на сефадексе С-100); лиофильно высушенные, очищенные антигены протея, полученные методом контролируемого протеолиза.
Процесс изготовления предлагаемой вакцины состоит из сведения всех компонентов.
П р и м е р 1. Для приготовления 100 мл ассоциированной вакцины берут 10 мл стафилококкового анатоксина, содержащего 50 ЕС в 1 мл; 15 мл синегнойного анатоксина, содержащего 100 мкг белка в 1 мл; 1 мл протейной вакцины, содержащей 1 мг белка в 1 мл; 3,75 мл цитоплазматического антигена стафилококка, содержащего 4 мг белка в 1 мл.
К полученной смеси антигенов добавляют гидроокись алюминия в количестве 8,5-9,5 мл гидроокиси, содержащей 12,5-13,5 мг/мл. Доводят объем до 100 мл физиологическим раствором. Тщательно перемешивают и оставляют для сорбции на 1 сут при комнатной температуре.
Полученная ассоциированная вакцина содержит в 1 мл:
Стафилококковый анаток- син 5 ЕС ЦПА 0,15 мг белка
Растворимые антигены протея 10 мкг белка
Анатоксин синегнойной палочки 15 мкг белка Гидроокись алюминия 1 мг
Физиологический раствор Остальное
П р и м е р 2. Ассоциированная вакцина содержит в 1 мл: стафилококкового анатоксина 2,5 ЕС, остальные компоненты взяты с тех же количествах, как в примере 1.
П р и м е р 3. Ассоциированная вакцина содержит в 1 мл: ЦПА 0,1 мг белка, остальные компоненты в тех же количествах, как и в примере 1.
П р и м е р 4. Ассоциированная вакцина содержит в 1 мл: анатоксин синегнойной палочки 10 мкг белка, остальные компоненты в количествах, как в примере 1.
П р и м е р 5. Ассоциированная вакцина содержит в 1 мл: растворимые антигены протея 5 мкг белка, остальные компоненты в тех же количествах, как в примере 1.
П р и м е р 6. Ассоциированная вакцина содержит в 1 мл:
Стафилококковый анаток- син 10 ЕС ЦПА 0,2 мг белка
Растворимые антигены протея 20 мкг белка
Анатоксин синегнойной палочки 30 мкг белка Гидроокись алюминия 2 мг
Физиологический раст- вор Остальное
Полученные варианты отвечали требованиям, предъявляемым к медико-биологическим препаратам, и обладали стерильностью, апирогенностью, безвредностью при п/к введении морским свинкам массой 300-350 г по 1,5 мл в оба бока, нетоксичностью.
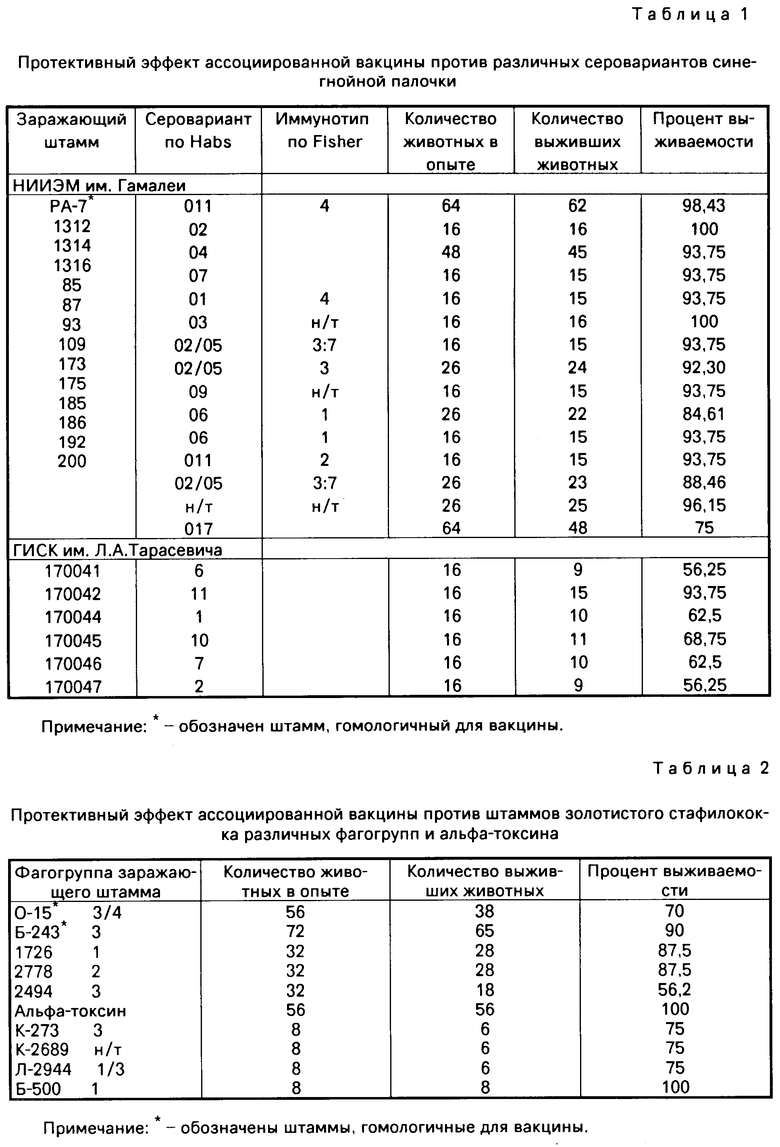
В табл.1,2,3 представлены данные по изучению протективного эффекта ассоциированной вакцины, приготовленной по примерам 1, 6 против различных серовариантов синегнойной палочки, протея и различных фагогрупп и альфа-токсина стафилококка.
Протективный эффект препарата оценивали по проценту выживших иммунизированных мышей после заражения живыми вирулентными культурами протея, синегнойной палочки и стафилококка вакцинных и гетерологичных штаммов.
Защитные свойства препарата относительно штаммов синегнойной палочки оказались достаточно высокими. Вакцина защищала около 100% животных от 6-8 LD50 гомологичного штамма РА-7, 56-100% от 3-4 LD50 гетерологичных штаммов из коллекции ГИСК им. Л.А.Тарасевича и НИИЭМ им. Г.Ф.Гамалеи АМН СССР.
Ассоциированная вакцина защищала 70-90% мышей, инфицированных двумя гомологичными штаммами стафилококка, 56-100% животных от 7 гетерологичных штаммов, и всегда все опытные мыши выживали после введения альфа-токсина.
При заражении иммунизированных животных культурами протея наблюдали гибель при введении вакцинных штаммов, а при инфицировании гетерологичными штаммами выживало от 52 до 83% мышей.
Таким образом, в экспериментах наблюдали достаточно высокий протективный эффект ассоциированного препарата в отношении гомологичных и гетерологичных штаммов стафилококка, протея и синегнойной палочки.
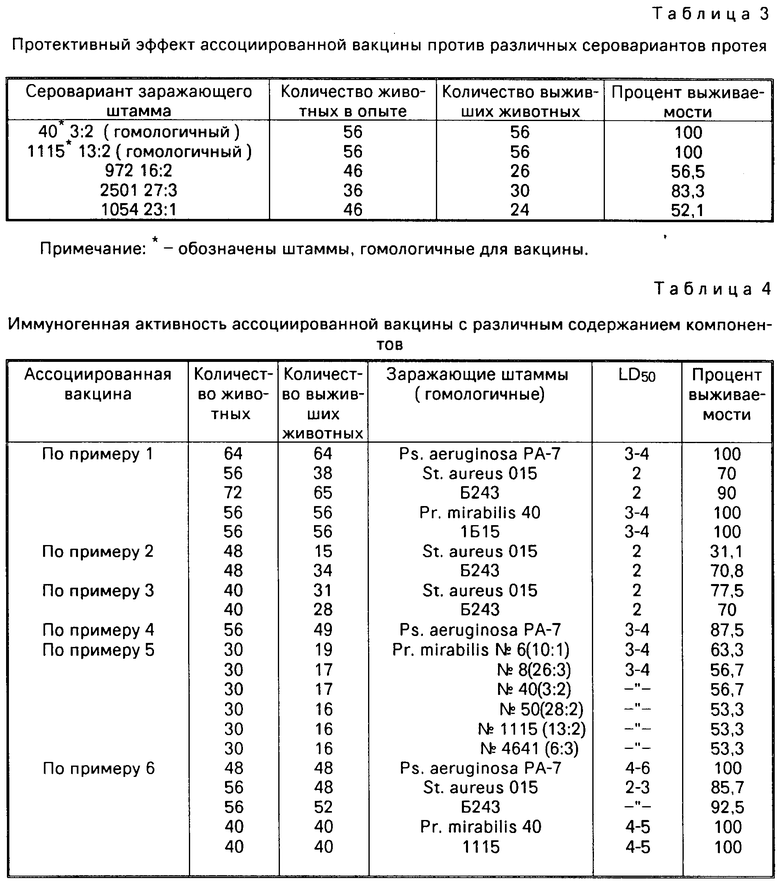
Результаты изучения иммуногенной активности ассоциированной вакцины с различным содержанием компонентов приведены в табл.4.
Как видно из табл.4, иммуногенная активность ассоциированной вакцины с содержанием одного из компонентов в количестве ниже минимального была ниже по сравнению с иммуногенной активностью ассоциированной вакцины с оптимальным содержанием компонентов (вакцина по примерам 1, 6) даже при проверке защитного эффекта против гомологичных штаммов.
Поскольку ассоциированная вакцина с оптимальным содержанием компонентов обладала высокими иммуногенными свойствами, увеличение дозировок компонентов является нецелесообразным из-за увеличения белковой нагрузки в препарате, предназначенном для применения на людях.
Установлено, что введение ассоциированной вакцины сопровождается изменениями показателей клеточного и гуморального иммунитета, о чем свидетельствует накопление Т- и Б-лимфоцитов в крови животных и повышение титров гуморальных антител, выявляемых в РНГА и в реакции нейтрализации гемолиза кроличьих эритроцитов, вызываемого α-токсином стафилококка.
Однократное введение ассоциированной вакцины обеспечивало выживаемость животных на уровне 70-80% в течение 6-8 недель после иммунизации, что является достаточным для профилактического препарата.
Таким образом, предлагаемая ассоциированная вакцина обладает высокими иммуногенными свойствами, обеспечивает высокий протективный эффект в течение 6-8 недель против гомологичных и гетерологичных штаммов возбудителей, стимулирует гуморальный и клеточный иммунитет. Вакцина может быть использована для иммунопрофилактики смешанных инфекций условно-патогенной этиологии в хирургических, акушерских, травматологических и ожоговых клиниках.
| название | год | авторы | номер документа |
|---|---|---|---|
| БЕСКЛЕТОЧНАЯ АНТИСТАФИЛОКОККОВАЯ ВАКЦИНА ДЛЯ ЛЕЧЕНИЯ ХРОНИЧЕСКОЙ СТАФИЛОКОККОВОЙ ИНФЕКЦИИ | 1995 |
|
RU2122862C1 |
| ПОЛИКОМПОНЕНТНАЯ ВАКЦИНА ДЛЯ ИММУНОПРОФИЛАКТИКИ И ИММУНОТЕРАПИИ ЗАБОЛЕВАНИЙ, ВЫЗЫВАЕМЫХ УСЛОВНО-ПАТОГЕННЫМИ МИКРООРГАНИЗМАМИ | 2002 |
|
RU2209081C1 |
| ВАКЦИНА ПРОТИВ ИНФЕКЦИЙ, ВЫЗЫВАЕМЫХ УСЛОВНО-ПАТОГЕННЫМИ ВОЗБУДИТЕЛЯМИ | 2001 |
|
RU2204412C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИКОМПОНЕНТНОЙ ВАКЦИНЫ ДЛЯ ИММУНОТЕРАПИИ ЗАБОЛЕВАНИЙ, ВЫЗЫВАЕМЫХ УСЛОВНО-ПАТОГЕННЫМИ МИКРООРГАНИЗМАМИ | 1994 |
|
RU2083223C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭКЗОТОКСИНА А СИНЕГНОЙНОЙ ПАЛОЧКИ | 1986 |
|
RU1410527C |
| СПОСОБ ПОЛУЧЕНИЯ ИММУННОЙ СЫВОРОТКИ | 1990 |
|
SU1775908A1 |
| РАНОЗАЖИВЛЯЮЩЕЕ СРЕДСТВО | 2000 |
|
RU2180241C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПИОБАКТЕРИОФАГА | 1992 |
|
RU2036232C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭКЗОТОКСИНА А PSEUDOMONAS AERUGINOSA | 1989 |
|
RU1596770C |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ КОКЛЮШНОГО ЭНДОТОКСИНА | 1994 |
|
RU2081417C1 |
Использование: медицинская микробиология, ассоциированная вакцина для иммунопрофилактики смешанных условно-патогенных инфекций. Сущность изобретения: вакцина содержит в качестве протективных антигенов анатоксины стафилококка и синегнойной палочки, цитоплазматический антиген стафилококка, растворимые антигены штаммов протея NN 6,8,40,508,1115,4641. Вакцина обладает высокими иммуногенными свойствами, обеспечивает высокий протективный эффект в течение 6-8 недель против гомологичных и гетерологичных штаммов возбудителей, стимулирует гуморальный и клеточный иммунитет. 4 табл.
СПОСОБ ПОЛУЧЕНИЯ АССОЦИИРОВАННОЙ ВАКЦИНЫ ДЛЯ ПРОФИЛАКТИКИ ИНФЕКЦИЙ, ВЫЗЫВАЕМЫХ УСЛОВНО-ПАТОГЕННЫМИ БАКТЕРИЯМИ, включающий раздельное выделение протективных антигенов из штаммов Staphylococcus aureus, Pseudomonas aeruginosa, Proteus mirabilis с последующим их смешиванием в физрастворе, отличающийся тем, что из штамма Staphylococcus aureus N Б-243 выделяют цитоплазматический антиген, из токсинопродуцирующего штамма Pseudomonas aeruginosa НИИЭМ N РА-7 получают анатоксин синегнойной палочки, из клинических штаммов Proteus mirabilis N 6,8,40,508,1115,4641 выделяют растворимые антигены путем контролируемого протеолиза, полученные антигены смешивают в физрастворе из расчета содержания их в 1 мл вакцины 0,15 0,2 мг белка, 15 30 мкг белка, 10 20 мкг белка соответственно и в смесь дополнительно добавляют коммерческий стафилококковый анатоксин и гидроокись алюминия в количестве 5-10 ЕС и 1-2 мг соответственно.
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Крейнин Л.С., Егорова Н.Б., Станиславский Е.С | |||
| и др | |||
| Ассоциированная стафило-протейно-псевдомонас вакцина | |||
| Сообщение II | |||
| Токсичность вакцины в "хронических" опытах и ее способность защищать животных от заражения протеем и стафилококком | |||
| - Журнал микробиологии, эпидемиологии, иммунобиологии, 1983, n 5, с.87-92. | |||
Авторы
Даты
1995-05-20—Публикация
1986-01-02—Подача