Изобретение относится к области биотехнологии, генной инженерии, иммунологии и может быть использовано для проведения серодиагностики HTLV-I/II.
T-лимфотропные вирусы человека I и II типа (human T-cell lymphotropic viruses type I and II, HTLV-I/II) относятся к семейству Retroviridae, подсемейству Oncovirinae. К этому подсемейству относится также вирус лейкоза крупного рогатого скота (bovine lymphotropic virus, BLV) и T-лимфотропные вирусы обезьян (simian T-lymphotropic virus, STLV). HTLV-I/II проявляют высокую тропность T-лимфоцитам, особенно к субтипу хелперов с фенотипом OKT4/leu3+, причем вирусы вызывают их неопластическую трансформацию. На первых стадиях вирусной инфекции T-клетки теряют цитотоксические свойства, а позже оказываются неспособными распознавать антиген-мишень [1].
Вирус лейкоза человека I типа этиологически ассоциирован с HTLV-I-зависимым T-клеточным лейкозом/лимфомой взрослых (adult T-cell leukemia/lymphoma, ATL) [2], протекающим как в острой, так в хронической и латентной формах. Кроме того, провирусная ДНК найдена у пациентов со сходными гемобластозами. Не исключено, что инфекция HTLV-I играет роль в этиологии различных B-клеточных лимфом [3]. В странах Южного полушария инфекция HTLV-I также может приводить к развитию HTLV-I-accoциированной миелопатии/тропического спастического парапареза (HTLV-I-associated myelopathy/tropical spastic paraparasis, HAM/TSP), протекающих в виде медленной прогрессивной миелопатии с высокой летальностью [4]. Другими воспалительными состояниями, в ряде случаев ассоциированными с HTLV-I инфекцией, возможно, являются альвеолит, полимиозит, артрит, инфекционные дерматиты, HTLV-I-ассоциированный синдром Шегрена, увеит [5].
Напротив, клиника HTLV-II ассимптоматична, поскольку не найдено достоверных, ассоциированных с этим вирусом заболеваний. Однако в ряде случаев отмечается лимфогрануломатоз и "тропическая" атоксическая нейропатия.
Заражение лифотропными вирусами человека I и II типа, по-видимому, происходит при попадании в кровяное русло зараженных лимфоидных клеток. Основные пути передачи вируса включают парентеральный, половой и вертикальный.
HTLV-I известен как эндемик на Юго-Востоке Японии, в Восточной и Центральной Африке, в Меланезии. Высокий уровень инфицированности вирусом показан также для некоторых изолированных популяций, таких как индейцы Южной Америки, Австрало-Меланизийские аборигены, изолированные популяции евреев в Иране и пигмеи Центральной Африки [6]. Филогенетический анализ последовательности ДНК HTLV-I позволяет разделить этот вирус на три больших класса, названных по их географическому распределению, а именно: Меланезийский, Центрально-Африканский и Космополитический (наиболее широко представленный). Более детальная характеристика, основанная на сиквенсе LTR-последовательности, подразделяет Космополитический класс на 4 субтипа - A (Трансконтинентальный), B (Японский), C (Западно-Африканский) и D (Северо-Африканский).
HTLV-II - эндемик среди индейцев Юга, Севера и Центральной части Америки, пигмеев Центральной Африки и коренного населения Центральной Азии. Следует отметить, что за последние 15-20 лет наблюдается неуклонный рост числа инфицированных в странах Европы - Италии, Испании, Англии. HTLV-II в молекулярном плане подразделен на два прототипа, описанных как субтип A (MO) и субтип B (NRA).
Инфицированность HTLV-I/II среди основных популяций эндемиченых регионов у клинически здоровых носителей составляет от 0.5 до 20.0% случаев в зависимости от пола и возраста. На всей остальной территории содержание антител в сыворотках крови здоровых доноров и случайно отобранных групп населения либо отсутствует, либо крайне низко и не превышает 0,01% [7, 8]. Важно отметить, что в странах Европейского сообщества основными группами риска являются проститутки, венерологические больные, наркоманы, применяющие наркотики внутривенно, пациенты, нуждающиеся во множественных переливаниях крови, а также дети, рождающиеся от инфицированных матерей. Значительная часть выявляемых вирусоносителей проживает в мегаполисах со значительным числом выходцев из эндемичных регионов. Общее число инфицированных на 1996 год составило более 20 миллионов человек.
На территории России эпидемический очаг был обнаружен на о. Сахалин [8], в остальных регионах России отмечались лишь спорадические случаи [7, 8].
Отсутствие эпидемического характера распространения HTLV-I/II на всей территории России возможно связано с незначительным количеством заносов вируса из эпидемических очагов и возможно отсутствием разнообразия субтипов HTLV-I/II. Поэтому для более корректного обследования сывороток людей, проживающих на территории России, на содержание антител к HTLV-I/II антигены для иммуноферментных систем необходимо производить при использовании плазмид, полученных на основе отечественных изолятов. В данном изобретении используется полипептид, полученный при помощи плазмиды, содержащей ген gag (общий для HTLV-I и HTLV-II), выделенный от инфицированного донора, проживающего на территории России.
Область gag вируса лейкоза человека локализуется в районе 824 - 2113 пар нуклеотидов (п.н.) генома и кодирует общий предшественник GAG с молекулярной массой 53 кДа, который нарезается с помощью вирусоспецифической протеазы на три группоспецифических белка p19, p24 и p15 - (824-1214 п.н.), (1214-1855 п.н.) и (1855-2119 п.н.). Белки GAG являются основными компонентами вирусной частицы, образуя сердцевину вириона, матрикс и нуклеокапсид соответственно вышеприведенным координатам.
Сущность данного технического решения состоит в том, что предложен новый, оригинальный, искусственно созданный полипептид, состоящий из продукта экспрессии фрагмента гена gag вируса лейкоза человека, слитый с бета-галактозидазой E. coli, связывающий антитела к продукту гена gag HTLV-I/II, фрагмент ДНК ATLG 579, штамм E.coli HB101, трансформированный рекомбинантной плазмидой pATLG 579, содержащей фрагмент ДНК ATLG 579.
Штамм-продуцент характеризуется следующими признаками: клетки прямые, палочковидной формы, подвижные с перитрихиальными жгутиками, грамотрицательные, неспороносные. Клетки хорошо растут на среде LB и других питательных средах, используемых для культивирования Escherichia coli, и простых питательных средах, содержащих 30-50 мкг/мл ампициллина. При росте на жидких средах клетки образуют ровную интенсивную муть.
При выращивании на питательных агаризованных средах при 37oC колонии клеток гладкие, круглые, блестящие, серые, мутные, прижатые, края ровные. Клетки хорошо растут в пределах от 4 до 45oC при оптимуме pH от 6,8 до 7,5. В качестве источника азота клетки используют как минеральные соли в аммонийной и нитратной форме, так и органические формы в виде пептона и аминокислот. Нитраты восстанавливают до нитритов. В качестве источника углерода используют глюкозу и фруктозу. Желатину не разжижают, мальтозу не сбраживают, индол не образуют, ацетат не усваивают; уреазная активность не обнаружена.
Трансформация компетентных клеток E.coli HB101 плазмидой с промотором LacZ оперона проведена по стандартным методикам. Полученные клоны клеток с плазмидами выращивают на среде LB при температуре 37oC. Продуктивность штамма при использовании плазмидного вектора экспрессии pUR290 с lac-промотором составляет около 200-350 мкг рекомбинантного белка на 1 мл клеточной суспензии при плотности культуры 1•10 млн•кл в мл. Рекомбинантный белок с молекулярной массой 145 килодальтона стабилен при температуре 4oC в течение 5-6 месяцев.
Выделенный и очищенный из штамма-продуцента полипептид G 579, иммобилизованный на твердом носителе, связывает антитела продуктам гена gag HTLV-I/II в сыворотках крови и других биологических жидкостях. Штамм депонирован в музее НИИ вирусологии им. Д.И. Ивановского РАМН.
Пример 1. Получение промежуточного фрагмента ATLG 2131.
В качестве источника HTLV-I/II-gag-специфических нуклеотидных последовательностей использовали мононуклеарные клетки, полученные от HTLV-инфицированного донора. Мононуклеары выделяли из гепаринизированной крови донора с помощью центрифугирования в градиенте фиколл/гипак. 10 мкл клеток ресуспендировали в 100 мкл лизирующего буфера, содержащего 10 мМ трис-HCl, pH 8,3; 1,0 мМ EDTA; 0,5% NP-40; 0,5% Tween-20 и протеиназу K в концентрации 200 мкг/мл. Лизис клеток осуществляли в течение двух часов при 56oC. Затем лизат инкубировали 10 мин при 85oC для инактивации протеиназы.
Фрагмент ДНК (использована нуклеотидная последовательность, опубликованная Seiki M. [9]), соответствующий участку LTR-gag-pol HTLV-I и кодирующей область генома с координатами 145-2276 (2131 п.н.) был амплифицирован в цепной полимеразной реакции (PCR) с использованием полимеразы BIOTAQ (Биомастер ЛТД, Россия) и пары праймеров:
5'-GGAGGGCAGCTCAGCACCGGC-3' (145-165)
5'-CGAGTGTCTGGGGTATAACCG-3' (2256-2276)
Олигонуклеотиды получены на синтезаторе "Applied Biosystems 381A DNA" фосфорамидатным методом и очищены с применением картриджа (Applied Biosystems Inc.).
Все реакции при постановке PCR проведены в объеме 100 мкл, содержащем по 50 pmol каждого праймера, 50 mM Трис-HCl (pH 8.8), 10 mM MgCl4, 10 mM (NH4)2SO4, 10 мкл лизата, содержащего вирусоспецифическую ДНК, 2.5 U ДНК-полимеразы из Thermus aquaticus (BIOTAQ, Биомастер ЛТД, Россия), 2,5 mM каждого из нуклеотидтрифосфатов и 50 мкл минерального масла (Sigma, USA). Реакция проведена в 40 циклов по следующей схеме:
- 94oC - 1 мин,
- 58oC - 1 мин,
- 72oC - 2 мин.
Анализ PCR-продукта.
Порцию в 4 мкл от продукта PCR-реакции смешивали с 4 мкл буфера образца, наносили на 1,5% агарозный гель на трис-ацетатном буфере pH 8,0 и проводили электрофорез. Необходимый фрагмент вырезали под мягким ультрафиолетом, а выделение ДНК из брусочков агарозного геля осуществляли с применением набора Gene Clean, как описано в прилагаемой к нему инструкции.
Пример 2. Конструирование промежуточной плазмиды pSma2131.
Выделенный фрагмент ДНК лигировали с использованием ДНК-лигазы фага T4 фирмы "Boehringer mannheim" (ФРГ) с гидролизированной SmaI формой ДНК pUC-19. Гидролиз ДНК pUC-19 ферментом SmaI фирмы "Boehringer mannheim" проводился в присутствии буфера для этого фермента. После соответствующей инкубации трансформировали полученным препаратом компетентные клетки E.coli DH-5a. Отбор трансформированных клеток осуществляли по способности трансформантов расти на среде, содержащей ампициллин. Были отобраны клоны, содержащие плазмиду размером 9,4 тыс.п.н.
Пример 3. Получение фрагмента ДНК ATLG 579.
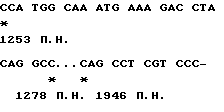
Промежуточную плазмиду pSma2131 использовали как источник нативной ДНК для дальнейшей амплификации фрагмента с координатами 1253-1952 п.н. последовательности HTLV-I, опубликованной Seiki М. et. al. в 1983. С этой целью была синтезирована внутренняя пара праймеров, содержащая в случае 5' олигонуклеотида сайт для BamHI рестриктазы, а в случае 3' праймера нуклеотидную последовательность для ClaI сайта:
5'-GGATCCATGGCAAATGAAAGACCTA-3' (1253-1273) BamHI
5'-ATCGATGGGGGGGGGACGAGGCTGAGTGCA-3' (1929-1952) ClaI
Получение олигонуклеотидов, реакции постановки PCR, анализ PCR-продуктов проводили, как это описано в примере 1.
Пример 4. Конструирование плазмиды pATLG 579.
Рекомбинантная плазмида pATLG 579 получена путем лигирования с использованием ДНК-лигазы фага Т4 фирмы "Boehringer mannheim" (ФРГ) ДНК амплифицированного фрагмента (размером 699 п.н.), выделенного из агарозного геля и гидролизированного ферментами BamHI и ClaI фирмы "Boehringer mannheim" в присутствии буферов для этих ферментов с линеаризированной (гидролизом вышеперечисленных рестриктаз) формой ДНК плазмидного вектора pUR 290. После соответствующей инкубации трансформировали полученным препаратом компетентные (обработанные CaCl2) клетки E.coli HB101. Отбор трансформированных клеток осуществляли по способности трансформантов расти на среде, содержащей ампициллин. Были отобраны клоны, содержащие плазмиду размером 5,9 тыс.п.н. Плазмиду со вставкой в прямой ориентации, относительно бета-галактозидазы, отбирали по ее способности синтезировать рекомбинантный полипептид величиной 145 кДа. Полученная плазмида, в которой ориентация гена gag HTLV-I/II совпадала с рамкой считывания гена бета-галактозидазы была обозначена pATLG 579. Рекомбинантный белок получали в виде телец включения.
Все манипуляции проводили с использованием стандартных биотехнологических методик, опубликованных в сборнике (Маниатис Т., Фрич Э., Сэмбрук Дж. , [10]).
В конце описания приведена нуклеотидная последовательность плазмиды pATLG 579 и аминокислотная последовательность гибридного белка, синтезируемого под контролем данной плазмиды.
Пример 5. Анализ уровня синтеза гибридного белка, обладающего антигенными свойствами E.coli HB101/pATLG 579.
Анализ белков в лизатах клеток E.coli HB101, содержащих гибридную плазмиду pATLG 579, проводили следующим образом. Два мл суспензии клеток E.coli HB101, содержащих плазмиду pATLG 579, выросших в течение ночи из отдельной колонии до концентрации 2000 млн. клеток/мл в L-бульоне, содержащем ампициллин, осаждали центрифугированием (12000g, 1 мин) и ресуспендировали в 200 мкл буфера, содержащего 50 mM трис HCl pH 7,8, 2,5% додецилсульфата натрия, 10% глицерина, 0,7% - меркаптоэтанола и 0,1% бромфенолового синего. Полученные препараты кипятили 5 мин на водяной бане с последующим анализом методом электрофореза [11]. В лизатах бактерий, содержащих плазмиду pATLG 579, обнаружен дополнительный белок с молекулярной массой 145 кДа.
Антигенную активность белка с молекулярной массой 145 кДа анализировали с помощью метода иммуноблота. Полученный гибридный белок обладал антигенной активностью HTLV-I/II. Уровень синтеза гибридного белка составлял не менее 30% от тотального клеточного белка.
Изобретение позволяет получать с 1 л клеточной суспензии 200-350 мг белка, обладающего антигенными свойствами HTLV-I/II. При этом 579 ак гибридного белка представлены следующим образом: 341 ак бета-галактозидазы, 2 ак кодируются полилинкерной последовательностью векторной плазмиды pUR 290, 234 ак представляют собой фрагмент гена gag HTLV-I/II и 2 ак кодируются полилинкером pUR 290 (терминатор).
Пример 6. Демонстрация возможности использования целевого продукта для создания диагностикума на HTLV-I/II.
Препараты белков, приготовленные по методике, изложенной в примере 5, разделяли методом электрофореза в ПААГ и анализировали методом иммуноблота с помощью сыворотки пациента, инфицированного HTLV-I, либо HTLV-II. В препарате белков, полученных из клеток, содержащих гибридную плазмиду pATLG 579, выявляли дополнительные полосы белков, специфически реагирующих с антителами к GAG HTLV-I/II. В препарате, использовавшемся в качестве контроля, приготовленном из клеток, содержащих исходный вектор pUR 290, такие полосы не идентифицированы.
Таким образом, плазмида pATLG 579 детерминирует в клетках E.coli синтез белков, обладающих антигенными свойствами GAG белков HTLV-I/II, поэтому данную плазмиду и штамм-продуцент можно использовать для создания диагностикумов на выявление антител к HTLV-I/II, циркулирующих у населения, проживающего на территории России.
Список литературы
1. Richardson J.H., Edwards A.J., Cruickshank J.K., Rudge P., and Dalgleish A. G. In vivo cellular tropism of human T-cell leukemia virus type I. // J. Virol. -1990, -Vol.64, P.5682-5687.
2. Hinuma. Y., Nagata K., Hanaoka M., Nakai M., Matsumoto Т., Kinoshita I. , Shirakawa S. , and Miyoshi. Adult, T-cell leukemia: antigen in an ATL cell line and detection of antibodies to the antigen In human sera. // Proc. Natl.Acad. Sci.USA. -1981, -Vol.78, P. 6476-6480.
3. Pancake В.A., Zucker-Franklin D. The difficulty of detecting HTLV-I proviral sequence in patients with Mycosis Fungoides. // J. of Acquired Immune Deficiency Syndromes and Human Retrovirology -1996, -Vol. 13, -No.4, -P.314-319.
4. Osame M., Usuku K., Izumo S., Ijuchi N., Amitani H., Igata A., Matsumoto M., and Tara M. HTLV-I associated myelopathy, a new clinical entity. // Lancet - 1986, 1:1031-1032.
5. Mochizuki M., Ono A., Ikeda E., Hikita N., Watanabe Т., Yamaguchi K., Sagawa K. , and Ito K. HTLV-I uveits. // J. of Acquired Immune Deficiency Syndromes and Human Retrovirology. - 1996, -Vol. 13, -No.1, P. 50-56.
6. Yamashita M., Ido E., Miura Т., and Hayami M. Molecular epidemiology of HTLV-I in the world. // J. of Acquired Immune Deficiency Syndromes and Human Retrovirology. -1996, -Vol.13 - No.1, -P. 124-131.
7. Сенюта. Н.Б., Степина В.Н., Гурцевич В.Э., Мазурин B.C., Яковлева Л. С. Антитела к вирусу Т-клеточного лейкоза человека в сыворотках крови у жителей Сахалина и Южно-Курильска. // Экспериментальная онкология -1988, Т.10, Н.2, C.37-38.
8. Gressain A. , Malet C. , Robert-Lamblin J., Lepera A., David P., Chichlo B., Sousova O., Stepina V., Gurtsevitch V., Tortevoye P., Hubert A., de The G. Serological evidence of HTLV-I but not HTLV-II infection in ethnic groups of Northern and Easten Siberia. // J. of Acquired Immune Deficiency Syndromes and Human Retrovirology. -1996, -Vol. 11, -No.4, P.413-414.
9. Seiki M., Hattori S., Hirayama Y. and Yoshida M. Human adalt T-cell leukemia virus: complete nucleotide sequence of the provirus genome integrated in leukemia cell DNA. // Proc. Natl. Acad.Sci. -1983. -Vol.80, -P. 3618-3622.
10. Маниатис Т. , Фрич Э. и Сэмбрук Дж. Методы генетической инженерии. Молекулярное клонирование. Пер.англ. -М., 1984.
11. Laemmli U.K. Cleavage of structural proteins during the assembly of the head of bacteriophage T4. // Nature. - 1970, -Vol. 227, -No.5259, -P. 680-685.


Изобретение относится к области биотехнологии, генной инженерии, иммунологии и может быть использовано для проведения серодиагностики HTLV-I/II. Изобретение представлено новым, оригинальным, искусственно созданным плипептидом, состоящим из продукта экспрессии фрагмента гена gag HTLV-1, слитого с бета-галактозидазой E.coli, и реагирующим с антителами к продукту гена gag HTLV-I/II, фрагментом ДНК ATLG 579, штаммом E.coli HB101, трансформированным рекомбинантной плазмидой pATLG 579, содержащей фрагмент ДНК ATLG 579. Источником HTLV-I/II-gag-специфических нуклеотидных последовательностей служили мононуклеарные клетки HTLV-инфицированного донора. Фрагмент ДНК, соответствующий области гена gag HTLV-I/II и кодирующий область генома с координатами 1253 - 1952 п.н., был амплифицирован в цепной полимеразной реакции (PCR). Рекомбинантная плазмида pATLG 579 получена путем лигирования с использованием ДНК-лигазы фага Т4 ДНК амплифицированного фрагмента (размером 699 п.н.), выделенного из агарозного геля и гидролизированного ферментами BamHI и ClaI с линеаризированной формой ДНК плазмидного вектора pUR 290. После инкубации компетентные клетки E.coli трансформируют гибридной ДНК с последующим отбором трансформированных колоний клеток. Изобретение позволяет получать с 1 л клеточной суспензии 200-350 мг белка, обладающего антигенными свойствами HTLV-I/II. 3 с.п. ф-лы.
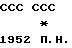
2. Рекомбинантная плазмидная ДНК pATLG 579 размером 5,9 т.п.н., содержащая BamY-II-Clal фрагмент вектора pUR 290 и кодирующая полипептид G579 с молекулярным весом 145 кДа, предназначенный для определения антител к вирусам Т-клеточного лейкоза человека I и II типа, состоящий из бета-галактозидазы, двух аминокислотных остатков Ser и Val, кодируемых полилинкерной областью, и вирусспецифической части, кодируемой геном gag, содержащим фрагмент по п.1.
| RU 93058018, 27.10.1996 | |||
| 0 |
|
SU181107A1 | |
Авторы
Даты
2000-05-27—Публикация
1998-07-02—Подача