Изобретение относится к области аналитической химии, к новому методу разделения и определения ионов, использующему эффекты неравновесных гетерофазных процессов, в частности эффекты ионного обмена.
Известен способ ионообменного разделения с последующим кондуктометрическим определением ионов - метод ионной хроматографии [Small Н., Stevens T. S. , Bauman W.C., Novel ion exchange chroma-tographic method using conductometric detection, Anal. Chem., 1975, V.47, N 11, P.1801-1809]. Согласно данному способу для разделения смеси ионов используется разделяющий ионообменник, заполняющий хроматографическую колонку, через которую под высоким давлением (десятки бар) пропускают элюент, в поток которого в первый момент времени кратковременно дозируют смесь ионов. Элюент представляет собой раствор, содержащий смесь оснований или солей слабых кислот при анализе анионов и смесь кислот при анализе катионов. После разделяющей колонки последовательно расположены подавитель и датчик кондуктометра. В качестве подавителя обычно используют ионообменную колонку с катионитом в водородной форме при анализе анионов или с анионитом в гидроксильной форме при анализе катионов. Датчик чувствительного кондуктометра с электрической компенсацией сигнала имеет хорошо промываемый объем величиной в 10-50 мкл.
Способ позволяет селективно разделять и с хорошей воспроизводимостью (1-5%) определять сложные смеси ионов с низкими концентрациями, пределы обнаружения составляют 0,1-1,0 мкмоль/л. Длительность одного анализа обычно составляет 10-30 мин. К недостаткам метода можно отнести не очень высокую эффективность разделения (2-5 тыс. теоретических тарелок). Кроме того, метод требует сложного и дорогого оборудования, например, насосов высокого давления и материалов - разделяющих ионообменников.
Известна проточная ячейка - устройство для исследования ионного обмена, имеющая фиксированный тонкий слой зернистого ионообменника [Сенявин М.М. Ионный обмен в технологии и анализе неорганических веществ, М., Химия, 1980, с. 88-90]. Ячейка содержит корпус с установленной в центральной части пластиной из ионообменника, расположенный в верхней части корпуса трехходовой кран, соединенный с трубопроводами для подачи воды, раствора изучаемого иона и десорбирующего раствора. За счет быстрого пропускания растворов в ячейке осуществляется режим хронометрируемой сорбции каждым зерном ионообменника при постоянной концентрации сорбируемого вещества на границе зерна.
Ячейка служит для получения кинетической кривой ионного обмена - зависимости концентрации сорбированного ионообменником вещества от времени, по которой можно определить коэффициент внутренней диффузии сорбируемого вещества.
Несмотря на полезность ячейки при определении кинетических характеристик ионного обмена (в том числе, многокомпонентного ионного обмена), она не позволяет наблюдать электрические эффекты ионного обмена и, следовательно, использовать эти эффекты для анализа смесей ионов.
Наиболее близким к предлагаемому способу является метод потенциометрии с применением ионоселективных электродов [Морф В. Принципы работы ионоселективных электродов и мембранный транспорт. Перевод с английского под редакцией О. М. Петрухина, М., Мир, 1985, 280 с.]. В способе используется электрохимическая ячейка с анализируемым раствором, в который погружены ионоселективные электроды и электрод сравнения, подключенные к чувствительному вольтметру. Ионоселективный электрод представляет собой герметичную камеру, закрытую с одной стороны ионоселективной мембраной. В камеру залит раствор, в который опущен металлический электрод. Внутренний раствор и мембрана служат для селективного транспорта определяемых ионов, с помощью которых осуществляется перенос электрического заряда, что приводит к изменению потенциала мембраны, измеряемого вольтметром.
Способ позволяет достичь высокой селективности и чувствительности в определении ряда ионов. К недостаткам метода можно отнести отсутствие возможности анализировать смеси ионов и недостаточную универсальность способа из-за отсутствия электродов на многие ионы.
Наиболее близким техническим решением устройства является электрохимическая ячейка для твердофазного разделения и определения ионов, включающая аналитическую камеру с исследуемым раствором, две вспомогательные камеры с растворами электролитов, ионообменную мембрану и два электрода, соединенные внешней электрической цепью со средством измерения потенциала [Морф В. Принципы работы ионоселективных электродов и мембранный транспорт. Перевод с английского под редакцией О.М. Петрухина, М., Мир, 1985, с.12-13].
Аналитическая камера с исследуемым раствором представляет собой камеру, заполненную исследуемым раствором.
Первая вспомогательная камера с раствором электролита - ионоселективный электрод (ИСЭ) - представляет собой гальванический полуэлемент, состоящий из ионоселективной (ионообменной) мембраны, внутреннего контактирующего раствора и внутреннего электрода сравнения.
Вторая вспомогательная камера с раствором электролита - электрод сравнения - представляет собой гальванический полуэлемент, образованный внешним электродом сравнения, погруженным в стандартный электролит.
Электроды соединены внешней электрической цепью со средством измерения потенциала, например вольтметром.
Внутренний раствор и мембрана первой вспомогательной камеры служат для селективного транспорта определяемых ионов, с помощью которых осуществляется перенос электрического заряда, что приводит к изменению потенциала мембраны, измеряемого вольтметром.
Однако, конструкция электрохимической ячейки с разнесенными вспомогательными камерами не позволяет осуществить процесс многокомпонентного ионного обмена (с числом компонентов не менее трех) внутри ионообменной мембраны, так как внутренний раствор второй вспомогательной камеры не контактирует с мембраной. В связи с этим рассмотренная ячейка не способна в принципе измерять электрические эффекты нестационарного многокомпонентного ионного обмена.
Задачей настоящего изобретения является создание нового способа и ячейки для разделения и определения ионов, обладающего универсальностью, достаточной для анализа смесей ионов, как анионов, так и катионов, и простотой исполнения.
Поставленная задача решается созданием нового способа твердофазного разделения и определения ионов, в котором определение проводят в электрохимической ячейке с аналитической и двумя вспомогательными камерами. Камеры выполнены проточными и имеют одну общую стенку в виде катионообменной или анионообменной мембраны, контактирующей непосредственно с электродами. Через вспомогательные камеры, с одновременным наложением внешнего потенциала до получения постоянной величины измеряемого сигнала, пропускают соответственно растворы кислоты или основания и солевые растворы с расходом, определяемым формулой: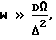
где D - коэффициент диффузии анализируемого иона в фазе мембраны, Δ - толщина мембраны, Ω - объем камеры. Пробу анализируемого раствора дозируют в поток деионизованной воды, поступающий в дополнительную камеру, установленную внутри одной из камер непосредственно на мембране, регистрируют зависимость ϕ/t или ϕ′/t, где ϕ - значение потенциала, ϕ′ - значение производной потенциала по времени, t - время от момента ввода пробы, при этом по высоте скачка потенциала судят о количестве, а по времени регистрации скачка потенциала - о природе анализируемых ионов.
Кроме того, поставленная задача решается тем, что электрохимическая ячейка для твердофазного разделения и определения ионов, включающая аналитическую камеру с исследуемым раствором, две вспомогательные камеры с растворами электролитов, ионообменную мембрану и два электрода, соединенные внешней электрической цепью со средством измерения потенциала, выполнена в виде корпуса с расположенной в нем ионообменной мембраной, герметично соединенной по периферии со стенками корпуса и образующей с последними вспомогательные камеры, в одной из вспомогательных камер расположена аналитическая камера, выполненная в виде цилиндра с основаниями, одним из которых является ионообменная мембрана, аналитическая и вспомогательные камеры снабжены патрубками ввода и вывода соответственно исследуемого раствора и растворов электролитов, соединенными с линиями подачи и отвода указанных растворов, при этом линия подачи исследуемого раствора снабжена дозатором, электроды расположены с двух сторон ионообменной мембраны в непосредственном контакте с последней, один из них выполнен в виде сетки с токоподводом, а вторым электродом является цилиндр аналитической камеры.
На фиг. 1 представлена схема предложенной электрохимической ячейки для твердофазного разделения и определения ионов.
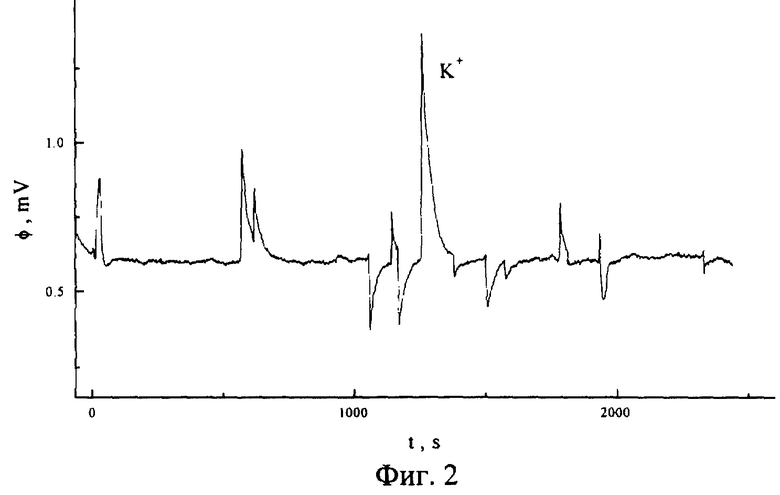
На фиг.2 представлена потенциограмма ионов калия.
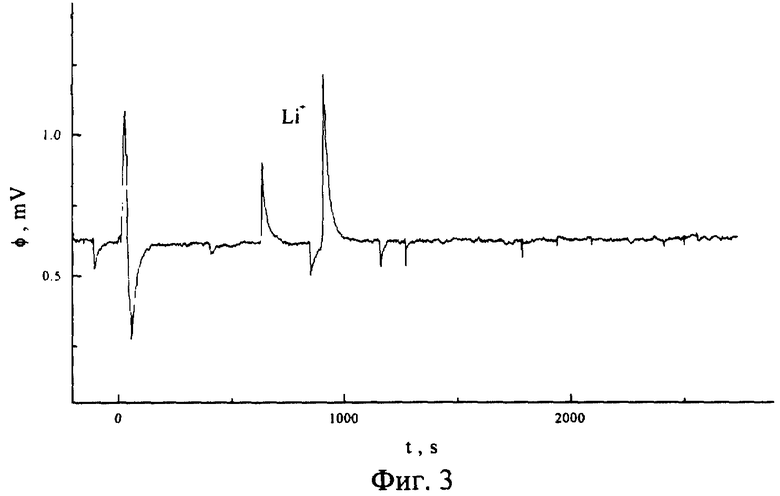
На фиг.3 представлена потенциограмма ионов лития.
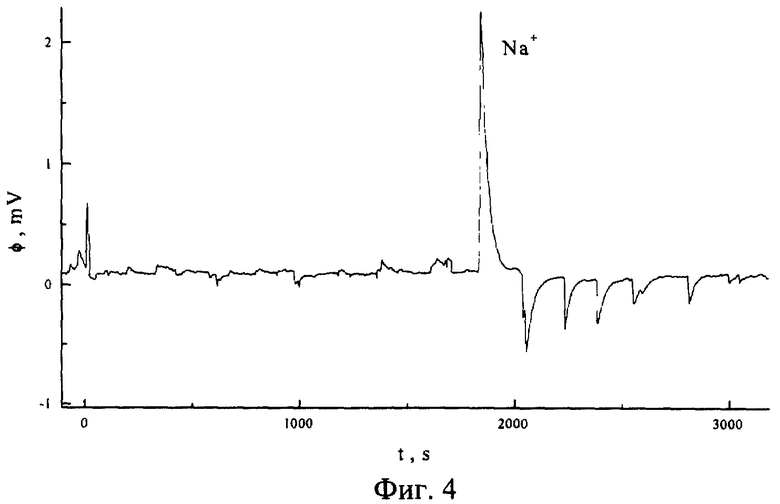
На фиг.4 представлена потенциограмма ионов натрия.
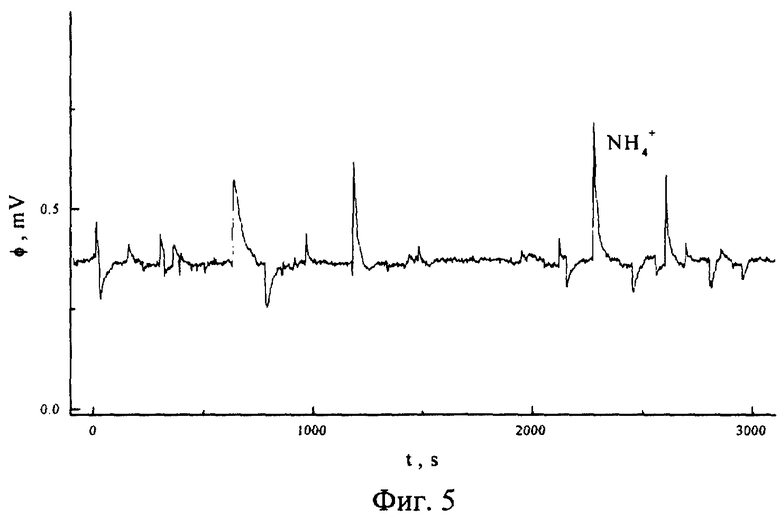
На фиг.5 представлена потенциограмма ионов аммония.
На фиг. 6 представлена потенциограмма смеси катионов лития, натрия и аммония.
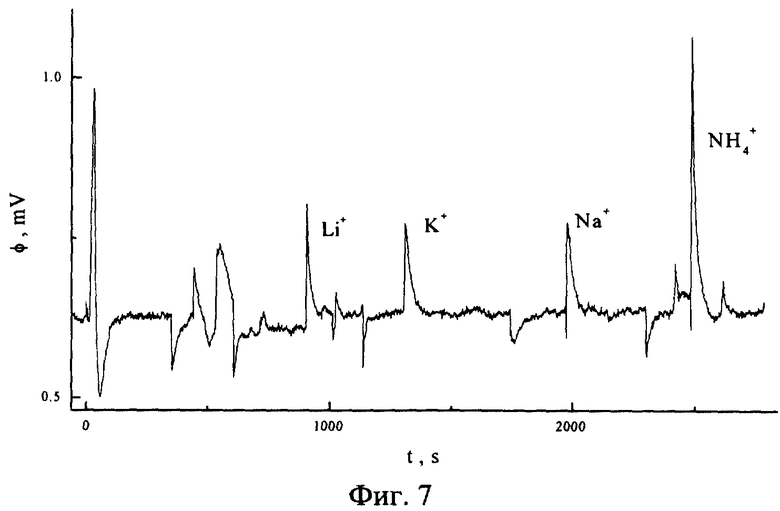
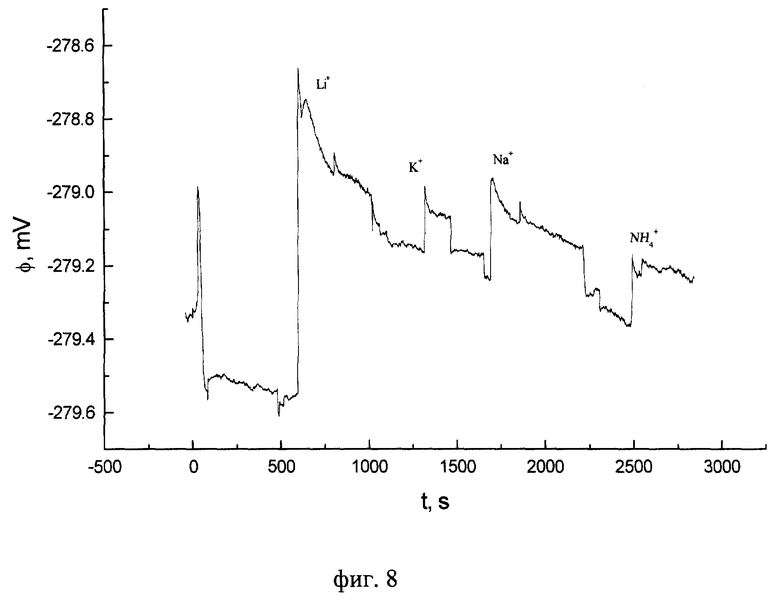
На фиг. 7, 8 представлены потенциограммы смеси катионов лития, натрия, калия и аммония.
Заявляемые способ и ячейка базируются на принципе кинетического ионообменного разделения фронтов ионов в твердой фазе; принципе использования явления макроскопического электрического поля в нестационарном многокомпонентном ионном обмене для регистрации достижения фронтом иона чувствительной зоны внутри ионита; принципе усиления электрических эффектов кинетики многокомпонентного ионного обмена за счет проскока коионов внутрь ионита.
Известно, что подвижность ионов в твердой фазе отличается от их подвижности в жидкой фазе, причем подвижности в твердой фазе - если ею является ионит - сильно зависят от сорбируемости ионов [Гельферих Ф. Иониты. Основы ионного обмена. Пер. с англ. Под ред. С.М. Черноброва, М., Изд-во иностр. литер. , 1960, 490 с.]. Это усиление селективности твердой фазы по отношению к жидкой фазе дает возможность гораздо лучше разделять фронты ионов и поэтому ограничиться относительно малыми длинами их пути.
Для регистрации момента достижения фронтом иона некоторой геометрической поверхности внутри твердой фазы в предлагаемом способе используется явление макроскопического электрического поля в нестационарном многокомпонентном ионном обмене (МЭП-МИО). МЭП-МИО возникает вследствие кратковременного (кинетического) нарушения электрического баланса в ионите. Так, внесение в стационарную систему, содержащую ионит и два противоположных потока макрокомпонентов, малого количества третьего компонента и прохождение его фронтом границы раздела зон макрокомпонентов приводит к нарушению диффузионного потенциала системы. Для получения такого эффекта диффузионные коэффициенты (D) и потоки ионов (J) должны удовлетворять следующим неравенствам:
DM1 < DM2; DM1 < Dm; (JM1Jm) > 0,
где индексы M1, M2 относятся к макрокомпонентам, а m - к микрокомпоненту. Несмотря на то, что возникающее поле носит макроскопический характер, его величина обычно очень мала, и поэтому прямая его регистрация чрезвычайно затруднительна.
Другой причиной, приводящей к изменению стационарного диффузионного поля - проскок в ионит коионов. Этот эффект приводит к гораздо более сильным полям, однако проскоку коионов внутрь ионита препятствует доннановский барьер - электростатический потенциал той же полярности, что и коионы. Если путем выбора концентраций макрокомпонентов или с помощью наложения внешнего поля скомпенсировать доннановский потенциал на границе ионита почти полностью - так, чтобы возникающий кинетический потенциал нейтрализовал его оставшуюся часть, то тогда явление МЭП-МИО приведет к сильному электрическому эффекту.
При разработке способа анализа смесей электролитов использовали ячейку, схема которой дана на фиг. 1. Ее главным элементом является ионообменная мембрана 1, разделяющая три гидравлически не связанные проточные камеры: вспомогательные 2 и 3 и аналитическую 4. К аналитической камере подключен дозатор 5. С мембраны снимают потенциалы два электрода: сетка 6 с токоподводом и кольцевой электрод (цилиндр аналитической камеры 4). Эти электроды связаны последовательно с конденсатором 7 (емкостью 15 мкФ) и с высокоомным входом вольтметра 8, подключенного с помощью аналого-цифрового преобразователя (АЦП) к персональному компьютеру IBM PC 486 с необходимым программным обеспечением. С помощью устройства с обратной функцией (ЦАП) задаваемая компьютером постоянная ЭДС (0 ± 5 В, точность 0,5 мВ) источника ЭДС 9 поступает на электроды ячейки через резистор 10, номинал которого имеет порядок сопротивления мембраны 1. Мембрана 1 катионообменная (марки мембран: SKE-40, SKE-708, SKE-596, SKE- 503, Nafion с сульфогруппами; промышленная мембрана МК-40, Россия) или анионообменная (Nafion с аммониевыми основаниями; промышленная мембрана МА-40, Россия) имеет форму круглой пластинки диаметром 20 мм. Электроды изготовлены из благородных металлов (платиновая сетка и палладиевый цилиндр аналитической камеры). Эта схема позволяет измерить зависимость производной потенциала мембраны (ϕ′) от времени. Для измерения зависимости потенциала мембраны (ϕ) от времени следует исключить из схемы конденсатор 7.
Пример 1.
Через аналитическую камеру 4 объемом 0,5 мл со скоростью 1 мл/мин пропускают бидистиллированную воду (С); через вспомогательную камеру 3 объемом 1,5 мл со скоростью 0,5 мл/мин пропускают разбавленный раствор (0,5 мМ) ортофосфорной кислоты (В); через камеру 2 объемом 2,0 мл со скоростью 0,5 мл/мин пропускают раствор (А) иодида тетраметиламмония (ТМА; 3,2 мМ). Между электродами внешним источником ЭДС 9 создают постоянную разность потенциалов, равную 300 мВ. Перед вводом пробы систему длительное время (не менее 1 часа) выдерживают в указанном режиме. Этот же режим поддерживают и при проведении анализа. В начале анализа в поток С с помощью дозатора 5, расположенного непосредственно перед аналитической камерой 4, вводят порцию анализируемого раствора (5 мкмоль/л KCl) объемом 20 мкл. Далее регистрируют производную потенциала мембраны ϕ′ от времени с помощью высокоомного вольтметра. Все реактивы, использованные для приготовления растворов, имели квалификацию "хч" или "осч".
Результаты анализа представлены на фиг.2. В момент ввода пробы на потенциограмме наблюдается пик ввода пробы, затем устанавливается горизонтальная базовая линия, а в интервале 1200-1300 с после ввода пробы наблюдается острый пик иона калия, амплитуда которого составляет более 1 мВ. Присутствие на потенциограмме других, более мелких, пиков обусловлено примесями, содержащимися в реагентах.
Примеры 2-7 иллюстрируют анализ растворов других катионов и их смесей (фиг. 3-8). Условия проведения опытов те же, что и в примере 1.
В частности, на фиг. 7 показана зависимость производной потенциала ϕ′ от времени для смеси веществ, содержащих ионы лития, натрия, калия и аммония (введено: (64 Li+ + 40 К+ + 32 Na+ + 32 NH4 +) пмоль), а на фиг. 8 - зависимость потенциала мембраны ϕ от времени для той же смеси ионов.
Из представленных примеров следует, что предлагаемые способ и ячейка для его осуществления позволяют осуществлять очень чувствительный анализ многокомпонентных смесей ионов различной природы. Способ твердофазного разделения и определения ионов по качеству (эффективности) разделения превосходит метод ионной хроматографии, сопоставим с современным капиллярным электрофорезом, однако является гораздо более простым в исполнении.
| название | год | авторы | номер документа |
|---|---|---|---|
| СИСТЕМА ИЗОТОПНОГО ХРОМАТО-МАСС-СПЕКТРОМЕТРИЧЕСКОГО АНАЛИЗА ОРГАНИЧЕСКИХ ГАЗОВЫХ СМЕСЕЙ И ТВЕРДОЭЛЕКТРОЛИТНАЯ ЯЧЕЙКА | 2006 |
|
RU2315289C1 |
| СИСТЕМА ИЗОТОПНОГО ХРОМАТО-МАСС-СПЕКТРОМЕТРИЧЕСКОГО АНАЛИЗА ОРГАНИЧЕСКИХ ГАЗОВЫХ СМЕСЕЙ | 2008 |
|
RU2383013C1 |
| СОСТАВ МЕМБРАНЫ ИОНОСЕЛЕКТИВНОГО ЭЛЕКТРОДА ДЛЯ ОПРЕДЕЛЕНИЯ АКТИВНОСТИ ПЕРРЕНАТ-ИОНОВ | 1994 |
|
RU2083979C1 |
| СПОСОБ СОРБЦИОННОГО КОНТРОЛЯ ЗАГРЯЗНЕНИЯ ВОДНЫХ ОБЪЕКТОВ | 2000 |
|
RU2176788C1 |
| УЗЕЛ ВОССТАНОВЛЕНИЯ ДЛЯ МАСС-СПЕКТРОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ ИЗОТОПНОГО СОСТАВА ВОДОРОДА ВОДЫ И ОРГАНИЧЕСКИХ КИСЛОРОДОСОДЕРЖАЩИХ СОЕДИНЕНИЙ | 2011 |
|
RU2477464C1 |
| ИОНОСЕЛЕКТИВНЫЙ ПОЛЕВОЙ ТРАНЗИСТОР | 1995 |
|
RU2097755C1 |
| УСТРОЙСТВО ФОРМИРОВАНИЯ ТЕРМОЛИНЗЫ ДЛЯ ТЕРМОЛИНЗОВОЙ СПЕКТРОМЕТРИИ | 2005 |
|
RU2282180C1 |
| Способ определения газов в металлах и металлических сплавах | 1983 |
|
SU1190722A1 |
| Мембрана ионоселективного электрода для определения нитрит-иона | 1982 |
|
SU1050363A1 |
| Электрохимическая ячейка для ультрамикроанализа | 1984 |
|
SU1288571A1 |

Твердофазное разделение и определение ионов основаны на применении электрохимической ячейки с аналитической и двумя вспомогательными камерами, ионообменной мембраной и электродами и регистрации электрических потенциалов. Определение проводят в ячейке, камеры которой выполнены проточными и имеют одну общую стенку в виде катионообменной или анионообменной мембраны, контактирующей непосредственно с электродами. Через вспомогательные камеры с одновременным наложением внешнего потенциала до получения постоянной величины измеряемого сигнала пропускают соответственно растворы кислоты или основания и солевые растворы с расходом, который вычисляется по соответствующей формуле. По высоте скачка или пика потенциала судят о количестве, а по времени регистрации скачка потенциала - о природе анализируемых ионов. Обеспечена высокая селективность и чувствительность в определении ряда ионов. 2 с.п. ф-лы, 8 ил.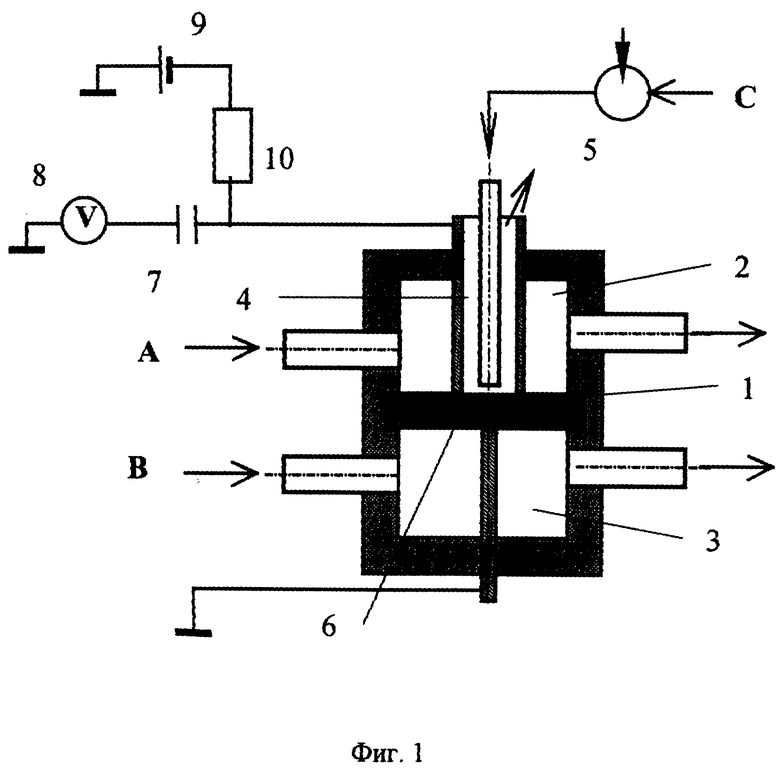
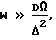
где D - коэффициент диффузии анализируемого иона в фазе мембраны;
Δ - толщина мембраны;
Ω - объем камеры,
а пробу анализируемого раствора дозируют в поток деионизованной воды, поступающий в дополнительную камеру, установленную внутри одной из камер непосредственно на мембране, регистрируют зависимость ϕ/t или ϕ′/t, где ϕ - значение потенциала, ϕ′ - значение производной потенциала по времени, t - время от момента ввода пробы, при этом по высоте скачка или пика потенциала судят о количестве, а по времени регистрации скачка потенциала - о природе анализируемых ионов.
| МОРФ В | |||
| Принципы работы ионоселективных электродов и мембранный транспорт.-М.: Мир, 1985, с.12-13 | |||
| Ионоселективный дифференциальный датчик | 1983 |
|
SU1265574A1 |
| RU 2001394 C1, 15.10.93 | |||
| US 3655528 A, 11.04.72 | |||
| US 3865708 A, 11.02.75. | |||
Авторы
Даты
2000-05-27—Публикация
1999-03-16—Подача