Изобретение относится к быстрому анализу для выявления и/или определения глутатионовых S-трансфераз (GSTs) для использования при оценке состояния органа.
Уровень техники
GSTs представляют мультигенное семейство белков, состоящих, в основном, из изоформ α,μ,θ и π-классов и ответственных за детоксикацию ряда ксенобиотиков, в основном, путем конъюгации с глутатионом. Альфа GST (αGST) является основной печеночной формой и равномерно распределена в печени. Напротив, PiGST (πGST) находится, в основном, в эпителиальных клетках, выстилающих желчные протоки. Подобное уникальное распределение имеет место также в почках, где αGST находится в проксимальных канальцах, a πGST ограничена областью дистальных канальцев нефрона. Из этого можно сделать вывод, что измерение уровней GST в плазме или моче облегчит мониторинг состояния как печени, так и почек индивидуума. Действительно, многие авторы использовали замеры GST, чтобы оценить повреждение как печени, так и почек у индивидуумов, которым была сделана пересадка органа, или у которых был поражен орган вследствие воздействия токсинов печени или почек (см., например, Trull, a.k. et al., Transplantation (1994) 58, 1345-1'351).
В настоящее время такие измерения, как правило, выполняются с использованием радиоиммуноанализа (RIA). Однако, в последнее время ряд ферментных иммуноанализов (EIAs) на основе микротитрационного планшета стало возможно получать из компании Biotrin International Limited, Mount Merrion, County Dublin, Ireland, и они позволяют измерять уровни α и πGST в биологических жидкостях. Эти EIAs теперь широко применяются учеными, несмотря на некоторый первоначальный скептицизм (см. Beckett, G.J. and Hayes J.D. Advances in Clinical Chemistry (1993) 30, p.325)). Таким образом, в настоящее время RIA является способом определения, который выбирают многие, работающие в этой области. Обе эти методики имеют определенные недостатки, так как они требуют как специализированного оборудования, так и наличия высококвалифицированных и компетентных работников для получения существенных и точных результатов. Такие анализы являются относительно длительными, и от их начала до завершения проходит, в среднем, два и более часов. Следовательно, необходим более быстрый анализ на GSTs.
Способы определения изоферментов GST имеют тенденцию к усложнению, о чем свидетельствует использование флуорометрического иммуноанализа с разрешением времени (TR-IFMA). В работе Tiainen, P et al. (Clin. Chem. (1996) 42 2, 334-335) сравнивается ферментный иммуноанализ (EIA) и TR-IFMA для α-GST. В качестве EIA использовался Hepkit (товарный знак Biotrin International, Dublin). Было обнаружено, что в Hepkit была достигнута большая точность анализа, чем в TR-IFMA. Установлено также, что TR-IFMA является несколько более трудоемким, чем Hepkit, потому что большее количество репликаций (четыре) и циклов промывания потребовалось для завершения процедуры анализа. Поэтому ясно, что современные исследования в области выявления и количественного определения GST сосредоточены на разработке более совершенных и сложных систем определения, таких, как TR-IFMA.
За пациентами, которые перенесли пересадку органа, или у которых имеются поражения органа вследствие воздействия токсинов печени или почек, должно вестись тщательное наблюдение. Это в особенности важно для пациентов, которым был пересажен орган, и которые проходят период посттрансплантационной терапии с использованием иммуносупрессантов, в частности, циклопорина. После выписки из больницы они должны находиться под постоянным наблюдением, что в настоящее время связано с частыми возвращениями в больницу для проведения необходимых анализов на GST и других. Соответственно, было бы желательно, чтобы такие люди имели средство самоконтроля, которое сокращало бы количество посещений больницы, а также,
- что более важно, - давало бы пациенту и врачу возможность раннего определения необходимости вмешательства в том случае, когда выявлено превышение нормального уровня GST.
Таким образом, способ, который позволил бы осуществлять более быстрое и простое определение GST в плазме, моче и других биологических жидкостях, например, в желчи, обладал бы большими преимуществами, так как он позволял бы врачу наблюдать за состоянием печени или почки пациента, не прибегая к длительным или дорогостоящим исследованиям в больничных условиях.
Другой областью, где требуется быстрый анализ, является оценка органа перед трансплантацией или в экспериментах ex vivo. В настоящее время не существует общепринятого способа оценки донорского органа перед его трансплантацией реципиенту. Соответственно, невозможно точно предсказать окончательный результат операции по трансплантации, если не было определено первоначальное качество донорского органа. Любой способ, который помог бы оценить состояние донорского органа перед трансплантацией, в значительной степени способствовал бы оценке окончательного результата операции и мог бы позволить врачу по возможности раньше прибегнуть к посттрансплантационной поддерживающей терапии, чтобы предотвратить потерю трансплантанта вследствие его плохого качества или отторжения рецепиентом.
Как часть обычных процедур по реабилитации органа, донорский орган приводится в равновесное состояние или перфузируется определенными реагентами (например, буфером Висконсинского Университета) после удаления из организма донора. Этот и другие реагенты служат для поддержания ex vivo целостности органа при низких температурах (4 - 10oC) до введения его в организм реципиента, а также для поддержания сохраняемого органа в равновесном состоянии с температурой тела (37oC) до хирургической операции по пересадке реципиенту. Очевидно, что качество донорского органа будет зависеть от многих факторов, таких, как состояние здоровья донора, время и температура его хранения ex vivo, процедуры обработки, качества консервации использованных реагентов. Так, повреждение трансплантанта ex vivo, обусловленное каким-либо из вышеуказанных факторов, могло бы наблюдаться посредством оценки утечки ферментов из органа.
Быстрые анализы известны. Например, в патенте ЕР 0291 194 B1 описаны и заявлены устройство и способ аналитического тестирования с использованием этого устройства, которые пригодны для использования в домашних условиях и хирургических кабинетах клиник, и которые дают быстрый аналитический результат и требуют минимальной степени квалификации и усилий пользователя. Указано, что устройство особенно приемлемо для определения беременности. Какие-либо упоминания о GSTs отсутствуют. Уровни маркерных гормонов у беременной женщины, таких, как хорионгонадотропин человека (HCG), обычно присутствуют в более высоких концентрациях и, таким образом, могут быть определены легче, чем уровни GSTs у вышеописанных пациентов, для которых повышенные уровни GST являются опасными или указывающими на клинические явления, представляющие угрозу для жизни в будущем.
Трудность использования измерений ферментной активности для различения изоформ GSTs хорошо документально отражена (См. выше Beckett G.J. and Hayes, J. D. (1993)). Как указано выше, другие исследователи использовали RIA (Howie, A. F. et al. (Clinica Chimica Acta (1989) 184, 269 - 278) и TR-IFMA (Tiainen, P. and Karhi, K.K. Clin. Chem. (1994) 40-2, 184 - 189) для определения GSTs. Каждая из этих методик является очень чувствительной для определения биомолекул. Однако каждая методика требует специализированного оборудования и квалифицированного персонала. Например, TR-IFMA требует использования специального флуорометра с разрешением времени.
Понятно, что требуется такая методика, которая была бы приемлемой для не специалистов или в кризисных ситуациях, когда требуется быстрый и простой анализ. Примером кризисной ситуации может быть повреждение печени или почки после трансплантации, или потенциальные нарушения в печени, вызванные передозировкой парацетамола.
Описание изобретения
В соответствии с этим, изобретение представляет собой способ быстрой оценки состояния органа в объекте на основе определения одного или более изоферментов глутатионовой S-трансферазы (GST) в различных биологических жидкостях; и этот способ включает в себя контактирование меченого частицами антитела против GST, специфичного для указанного изофермента, с образцом биологической жидкости, в которой предполагается содержание указанного изофермента, причем указанное антитело имеет чувствительность, достаточную для определения, как минимум, пикомолярного количества указанного изофермента, и захват комплекса меченое частицами антитело/изофермент на иммобилизованном антителе для получения визуально различимого сигнала.
Под понятием "быстрый" имеется в виду то, что выявление или определение изофермента GST обычно происходит за промежуток времени порядка 30 минут от первоначального контакта с меченым частицами анти-GST.
Под состоянием органа здесь понимается повреждение органа после иммунологического или токсикологического поражения.
Специалистам в данной области будет понятно, что значительные преимущества данного изобретения связаны с его простотой, так что оно может использоваться лицами, которые имеют лишь небольшую (или вообще не имеют) подготовку для наблюдения за своим собственным состоянием здоровья, а также оно обеспечивает быстрое получение информации в кризисных ситуациях такого типа, как описанные выше.
Предпочтительно, GST представляет собой αGST, πGST или μGST печеночного или почечного происхождения.
Более предпочтительно, GST представляет собой αGST или πGST печеночного или почечного происхождения.
Особым требованием любого быстрого анализа на GST является антитело с необходимой восприимчивостью к GST.
В случае αGST было индуцировано поликлональное антитело со способностью определения низких концентраций αGST, вплоть до 6,5 нг/мл, как будет описано ниже, что имеет большое значение для чувствительности способа в целом.
В общем случае, антитело, которое может быть моноклональным или поликлональным, со способностью определения таких низких концентраций изоферментов GST, как 5 нг/мл, является предпочтительным для использования в соответствии с данным изобретением.
Антитело против GST, связанное с твердой фазой, может быть поликлональным антителом, а более конкретно, поликлональным lgG. Однако в некоторых случаях, например, в случае πGST, твердофазное антитело является, предпочтительно, моноклональным антителом.
Антитело против GST может быть связано с нитроцеллюлозной мембраной известного типа, например, такой, которая может быть получена германской компанией Schleicher and Schuell GmbH. Такие мембраны имеют естественную способность к связыванию белков, включая иммуноглобулины. Однако было бы важно, чтобы различные твердые подложки, по сути известные, могли бы использоваться как подложка для иммобилизованного антитела. Такие подложки здесь упоминаются, в основном, как твердая фаза.
Нитроцеллюлозная мембрана может иметь величину пор в диапазоне 5 - 10 μm.
Неспецифичные сайты связывания на нитроцеллюлозной мембране выборочно блокируются в зависимости от вида анализа, в соответствии с вышеописанным. Блокирование неспецифических сайтов связывания может быть достигнуто обработкой белком, таким, как коровий сывороточный альбумин или молочный белок, или обработкой полимером, таким, как поливинил-пирролидон, при помощи известного способа.
Твердая фаза может иметь различные конструкции и включать устройства такого типа, как описано в вышеупомянутом патенте ЕР 0 291 194 B1, с учетом того, что используемое антитело против GST имеет требуемую специфичность.
Под специфичностью используемого антитела против GST понимается восприимчивость антитела к соответствующей GST. Эта восприимчивость выражена скорее как определяемая концентрация анализируемого вещества, чем посредством более теоретических способов выражения, таких, как Ka специфической восприимчивости при данной концентрации.
Твердая фаза может быть помещена в корпус из пластмассы и снабжена фитильком на одном или на обоих концах для облегчения хроматографического движения компонентов иммуноанализа.
Биологическая жидкость, используемая в способе по данному изобретению, может быть желчью, плазмой, сывороткой или мочой, а более предпочтительно, плазмой, сывороткой или мочой.
Биологическая жидкость может быть разбавленной или неразбавленной (чистой).
Биологическая жидкость может также быть перфузатом, и, таким образом, способ по данному изобретению может быть использован для оценки органа до трансплантации или при экспериментах ex vivo.
Как указано выше, не существует общепризнанного способа для оценки донорских органов. Мы показали, что быстрое определение GST в перфузатах возможно при использовании способа по данному изобретению как маркера состояния органа ex vivo. Скорость определения является существенной в этой ситуации, так как донорский орган подвергается воздействию однонаправленной и постоянной гипоксии ex vivo, что, в конечном итоге, приведет к необратимым нарушениям и сделает орган непригодным для трансплантации. Поэтому любой анализ, который позволит осуществлять оценку органа, будет иметь большую важность для врача.
Биологическая жидкость контактирует с меченым частицами антителом против GST, так что определяемый изофермент GST связывается с указанным меченым частицами антителом против GST до того, как он контактирует с иммобилизованным антителом. Частицы, которые могут быть использованы в качестве меток, включают в себя коллоидные частицы, латексные частицы и частицы металлического золя. Частицы металлического золя могут быть золотыми частицами, имеющими средний диаметр в диапазоне 15 - 40 нм. Такие золотые частицы могут быть закуплены; они продаются, например, компанией Janssen Life Sciences Products.
Меченое частицами антитело против GST может также быть помещено у погружаемого в образец конца любого устройства для вступления в контакт с биологической жидкостью в соответствии с данным изобретением.
Использование меченого частицами антитела против GST означает, что отсутствует стадия амплификации. Так, в случае, когда имеет место определение изоферментов GST меченым частицами антителом против GST, определение может быть основано просто на непосредственном взаимодействии антитела с антигеном с использованием меченых частицами антител для определения антигена или визуализации взаимодействия с соответствующими преимуществами в вышеописанных ситуациях.
Все это тем более удивительно, если принять во внимание, что, как это видно из литературы, у ученых имеется определенный скептицизм даже относительно использования EIA для определения GST, и даже посредством системы амплификации, что повышает чувствительность определения.
Наличие фитилька на каждом конце твердой фазы, как описано выше, является особенно предпочтительным, когда используется меченый частицами lgG против GST, так как он облегчает хроматографическое движение меченого частицами lgG. Например, в случае нитроцеллюлозной мембраны наличие фитилька на погружаемом в образец конце и другого - наверху мембраны, будет облегчать хроматографическое движение меченого золотом lgG, предварительно распыленного на мембране. Далее, нанесение очищенной GST поверх иммобилизованного lgG против GST на мембране будет действовать как внутренний/процедурный контроль для функции меченого золотом конъюгата lgG против GST.
В этом варианте присутствие жидкости в биологическом образце ресуспендирует меченый золотом lgG против GST, и присутствие любого изофермента GST связывается меченым золотом lgG. Этот комплекс затем мигрирует вверх и вдоль мембраны, притягиваемый верхним фитильком. Если присутствует достаточное количество изофермента GST, то комплекс, состоящий из GST и меченого золотом lgG против GST, иммобилизуется на мембране, где присутствует связанный lgG против GST. Результатом является положительный сигнал, указывающий, что в образце присутствует GST. Излишки меченого золотом конъюгата lgG против GST будут связываться с процедурным контролем (GST) на мембране.
Будет также очень важно, чтобы, при использовании меченого частицами антитела для связывания антигена в биологическом образце, определение связанного GST могло осуществляться за один этап посредством анализа, который можно назвать анализом "в одном сосуде".
В изобретении рассмотрен также набор для осуществления вышеописанного способа определения GST, который содержит антитело против GST, являющееся специфичным для изофермента GST, в соответствии с описанным в данном изобретении.
Описываемый здесь анализ отличается от вышеупомянутых иммуноанализов типа EIA и RIA двумя основными аспектами, Во-первых, порядок определения антигена является другим, так как в способе по данному изобретению антиген сначала связывается с меченым частицами антителом (PLA), а затем этот комплекс антиген-PLA захватывается иммобилизованным антителом, чтобы получить положительный сигнал. Таким образом, нет никакой необходимости в каких-либо промежуточных этапах, например, промывании мембраны для удаления несвязанного материала (например, других компонентов мочи, крови или перфузата) или добавлении какого-либо реагента амплификации для облегчения определения связанного комплекса антиген-PLA, т.е. комплекс является, фактически, "самоопределяющим".
Это положение резко отличается от того, которое имеет место в современных способах иммуноопределения GST (EIA/RIA), где антиген сначала контактирует с иммобилизованным антителом, а после многочисленных продолжительных процедур промывания с целью удаления несвязанных/мешающих компонентов конъюгат антитела (антитело-фермент или радиоактивно меченое антитело) добавляется в комплекс антиген-антитело для определения связанного антигена. В случае, когда используются антитело-ферментные конъюгаты, необходимо всегда добавлять дополнительный реагент, субстрат, вследствие чего связанный фермент определяется путем появления окрашенного продукта. Использование методик как ферментного, так и радиационного иммуноанализа, требует дорогостоящего и сложного оборудования, чтобы дать возможность исследователю или работнику лаборатории интерпретировать значение экспериментальных данных. При использовании быстрого анализа для иммуноопределения GST по данному изобретению конечный результат просто определяется присутствием или отсутствием цвета (банда) и легко интерпретируется любым лицом, не являющимся специалистом.
Второе важное отличие способа по данному изобретению от известных способов уже было указано выше и заключается в отсутствии потребности в амплификации сигнала для облегчения иммунообнаружения GST в случае настоящего анализа. Фактически, чувствительность определения, необходимая для быстрого определения GST по данному изобретению, присуща данному анализу. Не требуется никаких посторонних реагентов амплификации помимо меченого частицами антитела и иммобилизованного антитела. Во всех других методиках для иммуноопределения GST используется способ амплификации сигнала, включающий ферментное образование окрашенного продукта (EIA), флуоресцентное усиление с использованием меченых Eu3+ антител (TR-IFMA) и распространенную амплификацию сигнала, связанную с эмиссией частиц из атомного ядра (т.е. радиоактивное определение) (RIA).
Краткое описание чертежей
На фиг. 1 схематически представлено проведение быстрого анализа по данному изобретению с использованием меченого золотом lgG против αGST и связанного мембраной lgG против αGST, в соответствии с примерами 2 и 3; и
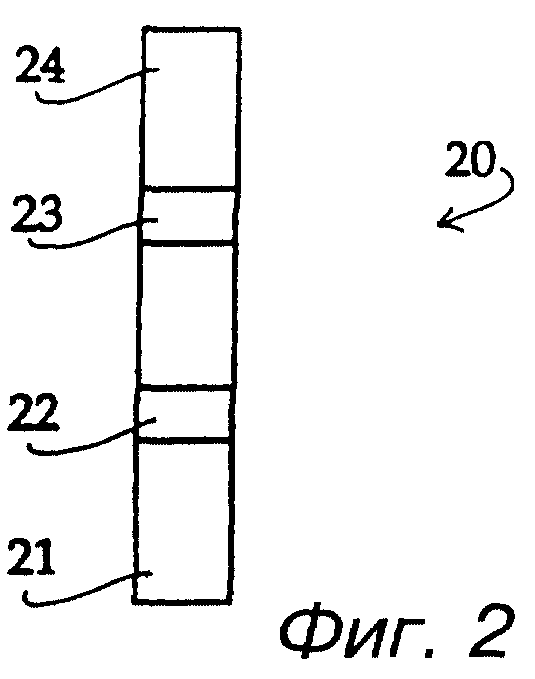
На фиг. 2 схематически представлено проведение быстрого анализа по данному изобретению с использованием меченого золотом lgG против αGST и связанного мембраной lgG против αGST, в соответствии с примером 4.
Способы осуществления изобретения
Далее изобретение будет проиллюстрировано со ссылкой на следующие примеры.
Пример 1
Очистка αGST и образование антисывороток с использованием очищенной αGST
Очистка αGST
Печень человека была получена при аутопсии. Гомогенизация печени была осуществлена путем добавления 113,2 г печени в буфер гомогенизации при pH 7.2, имеющий следующий состав:
10 mM фосфата натрия
250 mM сахарозы
1 mM EDTA,
с последующей дезинтеграцией клеток в течение 2 минут при 4oC в гомогенизаторе Уоринга (Уоринг является товарным знаком). Полученный гомогенат был центрифугирован при 11 500 g в течение 10 минут, после чего супернатант был удален и снова центрифугирован при 48 000 g в течение 45 минут. Окончательный супернатант (380 мл) был подвергнут экстенсивному диалиэу на 20 mM Tris-HCI при pH 7.8 и 4oC. После завершения диализа диализат был нанесен на колонку с иммобилизованной 3-гексил-GSH-сефарозой. α-GST специфично связывался с этой колонкой и был элюирован с использованием 0,3 mM S-гексил-CSH.
Затем проверка контроля качества проводилась следующим образом:
1. Очищенная таким образом αGST была проверена посредством SDS-PAGE и оказалась чистой.
2. Очищенная: αGST взаимодействовала с антисывороткой против αGST, но не с антисывороткой против анти-πGST или анти-μGST.
3. Изоэлектрическое фокусирование показало два бэнда при pl (изоэлектрические точки) 8.5 и 7.8. Очищенный B1B1 ( αGST) давал один бэнд при pl 8.5, Соответственно, очевидно, что бэнд с pl 7.8 может быть B2, содержащий димер αGST.
Подготовка антисыворотки αGST человека
Подготовка антисыворотки αGST человека производилась следующим образом через определенный период времени при использовании кроликов (внутренний I. D.: Syncor G и Н) и по следующей схеме.
День 1-й:
Произвели опытное кровотечение в объеме 5 мл пресыворотки из уха кролика, затем смешали 0,5 мл антигена αGST человека (100 μg) с таким же объемом полного адъюванта Фрейнда. Гомогенизировали антиген и адъювант для получения хорошей эмульсии. Затем эту смесь подкожно вводили в многочисленные участки на спине кролика, которая предварительно была выбрита.
День 28-й
Произвели опытное кровотечение в объеме 5 мл пресыворотки из уха кролика, затем смешали 0,5 мл антигена αGST человека (100 μg) с таким же количеством полного адъюванта Фрейнда. Гомогенизировали антиген и адъювант для получения хорошей эмульсии. Затем эту смесь подкожно вводили в многочисленные участки на спине кролика.
День 42-й
Произвели опытное кровотечение и взяли 10 мл крови из уха кролика.
День 56-й
Вторая вакцинация была сделана кролику, как это описано для Дня 28-го.
День 70-й
Произвели опытное кровотечение и взяли 10 мл крови из уха кролика. Когда титр был достаточно высоким, кролика умертвили и собрали максимальное количество крови.
Очистка антитела:
10 мл антисыворотки (кролика) поместили в 10 мл колонку с протеин А-сефарозой, предварительно уравновешенной в забуфренном фосфатом физиологическом растворе (PBS). Весь lgG кролика связывался с Протеином А и элюировался с использованием 0,1 М глицина при pH 3.0. Чистота устанавливалась посредством SDS-PAGE, а функциональность (активность против GST) - посредством сенсибилизации титрационного микропланшета, анализов дот-блота и вестерн-блота и непосредственной конъюгации с пероксидазой хрена (HRP).
В случае сенсибилизации титрационного микропланшета концентрация используемой анти-αGST составляет 1 μg/ml в 0,1 М в буфере карбоната натрия при pH 9.6.
Было обнаружено, что концентрация конъюгата lgG-HRP против αGST для использования в ферментном иммуноанализе на определение αGST, имеющем диапазон определения 0 - 50 нг/мл, составляла 77 нг/мл. Это указывает на высокую чувствительность антитела, так как обычно концентрация, требующаяся для таких ферментных иммуноанализов (например, EIA, маркированный товарным знаком Mukit компании Biotrin International Limited, Mount Merrion, County Dublin, Ireland, и EIAs других компаний), была бы более 700 - 7000 нг/мл для других конъюгатов lgG-HRP кролика.
Пример 2
Анализ на αGST на основе частиц
1. lgG против αGST (0,5 мг/мл в PBS) был напылен в виде линии на полосках (3 мм х 8 см) микроцеллюлозной мембраны. При подготовке мембраны не имел место этап блокирования. Однако включение такой процедуры может способствовать стабильности полосок и уменьшению неспецифического связывания.
2. Антитела против αGST были мечены золотыми частицами (диаметром 15 и 40 нм), поставленными контрактным производителем вместе с антителом, и хранились в 0,1% (w/v)
азиде натрия в 2 mM тетрабората натрия при pH 7.2 в качестве разбавителя.
Процедура анализа
1. Содержащие αGST образцы были смешаны с данным объемом меченого золотом lgG против αGST с использованием следующего разбавителя:
1% (w/v) альбумин коровьей сыворотки
1% (w/v) TWEEN-20
в PBS, pH 7.2
и были испытаны, как будет описано ниже.
2. Микроцеллюлозная мембрана, предварительно покрытая lgG против αGST (1 - 3 мм шириной), была погружена в смесь и оставлена там на период до 3 - 5 минут.
Процедура испытания
Процедура быстрого анализа осуществлялась на следующих образцах (Образцы NN 1-5):
Образец N 1. αGST при 25 μg/ml (25 мг/л).
Образец N 2. Три разбавленных образца мочи при известных концентрациях αGST: а) 6,01, b) 18,34 и с) 1,03 нг/мл, соответственно - перед разбавлением 1/5).
Образец N 3. Только разбавитель.
Образец N 4. πGST.
Образец 5. αGST при 50 нг/мл (50 μg/L).
Результаты
Образец N 1. Сигнал был получен для раствора 25 μg/ml, что показывает, что даже при уровнях 1000x больше, чем нормальные уровни мочевой αGST, не наблюдалось никакого "хук-эффекта" (ложного положительного эффекта).
Образец N 2a-2c. αGST, присутствующая во всех трех образцах мочи (разбавленных 1/5 в буфере разбавления), была определена, и интенсивность сигнала была пропорциональна первоначальной концентрации αGST, как это было отмечено тремя независимыми наблюдателями.
Образец N 3. Не наблюдалось никакого сигнала, когда только разбавитель испытывался в ходе быстрого анализа.
Образец N 4. Не наблюдалось никакого сигнала.
Образец N 5. Этот раствор давал ясно определяемый сигнал в ходе анализа.
Пример 3
Анализ на αGST на основе частиц
1. lgG против αGST (мышиный моноклональный; 1 мг/мл в PBS) был иммобилизован на полосках нитроцеллюлозной мембраны (0,5 х 4 см).
2. Полоски были блокированы инкубацией в течение 30 минут при комнатной температуре в растворе 2% (w/v) обезжиренного молока и 2% (w/v) поливинилпирролидона в Tris-забуфренном физиологическом растворе, pH 7.4, содержащем 0,5% (w/v) Tween 20.
3. Полоски были промыты дистиллированной водой и высушены в течение одного часа при комнатной температуре.
4. Антитела против αGST были мечены золотыми частицами (диаметром 40 нм), поставляемыми контрактным производителем
вместе с антителом, и хранились в 0,1% (w/v) азиде натрия в 2 mM тетрабората натрия при pH 7.2 в качестве разбавителя.
Процедура анализа
1. Содержащие αGST образцы смешали с данным объемом меченого золотом lgG против αGST с использованием Tris-забуфренного физиологического раствора, pH 7.4, содержащего 0,5% (w/v) Tween 20 в качестве разбавителя.
2. Полоска нитроцеллюлозной мембраны, предварительно покрытая lgG против αGST, была погружена в смесь и оставлена там на период до 5 минут.
Процедура испытания
Процедура быстрого анализа осуществлялась на следующих образцах:
Образец N 1: αGST при 250 нг/мг.
Образец N 2: Только разбавитель.
Результаты:
Образец N 1: Ясно определяемый сигнал был получен в ходе анализа.
Образец N 2: Никакого сигнала не было получено, когда в ходе анализа испытывался только разбавитель.
Принцип методики и интерпретация результатов для примеров 2 и 3
Меченый золотом lgG против αGST мигрирует вверх по мембране. Если αGST присутствует в смеси, то комплекс, состоящий из меченого золотом lgG и αGST, связывается с иммобилизованным lgG против αGST на мембране с образованием розово-красной линии (осадок). Если αGST не присутствует в смеси, то меченый золотом lgG против αGST хроматографирует к верху мембраны, и никакой линии (осадка) не наблюдается.
Эта методика может быть также проиллюстрирована со ссылкой на фиг. 1. На фиг. 1 полоска нитроцеллюлозной мембраны показана в общем виде позицией 10, и она показана погружающейся в образец биологической жидкости в резервуаре 11, содержащем меченый золотом lgG против αGST. Бэнд (1-3 мм) иммомилизованного lgG против αGST показан пунктирной линией поз. 12. Направление потока образца на нитроцеллюлозной мембране 10 показано стрелкой. Меченый золотом lgG против αGST связывает αGST, если она присутствует, мигрирует вверх по мембране и захватывается иммобилизованным lgG в области 12. Нитроцеллюлозная мембрана 10 остается в контакте с образцом в течение 3 - 5 минут и затем удаляется, как это отображено полосками А и В. Если αGST присутствует (положительный результат), наблюдается розово-красная линия (линия осаждения), как показано на полоске А. Если αGST отсутствует (отрицательный результат), никакой розово-красной линии не образуется в области 12, как показано на полоске В. Расположение, представленное на фиг. 1, является чисто иллюстративным, и в промышленном варианте меченый золотом анти- αGST будет находиться (в качестве мобильной фазы) на нитроцеллюлозной мембране у погруженного в образец конца 13.
Конкретные преимущества этого быстрого анализа будут очевидны, поскольку вся процедура состоит только из одного этапа. Однако он будет представлять большую ценность, если будет являться существенным усовершенствованием обычных иммуноанализов на основе титрационных микропланшетов.
Пример 4
Анализ на αGST на основе частиц
1. lgG против αGST (мышиный моноклональный; 1 мг/мл в PBS) был иммобилизован на полосках (0,5 х 4 см) нитроцеллюлозной мембраны в области, расположенной на расстоянии примерно 1 см от верха полоски.
2. Полоски были блокированы инкубацией в течение 30 минут при комнатной температуре в растворе 2% (w/v) обезжиренного молока и 2% (w/v) поливинилпирролидона в Tris-забуфренном физиологическом растворе, pH 7.4, содержащем 0,5% (w/v) Tween 20.
3. Полоски были промыты дистиллированной водой и высушены при комнатной температуре.
4. Антитела против αGST были мечены золотыми частицами (диаметром 40 нм), поставляемыми контрактным производителем с антителом, и хранились в 0,1% (w/v) азиде натрия в 2 mM тетрабората натрия при pH 7.2 в качестве разбавителя.
5. Меченые золотом антитела против αGST наносились на полоски нитроцеллюлозной мембраны в области, расположенной на расстоянии приблизительно 3 см от верха полоски. Перед нанесением меченых золотом антител подслой из 30% (w/v) сахарозы в дистиллированной воде был нанесен на эту область полоски.
Процедура анализа:
1. Содержащие αGST образцы наносились на полоски нитроцеллюлозной мембраны.
Процедура испытания
Процедура быстрого анализа проводилась на следующих образцах:
Образец N 1: αGST при 250 нг/мл, с использованием Tris-забуфренного физиологического раствора, pH 7.4, содержащего 0,5% (w/v) Tween 20 в качестве разбавителя.
Образец N 2: αGST при 25 нг/мл, с использованием Tris-забуфренного физиологического раствора, pH 7.4, содержащего 0,5% (w/v) Tween 20 в качестве разбавителя.
Образец N 3: Только разбавитель.
Образец N 4: Два образца разбавленного перфузата с известными концентрациями αGST (а) 6716 и (b) 29295 нг/мл, перед разбавлением 1/20.
Образец N 5: Три образца разбавленной сыворотки с известными концентрациями αGST (а) 26,62; (b) 119,34 и (с) 251,86 нг/мл, перед разбавлением 1/20.
Образец N 6: Три образца разбавленной желчи с известными концентрациями (а) 7,26; (b) 31,93 и (с) 68,12 нг/мл, перед разбавлением 1/20.
Образец N 7: Образец разбавленной мочи с известной концентрацией 88,07 нг/мл перед разбавлением 1/20.
Результаты
Образец N 1: Ясно различимый сигнал был получен в ходе анализа.
Образец N 2: Ясно различимый сигнал был получен в ходе анализа.
Образец N 3: Никакого сигнала не было получено, когда только разбавитель испытывался в ходе анализа.
Образец N 4: Было определено присутствие αGST в обоих образцах перфузата.
Образец N 5: Никакого сигнала не было получено при испытании образца сыворотки, содержащего 26,62 нг/мл αGST (перед разбавлением 1/20). Это указывает на то, что анализ не определяет αGST при уровнях, соответствующих нормальным уровням сыворотки. Было определено присутствие αGST в образцах, содержащих 119,34 и 251,86 нг/мл αGST (перед разбавлением 1/20).
Образец N 6: Никакого сигнала не было получено, когда испытывались образцы желчи, содержащие 7,26 и 31,93 нг/мл αGST (перед разбавлением 1/20). Это указывает на то, что анализ не определяет αGST при этих уровнях. Была определена αGST, присутствующая в образце, содержащем 68,12 нг/мл αGST (перед разбавлением 1/20).
Образец N 7: Было определено присутствие αGST в образце мочи.
Принцип методики и интерпретации результатов для примера 4
Так как испытываемый образец мигрирует вдоль полоски нитроцеллюлозной мембраны, он смешивается с мечеными золотом антителами против αGST на полоске. Если αGST присутствует в образце, меченые антитела против αGST связываются с αGST, образуя комплекс антитело-антиген. Этот комплекс мигрирует вдоль полоски и связывается с lgG против αGST, иммобилизованным на полоске с образованием розово-красной линии. Если αGST отсутствует в образце, меченые антитела против αGST мигрируют в верхнюю часть полоски, и никакой линии не наблюдается.
Эта методика также проиллюстрирована на фиг. 2. Полоска нитроцеллюлозной мембраны показана в общем виде позицией 20; около ее конца 21 находится область 22, несущая меченые золотом антитела против αGST. Выше на полоске 20 находится область 23 с иммобилизованным lgG против αGST в виде бэнда. Образец наносится на конец 21 и мигрирует вдоль полоски к концу 24. В это время образец смешивается с мечеными золотом антителами против αGST в области 22 и с αGST, если она присутствует в образце, связывается с мечеными золотом антителами, образуя комплекс атитело-антиген. Этот комплекс связывается с lgG против αGST, иммобилизованным в области 23, и образует розово-красную линию. Если αGST отсутствует в образце, никакой розово-красной линии в области 23 не образуется.
Пример 5
Анализ на πGST на основе частиц
1. lgG против πGST (мышиный моноклональный; 0,6 мг/мл в PBS) был пятнами нанесен на полоски нитроцеллюлозной мембраны
(1 μl/точка ≡ 0,6 μg). При подготовке мембраны отсутствовал этап блокирования, однако, включение такой процедуры может способствовать стабильности полоски и уменьшить неспецифичное связывание.
2. Антитела против πGST (кроличьи поликлональные) были мечены золотыми частицами (диаметром 40 нм), поставляемыми контрактным производителем вместе с антителом, и хранились в
0,1% (w/v) азиде натрия в 2 mM тетрабората натрия при pH 7.2 в качестве разбавителя.
Процедура анализа
1. Содержащие πGST образцы (10 μl каждый @ 1 - 500 μg/ml) были смешаны с данным объемом (50 μl) меченого золотом lgG против πGST и 140 μl следующего разбавителя:
1% (w/v) альбумин коровьей сыворотки
1% (w/v) TWEEN 20
в PBS, pH 7.2
и были испытаны, как это описано ниже.
2. Нитроцеллюлозная мембрана, предварительно покрытая lgG против πGST (0.6 μg/точка), была погружена в смесь и оставлена там на период до 3 - 15 минут.
Процедура испытания
Процедура быстрого анализа проводилась на следующих образцах:
Образцы NN 1 - 4: содержащие только πGST в буфере;
Образец N 5: содержащий только буфер; и
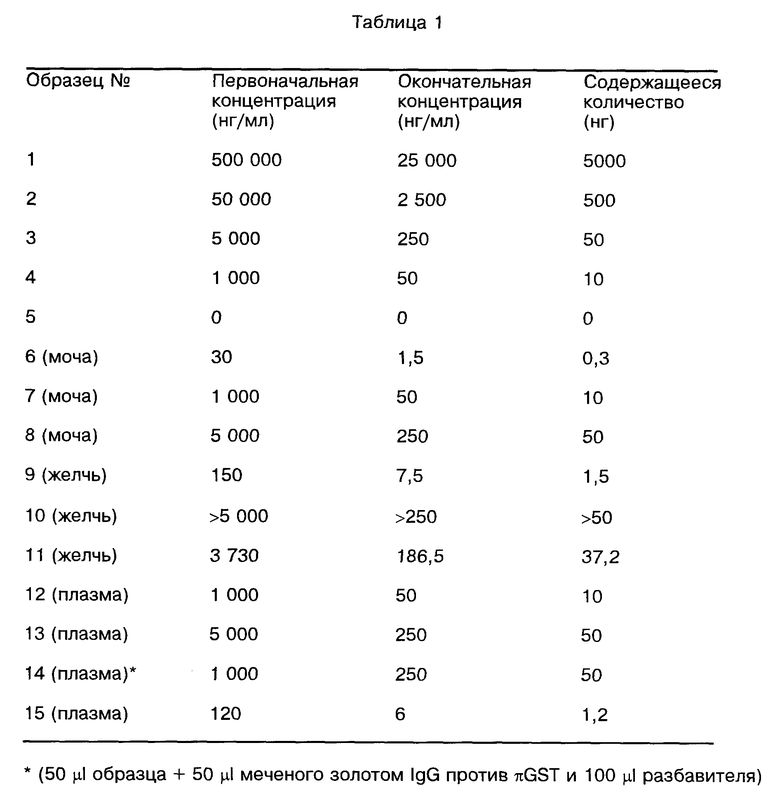
Образцы NN 6 - 15: моча, желчь и плазма, содержащие πGST, как представлено в табл. 1.
В образцах NN 7 и 8 (моча) и 12 и 13 (плазма) распространился потенциал действия очищенной πGST. Однако образцы желчи содержали неактивную πGST.
Результаты
Результаты приведены в табл. 2.
Из приведенных результатов видно, что πGST определяется в образцах мочи, желчи и плазмы. Чувствительность анализа составляет около 50 нг/мг, но, вероятно, оптимизация анализа могла бы повысить этот уровень чувствительности. Однако этот уровень πGST уже наблюдался в биологических образцах (например, в желчной и тканевой перфузионных средах).
Было обнаружено, что для определения πGST этим анализом необходим моноклонально-поликлональный иммуносэндвич. Однако возможно, что если поликлональное антитело достаточной чувствительности было идентифицировано, то этот lgG будет функционировать в ходе анализа (как в случае вышеописанного быстрого анализа на αGST). В альтернативном варианте анализ моноклонально-моноклонального типа может также обеспечить достаточную чувствительность.
Пример 6
Анализ на πGST на основе частиц
1. lgG против πGST (машиный моноклональный; 0,6 мг/мл в PBS) был иммобилизован на полосках нитроцеллюлозной мембраны (0,5 х 4 см).
2. Полоски были блокированы инкубированием в течение 30 минут при комнатной температуре в растворе 2% (w/v) обезжиренного молока и 2% (w/v) поливинилпирролидона в Tris-забуфренном физиологическом растворе, pH 7.4, содержащем 0,5% (w/v) Tween 20.
3. Полоски были промыты в дистиллированной воде и высушены в течение 1 часа при комнатной температуре.
4. Антитела против πGST были мечены золотыми частицами (диаметром 40 нм), поставляемыми контрактным производителем вместе с антителом, и хранились в 0,1% (w/v) азиде натрия в 2 mM тетрабората натрия при pH 7.2 в качестве разбавителя.
Процедура анализа:
1. Содержащие, πGST образцы смешивались с данным объемом меченого золотом lgG против πGST с использованием Tris-забуфренного физиологического раствора, pH 7.4, содержащего
0,5% (w/v) Tween 20 в качестве разбавителя.
2. Полоска нитроцеллюлозной мембраны, предварительно покрытая lgG против π GST, была погружена в смесь и оставлена там на период до 30 минут.
Процедура испытания:
Процедура быстрого анализа проводилась на следующих образцах:
Образец N 1: πGST при 250 нг/мг
Образец N 2: Только разбавитель
Результаты:
Образец N 1: Ясно определяемый сигнал был получен в ходе анализа.
Образец N 2: Не было получено никакого сигнала, когда в ходе анализа испытывался только разбавитель.
Принцип и методика интерпретации результатов для примеров 5 и 6
Меченый золотом lgG против πGST мигрирует вверх по мембране. Если πGST присутствует в смеси, то комплекс, состоящий из меченого золотом lgG и πGST, связывается с иммобилизованным моноклональным lgG против πGST на мембране с образованием розово-красной линии (осаждение). Если πGST отсутствует в смеси, то меченый золотом lgG против πGST хроматографирует к верху мембраны и никакой линии (осаждение) не наблюдается.
Очень важно, что этот анализ также представляет собой значительный шаг вперед по сравнению с обычными анализами на основе титрационных микропланшетов (или мембран), так как вся процедура состоит из единственного этапа.
Пример 7
Анализ на πGST на основе частиц
1. lgG против πGST (мышиный моноклональный; 0,6 мг/мл в PBS) был иммобилизован на полосках нитроцеллюлозной мембраны (0,5 х 4 см) в области, расположенной на расстоянии примерно 1 см от верхнего конца полоски.
2. Полоски были блокированы инкубацией в течение 30 минут при комнатной температуре в растворе 2% (w/v) обезжиренного молока и 2% (w/v) поливинилпирролидона в Tris-забуфренном физиологическом растворе, pH 7.4, содержащем 0,5% (w/v) Tween 20.
3. Полоски были промыты в дистиллированной воде и высушены в течение одного часа при комнатной температуре.
4. Антитела против π0[GST были мечены золотыми частицами (диаметром 40 нм), поставляемыми контрактным производителем с антителами, и хранились в 0,1% (w/v) азиде натрия в 2 mM тетрабората натрия при pH 7.2 в качестве разбавителя.
5. Меченые золотом антитела против πGST были нанесены на полоски нитроцеллюлозной мембраны на участок, расположенный на расстоянии примерно 3 см от верха полоски. Перед нанесением меченых золотом антител подслой из 30% (w/v) сахарозы в дистиллированной воде был нанесен на этот участок полоски.
Процедура анализа:
1. Содержащие πGST образцы были нанесены на полоски нитроцеллюлозной мембраны.
Процедура испытания
Процедура быстрого анализа осуществлялась на следующих образцах:
Образец N 1: πGST при 250 нг/мл с использованием Tris-забуфренного физиологического раствора, pH 7.4, содержащего 0,5% (w/v) Tween 20 в качестве разбавителя.
Образец N 2: πGST при 25 нг/мл с использованием Tris-забуференного физиологического раствора, pH 7.4, содержащего 0,5% (w/v) Tween 20 в качестве разбавителя.
Образец N 3: Только разбавитель.
Результаты:
Образцы NN 1 и 2: Ясно определяемый сигнал был получен в ходе анализа для обоих образцов, и интенсивность сигнала была пропорциональна концентрации πGST.
Образец N 3: Никакого сигнала не было получено, когда в ходе анализа испытывался только один разбавитель.
Принципы методики и интерпретации результатов для примера 7
Так как образец испытания мигрирует вдоль полоски нитроцеллюлозной мембраны, он смешивается с мечеными золотом антителами против πGST на полоске. Если πGST присутствует в образце, меченые антитела против πGST образуют комплекс антитело-антиген. Этот комплекс связывается с lgG против πGST, иммобилизованным на полоске, и образует розово-красную линию. Если πGST отсутствует в образце, меченые антитела против πGST мигрируют к верхней части полоски, и никакой линии не наблюдается. Таким образом, эта методика соответствует той, что была изложена в связи с примером 4 и проиллюстрирована на фиг.2.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ СОСТОЯНИЯ ПЕЧЕНИ | 1996 |
|
RU2164027C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ИЛИ ОБНАРУЖЕНИЯ ПОВРЕЖДЕНИЯ ОРГАНА-ДОНОРА ПОСЛЕ КСЕНОТРАНСПЛАНТАЦИИ НА ОСНОВЕ АНАЛИЗА ВЕЩЕСТВ, ПОЛУЧЕННЫХ ИЗ ОРГАНА-ДОНОРА | 1995 |
|
RU2157540C2 |
| СТАБИЛИЗИРУЮЩАЯ СРЕДА ДЛЯ α-GST В МОЧЕ И СПОСОБ ОПРЕДЕЛЕНИЯ КОЛИЧЕСТВА α-GST В МОЧЕ | 1994 |
|
RU2142136C1 |
| АНАЛИЗ ИММУНОДЕТЕКЦИИ КОМПЛЕКСА MYCOBACTERIUM TUBERCULOSIS | 2008 |
|
RU2473095C2 |
| ТЕСТ-СИСТЕМА ДЛЯ ПОЛУКОЛИЧЕСТВЕННОГО ИММУНОХРОМАТОГРАФИЧЕСКОГО АНАЛИЗА | 2012 |
|
RU2510510C1 |
| СПОСОБ ВЫСОКОЧУВСТВИТЕЛЬНОГО ИММУНОХРОМАТОГРАФИЧЕСКОГО АНАЛИЗА С ДВОЙНОЙ КОНКУРЕНЦИЕЙ | 2020 |
|
RU2748901C1 |
| Тест-система для визуального полуколичественного иммунохроматографического анализа | 2018 |
|
RU2707526C1 |
| СПОСОБ СНИЖЕНИЯ ПРЕДЕЛА ОБНАРУЖЕНИЯ ИММУНОХРОМАТОГРАФИЧЕСКИХ МЕТОДОВ КОНТРОЛЯ СОДЕРЖАНИЯ НИЗКОМОЛЕКУЛЯРНЫХ СОЕДИНЕНИЙ | 2011 |
|
RU2497126C2 |
| ИММУНОДИАГНОСТИКУМ И СПОСОБ ТВЕРДОФАЗНОГО ИММУНОАНАЛИЗА НА ЕГО ОСНОВЕ | 1992 |
|
RU2092853C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ РАСТИТЕЛЬНЫХ ВИРУСОВ | 1994 |
|
RU2083986C1 |

Изобретение относится к медицине, а именно к быстрому анализу для выявления и/или определения глутатионовых S-трансфераз (GSTs) для использования при оценке состояния органа. Сущность способа оценки состояния органа по определению изоферментов глутатионовой S-трансферазы в различных биологических жидкостях включает в себя контактирование меченого частицами комплекса антитело-изофермент на иммобилизованном антителе для получения визуально определяемого сигнала. Преимущество способа заключается в разработке быстрого и простого способа определения указанных ферментов в различных биологических жидкостях. 2 с. и 10 з.п. ф-лы, 2 ил., 2 табл.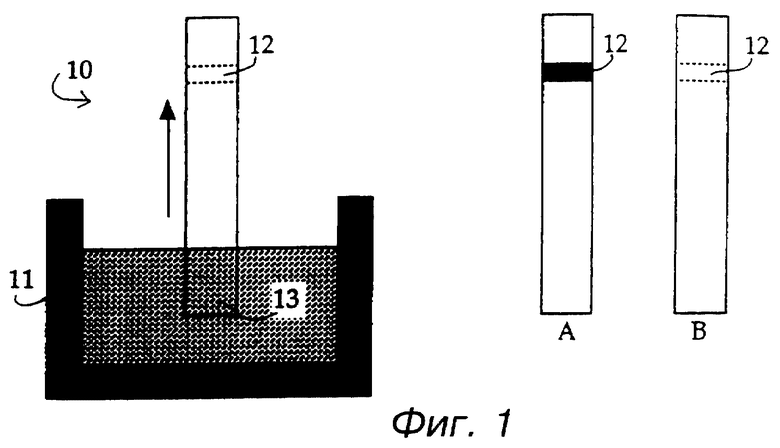
| СПОСОБ СТЕРЕОСПЕЦИФИЧЕСКОГО АНАЛИЗА И СПОСОБ ПОЛУЧЕНИЯ КОНЪЮГАТА ДЛЯ СТЕРЕОСПЕЦИФИЧЕСКОГО АНАЛИЗА | 1993 |
|
RU2089912C1 |
| CHARD T | |||
| An Introduction to radioimmunoassay and related technigues Elsevier/North-Holland Biomedical Press, 1978 | |||
| BECKETT D.J., HAYES J.D | |||
| Glutathione Stransferases: biomedical applications, Advances in linical chemistry, 1993 v | |||
| Способ обработки медных солей нафтеновых кислот | 1923 |
|
SU30A1 |
Авторы
Даты
2000-08-20—Публикация
1996-04-02—Подача