Изобретение относится к медицине, преимущественно к брюшной хирургии, и может быть использовано для лечения больных с повреждениями и заболеваниями гепатикохоледоха.
Необходимость пластики гепатикохоледоха возникает при ятрогенных его повреждениях, травматических ранениях, стриктурах, а также после удаления опухолей и при пролежнях его стенки, вызванных желчными камнями.
Для пластики чаще всего применяют ткани самого гепатикохоледоха. Для этого после удаления опухоли или иссечения стриктуры выполняют мобилизацию обоих концов оставшейся части гепатикохоледоха, а затем сшивают его концы на дренажной трубке, введенной в просвет гепатикохоледоха. В случаях дефекта только передней стенки гепатикохоледоха возможна пластика его путем сшивания в поперечном направлении, а при рубцовой стриктуре - вначале продольное ее рассечение, а затем сшивание гепатикохоледоха в поперечном направлении /по Гейнеке-Микуличу/. Однако такое сшивание концов гепатикохоледоха возможно только при дефектах его стенки, равных 1,5-2,0 см. Если рубцовая стриктура или поврежденная часть гепатикохоледоха более 2,0 - 3,0 см, то необходимо применять другие способы его пластики /Э. И. Гальперин, Ю. М. Дедерер "Нестандартные ситуации при операциях на печени и желчных путях" - М.: Медицина. - 1987. - С. 158-163/.
Для пластики больших дефектов и рубцовых стриктур гепатикохоледоха применяют 3 основных способа пластики: a - сегментом тонкой кишки; б - аутовеной; в - тефлоновым протезом /Э.И. Гальперин, Ю.М. Дедерер, там же, с. 161/.
Пластика гепатикохоледоха сегментом тонкой кишки предполагает выкраивание /выключение из пищеварения/ петли тонкой кишки по Ру, длиной до 1 м, с последующим наложением анастомоза с проксимальной частью гепатикохоледоха. Для предупреждения рубцового сужения вновь созданного анастомоза его формирование /наложение/ осуществляют на сменном транспеченочном дренаже, так называемом СТД, или дренажную трубку выводят на переднюю брюшную стенку по Фелькеру через выключенную по Ру петлю тонкой кишки /Э.И. Гальперин, Ю.М. Дедерер, там же, с. 167-178/. Эта трубка служит каркасом, вокруг которого происходит формирование анастомоза достаточного размера. Такую дренажную трубку извлекают из зоны анастомоза через 1,5-2,0 года.
В патентной литературе описан "Способ лечения высокой непроходимости желчных протоков" /А.С. N 1572556, МПК A 61 M 17/00, опубл. бюл. N 23 1990 г. /, в котором предусмотрено проведение дренажной трубки через разрез холедоха. Конец дренажной трубки выводят на переднюю поверхность печени. Затем отключают участок тонкой кишки. Конец дренажной трубки прошивают П-образными швами, которые проходят через ткань печени. После этого обе стенки отключенной петли кишки прошивают сквозной лигатурой-держалкой. Кнаружи от сквозного шва П-образными швами, проведенными через дренажную трубку и печень, прошивают обе стенки тонкой кишки. Эти лигатуры завязывают. Квнутри от П-образных швов иссекают над дренажной трубкой обе стенки отключенной петли тонкой кишки вместе с лигатурой-держалкой. Рассекают переднюю стенку выключенной петли тонкой кишки кнаружи от П-образных швов. Образовавшийся дефект в стенке тонкой кишки ушивают над дренажной трубкой. Свободный конец последней выводят на кожу.
Известен также "Способ восстановления общего желчного и вирсунгова протока при их случайном повреждении во время операции" /А.С. N 1558395, МПК A 61 M 17/00, опубл. бюл. N 15 1990 г./, согласно которого вводят трансдуоденально, а далее транспапиллярно полихлорвиниловую дренажную трубку. Затем выделяют переднюю стенку двенадцатиперстной кишки и пересекают ее на уровне верхнего края головки поджелудочной железы. После этого головку поджелудочной железы инвагинируют в просвет двенадцатиперстной кишки путем наложения двухрядных серозно-мышечных швов между стенкой двенадцатиперстной кишки и брюшинным покровом поджелудочной железы и гепатодуоденальной связки.
Как видно, такие реконструктивные операции весьма сложны в техническом исполнении. Требуют высокой квалификации врача-хирурга. Они весьма травматичны, сопровождаются большой летальностью /до 27%/ и низкой эффективностью результатов операции /неудовлетворительные исходы достигают 30%/ /Круглов Е. Е. "Хирургическая коррекция повреждений внепеченочных желчных протоков и их последствий" - Автореф. дис. канд. мед наук. - М. - 1996. - С. 14-15/.
В последние годы в связи с широким использованием видеоэндоскопической аппаратуры для операций на внепеченочных желчных ходах предпринимались попытки лапароскопических операций по пластике гепатикохоледоха. Однако возможности такого вида операций на гепатикохоледохе ограничены. Поэтому при стенозах желчных протоков лучше использовать открытые операции /Галлингер Ю.И. "Эндоскопическая хирургия стенозов пищевода и желчных протоков" - Российск. журн. гастроэнтерол. , гепатол. и колопроктол. - 1997. - N 3. - С. 30-34/. Кроме того, клинический опыт показал, что поскольку при эндоскопических операциях наряду с механическим разделением тканей применяется коагуляционный способ остановки кровотечения, то впоследствии в гепатодуоденальной связке развиваются грубые рубцовые изменения, весьма затрудняющие выполнение пластических операций на гепатикохоледохе.
При аутовенозной пластике резецированную часть гепатикохоледоха замещают трансплантатом из аутовены, предварительно заготовленной из большой подкожной вены бедра. При такой пластике обязательно мобилизуют двенадцатиперстную кишку по Кохеру для смещения ее кверху, уменьшая тем самым величину дефекта и сближая заднюю стенку гепатикохоледоха для наложения на нее швов. Затем в просвет гепатикохоледоха вводят сменный транспеченочный дренаж, а на переднюю стенку гепатикохоледоха накладывают и пришивают "заплату" из аутовены. Зону анастомоза дополнительно укрывают прядью сальника /Э.И. Гальперин, Ю.И. Дедерер, там же, с. 161-162/.
В качестве прототипа заявляемого изобретения взят "Способ пластики внепеченочных протоков" /патент РФ N 1812970. МПК A 61 M 17/00, опубл. бюл. N 16 1993 г./. Сущность способа, взятого в качестве протипа, состоит в том, что с целью снижения частоты постпластических осложнений путем предупреждения рубцевания просвета анастомоза и обеспечения эпителизации интимы аутотрансплантата из вены, в дистальный конец гепатикохоледоха вводят дренажную трубку и выводят ее транспапиллярно в двенадцатиперстную кишку через большой дуоденальный сосочек. На свободный конец этой трубки одевают трансплантат из аутовены, предварительно заготовленный из большой подкожной вены бедра и консервированный в среде 199. Затем сшивают ауторансплантат с дистальным концом гепатикохоледоха конец в конец. После этого свободный конец дренажной трубки вводят в проксимальную часть гепатикохоледоха и создают анастомоз конец в конец. Через 1,5 месяца дренажную трубку удаляют из гепатикохоледоха трансдуоденально. Экспериментальные исследования показали, что через 1-1,5 месяца после пластики интима аутовенозного трансплантата эпителизируется, а его стенка прорастает соединительной тканью, плотность которой больше в поверхностном слое.
Данный способ обладает следующими недостатками: 1 - нанесение больному дополнительной травмы - операции по заготовке трансплантата из большой подкожной вены бедра, что также может вызвать нарушение оттока венозной крови в системе большой подкожной вены бедра, 2 - существует потребность в создании условий для консервирования трансплантата /устройство, среда, стерильность, наблюдение, лабораторный контроль/; 3 - не исключаются рубцовые изменения трансплантата после его имплантации; 4 - сам трансплантат /бедренная вена/ тонкостенное образование, имеющее слабовыраженную мышечную оболочку, обладает слабой прочностью, эластичностью и растяжимостью. Эти недостатки устраняются в предлагаемом техническом решении.
Целью настоящего изобретения является упрощение способа пластики гепатикохоледоха, снижение травматичности операции и предупреждение рубцового сужения зоны пластики. Поставленная цель достигается тем, что у больного во время операции лапаратомии для пластики гепатикохоледоха используют участок реканализированной пупочной вены, взятой из круглой связки печени. При этом аутовенозный трансплантат на половину своей длины выворачивают интимой наружу, наслаивая на вторую его половину с тем, чтобы образовался двухстенный аутотрансплантат, свнутри и снаружи покрытый интимой.
Выбор аутотрансплантатом пупочной вены обусловлен тем, что она располагается рядом с гепатикохоледохом в круглой связке печени. После рождения человека она не функционирует. Внутриутробно по ней протекала артериальная кровь от плаценты. Поэтому стенки ее более толстые, эластичные, легко растяжимы. Кроме того, облитерация пупочной вены, наступившая после рождения человека/перевязки пуповины/, никогда не сопровождается грубым рубцеванием. Просвет ее легко восстанавливается при введении в нее зонда. Причем реканализацию пупочной вены можно повторить через 2-3 и более лет после первой, поскольку грубого рубцевания ее просвета не происходит, а строение стенки, в том числе интимы, всегда сохраняется.
Подробное описание изобретения и примеры его практической реализации
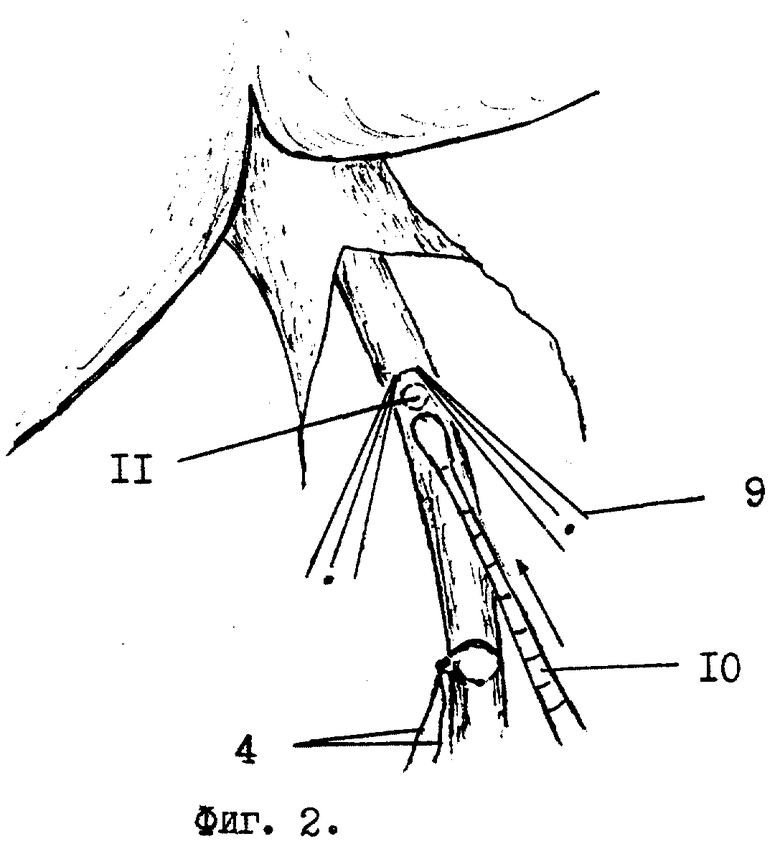
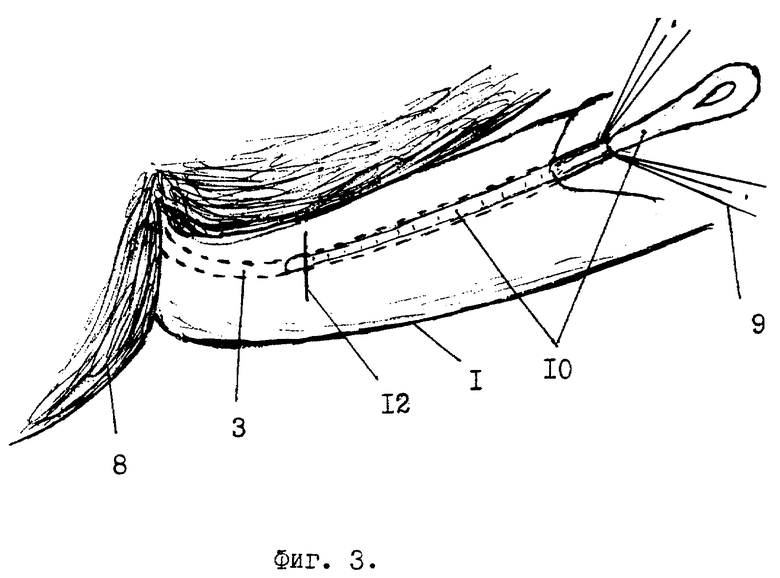
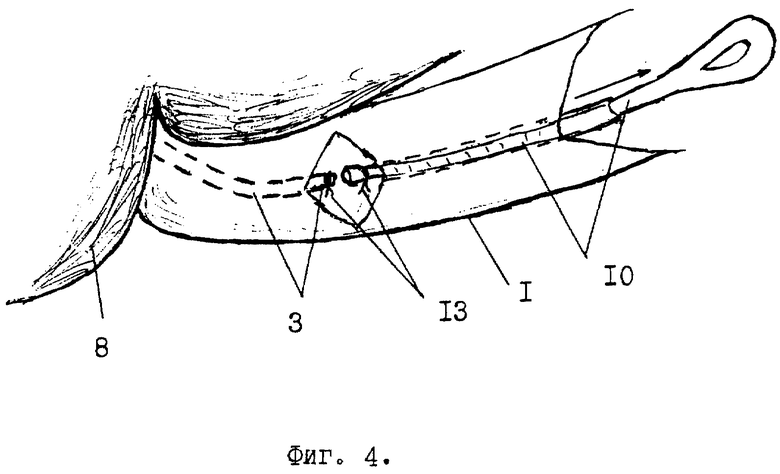
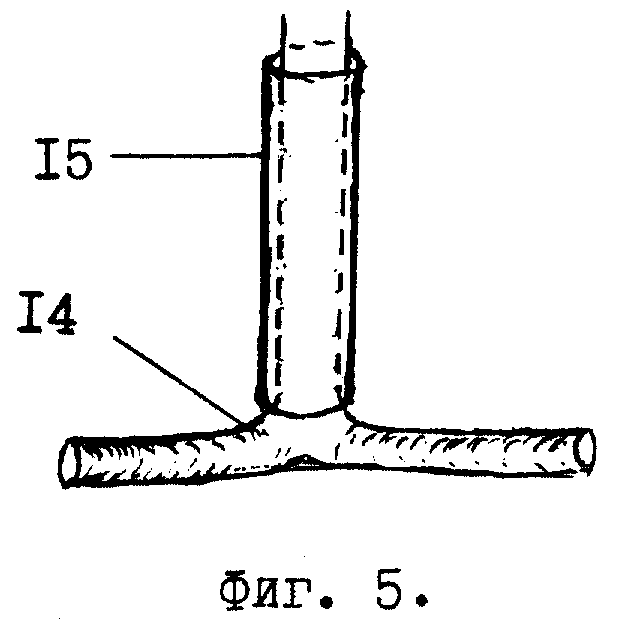
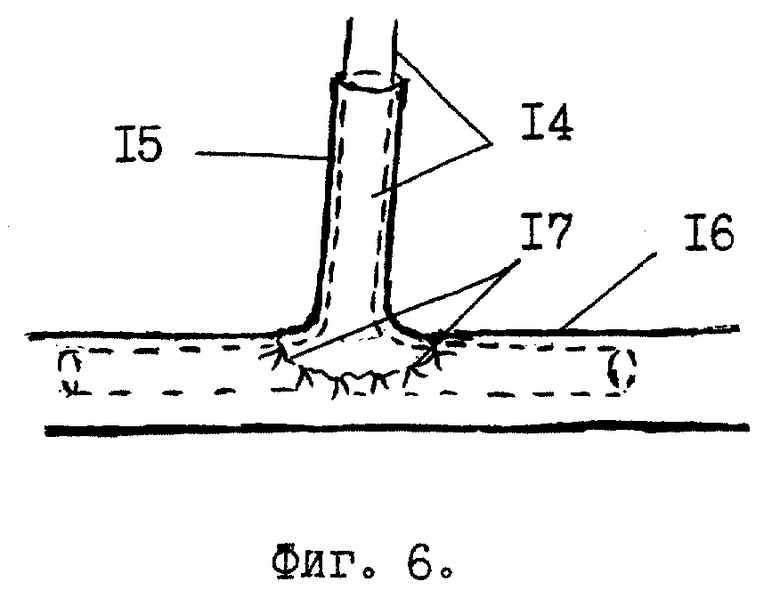
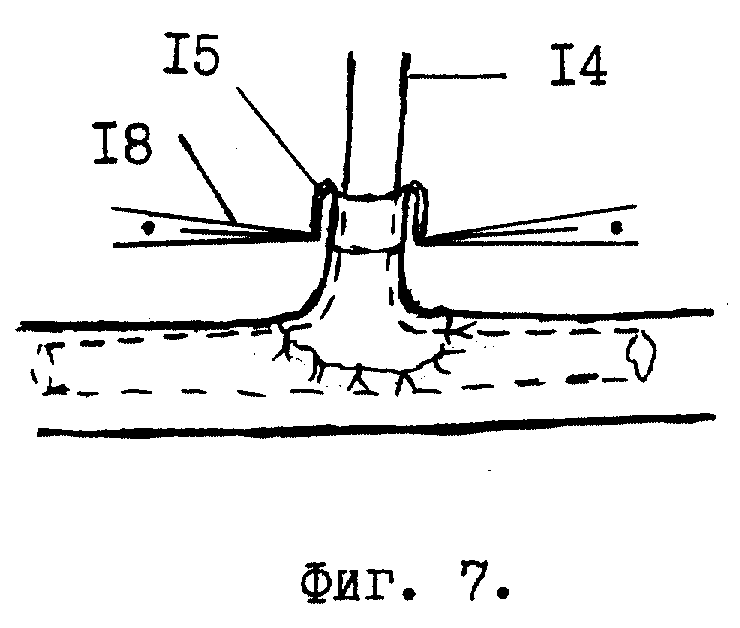
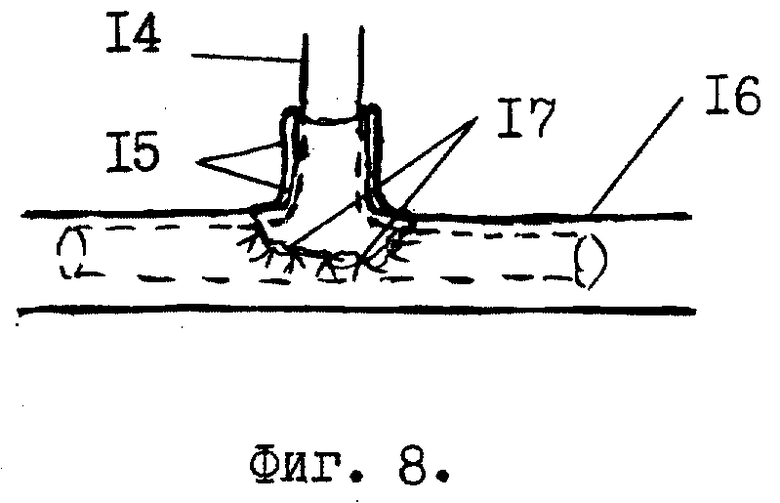
У больного во время операции лапаратомии в подпеченочном пространстве обнаруживают зону рубцового сужения или повреждения гепатикохоледоха. Иссекают зону рубцового сужения и измеряют размеры дефекта гепатикохоледоха. В рядом расположенной круглой связке /фиг.1 поз. 1/ печени /8/ ближе к передней брюшной стенке рассекают брюшину /3/ длиной 3-4 см. В жировой клетчатке круглой связки /1/ зажимом Пеана находят пупочную вену /3/ в виде тяжа диаметром 0,7-0,9 см. На дистальную ее часть накладывают лигатуру /4/. Под пупочную вену /3/ подводят указательный палец /5/ левой руки, покрытый марлевой салфеткой /6/. Скальпелем в поперечном направлении над пальцем /5/ производят надрез /7/ передней стенки пупочной вены /3/ до ее интимы. Надсеченную переднюю стенку пупочной вены /3/ захватывают двумя зажимами /фиг. 2, поз. 9/ типа "Москит" удержания и обнажения ее просвета. Удерживая пупочную вену /3/ зажимами /9/ типа "Москит" и лигатурой /4/ в обнаженной ее просвет /11/ вводят с небольшим усилием маточный зонд /10/ для ее реканализации. По делению на маточном зонде /10/ определяют длину реканализированной части пупочной вены /3/, которая должна быть в 2,5 раза больше длины дефекта гепатикохоледоха. Визуально и пальпаторно определяют конец маточного зонда /фиг. 3, поз. 10/ в пупочной вене /3/ на правой боковой поверхности круглой связки /1/ печени. В проекции кончика маточного зонда /10/ на круглой связке делают разрез /12/ брюшины длиной 1,5 см. Зажимом Пеана обнаруживают пупочную вену /фиг. 4, поз. 3/, подводят под нее 2 лигатуры /13/, одну из которых завязывают проксимальнее конца маточного зонда /10/, а другую - на маточном зонде перед булавовидным расширением его конца. Пупочную вену /3/ пересекают между наложенными лигатурами /13/ и тракцией маточного зонда /10/ к себе извлекают пупочную вену /3/ из круглой связки /1/. Дистальный конец аутотрансплантата отсекают по линии поперечного надреза /фиг. 1, поз. 7/ передней стенки пупочной вены /3/. Затем на вертикальную ветвь Т-образной дренажной трубки /фиг. 5, поз. 14/ до ее основания одевают аутотрансплантат /15/. После этого горизонтальную ветвь Т-образной дренажной трубки /фиг. 6, поз. 14/ вводят в просвет гепатикохоледоха /16/, через имеющийся в нем дефект /17/ стенки. В результате нижний конец аутотрансплантата /15/ расположится в зоне дефекта /17/. Захватив нижний край аутотрансплантата /15/ зажимом типа "Москит" и анатомическим пинцетом, его растягивают в стороны для расширения просвета и подшивают одиночными швами к краям дефекта /17/ гепатикохоледоха /16/. Затем верхний край аутотрансплантата /15/ захватывают зажимами /фиг. 7, поз. 18/ типа "Москит" и, выворачивая наизнанку, постепенно наслаивают на нижнюю его часть /для образования двухстенного аутотрансплантата/ и дополнительно фиксируют одиночными лигатурами к краям дефекта /фиг. 8, поз. 17/ гепатикохоледоха /16/. В результате снаружи и свнутри аутотрансплантат /15/ покрыт интимой /внутренней оболочкой/. Свободный конец вертикальной ветви Т-образной дренажной трубки /14/ выводят наружу через прокол передней брюшной стенки, а сам аутотрансплантат /15/ дополнительно окутывают прядью сальника для гермитизации. Т-образная дренажная трубка находится в просвете гепатикохоледоха 4 - 6 месяцев после операции. В первые 2 недели ее периодически /1-2 раза в неделю/ промывают теплым /37,0oC/ 0,25% раствором новокаина в количестве 60 - 100 мл. Затем закрывают наглухо до момента извлечения ее из гепатикохоледоха. Спустя 4 - 6 месяцев после операции Т-образную дренажную трубку извлекают из гепатикохоледоха наружу тракцией за свободную часть вертикальной ветви после контрольной холефистулографии /контрастное вещество вводят через данную дренажную трубку в гепатикохоледох/ и инъекций обезболивающего средства /кеторол/ и спазмолитиков /платифиллин/ в терапевтических дозах.
Пример. Б-ная С-н, 37 лет /и.б. N 22677/1789 / поступила в хирургическое отделение БСМП N 1 г. Ростова-на-Дону с диагнозом: постхолецистэктомический синдром, механическая желтуха. Из анамнеза выяснено, что 10 дней тому назад была оперирована лапараскопическим способом по поводу хронического калькулезного холецистита. После операции стала нарастать желтуха. В анализе крови общий билирубин 210 мкмоль/л, прямой билирубин 154 мкмоль/л. Начато обследование больной с целью выяснения причины механической желтухи. Ультразвуковое исследование печени и внепеченочных желчных ходов выявило расширение внутрипеченочных желчных протоков, общий желчный проток диаметром до 1,2 см, виализировался не на всем протяжении. При дуоденоскопии выделения желчи из большого дуоденального сосочка не отмечено. Выполнена эндоскопическая папиллотомия с ретроградной панкреатохолангиографией: панкреатический проток не изменен, гепатикохоледох обрывается в супрадуоденальной части и контрастное вещество не попадает во внутрипеченочные желчные ходы. Таким образом, диагностирована полная непроходимость супрадуоденальной части гепатикохоледоха.
В связи с таким состоянием гепатикохоледоха и нарастающей желтухой больной было предложено хирургическое лечение. Во время лапаратомии при тщательной ревизии гепатикохоледоха обнаружены 2 клипсы на супрадуоденальной его части с некротическими и рубцовыми тканями. При этом одна из клипс перфорировала гепатикохоледох, проникая в него до задней стенки. Это деформировало его просвет и создавало препятствие для оттока желчи. Вторая клипса с рубцовыми тканями вокруг нее еще более деформировала гепатикохоледох. После удаления обеих клипс, иссечения некротизированных и рубцовых тканей в гепатикохоледохе образовалось отверстие размерам 2,0 см. Через это отверстие выполнена операционная холангиография. Вначале контрастное вещество введено в проксимальном направлении - получено контрастирование верхней части гепатикохоледоха и внутрипеченочных желчных ходов. Они расширены. Затем контрастное вещество введено в дистальную часть гепатикохоледоха. Он обычного калибра, без дополнительных теней в просвете. Контрастное вещество свободно поступало в двенадцатиперстную кишку. Следующим этапом операции следовало закрыть дефект в гепатикохоледохе. Осуществить это путем сшивания его краев не представлялось возможным в связи с выраженными рубцовыми изменениями тканей в гепатодуоденальной связке после первой лапароскопической операции. Поэтому решено выполнить пластику гепатикохоледоха аутовеной, заготовленной из круглой связки печени /пупочной веной/.
Был заготовлен аутотрансплантат из пупочной вены длиной 50 мм по описанному способу. Аутотрансплантат одет на вертикальную ветвь Т-образной дренажной тройки до ее основания. Горизонтальная ветвь этой дренажной трубки введена в просвет гепатикохоледоха через его дефект. Нижний край аутотрансплантата оказался в зоне дефекта гепатикохоледоха. Он захвачен зажимом и пинцетом, растянут в стороны и подшит одиночными швами к краям дефекта гепатикохоледоха. Верхняя часть аутотрансплантата вывернута наизнанку и постепенно наслоена на нижнюю его часть так, чтобы интима его располагалась снаружи. В результате дефект гепатикохоледоха был полностью закрыт двухстенным аутотрансплантатом из пупочной вены. При этом интима данного сосуда была свнутри и снаружи аутотрансплантата. Свободная часть вертикальной ветви Т-образной дренажной трубки выведена наружу через прокол передней брюшной стенки. В подпеченочное пространство к зоне операции подведены еще 2 дренажные трубки, которые выведены наружу через отдельный прокол передней брюшной стенки. Аутотрансплантат дополнительно окутан прядью сальника. Операционная рана ушита. Послеоперационное течение гладкое. Обе дренажные трубки из подпеченочной области удалены на 4 сутки. По вертикальной ветви Т-образного дренажа оттекало 150 - 100 мл желчи в сутки, постепенно ее количество уменьшилось до 40 - 50 мл в день. Т-образную дренажную трубку промывали 1 - 2 раза в неделю теплым раствором новокаина, а спустя 2 недели после операции ее пережали. Болей в животе у больной не появилось. При холефистулографии в этот срок выявлено, что контрастное вещество поступает по Т-образной дренажной трубке в проксимальном направлении, заполняя внутрипеченочные желчные ходы и верхнюю часть гепатикохоледоха, а также в дистальном направлении, оттекая по нижней части гепатикохоледоха в двенадцатиперстную кишку. Желтуха у больной уменьшалась и совсем прошла. Через 1 месяц после операции билирубин крови составил: общий -37,0 мкмоль/л, прямой - 22 мкмоль/л. Больная выписана на амбулаторное лечение. Т-образная дренажная трубка извлечена из гепатикохоледоха через 5 месяцев после операции. Осложнений не было. Больная осмотрена через 2 месяца: чувствует себя хорошо, жалоб нет, работает по специальности, желтухи нет. Общий билирубин крови - 17 мкмоль/л.
Разработанный способ пластики гепатикохоледоха применен у 3 больных. Получен благоприятный результат. По сравнению с прототипом заявляемый способ обладает следующими преимуществами: 1 - не требует выполнения дополнительной операции по заготовке аутотрансплантата из большой подкожной вены бедра; 2 - нет необходимости создавать условия для консервирования заготовленного аутотрансплантата; 3 - аутотрансплантат из пупочной вены состоит из двух стенок, покрытых интимой свнутри и снаружи, что уменьшает возможность грубого рубцового его изменения; 4 - аутотрансплантат из пупочной вены более эластичен и растяжим, что позволяет без особых усилий расширять его просвет при подшивании к краям дефекта гепатикохоледоха.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ ГНОЙНОГО ПАНКРЕАТИТА | 1992 |
|
RU2064779C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ДЕСТРУКТИВНОГО ПАНКРЕАТИТА | 2006 |
|
RU2334474C1 |
| СПОСОБ ЛЕЧЕНИЯ ПЕЧЕНОЧНОЙ НЕДОСТАТОЧНОСТИ | 1993 |
|
RU2078595C1 |
| СПОСОБ ЛЕЧЕНИЯ ДЕСТРУКТИВНОГО ПАНКРЕАТИТА | 1998 |
|
RU2141355C1 |
| СПОСОБ ЛЕЧЕНИЯ ТРОФИЧЕСКИХ ЯЗВ ПРИ ДИАБЕТИЧЕСКОЙ СТОПЕ | 2008 |
|
RU2359624C1 |
| СПОСОБ ПРЕДУПРЕЖДЕНИЯ ПЕРИТОНИТА ПРИ НЕСОСТОЯТЕЛЬНОСТИ ШВОВ КОНЦЕВОЙ КОЛОСТОМЫ | 1999 |
|
RU2163468C2 |
| СПОСОБ ПРЕДУПРЕЖДЕНИЯ ВОЗНИКНОВЕНИЯ ОСЛОЖНЕНИЙ ПРИ ПОСЛЕОПЕРАЦИОННОМ ЛЕЧЕНИИ БОЛЬНЫХ | 2006 |
|
RU2320335C1 |
| СПОСОБ ПЛАСТИКИ ВНЕПЕЧЕНОЧНЫХ ЖЕЛЧНЫХ ПРОТОКОВ | 2000 |
|
RU2173958C1 |
| СПОСОБ УШИВАНИЯ КУЛЬТИ ДВЕНАДЦАТИПЕРСТНОЙ КИШКИ | 1999 |
|
RU2143850C1 |
| СПОСОБ ПЛАСТИКИ ДОЛЕВЫХ ПЕЧЕНОЧНЫХ ПРОТОКОВ | 2007 |
|
RU2342082C1 |
Изобретение относится к медицине, брюшной хирургии, может быть использовано для лечения больных с заболеваниями гепатикохоледоха. Используют аутотрансплантат длиной в 2,5 раза превышающей величину дефекта гепатикохоледоха. Одевают трансплантат до основания на вертикальную ветвь Т-образной дренажной трубки. Горизонтальную часть трубки вводят в просвет гепатикохоледоха через дефект в стенке. Нижнюю часть аутотрансплантата располагают в зоне дефекта. Растягивают нижнюю часть трансплантата и подшивают к краям дефекта. Верхнюю часть аутотрансплантата выворачивают наизнанку и наслаивают на нижнюю часть. Дополнительно фиксируют вывернутый край аутотрансплантата к краям дефекта. Свободную часть вертикальной ветви Т-образной трубки выводят наружу. Сохраняют Т-образную трубку в просвете 4-6 месяцев. Извлекают трубку тракцией наружной части вертикальной ветви. Способ обеспечивает снижение травматичности операции и предупреждение рубцового сужения зоны пластики. 8 ил.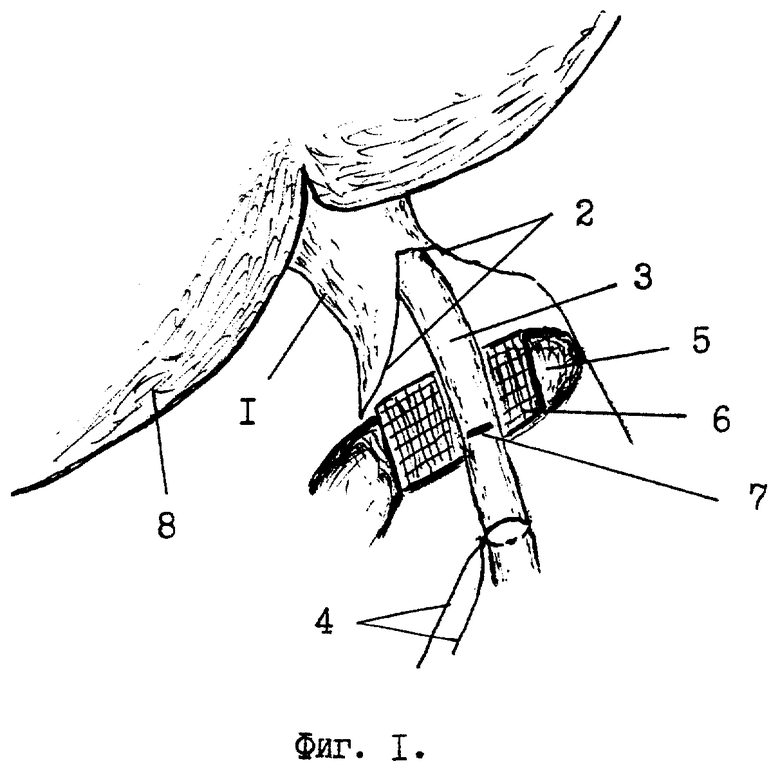
Способ пластики гепатикохоледоха, предусматривающий закрытие дефекта его стенки аутотрансплантатом из вены, отличающийся тем, что заготовку аутотрансплантата производят из реканализированной пупочной вены, длиной в 2,5 раза превышающей величину дефекта стенки гепатикохоледоха, после чего аутотрансплантат одевают до основания на вертикальную часть Т-образной дренажной трубки, а горизонтальную ее часть вводят в просвет гепатикохоледоха через дефект его стенки так, чтобы нижняя часть аутотрансплантата располагалась в зоне дефекта, растягивают нижнюю часть аутотрансплантата в стороны и подшивают к краям дефекта одиночными швами, затем верхнюю часть аутотрансплантата выворачивают наизнанку и наслаивают на его нижнюю часть с тем, чтобы аутотрансплантат оказался двухстенным и был покрыт интимой вены снутри и снаружи, дополнительно фиксируют одиночными швами вывернутый край аутотрансплантата к краям дефекта гепатикохоледоха и окутывают прядью сальника, свободную часть вертикальной ветви Т-образной дренажной трубки выводят наружу через прокол передней брюшной стенки, а саму Т-образную трубку сохраняют в просвете гепатикохоледоха 4 - 6 месяцев, после чего извлекают тракцией наружной части вертикальной ее ветви.
| Способ пластики внепеченочных желчных протоков | 1990 |
|
SU1812970A3 |
Авторы
Даты
2000-09-27—Публикация
1999-12-31—Подача