Изобретение относится к новым производным аминокислоты с биологической активностью, более конкретно к производным валинамида, способу их получения и способам получения промежуточных продуктов.
Известны производные аминокислоты, обладающие биологической активностью, в частности фунгицидной активностью (см. заявку EP N 0587110 A2, МКИ: C 07 D 307/81, A 01 N 43/38, 16.03.1994 г.).
Задачей изобретения является расширение ассортимента производных аминоксилоты, обладающих биологической активностью, в частности фунгицидной активностью.
Поставленная задача решается предлагаемыми производными валинамида общей формулы (I)
в которой R - хлор, метил, этил или метокси.
Соединения формулы (I) содержат два хиральных центра и таким образом могут находиться в виде различных смесей энантиомеров и диастереомеров, которые можно обычным образом разделять. Как индивидуальные энантиомеры и диастереомеры, так и также смеси входят в объем настоящего изобретения.
Производные валинамида вышеприведенной общей формулы (I) получают путем взаимодействия соединения формулы (II)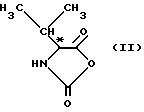
с соединением общей формулы (III):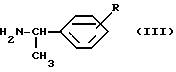
в которой R имеет вышеуказанное значение,
в среде разбавителя и возможно в присутствии вспомогательного средства.
Предпочтительны те соединения формулы (I), в которых в случае соответствующей аминокислоты речь идет о соединении с L-конфигурацией, а используемый амин формулы (III) либо является рацемическим, либо имеет R-конфигурацию или S-конфигурацию у асимметрического атома углерода.
Используемые для осуществления являющегося вторым объектом изобретения предлагаемого способа в качестве исходных веществ оксазолидиндионы формулы (II) известны. Их можно получать за счет того, что соответствующие аминокислоты обычным образом вводят во взаимодействие с фосгеном.
Амины формулы (III) представляют собой общеизвестные соединения органической химии.
В качестве разбавителей для предлагаемого способа используют инертные органические растворители, как, например, кетоны, как ацетон или метилэтилкетон; сложные эфиры, как этилацетат или метилацетат; амиды, как диметилформамид; нитрилы, как ацетонитрил; хлорированные углеводороды, как метиленхлорид или тетрахлорметан; углеводороды, как толуол; или простые эфиры, как тетрагидрофуран, а также возможно воду и их смеси.
Предлагаемый способ можно осуществлять в присутствии буфера в качестве вспомогательного средства. При этом можно использовать все обычные буферные системы, в особенности, например, боранат натрия с борной кислотой.
При осуществлении предлагаемого способа температуры можно изменять в широких пределах. В общем, работают при температурах от -100 до +150oC, предпочтительно при температурах от -60 до +100oC.
При осуществлении предлагаемого способа на моль оксазолидинона формулы (II) используют в общем от одного до десяти молей, предпочтительно от одного до пяти молей, амина формулы (III).
В особом варианте осуществления предлагаемого способа амин формулы (III) используют одновременно также в качестве разбавителя.
Переработку реакционной смеси и выделение целевого продукта осуществляют стандартными методами.
Изобретение относится как к индивидуальным изомерам, так и также к смесям соединений формулы (I). Эти смеси можно разделять на компоненты обычными методами, например, путем селективной кристаллизации из пригодных растворителей или путем хроматографии на силикагеле или оксиде алюминия. Рацематы можно разделять на индивидуальные энантиомеры обычными способами, так, например, путем солеобразования с оптически активными кислотами, как камфорсульфокислота или дибензоилвинная кислота, и путем селективной кристаллизации или путем дериватизации с помощью пригодных, оптически активных реагентов, разделения диастереомерных производных и обратного расщепления или разделения на оптически активном носителе колоночной хроматографии.
Производные валинамида вышеприведенной общей формулы (I) пригодны в качестве промежуточных продуктов для получения известных производных аминокислот общей формулы (IV)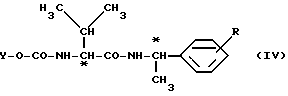
в которой R имеет вышеуказанное значение,
Y - арил, аралкил или алкил, предпочтительно изопропил и втор-бутил, или фенил, бензил или циклопентил, каждый из которых возможно замещен хлором, метилом и/или метоксигруппой, которые проявляют фунгицидную активность.
Получение производных аминокислот формулы (IV) осуществляют за счет того, что соединение формулы (I) подвергают
а) взаимодействию с соединением общей формулы (V):
Y-O-CO-Z, (V)
в которой Y имеет вышеуказанное значение,
Z - галоген или группа -O-CO-OY, где Y имеет вышеуказанное значение,
в среде разбавителя и возможно в присутствии акцептора кислоты и катализатора, при температурах от -100 до +120oC.
или
б) взаимодействию с фосгеном в среде разбавителя и возможно в присутствии акцептора кислоты при температурах от -100 до +120oC с последующим взаимодействием получаемого при этом соединения со спиртом общей формулы (VI)
Y-OH, (VI)
в которой Y имеет вышеуказанное значение,
при температурах от -100 до +120oC.
Способы (а) и (б) представляют собой дальнейшие объекты изобретения.
Производные кислот формулы (V) и спирты формулы (VI) представляют собой общеизвестные соединения органической химии.
В качестве разбавителей для осуществления способов (а) и (б) используют инертные органические растворители, такие как кетоны, как ацетон или метилэтилкетон; сложные эфиры, как этил- или метилацетат; амиды, как диметилформамид; нитрилы, как ацетонитрил; хлорированные углеводороды, как метиленхлорид или тетрахлорметан; углеводороды, как толуол, или простые эфиры, как тетрагидрофуран, а также возможно воду и их смеси.
В качестве акцепторов кислоты применяют обычные неорганические и органические, связывающие кислоту вещества. К ним предпочтительно относятся третичные амины, как триэтиламин, пиридины или N-метилпиперидин, а также неорганические основания, например, гидроксиды металлов, как гидроксид натрия или калия, или карбонаты металлов, как карбонат натрия или карбонат кальция.
Способ (а) можно осуществлять в присутствии катализатора. В качестве примера следует указать 4-диметиламино-пиридин, 1-гидрокси-бензотриазол или диметилформамид.
При осуществлении способов (а) и (б) температуры можно изменять в широких пределах. В общем работают при температурах от -100 до +120oC0, предпочтительно от -60 до +50oC.
При осуществлении способа (а) на один моль соединения формулы (I) используют в общем от одного до двух молей, предпочтительно от одного до полутора молей, производного кислоты формулы (V).
При осуществлении способа (б) предпочтительно используют эквимолярные количества. В некоторых случаях оказывается предпочтительным работать с ди- или трифосгеном вместо фосгена соответственно использовать избыток спирта формулы (VI).
Полученные согласно способам (а) и (б) замещенные производные аминокислот общей формулы (IV) можно очищать и разделять на компоненты обычными способами, как, например, кристаллизация из пригодного растворителя или хроматография на силикагеле соответственно на оксиде алюминия. Рацематы можно разделять обычными способами на индивидуальные энантиомеры.
Нижеследующие примеры поясняют настоящее изобретение.
Пример 1. L-Валин-4-метилфенэт-1-ил-амид.
23,6 г (0,175 моль) 4-Метилфенэт-1-ил-амина в 100 мл ацетонитрила при температуре -10oC в течение времени от 4 до 6 ч смешивают с 5,0 г (0,035 моль) 4-изопропил-оксазолидин-2,5-диона. Реакционную смесь дополнительно перемешивают в течение примерно 18 ч при комнатной температуре и затем растворитель, а также избыточный амин отгоняют в вакууме.
Полученный сырой продукт можно использовать непосредственно дальше для получения соединения формул (IV-I).
После очистки в высоком вакууме получают 7,0 г (84,5% от теоретически рассчитанного количества) L-Валин-4-метилфенэт-1-ил-амида.
1H-ЯМР (дейтерированный диметилсульфоксид; δ (м.д.)): 0,74 - 0,87 (дм, 6H, 2CH3); 1,33 (д, 3H, CH3); 1,62 (5, 2H, NH2; 1,77 - 1,87 (м, H, CH); 2,26 (с, 3H, CH3); 2,93 (д, H, CH); 4,85 - 4,95 (м, H, CH); 7,09 - 7,21 (м, 4H, фенильные протоны); 8,13 (м, H, NH).
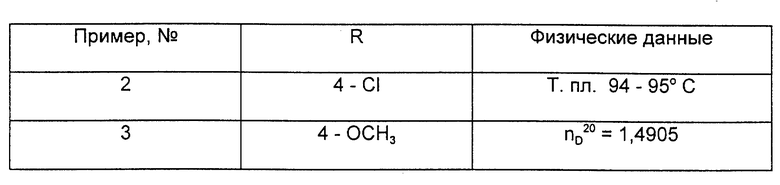
Соответственно примеру 1 и согласно вышеописанной общей методике осуществления способа получения целевых продуктов получают еще следующие соединения общей формулы (I) (см. таблицу в конце описания).
Пример 4. L-Валин-2-(3,4-диметоксифенил)этиламид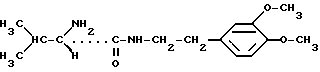
10,2 г (0,055 моль) 2-(3,4-Диметоксифенил)этиламина в 60 мл ацетона при 50oC и в течение 2-3 ч смешивают с 2,0 г (0,1398 моль) 4-изопропил-оксазолидин-2,5-диона. Реакционную смесь дополнительно перемешивают в течение 18 ч и затем растворитель, а также избыточный амин отгоняют в вакууме.
Получают 3,5 г (90% от теоретически рассчитанного количества) сырого продукта достаточной степени чистоты, который можно использовать непосредственно дальше для получения соединения формулы (IV).
1H-ЯМР (дейтерированный диметилсульфоксид; δ (м.д.)): 0,75 (д, 3H, CH3); 0,84 (д, 3H, CH3); 1,81 - 1,92 (м, H, CH); 2,65 (т, 2H, CH2); 3,21 - 3,35 (м, 2H, CH2); 3,45 (с, 2H, NH2); 3,71 (с, 3H, CH3); 3,74 (с, 3H, CH3); 6,7 - 6,89 (м, 3H, ароматические протоны); 7,96 (м, H, NH).
Пример 5.
А. Способ (а) получения промежуточных соединений (IV).
1 г (0,0043 моль) L-Валин-4-метилфенэт-1-ил-амида (см. пример 1) и 0,62 г (0,0045 моль) карбоната калия при -10oC суспендируют в 50 мл метиленхлорида и смешивают с 0,8 г (0,0065 моль) изопропилового эфира хлормуравьиной кислоты в 10 мл метиленхлорида. Реакционную смесь дополнительно перемешивают в течение примерно 18 ч при комнатной температуре, выливают в воду со льдом, фазы разделяют и водную фазу экстрагируют многократно метиленхлоридом. Объединенные органические фазы сушат над сульфатом натрия и концентрируют.
Получают 1,35 г (98% от теоретически рассчитанного количества) N-(изопропокси-карбонил)-L-валин-4-метилфенэт-1-ил-амида с температурой плавления 160oC.
Б. Способ (б) получения промежуточных соединений (IV).
В 300 мл метиленхлорида при температуре -50oC растворяют 0,1 моль L-валин-4-метилфенэт-1-ил-амида (см. пример 1) и 0,1 моль триэтиламина. В этот раствор вводят 0,12 моль фосгена. Реакционную смесь в течение 4 ч оставляют нагреваться до комнатной температуры. После этого прикапывают раствор из 0,12 моль изопропанола в 50 мл метиленхлорида и дополнительно перемешивают в течение 1 ч при температуре 50oC.
После обработки получают 16,9 г N-(изопропоксикарбонил)-L-валин-4-метилфенэт-1-ил-амида с температурой плавления 160oC.
Производные валинамида вышеприведенной общей формулы (I) исследовались в отношении фунгицидного действия на различного вида грибки. При этом установлено, что они проявляют 100%-ное действие при норме расхода 250-500 г/га.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ВАЛИНАМИДА В ВИДЕ РАЦЕМАТА ИЛИ В R(+)-КОНФИГУРАЦИИ L-ИЗОМЕРА, ОБЛАДАЮЩИЕ ФУНГИЦИДНОЙ АКТИВНОСТЬЮ | 1991 |
|
RU2015962C1 |
| ФУНГИЦИДНОЕ СРЕДСТВО И СПОСОБ БОРЬБЫ С ГРИБКАМИ | 1994 |
|
RU2176449C2 |
| ПРОИЗВОДНЫЕ АМИДОВ АМИНОКИСЛОТ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, СЕЛЬСКОХОЗЯЙСТВЕННЫЕ ИЛИ САДОВЫЕ ФУНГИЦИДЫ И СПОСОБ УНИЧТОЖЕНИЯ ГРИБОВ | 1995 |
|
RU2129548C1 |
| ПРОИЗВОДНЫЕ ГАЛОГЕНЗАМЕЩЕННОГО БЕНЗИМИДАЗОЛА И ИХ КИСЛОТНО-АДДИТИВНЫЕ СОЛИ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ И ФУНГИЦИДНОЕ СРЕДСТВО | 1996 |
|
RU2170735C2 |
| ХЛОРИДЫ ХЛОРПИРИДИНИЯ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1995 |
|
RU2138481C1 |
| СПОСОБЫ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 1,4-ДИГИДРОПИРИДИН-3,5-ДИКАРБОНОВОЙ КИСЛОТЫ В ВИДЕ R-ИЗОМЕРОВ И ИХ СОЛЕЙ, ИСХОДНЫЕ И ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ ДЛЯ ИХ ПОЛУЧЕНИЯ | 1995 |
|
RU2155752C2 |
| ПРОИЗВОДНЫЕ ТРИАЗОЛИЛА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФУНГИЦИДНОЕ СРЕДСТВО | 1995 |
|
RU2158734C2 |
| ПРОИЗВОДНЫЕ ОКСИМА, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФУНГИЦИДНОЕ СРЕДСТВО И СПОСОБ БОРЬБЫ С ГРИБКОВЫМИ ЗАБОЛЕВАНИЯМИ | 1995 |
|
RU2154629C2 |
| ПРОИЗВОДНЫЕ СУЛЬФОНИЛАМИНОКАРБОНИЛТРИАЗОЛИНОНА И ИХ СОЛИ, ИСХОДНЫЕ СОЕДИНЕНИЯ ДЛЯ ИХ ПОЛУЧЕНИЯ И ГЕРБИЦИДНОЕ СРЕДСТВО НА ИХ ОСНОВЕ | 1993 |
|
RU2125559C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 3-ХИНОЛОНКАРБОНОВОЙ КИСЛОТЫ | 1994 |
|
RU2138483C1 |
Описываются новые производные валинамида общей формулы (I), в которой R - хлор, метил, этил или метокси. Соединения формулы (I) можно применять в качестве фунгицидного средства, а также для получения промежуточных соединений. Описывается также способ их получения и способы получения промежуточных продуктов. 4 с.п. ф-лы, 1 табл.

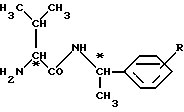 в которой R - хлор, метил, этил или метокси.
в которой R - хлор, метил, этил или метокси.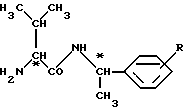
в которой R - хлор, метил, этил или метокси,
отличающийся тем, что соединение общей формулы (II)
подвергают взаимодействию с соединением общей формулы (III)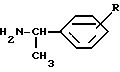
в которой R имеет вышеуказанное значение,
в среде разбавителя и, возможно, в присутствии вспомогательного средства.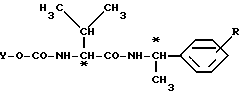
в которой R - хлор, метил, этил или метокси,
Y - алкил, арил или аралкил,
отличающийся тем, что соединение общей формулы (I)
где R имеет вышеуказанное значение,
подвергают взаимодействию с соединением общей формулы (V)
Y-О-СО-Z,
в которой Y имеет вышеуказанное значение,
Z - галоген или группа -О-СО-ОY, где Y имеет вышеуказанное значение,
в среде разбавителя и, возможно, в присутствии акцептора кислоты и катализатора при температурах от -100 до +120oC.
в которой Y и R имеют указанные в п.3 значения,
отличающийся тем, что соединение общей формулы (I)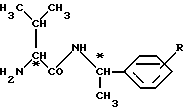
в которой R имеет указанное в п.3 значение,
подвергают взаимодействию с фосгеном в среде разбавителя и, возможно, в присутствии акцептора кислоты при температурах от -100 до +120oC с последующим взаимодействием получаемого при этом соединения со спиртом общей формулы (VI)
Y-ОН,
в которой Y имеет указанное в п.3 значение,
при температурах от -100 до +120oC.
Приоритет по пунктам и признакам:
28.06.1994 по пп.1 и 2 - соединения формулы (I), у которых R находится в положении 4; по пп.3 и 4 - соединения формулы (IV), у которых R находится в положении 4; Y - изопропил и втор-бутил.
| ПОЛЯРИЗАЦИОННО-ОПТИЧЕСКИЙ СПОСОБ ОПРЕДЕЛЕНИЯ ВНУТРЕННИХ НАПРЯЖЕНИИ В ТВЕРДЫХ ТЕЛАХ | 0 |
|
SU274453A1 |
| WO 9301166 А, 21.01.1993 | |||
| US 3676492 А, 11.07.1972 | |||
| Припоечное стекло | 1976 |
|
SU587110A1 |
| Chem | |||
| Abstr | |||
| Запальная свеча для двигателей | 1924 |
|
SU1967A1 |
| Приспособление к станкам глубокого сверления для автомагического управления работой сверла | 1958 |
|
SU117279A1 |
| Chem | |||
| Abstr | |||
| Сплав для отливки колец для сальниковых набивок | 1922 |
|
SU1975A1 |
| Сатурационный аппарат | 1924 |
|
SU10920A1 |
| SU 924038 А, 30.04.1982 | |||
| 1969 |
|
SU415413A1 | |
Авторы
Даты
2000-10-10—Публикация
1995-06-16—Подача