Настоящее изобретение относится к новому способу разделения карбинола, формулы 1 на его энантиомеры, а также к рацемизации одного из них, осуществляя способ в определенной последовательности до получения высокого выхода требуемого энантиомера. Стереоизомеры формулы 1 являются основными соединениями для синтеза энантиомеров соединения формулы 2.
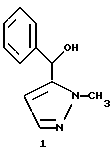

Соединение формулы 2 (±)-5-{[(N,N-диметиламиноэтокси)- фенил]метил}-1-метил-1H-пиразол является соединением, обладающим анальгетическим действием, и которое проходит в настоящее время клинические испытания; оно описано в европейском патенте EP 289380. Синтез и исследования обоих энантиомеров 2 как анальгетиков описаны в литературе (J.A.Hueso, J.Berrocal, B.Gutierrer, A. J. Farre u J.Frigola. Bioorganic & Medicinal Chemistry Letters, 1993, 3, 269-272); из результатов этих исследований следует, что правовращающий энантиомер наиболее активен.
Энантиомеры (+) и (-) соединения формулы 2 получают, соответственно, алкилированием (+) и (-) стереоизомеров соединения формулы 1. Стереоизомер (+) соединения 1 получают с очень низким выходом из (R)-этилманделата, что определило таким образом абсолютную конфигурацию (R)-(+) соединения 1. Энантиомеры 1 также можно получить сложными способами разделения на хроматографической колонке или путем фракционных кристаллизаций из сложных диастереоизомерных сложных эфиров, образуемых путем реакции соединения 1 с (+)-O-ацетилминдальной кислотой. Выход составляет 22% для энантиомера (-) соединения 1 и 25% для энантиомера (+) соединения 1 (обозначенные далее (-)-1 и (+)-1).
С другой стороны использование биокатализаторов при разделении рацемических смесей подробно описано в документах:
[a) "Microbial reagents in organic synthesis" Stefano Servi, Kluwer Academic Publishers, Лондон, 1992;
b) "Enzymes in synthetic organic chemistry", C.H.Wong u G.M. Whitesides, Elsevier Science, Oxford 1994;
c) "Biotransformations in Organic Chemistry", K.Faber, Lange и Springer, 1995].
Существует множество различных классов ферментов, используемых для разделения стереоизомеров, включая гидролазы (в частности, липазы, протеазы и эстеразы), лиазы и оксидоредуктазы. Гидролазы являются одним из самых привлекательных для использования в разделении энантиомеров, поскольку они доступны по невысоким ценам, и некоторые из них демонстрируют достаточную устойчивость к органическим растворителям.
Использование органических растворителей в реакциях, катализируемых ферментами, имеет ряд преимуществ:
a) большая часть органических субстратов более растворима в органических растворителях, чем в воде;
б) рекуперация продуктов реакции очень сильно облегчается;
в) ферменты легко рекуперировать и использовать повторно;
г) в некоторых случаях наблюдается высокая энантиоселективность.
Несмотря на преимущества использования ферментов в органических растворителях имеются и некоторые недостатки:
а) поиск подходящего растворителя;
б) низкая скорость реакции;
в) уменьшение оптической чистоты целевых продуктов в реакциях, имеющих реверсивный характер [см. a) A.M.Klibanov. Trends Biochem.Sci 1989, 14, 141;
b) C.S. Chen, C.J.Sih, Angew. Chem. Int. Ed.Engl., 1989, 28, 695]. Подтверждение того факта, что некоторые ферменты могут действовать в органических растворителях, послужило одной из главных причин резкого увеличения за последнее десятилетие использования реакций биопревращений для получения продуктов, имеющих терапевтический и промышленный интерес. [см.: a) A.N.Collins, G.N.Sheldrake, S.Crosby "Chirality in Industry" Wiley, Лондон, 1992;
b) S.C.Stinson, Chem. & Eng. News, 1994, 38;
c) A.C.Margolin, Enzyme Microb. Techol. 1993, 15, 266].
Задача настоящего изобретения состоит в разработке экономически выгодного способа получения правовращающего стереоизомера (R)-(+) соединения 1, который мог бы быть одновременно полезен для получения левовращающего стереоизомера (S)-(-) этого же соединения 1.
Способ, к которому относится настоящее изобретение, основывается на биокатализе, где используется биокатализатор для обеспечения избирательной трансэтерификации между рацемическим спиртом 1 и сложным эфиром формулы 3, где R1 представляет собой метил или этил и R2 представляет собой винил или изопропенил. С помощью фермента, обеспечивающего соответствующую стереоселективность, можно получить реакционную смесь, содержащую непрореагировавший энантиомер 1, а также сложный эфир формулы 4, где R1 представляет собой метил или этил, полученный из другого энантиомера 1.


Для отделения и рекуперации непрореагировавшего спирта и полученного сложного эфира можно, таким образом, относительно просто применить известные химические методы, такие как хроматография или кристаллизация. Другой аспект изобретения состоит в проведении гидролиза полученного сложного эфира с использованием кислотного или основного катализатора таким образом, чтобы получить соединение 1 с рацемизацией последнего или с сохранением конфигурации. В случае когда получают рацемическую смесь соединения 1, то ее затем можно снова обработать с участием указанного биокатализатора для осуществления вышеописанной трансэтерификации, и так последовательно несколько раз. Таким образом добиваются практически полной трансформации рацемического субстрата 1 с образованием требуемого энантиомера.
Стратегия, используемая в настоящем изобретении, состоит в том, чтобы последовательно комбинировать энзиматическую трансэтерификацию карбинола 1 и химическую трансформацию с рацемизацией. Ферментами, наиболее подходящими для осуществления трансэтерификации, являются гидролазы, главным образом липазы, выделяемые микроорганизмами, в свободном виде или иммобилизованные. Сложными эфирами, используемыми в качестве ацилирующих агентов, являются сложные енольные эфиры формулы 3, где R1 представляет собой метил или этил и R2 представляет собой винил или изопропенил. Реакция трансэтерификации протекает в отсутствие растворителя или в соответствующем растворителе, таком как гексан, циклогексан, толуол, ацетон, диоксан, тетрагидрофуран, этанол и т. д. при температуре между 20oC и температурой рефлюкса в течение времени, необходимого для осуществления трансформации, это время может колебаться от 6 до 48 часов. Добавление молекулярного сита в середине реакции может повысить активность и сократить содержание воды. Протекание реакции ацилирования легко контролируется ядерным магнитным резонансом протона. Непрореагировавший энантиомер 1 отделяется от другого этерифицированного энантиомера 4 хроматографией на колонке с силикагелем или кристаллизацией в соответствующем растворителе. Оптическую чистоту анализируют с помощью хиральной высокоэффективной жидкостной хроматографии (ВЭЖХ).
Этерифицированный энантиомер 4 гидролизуют, чтобы затем получить рацемический карбинол 1 или соответствующий гомохиральный карбинол. Гидролиз осуществляется соответственно в кислой или основной среде при температуре между 60oC и температурой рефлюкса в течение периода времени от 2 до 24 часов.
Путем алкилирования стереоизомеров (+) и (-) соединения 1 диметиламинохлорэтаном в условиях фазового перехода и последующей обработки лимонной кислотой, получают соответственно стереоизомеры (+) цитрат и (-) цитрат соединения 2.
Вышеописанный способ трансэтерификации рацемического карбинола 1 для получения гомохирального карбинола и гидролиза образованного гомохирального сложного эфира для получения соответствующего гомохирального спирта или же рацемического спирта, а также подробное описание примеров, данных ниже, приведены исключительно для иллюстрации и не должны ограничивать рамки настоящего изобретения.
Пример 1
Разделение (±)-5-(фенил)-гидроксиметил-1-метил- 1H-пиразола, (±)-1, липазой PS:
Смесь 100 г вышеуказанного рацемического карбинола, 50 г активированной липазы PS выпускаемой AMANO PHARMACEUTICAL COMPANY Ltd. (NACOYA-JP), 50 г активированного молекулярного сита с ячейками в 3 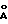 и 1000 мл винилацетата взбалтывают при температуре 60oC в течение 24 часов. С помощью анализа 1H-ЯМР определяют, что субстрат ацетилирован на 55%, проводят фильтрацию, чтобы отделить липазу и молекулярное сито, и при пониженном давлении выпаривают винилацетат. Остаток растворяют в циклогексане, и из него получают кристаллизацией 36 г (72%) (+)-5-(фенил) гидроксиметил-1-метил-1H-пиразола, (+)-1, с оптической чистотой более 96% (избыток энантиомера, определяемый ВЭЖХ = 92%); точка плавления: 80-83oC; ИК (KBr) 3237, 1456, 1394, 1294, 1193, 1058, 1006, 785, 765, 708, 701 см-1; [α]D + 16,2 (c=1, CHCl3). Выпаривание растворителя дает 76,5 г в основном (-)-5-(фенил) метилкарбонилоксиметил-1-метил-1H-пиразола, (-)-4, где R1 представляет собой метил.
и 1000 мл винилацетата взбалтывают при температуре 60oC в течение 24 часов. С помощью анализа 1H-ЯМР определяют, что субстрат ацетилирован на 55%, проводят фильтрацию, чтобы отделить липазу и молекулярное сито, и при пониженном давлении выпаривают винилацетат. Остаток растворяют в циклогексане, и из него получают кристаллизацией 36 г (72%) (+)-5-(фенил) гидроксиметил-1-метил-1H-пиразола, (+)-1, с оптической чистотой более 96% (избыток энантиомера, определяемый ВЭЖХ = 92%); точка плавления: 80-83oC; ИК (KBr) 3237, 1456, 1394, 1294, 1193, 1058, 1006, 785, 765, 708, 701 см-1; [α]D + 16,2 (c=1, CHCl3). Выпаривание растворителя дает 76,5 г в основном (-)-5-(фенил) метилкарбонилоксиметил-1-метил-1H-пиразола, (-)-4, где R1 представляет собой метил.
Пример 2
Гидролиз и рацемизация (-)-5-(фенил)метилкарбонилокси-метил-1- метил-1H-пиразола, (-) -4:
76,5 г (-)-5-(фенил)метилкарбонилоксиметил-1-метил-1H-пиразола, (-)-4, нагревают с обратным холодильником в 300 мл 6 н. соляной кислоты в течение 12 часов, фильтруют при нагревании и подщелачивают раствор гидроксидом аммония, чтобы получить 61,4 г рацемического карбинола (±)-5-(фенил)гидроксиметил-1-метил-1H-пиразола, (±)-1, точка плавления 105-106oC; ИК (KBr) 3225, 1457, 1398, 1208, 1200, 1018, 1009, 794, 751, 702 см-1; энантиометрический избыток, определяемый ВЭЖХ=0.
Пример 3
Разделение (±)-5-(фенил)гидроксиметил-1-метил-1H-пиразола, (±)-1, липазой PS:
Смесь 61,4 г карбинола (±)-1, полученного в примере 2, 30,7 г активированной липазы PS, выпускаемой AMANO PHARMACEUTICAL COMPANY (NACOYA-JP), 30,7 г активированного молекулярного сита с ячейками  и 600 мл винилацетата взбалтывают при 56oC в течение 36 часов. С помощью анализа ЯМР протона определяют, что субстрат ацетилирован на 53%, затем проводят фильтрацию, чтобы отделить липазу и молекулярное сито, и выпаривают при пониженном давлении винилацетат. Остаток растворяют в циклогексане, из которого получают кристаллизацией 21,7 г (71%) (+)-5-(фенил)гидроксиметил-1-метил-1H-пиразола, (+)-1, с оптической чистотой выше 95%, точка плавления: 79-85oC [α]D= +16,0 (c= 1, CHCl3). Выпаривание растворителя дает 45,8 г в основном (-)-5-(фенил)метилкарбонилоксиметил-1-метил- 1H-пиразол а, (-)-4, где R1 представляет собой метил.
и 600 мл винилацетата взбалтывают при 56oC в течение 36 часов. С помощью анализа ЯМР протона определяют, что субстрат ацетилирован на 53%, затем проводят фильтрацию, чтобы отделить липазу и молекулярное сито, и выпаривают при пониженном давлении винилацетат. Остаток растворяют в циклогексане, из которого получают кристаллизацией 21,7 г (71%) (+)-5-(фенил)гидроксиметил-1-метил-1H-пиразола, (+)-1, с оптической чистотой выше 95%, точка плавления: 79-85oC [α]D= +16,0 (c= 1, CHCl3). Выпаривание растворителя дает 45,8 г в основном (-)-5-(фенил)метилкарбонилоксиметил-1-метил- 1H-пиразол а, (-)-4, где R1 представляет собой метил.
Пример 4
Разделение (±)-5-(фенил)гидроксиметил-1-метил- 1H-пиразола, (+)-1, липазой PS:
Смесь 3,5 г карбинола (±)-1, 7,4 г активированной липазы PS выпускаемой AMANO PHARMACEUTICAL COMPANY Ltd. (NACOYA-JP) и 100 мл вилинацетата взбалтывают при 62oC в течение 13 часов. С помощью анализа ЯМР-протона определяют, что субстрат ацетилирован на 50%, затем проводят фильтрацию, чтобы отделить липазу и молекулярное сито, и выпаривают винилацетат при пониженном давлении. Остаток подвергают хроматографии на колонке из силикагеля со смесью диэтиловый эфир:гексан (2:1) в качестве элюанта, и получают 2,1 г (98%) (-)-5-(фенил)метил-карбонилоксиметил- 1-метил-1Н-пиразола, (-)-4, где R1 представляет собой метил. При последующем элюировании диэтиловым эфиром получают 1,7 г (98%) (+)-5-(фенил)гидроксиметил-1-метил-1H-пиразола, (+)-1 с энантиометрическим избытком, определяемым ВЭЖХ=94%.
Пример 5
Гидролиз с сохранением конфигурации (-)-5-(фенил)метилкарбонилоксиметил-1-метил-1H-пиразола, (-)-4:
2,3-г (-)-5-(фенил)метилкарбонилоксиметил-1-метил-1H-пиразола, (-)-4, нагревают с обратным холодильником в 4 мл 20% гидроксида натрия и 10 мл этанола в течение 2 часов, выпаривают этанол, добавляют 10 мл воды, осуществляют экстракцию диэтиловым эфиром, сушку сульфатом магния, фильтрацию и получают из раствора 1,8 г (95%) (-)-5-(фенил)гидроксиметил-1-метил-1H-пиразола, (-)-1, с оптической чистотой выше 94%, [α]D= -16,1 (с=1, CHCl3).
Пример 6
Получение цитрата (+)-5-{[N,N-диметиламиноэтоксифенил]метил}- 1-метил-1Н-пиразола, (+)-2 цитрата.
Нагревают с обратным холодильником в течение 7 часов смесь 12,7 г (+)-5-(фенил) гидроксиметил-1-метил-1H-пиразола, (+)- 1, в 250 мл толуола, 125 мл 50% гидроксида натрия, 3 г хлористого триэтилбутиламмония и 14,6 г хлоргидрата диметиламинохлорэтана. Из холодной смеси экстрагируют с помощью толуола 16,2 г (92,6%) (+)- 5-{[N,N-диметиламиноэтокси)-фенил]метил}-1-метил-1H-пиразола, (+)-2.
Взбалтывают при 40oC смесь 15 г (+)-5-{[N,N-диметиламиноэтокси)-фенил] метил} -1-метил-1H-пиразола, (+)-2, и 13,5 г моногидрата лимонной кислоты в этаноле до полного растворения. Из этого раствора выделяют кристаллизацией 24,7 г (94,5%) цитрата (+)-5-{[N,N-диметиламиноэтокси)-фенил]метил}-1-метил-1H- пиразола, (+)-2, точка плавления 129-131oC, [α]D= +8,3 (с=1, H2O).
Пример 7
Получение цитрата (-)-5-{ [N, N-диметиламиноэтокси)фенил]метил} -1-метил-1H-пиразол, (-)-2 цитрата.
Действуя так же, как в примере 6, и используя энантиомер (-)-5- (фенил)гидроксиметил-1-метил-1H-пиразол, (-)-1 как продукт разделения, получают (-)-5-{[N,N-диметиламиноэтокси)-фенил]метил} -1-метил-1H-пиразол, (-)-2 цитрат, точка плавления 128-130oC [α]D= -8,2 (с=1, H2O).
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНОЕ ТИЕНИЛАЗОЛИЛАЛКОКСИЭТАНАМИНА, СПОСОБ ЕГО ПОЛУЧЕНИЯ (ВАРИАНТЫ), ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ПРОМЕЖУТОЧНЫЙ ПРОДУКТ И СПОСОБ ЕГО ПОЛУЧЕНИЯ (ВАРИАНТЫ) | 1999 |
|
RU2213743C2 |
| СПОСОБ ПОЛУЧЕНИЯ РАЦЕМИЧЕСКИХ И ЭНАНТИОМЕРНО ЧИСТЫХ ПРОИЗВОДНЫХ 1,5-ДИАРИЛ-3-ТРИФТОРМЕТИЛ-Δ-ПИРАЗОЛИНОВ | 2002 |
|
RU2288915C2 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ НЕЙРОГЕННОГО ВОСПАЛЕНИЯ | 1999 |
|
RU2212237C2 |
| ПРОИЗВОДНЫЕ ПИРАЗОЛИНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1999 |
|
RU2233272C2 |
| ПРИМЕНЕНИЕ ПРОИЗВОДНЫХ ПИРАЗОЛИНА ПРИ ПОЛУЧЕНИИ ЛЕЧЕБНОГО СРЕДСТВА ДЛЯ ПРЕДУПРЕЖДЕНИЯ И/ИЛИ ЛЕЧЕНИЯ БОЛЕЗНЕЙ, СВЯЗАННЫХ С ПРОЛИФЕРАЦИЕЙ КЛЕТОК | 2002 |
|
RU2305545C2 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ИЗОТИАЗОЛ-ПИРИДОН АЦЕТИДИНИЛА И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1991 |
|
RU2041226C1 |
| ПРОИЗВОДНЫЕ АРИЛ(ИЛИ ГЕТЕРОАРИЛ)АЗОЛИЛКАРБИНОЛА ДЛЯ ЛЕЧЕНИЯ РЕСПИРАТОРНЫХ ЗАБОЛЕВАНИЙ | 2002 |
|
RU2294198C2 |
| ПРОИЗВОДНЫЕ АЗЕТИДИНА ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, ОБЛАДАЮЩИЕ АНТИМИКРОБНОЙ АКТИВНОСТЬЮ | 1991 |
|
RU2044735C1 |
| ПРОИЗВОДНЫЕ 4-(2-ПИРИМИДИНИЛ)-1-ПИПЕРАЗИНИЛА ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ | 1991 |
|
RU2071474C1 |
| ПРОИЗВОДНЫЕ БЕНЗАТИАЗИНОВ | 1991 |
|
RU2032679C1 |
Настоящее изобретение относится к способу преимущественного получения энантиомера (R)-(+)-5-(фенил) гидроксиметил-1-метил-1Н-пиразола (R-(+)-1) с высоким выходом выделением из рацемической смеси (±)-5-(фенил)гидроксиметил-1-метил-1H-пиразола формулы 1, характеризующемуся последовательным осуществлением способа, который включает использование липазы, обладающей ферментной активностью, в реакции избирательной трансэтерификации, с помощью сложного эфира формулы 3: R1СООR2, где R1 представляет метил или этил, R2 - винил или изопропенил. В результате трансэтерификации получают смесь, содержащую непрореагировавший R-(+)-1 и сложный эфир (S)-(-)-5-(фенил) алкилкарбонилоксиметил-1-метил-1H-пиразола, формулы 4, где R1 представляет метил или этил. Непрореагировавший энантиомер R-(+)-1 отделяют от указанного эфира хроматографией или кристаллизацией в соответствующем растворителе с рекуперацией R-(+)-1 и осуществляют гидролиз полученного сложного эфира. 5 з.п. ф-лы.



отличающийся тем, что осуществляют избирательную трансэтерификацию между сложным эфиром формулы 3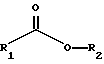
где R1 представляет собой метил или этил;
R2 представляет собой винил или изопропенил,
и энантиомером карбинола S-(-)-5-(фенил) гидроксиметил-1-метил-1Н-пиразола, S-(-)-1, указанной рацемической смеси с использованием как катализатора липазы, обладающей ферментной активностью в реакции трансэтерификации, что приводит к получению реакционной смеси, содержащей непрореагировавший энантиомер R-(+)-1 и S-(-)-5(фенил)алкилкарбонилоксиметил-1-метил-1Н-пиразол формулы 4
где R1 представляет собой метил или этил, обозначаемый S-(-)-4,
непрореагировавший энантиомер R-(+)-1 отделяют от полученного сложного эфира S-(-)-4 хроматографией или кристаллизацией в соответствующем растворителе с рекуперацией энантиомера (R) - (+)-5-(фенил)-гидроксиметил-1-метил-1Н-пиразола, R-(+)-1, и осуществляют гидролиз полученного сложного эфира S-(-)-4.
| J.A.HUESO et al | |||
| Bioorganic and Medicine Chemistry Letters | |||
| Способ изготовления фанеры-переклейки | 1921 |
|
SU1993A1 |
| МЕХАНИЗМ ИЗМЕНЕНИЯ МАСШТАБА ИЗОБРАЖЕНИЯ БИНОКУЛЯРНОЙ СИСТЕМЫ | 0 |
|
SU289380A1 |
| ЭЛЕКТРОННЫЙ РЕГУЛЯТОР УРОВНЯ | 0 |
|
SU321918A1 |
| Способ получения 1-замещенных пиразолонов-5 или их солей | 1974 |
|
SU545258A3 |
| ? | |||
Авторы
Даты
2001-01-27—Публикация
1996-12-04—Подача