Область изобретения
Настоящее изобретение относится к новому способу синтеза 5-метокси-2-[[(4-метокси-3,5-диметил-2- пиридинил)-метил] сульфинил] -1Н-бензимидазола, известного под общим названием омепразол. Кроме того, настоящее изобретение также относится к производству из него фармацевтического препарата и его применению в медицине.
Предпосылки изобретения и прототип
Омепразол является ингибитором секреции желудочной кислоты, что делает его полезным в качестве противоязвенного агента. Патент США 4255431 (соответствующий EP 0005129) раскрывает способ получения этого класса замещенных бензимидазолов. Указанный способ включает в себя сочетание реакционных стадий. Последние три стадии данного способа используют более чем один растворитель и требуют выделения промежуточных соединений, чтобы получить конечный продукт омепразол. Полученный продукт загрязнен исходными материалами и побочными продуктами.
Заявка WO 91/18805 описывает усовершенствованный способ синтеза омепразола. Этот способ включает в себя стадию окисления и процедуру обработки омепразола. На стадии окисления используют м-хлорпероксибензойную кислоту в системе метиленхлорид/вода при практически постоянном pH примерно от 8,0 до 8,6. Процедура обработки включает в себя кристаллизацию омепразола путем добавления алкилформиата.
Другой способ производства омепразола описан в патенте США 5391752. Этот способ описывает только стадию окисления. На указанной стадии в качестве окисляющего агента используют монопероксифталат магния. Полученный продукт загрязнен исходным материалом и побочными продуктами.
Еще один способ производства соединений, демонстрирующих структурное подобие омепразолу, раскрыт в патенте США 4619997. Промежуточные соединения выделяют, но не очищают, и в химических стадиях в ходе всего процесса используют различные растворители.
В свете вышесказанного ясно, что все еще существует необходимость в новом удобном и более эффективном способе производства омепразола.
Сущность изобретения
Далее следует описание усовершенствованного способа. Приведенная ниже схема 1 иллюстрирует последовательно три основные реакционные стадии в производстве омепразола. На этой схеме указаны полные химические названия, а также краткие названия для исходного материала и различных промежуточных соединений. Исходный материал, так же как используемые реагенты, легко могут быть получены посредством описанных в литературе способов.
СХЕМА 1
Стадия 1:
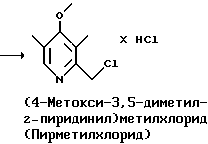
Стадия 2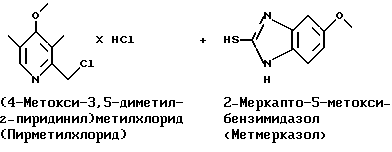

Стадия 3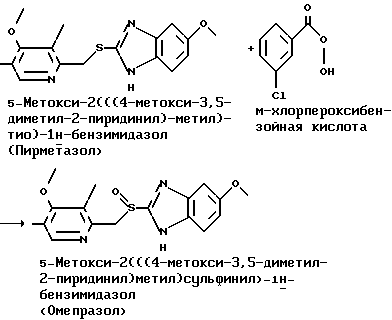
Преимущества усовершенствованного способа по настоящему изобретению раскрыты в следующих параграфах.
Изобретение решает задачу разработки способа производства омепразола с помощью всех трех реакционных стадий, описанных выше, причем их проводят без выделения или очистки промежуточных соединений и проводят в одной главной системе растворителей, общей для всей реакционной последовательности. Такой способ исключает времяпотребляющие стадии выделения или очистки промежуточных соединений или замены растворителя по ходу процесса и, таким образом, является более эффективным благодаря высокой производительности. Следующее важное преимущество такого способа заключается в том, что исключено обращение с токсичными и возможно мутагенными промежуточными соединениями, такими как пирметилхлорид, обусловленное выделением и очисткой.
Другая предпочтительная задача, которую решает настоящее изобретение, заключается в разработке способа, использующего систему растворителей, которая экологически безопасна, чтобы избежать сброса вредных растворителей. Существует общая заинтересованность со стороны экологических групп как внутри, так и вне фармацевтической индустрии в том, чтобы эта индустрия развивала и использовала экологически безопасные способы. В некоторых странах правительство также ввело ограничения на выброс вредных хлорсодержащих растворителей в воздух.
Удивительно, но новый способ по настоящему изобретению дает омепразол высокой чистоты без выделения или очистки промежуточных соединений. Полученный омепразол может быть при желании подвергнут дальнейшей обработке на стадии очистки и/или по желанию переработан в фармацевтически приемлемые соли.
Другой задачей настоящего изобретения является разработка способа для стадии возможной очистки омепразола.
Далее, настоящую реакционную последовательность, начиная от пирметилового спирта через пирметилхлорид и пирметазол, дающую омепразол, можно осуществлять в одной главной системе растворителя, используемой на протяжении всей реакционной последовательности. Эта система растворителей предпочтительно инертна по отношению ко всем реагентам и пригодна для всех трех стадий этого способа.
Подробное описание изобретения
На стадии 1 пирметиловый спирт подвергают взаимодействию с избытком тионилхлорида или другого подходящего хлорирующего агента, дающего возможность получать алкилхлориды, т. е. пирметилхлорид. Эту реакцию предпочтительно проводят при комнатной температуре и в течение приблизительно 30 мин. Эту реакцию можно также проводить при температуре от -5 до 25oC.
Взаимодействие проводят в системе растворителей, которую используют на протяжении всей реакционной последовательности, представленной на схеме 1, т. е. от пирметилового спирта до омепразола. Такая система растворителей, пригодная для настоящего способа, содержит один главный растворитель и возможно один или более чем один сорастворитель. Этот главный растворитель представляет собой растворитель, предпочтительно несмешивающийся с водой, например четыреххлористый углерод, 1,1,2-трихлорэтан, хлороформ, метиленхлорид или толуол. Толуол особенно предпочтителен с экологической точки зрения.
К тому же, эта система растворителей возможно может содержать сорастворитель (ли) для дальнейшего улучшения/повышения растворимости реагентов или продуктов в ходе всей реакционной последовательности. Система растворителей будет функционировать без добавления сорастворителя, однако добавление такого сорастворителя будет увеличивать производительность способа, т.е. выход по объему. Предпочтительными сорастворителями являются спирты и особенно низшие спирты, содержащие 1-4 атома углерода, причем углеродная цепь может быть разветвленной или нормальной.
Примеры систем растворителей включают в себя, но не ограничены этим, 70-80% (об. ) метиленхлорида или толуола и 20-30% (об.) низшего спирта, например этанола.
На стадии 2 пирметилхлорид, образовавшийся на стадии 1, подвергают взаимодействию с метмерказолом в щелочных условиях, например получают водный щелочной раствор метмерказола и смешивают его с пирметилхлоридом в присутствии катализатора фазового переноса. Взаимодействие предпочтительно проводят при температуре 30-60oC в течение длительного периода времени.
Метмерказол загружают в примерно стехиометрическом количестве по отношению к пирметилхлориду. Можно использовать катализатор фазового переноса, например третичный амин, предпочтительно бромид тетрабутиламмония.
Образовавшиеся две фазы разделяют, и водная фаза может быть экстрагирована используемым несмешивающимся с водой органическим растворителем, таким как метиленхлорид или толуол. Более того, можно добавить спирт к раствору пирметазола для улучшения растворимости образовавшегося промежуточного пирметазола.
На стадии 3 м-хлорпероксибензойную кислоту растворяют в несмешивающимся с водой органическом растворителе, таком как метиленхлорид или толуол, м-хлорпероксибензойную кислоту загружают в полученный пирметазол в буферной двухфазной системе, состоящей из несмешивающегося с водой растворителя, такого как метиленхлорид или толуол, и водного основания, такого как гидрокарбонат натрия или калия. Органический растворитель может возможно быть разбавлен спиртом для повышения растворимости м-хлорпероксибензойной кислоты. Окисление м-хлорпероксибензойной кислотой предпочтительно осуществляют при температуре между 0 и 25oC. Полученный продукт экстрагируют в щелочную водную фазу и образовавшийся продукт осаждают из водной фазы посредством снижения pH раствора до приблизительно 9 при температуре окружающей среды. Омепразол выделяют и промывают. Общий выход в данном способе обычно выше чем 75%.
Можно провести дополнительную очистку кристаллизацией из одного или нескольких органических растворителей или осаждением из щелочной водной среды посредством снижения pH добавлением кислоты или алкилформиата.
Примеры подходящих кислот включают в себя, но не ограничены этим, карбоновые кислоты, такие как муравьиная кислота, уксусная кислота или лимонная кислота, и минеральные кислоты, такие как хлороводород, бромоводород, фтороводород, иодоводород, серная кислота, азотная кислота или фосфорная кислота. Предпочтительными кислотами являются карбоновые кислоты. Подходящие алкилформиаты включают в себя, но не ограничены этим, метилформиат и этилформиат. Предпочтительным алкилформиатом является метилформиат.
Более подробно настоящее изобретение описано в следующих неограничивающих примерах.
Изготовление омепразола
Пример 1
17,8 г (0,15 моль) тионилхлорида в 13 мл метиленхлорида загружают в раствор 16,8 г (0,10 моль) пирметилового спирта в метиленхлориде при комнатной температуре. Раствор перемешивают в течение приблизительно 30 мин.
18,0 г (0,10 моль) метмерказола, 47,3 г (0,58 моль) водного гидроксида натрия (50% мас. /мас. ) и бромида тетрабутиламмония (0,9 г) смешивают при температуре окружающей среды. При температуре между 25 и 40oC добавляют раствор пирметилхлорида и смесь кипятят с обратным холодильником в течение 1-2 ч. Разделяют две фазы и водную фазу промывают метиленхлоридом. Органические фазы объединяют.
10,4 г (0,10 моль) бикарбоната калия, растворенного в воде, добавляют к раствору пирметазола.
22,3 г (0,099 моль) м-хлорпероксибензойной кислоты (76,5% мас./мас.), растворенной в 42 мл метиленхлорида и 10 мл этанола, загружают в полученную смесь пирметазола в метиленхлориде и бикарбоната калия в воде. Окисление проводят при 0-15oC. Продукт экстрагируют в водную фазу при щелочном pH посредством добавления гидроксида натрия. Две фазы разделяют и органическую фазу промывают щелочным водным раствором. Водные фазы объединяют.
Омепразол осаждают из водной фазы посредством добавления 12 мл метилформиата, фильтруют, промывают смесью вода/метанол и сушат. Омепразол получают с выходом 76%.
Пример 2
13,1 г (0,11 моль) тионилхлорида загружают в толуольный раствор 16,7 г (0,10 моль) пирметилового спирта при комнатной температуре. Реакцию продолжают в течение приблизительно 30 мин.
Образовавшийся пирметилхлорид в толуоле смешивают с щелочным водным раствором 18,0 г (0,10 моль) метмерказола. Реакцию проводят в присутствии 0,9 г бромида тетрабутиламмония при 40oC в течение пары часов. Две фазы разделяют и водную фазу экстрагируют толуолом. Для улучшения растворимости полученного продукта добавляют этанол прежде чем охлаждать этот раствор до комнатной температуры.
24,4 г (0,10 моль) м-хлорпероксибензойной кислоты в 42 мл толуола и 10 мл этанола загружают в двухфазную систему, полученную из полученного ранее толуольного раствора пирметазола и бикарбоната калия (13,8 г) в воде (120 мл). Окисление осуществляют при температуре между 0oC и температурой окружающей среды. Продукт экстрагируют в щелочную водную фазу добавлением гидроксида натрия. Две фазы разделяют и органическую фазу промывают водой. Омепразол осаждают посредством снижения pH раствора до приблизительно 9 при температуре окружающей среды. Омепразол выделяют, промывают и сушат. Общий выход примерно 77%.
Дополнительная очистка омепразола
Пример 3
20,0 г (0,0579 моль) омепразола, полученного в соответствии с примером 1, 125 мл метанола и 54 мл воды смешивают при температуре окружающей среды.
Продукт растворяют при щелочном pH посредством добавления гидроксида натрия. Раствор фильтруют и охлаждают до приблизительно 0oC.
Продукт осаждают добавлением разбавленной уксусной кислоты, фильтруют и промывают смесью вода/метанол, а затем сушат. Омепразол получают с выходом 90%.
Пример 4
11,2 г (0,0324 моль) омепразола, полученного в соответствии с примером 1, 1,69 мл метанола, 34 мл метиленхлорида и 0,3 мл аммиака смешивают при температуре окружающей среды и полученный раствор фильтруют.
Продукт осаждают выпариванием метиленхлорида при пониженном давлении.
Добавляют 0,3 мл аммиака и суспензию охлаждают до 0oC.
Продукт фильтруют, промывают метанолом, содержащим примерно 1% об./об. аммиака, и сушат. Омепразол получают с выходом 90%.
С экологической точки зрения наилучшим воплощением одного из аспектов настоящего изобретения является способ, описанный в примере 2.
Способ получения Омепразола включает три стадии, которые проводят без выделения или очистки в одной системе растворителей: хлорирование (4-метокси-3,5-диметил-2-пиридинил)метилового спирта хлористым тионилом или другим подходящим хлорирующим агентом; взаимодействие полученного (4-метокси-3,5-диметил-2-пиридинил)метилхлорида с 2-меркапто-5-метоксибензимидазолом в присутствии основания с последующим взаимодействием полученного 5-метокси-2-(((4-метокси-3,5-диметил-2-пиридинил)метил)тио)-1Н-бензимидазола с м-хлорпероксибензойной кислотой. Система растворителей содержит главный растворитель, предпочтительно не смешивающийся с водой (ССl4, СНС13, CH2Cl2 или толуол), и сорастворитель (предпочтительно, С1-С4спирты) для увеличения производительности способа. 11 з.п. ф-лы.
стадия 1: 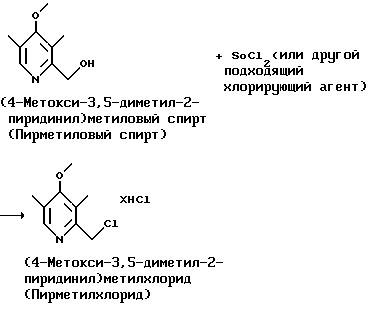
стадия 2: 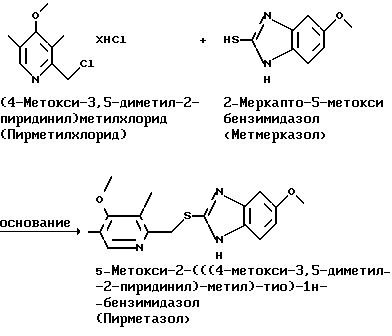
стадия 3: 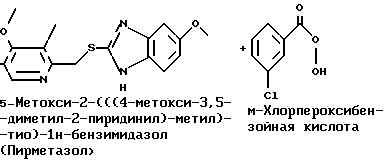
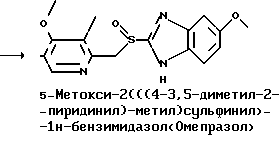
отличающийся тем, что реакционные стадии проводят последовательно без выделения промежуточных соединений, образующихся по ходу проведения способа, с использованием одной главной системы растворителей, общей для всей реакционной последовательности.
| Дугогасительная камера для автоматического выключателя постоянного тока | 1960 |
|
SU139695A1 |
| US 4255431 A, 10.03.1981 | |||
| US 4619997 A, 28.10.1986. | |||
Авторы
Даты
2001-05-10—Публикация
1996-12-05—Подача