Изобретение относится к азотсодержащим соединениям, которые могут представлять собой активное вещество фармацевтической композиции, проявляющей активность в качестве антагониста нейрокинина, более конкретно к производным арилглицинамидов и фармацевтической композиции, содержащей эти соединения.
Известны производные 4-карбоксамидопиридина, которые могут представлять собой активное вещество фармацевтической композиции, проявляющей активность в качестве антагониста нейрокинина (см. заявку WO 94/10 146, кл. C 07 D 211/58, A 61 K 31/445, 11.05.1994 г.).
Задачей изобретения является разработка новых азотсодержащих соединений, которые могут представлять собой активное вещество фармацевтической композиции, проявляющей активность в качестве антагониста нейрокинина.
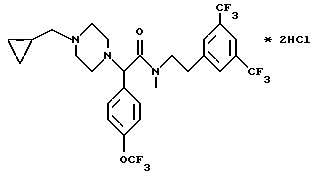
Поставленная задача решается предлагаемыми производными арилглицинамидов общей формулы (I)
и их фармацевтически приемлемыми солями, где Ar означает незамещенный или от одного до пяти раз замещенный фенил или же незамещенный или от одного до двух раз замещенный нафтил (причем заместители фенильного и нафтильного фрагментов независимо друг от друга представлены атомами галогена (фтора, хлора, брома, иода), гидроксильной группой, алкилом с числом атомов углерода от одного до четырех, алкоксилом с числом атомов углерода от одного до четырех, трифторметильной, трифторметоксильной группой или группой -NR9R10, в которой R9 и R10 независимо друг от друга означают атом водорода, или метил, Ar может означать также фенил, замещенный -O(CH2)O- или -O(CH2)2O - группой;
R1 и R2 вместе с атомом азота, с которым они связаны, образуют цикл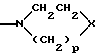
в котором p означает числа 2 или 3
X означает группу N(CH2)nR6 или CR7R8, где n означает числа 0, 1 или 2,
R6 означает циклоалкил с числом атомов углерода от трех до семи, фенил или нафтил, причем фенил может быть от одного до трех раз замещен атомами галогена (фтора, хлора, брома, иода),
R7 и R8 имеют одно из следующих значений:
а) R7 и R8 означают атом водорода, если R3 означает фенил,
б) R7 означает фенил, пиперидинил, 1-метил-пиперидинил группой или группы следующих формул: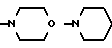
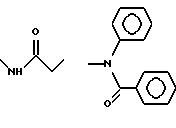
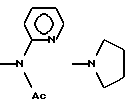
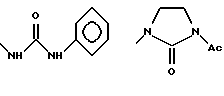

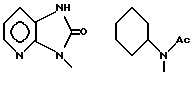
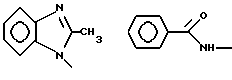
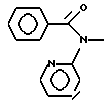
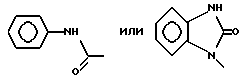
в тех случаях, когда R8 означает атом водорода, карбамоил, ацетиламин, ацетил-N-метил-амин или нитрил,
в) R7 и R8 вместе образуют остаток
R3 означает атом водорода, или фенил,
R4 означает фенилалкил или нафтилалкил с числом атомов углерода в алкильных фрагментах от одного до четырех, причем фенил может быть от одного до трех раз замещен атомами галогена (фтора, хлора, брома, иода), алкилом с числом атомов углерода от одного до четырех, алкоксильной группой с числом атомов углерода от одного до четырех или трифторметилом,
R5 означает атом водорода, алкил с числом атомов углерода от одного до четырех, циклоалкил с числом атомов углерода от трех до шести, карбоксиметил или карбамоилметил.
Соединения общей формулы I могут включать кислотные функциональные группы, главным образом карбоксильные группы, и/или основные группы, например, аминные функции. Поэтому соединения общей формулы I могут быть получены в виде внутренних солей, солей с применяемыми в фармацевтической практике неорганическими кислотами, например, с соляной кислотой, серной кислотой, фосфорной кислотой, сульфоновой кислотой, или с такими органическими кислотами, как, например, малеиновая, фумаровая, лимонная, винная или уксусная кислота, или же они могут быть получены в виде солей с применяемыми в фармацевтической практике основаниями, например с гидроксидами щелочных или щелочноземельных металлов, с карбонатами, с гидроксидами цинка или аммония или с органическими аминами, например с диэтиламином, триэтиламином, триэтаноламином и с другими аминами.
Соответствующие изобретению соединения могут представлять собой рацематы, но они могут быть получены и в виде чистых энантиомеров, то есть в (R)- или в (S)-форме.
В первую группу предпочтительных производных арилглицинамидов формулы (I) входят соединения, у которых
R1 и R2 вместе с атомом азота, с которым они связаны, образуют шестичленное кольцо формулы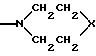
где X означает группу N(CH2)nR6 или CR7R8, где n, R6, R7 и R8 имеют определенное выше значение.
Во вторую группу предпочтительных производных арилглицинамидов формулы (I) входят соединения, у которых
X означает группу формулы N(CH2)nR6, в которой n означает числа 0, 1 или 2, предпочтительно 0,
R6 означает циклоалкил с числом атомов углерода от трех до семи или фенил.
В третью группу предпочтительных производных арилглицинамидов формулы (I) входят соединения, у которых
n означает число 0,
R6 означает циклоалкил с числом атомов углерода от трех до семи, предпочтительно циклобутил или циклогексил.
В четвертую группу предпочтительных производных арилглицинамидов формулы (I) входят соединения, у которых
X означает CR7R8, где
R7 и R8 имеют одно из следующих значений:
a) R7 и R8 означают атом водорода, если R3 представлен фенилом,
б) R7 означает фенил, пиперидинил, группы следующих формул: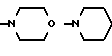

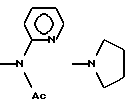

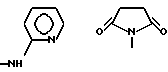
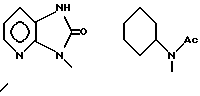

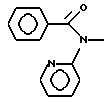
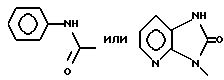
если R8 означает атом водорода, карбамоил, ацетиламин, ацетил-N-метиламин или нитрил, или
в) R7 и R8 вместе образуют остаток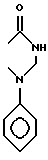
В пятую группу предпочтительных производных арилглицинамидов формулы (I) входят соединения, у которых
R7 и R8 имеют одно из следующих значений:
a) R7 и R8 означают атом водорода, если R3 представлен фенилом,
б) R7 означает фенил или группы следующих формул: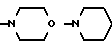
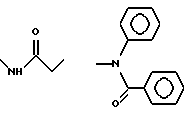

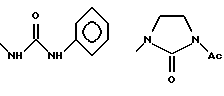
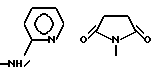
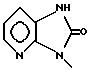
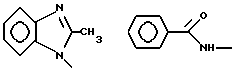
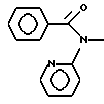
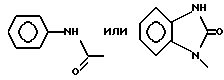
предпочтительно R7 означает фенил или группы
если R8 означает атом водорода или нитрил,
в) R7 и R8 вместе образуют остаток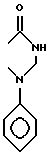
В частности, предпочитаются соединения пятой группы, у которых R7 означает пиридил и R8 означает атом водорода.
В шестую группу предпочтительных производных арилглицинамидов формулы (I) входят соединения, у которых
Ar означает незамещенный или от одного до двух раз замещенный фенил или незамещенный нафтил, причем заместители у фенильного фрагмента независимо друг от друга представлены атомами галогена (фтора, хлора, брома, иода), гидроксильной, метилом, метоксилом, трифторметилом, трифторметоксилом или диметиламиногруппой, или же
Ar означает замещенный -OCH2O-группой фенил, причем диоксиметиленовая группа соединяет 2,3- или 3,4-положения фенильного кольца.
В седьмую группу предпочтительных производных арилглицинамидов формулы (I) входят соединения, у которых
Ar означает незамещенный или от одного до двух раз замещенный фенил или незамещенный нафтил, причем заместители у фенильного фрагмента независимо друг от друга представлены атомами галогена (фтора, хлора, брома), метоксилом или трифторметилом, или же
Ar означает замещенный -OCH2O-группой фенил, причем диоксиметиленовая группа соединяет 2,3- или 3,4-положения фенильного кольца.
В частности, предпочитаются соединения седьмой группы, у которых Ar означает фенил, 3,4-дихлорфенил, 3,4-диметоксифенил или 3,4-метилендиоксифенил.
В восьмую группу предпочтительных производных арилглицинамидов формулы (I) входят соединения, у которых
R3 означает атом водорода.
В девятую группу предпочтительных производных арилглицинамидов формулы (I) входят соединения, у которых
R3 означает атом фенил.
В десятую группу предпочтительных производных арилглицинамидов формулы (I) входят соединения, у которых
R4означает фенилалкил с числом атомов углерода в алкильном фрагменте от одного до трех и где фенил может нести один или два заместителя, причем заместители независимо друг от друга представлены атомами галогена (фтора, хлора, брома, иода), метилом, метоксилом, трифторметилом или
R5 означает атом водорода, алкил с числом атомов углерода от одного до трех, карбоксиметил, карбамоилметил или фенэтил.
В частности, предпочитаются соединения десятой группы, у которых
R4 означает группу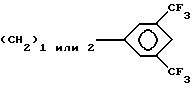
R5 означает атом водорода или метил.
В одиннадцатую группу предпочтительных производных арилглицинамидов формулы (I) входят соединения, представленные следующими формулами: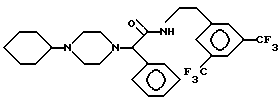

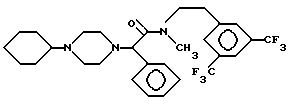
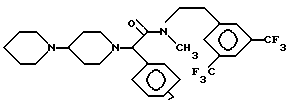
или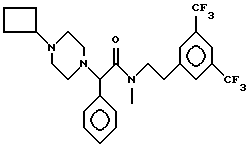
Как указывалось выше, соединения согласно изобретению могут применяться в качестве антагониста нейрокинина.
Результаты исследования соответствующих изобретению соединений:
Сродство к NK1-рецептору (рецептору на вещество P) определяют на клетках лимфобластомы человека (IM-9) с клонированными NK1 - рецепторами, причем измеряют вытеснение меченого 125J вещества P. Полученные таким образом значения Ki показывают эффективность соединений:
Ki
Соединение по примеру 3: 1,4 нмоль/л
Соединение по примеру 4: 1,0 нмоль/л
Соединение по примеру 5: 1,3 нмоль/л
Соединение по примеру 33: 1,3 нмоль/л
Соединение по примеру 40: 1,6 нмоль/л
Соединение по примеру 41: 1,4 нмоль/л
Соединение по примеру 44: 1,1 нмоль/л
Соединение по примеру 45: 2,3 нмоль/л
Соединение по примеру 46: 6,4 нмоль/л
Соединение по примеру 47: 4,2 нмоль/л
Соединение по примеру 53: 9,2 нмоль/л
Соединение по примеру 54: 1,4 нмоль/л
Соединение по примеру 56: 1,5 нмоль/л
Соединение по примеру 58: 2,8 нмоль/л
Соединение по примеру 59: 2,1 нмоль/л
Соединение по примеру 60: 6,8 нмоль/л
Соединение по примеру 61: 1,7 нмоль/л
Соединение по примеру 62: 11,8 нмоль/л
Соединение по примеру 63: 180 нмоль/л
Соединение по примеру 64: 7,0 нмоль/л
Соответствующие изобретению соединения представляют собой ценные антагонисты нейрокинина (тахикинина), антагонизм которых проявляется главным образом на NK1-рецепторах, но они проявляют также свойства NK2- и NK3-антагонистов.
Соответствующие изобретению соединения представляют собой ценные антагонисты нейрокинина (тахикинина), которые оказались антагонистами как вещества P, так и нейрокинина A и, соответственно, нейрокинина Б. Они могут быть полезны при лечении и профилактике болезней, связанных с нейрокининами. Это может быть лечение и профилактика воспалительных и аллергических заболеваний дыхательных путей, таких как астма, хронический бронхит, эмфизема, ринит, кашель, таких заболеваний глаз, как конъюктивит и ирит,
таких заболеваний кожи, как дерматит при контактной экземе, крапивница, псориаз, солнечный ожог, укусы насекомых, нейродермит, чесотка, постгерпетические боли,
таких заболеваний желудочно-кишечного тракта, как язвы желудка и двенадцатиперстной кишки, Colitis ulcerosa (язвенный колит), Morbus Crohn, Colon irritabile, M. Hirschsprung, таких заболеваний суставов, как ревматоидный артрит, реактивный артрит и синдром Рейтера;
эти соединения пригодны для лечения заболеваний центральной нервной системы, таких как деменция (слабоумие), болезнь Альцгеймера, шизофрения, психозы, депрессия, головные боли (например, мигрень или головная боль при гипертонии), эпилепсия;
они пригодны для лечения злокачественных опухолей, коллагенозов, дисфункции мочевыводящих путей, геморроидальных состояний, тошноты и рвоты, вызванных, например, облучением или приемом цитостатиков или же двигательной активностью и болями разного рода.
В силу изложенного выше, изобретение относится также к применению соответствующих изобретению соединений в качестве лекарственных средств и к содержащим эти соединения лекарственным формам. Предпочтительно их применение для лечения людей. Они могут вводиться в человеческий организм внутривенно, подкожно, внутримышечно, внутрибрюшинно, через слизистую оболочку носа, ингаляционно, через кожу; при желании их введение можно интенсифицировать с помощью ионофореза или других известных из литературы вспомогательных средств, возможно и пероральное введение.
Для парентерального введения соединения формулы I или их физиологически приемлемые соли переводят в растворы, суспензии или эмульсии с возможным использованием обычных в этой области веществ, таких как растворители, эмульгаторы или другие вспомогательные вещества. В качестве растворителей могут, например, использоваться вода, физиологические растворы поваренной соли или спирты, например этанол, пропандиол или глицерин, растворы сахаров, такие как растворы глюкозы или маннита, но также и смеси различных растворителей.
Кроме того, эти соединения могут применяться и в лекарственных формах для имплантации, например, с полиактидом, полигликолидом или полигидроксимасляной кислотой, а также в лекарственных формах для введения через нос.
Пероральная эффективность соединений общей формулы I может быть показана в следующем далее стандартном опыте:
Торможение вызванного действием NK1 снижения давления крови у анестезированных морских свинок.
Интраперитональным введением пентобарбитала в дозе 50 мг/кг анестезируют морских свинок весом 300-500 г и подключают их к аппарату искусственного дыхания с интенсивностью 10 мл комнатного воздуха на кг веса с частотой 60 вдохов в минуту. Давление крови измеряют непосредственно в шейной артерии. Для внутривенного введения веществ используют канюлю в шейной вене.
Внутривенным введением агониста NK1[ β Ala4, Sar9, Met(O)2]11SP(4-11)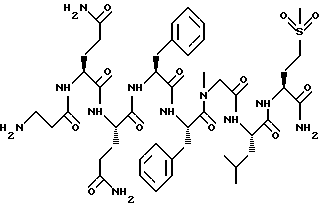
в дозе 0,2 мкмоль/кг вызывают кратковременное снижение давления крови, которое поддерживают повторным введением агониста NK1 с интервалом в 10 минут. Затем через двенадцатиперстную кишку вводят антагонист нейрокинина и вызывают снижение давления крови повторным введением агониста NK1 с интервалом в 10 минут.
Определяют торможение падения давления крови, вызываемого названным выше агонистом NK1, измеряя его до и после введения антагониста нейрокинина.
Для соединения по примеру 5 определено значение ID50, равное 1,4 мг/кг (ID50 - это доза, снимающая вызванное агонистом NK1 падение давления крови на 50%).
Соответствующие изобретению соединения могут быть получены общеизвестными способами.
Получение этих соединений может проводиться различными способами. Два из наиболее часто используемых способов приводятся на схеме, приведенный в конце описания.
Способ А. Получение амида из карбоновой кислоты и амина HN(R5)R4 может осуществляться различными способами. К обычным способам относятся применяемые в химии пептидов реакции сочетания. При этом к реагирующим соединениям добавляют близкие к эквивалентным количества таких вспомогательных реагентов, как тетрафторборат O-бензотриазолилтетраметилурония, дициклогексилкарбодиимид с 1-гидроксибензтриазолом, карбонилдиимидазол и аналогичные соединения. Подходящими растворителями при этом являются диметилформамид, тетрагидрофуран, метиленхлорид, хлороформ, ацетонитрил или другие инертные растворители или их смеси. Оптимальный температурный интервал лежит в пределах между -50oC и +120oC, предпочтительно между 0oC и 40oC.
Можно также, используя известные способы, предварительно перевести карбоновую кислоту действием тионилхлорида, сульфурилхлорида, фосфортрихлорида, фосфорпентахлорида или фосфортрибромида или их смесей в соответствующий галогенангидрид и провести затем его реакцию с амином HN(R5)R4 в таком инертном растворителе, как, например, метиленхлорид, тетрагидрофуран или диоксан при температурах от -50oC до +100oC, обычно между 0oC и 20oC.
Еще один вариант включает на первой стадии превращение карбоновой кислоты известными способами в ее алкиловый эфир (обычно это метиловый эфир), который затем вводят в реакцию с амином HN(R5)R4 в таком инертном растворителе, как, например, диметилформамид, диоксан или тетрагидрофуран. Температура реакций лежит в пределах от 20oC до 150oC, обычно в интервале от 50oC до 120oC. Эту реакцию можно также проводить в аппаратуре под давлением.
Способ Б. В этой последовательности операций полученное известными способами производное α -галоген-арилацетамида вводят в реакцию с амином HN(R1)R2. В результате этой реакции отщепляется галогенводород, и для связывания выделившегося или же избыточного галогенводорода применяют такие неорганические основания, как, например, карбонат калия, бикарбонат натрия или карбонат кальция, а также органические основания, например триэтиламин, основание Гунига, пиридин или 4-диметиламинопиридин, или же реакцию проводят с избытком амина HN(R1)R2. При этом используют диметилформамид, тетрагидрофуран, диоксан или другие инертные растворители. Температура реакций лежит в пределах от 0oC до 100oC, обычно в интервале от 10oC до 80oC.
Способ В. Соответствующие изобретению соединения, структурный элемент R5 которых не означает атом водорода, могут быть получены также следующим образом: сначала по способу А или по способу Б синтезируют соединение, у которого R5 означает атом водорода, и после этого проводят N-алкилирование с введением алкильной, циклоалкильной или карбоксиметильной группы. Для этого соответствующее изобретению соединение с атомом водорода в роли R5 депротонируют действием эквивалентного количества гидрида натрия, амида натрия, гидроксида калия, метилата натрия или другого сильного основания. Для реакции используют безводные инертные растворители, например тетрагидрофуран, диоксан или диэтиловый эфир. После этого медленно прибавляют соответствующее алкилирующее средство в виде соответствующего галогенида, тозилата или мезилата. Взаимодействие проводят в температурном интервале от -50oC до +100oC, обычно в пределах от 0oC до +50oC. Этот способ подробно описан в примере 33.
Примеры
Пример 1.
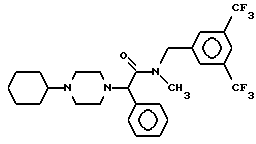
Первая стадия. В 150 мл безводного диметилформамида растворяют 2,2 г 1-циклогексилпиперазина, добавляют 2 г карбоната калия, 20 минут перемешивают при комнатной температуре и охлаждают до температуры 5oC. Затем прибавляют 2,7 г метилового эфира (R,S)- α -бромфенилуксусной кислоты и оставляют образующуюся суспензию на ночь при перемешивании при комнатной температуре. Осадок отфильтровывают и упаривают фильтрат, остаток растворяют в этилацетате и экстрагирут дважды 10%-ным раствором бикарбоната калия и один раз насыщенным раствором хлорида натрия. Органическую фазу сушат сульфатом натрия, фильтруют и упаривают. Получают 3,7 г метилового эфира (R,S)-1-циклогексил-4-пиперазино-фенилуксусной кислоты в виде желтого масла.
Выход около 100%.
Вторая стадия. В 10 мл метанола растворяют 2,3 г полученного на первой стадии продукта, прибавляют 14 мл 1н. раствора гидроксида натрия и оставляют образующуюся эмульсию при перемешивании при комнатной температуре на ночь. Затем прозрачный раствор нейтрализуют добавлением 14 мл 1н. раствора соляной кислоты, упаривают досуха, экстрагируют остаток изопропанолом, отфильтровывают твердое вещество и упаривают фильтрат. Остаток снова растирают с изопропанолом, отсасывают твердое вещество и объединяют его с полученным ранее осадком. Таким образом получают 1,6 г (R,S)-1-циклогексил-4- пиперазино-фенилуксусной кислоты в виде твердого вещества.
Выход 75%.
Третья стадия. В 60 мл смеси тетрагидрофурана и метиленхлорида (1:1) суспендируют 0,6 г полученного на второй стадии продукта, 0,48 г 3,5-бис-(трифторметил)-бензиламина и 0,32 г 1-гидроксибензтриазола, добавляют 0,7 мл основания Гунига до значения pH 8,5, затем 0,77 г тетрафторбората O-бензотриазолил- тетраметилурония и оставляют при перемешивании на ночь при комнатной температуре. Прозрачную реакционную массу упаривают в вакууме, остаток растворяют в метиленхлориде и два раза встряхивают с 10%-ным раствором бисульфата калия, один раз с насыщенным раствором хлорида натрия, два раза с 10%-ным раствором бикарбоната калия и один раз с насыщенным раствором хлорида натрия. Органическую фазу сушат над сульфатом натрия, фильтруют и упаривают с получением кристаллического продукта. Получают 0,685 г N-(3,5-бис-трифторметилбензил)амида (R, S)-1-циклогексил-4-пиперазино-фенилуксусной кислоты в виде желтоватого твердого вещества.
Выход 64%, т. пл. 124-129oC, масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 528,2.
Пример 2.
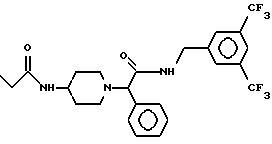
Первая стадия. В 30 мл безводного метиленхлорида растворяют 0,49 г 3,5-бис-(трифторметил)-бензиламина, прибавляют 0,3 мл триэтиламина, охлаждают смесь в бане со льдом и в течение 20 минут прибавляют по каплям раствор 0,46 г хлорангидрида (R,S)- α-бромфенилуксусной кислоты в 10 мл метиленхлорида. Реакционную массу оставляют на два дня при комнатной температуре, отгоняют растворитель, растирают твердый остаток с серным эфиром, отсасывают и упаривают фильтрат. В результате получают N(бис- трифторметилбензил)-амид α -бромфенилуксусной кислоты в виде светло-бежевого твердого вещества.
Выход 43,5%.
Вторая стадия. В 30 мл безводного диметилформамида растворяют 0,21 г гидрохлорида 4-пропиониламино-пиперидина, прибавляют 0,33 г карбоната калия и 30 минут перемешивают при комнатной температуре. К полученной смеси в течение 20 минут прибавляют по каплям раствор 0,68 г полученного на первой стадии продукта в 10 мл диметилформамида и оставляют при перемешивании на ночь при комнатной температуре. Суспензию фильтруют, фильтрат упаривают, полученный в виде масла остаток растворяют в этилацетате и экстрагируют два раза 10%-ным раствором бикарбоната калия и один раз насыщенным раствором хлорида натрия. Органическую фазу сушат над сульфатом натрия, фильтруют, фильтрат упаривают, а полученный частично твердый остаток растирают с диэтиловым эфиром и отсасывают. В результате получают 0,33 г N-(3,5-бис-трифторметил-бензил)-амида (R, S)-4-пропиониламино-1-пиперидино-фенилуксусной кислоты в виде белого твердого вещества.
Выход 64%, т. пл. 189-191oC, масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 516,4.
Аналогично могут быть получены другие соответствующие изобретению соединения, например, приведенные далее:
Пример 3.
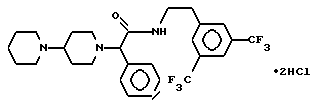
Т. пл. 235-238oC, масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 542,2.
Пример 4.
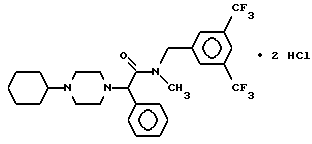
Т. пл. > 240oC (разл.), масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 542,3.
Пример 5.
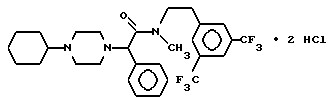
Т. пл. 158-164oC, масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 556,4.
Пример 6.
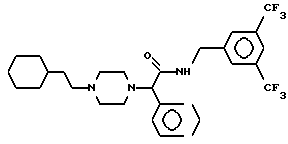
Т. пл. 97-99oC, масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 556,3.
Пример 7.

Т. пл. > 240oC (разл.), масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 528,4.
Пример 8.

Т. пл. 102-105oC, масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 640,3.
Пример 9.
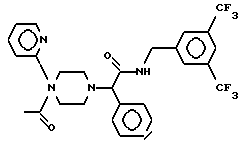
Т. пл. 141-149oC, масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 579,2.
Пример 10.
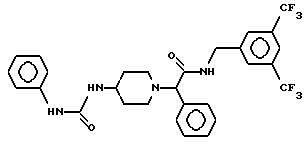
Т. пл. 218-223oC, масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 579,3.
Пример 11.
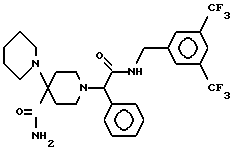
Т. пл. > 220oC (разл.), масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 571,3.
Пример 12.

Т. пл. 205-210oC, масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 591,3.
Пример 13.

Т. пл. 87-95oC, масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 571,2.
Пример 14.

Т. пл. 164-166oC, масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 537,3.
Пример 15.

Т. пл. 208-210oC, масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 578,3.
Пример 16
Т. пл. 110-115oC, масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 542,3.
Пример 17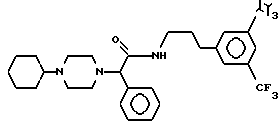
Т. пл. 118-123oC, масс-спектр при бомбардировке быстрыми атомами: (M+H)+ = 556,3.
Пример 18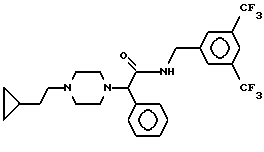
Т. пл. 134-136oC. масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 514,3.
Пример 19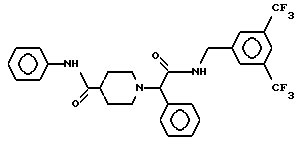
Т. пл. > 240oC (разл.), масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 564.
Пример 20.
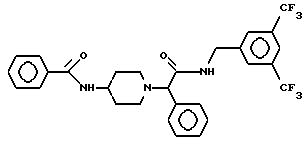
Т. пл. 180-185oC, масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 564,3.
Пример 21.
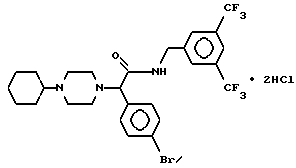
Т. пл. 228-232oC, масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 606/608.
Пример 22.
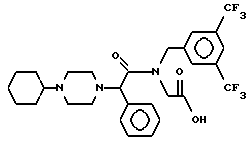
Т. пл. 70-73oC, масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 586.
Пример 23.
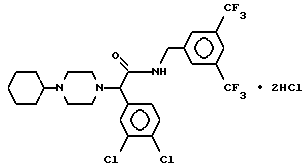
Т. пл. 248-254oC, масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 596/598/600.
Пример 24.
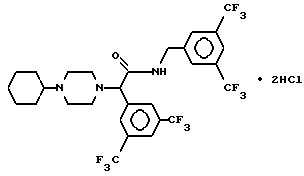
Т. пл. 210oC, масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 664,1.
Пример 25.
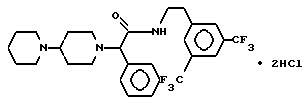
Т. пл. 192-199oC, масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 542,3.
Пример 26.
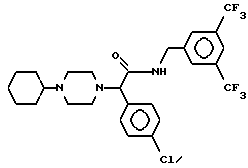
Т. пл. 112-118oC, масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 562/564.
Пример 27.
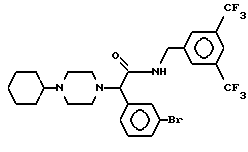
Т. пл. 124-127oC, масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 606/608.
Пример 28.
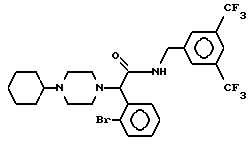
Т. пл. 118-120oC, масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 606/608.
Пример 29.

Т. пл. 120-122oC, масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 562/564.
Пример 30.
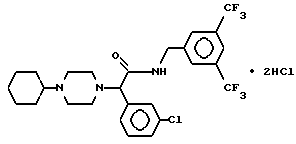
Т. пл. > 240oC, масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 562/564.
Пример 31.
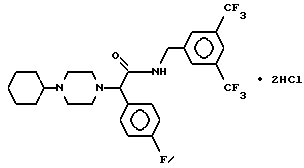
Т. пл. > 240oC, масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 546,3.
Пример 32.
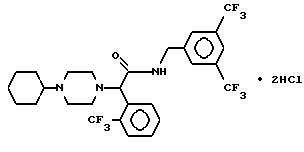
Т.пл. 125-130oC (разл.), масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 610,4.
Пример 33.

С помощью бикарбоната калия переводят в соответствующее свободное основание 0,3 г полученного по примеру 25 соединения, высушивают его и растворяют в 5 мл безводного тетрагидрофурана. К раствору добавляют 34 мг 60%-ного гидрида натрия в виде суспензии в масле, 1,5 часа перемешивают при комнатной температуре, после этого прибавляют 0,1 г метилиодида и оставляют на ночь при перемешивании. К реакционной массе прибавляют 2 мл смеси (1:1) тетрагидрофурана и воды, затем прибавляют 25 мл воды и трижды экстрагируют серным эфиром. Объединенные эфирные экстракты сушат над сульфатом натрия и упаривают в вакууме. В результате получают 170 мг целевого соединения в виде свободного основания (масло). Добавлением раствора избытка хлористого водорода в эфире его переводят в дигидрохлорид, выпадающий в виде желтых кристаллов.
Выход 113 мг (36%).
Т. пл. > 240oC, масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 556,4.
Пример 34.
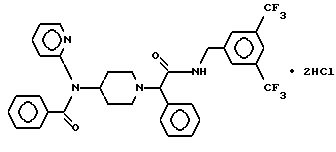
Т. пл. 145-151oC, масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 641,3.
Пример 35.
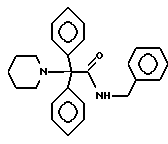
Т.пл. 175-176,5oC
Пример 36.
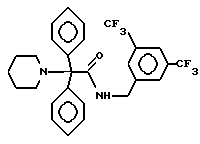
Т.пл. 157-158oC
Пример 37.
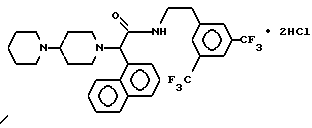
Т. пл. 155-172oC, масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 592,2.
Пример 38.
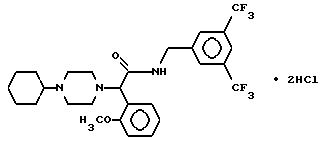
Т. пл. 142-150oC, масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 558,2.
Пример 39.
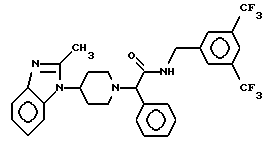
Т. пл. 107-111oC, масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 575,6.
Пример 40.
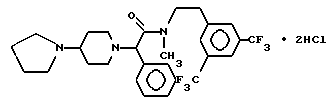
Т.пл. > 230oC
Пример 41.
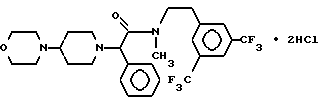
Т.пл. > 230oC
Пример 42.
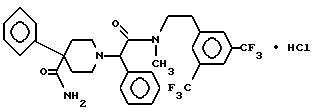
Т. пл. 127-137oC, масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 592.
Пример 43.
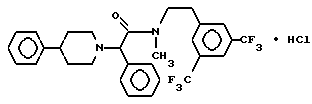
Т. пл. 106-110oC, масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 549,4.
Пример 44.
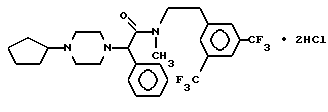
Т. пл. 133-143oC, масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 542,3.
Пример 45.
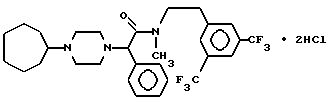
Т. пл. 110-120oC, масс-спектр при бомбардировке быстрыми атомами: (М+H)+ = 570,4.
Пример 46.

Т.пл. 212-216oC (разл.), масс-спектр при бомбардировке быстрыми атомами: (М+Н)+ = 624,3/626,3/628,3.
Пример 47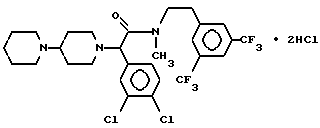
Т. пл. 244-246oC (разл), масс-спектр при бомбардировке быстрыми атомами: (M+H)+ = 624,1/626,2/628.
Пример 48
Т. пл. 113-123oC (разл), масс-спектр при бомбардировке быстрыми атомами: (M+H)+ = 550,3.
Пример 49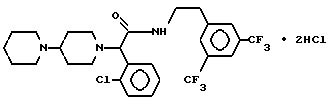
Т.пл. 195-205oC (разл).
Пример 50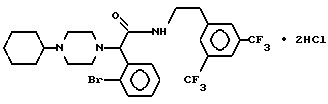
Т. пл. 210-218oC, масс-спектр при бомбардировке быстрыми атомами: (M+H)+ = 620/622.
Пример 51.
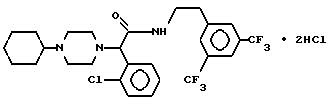
Т. пл. 215-224oC, масс-спектр при бомбардировке быстрыми атомами: (M+H)+ = 576/578.
Пример 52.

Т. пл. 85-92oC, масс-спектр при бомбардировке быстрыми атомами: (M+H)+ = 572,5.
Пример 53.
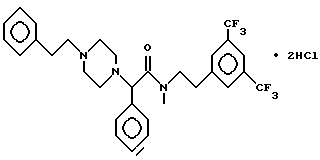
т. пл. 148-156oC, масс-спектр при бомбардировке быстрыми атомами: (M+H)+ = 578,4.
Пример 54.
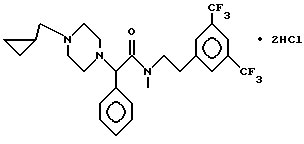
Т. пл. 113-117oC (разл), масс-спектр при бомбардировке быстрыми атомами: (M+H)+ = 528,5.
Пример 55.
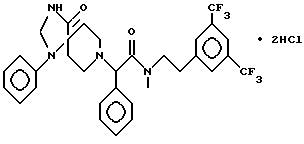
Т. пл. 265-268oC (разл), масс-спектр при бомбардировке быстрыми атомами: (M+H)+ = 619,3.
Пример 56.

Т.пл. 236-238oC (разл.), масс-спектр при бомбардировке быстрыми атомами: (M+H)+ = 528,3.
Пример 57.
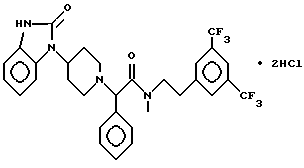
Т. пл. 177-187oC, масс-спектр при бомбардировке быстрыми атомами: (M+H)+ = 605,3.
Пример 58.

Т. пл. 123-133oC, (разл.), масс-спектр при бомбардировке быстрыми атомами: (M+H)+ = 616,3
Пример 59.
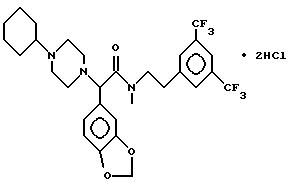
Т. пл. 87-97oC, масс-спектр при бомбардировке быстрыми атомами: (M+H)+ = 600,2
Пример 60.
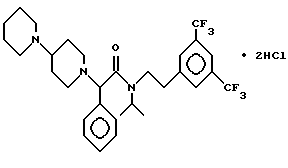
Т.пл. > 230oC.
Пример 61.
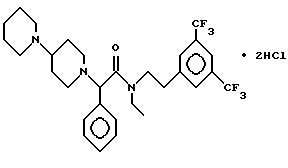
Т.пл. > 230oC.
Пример 62.
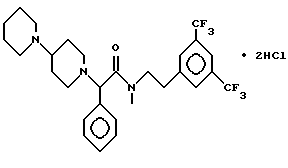
Т.пл. > 230oC.
Пример 63.

Т. пл. 91-98oC, масс-спектр при бомбардировке быстрыми атомами: (M+H)+ = 574,4.
Пример 64.
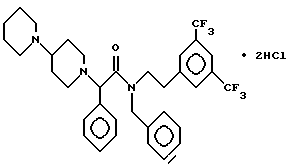
Т.пл. 234-236oC.
Пример 65.
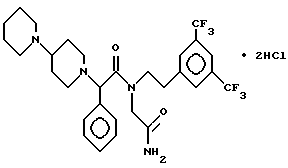
Т.пл. 195-198oC.
Пример 66.
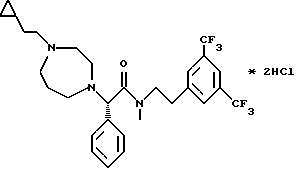
Т.пл. 129-134oC.
Пример 67.
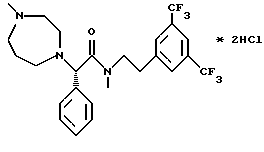
Т.пл. 138-148oC.
Пример 68.
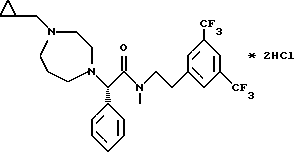
Т.пл. 75-80oC.
Пример 69.
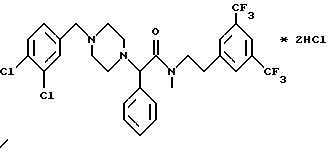
Т.пл. 168-173oC.
Пример 70.
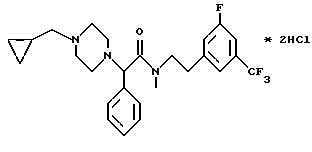
Т.пл. 223-225oC.
Пример 71.
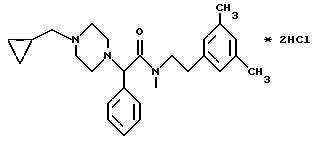
Т.пл. 224-227oC.
Пример 72.
Т.пл. 117-124oC.
Пример 73.

Т.пл. 160-161oC
Примеры фармацевтической композиции
Раствор для инъекций
200 мг Активное вещество*,
1,2 мг монокалиевая соль фосфорной кислоты (KH2PO4),}(буфер)
0,2 мг динатриевая соль фосфорной кислоты (Na2HPO4•2H2O),
94 мг хлорид натрия или} (изотонические составляющие),
520 мг глюкоза
4 мг альбумин (для защиты от протеаз),
q.s раствор гидроксида натрия,} до значения pH 6
q.s. соляная кислота,
до 10 мл вода для инъекций
Раствор для инъекций
200 мг Активное вещество*,
94 мг хлорид натрия или
520 мг глюкоза,
4 мг альбумин,
q.s. раствор гидроксида натрия,} до значения pH 9
q.s соляная кислота,
до 10 мл вода для инъекций.
Лиофилизат
200 мг Активное вещество*,
520 мг маннит (изотоническая и структурообразная добавка),
4 мг альбумин.
Растворитель 1 для лиофилизата
10 мл воды для инъекций.
Растворитель 2 для лиофилизата
20 мг полисорбата® 80 = твина® 80 (поверхностно-активное вещество)
10 мл воды для инъекций.
* Активное вещество: соответствующее изобретению соединение, например, по примерам от 1 до 78.
Дозировка для человека весом 67 кг от 1 до 500 мг.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ КСАНТИНА И ИХ ФАРМАКОЛОГИЧЕСКИ ПЕРЕНОСИМЫЕ СОЛИ | 1993 |
|
RU2138500C1 |
| ПРОИЗВОДНЫЕ ФЕНИЛАМИДИНА | 1996 |
|
RU2184726C2 |
| ПРОИЗВОДНЫЕ ПИПЕКОЛИНОВОЙ КИСЛОТЫ И ИХ СОЛИ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1993 |
|
RU2140911C1 |
| ПРОИЗВОДНЫЕ ОКСАДИАЗОЛА | 1997 |
|
RU2182905C2 |
| ПРИМЕНЕНИЕ КАРБОЦИКЛИЧЕСКИ И ГЕТЕРОЦИКЛИЧЕСКИ АНЕЛЛИРОВАННЫХ ДИГИДРОПИРИДИНОВ И ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫХ СОЛЕЙ В КАЧЕСТВЕ БЛОКАТОРА НЕСЕЛЕКТИВНЫХ КАНАЛОВ КАТИОНОВ ПРИ ЗАЩИТЕ ГОЛОВНОГО МОЗГА И ЛЕЧЕНИИ ХРОНИЧЕСКОЙ БРОНХИАЛЬНОЙ АСТМЫ | 1991 |
|
RU2149000C1 |
| ПРОИЗВОДНЫЕ ФЕНИЛАМИНОИМИДАЗОЛИНА ИЛИ ФЕНИЛИМИНОИМИДАЗОЛИДИНА, ОБЛАДАЮЩИЕ СВОЙСТВАМИ АГОНИСТА α-АДРЕНОРЕЦЕПТОРОВ, И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1996 |
|
RU2230061C2 |
| ПРОИЗВОДНЫЕ БЕНЗОИЛГУАНИДИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1997 |
|
RU2181720C2 |
| 4-АМИНОПИРИДИНЫ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1994 |
|
RU2126388C1 |
| ПРОИЗВОДНЫЕ ИЗОХИНОЛИНА И ИХ СОЛИ | 1994 |
|
RU2136664C1 |
| СПОСОБ ПОЛУЧЕНИЯ АРОМАТИЧЕСКИХ ПРОИЗВОДНЫХ ИЛИ ИХ СОЛЕЙ С ОРГАНИЧЕСКИМИ ИЛИ НЕОРГАНИЧЕСКИМИ КИСЛОТАМИ ИЛИ ИХ РАЦЕМАТОВ | 1990 |
|
RU2084453C1 |

Описываются новые производные арилглицинамидов общей формулы I или их фармацевтически приемлемые соли, где Аr означает незамещенный или от одного до пяти раз замещенный фенил или же незамещенный или от одного до двух раз замещенный нафтил, причем заместители фенильного и нафтильного фрагментов независимо друг от друга представлены атомами галогена (фтора, хлора, брома, иода), гидроксильной группой, алкилом с числом атомов углерода от одного до четырех, алкоксилом с числом атомов углерода от одного до четырех, трифторметильной, трифторметоксильной группой или группой -NR9R10, в которой R9 и R10 независимо друг от друга означают атом водорода, метил, Ar может означать также фенил, замещенный -O(СН2)O- или -O(CH2)2O-группой; R1 и R2 вместе с атомом азота, с которым они связаны, образуют цикл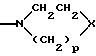
в котором р означает числа 2 или 3, Х означает группу N(CH2)nR6 или CR7R8, где n означает числа 0,1 или 2, R6 означает циклоалкил с числом атомов углерода от трех до семи, фенил или нафтил, причем фенил может быть от одного до трех раз замещен атомами галогена (фтора, хлора, брома, иода), R7 и R8 имеют одно из следующих значений: a) R7 и R8 означают атом водорода, если R3 означает фенил, б) R7 означает фенил, пиперидинил, 1-метил-пиперидинил или группы следующих формул: (а) в тех случаях, когда R8 означает атом водорода, карбамоил, ацетиламин, ацетил-N-метил-амин или нитрил, в) R7 и R8 вместе образуют остаток (в), R3 означает атом водорода или фенил, R4 означает фенилалкил или нафтилалкил с числом атомов углерода в алкильных фрагментах от одного до четырех, причем фенил может быть от одного до трех раз замещен атомами галогена (фтора, хлора, брома, иода), алкилом с числом атомов углерода от одного до четырех, алкоксильной группой с числом атомов углерода от одного до четырех или трифторметилом, R5 означает атом водорода, алкил с числом атомов углерода от одного до четырех, циклоалкил с числом атомов углерода от трех до шести, карбоксиметил или карбамоилметил. Соединения проявляют активность антагониста нейрокинина. Описывается также фармацевтическая композиция, содержащая эти соединения. 2 с. и 16 з.п. ф-лы.
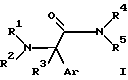

или их фармацевтически приемлемые соли,
где Ar означает незамещенный или от одного до пяти раз замещенный фенил, или же незамещенный, или от одного до двух раз замещенный нафтил, причем заместители фенильного или нафтильного фрагментов независимо друг от друга представлены атомами галогена (фтора, хлора, брома, иода), гидроксильной группой, алкилом с числом атомов углерода от одного до четырех, алкоксилом с числом атомов углерода от одного до четырех, трифторметильной, трифторметоксильной группой или группой -NR9R10, в которой R9 и R10 независимо друг от друга означают атом водорода, метил, Ar может означать также фенил, замещенный -O(CH2)O- или -O(CH2)2O-группой;
R1 и R2 вместе с атомом азота, с которым они связаны, образуют цикл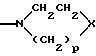
в котором p означает числа 2 или 3;
Х означает группу N(CH2)nR6 или CR7R8, где n означает числа 0, 1 или 2;
R6 означает циклоалкил с числом атомов углерода от трех до семи, фенил или нафтил, причем фенил может быть от одного до трех раз замещен атомами галогена (фтора, хлора, брома, иода);
R7 и R8 имеют одно из следующих значений:
а) R7 и R8 означают атом водорода, если R3 означает фенил,
б) R7 означает фенил, пиперидинил, 1-метилпиперидинил или группы следующих формул: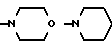
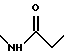
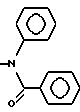

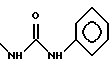
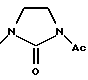

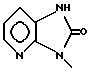
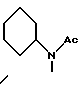
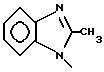
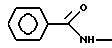
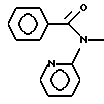
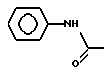
или
в тех случаях, когда R8 означает атом водорода, карбамоил, ацетиламин, ацетил-N-метиламин или нитрил,
в) R7 и R8 вместе образуют остаток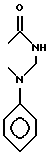
R3 означает атом водорода или фенил;
R4 означает фенилалкил или нафтилалкил с числом атомов углерода в алкильных фрагментах от одного до четырех, причем фенил может быть от одного до трех раз замещен атомами галогена (фтора, хлора, брома, иода), алкилом с числом атомов углерода от одного до четырех, алкоксильной группой с числом атомов углерода от одного до четырех или трифторметилом;
R5 означает атом водорода, алкил с числом атомов углерода от одного до четырех, циклоалкил с числом атомов углерода от трех до шести, карбоксиметил или карбамоилметил.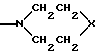
где Х означает группу N(CH2)nR6 или CR7R8, где n, R6, R7 и R8 имеют определенное в п.1 значение.
а) R7 и R8 означают атом водорода, если R3 представлен фенилом,
б) R7 означает фенил, пиперидинил, группы следующих формул
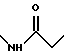
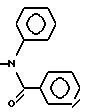
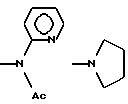

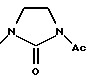
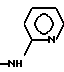
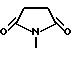

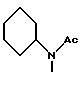
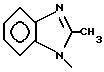
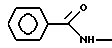
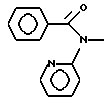

или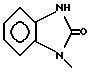
если R8 означает атом водорода, карбамоил, ацетиламин, ацетил-N-метиламин или нитрил или
в) R7 и R8 вместе образуют остаток
7. Соединение по п.6, у которого R7 и R8 имеют одно из следующих значений:
а) R7 и R8 означают атом водорода, если R3 представлен фенилом,
б) R7 означает фенил или группы следующих формул: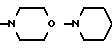


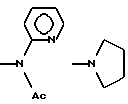
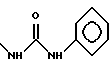

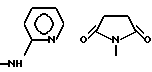
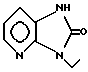

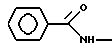
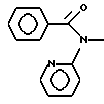
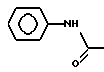
или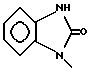
если R8 означает атом водорода, карбамоил или нитрил, или
в) R7 и R8 вместе образуют остаток
8. Соединение по п.7, у которого R7 означает фенил, группы
или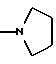
если R8 означает атом водорода или нитрил.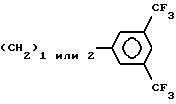
R5 означает атом водорода или метил.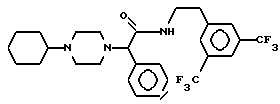
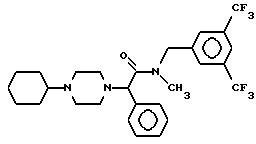
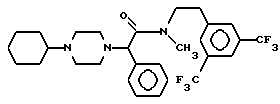
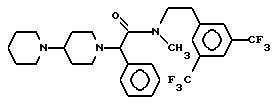
или
18. Фармацевтическая композиция, проявляющая активность в качестве антагониста нейрокинина, отличающаяся тем, что она содержит соединение по одному из пп.1 - 17.
Приоритет по признакам:
14.04.95 - все признаки изобретения за исключением следующих: Ar - фенил, замещенный группой -OCH2O- или -O(CH2)2O-; p = 3, R7 - фенил, пиперидинил, 1-метилпиперидинил; R8 - циано; R5-группа-CH2C(O)NH2;
25.05.95 - Ar - фенил, замещенный группой -OCH2O- или -O(CH2)2O-; p = 3, R7 - фенил, пиперидинил, 1-метилпиперидинил; R8 - циано; R5-группа-CH2C(O)NH2.
| Экономайзер | 0 |
|
SU94A1 |
| SU 1227109 A, 23.04.1986 | |||
| Экономайзер | 0 |
|
SU94A1 |
Авторы
Даты
2001-05-27—Публикация
1996-04-11—Подача