Изобретение относится к новым анеллированным производным дигидропиридина, обладающим биологической активностью, более конкретно к производным изохинолина и их солям.
Известны производные изохинолина и их соли, обладающие кардиозащитной активностью и защищающей головной мозг активностью (см. заявку ЕР N 0288048 A2, кл. C 07 D 217/14, C 07 D 217/16, C 07 D 495/05, A 61 К 31/44, опубл. 26.10.1988 г.).
Задачей изобретения является расширение ассортимента производных изохинолина, обладающих ценными биологическими свойствами.
Поставленная задача решается предлагаемыми производными изохинолина общей формулы (I)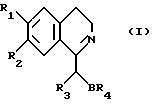
в которой R1 и R2 независимы друг от друга и означают гидроксил, алкоксил с 1 - 4 атомами углерода, галоген, алкил с 1-4 атомами углерода, бензилокси; B - группа -O-, -S- или -CHR5, в которой R5 означает водород или алкил с 1 - 6 атомами углерода; R3 - 2- или 3-тиенил, циклоалкил с 4-7 атомами углерода, или группа формулы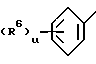
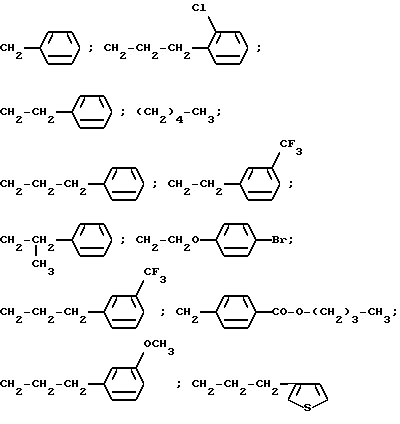
где R6 означает галоген или алкоксил с 1 - 4 атомами углерода, u - 0, 1 или 2; R4 - алкенил с 3-6 атомами углерода, незамещенный или замещенный фенилом, алкил с 1-13 атомами углерода, возможно замещенный заместителем из группы, включающей тиенил, адамантил, циклогексил, бензил-окси-группу, фенокси-группу и фенил, причем последний или содержащийся в фенокси-группе фенил может быть моно-, ди- или тризамещенным остатком из группы, включающей гидроксил, алкоксил с 1 - 4 атомами углерода, галоген, трифторметил, двуокись азота и алкил с 1 - 4 атомами углерода, или двумя незамещенными фенильными группами, группы формул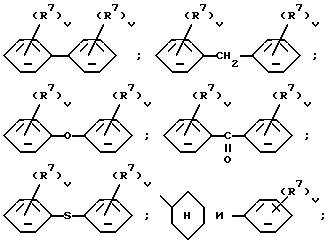
где R7 означает галоген, а трифторметил, двуокись азота, а v - 0, 1, 2, или их солями с физиологически переносимыми кислотами или комплексообразователями.
Соединения формулы (I) образуют таутомеры формулы (II)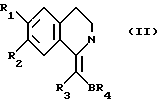
Таутомеры можно разделять по известным методам, например, путем хроматографии на колонке или избирательного восстановления (бораном натрия или каталитического восстановления).
Соединения формулы (II) могут иметься в цис- или транс-форме;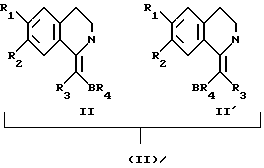
В случае, если структура соединения не указана, то формула (I) включает также соединения структуры II.
В первую группу предпочтительных производных изохинолина общей формулы (I) входят соединения, у которых R2 означает группу формул
Во вторую группу предпочтительных производных изохинолина общей формулы (I) входят соединения, у которых R1 и R2 каждый означает метоксигруппу.
В третью группу предпочтительных производных изохинолина общей формулы (I) входят соединения, у которых R3 означает фенил или циклогексил.
В четвертую группу предпочтительных производных изохинолина общей формулы (I) входят соединения, у которых B означает O или CH2.
Соединения формулы (I) можно получать известными приемами. Так, например, в присутствии агента конденсации соединение общей формулы (IV)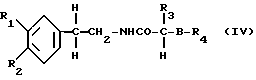
в которой R1-R4 имеют вышеуказанные значения, можно циклизировать до соответствующих соединений.
В качестве агента конденсации для проведения этого способа пригодны сильные люисовские кислоты, такие, как, например, хлорокись фосфора, пентахлорид фосфора, трихлорид фосфора, полупятиокись фосфора, тетрахлорид титана, трифторид бора, тетрахлорид олова, а также неорганические кислоты, такие, как, например, полифосфорная кислота, серная кислота, фторсульфокислота и фтористоводородная кислота, или смеси агентов конденсации, такие, как, например, смесь хлорокиси фосфора и пентахлорида фосфора, или смесь полупятиокиси фосфора и алкилсульфокислоты с 1 - 4 атомами углерода, содержащая, например, примерно 10 вес,% P2O5.
Циклизацию можно проводить в присутствии растворителя. Пригодны все инертные растворители, имеющие достаточную способность к растворению реагентов и достаточно высокую точку кипения, такие, как, например, бензол, алкилбензолы (например, толуол, ксилол), хлорбензолы, хлороформ, ацетонитрил, декалин. Предпочтительным вариантом способа является использование в качестве агента конденсации смеси хлорокиси фосфора и ацетонитрила или смеси алкилсульфокислоты с 1-4 атомами углерода и полупятиокиси фосфора, без добавки растворителей.
Предпочтительно циклизация осуществляется с использованием смеси хлорокиси фосфора и ацетонитрила или в сложных случаях с использованием смеси полупятиокиси фосфора и алкилсульфокислоты с 1-4 атомами углерода (предпочтительно метансульфокислоты).
Реакцию можно осуществлять в широких пределах температуры, предпочтительно при температуре от 50oC до температуры кипения реакционной смеси.
В зависимости от исходного соединения формулы IV время реакции составляет 2-15 часов.
Исходное соединение формулы (IV) можно также получать известными приемами.
Соединения формулы (I) представляют собой основания, их можно переводить обычным образом при использовании неорганических или органических кислот, а также солеобразователей и комплексообразователей веществ в любые физиологически переносимые аддукты (соли).
Пригодными для солеобразования кислотами являются, например, соляная кислота, бромистоводородная кислота, йодистоводородная кислота, фтористводородная кислота, серная кислота, фосфорная кислота, азотная кислота, уксусная кислота, пропионовая кислота, масляная кислота, капроновая кислота, валериановая кислота, щавелевая кислота, малоновая кислота, янтарная кислота, малеиновая кислота, фумаровая кислота, молочная кислота, винная кислота, лимонная кислота, яблочная кислота, бензойная кислота, п.-гидроксибензойная кислота, фталевая кислота, коричная кислота, салициловая кислота, аскорбиновая кислота, метансульфокислота и тому подобные кислоты.
Соединения формулы (I) можно давать орально, парентерально или локально. Желаемая терапевтическая доза зависит от назначения и конкретного препарата. Ее можно определять экспериментальным путем. Пригодными препаратами являются, например, таблетки, капсулы, суппозитории, растворы, соки, эмульсии, аэрозоль или диспергируемые порошки. Соответствующие таблетки можно получать, например, путем смешивания активного вещества или активных веществ с известными вспомогательными веществами, например, инертными разбавителями, такими, как, например, карбонат кальция, фосфат кальция или лактоза, разрыхлителями, такими, как кукурузный крахмал или альгиновая кислота, связующими, такими, как крахмал или желатина, смазками, такими, как стеарат магния или тальк, и/или веществами для получения препаратов продленного действия, такими, как карбоксиполиметилен, карбоксиметилцеллюлоза, ацетофталат целлюлозы или поливинилацетат. Таблетки могут состоять из нескольких слоев.
Получение производных изохинолина формулы (I) поясняется нижеследующими примерами.
Пример 1.
Амид N-[2-(3.4-диметоксифенил)]-O-(3-фенилпропил)фенилуксусной кислоты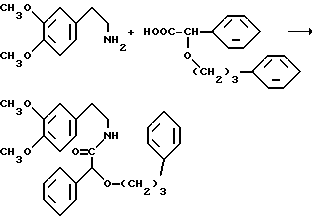
30,3 г (113 ммоль) O-(3-фенилпропил)-фенилуксусной кислоты растворяют в 250 мл абс. тетрагидрофурана, к смеси добавляют 18,14 г (112 ммоль) карбонилдиимидазола, затем перемешивают в течение 2 часов при комнатной температуре. К этому реакционному раствору при охлаждении льдом добавляют каплями 20,27 г (112 ммоль) 2-(3,4-диметоксифенил)этиламина в 50 мл абс. тетрагидрофурана, после чего перемешивают при комнатной температуре в течение дальнейших 15 часов. Затем растворитель отгоняют в вакууме, остаток растворяют в 250 мл сложного этилового эфира уксусной кислоты, промывают 3 раза 1 н. хлористоводородной кислотой, каждый раз 100 мл, 2 раза насыщенным раствором бикарбоната натрия, каждый раз 75 мл, и 2 раза насыщенным раствором хлористого натрия, каждый раз 50 мл. Раствор сложного этилового эфира уксусной кислоты сушат над сульфатом магния и сгущают в вакууме.
Получают 44,28 г (91,3% теории) маслянистого продукта, который без очистки можно подвергать дальнейшей переработке.
Вариант:
Амид N-[2-(3,4-диметоксифенил)этил]-миндальной кислоты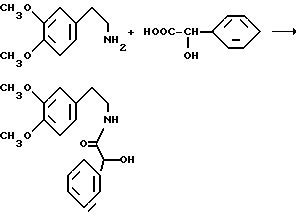
33,2 г (0,2 моль) сложного метилового эфира миндальной кислоты и 72 г (0,4 моль) 2-(3,4-диметоксифенил)-этиламина в атмосфере азота и при перемешивании в течение 5 часов нагревают с обратным холодильником до 160-165oC (для удаления выделяющегося метанола). Охладившийся остаток растворяют в 300 мл сложного этилового эфира уксусной кислоты, промывают 2 раза 2 н. хлористоводородной кислотой, каждый раз 100 мл, и раз насыщенным раствором бикарбоната натрия и насыщенным раствором хлористого натрия и сушат над сульфатом магния, затем растворитель отгоняют. Кристаллический остаток растворяют в 200 мл сложного этилового эфира уксусной кислоты, а продукт реакции выделяют 160 мл н. гексана.
Выход: 51,2 г (80,95% теории), т.пл.: 89 - 91oC.
Амид N-[2-(3,4-диметоксифенил)этил]-O-метилминдальной кислоты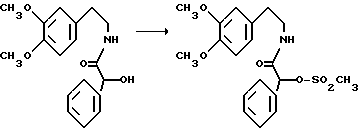
К раствору 19,6 г (62,2 ммоль) амида N-[2-(3,4-диметоксифенил)этил] метилминдальной кислоты в 60 мл абс. пиридина каплями добавляют при перемешивании и охлаждении 7.8 (69 ммоль) хлорида метансульфокислоты. причем температуру реакционного раствора держат при -15 до -5oC. После 5 часов перемешивания при комнатной температуре прибавляют 200 г льда и при охлаждении льдом подкисляют 180 мл 4 н. хлористоводородной кислоты. Кислый раствор 2 раза экстрагируют путем встряхивания, каждый раз 400 мл сложного этилового эфира уксусной кислоты, и органическую фазу промывают 2 раза водой, каждый раз 50 мл, и 2 раза насыщенным раствором хлористого натрия, затем раствор сушат над сульфатом магния, и растворитель отгоняют в вакууме. Кристаллический остаток переосаждают 100 мл сложного этилового эфира уксусной кислоты и 50 мл н.-гептана, при этом получают 16,3 г (66,6% теории) целевого продукта, т.пл.: 89 - 90oC.
Амид N-[2-(3,4-диметоксифенил)этил]-O-(3-фенилпропил)фенилуксусной кислоты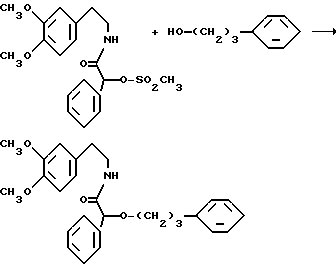
1,95 г (5 ммоль) амида N-[2-(3,4-диметоксифенил)этил]метилминдальной кислоты растворяют в 3,4 r (24 ммоль) 3-фенил-1-пропанола и при перемешивании течение 30 минут нагревают до 100oC. После охлаждения до комнатной температуры реакционный продукт растворяют в 100 мл сложного этилового эфира уксусной кислоты, промывают 2 раза насыщенным раствором бикарбоната натрия и раз раствором хлористого натрия и сушат над сульфатом магния, растворитель отгоняют в вакууме.
Маслянистый продукт реакции очищают хроматографическим путем на колонке, содержащей силикагель, с применением в качестве элюента смеси сложного этилового эфира уксусной кислоты и н.-гептана в соотношении 1:1. При этом получают 1,54 г (71,5% теории) диэтилового эфира в качестве масла.
(R, S)-3,4-дигидро-6,7-диметоксиизохинолин-1-ил)-2-фенил-2-(3- фенилпропил)-диэтиловый эфир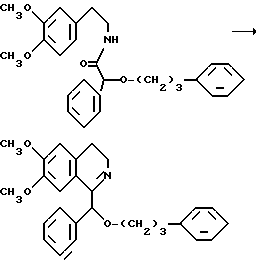
Раствор 44,28 г (102,3 ммоль) амида N-[2,3,4-диметилфенил)этил]- O-(3-фенилпропил)фенилуксусной кислоты и 46,93 г (307 ммоль) хлорокиси фосфора в 300 мл ацетонитрила в течение часа нагревают с обратным холодильником в атмосфере азота до кипения. После охлаждения до комнатной температуры реакционную смесь растворяют в 1 л сложного этилового эфира уксусной кислоты, промывают 2 раза ледяной водой, каждый раз 150 мл, 3 раза насыщенным раствором бикарбоната натрия, каждый раз 150 мл, и 2 раза насыщенным раствором хлористого натрия, каждый раз 100 мл, затем сушат над сульфатом магния, растворитель отгоняют в вакууме. Остаток растворяют в 110 мл ацетона и при перемешивании и охлаждении льдом подкисляют эфирной хлористоводородной кислотой, при этом выкристаллизовываются 17,6 r (38,68% теории) целевого продукта в качестве гидрохлорида, т. пл.: 176 - 178oC.
Пример 2.
Амид N-[2-(3,4-диметоксифенил)этил]-S-(фенилпропил)фенилуксусной кислоты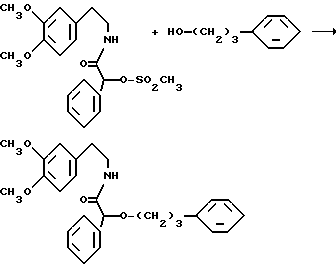
3,93 г (10 ммоль) амида N-[2-(3,4-диметоксифенил)этил]-O- метилминдальной кислоты и 4,65 г (30 ммоль) 3-фенил-н.-пропилмеркаптана в течение 30 минут нагревают при перемешивании до 100oC. Охлажденный продукт реакции растворяют в 100 мл сложного этилового эфира уксусной кислоты, 2 раза промывают насыщенным раствором бикарбоната натрия, каждый раз 20 мл, и раз - насыщенным раствором хлористого натрия. После сушки над сульфатом магния растворитель отгоняют в вакууме. Маслянистый остаток очищают хроматографическим путем на колонке, содержащей силикагель, с применением в качестве элюента смеси сложного этилового эфира уксусной кислоты и н.-гептана в соотношении 1:1 (элюат). Выход: 2.55 г (56,8% теории).
(R,S)-(3,4-дигидро-6,7-диметоксиизохинолин-1-ил)-2-фенил-2-(3- фенилпропил)-тиоэфир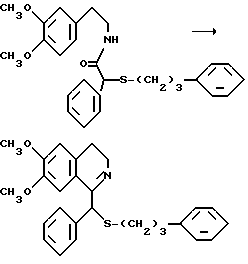
2,55 r (5,67 ммоль) амида N-[2-(3,4-диметоксифенил)этил]-3-(3- фенилпропил)-фенилуксусной кислоты и 2,6 г (17 ммоль) хлорокиси фосфора нагревают в 35 мл ацетонитрила в течение 1,5 часов в атмосфере азота и при перемешивании до 100oC. К реакционному раствору добавляют при комнатной температуре 125 мл сложного этилового эфира уксусной кислоты, затем промывают 3 раза ледяной водой, каждый раз 25 мл, 3 раза насыщенным раствором бикарбоната натрия, каждый раз 25 мл, и раз насыщенным раствором хлористого натрия, после чего сушат над сульфатом магния.
После отгонки органической фазы в вакууме маслянистый остаток очищают на колонке, содержащей силикагель, с применением в качестве элюента сложного этилового эфира уксусной кислоты. При этом получают 1,18 г целевого продукта в качестве аморфного вещества.
Пример 3.
Амид N-[2-(3,4-диметоксифенил)этил]-2,5-дифенилпентанкарбоновой кислоты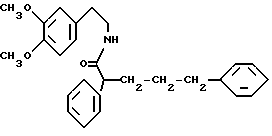
Раствор 3,0 г (11,8 ммоль) 2,5-дифенилпентанкарбоновой кислоты и 1,91 г (11,8 ммоль) карбонилдиимидазола в течение часа перемешивают при комнатной температуре, после чего добавляют раствор 2,13 г (11,8 ммоль) 2-(3,4-диметилэтоксифенил)этиламина в 20 мл тетрагидрофурана и перемешивают в течение ночи при комнатной температуре, после отгонки растворителя остаток растворяют в сложном этиловом эфире уксусной кислоты. Органическую фазу промывают 2 раза 1 н. хлористоводородной кислотой, каждый раз 15 мл, и 2 раза насыщенным раствором бикарбоната натрия, каждый раз 20 мл, а затем насыщенным хлористого натрия. После сушки над сульфатом магния и отгонки растворителя получают 4,9 г (100% теории) целевого продукта в качестве масла, подвергаемого без очистки дальнейшей переработке.
(R,S)-(3,4-дигидро-6,7-диметоксиизохинолин-1-ил)-1,4-дифенилбутан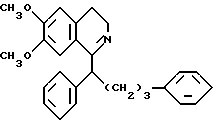
Раствор 4,9 г (11,75 ммоль) амида N-[2-(3,4-диметоксифенил)этил]- 2,5-дифенилпентанкарбоновой кислоты и 5,39 г (35,2 ммоль) хлорокиси фосфора в 40 мл абс. ацетонитрила в течение 1,5 часов в атмосфере азота и при перемешивании нагревают с обратным холодильником. Реакционный раствор разбавляют 150 мл сложного этилового эфира уксусной кислоты и последовательно промывают два раза ледяной водой, каждый раз 40 мл, 3 раза насыщенным раствором бикарбоната натрия, каждый раз 30 мл, и раз насыщенным раствором хлористого натрия. Органическую фазу сушат над сульфатом магния. После отгонки растворителя в вакууме маслянистый остаток растворяют в ацетоне и подкисляют эфирной соляной кислотой.
При этом целевой продукт получают в качестве аморфного твердого вещества в виде гидрохлорида. Выход: 2,6 г (50,8% теории).
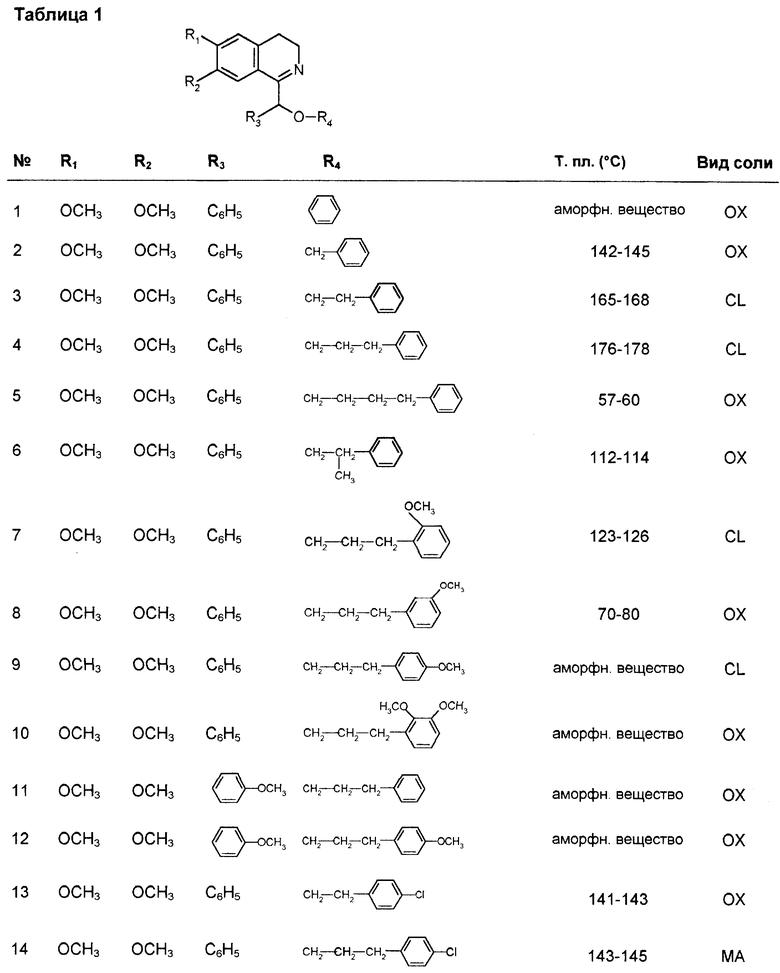
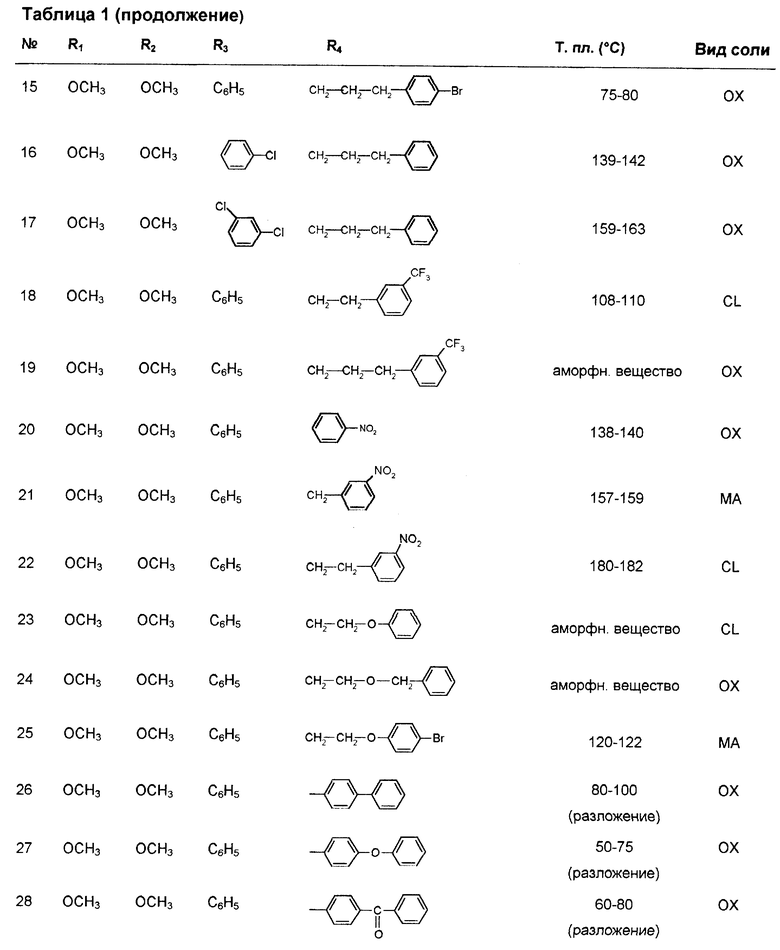
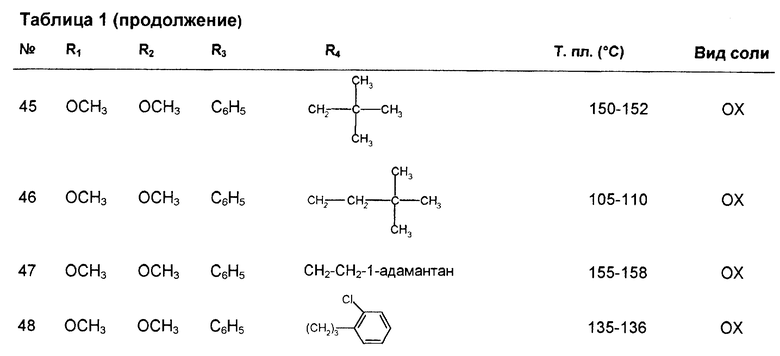
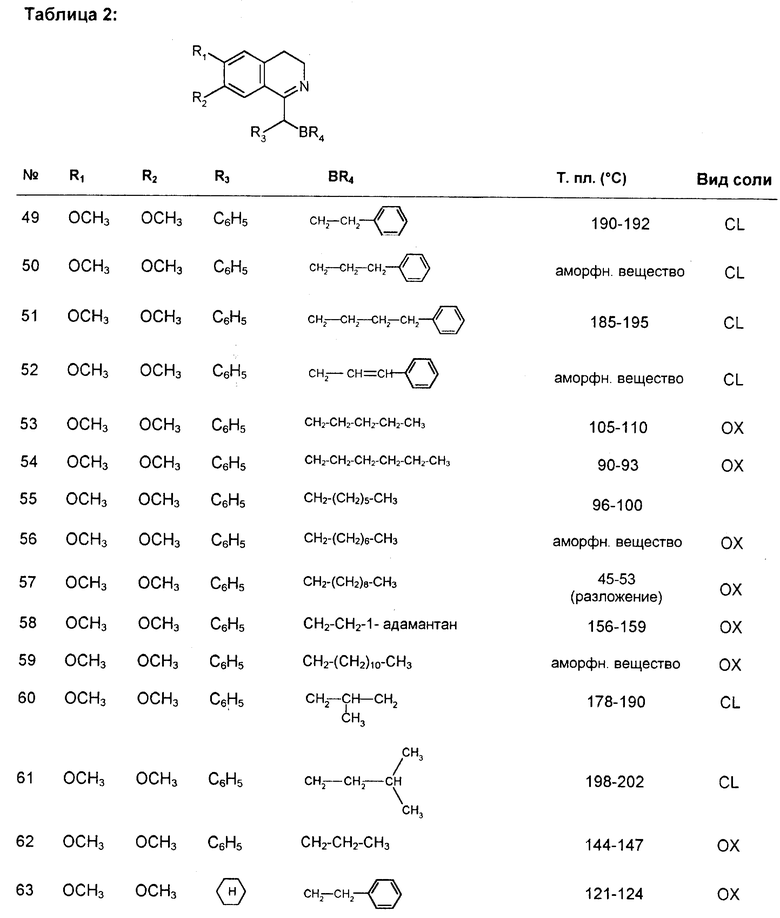
В таблицах 1, 2 сведены дальнейшие соединения согласно изобретению. Получение этих соединений может проводиться аналогично вышеописанным способам. В таблицах 1, 2 использованы следующие условные сокращения:
OX = оксалат
CL = гидрохлорид
MA = малеинат
Соединения согласно изобретению, которые относятся к категории малотоксичных веществ, пригодны для лечения дегенеративных и некротизирующих заболеваний головного мозга. Представляется также возможным профилактическое лечение больных, угрожаемых в отношении таких заболеваний. Такое действие соединений основано не на улучшении кровоснабжения ткани. Поэтому соединения пригодны для новой формы лечения при эпилепсии и болезни Альцгеймера, они являются, в частности, пригодными для лечения больных, потерпевших инсульт или угрожаемых в отношении инсульта.
Они могут также применяться для получения средств, пригодных для лечения хронически воспалительных процессов, колита Ulcerosaa и болезни Крона, и средств с антипролиферативным действием. Действие соединений можно объяснить торможением неселективных катионных канальцев.
Основой патофизиологии хронической бронхиальной астмы являются воспалительные процессы, возникающие активацией воспалительных клеток (Барнс, 1987; Зайферти Шультц, 1991).
Регулируемая рецепторами активация воспалительных клеток, например, нейтрофильных гранулоцитов и тучных клеток или их постоянных линий, клеток HL-60 или сенсибилизированных, т.е. нагруженных гамма-глобулином E клеток RBL, тормозится независимо от вида стимулирующих агонистов (таких, как, например, эндотелии, активирующий тромбоциты фактор, лейкотриены, химиотактический пептид TM1-P или антиген против сенсибизированных тучных клеток) ингибиторами неселективных катионных канальцев (Ринк, 1990). Через эти канальцы в клетки поступает внеклеточный кальций, необходимый для персистенции вызываемых рецепторами активаций клеток (Пугни, 1990). В результате прекращения снабжения кальцием прерывается, имеет место блокада активации воспалительных клеток.
Классические антагонисты кальция дигидропиридинового или фенилалкиламинового типа не тормозят ни неселективные катионные канальцы, ни воспалительные процессы (Веллс и др., 1986).
Кинетика цитоплазматической концентрации ионов кальция в нагруженных Фура-2 клетках количественно определяется флюорометрией описанным Гринкиевичем и др. (1985) образом как критерий активации клеток или критерий их торможения ингибиторами неселективных катионных канальцев. Этот подход оказался в рамках настоящего изобретения надежным методом скрининга для обнаружения ингибиторов неселективных катионных канальцев.
Для специфического определения ингибиторов неселективных катионных канальцев годится так называемое функциональное торможение тапсигаргина. Тапсигаргин представляет собой описанный Таструпом и др. (Proc. Natl. Acad. Sci. (США), 87, 2466 2470, 1990) промотор опухолей, избирательно и необратимо тормозящий кальциевую аденозитрифосфоратазу внутриклеточных высокочувствительных по отношению к инозитолтрифосфату (IP3) накопителей Ca2+. Вследствие этого получается скорое опорожнение накопителей Ca2+. Как описано Дж. Путин (Calcium, 11, 611 - 624, 1990), опорожнение этих накопителей является физиологическим раздражителем для открытия неселективных катионных канальцев в оболочке клетки. Результатом является сильный вток Na+ и Ca2+ в клетку. Благодаря этим свойствам тапсигаргин пригоден в качестве косвенного стимулятора независимого от агонистов и IP3 открытия неселективных катионных канальцев.
В рамках настоящего изобретения стимуляция тапсигаргином неселективных катионных канальцев успешно проводилась на HL 60-клетках (лейкемических клетках человека), нейрональных клетках из аммонов рога и корковых клетках, а также на клетках RBL. Таким образом, было доказано существование этих канальцев в соответствующих клеточных линиях.
Цитоплазматическая концентрация Ca2+([Ca2+] , ) играет важную роль при пролиферации клеток, а также при росте опухолей (обзор, см. Л.Р. Пахарский, Journal of Medicine, 19 : 145 - 177, 1988). В частности, стимулируемому активацией рецепторами с последующим содействием активации IP3 втоку Ca2+ в клетку приписывают решающее значение для онкогенной пролиферации клеток (У. Киккава и И. Нишицука, Ann. REV. CELL-. BIOL., 2: 149 - 178, 1986). Эти процессы имеют значение также при образовании метастазов, а также при устойчивости ко многим лекарствам (так называемый "Multi-Drug-Resistance") (oбзор, см. вышеуказанную публикацию Л.Р. Пахарского). J. Med., 19:145 - 177, 1980.
Этa гипотезa подтверждается тем, что тапсигаргин в качестве косвенного стимулятора неселективных катионных канальцев приводит к перегрузке Ca2+ в клетке и сверх этого является высокоактивным промотором опухолей (В. Таструп и др., Proceedings of NATL. Acad. Sci.: (США) 87: 2466 - 2470, 1990.)
Блокада втока Ca2+ в неселективные катионные канальцы приводит к нормализации внутриклеточной концентрации ионов кальция и впоследствии к торможению роста опухоли и т.д.
Эти неселективные катионные канальцы не тормозятся классическими антагонистами кальция. Неожиданно было установлено, что предлагаемые соединения тормозят вток кальция в клетку через неселективные катионные канальцы.
Как показал С. Н. Мурч и др. (Lancet 339: 38-1 - 385, 15-го февраля 1992), эндотелин I играет важную роль в воспалительных заболеваниях кишки, таких, как, колит Ulcerosa или болезнь Крона. С помощью иммуногистохимических методов было обнаружено, что у больных, страдающих болезнью Крона в области подслизистого слоя, а также у больных, страдающих колитом Ulcerosa в области Lamina propia покровной ткани толстой кишки имеются в значительной мере сильно повышенные концентрации эндотелина I по сравнению со здоровыми нормальными лицами. Предполагается, что локальное выделение эндотелина вызывает сильные спазмы сосудов с последующей рассеянной ишемией с микроинфарктами, которые можно рассматривать как собственную причину указанных заболеваний. Вазоспазмогенная активность эндотелина объясняется перегрузкой Ca2+ в сосудистых миоцитах. При этом эндотелин в первую очередь вызывает вызываемое IP3 внутриклеточное высвобождение Ca2+ с последующим сильным трансмембранным втоком Ca2+ через нечувствительные к воздействию дигидропиридинов канальцы (М. С. Симонсон и др., Clin. Invest. Med. 14: 499 - 507, 1991; Т. Масакаи, J. Cardiovasc. Pharmacol. 100: 383 - 392, 1990). Эти канальцы представляют собой неселективные катионные канальцы, наличие которых также в клетках слизистой оболочки толстой кишки недавно было описано (Хр. Зимер и Г. Гегелейн, Europ. J. Physiol. 420: 319 -328,1992).
Пригодной моделью скрининга для обнаружения функциональных антагонистов эндотелина оказалась стимулируемая эндотелином активация нагруженных Фура-2 человеческих лейкемических клеток (клетка HL 60). Аналогично методу, описанному Г. Гринкиевичем и др. (J. Biol. Chem. 260: 3440 - 3450, 1985), спектрофлюорометрическим методом можно следить за внутриклеточной концентрацией Ca2+ в цитоплазме клеток HL 60 (в виде суспензий), и количественно определяется эта концентрация в качестве критерия активации клеток. Стимуляция осуществилась путем прибавления 0,1 ммоль эндотелина, ее можно было независимо от дозы тормозить с помощью предлагаемых соединений.
Функциональный антагонизм предлагаемых соединений по отношению к эндотелину является результатом блокады неселективных катионных канальцев. Поэтому доказательство функционального антагонизма по отношению к тапсигаргину на клетки RBL-hm1 также годится в качестве метода скрининга функциональных антагонистов эндотелина.
Проведение исследования.
В целях скрининга в свободной от Ca2+ инкубационной среде нагруженные Фура-2 адгезивные клетки RBM-1hm1 стимулируются 0,1 мкмоль тапсигаргина. По истечении 4 минут внеклеточный Ca2+ восстанавливают до 1,5 ммоль, и при помощи флюоресценции Фура-2 регистрируют чрезмерное повышение цитоплазматической концентрации Ca2+ вследствие происходящего сильного трансмембранного втока Ca2+ через неселективные катионные канальцы.
Этот втoк можно тормозить исключительно и в зависимости от дозы ингибиторами неселективных катионных канальцев. Ни классические антагонисты кальция, ни специфичные ингибиторы агонистов, которые возбуждают оборот IP3, не могут тормозить косвенно вызываемый тапсигаргином трансмембранный втoк Ca2+ Предлагаемые соединения отличаются торможением неселективных катионных канальцев.
Флюорометрическое измерение кальция в цитоплазме отдельных прилипающих клеток RBL-hm11 осуществляется аналогично описанному Куда и Огура (1986) методу, в котором применяют нейрональные клетки. Используют флюоресцентный микроскоп АКСИОВЕРТ 35 фирмы Цайсс в сочетании с имэджинг-системой фирмы Хамаматсу, состоящей из системы ICMS обработки изображений, камеры остаточного света с контрольным устройством и усилителем яркости изображений типа ОТЗ 3000.
Кинетику цитоплазматической концентрации Ca2+ постоянного записывают в виде кривой концентрации и времени после стимулируемой тапсигаргином (0,1 мкмоль) активации клеток. Сравнивают кривые двух активированных культур клеток в присутствии, а также при отсутствии 10 мкмоль испытуемого вещества. Площадь под этими кривыми (area under the curve = AUC) интегрируют и регистрируют как меру активации клеток. Степень тормозящей активности испытуемых ингибиторов неселективных катионных канальцев определяют по следующему уравнению: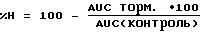
%H = процентное торможение втока кальция через неселективные катионные канальцы, который возбуждают и тормозят 10 мкмоль испытуемого вещества.
AUC торм. = площадь под кривой, которая записывается в присутствии стимулирующего средства и 10 мкмоль ингибиционного испытуемого вещества в качестве ингибитора.
AUC контроль = площадь под кривой, которую записывают только после прибавления стимулирующего средства.
Литература к вышеприведенным пояснениям:
Барнс П. Дж., И.В. Роджер и Н.К. Томсон
Pathogenesis of asthma, опублик. в "ASTHMA, basic machanisms and clinical management",
Изд. П. Дж. Барнс: Academic Press, Лондон, 1988
Гринкиевич Г., М. Поени и Р.И. Тсиен
A new generation of Ca2+-indicators with greatly improved fluorescence properties,
J. BIOL CHEM. 260: 3440 - 3450, 1985
Хайд, М. и М.А. Бивен
Calcium influx in a rat mast cell (RBL-2H3) line,
J. BIOL. CHRM. 266 15221 - 15229, 1991
Кудо, И. и А. Огура
Glutamate-induced increase in intracellular Ca2+-concentration in isolated hippo-campal neurones,
BR. J. PHARMACOL. 89, 191 - 198, 1986
Пугни, Дж. В., юн.
Capacitative Calcium entry revised,
CELL CALCIUM 11: 611 - 624, 1990
Ринк, Т. дж.
Receptor-mediated calcium entry, FEBS LETT. 268: 381 - 385, 1990
Зайферт, P. и Г. Шультц
The superoxide forming NADPH oxidase of phagocytes: An enzym system regulated by multiple mechanism,
REV. PHYSIOL. BIOCHEM. PHARMACOL. , Vol. 117,. издательство Шпрингер, 1991
Веллс, Е., С. Г. Джэксон, С.Т. Харпер, Дж. Манн и Р.П. Эаой
Characterization of primate bronchoalveolar mast cells II, inhibition of histamine, LTC4 and PGF2a release from primate bronchoalveolar mast and a comparison with rat peritoneal mast cells,
J. IMMUNOL. 137: 3941 - 3945, 1986.
Результаты испытаний
Определяется концентрация исследуемых соединений, обеспечивающая 50%-ное торможение неселективных катионных канальцев после стимуляции тапсигаргином (0,1 мкмоль тапсигаргина) в клетках RBL-hm1. Для всех исследуемых соединений она составляет 10-5 моль.
При помощи описываемого в нижеследующем испытания можно показать функциональную противовоспалительную активность предлагаемых соединений. Используют отдельные прилипающие к стеклянным пластинкам клетки RBL-2H3 (родственная тучным клеткам опухолевая клеточная линия).
Культивацию и прилипание RBL-2Н3-клеток осуществляют по описанному Хайдом и Бивеном (1991) методу. Для сенсибилизации адгезивных клеток RBL-2H3 клетки в течение 2 часов инкубируют при комнатной температуре в присутствии имеющегося в торговле разбавленного в соотношении 1 : 2000 раствора гаммаглобулина E, после чего клетки промывают. Путем прибавления 0,1 мл раствора комплекса динитрофенола и альбумина сыворотки крови крупного рогатого скота (антиген DNP-BSA; 10 мкг/мл) осуществляется сильная иммунологическая активация клеток, вызываемая цитоплазматической перегрузкой Ca2+. Флюорометрическое измерение кальция в цитоплазме отдельных прилипающих клеток RBL-2H3 осуществляется аналогично вышеупомянутому, описанному Куда и Огура (1986) методу, в котором применяют нейрональные клетки.
В качестве сравнительного вещества в этом исследовании служит хромоглицат (10 мкмоль), который вызывает приблизительно 50%-ное торможение индуцируемой антигеном активации клеток.
В этом испытании вышеуказанные соединения проявляют процентную активность, соответствующую указанным выше значениям.
В исследованиях на микрокультурах различных человеческих опухолевых клеточных линий, проведенных при помощи так называемого тетразолиевого анализа для определения антипролиферативной активности предлагаемых веществ, неожиданно показалось, что активность испытуемых соединений на 5 до 100 раз больше, чем у сравнительного вещества верапамила.
Антипролиферативную активность испытуемых соединений определяли с помощью описанного Мосманном (J. IMMUNOL METH. 65: 55-63, 1983), Денизотом и др. (J. IMMUNOL. METH 89: 271 - 277, 1986) и Дж. Элиасоном и др. (INT. J. CANCER 46: 113 - 117, 1990) испытания, в котором используют (МТТ бромид [3-(4,5-диметилтиазол-2-ил)-2,5- дифенил-тетразолин, продукта фирмы Хемикон Инк. Эль Сегундо, Ка, США. Этот индикатор метаболизируется только живыми клетками с интактными митохондриями до синего формазанового продукта. В нашем испытании использовались следующие типы человеческих опухолевых клеток: A 549 (аденокарцинома легких), A 431 (карцинома эпидермиса вульвы), PC 3 (аденокарцинома предстательной железы), SK BR 3 (аденокарцинома молочной железы), HT 29 (CX1 1) (аденокарцинома толстой кишки) и K 562 (хронически-миелоическая лейкемическая клетка).
Испытание проводилось на микротитровых пластинах, каждое углубление которой содержало 100 мкл клеточной суспензии (0,2 • 106 клеток/мл). В качестве инкубационной среды служила среда RPMI 1640 с 10% инактивированной термообработкой эмбриональной телячьей сыворотки крови и 50 мкг/мл гентамицина. Клеточные суспензии в течение 0, 24, 48 или 72 часов инкубировали при насыщенной влажности воздуха и при 37oC в атмосфере CO2 (5%) и воздуха (95%) в присутствии антипролиферативных испытуемых веществ, которые применялись в различных концентрациях, или же в их отсутствии. Испытуемые вещества растворяли в ДМСО (конечное разбавление 0,1%). После этого добавляли 10 мкл раствора МТТ (3 мг/мл), и по истечении 3 часов - 100 мкл раствора изопропанола, содержащего 0,08 н. хлористоводородной кислоты. По истечении дальнейшего часа определяли поглощение света при 570 нм (сравнительная длина волн 630 нм) при помощи считывающего устройства. Поглощение света непосредственно пропорционально количеству живых клеток. Полумаксимальные торможение достигается при концентрации исследуемых веществ, составляющей 1 мкг/мл.
Вазоспазмолитическая активность вышеуказанных функциональных антагонистов эндотелина или тапсигаргина подтверждалась опытом на изолированном сосудистом препарате. У ретроградно перфундированных, спонтанно бьющихся сердцах крыс по Лангендорффу венечная перфузия постоянно преобразовывалась в измеряемые величины путем электромагнитного измерения потока (аппаратура фирмы Хуго Закс Электроник, Марх). При помощи этой схемы измерения можно зарегистрировать с высокой точностью объем, продолжительность и характер течения сосудистых спазмов. В случае осуществления перфузии при 100 нмоль эндотелина перфузионный поток уменьшается от 11 до 5 мл/мин. Снижение перфузии можно снимать с помощью предлагаемых соединений. Между активностью предлагаемых соединений по отношению к торможению тапсигаргина у нагруженных Фура-2 клеток RBL-hm1 или по отношению к торможению эндотелина у нагруженных Фура-2 клеток HL 60, с одной стороны, и доказанной у препарата по Лангендорффу вазоспазмолитической активностью исследуемых соединений, было установлено явное взаимоотношение. Из этого можно заключить, что в основу вазоспазмолитического антагонизма эндотелина исследуемых соединений положена блокада неселективных катионных канальцев.

Изобретение относится к новым анеллированным производным дигидропиридина, обладающим биологической активностью, более конкретно к производным изохинолина и их солям формулы I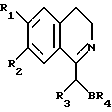
в которой R1 и R2 независимы друг от друга и означают гидроксил, алкоксил с 1 - 4 атомами углерода, галоген, алкил с 1-4 атомами углерода, бензилокси; В - группа -О-, -S- или -СНR5, в которой R5 означает водород или алкил с 1 - 6 атомами углерода; R3 - 2- или 3-тиенил, циклоалкил с 4-7 атомами углерода, или группа формулы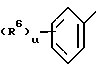
где R6 означает галоген или алкоксил с 1 - 4 атомами углерода, u - 0, 1 или 2; R4 - алкенил с 3-6 атомами углерода, незамещенный или замещенный фенилом, алкил с 1-13 атомами углерода, возможно замещенный заместителем из группы, включающей тиенил, адамантил, циклогексил, бензилокси-группу, фенокси-группу и фенил, причем последний или содержащийся в фенокси-группе фенил может быть моно-, ди- или тризамещен остатком из группы, включающей гидроксил, алкоксил с 1 -4 атомами углерода, галоген, трифторметил, двуокись азота и алкил с 1 - 4 атомами углерода, или двумя незамещенными фенильными группами, группы формул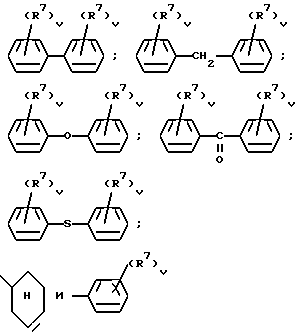
где R7 означает галоген, а трифторметил, двуокись азота, а v - 0, 1,2, или их соли с физиологически переносимыми кислотами или комплексообразователями. В исследованиях на микрокультурах различных человеческих опухолевых клеточных линий, проведенных при помощи так называемого тетразолиевого анализа, предлагаемые вещества показали высокую антипролиферативную активность по сравнению с верапамилом. 4 з.п. ф-лы, 2 табл.

в которой R1 и R2 независимы друг от друга и означают гидроксил, алкоксил с 1 - 4 атомами углерода, галоген, алкил с 1 - 4 атомами углерода, бензилокси;
В - группа -О-, -S- или -CHR5, в которой R5 означает водород или алкил с 1 - 6 атомами углерода.
R3-2-или 3-тиенил, циклоалкил с 4 - 7 атомами углерода, или группа формулы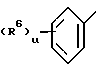
где R6 означает галоген или алкоксил с 1 - 4 атомами углерода, u -0,1 или 2,
R4 - алкенил с 3 - 6 атомами углерода, незамещенный или замещенный фенилом, алкил с 1 - 13 атомами углерода, возможно замещенный заместителем из группы, включающей тиенил, адамантил, циклогексил, бензилокси-группу, фенокси-группу и фенил, причем последний или содержащийся в фенокси-группе фенил может быть моно-, ди- или тризамещен остатком из группы, включающей гидроксил, алкоксил с 1 - 4 атомами углерода, галоген, трифторметил, двуокись азота и алкил с 1 - 4 атомами углерода, или двумя незамещенными фенильными группами, группы формул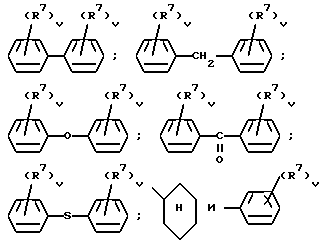
где R7 означает галоген, трифторметил, двуокись азота, а v-0,1,2, или их соли с физиологически переносимыми кислотами или комплексообразователями.
| RU 95105584 A1, 1992 | |||
| EP 358957 A, 1988 | |||
| 0 |
|
SU288048A1 | |
| ТСХИНЧЕСКАЯ БКБЛИОТЕЯА | 0 |
|
SU251194A1 |
Авторы
Даты
1999-09-10—Публикация
1994-12-14—Подача