Изобретение относится к химико-фармацевтической промышленности и касается экстракта листьев Аронии черноплодной, обладающего антиоксидантной активностью и оказывающего ингибирующее действие на все этапы перекисного окисления липидов в тканях печени, который может найти применение в качестве парафармацевтика в медицине и фармацевтической промышленности, а также способа его получения.
Известно, что в различных частях растений содержатся проантоцианидины, растущий интерес к которым обусловлен их ярко выраженной антиоксидантной активностью и целым рядом лечебно-профилактических свойств, который продолжает пополняться (1). Термин "олигомерные проантоцианидины" относят к конденсированным танинам, состоящим из не более 10 флаваноловых единиц. Биосинтетическими предшественниками проантоцианидинов являются флаван-3-ол (катехины) и флаван-3,4-диол (лейкоантоцианидины).
Известен способ получения гидроксифлавин-3,4-диолов из сырого растительного материала, например земляных орехов и коры сосны приморской, предусматривающий экстракцию водным раствором хлорида натрия; отделение водного экстракта от твердых примесей; обработку водного экстракта этилацетатом для получения раствора гидроксифлаван-3,4-диолов в этилацетате; обработку этилацетатного раствора избытком хлороформа; отделение осадка, содержащего гидроксифлаван-3,4-диолы; очистку гидроксифлаван-3,4-диолов последовательным растворением в этилацетате и осаждением хлороформом (2). Допускаются модификации, включающие возможность проведения экстракции на холоду и при нагревании; водой с последующим насыщением солью, насыщенным раствором хлорида натрия или другого подходящего электролита, органическим растворителем с последующим насыщением солью водного раствора; помимо хлороформа, для осаждения гидроксифлаван-3,4-дио могут быть использованы эфир, бензол, гексан и др. Конечный продукт содержит гидроксифлаван-3,4-диолы в форме мономера и димеров-пентамеров.
В усовершенствованном варианте способ получения проантоцианидинов из сырого материала включает экстракцию кипящей водой, охлаждение, фильтрацию, насыщение фильтрата хлоридом натрия или сульфатом аммония и далее, как указано выше (3).
Известен способ получения экстракта из зеленых листьев "гинго билоба" (4), содержащего проантоцианидины, а также флаванолы, предусматривающий экстракцию измельченных листьев водным кетоном (ацетон - 70% и вода - 30%) при 50 - 60oC; концентрирование извлечений для осаждения бифлавоноидов и гидрофобных веществ; фильтрацию водного концентрата; подщелачивание фильтрата для осаждения проантоцианидинов; отделение нерастворимой фракции, содержащей проантоцианидины; подкисление фильтрата; экстракция фильтрата C4 - C6 кетоном в присутствии сульфата аммония; высушивание кетоновой фазы. Этот способ регламентирует содержание проантоцианидинов, преследуя удаление проантоцианидинов и доводя их содержание от 35,2 до 6,46%.
Остальные способы используют для экстракции в разных модификациях: водный ацетон и насыщение экстракта натрия хлоридом и экстракцию этилацетатом. Классическими источниками проантоцианидинов для промышленного производства являются кора сосны приморской (препарат "Пикногенол") и семена красного винограда. Выделены проантоцианидины также из корней горца, фасоли адзуки и других трав, не произрастающих на территории России, а также из красного вина и пива.
Вышеупомянутые способы, исключая экстракт билоба, направлены на получение экстрактов с максимальным содержанием проантоцианидинов или требующие дополнительной очистки. Используемые источники изначально содержат высокие количества проантоцианидинов, но, к сожалению, не имеют широкого распространения на территории России (красный виноград, конский каштан), либо совсем не встречаются (сосна приморская, гинго билоба), либо требуют специального выращивания (земляные орехи, горец, фасоль адзуки) и т.д.
Есть сведения о желчегонной активности растительных полифенолов, выделенных из листьев рябины черноплодной (6). Однако данные об их составе и способе выделения отсутствуют.
Задачей настоящего изобретения является получение растительного экстракта, обладающего антиоксидантной активностью и содержащего комплекс флавоноидных мономеров и олигомерных проантоцианидинов; содержащих в основном димеры-пентамеры, не содержащие высокополимерных конденсированных танинов из достаточно распространенного в России, легкодоступного, относительно дешевого и устойчивого при хранении растительного источника.
Указанная задача достигается описываемым экстрактом листьев Аронии черноплодной, обладающим антиоксидантной активностью и оказывающим ингибирующее действие на все этапы перекисного окисления липидов в тканях печени, содержащим 72 - 78% фенольных соединений, включая не менее 25% олигомерных проантоцианидинов, а также способом его получения, заключающимся в том, что осуществляют экстракцию криопорошка листьев Аронии черноплодной (Aronia melanocarpa (Michx. Elliot), собранных перед началом и в период цветения, кипящим водным спиртом с последующим отделением водно-спиртовых извлечений, концентрированием их до водного отделением водно-спиртовых извлечений, концентрированием их до водного раствора, фильтрацией водного раствора, очисткой фильтрата петролейным или диэтиловым эфиром, экстракцией водного остатка смесью диэтилацетата и спирта (8 : 2) и концентрированием спиртоэтилацетатных извлечений до получения сухого остатка.
Преимущественно экстракцию криопорошка проводят 80%-ным спиртом дважды по 30 минут, концентрирование осуществляют при пониженном давлении и температуре 50 - 60oC, очистку фильтрата осуществляют до исчезновения зеленой окраски, экстракцию водного остатка смесью этилацетата и спирта осуществляют трижды при соотношении водного остатка и экстрагента (1 : 1), концентрирование спиртоэтилацетатных извлечений осуществляют сначала под атмосферным давлением, а затем под вакуумом.
В качестве сырьевого источника впервые используют криопорошок листьев Аронии черноплодной, собранных перед началом и в период цветения, что не сказывается на урожае плодов, обеспечивает возможность избежать конденсированных танинов и получить максимальное содержание проантоцианидинов и флавоноидов. Кратковременная экстракция 80% кипящим этанолом обеспечивает максимальное извлечение фенольных веществ при температуре 78 - 79oC. Фильтрация после отгонки спирта обеспечивает первый этап очистки, а обработка петролейным эфиром, при которой удаляются хлорофилл и липофильные вещества, завершает ее. Экстракция смесью этилацетата и спирта дает возможность одновременного извлечения проантоцианидинов и мономерных флавоноидов, а также других фенольных соединений.
Конечный продукт содержит не менее 25% олигомерных проантоцианидинов, из которых на долю димеров приходится - 27,1%, тримеров-тетрамеров - 28,4% и олигомеров с молекулярной массой выше 1200Д 0,5%. Мономерные соединения составляют 44%; полимерные конденсированные танины - менее 0,1%.
Изобретение иллюстрируется следующими примерами.
Пример
10 кг криопорошка (влажность 7%, крупность помола 0,5 мм), приготовленного по щадящей технологии (6) из листьев Аронии черноплодной, собранных перед началом и в период цветения, в экологически чистой местности, без применения пестицидов и фунгицидов, помещают в реактор (сталь/эмаль), снабженный паровой рубашкой, мешалкой и обратным холодильником; добавляют 50 л 80%-ного водного раствора этилового спирта (соотношение сырья и экстрагента 1 : 5 вес/об.); включают мешалку и пуском пара в рубашку нагревают массу до кипения и проводят экстракцию в течение 30 минут. Далее массу из реактора отфильтровывают с отжимом осадка и осадок возвращают в реактор. Добавляют свежую порцию экстрагента (50 л) и повторяют экстракцию.
Объединенные спиртовые извлечения концентрируют при пониженном давлении и температуре 50-55oC до примерно 17 л и полученный водный раствор сразу же фильтруют под вакуумом. Далее фильтрат очищают от хлорофилла и липофильных веществ, смешивая с петролейным эфиром (низкокипящая фракция), при соотношении фильтрата и эфира (1:1). Отстаивают в делительной воронке и отделяют водный слой. Операцию повторяют еще два раза до обесцвечивания водного слоя.
Очищенный водный остаток освобождают от возможных остатков эфира и дважды экстрагируют смесью этилацетата и спирта (8:2) при соотношении водного раствора и экстрагента (1:1). Объединенные спирто-этилацетатные извлечения упаривают сначала под атмосферным давлением, а затем под вакуумом до получения сухого остатка, который далее подвергают порошкованию. Выход конечного продукта 512 г, т.е. 5,1% от исходного сырья. Выход может колебаться от 4 до 6%, составляя в среднем 5%.
Полученный экстракт представляет собой аморфный порошок светло-бурого цвета, солоновато-вяжущего вкуса, практически без запаха. Легко растворим в спирте и водно-спиртовых растворах. При нагревании с кислым спиртом (реактив "бутанол-HCl") (специфичная проба на проантоцианидины) дает красное окрашивание.
Характеристика и свойства полученного экстракта представлены ниже.
1. Физико-химическая характеристика полученного экстракта.
1) Содержание влаги,%, не более - 10
Общее содержание золы, %, менее - 10
Содержание золы, нерастворимой в HCl, %, менее - 2
pH - 2,9-4,3
Растворимость - Легко растворим в спирте и водно-спиртовых растворах
УФ-спектр в этаноле, максимальное поглощение в интервале - 290 - 325 нм
Общее содержание полифенолов, определяемых по свободной фенольной группе методов Фолина-Чокальте, в пересчете на катехин,% (7) - -76
Общее содержание флаван-3,4-диоловых остатков в мономерной (лейкоантоцианидины) и конденсированной форме (проантоцианидины), высвобождаемых после деполимеризации, определяемых с реактивом "Бутанол-HCl" в пересчете на цианидин,% (7) - -62
Общее содержание олигомерных проантоцианидинов в пересчете на внутренний стандарт, выделенный на сефадексе LH-20,%, (7,8) - 31,5
Общее содержание катехинов, определяемых с ванилиновым реактивом, в пересчете на (+)-катехин,%, (7) - 34
Содержание флавоноловых гликозидов в пересчете на кверцитин,% - 14
2) Распределение компонентов фенольных соединений в зависимости от молекулярной массы - данные хроматографического анализа на сефадексе LH-20 (8)≅ 300Д (мономеры) - -44,0%
≈ 600Д (димеры) - -27,1%
≈ 900 - 1200Д (тримеры-тетрамеры) - -28,4%
> 1200Д, но ≅ 3000Д - -0,5%
Все пики показали развитие красного окрашивания с "Бутанол - HCl", однако наиболее интенсивное окрашивание наблюдалось 900 - 1200Д.
II. Оценка антиоксидантной активности экстракта.
А. Методом хемилюминесценции измерено общее содержание природных антиоксидантов (+AO) и их активность по отношению к перекисным радикалам модельной реакции окисления углеводорода (K7, константа взаимодействия с перекисными радикалами кумола, T=50oC):
(AO) = 0,73•10-6 моль/г экстракта;
K7 = 0,93•104 л/моль•с
Для сравнения в качестве стандарта выбран ионол - один из основных представителей группы антиоксидантов:
K7=1,47•104 л/моль•с
Б. Проверено действие экстракта на показатели перекисного окисления липидов (ПОЛ), инициированного CCl4.
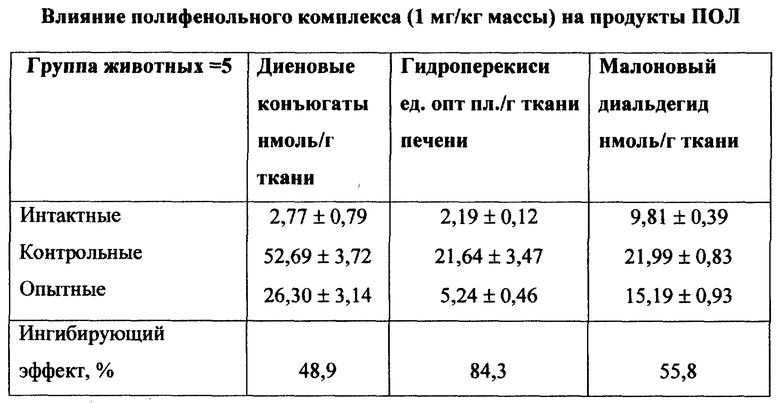
Мышам-самцам линии СВА вводили внутрижелудочно 0,25 мл 70%-ного раствора CCl4; через 15 - 20 мин животным вводили внутрижелудочно экстракт из расчета 1 мг/кг веса животного (опытная группа, 5 мышей); пяти животным контрольной группы вводили аналогичный объем физиологического раствора. Через двое суток животных забивали, выделяли печень и определяли продукты ПОЛ: диеновые конъюгаты (продукты начальных этапов ПОЛ); гидроперекиси (продукты более поздних этапов) и малоновый диальдегид (МДА, один из наиболее важных конечных продуктов). Полученные результаты (Таблица) показывают, что экстракт в одноразовой дозе (1 мг/кг массы тела) оказывает значимое (P<0,05) ингибирующее действие на ПОЛ на всех его этапах. Так, он подавлял образование диеновых конъюгатов на 48,9%; гидроперекисей - на 84,3% и малонового диальдегида - на 55,8%.
Расчет ингибирующего эффекта проводили по следующей формуле:
Ингибирующий эффект,% 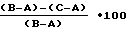
A - показатель интактных животных;
В - показатель контрольной группы;
C - показатель опытной группы (введен экстракт).
Конечный продукт по санитарно-химическим, микробиологическим и радиационным показателям отвечает требованиям и нормам, существующим для парафармацевтиков растительного происхождения (9).
СПИСОК ЛИТЕРАТУРЫ
1. OPC in Practice, Bert Schwitheros, "bioflavanols and their application". 1993, jul. 30., p.p. 1-99.
2. US, патент N 3436407, 549-400, 1969 г.
3. US, патент N 4698360, А 61 K 31/35, 1987.
4. US, патент N 4981688, A 61 K 35/78, 1991.
5. Вихтинская И.Л. и др. "Влияние полифенольных растительных комплексов на желчеобразование у крыс с дистрофией печени", тезисы докладов, 3-ий съезд фармакологов УССР, Винница, 1977, стр. 31.
6. RU, патент N 2110194, 1998 г.
7. Woterman P.G., Mole S., Analysis of phenolic plant metabolites., Blackwell Scientific Publications, Oxford, U.K., 1994.
8. Jn. "Plant flavanoids in biology and medicine: Biochemical, pharmacological and structure-activity relationships"., Ed. Cody V., Middletown E. , Harborne J., N. - J., 1986, p. 67-76.
9. "Гигиенические требования к качеству и безопасности продовольственного сырья и пищевых продуктов", СанПиН. 2.3.2.560-96, п. 6.10.2.1.
| название | год | авторы | номер документа |
|---|---|---|---|
| ОЗДОРОВИТЕЛЬНО-ПРОФИЛАКТИЧЕСКАЯ КОМПОЗИЦИЯ, ВКЛЮЧАЮЩАЯ КОМБИНАЦИИ СОЕВОГО ФОСФОЛИПИДНОГО КОМПЛЕКСА И ЭКСТРАКТОВ ЛЕКАРСТВЕННЫХ РАСТЕНИЙ, И БИОЛОГИЧЕСКИ АКТИВНАЯ ДОБАВКА НА ОСНОВЕ ЭТОЙ КОМПОЗИЦИИ | 2003 |
|
RU2252029C1 |
| ЭКСТРАКТ КАЛИНЫ, ОБЛАДАЮЩИЙ АНТИРАДИКАЛЬНОЙ АКТИВНОСТЬЮ | 2001 |
|
RU2220614C2 |
| ГИПОЛИПИДЕМИЧЕСКОЕ ФИТОСРЕДСТВО | 2013 |
|
RU2553309C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЭКСТРАКТА ИЗ ЯГОД МОРОШКИ АРКТИЧЕСКОЙ | 2021 |
|
RU2803797C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОАНТОЦИАНИДИНОВ ИЗ КОРЫ СОСНЫ ОБЫКНОВЕННОЙ | 2008 |
|
RU2375070C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОАНТОЦИАНИДИНОВ ИЗ ЛУБА КОРЫ БЕРЕЗЫ | 2008 |
|
RU2367460C1 |
| СПОСОБ ПЕРЕРАБОТКИ КОРЫ СОСНЫ | 2008 |
|
RU2400511C2 |
| СПОСОБ ПОЛУЧЕНИЯ УРСОЛОВОЙ КИСЛОТЫ | 2006 |
|
RU2329048C1 |
| СПОСОБ ПОЛУЧЕНИЯ АНТОЦИАНОВОГО КРАСИТЕЛЯ ИЗ ВЫЖИМОК ТЕМНЫХ СОРТОВ ЯГОД | 2012 |
|
RU2515478C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ АНТОЦИАНОВ В ЛЕКАРСТВЕННОМ РАСТИТЕЛЬНОМ СЫРЬЕ | 2013 |
|
RU2557953C2 |
Изобретение относится к химико-фармацевтической промышленности. Экстракт листьев Аронии черноплодной обладает антиоксидантной активностью и оказывает ингибирующее действие на все этапы перекисного окисления липидов в тканях печени. Содержит 72-78% фенольных соединений, в том числе не менее 25% олигомерных проантоцианидинов. Для его получения осуществляют экстракцию криопорошка листьев Аронии черноплодной (Aronia melanocarpa (Michx.) Elliot). Листья собирают перед началом и в период цветения. Экстрагируют кипящим водным спиртом с последующим отделением водно-спиртовых извлечений. Концентрируют их до водного раствора, его фильтруют. Очищают фильтрат петролейным или диэтиловым эфиром. Экстрагируют водный остаток смесью диэтилацетата и спирта при отношении в смеси 8 : 2 и концентрируют спиртоэтилацетатные извлечения до получения сухого остатка. Изобретение позволяет реализовать указанное назначение экстракта. 2 с. и 2 з.п. ф-лы, 1 табл.
| RU 93056445 A, 10.07.1996 | |||
| ВЕЩЕСТВО, ОБЛАДАЮЩЕЕ РАДИОПРОТЕКТОРНЫМ ДЕЙСТВИЕМ | 1991 |
|
RU2049473C1 |
| EP 0639336 A, 22.02.1995. | |||
Авторы
Даты
2001-07-27—Публикация
2000-05-05—Подача