Изобретение относится к биотехнологии и может быть использовано в технологии получения противовирусных средств широкого спектра действия.
Известен способ получения противовирусного средства, предусматривающий обработку платинида калия этилендиамином (Синтез комплексных соединений металлов платиновой группы. - М.: Наука, 1964, стр. 44).
Известен также способ получения противовирусного средства, предусматривающий синтез цис-дихлордиаминплатины (II) - ДДП - обработкой платинида калия аммониевой солью карбоновой кислоты, в качестве которой используют ацетат аммония, с последующим фильтрованием и кристаллизацией целевого продукта при охлаждении. Синтез ведут в течение 1,5 часа при температуре 100oC (там же, стр. 28). Синтез исходного материала ДДП длителен, используемый источник аммония дефицитен, при этом синтезируемый продукт токсичен (Биологические аспекты координационной химии, ред. Яцимирский К.Б., Киев: Наукова думка, 1978, стр. 152).
Наиболее близкий к заявляемому способу является способ получения противовирусного средства по заявке N 93037252/14, МКИ A 61 L 31/28, 33/24, который предусматривает обработку платинида калия аммониевой солью карбоновой кислоты, при этом в качестве аммониевой соли используют лигно-гуминовые соли карбоновой кислоты, которые предварительно синтезируют окислением лигнина в щелочной среде с последующим выделением лигно-гуминовых кислот их нейтрализацией аммиаком. Обработку платинида калия аммониевыми солями карбоновых кислот производят в режиме развитой акустической кавитации.
Окисление лигнина в щелочной среде приводит к увеличению молекулярной массы продукта - "лигнокислот" или же "гуминовых веществ", что приводит к увеличению мутности и агрегативной неустойчивости раствора "гуминовых веществ". Поэтому данный способ не обеспечивает получения качественных и стабильных лекарственных препаратов широкого спектра противовирусного действия.
Поставленная задача решается тем, что предложен способ получения противовирусного средства обработкой платинида калия аммониевыми солями лигно-гуминовых кислот под действием ультразвука в режиме развитой акустической кавитации, при этом окислению подвергают медицинский лигнин в щелочной среде при температуре 150-170oC в течение 0,5-1,5 часа при 2,0-2,5 МПа.
Как известно, под воздействием ультразвука в процессе обработки платинида калия аммониевыми солями лигно-гуминовых кислот происходит агрегирование веществ в растворе. Одновременно происходит увеличение количества химически активных центров.
Благодаря увеличению количества активных центров образуются комплексные высокомолекулярные агрегатные структуры.
Режимы окисления определялись экспериментально и выбирались из соображений получения оптимальных размеров молекул высокомолекулярных соединений.
Окисление медицинского лигнина в щелочной среде целесообразно проводить при температуре 150-170oC.
При снижении температуры ниже указанной для полного окисления приходится увеличивать время обработки, а при повышении температуры выше указанной происходит распад высокомолекулярных соединений на низкомолекулярные, что ведет к повышению мутности и снижению стабильности раствора.
Давление в реакторе определяет парциальное давление кислорода в обрабатываемом продукте, что влияет на скорость окисления.
Так, при давлении менее 2,0 МПа скорость окисления замедляется, что ведет к необходимости увеличения температуры или времени обработки.
При давлении больше 2,5 МПа интенсивность процесса увеличивается, что, как и при чрезмерном повышении температуры, приводит к разрушению высокомолекулярных соединений и снижению стабильности конечного продукта.
Таким образом, только при выбранных режимах окисления получаются молекулы оптимальных размеров, что обеспечивает получение качественных и стабильных препаратов.
Для подтверждения противовирусной активности полученного в результате использования заявленного способа препарата заявитель предлагает дополнить описание примерами использования указанного препарата для подавления вирусов гриппа и саркомы Рауса.
Таким образом, заявляемый способ отличается от прототипа тем, что в качестве лигно-гуминовых кислот, продуктов щелочного гидролиза лигнина, могут быть использованы окисленные энтеросорбенты на основе лигнина, такие как "Полифепан", "Лигносорб" и т.д.
Окисление медицинского лигнина в указанных условиях технологического процесса обеспечивает получение качественных и стабильных лекарственных препаратов широкого спектра противовирусного действия, что выгодно отличает его от средства по заявке РФ N 93037252.
"Полифепан" - неспецифический энтеросорбент (Рег. N 80/1211/3) представляет собой порошок коричневого цвета без запаха и вкуса, влажностью 65%. состоит в основном из лигнина и содержит не более 20% остаточных полисахаридов (гидроцеллюлозы).
"Лигносорб" (паста полифепана) ВФС 42-2203-93.
Все используемые в качестве исходного сырья вещества разрешены для приема внутрь организма.
Специальные исследования показали, что при окислении медицинского лигнина в условиях предлагаемого способа не происходит образования вредных для организма веществ, таких как полиароматические углеводороды, нитрозоамины и полихлорированные дицикло-п-диоксины.
Исследования противовирусной активности полученного согласно предлагаемому способу средства в отношении вирусов простого герпеса проводили с использованием перевиваемой культуры клеток почки эмбриона обезьяны (МА-104) и первичной культуры клеток куриных фибропластов.
Использовали вирусы простого герпеса 1-го и 2-го серотипов (штаммы "УС" N 571 и "ВН" N 572).
Испытания проводили после предварительной оценки токсичности препарата на указанных культурах клеток. В примерах использовали разведения препарата, составляющие 1/2 его минимальной токсической дозы, и принимали их за рабочую дозу препарата.
Нижеследующие примеры поясняют предлагаемое изобретение.
ПРИМЕР N 1
Исходную водно-щелочную суспензию медицинского лигнина (марки "Полифепан", рег. N 80/1211/3) - неспецифического энтерального copбента окисляли кислородом воздуха.
Состав суспензии
Содержание полифепана - 1 кг
Содержание щелочи (гидроксид натрия) - 100 г
Плотность суспензии - 1:9
Окисление проводили в реакторе с механическим перемешиванием при температуре 160 ± 5oC при давлении 2,5 MПa в течение 1 часа. Расход воздуха составил 5 л/мин.
Реакционную массу охлаждают до комнатной температуры и от раствора фильтрованием отделяют осадок. Фильтрат подкисляют серной кислотой до pH 2-3. Выпавший осадок отделяют фильтрованием, промывают дистиллированной водой, а затем водно-спиртовой смесью до установления pH 6,0-6,5 и высушивают при 105oC до постоянной массы. Полученные гуминовые кислоты нейтрализуют 5%-ным водным раствором аммиака из расчета 1 г гуминовых кислот на 80 мл указанного раствора, термостатируют в кипящей водяной бане до удаления избытка аммиака, фильтруют через бумажный фильтр и добавляют 30 об.% дистиллированной воды. В полученный раствор вносят по 0,17-0,27 мас.% платинида калия на 1 г гуминовых кислот и создают процесс развитой акустической кавитации под действием ультразвука с мощностью излучения 40 Вт/см и частотой 22 кГц в течение 1 мин. Далее раствор доводят меткой до 100 мл.
ПРИМЕР 2
Готовили растворы препарата в культуральной жидкости. Для оценки противовирусной активности использовали растворы препарата с рабочей дозой 0,03125 мг/мл. По 0,8 мл приготовленного раствора вносили в пробирки с монослойными культурами клеток и после контакта в течение 1 часа добавляли но 0,2 мл вирусов простого герпеса в десятичных разведениях. Полученную систему инкубировали в термостате при 37oC при ежедневном визуальном контроле. Регистрацию проводили на 5-6 сутки, когда цитопатическое действие вируса на клетки (ЦПД) достигало максимума. Инфекционную активность вируса оценивали по методу Рида и Менча. Противовирусную активность предлагаемого препарата оценивали по разнице титров вируса, выраженных в lg ТЦД 50/мл, в контрольных и опытных пробирках.
Предлагаемый препарат, взятый, как указано выше в концентрации 0,03125 мг/мл (рабочая доза) подавлял инфекционную активность вируса простого герпеса 2-ю серотипа ("ВН") в условиях эксперимента на 2,5 lg ТЦД
Противовирусная активность предлагаемого средства в отношении вируса простого герпеса 1-го серотипа ("УС") установлена в 10 раз ниже в таких же условиях по сравнению с вирусом 2-го серотипа ("ВН") и составила 100 ТЦД 50 мл.
Противовирусная активность ремантадина в равных условиях в отношении к вирусам герпеса составила 1,0-1,5 lg ТЦД 50/мл при его концентрации в культуральной жидкости равной 0,125 мг/мл (рабочая доза).
Таким образом, противовирусная активность предлагаемого средства с концентрацией в рабочей дозе, равной 0,03125 мг/мл, составляет 500 ТЦД 50/мл в отношении к вирусу простого герпеса 2-го серотипа (штамм "ВН") и 100 ТЦД 50/мл в отношении к вирусу простого герпеса 1-го серотипа (штамм "УС"). Противовирусная активность предлагаемого средства в 10-100 раз выше по сравнению с активностью ремантадина, содержащего в рабочей дозе 0,125 мг/мл препарата.
ПРИМЕР 3
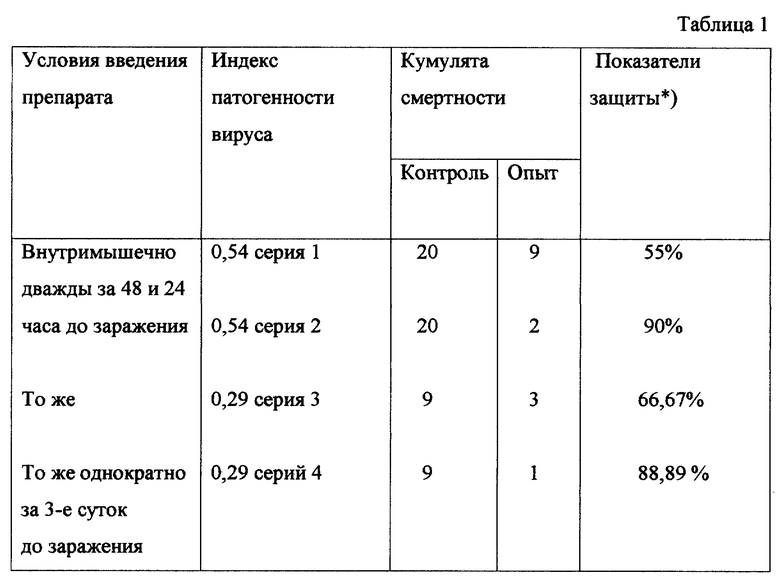
Для тестирования полученного в результате использования заявленного способа препарата последний в объеме 0,2 мл вводили внутримышечно белым мышам за 1-3 суток до заражения их вирусом гриппа типа A (PR-8). Контрольная группа препарата не получала. Результаты приведены в табл. 1
ПРИМЕР 4
14-дневным цыплятам породы "Белый леггорн" яйценосной линии "Хайсенс", высокочувствительных к вирусу саркомы Рауса BH-RSV(RAV-1) серологической подгруппы A, вводили суспензию данного вируса в крыловые перепонки в дозах 100 ОД-50 (левое крыло) и 100 ОД-50 (правое крыло). На 4-6 сутки у цыплят наступают некротические явления.
Для тестирования полученного в результате использования заявленного способа препарата последний в объеме 0,2 мл вводили за 24 и за 48 часов до заражения.
Контрольная группа препарат не получала.
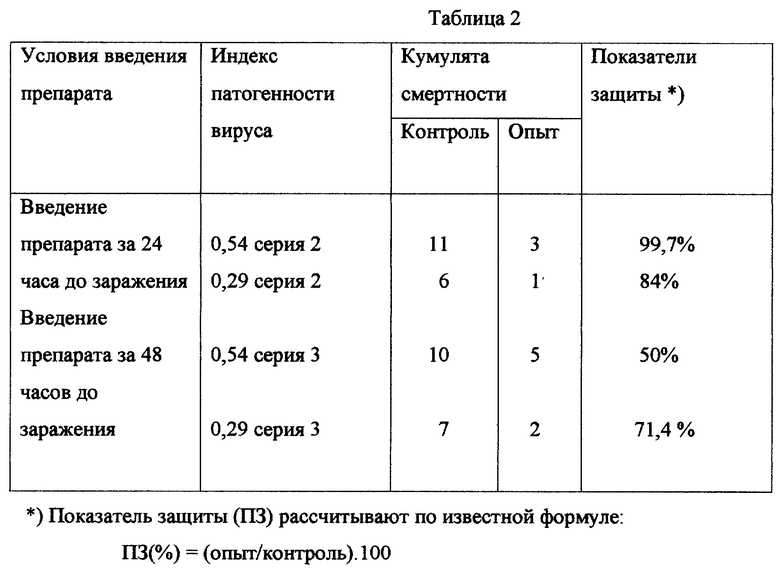
Результаты приведены в табл. 2
Как видно из таблицы, использование препарата обеспечивает защиту от вируса в среднем на 76%.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПРОТИВООПУХОЛЕВОГО СРЕДСТВА | 2000 |
|
RU2182482C1 |
| АНТИРАКОВОЕ СРЕДСТВО | 2001 |
|
RU2178702C1 |
| АНТИАНГИОГЕННОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2009 |
|
RU2404783C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА "ОЛИПИФАТ" ДЛЯ ЛЕЧЕНИЯ НЕОНКОЛОГИЧЕСКИХ ПАТОЛОГИЙ ОРГАНИЗМА | 1998 |
|
RU2141334C1 |
| ТВЕРДАЯ ДОЗИРОВАННАЯ ФОРМА ДЛЯ ПЕРОРАЛЬНОГО ПРИМЕНЕНИЯ, ОБЛАДАЮЩАЯ ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ (ВАРИАНТЫ) | 1995 |
|
RU2115415C1 |
| ЛЕКАРСТВЕННЫЙ ГЕЛЬ | 2000 |
|
RU2184564C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ ГЕМИНА С АНТИБАКТЕРИАЛЬНОЙ И ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ | 2011 |
|
RU2475498C1 |
| ПРОТИВОВИРУСНОЕ ГУМИНОВОЕ СРЕДСТВО | 2020 |
|
RU2753609C1 |
| КОНЪЮГАТЫ ГОССИПОЛА И НАТРИЙКАРБОКСИМЕТИЛЦЕЛЛЮЛОЗЫ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ПРОТИВОВИРУСНЫЕ СРЕДСТВА НА ИХ ОСНОВЕ | 2012 |
|
RU2499002C1 |
| Противовирусное средство на основе гуминовых кислот | 2018 |
|
RU2678986C1 |
Изобретение относится к медицине. Проводят обработку платинида калия под действием ультразвука в режиме развитой акустической кавитации аммониевой солью карбоновой кислоты. В качестве этой соли используют гуминовые вещества, выделенные из окисленного медицинского лигнина кислородом воздуха в водно-щелочной среде при температуре 150-170°С и давлении 2,0-2,5 МПа в течение 0,5-1,5 ч. Изобретение позволяет повысить стабильность продукта. 2 табл.
Способ получения противовирусного средства обработкой платинида калия под действием ультразвука в режиме развитой акустической кавитации аммониевой солью лигногуминовых карбоновых кислот, полученных окислением лигнина в щелочной среде, отличающийся тем, что окислению подвергают медицинский лигнин при 150-170°С в течение 0,5-1,5 ч при давлении 2,0-2,5 МПа.
| RU 93037252 A, 10.01.1997 | |||
| СПОСОБ ПОЛУЧЕНИЯ ВОДНОГО РАСТВОРА, СОДЕРЖАЩЕГО АКТИВНЫЕ ВЕЩЕСТВА АНТИВИРУСНОГО ДЕЙСТВИЯ | 1991 |
|
RU2104016C1 |
| US 4873226 A, 10.10.1989 | |||
| US 4419351 A, 06.12.1983. | |||
Авторы
Даты
2001-08-20—Публикация
2000-06-19—Подача