Изобретение относится к уничтожению боевых отравляющих веществ кожно-нарывного действия, а именно к разработке способа утилизации отравляющего вещества типа люизита.
В настоящее время для решения проблемы массового уничтожения ОВ кожно-нарывного действия типа люизит предложено несколько методов. Эти методы основаны на реакциях хлорирования, сплавления люизита с серой, обработки спиртовыми растворами алкоголятов щелочных металлов, высокотемпературного восстановления водородом. Однако эти технологии имеют ряд существенных недостатков и не прошли конкурсный отбор альтернативных методов уничтожения (утилизации) люизита. Для полномасштабного использования в России рекомендовано два способа: аммиачного восстановления и щелочного гидролиза.
Аммиачное восстановление люизита осуществляют в реакторе в интервале температур 650 - 700oC. Технический люизит, прошедший предварительную очистку фильтрованием, подают в реактор, где происходит его восстановление аммиаком до элементарного мышьяка и хлористого аммония. Образующуюся парогазовую смесь смешивают с водным потоком в скруббере, затем из водной суспензии последовательно выделяют мышьяк и хлористый аммоний.
Метод аммиачного восстановления люизита (аммонолиз) имеет следующие недостатки:
сложность проведения реакции (высокая температура);
необходимость в стадии подготовки ОВ к утилизации (узел фильтрации);
высокая взрыво - пожароопасность;
Основной технологией уничтожения (утилизации) люизита считается щелочной гидролиз с последующим электролизом реакционных масс и выделением мышьяка. На первой стадии люизит подвергают гидролизу при температуре 80-110oC путем добавления его в раствор едкого натра. Процесс полной дегазации люизита в этих условиях завершается в течение 0,5-1 часа, после чего раствор подают на стадию электролиза. В процессе электролиза получают мелкодисперсный мышьяк, и гипохлорит натрия [1].
При явных достоинствах первой стадии этой технологии дальнейшая переработка реакционной массы электролизом имеет ряд существенных недостатков:
высокая стоимость и сложность реализации процессов;
энергоемкость;
значительное количество побочных, в том числе токсичных отходов,
Кроме того, основным продуктом на второй стадии является мышьяк в мелкодисперсной форме. Однако, элементарный мышьяк находит весьма ограниченное применение. Наиболее широко используются неорганические мышьяксодержащие соединения.
Техническая задача данного изобретения - усовершенствование способа утилизации люизита щелочным гидролизом, позволяющее получать полезное мышьяксодержащее соединение, пригодное к реализации и длительному безопасному хранению - арсенат натрия.
Эта задача достигается обработкой реакционной массы, образующейся в процессе гидролиза люизита, водным раствором перекиси водорода в количестве, обеспечивающем окисление арсенита иона AsO3 3- в арсенат AsO4 3-. Упариванием реакционной массы до содержания арсенат-иона в реакционной массе 120 г/кг, охлаждением раствора при pH>13 до начала выкристаллизовывания арсената натрия и отделением последнего фильтрованием.
Согласно уравнениям реакции гидролиза люизита основным образующимся мышьяк содержащим соединением является арсенит натрия [2]. Образуемые при щелочном гидролизе люизита арсениты могут быть трансформированы в арсенаты при действии окислителей.
Исходя из этого, теоретически можно предложить следующую схему выделения арсената натрия из реакционной массы:
NaCl + Na3AsO3 + H2O ---> Na3AsO4 + NaCl ---> Na3AsO4 • 12H2O + NaCl.
Окисление может быть осуществлено различными типовыми окислителями. В качестве окислителя выбран широко распространенный товарный продукт 33%-ный водный раствор перекиси водорода. По сравнению с большинством других окислителей перекись водорода менее агрессивна и безопасна, кроме того практически не увеличивает общий объем получаемой реакционной массы (не считая воды).
Процесс проводят следующим образом. После разложения люизита продукты щелочного гидролиза охлаждают до температуры 20 - 30oC и обрабатывают избытком водного раствора перекиси водорода. Вследствие экзотермичности реакции окисления температура постепенно повышается до 80oC и в конце доводится до кипения. Полученную реакционную массу при интенсивном перемешивании кипятят 90 минут и горячей фильтруют. Смолообразные продукты, образующиеся при гидролизе, при кипячении коагулируются и легко отделяются на фильтре. Профильтрованный раствор прозрачен и имеет слабо желтый цвет.
Процесс окисления арсенита натрия происходит в соответствии с уравнением:
Na3AsO3 + H2O2 ---> Na3AsO4 + H2O.
После охлаждения фильтрата из раствора выкристаллизовывается соль арсената натрия с примесью хлорида натрия.
Установлено, что определяющими параметрами выхода арсената натрия в процессе выделения из реакционной массы являются: основность (pH) среды, концентрация арсенат иона AsO4 3- в реакционной массе, количество перекиси водорода.
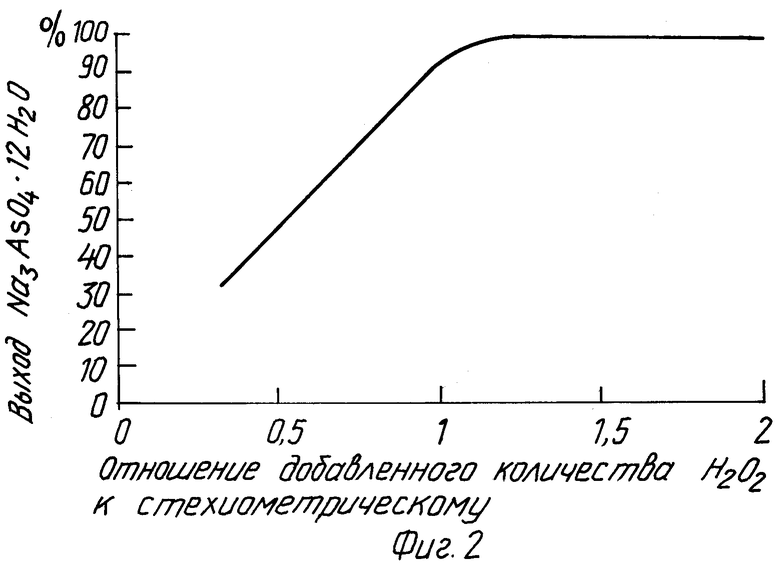
Достаточно полное выделение арсената происходит из концентрированных растворов, что требует отгонки определенного количества воды. Зависимость выхода арсената натрия и хлористого натрия от концентрации AsO4 3- в реакционных массах представлена на фиг. 1.
Как видно из приведенного графика, оптимальный выход выделившегося арсената достигается при содержании AsO4 3- в реакционной массе 120 г/кг. Такая концентрация позволяет количественно выделять арсенат натрия (кристаллогидрат) из раствора.
Наиболее полно арсенат натрия осаждается при температуре 0-5oC, при более низкой температуре увеличивается доля хлористого натрия в продукте, выше 10oC снижается выход осаждаемого кристаллогидрата. В пределах указанных границ состав осаждающегося продукта меняется незначительно.
Зависимости выхода продукта от количества добавляемой перекиси водорода представлена на фиг. 2.
Как видно из графика, 1,4-кратного избытка по сравнению со стехиометрическим отношением достаточно для проведения процесса, меньший избыток не целесообразен по соображениям надежности.
Из фильтрата, остающегося после отделения арсената натрия, содержащего остаточные количества арсената и хлорид натрия, удаляют примеси мышьяка известными методами.
В частности, микропримеси мышьяка удаляются в щелочной среде соосаждением с гидроокисью железа.
Оставшийся раствор, в котором практически остался хлористый натрий, упаривают. Вода возвращается обратно в процесс, а хлористый натрий используют в технических целях.
Предложенный способ утилизации люизита обладает следующими достоинствами:
практически полной конверсией люизита в безопасные соли арсената натрия;
простота технологического оформления процесса, реализуемого с использованием стандартного химического оборудования;
использование доступного исходного сырья (водного раствора перекиси водорода);
конечные продукты могут быть использованы в коммерческих целях, в частности арсенат натрия, который широко используется для наработки известных инсектицидных и фунгицидных препаратов;
предложенный способ отличается простотой, относительно малым количеством отходов, дешевизной и малым расходом реагентов.
Таким образом, предлагаемый способ утилизации реакционных масс, образующихся в результате щелочного гидролиза люизита, является более экономичным, позволяет при наименьших затратах получать полезные мышьяксодержащие соединения, пригодные к реализации и безопасному длительному хранению.
Пример 1. В реактор загружают 20%-ный водный раствор едкого натра (в расчете на мольное соотношение ЛЮИЗИТ : NaOH 1:6). Колбу с раствором нагревают до 35oC, после чего из капельной воронки начинают равномерно прикапывать люизит. Скоростью прикапывания регулируют температуру реакции и интенсивность выделения ацетилена.
После прибавления люизита смесь кипятят 1 час, после чего охлаждают до температуры 20oC и обрабатывают 1,4 мольным избытком перекиси водорода. Температуру в ходе прикапывания поддерживают в пределах 60 - 80oC. Полученную реакционную массу при интенсивном перемешивании нагревают, кипятят 90 минут и горячей фильтруют.
Смолообразные продукты, образующиеся при гидролизе, отфильтровывают, фильтрат охлаждают до температуры 0 - 5oC. Выпавшие кристаллы арсенат натрия отфильтровывают и высушивают до постоянной массы.
Осадок представляет собой белое кристаллическое вещество с содержанием арсената натрия Na3AsO412H2O - 96%, остаточное содержание люизита составляет < 1•10-5 мг/г. Выход арсената натрия - количественный > 99%.
Из фильтрата, остающегося после отделения арсената натрия, удаляют микропримеси мышьяка соосаждением с гидроокисью железа,
Пример 2. В реактор загружают 20%-ный водный раствор едкого натра (NaOH - 70,8 г, H2O - 267,2 мл). Колбу с раствором нагревают до 35oC, после чего из капельной воронки равномерно прикапывают 57,4 г люизита. Скоростью прикапывания регулируют температуру реакции и интенсивность выделения ацетилена.
После прибавления люизита смесь кипятят 1 час, после чего охлаждают до температуры 20oC и обрабатывают 52 мл перекиси водорода. Температуру в ходе прикапывания поддерживают в пределах 60 - 80oC. Полученную реакционную массу при интенсивном перемешивании нагревают, кипятят 90 минут и горячей фильтруют.
Смолообразные продукты (0,3 г), образующиеся при гидролизе, отфильтровывают, фильтрат охлаждают до температуры 0 - 5oC. Выпавшие кристаллы арсенат натрия отфильтровывают и высушивают до постоянной массы. Масса осадка составляет 113 г.
Осадок представляет собой белое кристаллическое вещество с содержанием арсената натрия Na3AsO4 • 12H2O - 96%, остаточное содержание люизита составляет < 1 • 10-5 мг/г. Выход арсената натрия - количественный > 99%.
Из фильтрата, остающегося после отделения арсената натрия, удаляют микропримеси мышьяка соосаждением с гидроокисью железа.
Оставшийся раствор, в котором практически остался хлористый натрий, упаривают. Полученный хлористый натрий в количестве 44,8 г используют в технических целях, а вода возвращается обратно в процесс.
Список используемой литературы:
1. Петрунин В. А. , Баранов Ю.И., Кузнецов А.Б. и др. Рос. хим. ж. (Ж. Рос. хим. о-ва им. Д.И. Менделеева), 1995, т. 39 N 4, с. 15-16.
2. Александров В. Н., Емельянов В.И. Отравляющие вещества. М.: Военное издательство, 1990.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПЕРЕРАБОТКИ АРСЕНИТА НАТРИЯ ГИДРОЛИЗНОГО В ТОВАРНУЮ ПРОДУКЦИЮ | 2012 |
|
RU2513846C1 |
| СПОСОБ ПЕРЕРАБОТКИ РЕАКЦИОННЫХ МАСС, ОБРАЗУЮЩИХСЯ ПРИ ЩЕЛОЧНОМ ГИДРОЛИЗЕ ЛЮИЗИТА, В ТЕХНИЧЕСКИЕ ПРОДУКТЫ | 2009 |
|
RU2396099C1 |
| СПОСОБ УНИЧТОЖЕНИЯ ЛЮИЗИТА | 2001 |
|
RU2209103C1 |
| СПОСОБ ПЕРЕРАБОТКИ ПРОДУКТОВ ДЕТОКСИКАЦИИ ЛЮИЗИТА | 2001 |
|
RU2198707C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭЛЕМЕНТНОГО МЫШЬЯКА | 2008 |
|
RU2409687C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЭЛЕМЕНТНОГО МЫШЬЯКА И ХЛОРИДА НАТРИЯ ИЗ ПРОДУКТОВ ЩЕЛОЧНОГО ГИДРОЛИЗА ЛЮИЗИТА | 2009 |
|
RU2412734C2 |
| СПОСОБ ПЕРЕРАБОТКИ РЕАКЦИОННЫХ МАСС, ОБРАЗУЮЩИХСЯ В ПРОЦЕССЕ ДЕТОКСИКАЦИИ ЛЮИЗИТА | 2001 |
|
RU2192297C1 |
| СПОСОБ ДЕТОКСИКАЦИИ ФРАГМЕНТОВ РАЗРУШЕННЫХ ПРОИЗВОДСТВЕННЫХ ЗДАНИЙ, ЗАГРЯЗНЕННЫХ ЛЮИЗИТОМ И ПРОДУКТАМИ ЕГО ПРЕВРАЩЕНИЙ | 2004 |
|
RU2299100C2 |
| СПОСОБ УТИЛИЗАЦИИ КОМПОЗИЦИИ МЫШЬЯКОРГАНИЧЕСКИХ ВЕЩЕСТВ ИЗ ГОСУДАРСТВЕННОГО МОГИЛЬНИКА, СОДЕРЖАЩЕЙ 10-ХЛОР-5,10-ДИГИДРОФЕНАРСАЗИН | 1998 |
|
RU2172195C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЭЛЕМЕНТНОГО МЫШЬЯКА ИЗ ВОДНЫХ И ВОДНО-ОРГАНИЧЕСКИХ РАСТВОРОВ МЫШЬЯКСОДЕРЖАЩИХ СОЕДИНЕНИЙ | 2008 |
|
RU2371391C1 |
Изобретение относится к уничтожению отравляющих веществ кожно-нарывного действия, а именно к разработке способа утилизации люизита. Предложен способ утилизации люизита, включающий щелочной гидролиз последнего раствором едкого натра, отличающийся тем, что образующиеся после гидролиза реакционные массы окисляют при 60-80°С водным раствором перекиси водорода до арсената натрия. Полученный раствор упаривают до содержания арсенат-иона в реакционной массе 120 г/кг, охлаждают до 0 - 5°С, арсенат натрия (Na3AsO4 • 12H2O) отделяют фильтрованием при рН среды >13. Изобретение позволяет повысить выход арсената натрия до 99%. 1 з.п.ф-лы, 2 ил.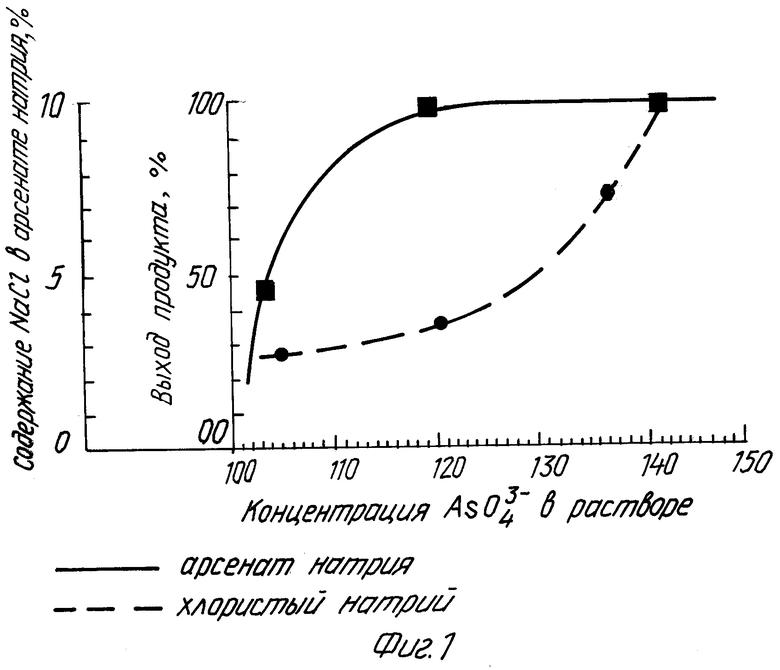
| ПЕТРУНИН B.A | |||
| и др | |||
| МАТЕМАТИЧЕСКОЕ МОДЕЛИРОВАНИЕ ПРОЦЕССА ЩЕЛОЧНОГО ГИДРОЛИЗА ЛЮИЗИТА | |||
| - Российский химический журнал, 1995, т | |||
| XXXIX, 4, с.15-16 | |||
| RU 94018719 А1, 10.04.1997 | |||
| ЗАРЯДНОЕ УСТРОЙСТВО ДЛЯ АККУМУЛЯТОРА, СЕТЬ ИЗ НЕСКОЛЬКИХ ЗАРЯДНЫХ УСТРОЙСТВ И СПОСОБ ИХ РАБОТЫ | 2011 |
|
RU2553617C2 |
| DE 3607424 А1, 10.09.1987 | |||
| DE 2919661 B2, 27.11.1998. | |||
Авторы
Даты
2001-08-20—Публикация
1999-01-25—Подача