Изобретение относится к области офтальмологии, в частности, к разработке новых препаратов, предназначенных для ухода за средствами контактной коррекции зрения - мягкими контактными линзами, которые обеспечивают их эффективную очистку от белковых отложений за счет расщепления последних протеолитическими ферментами.
В процессе ношения мягкие контактные линзы находятся в постоянном контакте со слезной жидкостью, роговицей и веком глаза, а также испытывают неблагоприятные воздействия со стороны внешней среды (дым, загрязнения воздуха, косметика, цветочная пыльца и др.). Образующиеся при этом отложения на поверхности контактных линз, как правило, включают следующие классы веществ: белки, липиды, муцины, неорганические вещества, факторы внешней среды, косметику. Белки являются естественными компонентами слезной пленки и ответственны за образование значительной части отложений. Содержание общего белка в слезной жидкости достаточно велико и составляет в норме около 20 г/л.
Микротравма глаза и раздражение поверхности роговицы повышают как общую секрецию слезной жидкости, так и концентрацию белка в ней, основными компонентами которого в числе 60 выделенных белковых фракций являются лизоцим, альбумины, глобулины и разнообразные гликопротеины [Петрович Ю.А., Терехина Н. А. Биохимия слезы и ее изменение при патологии // Вопросы мед. химии. - 1990. - Т. 36. - Вып. 3. - С. 13- 18]. Указанные белки, прежде всего лизоцим, являются при величинах pH 6,5 - 7,8, что соответствует нормальной кислотности слезной жидкости у большинства пациентов, сильно заряженными макромолекулами, способными легко адсорбироваться на полимерной поверхности мягких контактных линз и создавать непрозрачные или частично прозрачные белковые отложения. Указанные отложения существенно ухудшают как оптические свойства мягких контактных линз, так и комфортность их ношения, и сокращают в целом длительность их эксплуатации.
В отличие от неорганических отложений, прежде всего малорастворимых кальциевых солей и других загрязнений, легко удаляемых детергентами или комплексонами типа динатриевой соли этилендиаминтетрауксусной кислоты (Трилон Б) или солями лимонной кислоты, белковые отложения устойчивы к действию этих очищающих агентов, и борьба с ними составляет серьезную проблему клинического применения мягких контактных линз.
Среди предложенных методов удаления белковых отложений с поверхности мягких контактных линз известно применение специфических детергентов, например, специальных анионных ПАВ [Пат. США N 4808239 (1989), МКИ В 08 В 7/00] или алкилфенилполиэфиров [Пат. США N 3954965 (1976), МКИ A 61 К 31/78; Пат. США N 5190594 (1993), МКИ B 08 B 3/08], а также высокодисперсных абразивных материалов в присутствии анионных ПАВ [Пат. США N 4655957, МКИ C 11 Q 7/26, A 61 К 7/00; Пат. США N 5089053 (1992), МКИ B 08 B 3/08].
Однако наиболее эффективным методом удаления белковых отложений является обработка мягких контактных линз водными растворами протеолитических ферментов [Пат. США N 4285738 (1981), МКИ B 08 B 3/08], среди которых наиболее высокой очищающий способностью обладают бромелаин [Пат. США N 4521254 (1985), МКИ B 08 B 3/08], папаин [Пат. США N 4609493 (1986), МКИ C 11 D 1/06], панкреатин [Пат. США N 4921630 (1990), МКИ C 11 D 3/14], субтилизин A [Пат. США N 5281277 (1994), МКИ A 61 L 2/04], а также ферменты класса гликозидаз [Пат. США N 4710313 (1987), МКИ C 11 D 7/32]. Несмотря на то, что указанные растворы быстро и эффективно удаляют белковые отложения с поверхности контактных линз, использоваться они могут только в течение непродолжительного времени после приготовления, поскольку в водных растворах протеолитические ферменты нестабильны и полностью утрачивают свою активность в течение нескольких часов (папаин, панкреатин) или суток (субтилизин А).
В этой связи наиболее распространенными индивидуальными средствами для ферментной очистки мягких контактных линз стали ферментные таблетки, содержащие, наряду с компонентами буферного раствора и необходимыми активаторами, в среднем 10 мг папаина [Пат. США N 3910296 (1975), МКИ B 08 B 3/08], 25 - 50 мг панкреатина [Пат. США N 4096870 (1978), МКИ B 08 B 3/08] или 1 мг субтилизина А [Пат. США N 5356555 (1994), МКИ A 61 L 2/16], которые растворяют в дистиллированной воде, изотоническом растворе натрия хлорида или в специальном растворе для хранения, взятых в объеме 5-15 мл, что соответствует среднему объему контейнера для хранения и обработки мягких контактных линз. Таблетированные формы протеолитических ферментов имеют достаточно длительный срок хранения (1 год и более), однако имеют значительную стоимость, сложны в изготовлении, а их применение связано с затратами времени и дополнительными манипуляциями по растворению таблеток в используемых растворах.
Альтернативными и значительно более удобными для практического применения препаративными формами ферментных средств для очистки мягких контактных линз являются концентрированные растворы, несколько капель которых содержит эквивалентное таблеткам количество соответствующего фермента. Одним из способов длительного сохранения ферментной активности протеолитических ферментов в таких растворах, например, папаина [Пат. США N 4715899 (1987), МКИ В 08 В 3/08] является перевод фермента в инактивированную форму путем обработки тетратионатом натрия или другими соединениями, создающими дополнительные дисульфидные S-S связи в его структуре. Непосредственно перед использованием этого раствора для очистки контактных линз фермент снова переводят в активную форму путем восстановления цистеином или меркаптоэтанолом до соответствующей сульфгидрильной SH-формы. Существенным недостатком данного способа является необходимость использования цикла "дезактивация - активация", что делает этот метод сложным, дорогостоящим и практически непригодным для массового индивидуального применения.
Другим способом сохранения протеолитической активности ферментов в их концентрированных растворах является применение стабилизаторов, например, сульфита натрия и (или) пентабората натрия [Пат. США N 4404115 (1983), МКИ C 11 D 3/04]. Указанные стабилизаторы при их содержании в растворе от 1 до 15% (в среднем 4,5-9%) и концентрации фермента от 0,001 до 10% (предпочтительно 0,01-5%) обеспечивают сохранение протеазной активности в течение трех недель при температуре 37oC, что приблизительно соответствует 3 -4 месяцам хранения препарата при комнатной температуре. Однако круг протеолитических ферментов, пригодных для использования с данными стабилизаторами, ограничивается в основном бактериальными протеазами, например, субтилизинами матаксазой или алкалазой, для которых оптимальный диапазон рабочих значений pH находится в пределах 8-11. Кроме того, период времени, в течение которого ферментный препарат сохраняет свою активность, также недостаточно велик.
Наиболее близким по технической сущности к предлагаемому изобретению (прототип) является жидкий препарат для ферментной очистки мягких контактных линз от белковых отложений, содержащий, мас.%: 0,001 - 1,0 панкреатина, 0,05 - 2,0 борной кислоты и/или натрия тетраборнокислого, 0,1 - 1,50 натрия хлористого, 0,01 - 1,0 Трилона Б, 0,5 - 2,0 полиэтиленгликоля, 0,5 - 2,0 глицерина и воду [Пат. США N 5409546 (1995), МКИ В 08 В 3/08]. Недостатком указанного препарата является высокая концентрация воды, составляющая 91-99%, что способствует гидролитическому неферментативному расщеплению панкреатина, а также отсутствие эффективных антисептических компонентов, подавляющих развитие микроорганизмов в препарате при его длительном хранении. Значительное содержание Трилона Б при отсутствии добавок солей кальция не позволяет достигать высокой протеолитической активности при использовании данного концентрированного препарата при приготовлении рабочих разбавленных растворов.
Целью изобретения является разработка нового жидкого препарата, предназначенного для длительного использования в целях ферментной очистки мягких контактных линз от белковых отложений.
Сущность изобретения заключается в использовании водно-органического раствора панкреатина, содержащего стабилизаторы, обеспечивающие сохранение протеолитической активности фермента в течение длительного времени, и имеющего следующий количественный состав, мас.%:
Панкреатин - 0,1 - 1,0
Натрий хлористый - 0 - 5,0
Натрий тетраборнокислый - 1,0 - 4,0
Кислота борная - 0,5 - 2,0
Трилон Б - 0,1 - 0,5
Кальций хлористый - 0 - 0,1
Антисептик - 0,01 - 0,1
Полиэтиленгликоль - 0 - 25,0
Глицерин - 25,0 - 50,0
Вода - Остальное
Панкреатин, получаемый из препаратов поджелудочной железы крупного рогатого скота, является одним из наиболее удобных и безопасных протеолитических ферментных препаратов, обладающих высокой активностью. Панкреатин содержит важнейшие протеолитические ферменты панкреатического сока - трипсин и химотрипсин, которые расщепляют не только пептидные, но и амид- ные, эфирные, гидразидные и фосфамидные связи, при этом оптимум действия этих ферментов находится в диапазоне pH 8 - 9. Кроме протеолитических ферментов панкреатин содержит значительное количество амилазы, способной легко гидролизовать α-1-4- гликозидные связи полисахаридов [Клиническая ферментология. Под ред. Э. Щеклика. Варшава, 1966, с. 175 - 198], что может иметь важное значение для повышения эффективности очистки поверхности контактных линз от гликопротеинов. Панкреатин и его компоненты малотоксичны, обладают по сравнению с папаином значительно менее выраженным раздражающим действием на слизистые оболочки и широко используются в качестве лекарственных средств, в том числе и в виде глазных капель [Машковский М.Д. Лекарственные средства. Т. 2. М.: Медицина, 1993, с. 56 - 60]. В этой связи панкреатин обладает существенными преимуществами по сравнению с другими доступными протеолитическими ферментами для разработки на его основе средств для ферментной очистки мягких контактных линз.
Важнейшим компонентом предлагаемого препарата является Трилон Б. Известно, что каталитическая активность трипсина и химотрипсина очень сильно зависит от присутствия ионов кальция. С другой стороны, амилаза - один из компонентов панкреатина, содержит как минимум 1 моль ионов кальция на 1 моль фермента [Клиническая ферментология. Под. ред. Э. Щеклика. Варшава, 1966, с. 175-198], и по этой причине кальций всегда присутствует в препаратах панкреатина. Содержание Трилона Б в количестве 0,1 - 0,25 мас.% обеспечивает полное связывание кальция, подавляет таким образом автокатализ ферментов и способствует длительному сохранению их нативной структуры в растворе. Разбавление исходного концентрированного раствора в 25-50 раз путем добавления 5-10 его капель (0,2-0,4 мл) к 10 мл раствора для хранения мягких контактных линз обеспечивает концентрацию ионов кальция, необходимую для достижения достаточной протеолитической активности. Дополнительное введение в рецептуру исходного раствора хлористого кальция CaCl2 • 6 H2О в количестве до 0,1 мас.% позволяет практически в 2 раза повысить активность ферментов, однако требует увеличения содержания Трилона Б до 0,5 мас.% для достижения их необходимой стабильности в исходном концентрированном растворе при длительном хранении. При отсутствии Трилона Б и наличии хлорида кальция предлагаемый препарат, соответствующий в остальном примеру 1 (табл. 1) через месяц сохраняет свою протеолитическую активность только на 10%.
В целях достижения изотоничности конечного раствора ферментного препарата при использовании для его разбавления дистиллированной воды он может дополнительно содержать в своем составе до 5,0 мас.% натрия хлорида.
В качестве антисептиков, подавляющих развитие микроорганизмов в препарате при его хранении, был использован хлоргексидина биглюконат (20%-ный водный раствор) в количестве до 0,1 мас.% или полигексанид (полигексаметиленбигуангида гидрохлорид, 20%-ный водный раствор, Cosmocil CQ) производства фирмы ZENECA Ltd. (США), широко используемый в настоящее время в различных растворах для ухода за контактными линзами, в количестве до 0,01 мас.%.
Предельные соотношения воды, глицерина и полиэтиленгликоля марки ПЭГ-300 или ПЭГ-400 обеспечивают необходимую растворимость панкреатина и неорганических компонентов препарата в водно-органическом растворе, а также его реологические свойства и морозоустойчивость.
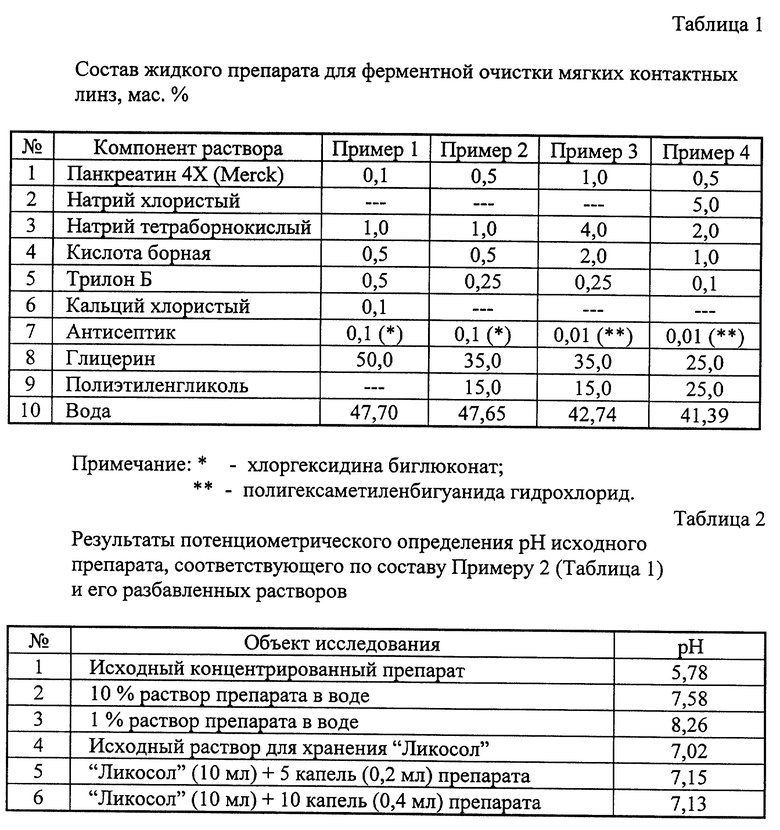
Пример 1. В 47,7 г воды последовательно растворяют при комнатной температуре 1,0 г натрия тетраборнокислого, 0,5 г кислоты борной, 0,5 г Трилона Б и 0,1 г кальция хлористого, добавляют 0,1 г панкреатина 4Х (Merck) и 0,1 г 20%-ного раствора хлоргексидина биглюконата, перемешивают при комнатной температуре в течение 1 ч и фильтруют. К фильтрату добавляют при перемешивании 50,0 г глицерина, следя за тем, чтобы температуре раствора не превышала 40oC, и получают 100 г жидкого ферментного препарата.
Препараты согласно примерам 2 - 4 получают аналогично. Состав предлагаемого препарата представлен в табл. 1.
Сохранению высокой стабильности ферментов панкреатина в предлагаемом водно-органическом растворе способствуют компоненты боратного буфера - натрий тетраборнокислый Na2B4O7•10H2O и кислота борная H3BO3, которые обладают способностью вступать во взаимодействие с глицерином с образованием кислых эфиров борной кислоты, что обеспечивает смещение величины pH из рабочего диапазона ферментов в область повышенной кислотности - до значений pH 5,5 - 6,0, что также подавляет автокатализ протеолитических ферментов панкреатина в растворе. При разбавлении исходных концентрированных растворов ферментов в 25 - 50 раз при обработке мягких контактных линз дистиллированной водой или специальным раствором для хранения "Ликосол" производства ООО "МЕДСТАР" [ТУ 9318-001-34704936-96] указанные эфиры борной кислоты подвергаются гидролизу, что приводит к увеличению значения pH практически до рабочего диапазона протеолитических ферментов (табл. 2).
Протеолитическую активность препаратов, соответствующих примерам 1 - 4 (табл. 1), в сравнении с чистым исходным панкреатином 4X производства фирмы Merck и известными таблетированными ферментными препаратами проводили по методике, описанной в Государственной фармакопее СССР IX издания [Ст. 362. Панкреатин] . Предлагаемый препарат согласно примеру 2 был также подвергнут анализу после 3, 6, 9 и 12 месяцев хранения в прозрачной полиэтиленовой таре на рассеянном свету при комнатной температуре.
Подготовка к анализу. Приготовление растворов.
Раствор A. 0,4 М раствор борной кислоты. 12,4 г борной кислоты растворяют в дистиллированной воде и доводят объем раствора до 500 мл.
Раствор B. Ацетатная смесь. Смешивают 250 мл 1 М раствора уксусной кислоты и 250 мл 1 М раствора ацетата натрия.
Раствор C. 0,2% раствор казеина. 0,2 г казеина по Гаммерстену заливают 20 мл дистиллированной воды, добавляют 5 мл 0,1 н. раствора едкого натра и нагревают на водяной бане до полного растворения. Охлаждают, добавляют 5 мл 0,4 М раствора борной кислоты (A) и доводят объем раствора до 100 мл.
Раствор D. Исследуемый раствор препарата. 2,0 или 4,0 г препарата, соответствующего примерам 1 - 4, растворяют в 50 мл дистиллированной воды и доводят объем раствора до 100 мл.
Проведение анализа.
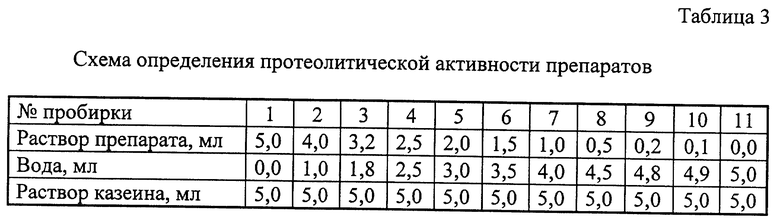
В 11 пронумерованных пробирок последовательно вносят градуированными пипетками исследуемый раствор препарата (D), дистиллированную воду и раствор казеина (C) в соответствии со следующей схемой (табл. 3).
Содержимое пробирок тщательно перемешивают и нагревают на водяной бане при температуре 40 ± 2oC в течение 30 мин. Через указанное время вынимают пробирки из бани и прибавляют в каждую по 0,5 мл ацетатной смеси (В). Та пробирка, в которой раствор сохраняет свою прозрачность, считается предельной. Пробирка N 11 не содержит фермента и является контрольной.
Протеолитическую активность водного раствора препарата (D) в единицах действия (ЕД) вычисляют по формуле:
ЕД = 50/D,
где D - количество раствора препарата (D), содержащегося в предельной пробирке, мл.
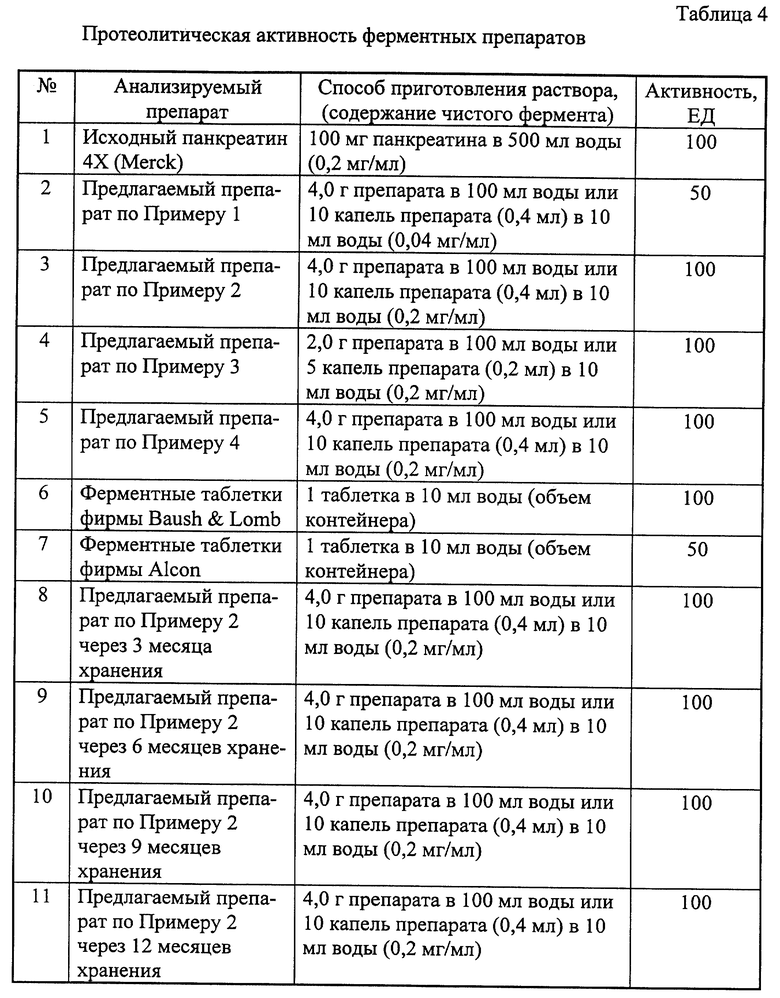
Результаты определения протеолитической активности представлены в табл. 4.
Данные табл. 4 свидетельствуют о том, что предлагаемый препарат по уровню своей протеолитической активности не уступает таблетированным ферментным препаратам фирм Baush & Lomb и Alcon и полностью сохраняет эту активность в течение 1 года хранения. При этом общая доза панкреатина, необходимого для эффективной очистки мягких контактных линз в объеме контейнера, за одну операцию сокращается с 25-50 мг в случае таблеток панкреатина [Пат. США N 4096870 (1978), МКИ В 08 В 3/08] и до 0,4-2 мг в случае предлагаемых растворов.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЭНЗИМАТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ОЧИСТКИ КОНТАКТНЫХ ЛИНЗ | 1998 |
|
RU2139095C1 |
| СОСТАВ ДЛЯ УХОДА ЗА КОНТАКТНЫМИ ЛИНЗАМИ | 2004 |
|
RU2275938C2 |
| МНОГОФУНКЦИОНАЛЬНЫЙ РАСТВОР ДЛЯ УХОДА ЗА МЯГКИМИ КОНТАКТНЫМИ ЛИНЗАМИ | 2010 |
|
RU2442608C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВОДОРАСТВОРИМОГО ИММОБИЛИЗОВАННОГО ФЕРМЕНТНОГО ПРЕПАРАТА | 1998 |
|
RU2137835C1 |
| ШТАММ БАКТЕРИЙ BACILLUS LICHENIFORMIS - ПРОДУЦЕНТ КОМПЛЕКСА ТЕРМОСТАБИЛЬНЫХ АМИЛОЛИТИЧЕСКИХ И ПРОТЕОЛИТИЧЕСКИХ ФЕРМЕНТОВ | 1998 |
|
RU2177995C2 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ГРИБКОВЫХ ЗАБОЛЕВАНИЙ КОЖИ НА ОСНОВЕ ГРИЗЕОФУЛЬВИНА | 1995 |
|
RU2122402C1 |
| ИНСЕКТИЦИДНЫЙ СОСТАВ | 1995 |
|
RU2111664C1 |
| ХИРУРГИЧЕСКИЙ КОСТНЫЙ ИМПЛАНТАТ | 1999 |
|
RU2175249C2 |
| СПОСОБ ПОЛУЧЕНИЯ БИОКОНСЕРВИРОВАННОГО САЛАТА | 2001 |
|
RU2218847C2 |
| СПОСОБ ЛЕЧЕНИЯ ПОРАЖЕНИЙ СИСТЕМ ОРГАНИЗМА, ОБУСЛОВЛЕННЫХ АКТИВАЦИЕЙ ПРОЦЕССА ПЕРЕКИСНОГО ОКИСЛЕНИЯ, И ЖИДКАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2008 |
|
RU2411034C2 |
Изобретение относится к области офтальмологии, в частности к предназначенным для ухода за средствами контактной коррекции зрения - мягкими контактными линзами. Препарат содержит панкреатин, натрий хлористый, натрий тетраборнокислый, кислоту борную, трилон-Б, кальций хлористый, антисептик, полиэтиленгликоль, глицерин и воду. Техническим результатом является длительное использование препарата при очистке мягких контактных линз от белковых отложений. 4 табл.
Жидкий препарат для ферментной очистки мягких контактных линз от белковых отложений следующего состава, мас.%:
Панкреатин - 0,1 - 1,0
Натрий хлористый - 0 - 5,0
Натрий тетраборнокислый - 1,0 - 4,0
Кислота борная - 0,5 - 2,0
Трилон Б - 0,1 - 0,5
Кальций хлористый - 0 - 0,1
Антисептик - 0,01 - 0,1
Полиэтиленгликоль - 0 - 25,0
Глицерин - 25,0 - 50,0
Вода - Остальноем
| US 5409546 A, 25.08.1995 | |||
| US 4404115 A, 13.07.1983 | |||
| US 4715899 A, 29.12.1987 | |||
| US 4096870 A, 27.06.1978 | |||
| КОМПОЗИЦИЯ ДЛЯ ОБРАБОТКИ КОНТАКТНЫХ ЛИНЗ | 1998 |
|
RU2139094C1 |
| ЭНЗИМАТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ОЧИСТКИ КОНТАКТНЫХ ЛИНЗ | 1998 |
|
RU2139095C1 |
| ПРИСПОСОБЛЕНИЕ ДЛЯ ОБРАБОТКИ ВНУТРЕННИХ СФЕРИЧЕСКИХ ПОВЕРХНОСТЕЙ | 0 |
|
SU175801A1 |
| СПОСОБ ПОЛУЧЕНИЯ ЦИКЛОГЕКСАНОНА | 2002 |
|
RU2205175C1 |
| Пюпитр для работы на пишущих машинах | 1922 |
|
SU86A1 |
Авторы
Даты
2001-10-20—Публикация
2000-04-20—Подача