Настоящее изобретение относится к новым аффиным лигандам, к их получению и к связыванию этих лигандов с матрицами, которые могут состоять из твердых, полутвердых, крупнозернистых или коллоидальных материалов, либо из растворимых полимеров. Кроме того, настоящее изобретение относится к новым конъюгатам аффинный лиганд-матрица, к их получению и к использованию для очистки белковых материалов, таких как, например, иммуноглобулины, инсулины, фактор VII, или человеческий гормон роста или их аналоги, производные, фрагменты и предшественники.
Современные методы очистки белков, в большинстве своем, основаны на хроматографической технике разделения, такой как, гельпроникающая хроматография (ГПХ), ионообменная хроматография (ИОХ), гидрофобная хроматография (ГХ), обращенно-фазовая хроматография высокого давления (ОФ-ЖХВД) и аффинная хроматография (АХ). Эти методы могут быть легко адаптированы для лабораторной очистки пептидов и белков, предназначенных для научно-исследовательских экспериментов, с получением чистых и биологически активных веществ. В большинстве случаев, в таких экспериментах, мало или вовсе не уделялось внимания экономичности процесса, подтверждению его целесообразности, или осуществлению тонкой очистки на месте, поскольку эти материалы крайне редко используются для клинических экспериментов, а поэтому трудовые затраты значительно превышают стоимость оборудования и матриц.
Однако, крупномасштабная промышленная обработка должна учитывать такие факторы, как экономичность, надежность матриц и их очистка на месте с использованием, например, NaOH, мочевины или этанола. В настоящее время, спрос на недорогостоящие и прочные матрицы, являющиеся стабильными в 1 М NaOH, 7 М мочевине, или 80% (об./об.) этаноле, удовлетворяется рядом поставщиков, специализирующихся на поставке продуктов для ГПХ, ИОХ, ГХ и ОФ-ЖХВД. Комбинация этих способов в течение многих лет позволяла получать почти чистые в своей основной массе белковые продукты, хотя использование конечных буферов и множества стадий очистки приводит к небольшому выходу продукта, к увеличению стоимости процедуры и к низкой стабильности основной массы препарата.
Уже давно стало понятно, что методы аффинной хроматографии должны быть также применимы для крупномасштабных операций. К сожалению, использование адсорбентов, образуемых природными биологическими лигандами, такими как, моноклональные или поликлональные антитела, приводит к удорожанию производства, поскольку эти лиганды часто сами требуют экстенсивной очистки и являются биологически и химически лабильными, что затрудняет иммобилизацию этих молекул с сохранением их биологической активности. Поэтому, уже давно назрела необходимость заменить дорогостоящие, химически и биологически лабильные моноклональные или поликлональные антитела менее дорогостоящими и более надежными лигандами, имитирующими специфичность антител.
Аффинная хроматография занимает уникальное место в технологии разделения, поскольку очищаемый белок избирательно и обратимо адсорбируется на комплементарном связывающем веществе, таком как, молекула антитела. При этом, коэффициенты очистки, при высоких выходах, часто составляют несколько тысяч раз, в отличие от стандартных методов очистки, где коэффициенты очистки составляют от 5 до 50 раз. Высокие коэффициенты очистки, получаемые при аффинной хроматографии, позволяют резко снизить число стадий очистки в последующем процессе. Кроме того, очень незначительный уровень специфического связывания, наблюдаемого при аффинной хроматографии, позволяет выделять данный белок из сложных биологических смесей; отделять формы белка с неправильной укладкой от нативных молекул и осуществлять специфическое выделение белка даже из больших объемов тканевых экстрактов или культур для ферментации.
Аффинный сорбент представляет собой твердую, обычно, проницаемую матрицу-носитель, с которой ковалентно связывается соответствующий лиганд и которая содержится в стандартной хроматографической колонке. Неочищенный образец, содержащий комплементарный биополимер, пропускают через матрицу-носитель в условиях, стимулирующих специфическое связывание с иммобилизованным лигандом. Колонку промывают буфером для удаления незадержанных молекул, а затем проводят стадию элюирования, в которой белок элюируют в его чистой форме. Типичный аффинный адсорбент состоит из твердого носителя, спейсерной "ножки" (спейсерная группа) и лиганда. Твердый носитель может быть изготовлен из агарозы, образованной из гранул, с открытой пористой структурой. Спейсерная группа может способствовать связыванию белка благодаря тому, что она делает лиганд более доступным. Длина и природа спейсерной группы может быть определена самим специалистом. Лиганд должен обладать способностью к специфическому и обратимому связыванию белка, предназначенного для очистки, даже после иммобилизации. Помимо антител, в качестве аффинных лигандов был использован ряд других соединений, включая кофакторы ферментов, аминокислоты, пептиды, белки, конканавалин А, лектин, тиолы и красители.
Аффинная хроматография была использована во многих способах применения. Исчерпывающий список дан, например, в "Affinity Chromatography A Practical Approach", IRL Press, 1985, и в "Affinity Chromatography, Principles and Methods", Pharmacia Fine Chemicals, 1979.
Для крупномасшабной очистки специфических ферментов или групп ферментов был использован стандартный субстрат или субстрат, аналогичный аффинным лигандам, а в частности, красители (Scawen M.D. & Atkinson Т. 1987, Reactive Dyes in Protein and Enzyme Technology, Ed. Clonis Y.D. et al.; Macmilian Press, pp. 51-85).
Аффинная хроматография на основе красителя уже в течение многих лет представляет для специалистов особый интерес из-за относительно низкой стоимости матриц, используемых в такой хроматографии, их надежности и устойчивости к NaOH, мочевине и этанолу. Некоторыми из лигандов, более широко используемых в аффинной хроматографии такого типа, являются различные реакционно-способные текстильные красители на основе триазина, иммобилизованные на агарозе и других носителях. Использование аффинной хроматографии на иммобилизованных красителях описано Lowe C.R. & Pearson J.C. (1984, Methods in Enzymology 104, pp.97-113). Были описаны селективные взаимодействия NAD+-связывающего центра алкогольдегидрогеназы лошадиной печени с красителями-аналогами синего Cibacron Blue F3G-A (Lowe C.R. et ai., 1986; Journal of Chromatography 376, pp.121-230). Кроме того, был проиллюстрирован метод селективной очистки, разработанный с использованием компьютерной технологии в целях получения новых аффинных адсорбентов, имитирующих фенил-аргинин-дипептидный субстрат, для очистки свиного панкреатического калликреина (Burton N. P. & Lowe C.R., 1992, Journal of Molecular Recognition 6, pp. 55-58).
В патенте США N 4562252 описана структура конкретного лиганда, состоящего из двух м-аминофенилбороксильных групп, связанных с триазиновым кольцом и используемого для выделения гликопротеинов.
Однако, несмотря на быстрый прогресс в области аффинной технологии за последние годы, остается актуальной необходимость в разработке технологий, с помощью которых для данного белка мог бы быть идентифицирован специфический имитирующий лиганд для приготовления недорогостоящих и стабильных аффинных колонок, которые позволили бы осуществлять многократную крупномасштабную очистку указанного белка, например, при выделении и очистке белковых материалов, таких как, иммуноглобулины, инсулины, фактор VII, человеческий гормон роста или их аналоги, производные, фрагменты и предшественники, происходящие от природных или рекомбинантных источников.
Настоящее изобретение относится к новым аффинным лигандам, к их получению и связыванию с матрицами; а также к использованию этих новых комплексов аффинный лиганд - матрица для очистки белковых материалов.
Настоящее изобретение основано на том соображении, что селективность гидрофобных лигандов может быть повышена путем увеличения сложности и пространственной геометрии гидрофобного компонента и что включение различных функциональных групп, способных принимать участие в электростатических и водородсвязывающих взаимодействиях, стимулирует селективные взаимодействия с белоксвязывающими сайтами. Эта работа привела к обнаружению характерной группы новых аффинных лигандов, которые, как было неожиданно обнаружено, могут быть, в основном, использованы для выделения и очистки белков с помощью аффинной хроматографии.
В отличие от вышеупомянутого селективного метода, в котором субстраты ферментов, их аналоги, или имитаторы субстратов используются в качестве лигандов, лиганды, описанные в настоящей заявке, направлены на любую поверхность белковой молекулы, что делает их принципиально применимыми для очистки любого белка. Эти лиганды были сконструированы с помощью техники компьютерного моделирования и/или скрининга библиотек лигандов-имитаторов. Кроме того, настоящее изобретение имеет то преимущество, что для конструирования и разработки лиганда не требуется какой-либо конкретной архитектуры для структуры белоксвязывающего сайта, а поэтому материалы и способы, описанные в настоящей заявке, имеют значительно большую ценность.
Отличительным признаком настоящего изобретения является разработка общего метода разделения, выделения и очистки белков. Было синтезировано семейство различных незначительно отличающихся друг от друга химических структур, которые способны взаимодействовать с различными белками. Структура лиганда, особенно эффективного для данного белка, была идентифицирована путем скрининга ряда лигандов, имеющих подходящие для настоящего изобретения связывающие свойства.
Так, например, аффинные лиганды высокой селективности и специфичности, которые в настоящее время используются для выделения и очистки иммуноглобулинов, часто являются белковыми материалами, происходящими либо от бактериальных, либо от рекомбинантных источников, и включают такие материалы, как Белок А, Белок G и Белок L. Иммобилизация этих и аналогичных белков часто приводит к значительной потере биологической активности. Продолжительное и многократное использование иммобилизованных белков в качестве аффинной среды приводит к дополнительному снижению биологической активности. Кроме того, природа этих биологических макромолекул накладывает жесткие ограничения на использование буферных солей, органических растворителей и уровней pH в аффинной хроматографии и аналогичных методах.
Новые аффинные лиганды настоящего изобретения могут быть использованы вместо белка А и белка G и являются значительно более гибкими в применении, более стабильными, менее дорогостоящими и часто дают эквивалентные уровни очистки.
Другим примером применения может служить использование новых аффиных матриц настоящего изобретения в биотехнологии.
Настоящее изобретение относится к конъюгатам "аффинный лиганд - матрица", содержащим лиганд общей формулы (а):
где R1 представляет атом водорода, алкильную группу, содержащую 1-6 атомов углерода, гидроксиалкильную группу, содержащую 1-6 атомов углерода, циклогексильную группу, аминогруппу, фенильную группу, нафтильную группу, 1-фенилпиразольную группу, индазольную группу, бензтиазольную группу, бензоксазольную группу или бензимидазольную группу, где каждое из бензольного, нафталинового, фенилпиразольного, индазольного, бензтиазольного, бензоксазольного или бензимидазольного колец необязательно замещено одним или несколькими заместителями, независимо выбранными из группы, включающей алкильные группы, содержащие, 1-6 атомов углерода; алкоксигруппы, содержащие, 1-6 атомов углерода; ацилокси- или ациламино-группы, содержащие 1-6 атомов углерода; амино-группы; гидроксильные группы; карбоксильные группы; сульфокислотные группы; карбамоильные группы; сульфамоильные группы; алкилсульфонильные группы, содержащие 1-6 атомов углерода или атомы галогена;
Y представляет атом кислорода, атом серы или группу N-R2;
Z представляет атом кислорода, атом серы или группу N-R3;
каждый из R2 и R3 независимо представляет атом водорода; алкильную группу, содержащую 1-6 атомов углерода; гидроксиалкильную группу, содержащую 1-6 атомов углерода; бензильную группу или 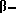 фенилэтильную группу;
фенилэтильную группу;
каждый из R4, R5 и R6 независимо представляет атом водорода; гидроксильную группу; алкильную группу, содержащую 1-6 атомов углерода; алкокси-группу, содержащую 1-6 атомов углерода; аминогруппу; ацилокси- или ациламино-группу, содержащую 1-6 атомов углерода; карбоксильную группу; сульфоксильную группу, карбамоильную или сульфамоильную группу; алкилсульфонильную группу, содержащую 1-6 атомов углерода; или атом галогена;
один из символов X представляет атом азота, а другой символ X представляет атом азота или атом углерода, несущий атом хлора или цианогруппу;
Q представляет бензольное, нафталиновое, бензтиазольное, бензоксазольное, 1-фенилпиразольное, индазольное или бензимидазольное кольцо;
n представляет целое число от 0 до 6;
p представляет целое число от 0 до 20; и
где указанный лиганд связан с матрицей-носителем в положении А необязательно посредством спейсерной группы, расположенной между матрицей и лигандом.
Необязательная спейсерная группа предпочтительно представлена общей формулой:
-T-[-L-V-]m-, (b)
где Т представляет атом кислорода, атом серы или группу N- R7, где R7 представляет атом водорода или алкильную группу, содержащую 1-6 атомов углерода;
V представляет атом кислорода, атом серы, группу -COO-, группу CONH или группу NHCO или группу - PO3-H-, группу NH-арилен-SO2-CH2-CH2 или N-R8, где R8 представляет атом водорода или алкильную группу, содержащую 1-6 атомов углерода;
L представляет необязательно замещенную углеводородную связь, содержащую от 2 до 20 атомов углерода; и
m = 0 или 1.
Матрица-носитель может быть любым соединением или материалом, состоящим или не состоящим из макрочастиц, растворимым или нерастворимым, пористым или непористым, который может быть использован для конъюгирования с аффинными лигандами с образованием конъюгата аффинный лиганд - матрица, и с помощью которого может быть осуществлено выделение аффинных лигандов из растворенных веществ в контактирующем растворе.
Hастоящее изобретение относится к новым конъюгатам аффинный лиганд - матрица, которые могут быть использованы для выделения и очистки белковых материалов, таких как, иммуноглобулины, инсулины, фактор VII, или человеческий гормон роста, или их аналоги, производные и фрагменты и предшественники, происходящие от природных или рекомбинантных источников.
В предпочтительном варианте, настоящее изобретение относится к новым конъюгатам аффинный лиганд - матрица, которые представлены общей формулой (I):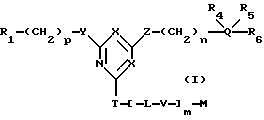
где R1, Y, Z, R2, R3, R4, R5, R6, X, Q, n и p определены выше;
T представляет атом кислорода, атом серы или группу N-R7;
V представляет атом кислорода, атом серы, группу -COO-, группу CONH, или группу NHCO или группу -PO3-H, группу NH- арилен-SO2-CH2-CH2 или группу N-R8,
каждый из R7 и R8 независимо представляет атом водорода или алкильную группу, содержащую 1-6 атомов углерода;
L представляет необязательно замещенную углеводородную связь, содержащую от 2 до 20 атомов углерода; и
m = 0 или 1; и
M представляет остаток матрицы-носителя.
Используемый в настоящем описании термин "алкильная группа, содержащая 1-6 атомов углерода", взятая отдельно или в комбинации с другими группами, означает прямую или разветвленную, насыщенную углеводородную цепь, имеющую 1-6 атомов углерода, такую как, например, метил, этил, н- пропил, изопропил, н-бутил, втор-бутил, изобутил, трет-бутил, н- пентил, 2-метилбутил, 3-метилбутил, н-гексил, 4-метилпентил, неопентил, н-гексил и 2,2-диметилпропил.
Используемый в настоящем описании термин "гидроксиалкильная группа, содержащая 1-6 атомов углерода", взятая отдельно или в комбинации с другими группами, означает прямую или разветвленную, насыщенную углеводородную цепь, имеющую 1-6 атомов углерода, замещенных одной или несколькими гидроксигруппами, предпочтительно одной гидроксигруппой, такими как, например, гидроксиметил, 2-гидроксиэтил, 3-гидроксипропил, 2-гидроксипролил, 4-гидроксибутил, 5-гидроксипентил и 6-гидроксигексил.
Используемый в настоящем описании термин "алкокси-группа, содержащая 1-6 атомов углерода", взятая отдельно или в комбинации с другими группами, означает прямой или разветвленный моновалентный заместитель, включающий алкильную группу, содержащую 1-6 атомов углерода, связанную через кислород простой эфирной группы, имеющей свою свободновалентную связь от кислорода, и содержащий 1-6 атомов углерода, например, метокси, этокси, пропокси, изопропокси, бутокси, пентокси.
Используемый в настоящем описании термин "галоген" означает фтор, хлор, бром или иод.
Используемый в настоящем описании термин "ацилокси или ациламино, содержащий от 1 до 6 атомов углерода" означает моновалентный заместитель, включающий алкильную группу, содержащую 1-5 атомов углерода, связанную посредством карбонилокси- или оксикарбонильной группы, такой как, метилкарбонилокси-, этилкарбонилокси-, метилоксикарбонильная или этилоксикарбонильная группа, или связанную посредством карбониламино- или аминокарбонильной группы, такой, как метилкарбониламино, этилкарбониламино, метиламинокарбонильная или этиламинокарбонильная группа.
Используемый в настоящем описании термин "алкилсульфонил, содержащий 1-6 атомов углерода" означает моновалентный заместитель, включающий алкильную группу, содержащую 1-6 атомов углерода, связанную посредством сульфонильной группы, такой как, например, метилсульфонил, этилсульфонил, н-пропилсульфонил, изопропилсульфонил, н-бутилсульфонил, втор- бутилсульфонил, изобутилсульфонил, трет-бутилсульфонил, н- пентилсульфонил, 2-метилбутилсульфонил, 3-метилбутилсульфонил, н-гексилсульфонил, 4-метилпентилсульфонил, неопентилсульфонил, н-гексилсульфонил и 2,2-диметипропилсульфонил.
Используемый в настоящем описании термин "один или несколько заместителей, независимо выбранных из..." предпочтительно относится к 1-3 заместителям. При этом, предпочтительно, если он относится к 1-2 заместителям, а более предпочтительно к одному заместителю.
В настоящем описании, термин "инсулин", независимо от того, используется ли он во многозначном смысле или в обобщенном смысле, относится как к природным инсулинам, так и к их аналогам и производным, и к предшественникам. Под термином "инсулин" подразумевается также инсулин, происходящий от любого вида животных, включая человека. В контексте настоящего описания, термин "аналог инсулина" означает инсулин человека, имеющий одну или несколько аминокислотных замен, одну или несколько аминокислотных делеций, одну или несколько аминокислотных инсерций, или комбинации указанных модификаций. Термин "производное инсулина" означает инсулин, химически модифицированный в одном или нескольких своих остатков. Термин "предшественник инсулина" означает любую молекулу, которая, после ее ферментативной или химической трансформации, образует инсулин, фрагменты инсулина, например, des-Thr(B30)-инсулина, аналоги инсулина или производные инсулина.
Используемый в настоящем описании термин "необязательно замещенная углеводородная связь, содержащая от 2 до 20 атомов углерода", означает одну или несколько линейных или разветвленных алкильных цепей, необязательно замещенных, например, гидрокси- или алкокси-группами, содержащими 1-6 атомов углерода, и необязательно соединенных вместе амино-, эфирными, тиоэфирными, сложноэфирными, амидными или сульфонамидными связями с образованием цепи, содержащей от 2 до 20 атомов углерода. Эта конструкция является предпочтительно гибкой. Конструкция таких необязательно замещенных углеводородных связей описана, например, в работе Lowe, C.R. & Dean, P.D.G., 1974, Affinity Chromatography, John Wiley & Sons, London, которая вводится в настоящее описание посредством ссылки.
В предпочтительном варианте настоящего изобретения, указанные конъюгаты представлены общей формулой (I):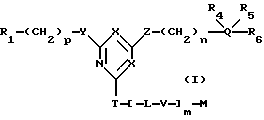
где представляет атом водорода, алкильную группу, содержащую 1-6 атомов углерода, гидроксиалкильную группу, содержащую 1-6 атомов углерода, циклогексильную группу, аминогруппу, фенильную группу или нафтильную группу, которая может быть замещена на бензольном или нафталеновом кольце алкильными группами, содержащими 1-6 атомов углерода, алкокси- группами, содержащими 1-6 атомов углерода, ацилокси- или ациламино-группами, содержащими 1-6 атомов углерода, аминогруппами, гидроксильными группами, карбоксильными группами, сульфоксильными группами, карбамоильными группами, cульфамоильными группами, алкилсульфонильными группами или атомами галогена;
Т представляет атом кислорода, атом серы или группу N- R7;
Y представляет атом кислорода, атом серы или группу N-R2;
Z представляет атом кислорода, атом серы или группу N-R3;
каждый из R2 и R3 независимо представляет атом водорода, алкильную группу, содержащую 1-6 атомов углерода, гидроксиалкильную группу, содержащую 1-6 атомов углерода, бензильную группу или 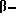 фенилэтильную группу;
фенилэтильную группу;
каждый из R4, R5 и R6 независимо представляет атом водорода, гидроксильную группу, алкильную группу, содержащую 1-6 атомов углерода, алкокси-группу, содержащую 1-6 атомов углерода, аминогруппу, ацилокси- или ациламино-группу, содержащую 1-6 атомов углерода, карбоксильную группу, сульфоксильную группу, карбамоильную или сульфамоильную группу, алкилсульфонильную группу или атом галогена;
один из символов X представляет атом азота, а другие символы X представляют атом азота или атом углерода, несущие атом хлора или цианогруппу;
V представляет атом кислорода, атом серы, -COO-, группу CONH, или группу NHCO, или группу -PO3H-, группу NH-арилен- SO2-CH2-CH2, или N-R8,
каждый из R7 и R8 независимо представляет атом водорода или алкильную группу, содержащую 1-6 атомов углерода;
L представляет необязательно замещенную углеводородную связь, содержащую от 2 до 20 атомов углерода; и
Q представляет бензольное или нафталиновое кольцо;
n представляет целое число от 0 до 6;
p представляет целое число от 0 до 20;
m = 0 или 1; и
М представляет остаток матрицы-носителя, который может быть любым соединением или материалом, состоящим или не состоящим из макрочастиц, растворимым или нерастворимым, пористым или непористым, который может быть использован в сочетании с аффинными лигандами с образованием нового конъюгата аффинный лиганд - матрица" общей формулы (I) и который служит удобным средством выделения аффинных лигандов из растворенных веществ в контактирующем растворе.
Следует отметить, что настоящее изобретение относится, inter alia, к использованию соединений, которые являются пиридинами, диазинами или триазинами, несущими заместитель T-[L-V]0-1-M, или его предшественник, и другие заместители, связанные с кольцом посредством гетероатома. Такими заместителями может быть любая (пространственно) затрудняющая группа, содержащая 0-10 или 20 атомов углерода.
В предпочтительном варианте настоящего изобретения R1 представляет фенильную или нафтильную группу, каждая из которых необязательно замещена на бензольном или нафталиновом кольце одним или несколькими группами, независимо выбранными из гидроксильных групп или карбоксильных групп.
В другом предпочтительном варианте настоящего изобретения R2 представляет атом водорода.
В другом предпочтительном варианте настоящего изобретения R3 представляет атом водорода.
В другом предпочтительном варианте настоящего изобретения R4 представляет атом водорода, гидроксильную группу, карбоксильную группу или аминогруппу.
В другом предпочтительном варианте настоящего изобретения R5 представляет атом водорода, гидроксильную группу, карбоксильную группу или аминогруппу.
В другом предпочтительном варианте настоящего изобретения R6 представляет атом водорода, гидроксильную группу, карбоксильную группу или аминогруппу.
В другом предпочтительном варианте настоящего изобретения, R7 представляет атом водорода.
В другом предпочтительном варианте настоящего изобретения Т представляет атом кислорода или группу NH.
В другом предпочтительном варианте настоящего изобретения Y представляет N-R2, где R2 является таким, как указано выше.
В другом предпочтительном варианте настоящего изобретения Z представляет N-R3, где R3 является таким, как указано выше.
В другом предпочтительном варианте настоящего изобретения оба X представляют атом азота.
В другом предпочтительном варианте настоящего изобретения Q представляет бензольное или нафталиновое кольцо.
В другом предпочтительном варианте настоящего изобретения n представляет 0 или 2.
В другом предпочтительном варианте настоящего изобретения p представляет 0 или 2.
В другом предпочтительном варианте настоящего изобретения m представляет 0 или 1.
В другом предпочтительном варианте настоящего изобретения L представляет этильную, пропильную, гидроксипропильную, бутильную, пентильную, гексильную, октильную или децильную группу, а V и m являются такими, как указано выше.
В другом предпочтительном варианте настоящего изобретения V представляет атом кислорода, группу -COO-, группу -PO3H-, или группу N-R8, а более предпочтительно атом кислорода или группу NH, а L и m являются такими, как указано выше.
В другом предпочтительном варианте настоящего изобретения m представляет 1, a L и V являются такими, как указано выше.
Термин "целое число между x и y" может включать величины x (включая нуль) и y.
Настоящее изобретение также относится к способам изготовления новых конъюгатов "аффинный лиганд - матрица" настоящего изобретения, предусматривающим проведение реакции, в любом порядке, галоген-содержащего гетероциклического соединения общей формулы (II):
где символы X имеют значения, указанные выше, a W обозначает атом галогена,
(i) с соединением общей формулы (III):
R1-(CH2)p-Y-H, (III)
где символы R1, Y и p являются такими, как указано выше, а H обозначает водород;
(ii) с соединением общей формулы (IV):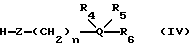
где символы R4, R5, R6, Q, Z и n имеют значения, определенные выше; и
(iii) либо с необязательно дериватизированной матрицей-носителем общей формулы V:
H-T-[-L-V-]m-M, (V)
где символы L, М, V, Т и m имеют значения, определенные выше,
либо со связывающей структурной единицей общей формулы (VI)
H-T-L-V-H, (VI)
где символы H, L, V и Т имеют значения, определенные выше,
с получением соединения общей формулы (VII)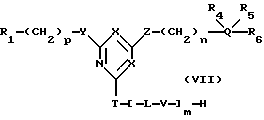
где R1, R4, R5, R6, Q, L, Т, V, X, Y, Z, m, n и p являются такими, как указано выше; а затем проведение реакции соединения общей формулы (VII) с матрицей-носителем, остаток которой представлен М, с использованием методов активации и присоединения, хорошо известных каждому специалисту.
Примерами галогенсодержащих гетероциклических соединений общей формулы (II) могут служить 5-хлор-2,4,6-трифторпиримидин, 5-циано-2,4,6-трихлорпиримидин, фторангидрид циануровой кислоты, бромангидрид циануровой кислоты, а в основном, хлорангидрид циануровой кислоты.
Примерами соединений общей формулы (III) могут служить амины, такие как, аммиак, метиламин, этиламин, пропиламин, изопропиламин, диизопропиламин, изобутиламин, амиламин, гексиламин, этаноламин, диэтаноламин, анилин, N-метиланилин, N-этиланилин, N-изопропиланилин, 1,4- диаминобутан, 1,6-диаминогексан, N-трет-бутиланилин, п-толуидин, п-бутиланилин, 2,4-диметиланилин, п-анизидин, п-этоксианилин, п- аминоацетанилид, п-аминофенол, п-хлоранилин, ортанилиновая кислота, метанилиновая кислота, сульфанилиновая кислота, 4-метил- анилин-2-сульфокислота, 4-метоксианилин-2-сульфокислота, анилин- 2,5-дисульфокислота, N-метилметанилиновая кислота, орто-, мета- и пара-аминобензойная кислота, п-аминобензамид, п- аминобензолсульфонамид, 1-амино-2-, 3-, 4-, 5-, 6-, 7- и 8- нафтол, 2-амино-3-, 4-, 5-, 6-, 7- и 8-нафтол, 5-, 6- и 7-амино- 1-нафтол-3-сульфокислота, N-бензиланилин, бензиламин, 4- метилбензиламин, 4-гидрокси-бензиламин, 4-метоксибензиламин, 4-ацетоксибензиламин, 4-ацетиламинобензиламин, N-метилбензиламин, 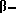 фенилэтиламин, N- бутилбензиламин, N-бензил
фенилэтиламин, N- бутилбензиламин, N-бензил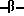 фенилэтиламин, N-(
фенилэтиламин, N-( гидрокси-этил)-бензиламин, N-трет- бутилбензиламин, N-бензилтирамин и тирамин; фенолы, такие как, фенол, орто-, мета- и пара-крезол, катехол, резорцин, гидрохинон, п-хлорфенол, 1-нафтол и 2-нафтол, 1-нафтол-4- нафтол-4-сульфокислота, 2-нафтол-6-сульфокислота и 2-гидрокси-3-нафтойная кислота; тиолы, такие как, этилтиол, тиогликолевая кислота, тиофенол и тио-п-крезол; и ароматические гетероциклы, такие как, 5-амино-1-фенилпиразол, 6-аминоиндазол, 2- аминобензимидазол, 2-амино-бензтиазол и 2-амино-5- хлорбензоксазол.
гидрокси-этил)-бензиламин, N-трет- бутилбензиламин, N-бензилтирамин и тирамин; фенолы, такие как, фенол, орто-, мета- и пара-крезол, катехол, резорцин, гидрохинон, п-хлорфенол, 1-нафтол и 2-нафтол, 1-нафтол-4- нафтол-4-сульфокислота, 2-нафтол-6-сульфокислота и 2-гидрокси-3-нафтойная кислота; тиолы, такие как, этилтиол, тиогликолевая кислота, тиофенол и тио-п-крезол; и ароматические гетероциклы, такие как, 5-амино-1-фенилпиразол, 6-аминоиндазол, 2- аминобензимидазол, 2-амино-бензтиазол и 2-амино-5- хлорбензоксазол.
Примерами соединений общей формулы (IV) являются амины, такие как, анилин, N-метиланилин, N-этиланилин, N- изопропиланилин, N-трет-бутиланилин, п-толуидин, п-бутиланилин, 2,4-диметиланилин, п-анизидин, п-этоксианилин, п-аминоацетанилид, п-аминофенол, п-хлоранилин, ортанилиновая кислота, метанилиновая кислота, сульфанилиновая кислота, 4-метиланилин-2-сульфокислота, 4-метоксианилин-2-сульфокислота, анилин-2,5-дисульфокислота, N- метилметанилиновая кислота, орто-, мета- и пара-аминобензойная кислота, 1-амино-2-,3-, 4-, 5-,6-,7- и 8-нафтол, 2-амино-3-, 4-,5-,6-,7- и 8-нафтол, 5-, 6- и 7-амино-1-нафтол-3-сульфокислота, п-аминобензамид, п-аминобензолсульфонамид, N- бензиланилин, бензиламин, 4-метилбензиламин, 4-гидроксибензиламин, 4-метоксибензиламин, 4-ацетоксибензиламин, 4- ацетиламинобензиламин, N-метилбензиламин, 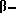 фенилэтиламин, N-бутилбензиламин, N-бензил
фенилэтиламин, N-бутилбензиламин, N-бензил фенилэтиламин, N-(
фенилэтиламин, N-(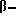 гидроксиэтил)-бензиламин, N-трет-бутилбензиламин, N-бензилтирамин и тирамин; фелолы, такие как, фенол, орто-, мета- и пара-крезол, катехол, резорцин, гидрохинон, п-хлорфенол, 1-нафтол и 2-нафтол, 1-нафтол-4-сульфокислота, 2-нафтол-6-сульфокислота и 2-гидрокси-3-нафтойная кислота; тиолы, такие как тиофенол и тио-п-крезол; и ароматические гетероциклы, такие как, 5-амино-1- фенилпиразол, 6-аминоиндазол, 2-аминобензимидазол, 2- аминобензтиазол и 2-амино-5-хлорбензоксазол.
гидроксиэтил)-бензиламин, N-трет-бутилбензиламин, N-бензилтирамин и тирамин; фелолы, такие как, фенол, орто-, мета- и пара-крезол, катехол, резорцин, гидрохинон, п-хлорфенол, 1-нафтол и 2-нафтол, 1-нафтол-4-сульфокислота, 2-нафтол-6-сульфокислота и 2-гидрокси-3-нафтойная кислота; тиолы, такие как тиофенол и тио-п-крезол; и ароматические гетероциклы, такие как, 5-амино-1- фенилпиразол, 6-аминоиндазол, 2-аминобензимидазол, 2- аминобензтиазол и 2-амино-5-хлорбензоксазол.
В качестве примеров матриц-носителей, остаток которой представлен М, могут служить нерастворимые матрицы-носители, такие как, природный полимер, например, полипептид или белок, такой как, перекрестносшитый альбумин или полисахарид, такой как, агароза, альгинат, караген, хитин, целлюлоза, декстран или крахмал; синтетические полимеры, такие как, полиакриламид, полистирол, полиакролеин, поливиниловый спирт, полиметилакрилат, перфторуглеводород; неорганические соединения, такие как, кремнезем, стекло, кизельгур, окись алюминия, окись железа, или другие окиси металлов, или сополимеры, составляющие любую комбинацию из двух или более природных полимеров, синтетических полимеров, или неорганических соединений. Понятие "матрицы-носители, остаток которых представлен М", также включает в себя растворимые матрицы-носители, которые содержат полимеры, такие как, декстран, полиэтиленгликоль, поливиниловый спирт или гидролизованный крахмал, и которые образуют конъюгаты аффинный лиганд - матрица, используемые для разделения жидкостей; или матрицы-носители, которые содержат такие соединения, как перфтордекалин, и которые образуют конъюгаты аффинный лиганд - матрица, используемые для изготовления аффинных эмульсий. Для большей ясности следует указать, что в контексте настоящего описания, понятие "матрица-носитель" означает любое соединение или материал (независимо от того, является ли он крупнозернистым или некрупнозернистым, растворимым или нерастворимым, пористым или непористым), который может быть использован для получения нового конъюгата аффинный лиганд-матрица настоящего изобретения и который обеспечивает удобный способ отделения аффинного лиганда от растворимых веществ в контактирующем растворе.
Кроме того, понятие "матрицы-носители, остаток которых представлен М", означает матрицы-носители, такие как, агароза, целлюлоза, декстран, крахмал, альгинат, караген, синтетические полимеры, кремнезем, стекло и окиси металлов, которые были модифицированы или являются модифицированными путем обработки активирующим агентом до или во время присоединения лиганда.
В предпочтительном варианте настоящего изобретения, М представляет необязательно активированную агарозу, кремнезем, целлюлозу, стекло, мелкий жемчуг, гидроксиэтилметакрилат, полиакриламид, стиролдивинилбензол, Hyper D, перфторуглеводороды.
М предпочтительно обозначает агарозу, необязательно активированную трезилом, сульфонилхлорилом, тозилом, винилсульфоном или эпокси.
В соответствии с настоящим изобретением, предпочтительными конъюгатами аффинный лиганд - матрица являются
i)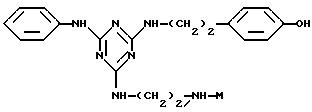
ii)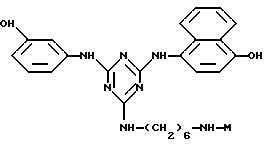
iii)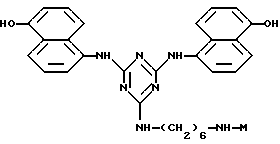
iv)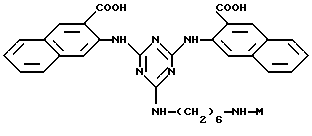
v)
vi)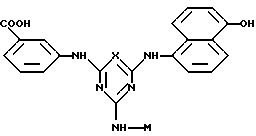
vii)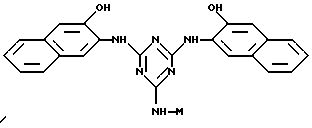
viii)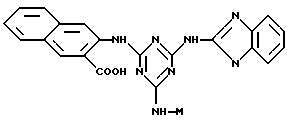
где М определен выше.
Существует большое число активирующих агентов, которые могут быть использованы в универсальных методах присоединения лигандов к матрице-носителю. Эти соединения и метод их использования хорошо известны специалистам, а поскольку в основе настоящего изобретения лежит природа лиганда, связываемого с матрицей, а не метод связывания, то любой из этих активирующих агентов может быть использован для изготовления новых конъюгатов "матрица-лиганд". Неограничивающими примерами таких активирующих агентов могут служить такие различные соединения, как бромистый циан, хлорангидрид циануровой кислоты, эпихлоргидрин, дивинилсульфон, п-толуолсульфонилхлорид, 1,1'- карбонилдиимидазол, метапериодат натрия, толуол-4-сульфонат-2- фтор-1-метилпиридиния, глицидоксипропилтриметоксисилан и 2,2,2- трифторэтансульфонилхлорид. Как показано выше, методы, которыми осуществляют такие стадии активации, хорошо известны специалистам.
Аналогично, для присоединения соединений общей формулы (IV) к матрице-носителю могут быть использованы конденсирующие агенты широкого ряда, такие как, агароза, целлюлоза, декстран, крахмал, альгинат, караген, кремнезем или стекло. И в этом случае, эти соединения и методы их использования хорошо известны специалистам, а поскольку, как и в предыдущем случае, в основе настоящего изобретения лежит природа лиганда, а не метод связывания, то любой из этих активирующих агентов может быть использован для изготовления новых конъюгатов матрица - лиганд. Неограничивающими примерами таких конденсирующих агентов могут служить N- этоксикарбонил-2-этокси-1,2-дигидрохинолин, дициклогексилкарбодиимид и 1-этил-3- (3-диметиламинопропил) - карбодиимид.
В качестве примеров связывающих звеньев общей формулы (VI), которые могут быть использованы для получения соединений общей формулы (VII), могут служить диамины, такие как, этилендиамин, N,N'-диметилэтилендиамин, N-этилэтилендиамин, N-(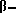 гидроксиэтил)-этилендиамин, пропилендиамин, N-метилпропилендиамин, N-(
гидроксиэтил)-этилендиамин, пропилендиамин, N-метилпропилендиамин, N-(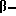 гидроксиэтил)-пропилендиамин, 1,4-диаминобутан, 1,5-диаминопентан, 1,6-диаминогексан, 1,7- диаминогептан, 1,8-диаминооктан, 1,9-диаминононан, 1,10-диаминодекан, 1,12-диаминододекан, пиперазин, 3-гидрокси-1,5-диаминопентан, м- и п-фенилендиамин, м- и п-аминобензиламин; аминоспирты, такие как этаноламин, N-метилэтаноламин, N-пропилэтаноламин, диэтаноламин, 3-гидроксипропиламин, 2,3-дигидроксипропиламин, изопропаноламин, 5-аминопентан-1-ол и 6-аминогексан-1-ол; аминофенолы, такие как, о-, м- и п-аминофенол; аминокарбоновые кислоты, такие как глицин, N-метилглицин, 3- и 4-aминомасляная кислота, 3-аминоизомасляная кислота, 5-аминовалериановая кислота, 6-аминокапроевая кислота, 7- аминогептановая кислота, м- и п-аминобензойная кислота; аминофосфоновые кислоты, такие как м-аминобензолфосфоновая кислота и п-аминобензилфосфоновая кислота; и аминоариленвинилсульфоновые предшественники, такие как анилин-3
гидроксиэтил)-пропилендиамин, 1,4-диаминобутан, 1,5-диаминопентан, 1,6-диаминогексан, 1,7- диаминогептан, 1,8-диаминооктан, 1,9-диаминононан, 1,10-диаминодекан, 1,12-диаминододекан, пиперазин, 3-гидрокси-1,5-диаминопентан, м- и п-фенилендиамин, м- и п-аминобензиламин; аминоспирты, такие как этаноламин, N-метилэтаноламин, N-пропилэтаноламин, диэтаноламин, 3-гидроксипропиламин, 2,3-дигидроксипропиламин, изопропаноламин, 5-аминопентан-1-ол и 6-аминогексан-1-ол; аминофенолы, такие как, о-, м- и п-аминофенол; аминокарбоновые кислоты, такие как глицин, N-метилглицин, 3- и 4-aминомасляная кислота, 3-аминоизомасляная кислота, 5-аминовалериановая кислота, 6-аминокапроевая кислота, 7- аминогептановая кислота, м- и п-аминобензойная кислота; аминофосфоновые кислоты, такие как м-аминобензолфосфоновая кислота и п-аминобензилфосфоновая кислота; и аминоариленвинилсульфоновые предшественники, такие как анилин-3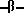 сульфатоэтилсульфон и анилин-4
сульфатоэтилсульфон и анилин-4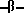 сульфатоэтилсульфон.
сульфатоэтилсульфон.
Реакция галогенсодержащих гетероциклических соединений общей формулы (II) с соединениями общей формулы (III), (IV) и (V) или (VI) может быть осуществлена в не смешиваемом с водой органическом растворителе; или в смешиваемом с водой органическом растворителе, или в смеси воды и смешиваемого с водой органического растворителя. Примерами подходящих не смешиваемых с водой органических растворителей являются толуол, ксилол или хлорбензол; примерами подходящих смешиваемых с водой органических растворителей являются ацетон, метилэтилкетон или диоксан. Первая реакция галогенсодержащего гетероциклического соединения может быть осуществлена при температурах от 0oC до 25oC, а идеально, от 0oC до 5oC; вторая реакция может быть осуществлена при температурах от 20oC до 50oC, а идеально от 30oC до 45oC; а третья реакция может быть осуществлена при температурах от 20oC до 100oC. В процессе этих реакций, продуцируемую неорганическую кислоту,
такую как, соляная кислота или фтористоводородная кислота, нейтрализуют с использованием связывающего кислоту агента, такого как, гидроксид натрия, карбонат натрия, бикарбонат натрия, гидроксид кальция или карбонат кальция.
Кроме того, соединения общей формулы (VII) могут взаимодействовать с реакционно-способным полимеризуемым мономером с образованием полимеризуемого соединения общей формулы (VIII):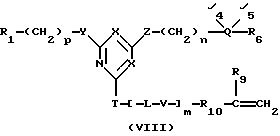
где R1, R4, R5, R6, Q, L, T, V, X, Y, Z, m, n и p являются такими, как указано выше; R9 представляет атом водорода или алкильную группу, содержащую 1-6 атомов углерода; R10 представляет карбонильную группу, метиленовую группу, группу -NH-CH2- или группу -S-CH2-. Примерами реакционноспособных полимеризуемых мономеров являются акрилоилхлорид, метакрилоилхлорид, аллилбромид, аллиламин или 3,4-эпоксибутен. Полимеризуемые соединения общей формулы (VIII) могут быть полимеризованы необязательно в присутствии других полимеризуемых мономеров с образованием конъюгатов аффинный лиганд - матрица общей формулы (I). Такие способы полимеризации хорошо известны специалистам.
Настоящее изобретение также относится к использованию всех указанных конъюгатов аффинный лиганд - матрица -носитель для разделения, выделения, очистки, количественной оценки, идентификации и характеризации белковых материалов, таких как, иммуноглобулины, инсулины, фактор VII, или человеческий гормон роста, либо их аналоги, производные и фрагменты, и предшественники.
Иммуноглобулины представляет собой семейство белков, часто обозначаемых Ig, которые имеют одинаковую структуру. Иммуноглобулины, в целом, часто называют антителами, и любое из этих названий может быть использовано для описания этой группы белков. Иммуноглобулины существуют в виде различных форм; например, наиболее известными типами антител являются IgA, IgD, IgE, IgG, IgM и IgY и их различные подклассы. Иммуноглобулины могут присутствовать в физиологических жидкостях организма, таких как, плазма, асциты, слюна, молоко или яичный желток, либо они могут быть продуцированы методами генной инженерии. Для получения желаемых свойств иммуноглобулинов, они могут быть модифицированы различными методами. Эти методы хорошо известны специалистам и позволяют получить модифицированные антитела, которые также заявлены в формуле изобретения настоящего изобретения. В качестве неограничивающих примеров способов модификации антител могут служить методы получения фрагментов антител, меченых антител, конъюгатов антител или антитело-содержащих гибридных белков путем химической модификации, путем обработки одним или несколькими ферментами, или путем использования комбинации того и другого метода. Существует большое количество химически модифицирующих реагентов и ферментов, которые могут быть использованы для модификации антитела, и эти соединения, а также их использование хорошо известны специалистам. Другим путем получения модифицированных или новых антител является их продуцирование методами генной инженерии. Эти методы хорошо известны специалистам и могут быть использованы для продуцирования, например, фрагментов антител или антитело- содержащих гибридных продуктов. Модифицированные или новые антитела, полученные методами генной инженерии, также заявлены в формуле изобретения.
Ценная группа конъюгатов аффинный лиганд - матрица-носитель представлена общей формулой (IX):
где R1, R4, R5, R6, M, Q, n и p указаны выше, a j представляет целое число от 2 до 20.
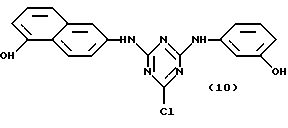
Особенно ценная группа конъюгатов аффинный лиганд - матрица-носитель представлена общей формулой (X):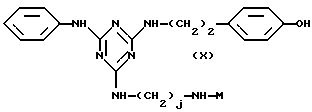
где j и M являются такими, как указано выше.
Обычно, реакция соединений общей формулы (XI):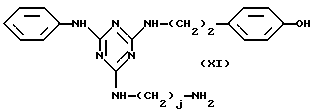
с 3-пропокси-(1,2-эпокси)-агарозой при температуре 10-30oC в присутствии связывающего кислоту агента приводит к продуцированию новых конъюгатов аффинный лиганд - матрица, которые обладают исключительной эффективностью при очистке белковых материалов. Эти новые конъюгаты аффинный лиганд - матрица обладают высокой аффинностью по отношению к белкам группы иммуноглобулинов. Эти уникальные свойства указанных конъюгатов делают их исключительно ценными при разделении, выделении, очистке, количественной оценке, идентификации и характеризации белков этого класса.
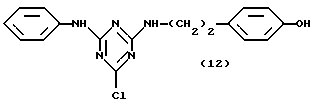
В другом предпочтительном варианте, настоящее изобретение относится к новым аффинным лигандам общей формулы (XII):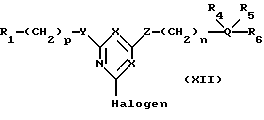
где R1, R4, R5, R6, Q, X, Y, Z, n и p являются такими, как указано выше, а галоген (Halogen) представляет атом фтора, хлора, брома или йода.
Кроме того, настоящее изобретение относится к способу связывания новых аффинных лигандов общей формулы (XII), описанных выше, с матрицей общей формулы (V), описанной выше, путем реакции новых аффинных лигандов с матрицей при температуре от -20oC до 121oC, необязательно в присутствии связывающего кислоту агента.
В другом предпочтительном варианте, настоящее изобретение относится к новым аффинным лигандам общей формулы (XIII):
где R1, R4, R5, R6, Q, X, Y, Z, m, n и p являются такими, как указано выше; a j представляет целое число от 2 до 20.
Кроме того, настоящее изобретение относится к способу получения вышеуказанных новых аффинных лигандов общей формулы (XIII) путем реакции соединения вышеописанной общей формулы (XII) с алкилендиамином общей формулы H2N- (CH2)j- NH2 при температурах от 0oC до 100oC в присутствии агента, связывающего кислоту.
В другом своем варианте, настоящее изобретение относится к новым аффинным лигандам общей формулы (XIV):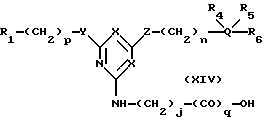
где R1, R4, R5, Q, X, Y, Z, m, n и p являются такими, как указано выше; q = 0 или 1, a j представляет целое число от 2 до 20.
Кроме того, настоящее изобретение относится к способу получения новых аффинных лигандов вышеуказанной общей формулы (XIV) путем реакции соединения вышеуказанной общей формулы (XII) с аминогидрокси-соединением общей формулы H2N-(CH2)j- (CO)q-OH при температурах от 0oC до 100oC, необязательно в присутствии агента, связывающего кислоту.
В другом своем варианте, настоящее изобретение относится к новым аффинным лигандам вышеуказанной общей формулы (VIII), где R1, R4, R5, R6, L, Q, Т, V, X, Y, Z, m, n и p являются такими, как указано выше; R9 представляет атом водорода или алкильную группу, содержащую 1-6 атомов углерода; R10 представляет карбонильную группу, метиленовую группу, группу - NH-CH2- или группу -S-CH2-, L предпочтительно представляет этильную, бутильную или гексильную группу, Т предпочтительно представляет группу -NH-, V предпочтительно представляет группу - NH-, a m предпочтительно равно 1.
В другом своем варианте, настоящее изобретение относится к новым аффинным лигандам общей формулы (XV):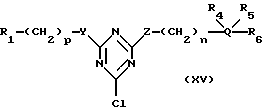
где R1, R4, R5, R6, Q, n и p являются такими, как указано выше.
В другом своем варианте, настоящее изобретение относится к новым аффинным лигандам общей формулы (XVI):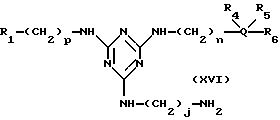
где R1, R4, R5, R6, Q, n и p являются такими, как указано выше, a j представляет целое число от 2 до 20.
В другом предпочтительном варианте, настоящее изобретение относится к аффинным лигандам общей формулы (XII), (XIII), (XIV), (VIII), (XV) и (XVI), где R1 представляет фенильную или нафтильную группу, каждая из которых необязательно замещена на бензольном или нафталиновом кольце одной или несколькими группами, независимо выбранными из гидроксильных или карбоксильных групп.
В другом предпочтительном варианте, настоящее изобретение относится к аффинным лигандам общей формулы (XII), (XIII), (XIV), (VIII), (XV) и (XVI), где R4 представляет атом водорода, гидроксильную группу, карбоксильную группу или аминогруппу.
В другом предпочтительном варианте, настоящее изобретение относится к аффинным лигандам общей формулы (XII), (XIII), (XIV), (VIII), (XV) и (XVI), где R5 представляет атом водорода, гидроксильную группу, карбоксильную группу или аминогруппу.
В другом предпочтительном варианте, настоящее изобретение относится к аффинным лигандам общей формулы (XII), (XIII), (XIV), (VIII), (XV) и (XVI), где R6 представляет атом водорода, гидроксильную группу, карбоксильную группу или аминогруппу.
В другом предпочтительном варианте, настоящее изобретение относится к аффинным лигандам общей формулы (XII), (XIII), (XIV), (VIII), (XV) и (XVI), где Q представляет бензольное или нафталиновое кольцо.
В другом предпочтительном варианте, настоящее изобретение относится к аффинным лигандам общей формулы (XII), (XIII), (XIV) и (VIII), где X представляет атом азота.
В другом предпочтительном варианте, настоящее изобретение относится к аффинным лигандам общей формулы (XII), (XIII), (XIV) и (VIII), где Y представляет группу -NH-.
В другом предпочтительном варианте, настоящее изобретение относится к аффинным лигандам общей формулы (XII), (XIII), (XIV) и (VIII), где Z представляет группу -NH-.
В другом предпочтительном варианте, настоящее изобретение относится к аффинным лигандам общей формулы (XII), (XIII), (XIV), (VIII), (XV) и (XVI), где n = 0 или 2.
В другом предпочтительном варианте, настоящее изобретение относится к аффинным лигандам общей формулы (XII), (XIII), (XIV), (VIII), (XV) и (XVI), где p = 0 или 2.
В другом предпочтительном варианте, настоящее изобретение относится к аффинным лигандам общей формулы (XIII), (XIV) и (XVI), где j = 2, 4 или 6.
В другом предпочтительном варианте, настоящее изобретение относится к аффинным лигандам вышеуказанной общей формулы (XI), где j представляет целое число от 2 до 20.
Предпочтительными аффинными лигандами настоящего изобретения являются: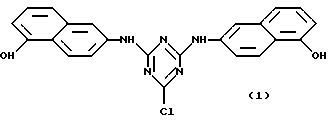
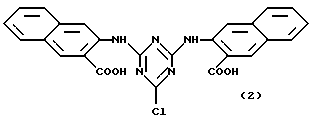
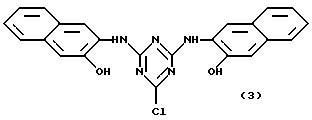
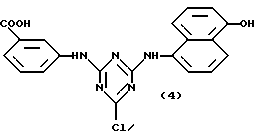
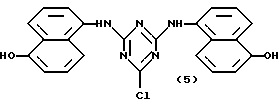
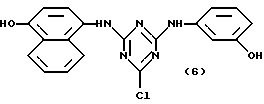
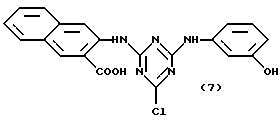

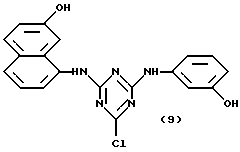


Кроме того, настоящее изобретение относится к способу связывания новых аффинных лигандов общих формул (VII), (XIII), (XIV) и (XI), определенных выше, с углеводной матрицей или матрицей из органического полимера путем реакции указанной углеводной матрицы или матрицы из органического полимера с активирующим агентом и последующей реакции активированной матрицы с новым аффинным лигандом, необязательно в присутствии агента, связывающего кислоту. Настоящее изобретение также относится к способу связывания новых аффинных лигандов общей формулы (XIV), определенной выше, с углеводной матрицей или с матрицей из органического полимера путем реакции конденсации с указанной матрицей. Настоящее изобретение также относится к способу связывания новых аффинных лигандов общих формул (VII), (XIII), (XVI) и (XI), определенных выше, с матрицами, полученными на основе окиси металла, стекла или двуокиси кремния, и необязательно покрытыми органическим полимером, путем реакции необязательно покрытых матриц на основе окиси металла, стекла или двуокиси кремния с активирующим агентом, и последующей реакции активированной матрицы с новым аффинным лигандом необязательно в присутствии агента, связывающего кислоту. В другом своем варианте, настоящее изобретение относится к способу связывания новых аффинных лигандов общей формулы (XIV), определенной выше, с матрицами из окиси металла, стекла или двуокиси кремния, необязательно покрытыми органическим полимером, путем конденсации этих лигандов с указанной матрицей. В другом своем варианте, настоящее изобретение относится к способу связывания новых аффинных лигандов общих формул (XV) и (XII), определенных выше, с матрицей общей формулы (V), определенной выше, путем реакции новых аффинных лигандов с матрицей при температуре от -20oC до 121oC, необязательно в присутствии агента, связывающего кислоту. Настоящее изобретение также относится ко всем конъюгатам аффинный лиганд - матрица, полученным вышеописанными способами.
В другом своем варианте, настоящее изобретение относится к использованию аффинных лигандов настоящего изобретения и конъюгатов аффинный лиганд - матрица, содержащих лиганды настоящего изобретения, для разделения, выделения, очистки, характеризации, идентификации или количественной оценки белков или белковых материалов, таких как, иммуноглобулины или их подклассы, фрагменты, предшественники, или производные, независимо от того, происходят они от природных или от рекомбинантных источников, например, иммуноглобулин G (IgG), иммуноглобулин М (IgM), иммуноглобулин А (IgA) или их подклассы, фрагменты, предшественники или производные, происходящие как от природных, так и от рекомбинантных источников. В другом своем варианте, настоящее изобретение относится к разделению, выделению, очистке, характеризации, идентификации или количественной оценке иммуноглобулинов любым способом, в котором указанные иммуноглобулины наносят на конъюгаты аффинный лиганд - матрица настоящего изобретения при pH 5,0-12,0, а затем удаляют, элюируют или десорбируют путем снижения pH до 4,9 или ниже.
Настоящее изобретение также относится к способу разделения или очистки белковых материалов, предусматривающему проведение аффинной хроматографии с использованием в качестве биоспецифического лиганда общей формулы (а), лиганда, описанного выше.
В другом своем варианте, настоящее изобретение относится к использованию аффинных лигандов настоящего изобретения и конъюгатов аффинный лиганд - матрица, содержащих лиганды настоящего изобретения, для разделения, выделения, очистки, характеризации, идентификации или количественной оценки инсулинов, их аналогов, производных, фрагментов и предшественников, происходящих как от природных, так и от рекомбинантных источников, а также фактора VII или человеческого гормона роста или их аналогов, производных, фрагментов и предшественников.
Например, была сконструирована библиотека, содержащая более 60 различных лигандов. Эту библиотеку скринировали с использованием частично очищенного предшественника инсулина, и отобранные лиганды иммобилизовали на агарозе путем твердофазного синтеза. С использованием соответствующей техники связывания, матрицы оптимизировали по длине и природе спейсерной группы, лигандной плотности и т. п. , в результате чего получали 3 прототипа, отличающиеся по своей динамической емкости связывания, составляющей 2-5 мг/мл. Рекомбинантный предшественник инсулина был очищен до чистоты более 95% из осветленного сбраживаемого дрожжевого бульона путем проведения одной стадии, имитирующей аффинную очистку в очень мягких условиях.
Таким образом, особенно предпочтительным использованием аффинных лигандов настоящего изобретения и конъюгатов аффинный лиганд - матрица, содержащих аффинные лиганды настоящего изобретения, является очистка инсулинов, их аналогов, производных, фрагментов и предшественников, происходящих как от натуральных, так и от рекомбинантных источников. Особенно предпочтительные конъюгаты - аффинный лиганд - матрица для такого использования содержат лиганд, выбранный из нижеследующих лигандов: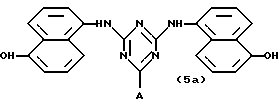
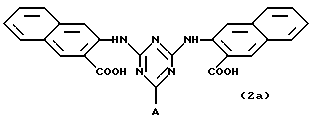
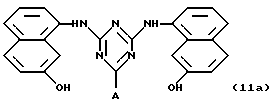
где лиганд связан с матрицей-носителем в положении А, как описано выше, необязательно посредством "спейсерной ножки", расположенной между матрицей и лигандом, представленным общей формулой (b), определенной выше. Предпочтительным лигандом является 11а, а предпочтительной матрицей-носителем является необязательно активированная агароза, целлюлоза, кремнезем или стекло.
В другом своем варианте, настоящее изобретение относится к разделению, выделению, очистке, характеризации, идентификации или количественной оценке инсулинов или аналогов инсулинов, их производных и предшественников любым способом, в котором указанные инсулины, производные, аналоги и предшественники инсулина наносят на конъюгаты аффинный лиганд - матрица настоящего изобретения при pH в пределах от 4,0 до 9,0, а затем удаляют, элюируют или десорбируют путем снижения pH до 3,99 или ниже, либо повышения до 9,01 или выше. Процедура элюции может быть, например, альтернативно, осуществлена путем понижения ионной силы или путем добавления сорастворителей, таких как органические растворители.
Более подробно, настоящее изобретение описано в нижеследующих примерах. Эти примеры приводятся лишь в иллюстративных целях и не должны рассматриваться как некое ограничение настоящего изобретения.
Пример 1
В данном примере проиллюстрирован синтез типичного аффинного лиганда, проведенный посредством реакции галогенсодержащих гетероциклических соединений общей формулы (II) с соединениями общей формулы (III) и (IV).
19,8 ч. анилина растворяли в 50 ч. ацетона, и этот раствор вводили в суспензию, полученную в результате выливания раствора 36,8 ч. хлорангидрида циануровой кислоты в 200 ч. ацетона в смесь, содержащую 50 ч. льда и 50 ч. воды. Смесь перемешивали 2 ч, в течение которых pH поддерживали между 6 и 7 путем добавления раствора, содержащего 16,8 ч. бикарбоната натрия и 300 ч. воды. По истечении этого времени, осадок 2-анилин-4,6-дихлор-1,3,5- триазина отфильтровывали, промывали водой, сушили в вакууме и кристаллизовали из дихлорметана.
Раствор 2,74 ч. тирамина в смеси 50 ч. ацетона и 10 ч. воды добавляли к раствору 4,82 ч. 2-анилин-4,6-дихлор-1,3,5-триазина в 100 ч. ацетона. Полученную смесь нагревали до температуры 50oC и выдерживали при этой температуре в течение 2 ч, при поддерживании pH от 6 до 7 путем добавления раствора 1,68 ч. бикарбоната натрия в 30 ч. воды. По истечении этого времени, осадок 2-анилин- 4-[ 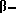 (4'-гидроксифенил)-этиламино]-6-хлор-1,3,5- триазина отфильтровывали, промывали водой и сушили в вакууме.
(4'-гидроксифенил)-этиламино]-6-хлор-1,3,5- триазина отфильтровывали, промывали водой и сушили в вакууме.
Пример 2
В данном примере проиллюстрирована методика иммобилизации продукта примера 1 на твердофазном носителе.
10 ч. агарозы, несущей аминогруппы, переносили в ацетоновый растворитель путем замены растворителя с использованием 100 ч. 30% водного раствора ацетона, затем 100 ч. 70% водного раствора ацетона, а затем 100 ч. ацетона. 1 ч. 2-анилин-4- [ 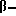 (4'-гидроксифенил)-этил- амино]-6-хлор-1,3,5-триазина растворяли в 20 ч. ацетона и нагревали до температуры 50oC. Этот теплый ацетоновый раствор добавляли к ацетоновой суспензии производного агарозы, несущего аминогруппы. К полученной суспензии добавляли раствор 0,42 ч. бикарбоната натрия в 5 ч. воды, и смесь перемешивали в течение 16 ч при 50oC. По истечении этого времени, агарозную матрицу-носитель отмывали от несвязанного 2-анилин-4-[
(4'-гидроксифенил)-этил- амино]-6-хлор-1,3,5-триазина растворяли в 20 ч. ацетона и нагревали до температуры 50oC. Этот теплый ацетоновый раствор добавляли к ацетоновой суспензии производного агарозы, несущего аминогруппы. К полученной суспензии добавляли раствор 0,42 ч. бикарбоната натрия в 5 ч. воды, и смесь перемешивали в течение 16 ч при 50oC. По истечении этого времени, агарозную матрицу-носитель отмывали от несвязанного 2-анилин-4-[  (4'-гидроксифенил)-этиламино]-6-хлор-1,3,5- триазина ацетоном. Затем полученный дериватизированный аффинный носитель переносили обратно в воду путем промывки сначала 70% водным раствором ацетона, затем 30% водным раствором ацетона и, наконец, водой.
(4'-гидроксифенил)-этиламино]-6-хлор-1,3,5- триазина ацетоном. Затем полученный дериватизированный аффинный носитель переносили обратно в воду путем промывки сначала 70% водным раствором ацетона, затем 30% водным раствором ацетона и, наконец, водой.
Пример 3
В этом примере проиллюстрировано использование новой аффинной матрицы, описанной в примере 2, в качестве специфической хроматографической матрицы для иммуноглобулинов.
1,25 ч. плазмы человека разбавляли 3,75 ч. водного фосфатного буфера, имеющего pH 7 и концентрацию 10 миллимоль на литр, а затем наносили на колонку, содержащую 1 ч. аффинной матрицы, полученной, как описано в примере 2. Затем аффинную колонку промывали фосфатным буфером до тех пор, пока УФ-мониторинг промывочных растворов не указывал на то, что весь несвязанный белок удален. Затем аффинную матрицу промывали цитратным буфером, имеющим pH 3,8 и концентрацию 0,2 миллимоль на литр, до тех пор, пока УФ-мониторинг промывочного раствора не указывал на то, что удаление связанного белка завершилось. Было обнаружено, что белок, содержащийся в этом промывочном растворе, является иммуноглобулином G.
В таблице 1, кроме того, представлены примеры новых аффинных лигандов настоящего изобретения, которые могут быть получены способом, описанным в примере 1, но с заменой 36,8 ч. хлорангидрида циануровой кислоты, использованного в примере 1, на соответствующее количество галогенсодержащего гетероциклического соединения, представленного в колонке II данной таблицы; а также, с заменой 19,8 ч. анилина, используемого в примере 1, на соответствующее количество амина, представленного в колонке III данной таблицы; и с заменой 2,74 ч. тирамина, используемого в примере 1, на соответствующее количество амина, представленного в колонке IV этой таблицы. Номера примеров указаны в колонке I данной таблицы.
Эти лиганды, описанные в примерах 4-38, могут быть присоединены к агарозной матрице методом, подробно описанным в примере 2, и использованы для очистки иммуноглобулина G методом, описанным в примере 3.
Пример 39
6 ч. этилендиамина добавляли к раствору 2,5 ч. 2-анилино-4-[ 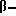 (4'-гидроксифенил)-этиламино] -6-хлор-1,3,5-триазина в 20 ч. толуола, и смесь нагревали при 100oC в течение 16 ч. Затем толуол выпаривали из смеси при пониженном давлении, и остаток 5 раз промывали 100 ч. воды, а затем сушили при 70oC.
(4'-гидроксифенил)-этиламино] -6-хлор-1,3,5-триазина в 20 ч. толуола, и смесь нагревали при 100oC в течение 16 ч. Затем толуол выпаривали из смеси при пониженном давлении, и остаток 5 раз промывали 100 ч. воды, а затем сушили при 70oC.
В таблице 2, кроме того, представлены примеры новых аффинных лигандов настоящего изобретения, которые могут быть получены способом, описанным в примере 39, но с заменой 2,5 ч. 2-анилино-4- [ 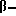 (4'-гидроксифенил)-этиламино]- 6-хлор-1,3,5-триазина, используемого в примере 39, на соответствующее количество хлортриазина, представленного в колонке II таблицы 2, и с заменой этилендиамина, используемого в примере 39, на соответствующее количество диамина или аминогидрокси- соединения, представленных в Колонке III таблицы 2.
(4'-гидроксифенил)-этиламино]- 6-хлор-1,3,5-триазина, используемого в примере 39, на соответствующее количество хлортриазина, представленного в колонке II таблицы 2, и с заменой этилендиамина, используемого в примере 39, на соответствующее количество диамина или аминогидрокси- соединения, представленных в Колонке III таблицы 2.
Пример 58
В этом примере проиллюстрирован способ иммобилизации соединения, полученного в примере 39, на твердофазном носителе.
60 ч. агарозы, несущей эпоксидные группы, промывали 300 ч. воды, а затем 300 ч. раствора, состоящего из 5,95 ч. бикарбоната калия, растворенного в 180 ч. метанола и 120 ч. воды. 1 ч. соединения, полученного, как описано в примере 39, растворяли в 60 ч. метанола и добавляли к раствору 40 ч. водного раствора бикарбоната калия. Затем 100 ч. этого водного раствора метанола добавляли к полученной суспензии из 60 ч. агарозы, несущей эпокси-группы, и полученную суспензию слегка перемешивали при комнатной температуре в течение 16 ч. Полученную матрицу на основе агарозы промывали сначала смесью 360 ч. метанола и 240 ч. воды, а затем 600 ч. воды.
Пример 59
Повторяли процедуру примера 3, за исключением того, что колонку, содержащую 1 ч. аффинной матрицы, которую получали как описано в примере 2, заменяли на колонку, содержащую 1 ч. аффинной матрицы, полученной, как описано в примере 58. Белок, содержащийся в промывочном растворе с pH 3,8, был снова идентифицирован как иммуноглобулин G.
Пример 60
В этом примере проиллюстрирована иммобилизация продукта, полученного в примере 39, на твердофазном носителе.
80 ч. агарозы последовательно промывали 1050 ч. воды, 1050 ч. 30%-ного водного раствора ацетона, 1050 ч. 70% водного раствора ацетона и 1425 ч. ацетона. 80 ч. агарозы затем суспендировали в 100 ч. ацетона, и полученную суспензию нагревали до 37oC. К агарозной суспензии добавляли 15 ч. пара-толуолсульфонилхлорида, растворенного в 15 ч. пиридина и 25 ч. ацетона, и полученную смесь выдерживали в течение 8 ч при 37oC. Затем активированную агарозу промывали 225 ч. ацетона, 225 ч. 70% водного раствора ацетона, затем 225 ч. 30% водного раствора ацетона, и наконец, 225 ч. воды.
45 ч. этой активированной матрицы промывали 225 ч. раствора, содержащего 2,3 ч. бикарбоната калия, растворенного в смеси 178 ч. метанола и 47 ч. воды. К активированной агарозной суспензии добавляли раствор 0,75 ч. соединения, полученного, как описано в примере 39, в смеси из 45 ч. метанола и 30 ч. воды, содержащей 1,5 ч. бикарбоната калия, а затем полученную смесь оставляли на 16 ч при комнатной температуре. Полученную аффинную матрицу промывали 270 ч. метанола и 180 ч. воды, содержащей 9 ч. бикарбоната калия, а затем 450 ч. воды.
Перед использованием, 115 ч. полученной аффинной матрицы суспендировали в растворе 0,36 ч. гидроксида натрия в 45 ч. воды.
Пример 61
При повторении процедуры примера 3, но с заменой колонки, содержащей 1 ч. аффинной матрицы, получение которой описано в примере 2, на колонку, содержащую 1 ч. аффинной матрицы, получение которой описано в примере 60, белок, содержащийся в промывочном растворе при pH 3,8, был снова идентифицирован как иммуноглобулин G.
Пример 62
10 ч. аффинной матрицы, полученной, как описано в примере 60, выдерживали в фосфатном буфере, имеющем pH 8,0, в течение 16 ч. Повторяли процедуру примера 3, за исключением того, что используемую там матрицу заменяли на эквивалентное количество этой новой аффинной матрицы, а вместо плазмы человека, используемой в примере 3, использовали бесклеточный супернатант от культуральной клеточной среды, содержащей мышиный иммуноглобулин. Белок, содержащийся в промывочном растворе с pH 3,8, снова был идентифицирован как мышиный иммуноглобулин М.
В таблице 3, кроме того, представлены примеры связывания новых аффинных лигандов настоящего изобретения, которые могут быть получены способом, описанным в примере 58, но с заменой нового аффинного лиганда, используемого в примере 58, на соответствующее количество нового аффинного лиганда, указанного в колонке II таблицы 3, и с заменой 39 ч. агарозы, активированной эпихлоргидрином и используемой в примере 58, на соответствующее количество углевода, указанного в колонке III таблицы 3, и активированного реагентом, указанным в колонке IV таблицы 3.
Пример 70
Повторяли процедуру получения лиганда, подробно описанную в примере 1, за исключением того, что 2,74 ч. тирамина подвергали реакции с 4,84 ч. 2-фенокси-4,6-дихлор-1,3,5- триазина вместо 4,82 ч. 2-анилино-4,6-дихлор-1,3,5-триазина с получением 2-фенокси-4-  [(4'-гидроксифенил)-этиламино]-6-хлор- 1,3,5-триазина, который может быть использован вместо 2-анилино-4-[
[(4'-гидроксифенил)-этиламино]-6-хлор- 1,3,5-триазина, который может быть использован вместо 2-анилино-4-[ 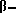 (4'-гидроксифенил)-этил- амино]-6-хлор-1,3,5-триазина для получения аффинной матрицы способом, описанным в примере 2. Аналогично, иммуноглобулин G может быть стандартным способом выделен из плазмы человека методом, описанным в примере 3.
(4'-гидроксифенил)-этил- амино]-6-хлор-1,3,5-триазина для получения аффинной матрицы способом, описанным в примере 2. Аналогично, иммуноглобулин G может быть стандартным способом выделен из плазмы человека методом, описанным в примере 3.
Пример 71
Вместо 4,84 ч. 2-фенокси-4,6-дихлор-1,3,5- триазина, используемого в примере 70, были использованы 5,16 ч. 2-фенилтио-4,6-дихлор-1,3,5-триазина, в результате чего был получен 2-фенилтио-4-[ 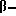 -(4'-гидроксифенил)-этиламино]-6- хлор- 1,3,5- триазин, который может быть аналогичным образом использован для очистки иммуноглобулина G.
-(4'-гидроксифенил)-этиламино]-6- хлор- 1,3,5- триазин, который может быть аналогичным образом использован для очистки иммуноглобулина G.
Пример 72
В этом примере проиллюстрирован альтернативный способ продуцирования конъюгатов аффинный лиганд - матрица, как описано в примере 2 и примере 58.
10 ч. агарозы, несущей аминоэтиламино-группы, перемешивали при 0-5oC с 5 ч. ацетона и 5 ч. водного фосфатного буфера, pH 7, при концентрации, составляющей 0,5 моль на литр. К этой суспензии добавляли 2,5 ч. раствора, содержащего 1 ч. хлорангидрида циануровой кислоты в 10 ч. ацетона, а затем смесь перемешивали в течение 1 ч при температуре 0-5oC. Полученную агарозу, активированную дихлортриазином, последовательно промывали 50 ч. 50% водного раствора ацетона, 50 ч. воды, 50 ч. 50% водного раствора ацетона и 100 ч. воды. 20 ч. промытой агарозы, активированной дихлортриазином, добавляли к 20 ч. водного раствора, содержащего 1 ч. тирамина в 200 ч. воды, и полученную суспензию перемешивали в течение 16 ч при комнатной температуре. По истечении этого времени, полученную дериватизированную матрицу промывали 200 ч. воды и добавляли к 20 ч. водного раствора, содержащего 0,55 ч. анилина, растворенного в 200 ч. воды. Полученную суспензию перемешивали в течение 16 ч при 90oC, после чего, дериватизированную матрицу промывали 200 ч. воды.
Пример 73
При повторении процедуры примера 3, но с заменой колонки, содержащей 1 ч. аффинной матрицы, получение которой описано в примере 2, на колонку, содержащую 1 ч. аффинной матрицы, получение которой описано в примере 72, белок, содержащийся в промывочном растворе с pH 3,8, был снова идентифицирован как иммуноглобулин G.
Пример 74
В этом примере проиллюстрирован синтез библиотеки конъюгатов аффинный лиганд - матрица настоящего изобретения, которые могут быть затем скринированы для определения их белок-связывающих свойств.
1 ч. агарозы, несущей аминогруппы, смешивали с 1 ч. 1 М фосфатно-калиевого буфера, pH 7,0, и оставляли для осаждения под действием силы тяжести. Забуференную амином агарозу переносили в реакционный сосуд и смешивали при 0-5oC с 0,5 ч. 0,5 М фосфатно-калиевого буфера, pH 7,0, и 0,5 ч. ацетона. Затем добавляли 1/4 ч. раствора, содержащего 1 ч. хлорангидрида циануровой кислоты в 10 ч. ацетона, и смесь перемешивали в течение 1 ч при 0-5oC, после чего, смесь фильтровали и последовательно промывали 10 ч. 50% ацетона, 6 ч. воды, 6 ч. 50% ацетона и 10 ч. воды, в результате чего получали агарозу, активированную 2,4-дихлор-сим-триазин-6-илом.
1 ч. агарозы, активированной 2,4-дихлор-сим-триазин-6-илом, добавляли к 5 молярным эквивалентам аминового соединения, представленного в колонке II таблицы 4 и растворенного в 2-3 ч. раствора, содержащего 1 ч. ацетона и 1 ч. воды, а затем доводили до нейтрального pH путем добавления гидроксида натрия. Суспензию перемешивали в течение 24 ч при 30oC. Полученную агарозу, активированную монохлорсим-триазин-6- илом, последовательно промывали 10 ч. диметилформамида, 10 ч. раствора, содержащего 3 ч. пропан-2-ола и 7 ч. 0,2 М гидроксида натрия, и 10 ч. воды, а затем оставляли для оседания под действием силы тяжести.
1 ч. монохлор-сим-триазин-6-ил-активированной агарозы добавляли к 5 молярным эквивалентам аминового соединения, представленного в колонке III таблицы 4 и растворенного в 2-3 ч. раствора, содержащего 1 ч. диметилформамида и 1 ч. воды, а затем доводили до нейтрального pH путем добавления гидроксида натрия. Суспензию размешивали в течение 72 ч при 85-95oC. Полученные конъюгаты аффинный лиганд - матрица последовательно промывали 10 ч. диметилформамида, 10 ч. раствора, содержащего 3 ч. пропан-2-ола и 7 ч. 0,2 М гидроксида натрия, и 10 ч. воды, а затем оставляли для оседания под действием силы тяжести. Синтезировали библиотеку конъюгатов аффинный лиганд - матрица настоящего изобретения. Примеры которых указаны в колонке I таблицы 4.
Пример 128
В этом примере проиллюстрирован метод скрининга, в результате которого могут быть идентифицированы белок-связывающие свойства конъюгатов аффинный лиганд - матрица, описанных в примере 74.
Хроматографические колонки с 1 мл полного объема упаковывали конъюгатами аффинный лиганд - матрица примеров 75-127. Эти колонки уравновешивали путем интенсивной промывки 10 мл 50 мМ фосфатно-натриевого буфера, pH 8,0. На каждую хроматографическую колонку наносили 1 мл раствора, содержащего 1,5 мг IgG человека на 1 мл 50 мМ фосфатно-натриевого буфера, pH 8,0, а затем колонку промывали 10 мл 50 мМ фосфатно- натриевого буфера, pH 8,0, для удаления несвязанного иммуноглобулина G. Связанный IgG элюировали путем интенсивной промывки каждой колонки 5 мл 50 мМ цитратно-натриевого буфера, pH 3,0. Содержание IgG в промывках и фракциях элюции определяли путем измерения оптической плотности при 280 нм по отношению к буферному контролю. Анализ полученных результатов
выявил, что все конъюгаты аффинный лиганд - матрица примеров 75-127 связывались с IgG человека. Отсюда видно, что для конъюгатов аффинный лиганд - матрица примеров 92, 99, 101, 102, 103, 111, 113 и 119 было достигнуто почти количественное элюирование связанного IgG, в результате чего, можно считать, что эти конъюгаты имеют исключительную эффективность при разделении, выделении или очистке человеческого IgG.
Пример 129
Селективное связывание и элюирование рекомбинантного фактора свертывания крови VIIa (rFVIIa), нанесенного на аффинную матрицу примера 181, из клеточной культуральной среды.
Процедура:
0,85 мл осажденного объема аффинной матрицы, полученной, как описано в примере 181, упаковывали в 5х50 мм-колонку (Pharmacia HR 5/5) и уравновешивали 20 мл буфера А: 20 мМ Трис, 50 мМ NaCl, 5 мМ CaCl2, pH 8,0. 5 мл супернатанта кондиционированной клеточной культуры ВHК, обогащенной 1,4 мг rFVIIa, наносили на упакованную колонку.
После отмывки несвязывающихся белков 10 мл буфера А, rFVIIa элюировали с использованием 5 мл буфера В: 20 мМ Трицитрат натрия, 50 мМ Трис, pH 8,0.
Скорость потока в процессе хроматографии составляла 0,3 мл/мин.
Поток, вытекающий с колонки, пропускали через устройство с УФ-монитором и собирали в 1 мл-фракции, и каждую фракцию анализировали на содержание rFVIIa и полного белка путем аналитической обращенно-фазовой высокоразрежающей жидкостной хроматографии (ОФ-ВРЖХ).
Результаты:
С помощью УФ-монитора было выявлено, что большая часть из УФ (280 нм)-абсорбирующегося материала выходила во время нанесения надосадочной фракции и последующей промывки буфером А. В процессе последующего элюирования буфером В, наблюдался заметный пик, который соответствовал ожидаемому размеру нанесенного количества rFVIIa.
ОФ-ВРЖХ-анализ собранных фракций показал, что 90% нанесенного количества rFVIIa выходило во фракциях в процессе элюции буфером В. Чистота rFVIIa в этих фракциях составляла выше 95%.
Результаты показали, что в данном случае достигается селективное связывание rFVIIa из обогащенных культуральных сред с используемым лигандом.
Пример 130
Очистка В-цепи1-29 инсулина - А-цепи1-21 А-А-К- инсулина на конъюгате аффинный лиганд - матрица примера 171
255 мг В-цепи1-29 инсулина - А-цепи1-21 Ala-Ala-Lys-инсулина (партия А202558) суспендировали в 51 мл H2O. Для солюбилизации предшественника добавляли 10 капель 1 М уксусной кислоты. Затем добавляли 0,2 М цитрат калия, pH 5,5 до полного объема 510 мл с получением раствора 0,12 мг/мл (ОФ-ВРЖХ- анализ). Измеренный pH составлял 5,53, ионная сила составляла 30,0 мСм/см, а окислительно-восстановительный потенциал составлял 273 мВ.
400 мл вышеуказанного раствора наносили на колонку Pharmacia К16 (1,6 х 6 см), упакованную 12 мл вышеуказанного конъюгата матрицы и уравновешенную в 0,2 М цитрате калия, pH 5,5, при 1,8 мл/мин при температуре окружающей среды. Эту колонку промывали в 50 мл 0,2 М цитрата калия, pH 5,5, а затем элюировали 0,1 М уксусной кислотой при 1,8 мл/мин. Было собрано 12 фракций по 5,0 мл.
Колонку очищали 50 мл 0,5 М NaOH и регенерировали 50 мл 0,1 М лимонной кислоты, 60% (об./об.) этанолом.
Образцы для ОФ-ВРЖХ- анализа разбавляли 2 М уксусной кислотой непосредственно перед анализом (см. табл. 5).
Таким образом, полный выход составил 83%.
Чистота продукта была определена с помощью ОФ-ВРЖХ-анализа и составила 94%. Оставшиеся примеси также были инсулиноподобными.
Пример 131
Очистка des-ThrB30 -инсулина на конъюгате аффинный лиганд - матрица примера 171
150 мг осадка des-ThrB30 -инсулина (INS-J-009) суспендировали в 50 мл H2O. Для растворения суспензии добавляли 5 капель 2 М уксусной кислоты. 0,2 М цитрат калия, pH 5,5, добавляли до объема 500 мл и получали концентрацию 0,076 мг/мл (ОФ-ВРЖХ-анализ). Измеренный pH составлял 5,52, ионная сила составляла 30 мСм/см, а окислительно- восстановительный потенциал составлял 264 мВ. 400 мл вышеуказанного раствора наносили на колонку Pharmacia К16 (1,6 х 6 см), упакованную 12 мл вышеуказанного конъюгата матрицы и уравновешенную в 0,2 М цитрате калия, pH 5,5, при 1,8 мл/мин при температуре окружающей среды. Эту колонку промывали в 50 мл 0,2 М цитрата калия, pH 5,5, а затем элюировали 0,1 М уксусной кислотой при 1,8 мл/мин. Были собраны 10 фракций по 5,0 мл.
Колонку очищали 50 мл 0,5 М NaOH и регенерировали 50 мл 0,1 М лимонной кислоты, 60% (об./об.) этанолом.
Образцы для ОФ-ВРЖХ- анализа разбавляли 2 М уксусной кислотой непосредственно перед анализом (см. табл. 6).
Таким образом, полный выход составил 71%.
Чистота продукта, определенная с помощью ОФ-ВРЖХ-анализа, составляла 91%, а остальные примеси являлись инсулиноподобными.
Пример 132
Очистка В-цепи1-29 инсулина-А-цепи1-21 А-А-К- инсулина на конъюгате аффинный лиганд - матрица примера 145
Два литра центрифугированного бульона (партия 628) доводили до pH 5,5 путем добавления 5 М NaOH, фильтровали через фильтр Leitz Tiefenfilter (Seitz EK), а затем снова фильтровали через фильтр Leitz Tiefenfilter (Seitz EKS). Концентрация, измеренная с помощью ОФ-ВРЖХ, составляла 0,006 мг/мл. Измеренная ионная сила составляла 12,2 мСм/см, а окислительно-восстановительный потенциал составлял 316 мВ.
1000 мл вышеуказанного раствора наносили на колонку Pharmacia К16 (1,6 х 6 см), упакованную 12 мл вышеуказанного конъюгата матрицы и уравновешенную в 0,2 М цитрате калия, pH 5,5, при 1,8 мл/мин при температуре окружающей среды. Колонку промывали в 50 мл 0,2 М цитрата калия, pH 5,5, а затем элюировали 0,1 М уксусной кислотой при 1,8 мл/мин. Было собрано 11 фракций по 5,0 мл.
Колонку очищали 50 мл 0,5 М NaOH и регенерировали 50 мл 0,1 М лимонной кислоты, 60% (об./об.) этанолом.
Образцы для ОФ-ВРЖХ-анализа разбавляли 2 М уксусной кислотой непосредственно перед анализом (см. табл. 7).
Таким образом, полный выход составил 63%.
Чистота продукта, определенная с помощью ОФ-ВРЖХ-анализа, составляла до 88%. Остальные примеси были инсулиноподобными.
Пример 133
Очистка В-цепи1-29 инсулина-А-цепи1-21 А-А-К- инсулина на конъюгате аффинный лиганд - матрица примера 171
Два литра центрифугированного бульона (партия 628) доводили до pH 5,5 путем добавления 5 М NaOH, фильтровали через фильтр Leitz Tiefenfilter (Seitz EK), а затем снова фильтровали через фильтр Leitz Tiefenfilter (Seitz EKS). Концентрация, измеренная с помощью ОФ-ВРЖХ, составляла 0,006 мг/мл. Измеренная ионная сила составляла 12,2 мСм/см, а окислительно-восстановительный потенциал составлял 316 мВ.
1000 мл вышеуказанного раствора наносили на колонку Pharmacia К16 (1,6 х 6 см), упакованную 12 мл вышеуказанного конъюгата матрицы и уравновешенную в 0,2 М цитрате калия, pH 5,5, при 1,8 мл/мин при температуре окружающей среды. Колонку промывали в 50 мл 0,2 М цитрата калия, pH 5,5, а затем элюировали 0,1 М уксусной кислотой при 1,8 мл/мин. Было собрано 11 фракций по 5,0 мл.
Колонку очищали 50 мл 0,5 М NaOH и регенерировали 50 мл 0,1 М лимонной кислоты, 60% (об./об.) этанолом.
Образцы для ОФ-ВРЖХ-анализа разбавляли 2 М уксусной кислотой непосредственно перед анализом (см. табл. 8).
Таким образом, полный выход составил 74%.
Чистота продукта, определенная с помощью ОФ-ВРЖХ-анализа, составляла до 86%. Остальные примеси были инсулиноподобными.
Пример 134
Очистка В-цепи (1-29) ЕЕАЕРК-инсулина- А-цепи (1- 21) ААК-инсулина на конъюгате аффинный лиганд - матрица примера 171
Центрифугированный дрожжевой бульон (партия Y44) фильтровали через фильтр Letz Tiefenfilter (Seitz EK) с получением концентрации 0,35 мг/мл (ОФ-ВРЖХ-анализ). Измеренный pH составлял 5,27, ионная сила составляла 7,38 мСм/см, а окислительно-восстановительный потенциал составлял 221 мВ.
120 мл вышеуказанного раствора наносили на колонку Pharmacia К16 (1,6 х 6 см), упакованную 12 мл вышеуказанного конъюгата матрицы и уравновешенную в 0,2 М цитрате калия, pH 5,5, при 1,8 мл/мин при температуре окружающей среды. Колонку промывали в 50 мл 0,2 М цитрата калия, pH 5,5, а затем элюировали 0,1 М уксусной кислотой при 1,8 мл/мин. Было собрано 11 фракций по 5,0 мл.
Колонку очищали 50 мл 0,5 М NaOH и регенерировали 50 мл 0,1 М лимонной кислоты, 60% (об./об.) этанолом.
Образцы для ОФ-ВРЖХ-анализа разбавляли 2 М уксусной кислотой непосредственно перед анализом (см. табл. 9).
Таким образом, полный выход составил 79%.
Чистота продукта была определена с помощью ОФ-ВРЖХ-анализа и составила 93%. Оставшиеся примеси также были инсулиноподобными.
Пример 135
Очистка В-цепи1-29 [AspB28]-инсулина -А- цепи 1-21А-А-К-инсулина на конъюгате аффинный лиганд-матрица примера 171
Центрифугированный бульон (партия GSG9414) доводили до pH 5,5 путем добавления 5 М NaOH, фильтровали через фильтр Leitz Tiefenfilter (Seitz EK), а затем снова фильтровали через фильтр Leitz Tiefenfilter (Seitz EKS). Концентрация, измеренная с помощью ОФ-ВРЖХ, составляла 0,02 мг/мл. Измеренная ионная сила составляла 17,0 мСм/см, а окислительно-восстановительный потенциал составлял 308 MB.
800 мл вышеуказанного раствора наносили на колонку Pharmacia К16 (1,6 х 6 см), упакованную 12 мл вышеуказанного конъюгата матрицы и уравновешенную в 0,2 М цитрате калия, pH 5,5, при 1,8 мл/мин при температуре окружающей среды. Эту колонку промывали в 50 мл 0,2 М цитрата калия, pH 5,5, а затем элюировали 0,1 М уксусной кислотой при 1,8 мл/мин. Были собраны 12 фракций по 5,0 мл.
Колонку очищали 50 мл 0,5 М NaOH и регенерировали 50 мл 0,1 М лимонной кислоты, 60% (об./об.) этанолом.
Образцы для ОФ-ВРЖХ-анализа разбавляли 2 М уксусной кислотой непосредственно перед анализом (см. табл. 10).
Таким образом, полный выход составил 75%.
Чистота продукта, определенная с помощью ОФ-ВРЖХ-анализа, составляла 84%, а остальные примеси являлись инсулиноподобными.
Пример 136
В данном примере, кроме того, проиллюстрирован способ скрининга, посредством которого могут быть идентифицированы белок-связывающие свойства конъюгатов аффинный лиганд - матрица настоящего изобретения.
Библиотеку конъюгатов аффинный лиганд - матрица настоящего изобретения синтезировали, как описано в примере 74, за исключением того, что 5 молярных эквивалентов аминового соединения, представленного в колонке II таблицы 4, заменяли на соответствующее количество аминового соединения, представленного в колонке II таблицы 5, а 5 молярных эквивалентов аминового соединения, представленного в колонке III таблицы 4, заменяли на соответствующее количество аминового соединения, представленного в колонке III таблицы 5. Была синтезирована библиотека конъюгатов аффинный лиганд - матрица настоящего изобретения. Примеры которой указаны в колонке I таблицы 5.
Хроматографические колонки с полным объемом 1 мл упаковывали конъюгатами аффинный лиганд - матрица примеров 137-180. Колонки уравновешивали путем интенсивной промывки 10 мл 0,2 М ацетата натрия, 0,1 М натрийхлоридным буфером, pH 5,0. 12 мл осветленной культуральной жидкости, содержащей 50 мг/мл предшественника человеческого инсулина, наносили на каждую хроматографическую колонку, которую затем промывали 12 мл 0,2 М ацетата натрия, 0,1 М натрийхлоридным буфером, pH 5,0 для удаления несвязанного вещества. Связанный предшественник человеческого инсулина элюировали путем интенсивной промывки каждой колонки 3 мл 2 М уксусной кислоты. Содержание предшественника человеческого инсулина в сквозном потоке, в промывке и во фракциях элюции определяли посредством высокоразрешающей жидкостной хроматографии (ВРЖХ) с использованием обращенно-фазовой колонки с двуокисью кремния С18 (4 х 250 м) и системы растворителей, содержащей буфер А (0,2 М сульфат натрия, 40 мМ фосфорная кислота и 10% (об./об.) ацетонитрил, pH 2) и буфер В (50% (об./об.) ацетонитрил) и подаваемой со скоростью потока 1 мл в минуту, и в соотношении 55% буфера А к 45% буферу В. Время элюции предшественника человеческого инсулина определяли путем сравнения со стандартными значениями.
Анализ результатов показал, что все конъюгаты аффинный лиганд - матрица примеров 139, 140, 145, 148, 153, 159, 162, 163, 164, 166, 167, 170, 171, 173 связывались с предшественником человеческого инсулина, который был проэлюирован в условиях, описанных в этом примере. Исходя из этого следует отметить, что конъюгаты аффинный лиганд - матрица примеров 139, 140, 145, 148, 153, 159, 162, 163, 164, 166, 167, 170, 171, 173 обладают исключительной эффективностью при разделении, выделении и очистке предшественника человеческого инсулина (см. табл. 11).
Пример 181
В данном примере продемонстрирован способ синтеза конъюгатов аффинный лиганд - матрица настоящего изобретения, которые являются эффективными для очистки фактора VII.
Конъюгат аффинный лиганд - матрица настоящего изобретения синтезировали, как описано в примере 74, за исключением того, что 5 молярных эквивалентов аминового соединения, представленного в колонке II таблицы 4, заменяли соответствующим количеством 2- аминобензимидазола, а 5 молярных эквивалентов аминового соединения, представленного в колонке III таблицы 4, заменяли на 3-амино-2-нафтойную кислоту. Этот конъюгат аффинный лиганд - матрица может быть использован для очистки фактора VIla примера 129 настоящего изобретения.
Пример 182
Очистка В-цепи1-29 ЕЕАЕРК-инсулина-А-цепи1-21 А-А-К-инсулина на конъюгате аффинный лиганд - матрица примера 171
50 мл ионообменного очищенного предшественника инсулина (В- цепь1-29-ЕЕАЕРК-инсулина-А-цепь1-21 А-А-К-инсулина при 2,2 мг/мл) наносили на колонку Pharmacia К16 (1,6 х 6 см), упакованную 12 мл конъюгата матрицы и уравновешенную в 0,2 М цитрате калия, pH 5,5, при 1,8 мл/мин при комнатной температуре. Эту колонку промывали в 50 мл 0,1 М цитрата калия, 0,2 М сульфата калия, pH 5,5, а затем элюировали 0,1 М уксусной кислотой при 1,8 мл/мин. Были собраны 5,0 мл-фракции.
Колонку очищали 50 мл 0,5 М NaOH и регенерировали 50 мл 0,1 М лимонной кислоты, 60% (об./об.) этанолом.
Образцы для ОФ-ВРЖХ-анализа разбавляли 2 М уксусной кислотой непосредственно перед анализом (см. табл. 12).
Была продемонстрирована динамическая емкость связывания 9,5 мг/мл матрицы с выходом предшественника 88%.
| название | год | авторы | номер документа |
|---|---|---|---|
| АФФИННЫЕ ЛИГАНДЫ, СВЯЗЫВАЮЩИЕ АНТИТЕЛА | 2005 |
|
RU2440582C2 |
| ГЛИЦЕРИН-СВЯЗАННЫЕ ПЭГИЛИРОВАННЫЕ САХАРА И ГЛИКОПЕПТИДЫ | 2007 |
|
RU2460543C2 |
| РЕГЕНЕРАЦИЯ ХРОМАТОГРАФИЧЕСКОЙ СТАЦИОНАРНОЙ ФАЗЫ | 2004 |
|
RU2350945C2 |
| ПРОИЗВОДНОЕ ИНСУЛИНА, РАСТВОРИМАЯ ПРОЛОНГИРОВАННАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ПРОЛОНГИРОВАНИЯ ГИПОГЛИКЕМИЧЕСКОГО ДЕЙСТВИЯ ПРИ ЛЕЧЕНИИ ДИАБЕТА | 1994 |
|
RU2164520C2 |
| ЛИПОФИЛЬНЫЕ ПРОИЗВОДНЫЕ ПЕПТИДНЫХ ГОРМОНОВ | 1996 |
|
RU2171261C2 |
| СПОСОБ ПОЛУЧЕНИЯ ИНСУЛИНОВЫХ СОЕДИНЕНИЙ | 2002 |
|
RU2376379C2 |
| ОЧИСТКА ИНСУЛИНА | 2012 |
|
RU2603752C2 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕТЕРОЛОГИЧНОГО ПОЛИПЕПТИДА В ДРОЖЖАХ Saccharomyces cerevisiae | 1990 |
|
RU2194758C2 |
| ПРОИЗВОДНЫЕ КОНДЕНСИРОВАННОГО 1,2,4-ТИАДИАЗИНА И КОНДЕНСИРОВАННОГО 1,4-ТИАЗИНА, ИХ ПОЛУЧЕНИЕ И ИСПОЛЬЗОВАНИЕ | 1997 |
|
RU2199542C2 |
| ПРОИЗВОДНЫЕ ПИРИДО-1,2,4-ТИАДИАЗИНА ИЛИ ПИРИДО-1,4-ТИАЗИНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБ ПРОЯВЛЕНИЯ ИНГИБИРУЮЩЕЙ ВЫДЕЛЕНИЕ ИНСУЛИНА АКТИВНОСТИ | 1997 |
|
RU2193564C2 |
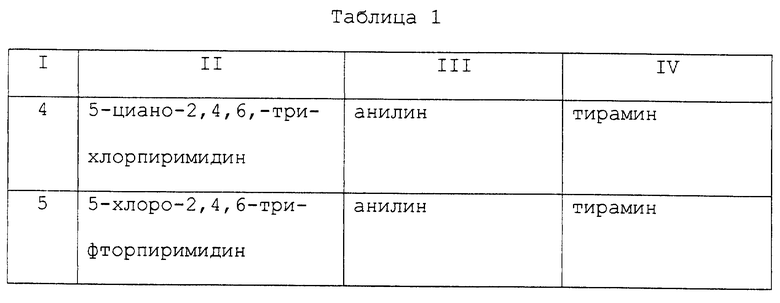
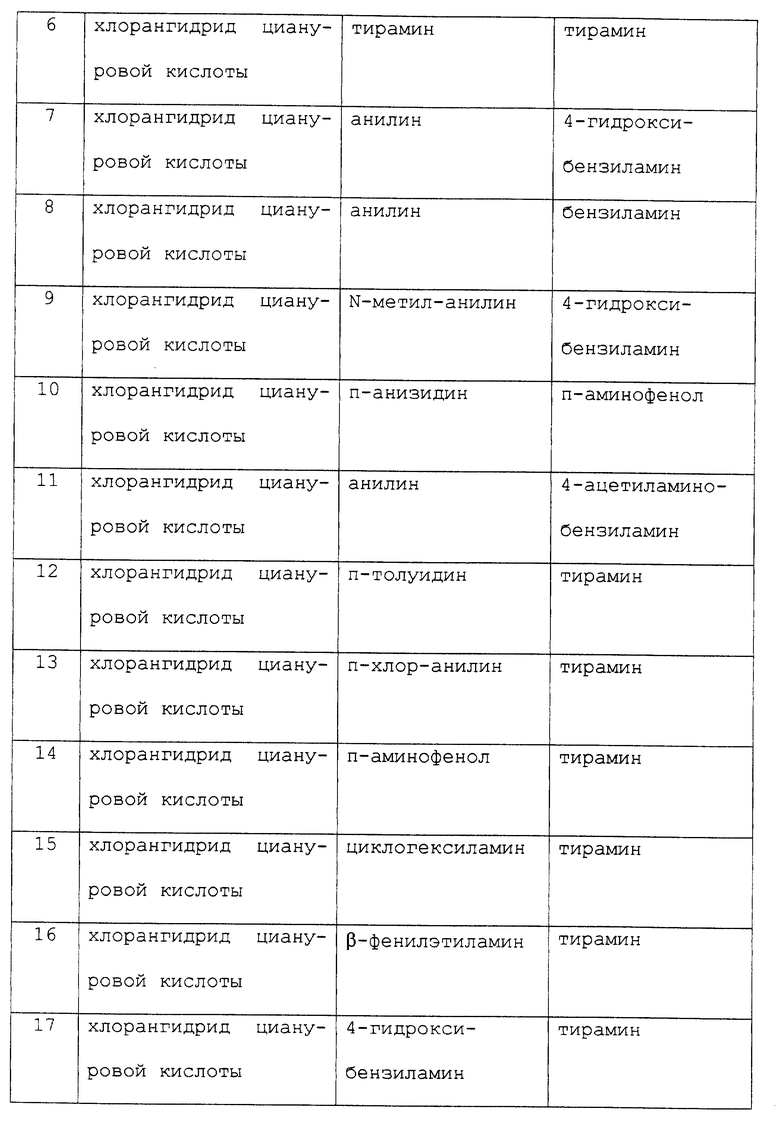

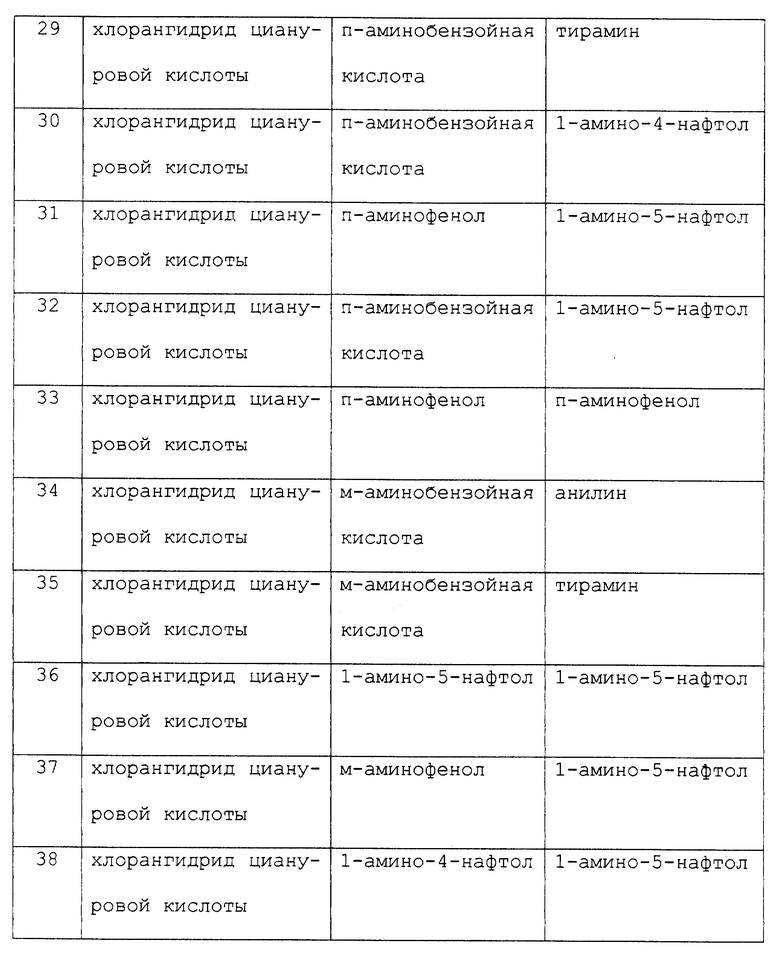
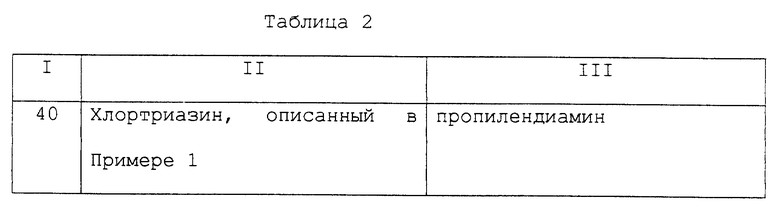



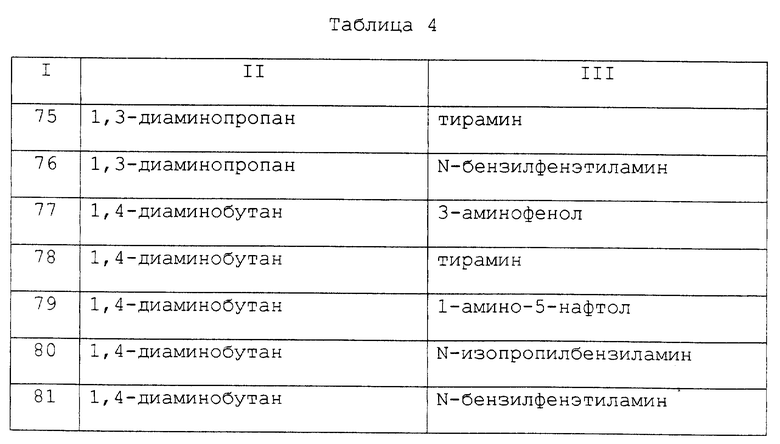


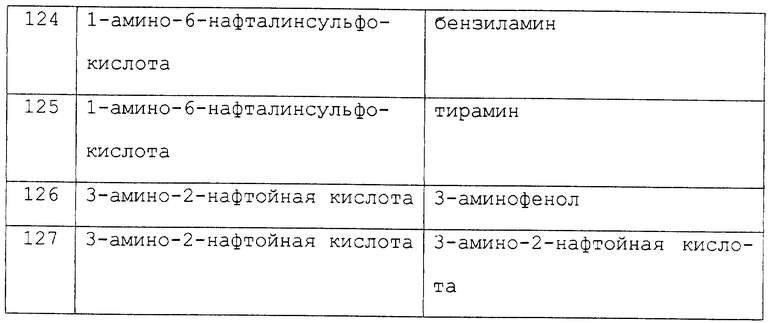
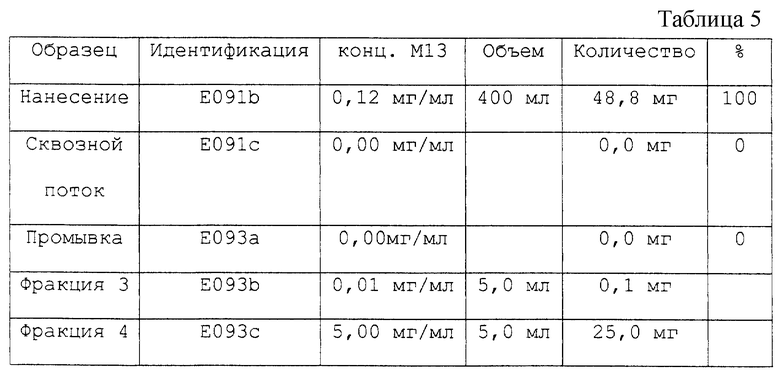

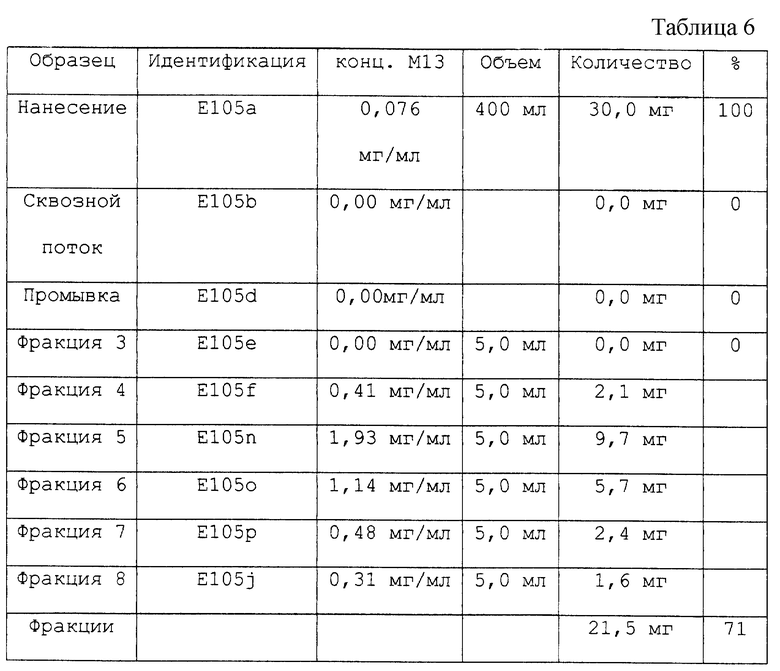


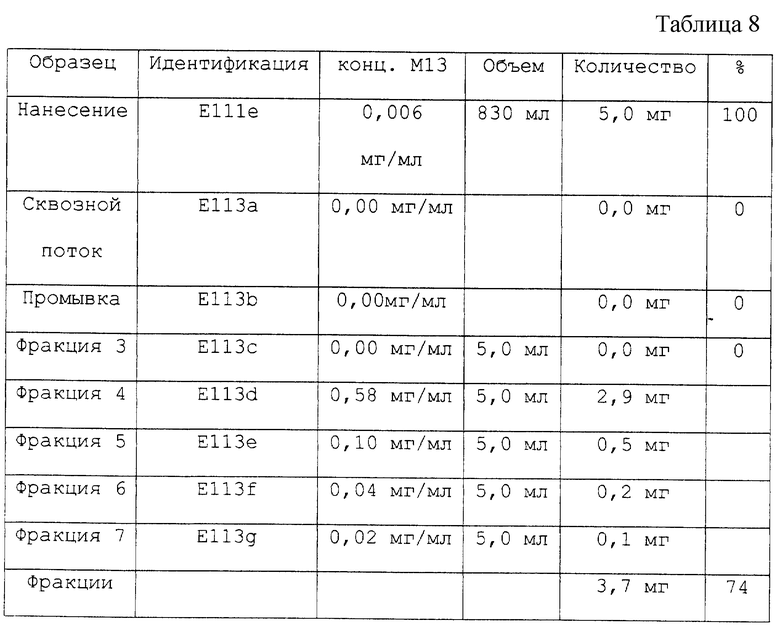
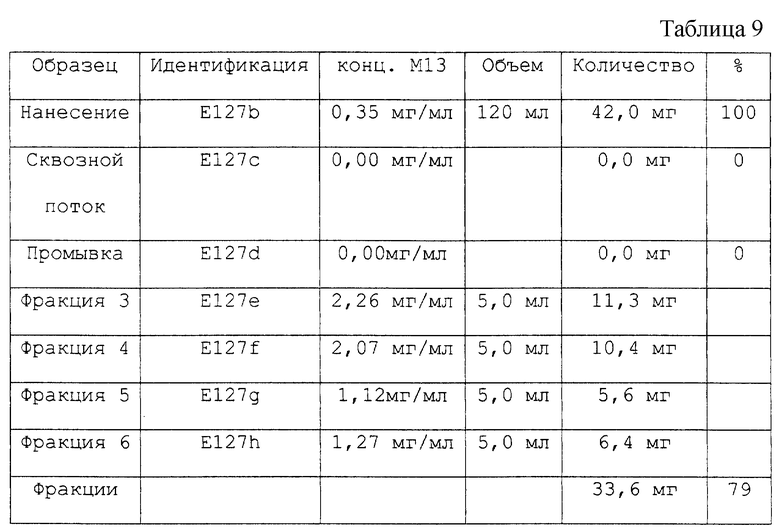
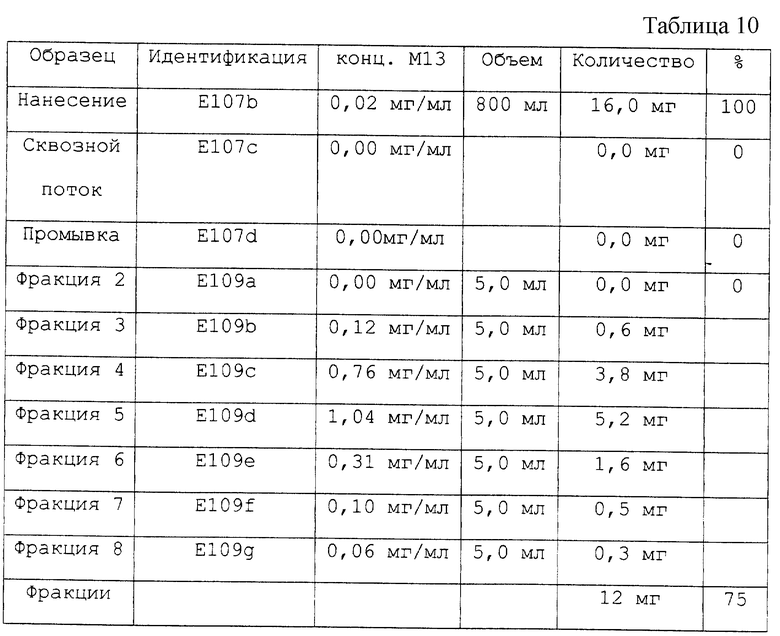
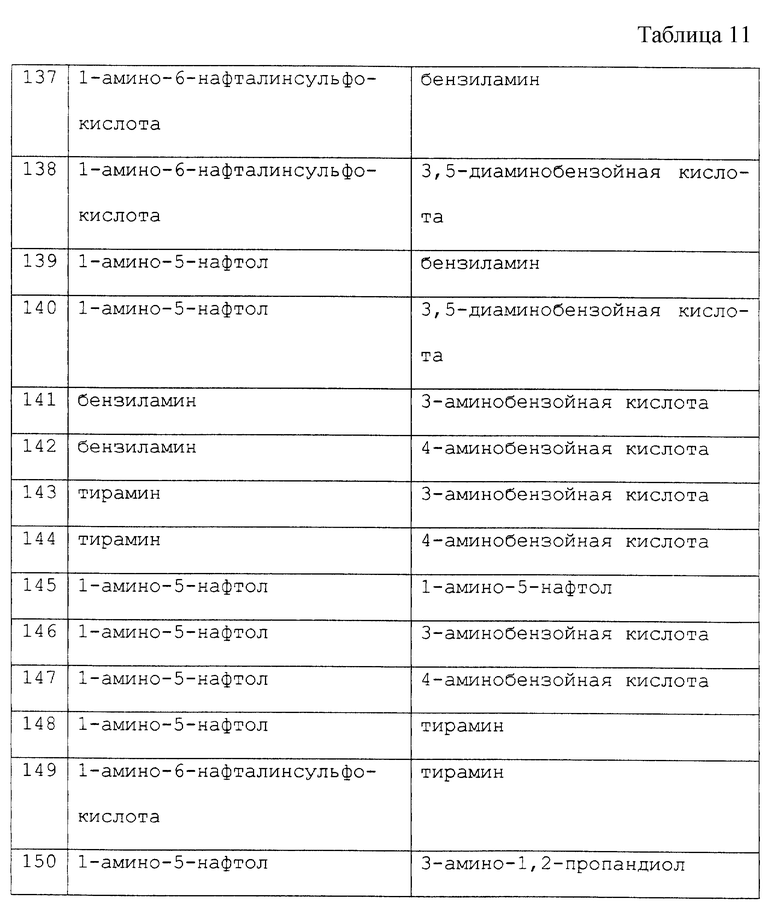


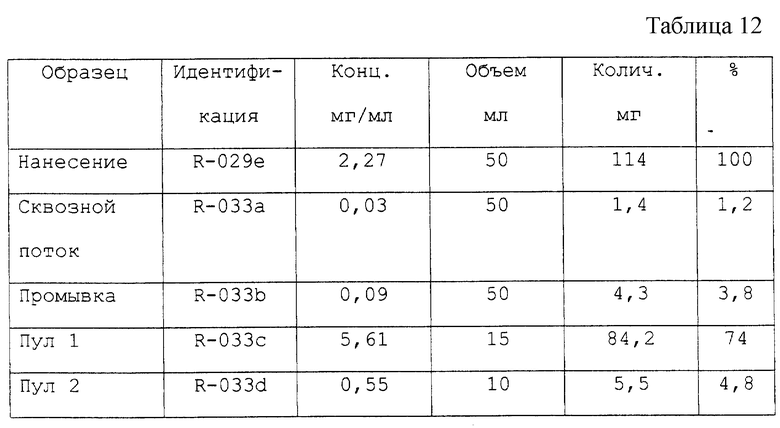
Изобретение относится к новым конъюгатам аффинный лиганд - матрица, содержащим лиганд, связанный с матрицей-носителем, необязательно посредством спейсерной группы, расположенной между матрицей и лигандом, и к новым конъюгатам аффинный лиганд - матрица, к их получению и использованию для очистки белковых материалов, таких как, например, иммуноглобулины, инсулины, фактор VII, или человеческий фактор роста, или его аналоги, производные и фрагменты, и их предшественники. Изобретение позволяет обеспечить получение недорогих и стабильных аффинных колонок. 26 с. и 57 з.п.ф-лы, 12 табл.
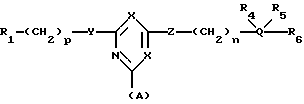
где R1 представляет атом водорода, алкильную группу, содержащую 1-6 атомов углерода, гидроксиалкильную группу, содержащую 1-6 атомов углерода, циклогексильную группу, аминогруппу, фенильную группу, нафтильную группу, 1-фенилпиразольную группу, индазольную группу, бензтиазольную группу, бензоксазольную группу или бензимидазольную группу, где каждое из бензольного, нафталинового, 1-фенилпиразольного, индазольного, бензтиазольного, бензоксазольного или бензимидазольного колец необязательно замещено одним или несколькими заместителями, независимо выбранными из группы, включающей алкильные группы, содержащие 1-6 атомов углерода; алкоксигруппы, содержащие 1-6 атомов углерода; ацилокси- или ациламиногруппы, содержащие 1-6 атомов углерода; аминогруппы, гидроксильные группы; карбоксильные группы; сульфокислотные группы; карбамоильные группы; сульфамоильные группы; алкилсульфонильные группы, содержащие 1-6 атомов углерода; или атомы галогена;
Y - атом кислорода, атом серы или группа N-R2;
Z - атом кислорода, атом серы или группа N-R3;
R2 и R3 каждый независимо представляет атом водорода; алкильную группу, содержащую 1-6 атомов углерода; гидроксиалкильную группу, содержащую 1-6 атомов углерода; бензильную группу или 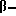 фенилэтильную группу;
фенилэтильную группу;
R4, R5 и R6 каждый независимо представляет атом водорода; гидроксильную группу; алкильную группу, содержащую 1-6 атомов углерода; алкоксигруппу, содержащую 1-6 атомов углерода, аминогруппу; ацилокси- или ациламиногруппу, содержащую 1-6 атомов углерода; карбоксильную группу, сульфоксильную группу, карбамоильную или сульфамоильную группу; алкилсульфонильную группу, содержащую 1-6 атомов углерода; или атом галогена;
один из Х - атом азота, а другой Х - атом азота или атом углерода, несущие атом хлора или цианогруппу;
Q представляет бензольное, нафталиновое, 1-фенилпиразольное, индазольное, бензтиазольное, бензоксазольное или бензимидазольное кольцо;
n = 0 - 6, целое число;
p = 0 - 20, целое число,
и где лиганд связан с матрицей-носителем в положении А необязательно посредством спейсерной группы, расположенной между матрицей и лигандом, при условии, что формула (а) не включает продукты реакции соединений 4-хлор-2,6-ди(фениламино)-1,3,5-триазин-3'-сульфокислоты, 4-хлор-2,6-ди(фениламино)-1,3,5-триазин-3', 2"-дисульфокислоты, и 4-хлор-2-(4"-аминофениламино)-1,3,5-триазин-3',2"-дисульфокислоты с Декстраном Т 500.
-T-[-L-V-]m-,
где Т - атом кислорода, атом серы или группа N-R7, где R7 - атом водорода или алкильная группа, содержащая 1-6 атомов углерода;
V представляет атом кислорода, атом серы, группу -СОО-, группу CONH, или группу NHCO, или группу -РO3Н-, группу NH-арилен-SO2-СН2-СН2, или группу N-R8, где R8 - атом водорода или алкильная группа, содержащая 1-6 атомов углерода;
L представляет необязательно замещенную углеводородную связь, содержащую 2-20 атомов углерода;
m = 0 или 1.
где R1, Y, Z, R2, R3 R4, R5, R6, X, Q, n и p определены выше;
T - атом кислорода, атом серы или группа N-R7;
V - атом кислорода, атом серы, группа -СОО-, группу CONH, или группа NHCO или группа -РO3Н-, группа NН-арилен-SO2-СН2-СН2, или группа N-R8;
R7 и R8 каждый независимо - атом водорода или алкильная группа, содержащая 1-6 атомов углерода;
L представляет необязательно замещенную углеводородную связь, содержащую 2 - 20 атомов углерода;
m = 0 или 1;
М - остаток матрицы-носителя.
i)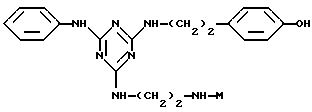
ii)
iii)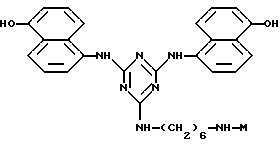
iv)
v)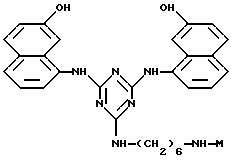
vi)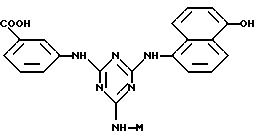
vii)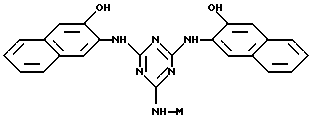
viii)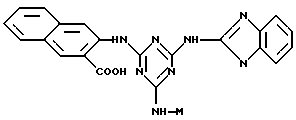
где М определен выше.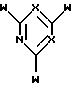
где X имеют значения, указанные выше;
W - атом галогена,
(i) с соединением общей формулы (III)
R1-(CH2)p-Y-H
где символы R1, p и Y определены выше
(ii) с соединением общей формулы (IV)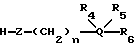
где R4, R5, R6, Q, Z и n определены выше и
(iii) либо с необязательно дериватезированной матрицей-носителем общей формулы (V)
H-T-[-L-V-]m-M,
где L, М, V, Т и m определены выше.
H-T-L-V-H,
где L, V и Т определены выше,
с получением соединения общей формулы (VII)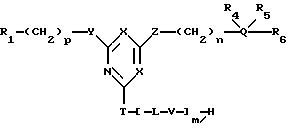
где R1, R4, R5, R6, Т, Q, L, V, X, Y, Z, m, n и р определены выше,
и последующей реакцией соединения общей формулы с (VII) матрицей-носителем.
где R1, R4, R5, R6 Q, X, Y, Z, n и p указаны выше;
галоген представляет атом фтора, хлора, брома или иода, при условии, что формула (XII) не включает такие соединения, как 4-хлор-2,6-ди(фениламино)-1,3,5-триазин-3'-сульфокислота, 4-хлор-2,6-ди(фениламино)-1,3,5-триазин-3', 2''-дисульфокислота и 4-хлор-2-(4"-аминофениламино)-1,3,5-триазин-3', 2"-дисульфокислота.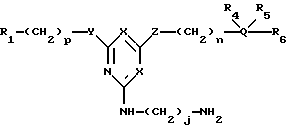
где R1, R4, R5, R6, Q, X, Y, Z, m, n и p указаны выше,
j = 2 - 20, целое число.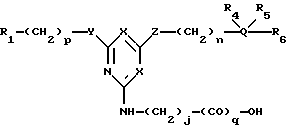
где R1, R4, R5, Q, X, Y, Z, m, n и p указаны выше;
q = 0 или 1;
j = 2 - 20, целое число.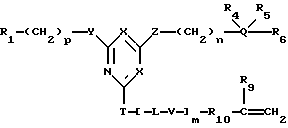
где R1, R4, R5, R6, L, Q, T, V, X, Y, Z, m, n и p определены выше;
R9 представляет атом водорода или алкильную группу, содержащую 1-6 атомов углерода;
R10 карбонильную группу, метиленовую группу, группу -NH-CH2- или группу -S-CH2-.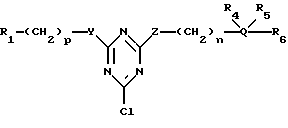
где R1, R4, R5, R6, Q, n и p определены выше,
при условии, что формула (XV) не включает соединения 4-хлор-2,6-ди(фенил-амино)-1,3,5-триазин-3'-сульфокислоты, 4-хлор-2,6-ди(фенил-амино)-1,3,5-триазин-3', 2"-дисульфокислоты, и 4-хлор-2-(4"-аминофениламино)-1,3,5-триазин-3',2"-дисульфокислоты.
где R1, R4, R5, R6, Q, n и p указаны выше;
j = 2 - 20, целое число.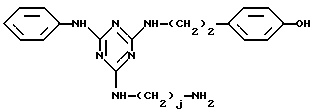
где j = 2 - 20, целое число.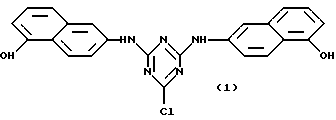
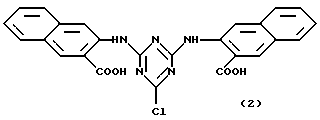
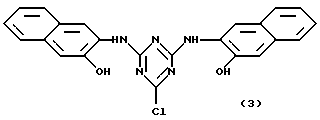
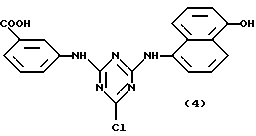
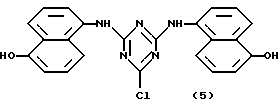
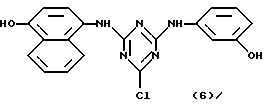
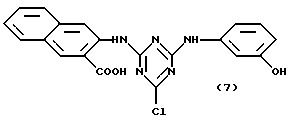

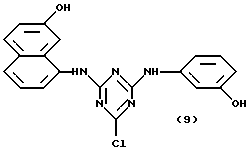
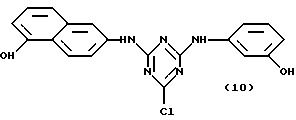
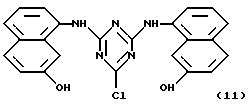
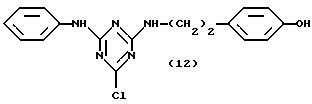
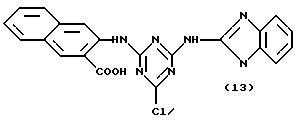
54. Аффинные лиганды по любому из пп.28, 30, 32, 34-53, применимые для получения конъюгатов аффинный лиганд - матрица.
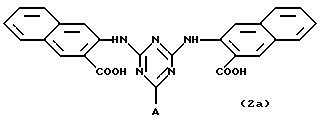
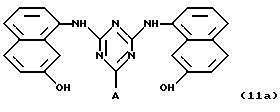
где лиганд присоединен к матрице-носителю в положении (А) необязательно посредством спейсерной группы, представленной общей формулой (b), определенной выше.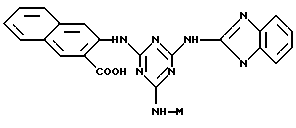
где М - остаток агарозы,
при котором FVIIa наносят на указанный конъюгат аффинный лиганд - матрица в присутствии 5мМ Са2+, а затем элюируют.
| BURTON N.P | |||
| LOWE C.P | |||
| JORNAL OF MOLECULAR RECOGNITION | |||
| Пуговица для прикрепления ее к материи без пришивки | 1921 |
|
SU1992A1 |
| DE 4445517 A (PALL CORP), 29.06.1995. | |||
Авторы
Даты
2001-10-27—Публикация
1996-09-19—Подача