Область, к которой относится изобретение
Изобретение относится к композициям для ухода за кожей, содержащим амид жирной кислоты и ретинол или ретиниловый сложный эфир, а также к косметическим способам, предусматривающим нанесение таких композиций на кожу.
Предпосылки создания изобретения
Ретинол (витамин А) представляет собой эндогенное соединение, которое в естественных условиях присутствует в организме человека, и имеет важное значение для нормальной дифференцировки эпителиальных клеток. Природные и синтетические производные витамина А широко применяются для лечения ряда кожных заболеваний, а также используются в качестве средств для восстановления биологических функций кожи или для обновления клеток кожи. Ретиноевая кислота используется для лечения ряда состояний кожи, например акне (угри), морщины, псориаз, старческие пятна и депигментация (обесцвечивание). См. , например, Vahlquist, A. et al. , J. Invest. Dermatol. , Vol. 94, Holland D. B. & Cunliffe, W. J. (1990), pp. 496-498; Ellis, C. N. et al. , "Pharmacology of Retinols in Skin", Vasel, Karger, Vol. 3 (1989), pp. 249-252; Lowe, N. J. et al. , "Pharmacology of Retinols in Skin", Vol. 3 (1989), pp. 240-248; Публикация РСТ заявки WO 93/19743.
Очевидно, что использование ретинола или сложных эфиров ретинола предпочтительней, чем использование ретиноевой кислоты. Ретинол присутствует в организме человека в естественных условиях и считается более безопасным, чем ретиноевая кислота. Сложные эфиры ретинола гидролизуются in vivo с продуцированием ретинола. Очевидно, что в коже ретиноловые сложные эфиры и ретинол метаболически превращаются в ретиноевую кислоту в соответствии со следующим механизмом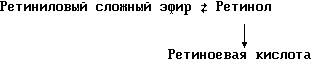
Однако большая часть эндогенно введенного ретинола быстро превращается в неактивные сложные эфиры жирной кислоты, которые сохраняются в эпидермальных клетках (кератиноцитах). Такая этерификация ретинола с образованием неактивных ретиниловых сложных эфиров в клетках достигается путем переноса жирной ацильной группы из ацил-СоА, катализируемого ферментом ацил-СоА-ретинолтрансферазой (ARAT), либо путем переноса ацильной группы из фосфатидилхолина, катализируемого ферментом лецитин-ретинол-ацилтрансферазой (LRAT). Эти реакции этерификации являются очень эффективными в кератиноцитах; а поэтому большинство (95%) из клеточных ретиноидов присутствуют в форме ретиниловых сложных эфиров жирной кислоты. Но, к сожалению, хотя ретинол и ретиниловые сложные эфиры являются более безопасными для использования, чем ретиноевая кислота, однако, их благоприятное действие на кожу является менее эффективным, чем действие ретиноевой кислоты.
Настоящее изобретение, отчасти, основано на обнаружении того факта, что некоторые N-замещенные амиды жирных кислот ингибируют эти реакции этерификации, и, таким образом, потенцируют действие ретинола путем увеличения количества присутствующего ретинола, превращающегося в ретиноевую кислоту. Таким образом, смесь N-замещенных амидов жирных кислот с ретинолом или ретиниловыми сложными эфирами имитирует действие ретиноевой кислоты, но, при этом, эта смесь является более безопасной для использования, чем ретиноевая кислота. В ранее поданной заявке на Европейский патент ЕР 0742005 (Unilever; дата приоритета 8 мая 1995), опубликованной 13 ноября 1996 (по дате приоритета настоящей заявки), описаны комбинации амидов жирных кислот с ретинолом или с ретиниловыми сложными эфирами. Однако в ЕР 0742005 не упоминаются ни конкретные N-замещенные амиды жирных кислот настоящего изобретения, ни какой-либо амид жирной кислоты с разветвленной алкоксисодержащей замещающей группой у атома азота.
Краткое описание изобретения
Настоящее изобретение относится, отчасти, к композиции для ухода за кожей, содержащей:
(а) от 0,001 до 10% ретинола или ретинилового сложного эфира;
(b) от 0,0001 до 50% N-замещенного амида жирной кислоты формулы I;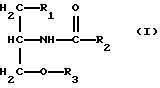
где R1 = алкил или алкокси, имеющий от 1 до 10 атомов углерода;
R2 = алкил или алкенил, имеющий от 8 до 25 атомов углерода;
R3 = алкил, содержащий 1-5 атомов углерода, или сложный эфир фосфорной кислоты; и
(с) косметически приемлемый носитель.
Настоящее изобретение также относится к косметическому способу ухода за кожей, предусматривающему местное нанесение данной композиции на кожу. Кроме того, настоящее изобретение относится к косметическому способу имитации действия ретиноевой кислоты на кожу, предусматривающему местное нанесение данной композиции на кожу.
Термин "уход за кожей (кондиционирование)", используемый в настоящем описании, означает предупреждение и/или лечение сухости кожи, повреждения кожи под действием солнечного излучения, возникновения морщин, старческих пятен и/или увядания кожи; повышение эластичности рогового слоя; отбеливание кожи; регуляцию экскреции кожного сала; а в основном, повышение качества кожи.
Был обнаружен тот факт, который лег в основу части настоящего изобретения, что N-замещенные амиды жирных кислот формулы I, взятые в концентрации 100 мкм, предпочтительно ингибируют, по крайней мере, на 20%, LRAT или ARAT-катализируемую реакцию этерификации ретинола, как было определено в микросомном in vitro-анализе (описанном ниже). Таким образом, присутствие N-замещенного амида жирных кислот формулы I в композициях настоящего изобретения способствует значительному увеличению эффективности ретинола и ретинилового сложного эфира в косметических композициях.
Описание предпочтительного варианта осуществления изобретения
Если это не оговорено особо, то все указанные количества ингредиентов даны по массе конечной композиции.
Композиции настоящего изобретения содержат в качестве первого главного ингредиента соединение, выбранное из группы, состоящей из ретинола и ретинилового сложного эфира. Термин "ретинол" включает, среди прочих, следующие изомеры ретинола: полностью-транс-ретинол, 13-цис-ретинол, 11-цис-ретинол, 9-цис-ретинол, 3,4-дидегидро-ретинол. Из них предпочтительными изомерами являются полностью-транс-ретинол, 13-цис-ретинол, 3,4-дидегидро-ретинол, 9-цис-ретинол. Наиболее предпочтительным является полностью-транс-ретинол, благодаря его широкой коммерческой доступности.
Ретиниловый сложный эфир представляет собой сложный эфир ретинола. Термин "ретинол" был определен выше. Ретиниловыми сложными эфирами, подходящими для использования в настоящем изобретении, являются сложные С1-С30-эфиры ретинола, предпочтительно С2-С20-сложные эфиры, а наиболее предпочтительно C2, С3 и С16-сложные эфиры, поскольку они являются наиболее коммерчески доступными. Примерами ретиниловых сложных эфиров являются, но не ограничиваются ими, ретинилпальмитат, ретинилформиат, ретинилацетат, ретинилпропионат, ретинилбутират, ретинилвалерат, ретинилизовалерат, ретинилгексаноат, ретинилгептаноат, ретинилоктаноат, ретинилнонаноат, ретинилдеканоат, ретинилундекандат, ретиниллаурат, ретинилтридеканоат, ретинилмиристат, ретинилпентадеканоат, ретинилгептадеканоат, ретинилстеарат, ретинилизостеарат, ретинилнонадеканоат, ретиниларахидонат, ретинилбегенат, ретиниллинолеат, ретинилолеат.
Предпочтительный сложный эфир для использования в настоящем изобретении выбирают из ретинилпальмитата, ретинилацетата и ретинилпропионата, поскольку эти сложные эфиры являются наиболее коммерчески доступными и, следовательно, наиболее дешевыми. Ретиниллинолеат также является предпочтительным благодаря своей эффективности.
Ретинол и/или ретиниловый сложный эфир используются в композиции настоящего изобретения в количестве от 0,001 до 10%, предпочтительно, в количестве от 0,01 до 1%, а более предпочтительно в количестве от 0,01 до 0,5%.
Вторым главным ингредиентом композиций настоящего изобретения является N-замещенный амид жирной кислоты формулы I: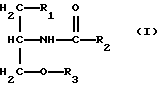
где R1 = алкил или алкокси, имеющий от 1 до 10 атомов углерода;
R2 = алкил или алкенил, имеющий от 8 до 25 атомов углерода;
R3 = алкил, содержащий 1-5 атомов углерода, или сложный эфир фосфорной кислоты.
R1, предпочтительно, представляет собой линейную насыщенную алкильную или алкоксигруппу, содержащую 1-5 атомов углерода, а наиболее предпочтительно 1 или 4 атомов углерода.
R2, предпочтительно, представляет собой линейную ненасыщенную алкенильную группу, содержащую от 10 до 20 атомов углерода, а наиболее предпочтительно, от 10 до 18 атомов углерода.
Оптимально, R2 представляет собой остаток линолевой кислоты (C18:2).
R3, предпочтительно, представляет собой либо метильную группу, либо сложный эфир фосфорной кислоты, а наиболее предпочтительно, сложный эфир фосфорной кислоты и холина или гликоля.
Наиболее предпочтительно, если N-замещенный амид жирной кислоты выбирают из соединений, имеющих нижеуказанные формулы А и В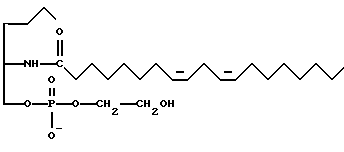
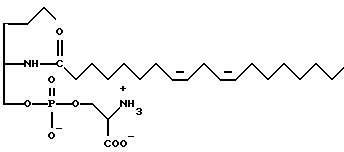
N-замещенный амид жирной кислоты содержится в композициях настоящего изобретения в количестве, составляющем от 0,0001 до 50%, предпочтительно от 0,01 до 10%, а наиболее предпочтительно от 0,1 до 5%.
N-замещенный амид жирной кислоты формулы I в концентрации 100 мкм предпочтительно ингибирует по крайней мере на 20% LRAT или ARAT-катализируемую реакцию этерификации ретинола, как было определено в микросомном in vitro-анализе.
Микросомный in vitro-анализ
Микросомы были получены, как описано J. C. Saari and D. L. Bredberg, в "СоА and Non-CoA Dependent Retinol Esterification in Retinal Pigment Epithelium" J. Biol. Chem. 263, 8084-90 (1988).
Раствор, содержащий 0,1 М фосфатно-натриевого буфера, рН 7,5 мМ дитиотреитола, 2 мг/мл альбумина бычьей сыворотки, 40 микромолей пальмитоил-СоА, 40 микромолей дилауроилфосфатидилхолина, 10 микромолей ретинола, и тестируемое соединение или растворитель (контроль) инкубировали в течение 1 часа при 37oС с микросомной фракцией, выделенной из бычьих эпителиальных клеток, содержащих ретинальный пигмент. После инкубирования реакцию гасили путем добавления равного объема этанола, и образовавшиеся ретиниловые сложные эфиры (ретиниллаурат из LRAT-катализируемой реакции, и ретинилпальмитат из ARAT-катализируемой реакции) экстрагировали гексаном. Для количественной оценки ретинилового сложного эфира, гексановый слой удаляли, упаривали в атмосфере азота, и остаток анализировали ро-средством ВЭЖХ на обращенно-фазовой колонке (3,9•300 мм) с C18 с использованием 80% метанола в тетрагидрофуране в качестве подвижной фазы, и посредством флуоресцентной детекции (возбуждение на 325 нм, излучение на 480 нм). Количество образовавшегося сложного эфира в присутствии растворителя (контроля) принимали за 100% и использовали для вычисления процента ингибирования образования сложного эфира в случае тестируемых соединений. В случае контроля, аликвоту микросом инактивировали путем кипячения в течение 5 минут, что приводило по крайней мере к 95%-ному ингибированию образования сложного эфира.
В предпочтительном варианте осуществления настоящего изобретения выбранный N-замещенный амид жирной кислоты, в концентрации 100 мкм, ингибирует по крайней мере на 40% LRAT- или ARAT-катализируемую реакцию этерификации ретинола.
Косметически приемлемый носитель
Композиция настоящего изобретения также включает косметически приемлемый носитель, который действует как разбавитель, диспергирующий агент или носитель для ретинола и/или ретинилового сложного эфира и N-замещенного амида жирной кислоты таким образом, что он облегчает их распределение при нанесении композиции на кожу.
Безводными носителями, или носителями, используемыми в добавлении к воде, могут быть жидкие или твердые смягчающие вещества, растворители, влагоудерживающие агенты, загустители и порошки. Особенно предпочтительным безводным носителем является полидиметилсилоксан и/или полидиметилфенилсилоксан. Силиконами настоящего изобретения могут быть силиконы с вязкостями, составляющими примерно от 10 до 10.000.000 мм2/с (сантистокс) при 25oС. Особенно предпочтительными являются смеси силиконов низкой и высокой вязкости. Эти силиконы изготавливаются компанией Дженерал Электрик (General Electric Company) под товарными знаками Vicasil, SE и SF, и компанией Dow Corning под серийными марками 200 и 550. Количество силикона, которое может быть использовано в композициях настоящего изобретения, варьируется примерно от 5 до 95%, а предпочтительно от 25 до 90% по массе композиции.
Косметически приемлемый носитель обычно составляет от 5 до 99,9%, предпочтительно, от 25 до 80% по массе композиции, и может быть использован в отсутствие других косметических добавок, то есть, может составлять всю остальную часть композиции (помимо активных ингредиентов). Предпочтительно, чтобы носитель содержал по крайней мере 50%, а более предпочтительно по крайней мере 80% воды по массе носителя. При этом предпочтительно, чтобы вода составляла по крайней мере 50%, а наиболее предпочтительно по крайней мере от 60 до 80% по массе композиции настоящего изобретения.
Необязательные материалы для ухода за кожей и косметические добавки
Масло или маслообразный материал могут присутствовать в композиции вместе с эмульгатором для образования эмульсии типа "вода в масле" или "масло в воде", главным образом, в зависимости от гидрофильно-липофильного баланса (ГЛБ) используемого эмульгатора.
Композиции настоящего изобретения содержат предпочтительно солнцезащитные вещества. Солнцезащитные вещества включают соединения, которые обычно используются для защиты от воздействия ультрафиолетового излучения. Характерными соединениями являются производные РАВА, циннамат и салицилат. Так, например, могут быть использованы октилметоксициннамат и 2-гидрокси-4-метоксибензофенон (известный так же, как оксибензон). Октилметоксициннамат и 2-гидрокси-4-метоксибензофенон являются коммерчески доступными соединениями, выпускаемыми под товарными знаками Parsol MCX и Бензофенон-3 соответственно. Точное количество солнцезащитного вещества, используемого в эмульсиях, может варьироваться в зависимости от степени нужной защиты от солнечного УФ-излучения.
Другие предпочтительные, но необязательные ингредиенты, выбирают из незаменимых жирных кислот (НЖК), то есть тех жирных кислот, которые имеют важное значение для образования плазматической мембраны всех клеток; так, например, в кератиноцитах недостаток НЖК приводит к гиперпролиферации этих клеток. Добавление в эти клетки НЖК позволяет корректировать это явление. Кроме того, НЖК усиливают липидный биосинтез эпидермиса и обеспечивают наличие липидов для формирования структур, выполняющих барьерную роль эпидермиса. Незаменимые жирные кислоты выбирают, предпочтительно, из линолевой кислоты, γ-линоленовой кислоты, гомо-γ-линоленовой кислоты, колумбиновой кислоты, эйкоза-(н-6,9,13)-триеновой кислоты, арахидоновой кислоты, тимнодоновой кислоты, гексаеновой кислоты и их смесей.
Другой предпочтительный, но необязательный ингредиент выбирают из азолов, например климбазола, бифоназола, клотримазола, кетоконазола, миконазола, эконазола, итраконазола, флуконазола, терконазола, бутоконазола, сульконазола, лионазола и их смесей. Азол может присутствовать в композициях настоящего изобретения в количестве от 0,001 до 50 мас. %, предпочтительно от 0,001 до 10 мас. %, а более предпочтительно от 0,1 до 5%.
В косметические композиции настоящего изобретения часто вводят смягчающие агенты. Уровни таких смягчающих агентов могут составлять от 0,5 до 50%, а предпочтительно от 5 до 30% по массе всей композиции. Смягчающие агенты могут быть классифицированы по таким общим химическим категориям, как сложные эфиры, жирные кислоты и спирты, полиолы и углеводороды.
Сложными эфирами могут быть сложные моно- или диэфиры. Подходящими примерами сложных диэфиров жирных кислот являются дибутиладипат, диэтилсебакат, диизопропилдимерат и диоктилсукцинат. Подходящими сложными эфирами жирных кислот с разветвленной цепью являются 2-этил-гексилмиристат, изопропилстеарат и изостеарилпальмитат. Подходящими сложными эфирами трехосновных кислот являются триизопропилтрилинолеат и трилаурилцитрат. Подходящими сложными эфирами жирных кислот с прямой цепью являются лаурилпальмитат, миристиллактат, олеилэуркат и стеарилолеат. Предпочтительными сложными эфирами являются кококаприлат/капрат (смесь кококаприлата и кококапрата), ацетат миристилового эфира пропиленгликоля, диизопропиладипат и цетилоктаноат.
Подходящими жирными спиртами и кислотами являются соединения, имеющие от 10 до 20 атомов углерода. Особенно предпочтительными являются такие соединения, как цетиловые, миристиловые, пальмитиловые и стеариловые спирты и кислоты.
Полиолами, которые могут служить в качестве смягчающих агентов, являются линейные и разветвленные алкилполигидроксильные соединения. Так, например, предпочтительными являются пропиленгликоль, сорбит и глицерин. Могут быть также использованы полимерные полиолы, такие как полипропиленгликоль и полиэтиленгликоль. Бутилен- и пропиленгликоль являются также особенно предпочтительными в качестве интенсификаторов впитываемости.
Примерами углеводородов, которые могут служить в качестве смягчающих агентов, являются углеводородные цепи, имеющие примерно от 12 до 30 атомов углерода. Конкретными примерами таких соединений являются минеральное масло, вазелин, сквален и изопарафины.
Другой категорией функциональных ингредиентов косметических композиций настоящего изобретения являются загустители. Загуститель обычно присутствует в количествах примерно 0,1-20%, а предпочтительно 0,5-10% по массе композиции. Примерами таких загустителей являются структурированные полиакрилатные материалы, поставляемые компанией B. F. Goodrich Company под товарным знаком Carbopol. Используемыми смолами могут быть такие смолы, как ксантановая камедь, каррагеновая камедь, желатин, камедь карайи, пектиновая смола и смола робинин. При определенных условиях функция загущения может быть осуществлена с использованием материала, который служит также в качестве силикона или смягчающего агента. Так, например, силиконовые смолы с вязкостью, превышающей 10 сантистоксов, и сложные эфиры, такие как стеарат глицерина, имеют двойную функцию.
В косметическую композицию настоящего изобретения могут быть введены порошки. Такими порошками являются мел, тальк, каолин, крахмал, смектитовые глины, химически модифицированный алюмосиликат магния, органически модифицированная монтмориллонитовая глина, гидратированный силикат алюминия, тонкодисперсный диоксид кремния, алюмооктенилсукцинат крахмала и их смеси.
В косметические композиции настоящего изобретения могут быть также включены и другие вспомогательные компоненты-добавки. Такими вспомогательными ингредиентами могут быть красители, замутнители и отдушки. Количества этих вспомогательных компонентов-добавок могут составлять примерно от 0,001 и вплоть до 20% по массе композиции.
Использование композиции
Композиция настоящего изобретения используется, главным образом, в качестве продукта для местного нанесения на кожу человека, а особенно, в качестве кондиционирующего и смягчающего кожу агента, а также для предупреждения образования или для сокращения количества морщин на коже, или улучшения внешнего вида увядшей кожи.
При использовании небольшого количества композиции, например от 1 до 100 мл, эту композицию наносят на обрабатываемые поверхности кожи из соответствующей емкости или аппликатора, а затем, если это необходимо, ее распределяют и/или втирают в кожу ладонью или пальцами, либо с использованием соответствующего приспособления.
Форма продукта и упаковка
Композиция настоящего изобретения, предназначенная для ухода за кожей путем местного применения, может быть изготовлена в виде лосьона, крема или геля. Эта композиция может быть упакована в подходящую емкость, которая соответствует вязкости этой композиции и пригодна для ее использования потребителем. Так, например, лосьон или крем могут быть упакованы во флаконы или в шариковый аппликатор, либо в распыляющее аэрозольное устройство или в баллон, снабженный дозатором насосного типа, пригодным для нажатия пальцем. Если данная композиция изготовлена в виде крема, то ее просто хранят в недеформируемом сосуде или в плотно закрытом сосуде, таком как тюбик или закрывающаяся крышкой косметическая баночка. Эта композиция может также заключаться в капсулы, такие как капсулы, описанные в патенте США 5063057.
Настоящее изобретение также относится к плотно закрывающейся емкости, содержащей косметически приемлемую композицию, описанную в настоящей заявке.
Настоящее изобретение более подробно проиллюстрировано в нижеследующих конкретных примерах.
Материалы и методы
Клеточная культура
Кератиноциты человека, выделенные из неонатальной крайней плоти путем обработки трипсином, культивировали на модифицированной по способу Дульбекко среде Игла (DME) и среде Хемса F12 (1: 1)/10% фетальной телячьей сыворотки в присутствии облученных фибробластов мыши 3Т3 для создания колоний делящихся кератиноцитов. Клетки культивировали в вышеуказанных условиях до их второго пассажа (включительно) и хранили в замороженном виде для дальнейшего использования. Замороженные кератиноциты второго пассажа оттаивали, засевали на вышеуказанную среду и культивировали в течение пяти дней, после чего их переносили на бессывороточную среду на основе MCDB 153 (KGM) для культивирования кератиноцитов, полученную от Clonetics Corporation, San Diego, CA, и содержащую 0,15 мМ Са, или бессывороточную среду (KSFM) для культивирования кератиноцитов, полученную от Gibco и содержащую 0,09 мМ Са. На 7-ой день, когда клетки достигали 80-90%-ной конфлюэнтности, их обрабатывали трипсином и засевали в бессывороточную среду для проведения различных экспериментов.
Анализ на трансглутаминазу
Анализ на трансглутаминазу и дифференцировку кератиноцитов
В процессе терминальной дифференцировки в эпидермисе, на внутренней поверхности периферического клеточного слоя образуется слой белка толщиной 15 нм, известный как ороговевший слой (СЕ). Этот ороговевший слой состоит из многочисленных различных белков, которые сшиты друг с другом посредством образования Nε-(γ-глутамил)лизиновых изодипептидных связей, катализируемого действием, по крайней мере, двух различных трансглутаминаз (Tgases), экспрессированных в эпидермисе. Трансглутаминаза I (TGasa I) экспрессируется в избытке в дифференцированных слоях эпидермиса, особенно в зернистом слое, но отсутствует в недифференцированном базальном эпидермисе. Таким образом, трансглутаминаза I может быть использована в качестве маркера эпидермальной дифференцировки кератиноцитов с высокими уровнями трансглутаминазы I, что указывает на их более дифференцированное состояние. Оценку состояния дифференцировки культивированных кератиноцитов проводили с помощью анализа ELISA на основе трансглутаминазы I с использованием антитела против трансглутаминазы I, как описано в нижеприведенных примерах.
Для примера 1 использовали следующую процедуру.
Кератиноциты (культивированные как описано выше) засевали в 96-луночные планшеты при плотности 3000 клеток на лунку в 200 мкл среды. После инкубирования в течение четырех дней, среду заменяли на среду, содержащую тестируемые соединения (6 дубликатов на тест). Клетки культивировали еще 72 часа, после чего среду отсасывали, и планшеты хранили при температуре -70oС. Затем планшеты удаляли из холодильника, и клетки промывали PBS. После добавления 100 мкл стерильной воды клетки разрушали путем замораживания при -70oС, а затем оттаивания. Клетки инкубировали в течение еще одного часа при комнатной температуре (К/Т) с PBS/3% BSA (буфер для промывки, альбумин бычьей сыворотки), а затем промывали свежей аликвотой буфера для промывки. Клетки инкубировали в течение 1 часа при 37oС с 50 мкл мышиного моноклонального первичного антитела (IgG) против трансглутаминазы человека, полученного от фирмы Biomedical Industries и разведенного 1: 2000 в буфере для промывки, а затем два раза промывали буфером для промывки. После этого клетки в течение 1 часа при 37oС инкубировали с 50 мкл вторичного антитела (Fab-фрагмента, конъюгированного с пероксидазой антитела против мышиных иммуноглобулинов IgG, полученного от Amersham), разведенного в отношении 1: 4000 в буфере для промывки, а затем два раза промывали буфером для промывки. Клетки инкубировали с раствором субстрата (4 мг о-фенилендиамина и 3,3 мкл 30% Н2О2 в 10 мл 0,1 М цитратного буфера, рН 5,0) в течение пяти минут, при комнатной температуре в темноте (под алюминиевой фольгой). Реакцию прекращали путем добавления 50 мкл 4 н. H2SО4. Оптическую плотность образцов считывали при 492 нм на планшет-ридере. Из шести дубликатов четыре дубликата обрабатывали обоими антителами, а два дубликата обрабатывали только вторичным антителом (то есть, для определения фонового связывания антитела, конъюгированного с ферментом). Уровни трансглутаминазы определяли путем вычитания фоновых значений из значений, полученных после каждой обработки, и определения средней квадратичной ошибки (±ср. кв. ош. ) для дубликатов, обработанных обоими антителами.
Для примера 2 использовали следующую процедуру.
Кератиноциты (культивированные как описано выше) засевали в 96-луночные планшеты при плотности 3000 клеток на лунку в 200 мкл среды для культивирования клеток. После инкубирования в течение четырех дней среду заменяли на среду, содержащую тестируемые соединения (6 дубликатов на тест). Клетки культивировали еще 12 часов, после чего среду отсасывали, и планшеты хранили при температуре -70oС. После удаления планшетов из холодильника клетки разрушали путем замораживания при -70oС и оттаивания, а затем три раза промывали PBS. Клетки инкубировали в течение еще одного часа при комнатной температуре (К/Т) с TBS/5% BSA буфером. Затем клетки инкубировали в течение 2 часов при 37oС с 100 мкл мышиного моноклонального антитела (IgG) против трансглутаминазы человека (первичного антитела), полученного от Biomedical Technologies Inc. и разведенного 1: 2000 в буфере TBS/1% BSA, а затем шесть раз промывали буфером для промывки (TBS/1% BSA/0,05% Твин-20). После этого клетки инкубировали в течение 2 часов при 37oС с 100 мкл Fab-фрагмента, конъюгированного с пероксидазой антитела против мышиных IgG вторичного антитела, полученного от Amersham и разведенного в отношении 1: 4000 в буфере для промывки, а затем три раза промывали буфером для промывки и три раза PBS. Клетки инкубировали с раствором субстрата (4 мг о-фенилендиамина и 3,3 мкл 30% Н2О2 в 10 мл 0,1 М цитратного буфера, рН 5,0) в течение пяти минут, при комнатной температуре, в темноте (под алюминиевой фольгой). Реакцию прекращали путем добавления 50 мкл 4 н. Н2SO4. Оптическую плотность образцов считывали при 492 нм на планшет-ридере. Из шести дубликатов четыре дубликата обрабатывали обоими антителами, а два дубликата обрабатывали только вторичным антителом (то есть, для определения фонового связывания антитела, конъюгированного с ферментом). Уровни трансглутаминазы I определяли путем вычитания фоновых значений из значений, полученных после каждой обработки, и определения средней квадратичной ошибки (±ср. кв. ош. ) для дубликатов, обработанных обоими антителами.
Анализ ДНК
Уровень трансглутаминазы I, обнаруживаемой после обработки клеток, должен зависеть от числа клеток, то есть, чем больше число клеток, тем больше уровень обнаруживаемой трансглутаминазы I. Уровень трансглутаминазы I был нормализован на содержание ДНК в клетках в той же самой лунке, что позволило устранить расхождения, обусловленные различием в числе клеток. Количественная оценка ДНК может быть, в частности, использована как индикатор числа клеток, включая число кератиноцитов, поскольку каждая клетка имеет, в сущности, идентичный геном, а поэтому идентичное количество ДНК. Следовательно, полное содержание ДНК клеток в лунке прямо пропорционально числу клеток в этой лунке. Количественную оценку ДНК использовали для нормализации данных уровней трансглутаминазы на количество клеток.
Кератиноциты засевали в 96-луночные планшеты при плотности 3000 клеток на лунку в 200 мкл среды. После инкубирования в течение четырех дней среду заменяли на среду, содержащую тестируемые соединения (6 дубликатов на тест). Клетки культивировали еще 72 часа, после чего среду отсасывали, и планшеты хранили в течение по крайней мере 1,5 часа при температуре -70oС. Затем, планшеты удаляли из холодильника, и оттаивали в течение 30 минут. После этого добавляли 100 мкл/лунку красителя Hoechst (в конечной концентрации 1 мкг/мл), и инкубировали в течение 15 минут, после чего планшеты покрывали и считывали на флуориметре (возбуждение на 360 нм и излучение на 460 нм). Раствор красителя удаляли и лунки промывали PBS при подготовке для анализа на трансглутаминазу.
Пример 1
Ретиноевая кислота является более эффективной, чем ретинол, в изменении состояния и дифференцировки кератиноцитов
Было исследовано влияние ретиноевой кислоты (RA) ретинола (ROH) на уровни трансглутаминазы, нормализованнми на содержание клеточных ДНК, после добавления ретиноевой кислоты (RA) и ретинола (ROH), результаты этого исследования представлены в таблице 1.
Все концентрации тестированной ретиноевой кислоты, то есть 2,5• 10-7M, 2,5•10-8М и 2,5•10-9M, способствовали снижению дифференцировки кератиноцитов при обработке в значительно большей степени, чем каждая из соответствующих концентраций 2,5•10-7М, 2,5•10-8М и 2,5•10-9M ретинола. Снижение уровня трансглутаминазы является дозозависимым как для ретиноевой кислоты, так и для ретинола. Это свидетельствует о том, что ретиноевая кислота имеет более сильное ингибирующее действие на эпителиальную дифференцировку кератиноцитов, чем ретинол.
Пример 2
Микросомная этерификация ретинола in vitro.
Микросомы были получены как описано J. C. Saari and D. L. Bredberg, в "СоА and Non-CoA Dependent Retinol Esterification in Retinal Pigment Epithelium" J. Biol. Chem. 23, 8084-90 (1988).
Раствор, содержащий 0,1 М фосфатно-натриевого буфера, рН 7,5 мМ дитиотреитола, 2 мг/мл альбумина бычьей сыворотки, 40 микромолей пальмитоил-СоА, 40 микромолей дилауроилфосфатидилхолина, 10 микромолей ретинола, и тестируемое соединение или растворитель (контроль), инкубировали в течение 1 часа при 37oС с микросомной фракцией, выделенной из бычьих эпителиальных клеток, содержащих ретинальный пигмент. После инкубирования реакцию гасили путем добавления равного объема этанола, и образовавшиеся ретиниловые сложные эфиры (ретинилпальмитат из ARAT-катализируемой реакции, и ретиниллаурат из LRAT-катализируемой реакции) экстрагировали гексаном. Для количественной оценки ретинилового сложного эфира гексановый слой удаляли, упаривали в атмосфере азота, и остаток анализировали посредством ВЭЖХ на обращенно-фазовой колонке (3,9•300 мм) с C18 с использованием 80% метанола в тетрагидрофуране в качестве подвижной фазы, и посредством флуоресцентной детекции (возбуждение на 325 нм, излучение на 480 нм). Количество образовавшегося сложного эфира в присутствии растворителя (контроля) принимали за 100%, и использовали для вычисления процента ингибирования образования сложного эфира в случае тестируемых соединений. В случае контроля аликвоту микросом инактивировали путем кипячения в течение 5 минут, что приводило по крайней мере к 95%-ному ингибированию образования сложного эфира. Полученные результаты систематизировали в табл. 2 и 3.
Соединения, представленные в табл. 2, тестировали при концентрации 100 мкм. Соединения, представленные в табл. 3, тестировали при концентрации 10 мкм.
Были также протестированы соединения формулы С, которые не входят в объем настоящего изобретения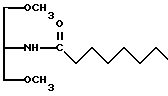
Как видно из результатов, представленных в табл. 2 и 3, N-замещенные амиды жирных кислот, где R2 имеет более 7 атомов углерода (то есть формулы А и В), являются сильными ингибиторами LRAT- или ARAT-катализируемой этерификации ретинола.
Пример 3
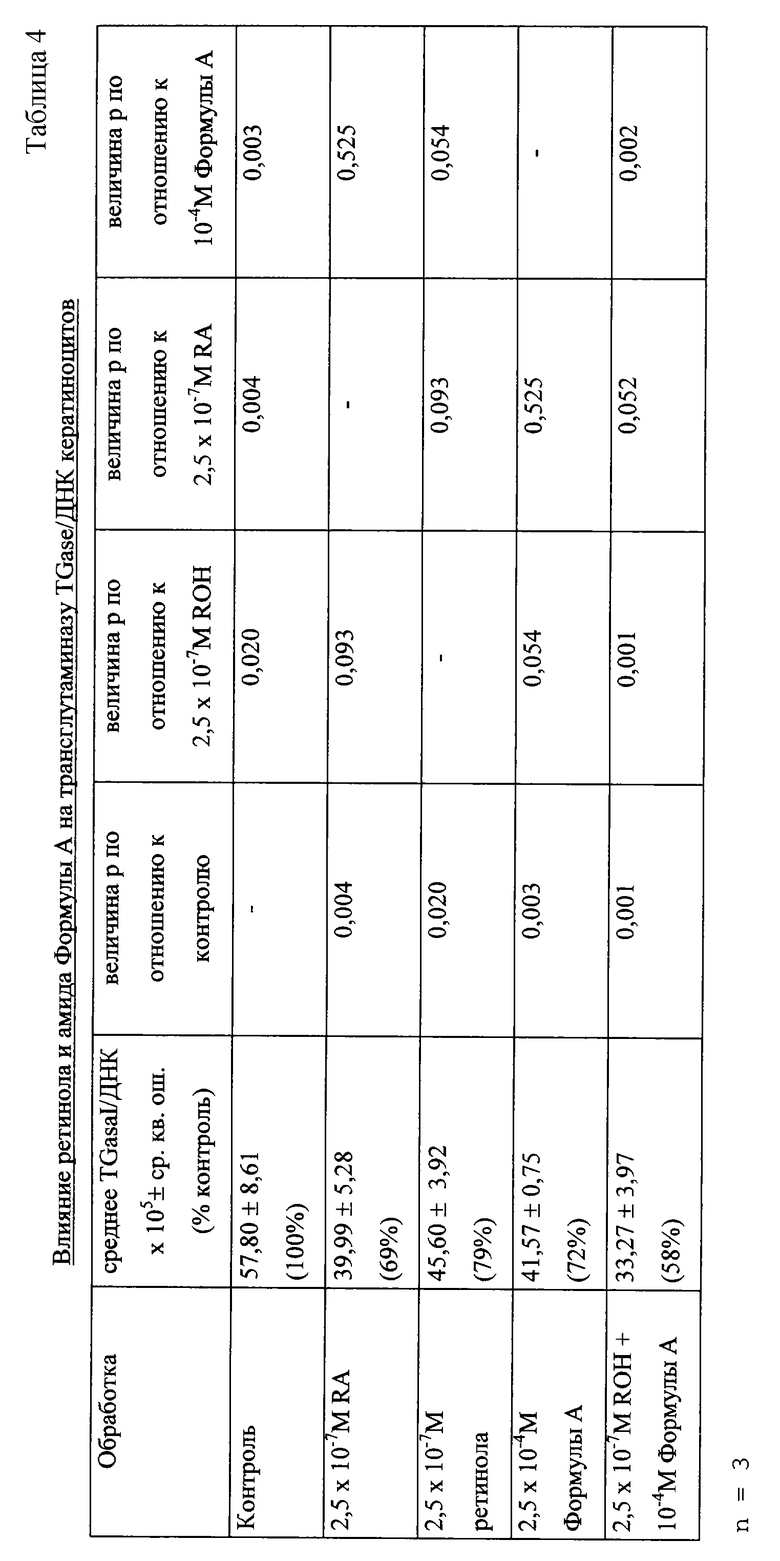
Было оценено действие соединений и комбинаций, перечисленных в табл. 4, на дифференцировку кератиноцитов. Результаты выражали как % от контроля. Уровень трансглутаминазы нормализовали на содержание ДНК.
Концентрация 2,5•10-7 M ретиноевой кислоты эффективно подавляет уровни трансглутаминазы I кератиноцитов (до 69% от контрольного уровня). Концентрации 2,5•10-7 М ретинола и 10-4 М соединения формулы А, используемые отдельно, являются менее эффективными в ингибировании уровня трансглутаминазы I кератиноцитов. Однако объединенные концентрации 2,5•10-7М ретинола +10-4M соединения формулы А ингибировали трансглутаминазу I кератиноцитов до уровня 58% от контрольных уровней. Этот пример также продемонстрировал хорошую корреляцию между данными микросомного анализа и данными, полученными при культивировании клеток.
В примерах 4-9 проиллюстрированы композиции настоящего изобретения для местного применения. Эти композиции могут быть получены стандартным способом. Они являются пригодными для применения в косметике. В частности, эти композиции могут быть использованы для нанесения на морщинистую, шероховатую, сухую, шелушащуюся, увядшую и/или УФ-поврежденную кожу в целях улучшения ее внешнего вида и чувствительности, а также для нанесения на здоровую кожу в целях предупреждения или замедления ее деградации.
Пример 4
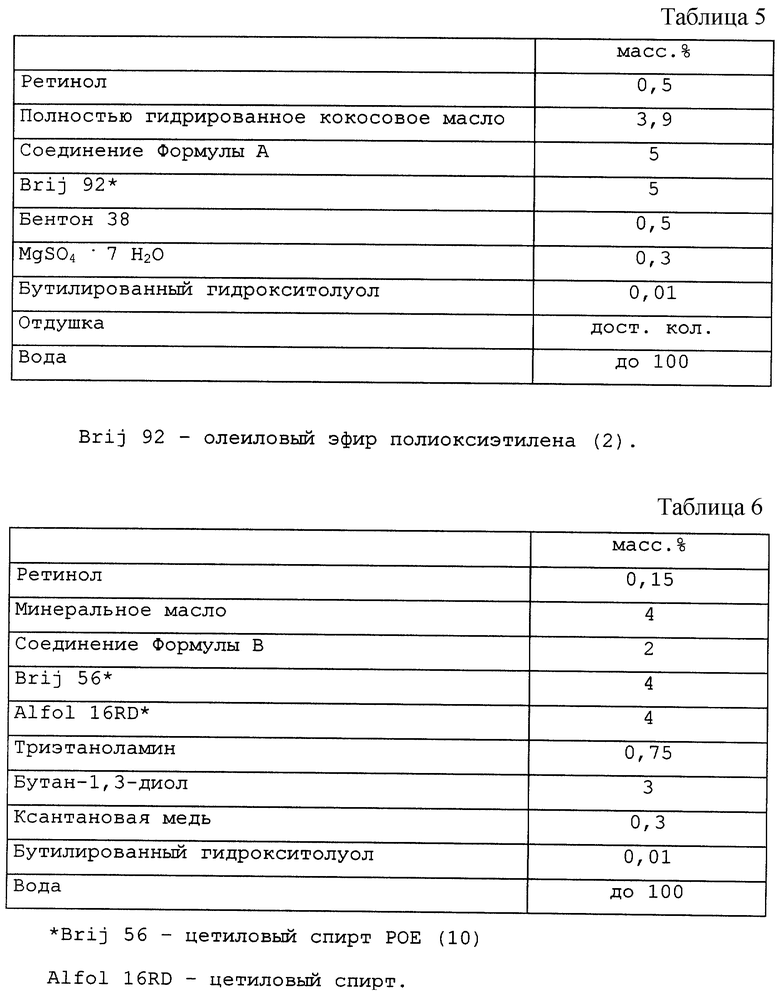
В этом примере (см. табл. 5) проиллюстрирована тонкодисперсная эмульсия типа "вода в масле", включающая композицию настоящего изобретения.
Пример 5
В этом примере (см. табл. 6) проиллюстрирован крем типа "масло в воде", включающий композицию настоящего изобретения.
Пример 6
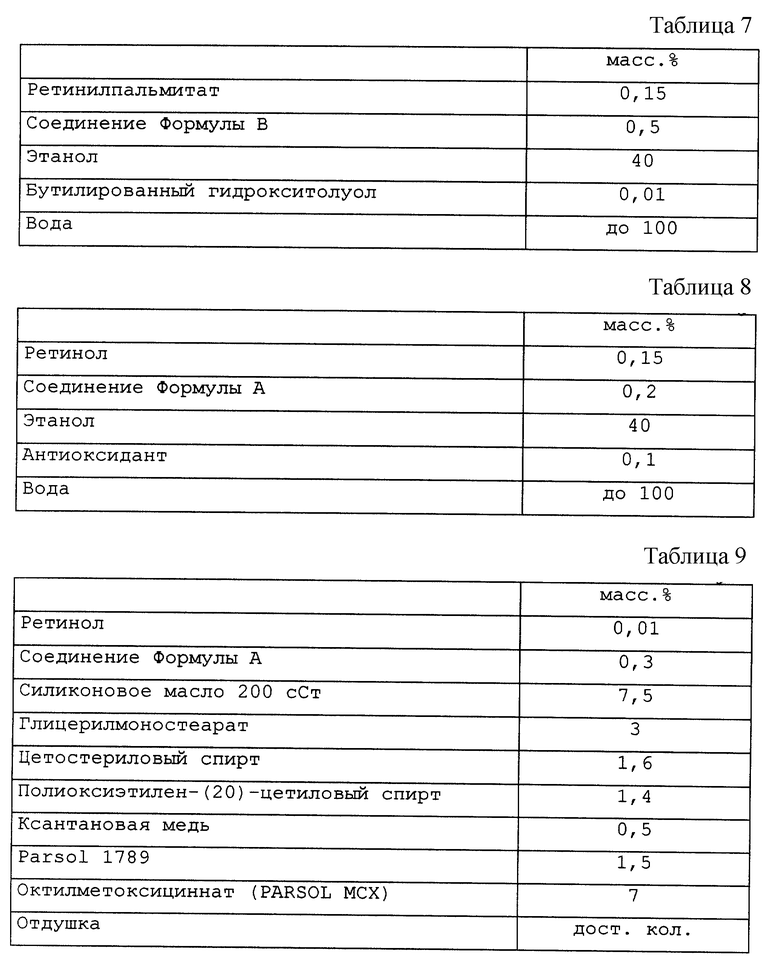
В этом примере (см. табл. 7) проиллюстрирован спиртовой лосьон, включающий композицию настоящего изобретения.
Пример 7
В этом примере (см. табл. 8) проиллюстрирован другой спиртовой лосьон, содержащий композицию настоящего изобретения.
Пример 8
В этом примере (см. табл. 9) проиллюстрирован солнцезащитный крем, включающий композицию настоящего изобретения.
Пример 9
В этом примере (см. табл. 10) проиллюстрирована безводная композиция для ухода за кожей, включающая комбинацию соединений настоящего изобретения.
Соединения, тестируемые в примерах, были получены из следующих источников:
Соединение - Источник
Ретинол - Sigma
Ретинилпальмитат - Sigma
Ретиноевая кислота - Sigma
N-замещенные амиды жирной кислоты - Университет в Утрехте, Нидерланды (University of Utrecht, Netherlands)
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИЯ ДЛЯ УХОДА ЗА КОЖЕЙ, КОСМЕТИЧЕСКИЕ СПОСОБЫ УХОДА ЗА КОЖЕЙ | 1997 |
|
RU2172167C2 |
| КОМПОЗИЦИЯ ДЛЯ УХОДА ЗА КОЖЕЙ, СПОСОБ УХОДА ЗА НЕЙ, СПОСОБ ИМИТАЦИИ ВОЗДЕЙСТВИЯ НА КОЖУ РЕТИНОЕВОЙ КИСЛОТЫ | 1997 |
|
RU2176498C2 |
| КОМПОЗИЦИЯ ДЛЯ УХОДА ЗА КОЖЕЙ, СПОСОБ УХОДА ЗА КОЖЕЙ, СПОСОБ ИМИТАЦИИ ВОЗДЕЙСТВИЯ НА КОЖУ РЕТИНОЕВОЙ КИСЛОТЫ | 1997 |
|
RU2175546C2 |
| КОМПОЗИЦИЯ ДЛЯ УХОДА ЗА КОЖЕЙ | 1998 |
|
RU2202336C2 |
| АНТИРАЗДРАЖИТЕЛИ В КОСМЕТИЧЕСКИХ КОМПОЗИЦИЯХ | 1999 |
|
RU2216312C2 |
| КОСМЕТИЧЕСКИЙ СПОСОБ ЛЕЧЕНИЯ КОЖИ | 2001 |
|
RU2287321C2 |
| КОСМЕТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ УХОДА ЗА КОЖЕЙ, СОДЕРЖАЩАЯ КУМИНОВЫЙ СПИРТ | 2000 |
|
RU2244537C2 |
| КОМПОЗИЦИЯ ДЛЯ УХОДА ЗА КОЖЕЙ, СОДЕРЖАЩАЯ ЦИС-9, ТРАНС-11 ЛИНОЛЕВУЮ КИСЛОТУ | 1999 |
|
RU2253443C2 |
| СОСТАВ ДЛЯ УХОДА ЗА КОЖЕЙ | 1997 |
|
RU2187998C2 |
| КОСМЕТИЧЕСКИЕ СОСТАВЫ | 1998 |
|
RU2203036C2 |

Изобретение относится к медицине, к композиции для ухода за кожей, содержащей 0,001-10,0% ретинола или его сложного эфира, 0,0001-50,0% ингибитора реакции этерификации ретинола (N-замещенный амид жирной кислоты) и носитель. Композиция потенцирует действие ретинола. Заявлен также способ ухода за кожей путем нанесения предложенной композиции и способ имитации воздействия на кожу ретиноевой кислоты. 3 с. и 5 з. п. ф-лы, 10 табл.
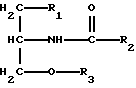
где R1 - алкил или алкокси, имеющий от 1 до 10 атомов углерода;
R2 - алкил или алкенил, имеющий от 8 до 25 атомов углерода;
R3 - алкил, содержащий 1-5 атомов углерода, или сложный эфир фосфорной кислоты;
и (с) косметически приемлемый носитель.
| Крем для кожи лица | 1990 |
|
SU1804835A1 |
| КРЕМ ДЛЯ УХОДА ЗА СУХОЙ УВЯДАЮЩЕЙ КОЖЕЙ ЛИЦА | 1993 |
|
RU2026668C1 |
| WO 9423694 A, 27.10.1994 | |||
| Способ выявления генных мутаций BRAF в опухолях человека | 2016 |
|
RU2631824C1 |
Авторы
Даты
2002-01-10—Публикация
1997-09-18—Подача