Ссылка на родственные заявки
Данная заявка является частично продолжением совместно рассматриваемую заявки на патент США 307305, поданной 16 сентября 1994 г., которая является частичным продолжением заявки на патент США 159687, поданной 30 ноября 1993 г., которая является частичным продолжением заявки на патент США 076239, поданной 11 июня 1993 г., которая является частичным продолжением заявки на патент США 717084, по которой в настоящее время выдан патент США 5228446 от 20 июня 1993 г., и заявки на патент США 716899, в настоящее время абандонированной, при этом обе заявки были поданы 18 июня 1991 г. и являются частичным продолжением заявки на патент США 569828, поданной 20 августа 1990 г., по которой в настоящее время выдан патент США 5088499 от 18 февраля 1992 г. и которая является частичным продолжением заявки на патент США 455707, поданной 22 декабря 1989 г., в настоящее время абандонированной.
Данная заявка является также частичным продолжением совместно рассматриваемой заявки на патент США 160232, поданной 30 ноября 1993, которая является частичным продолжением заявки на патент США 076250, поданной 11 июня 1993 г. , которая является частичным продолжением заявки на патент США 717084, по которой в настоящее время выдан патент США 5228446 от 20 июня 1993 г., и заявки на патент США 716899, в настоящее время абандонированной, при этом обе заявки были поданы 18 июня 1991 г. и являются частичным продолжением заявки на патент США 569828, поданной 20 августа 1990 г., по которой в настоящее время выдан патент США 5088499 от 18 февраля 1992 г. и которая является частичным продолжением заявки на патент США 455707, поданной 22 декабря 1989 г., в настоящее время абондонированной.
Каждая из указанных выше заявок включена в настоящее описание в качестве ссылки.
Область техники, к которой относится изобретение
Настоящее изобретение относится к новым композициям на основе липидов и стабилизирующих веществ и их применению. В частности настоящее изобретение относится к новым композициям на основе липидов и стабилизирующих веществ и к их применению при введении биологически активных агентов.
Предпосылки создания изобретения
Ультразвук лежит в основе дигностической техники визуализации изображения для изучения различных внутренних органов и тканей, например сосудистой сети, включая микрососудистые ткани. Ультразвук имеет ряд преимуществ перед другими методами диагностики. Например, диагностические методы ядерной медицины и методы с использованием рентгеновских лучей обычно связаны с облучением пациента ионизирующей электронной радиацией. Такая радиация может вызывать повреждение субклеточного материала, включая дезоксирибонуклеиновую кислоту (ДНК), рибонуклеиновую кислоту (РНК) и протеины. Ультразвук не относится к такому потенциально опасному излучению. Кроме того, ультразвуковой диагностический метод является относительно недорогим в сравнении с другими методами, включая компьютерную томографию (КТ) и ядерную магнитную томографию (ЯМТ), которые требуют сложного и дорогого оборудования.
Ультразвукая диагностика основана на воздействии на пациента звуковыми волнами. Звуковые волны ослабляются из-за поглощения тканями тела, проникают сквозь ткани или отражаются от них. Отражение звуковых волн от тканей, обычно обозначаемое как обратное рассеяние или отражающая способность, является физической основой формирования ультразвукового изображения. В этой связи необходимо отметить, что звуковые волны по-разному отражаются от различных тканей тела. Такое различие в отражении связано с рядом факторов, включая состав и плотность определенной обследуемой ткани. Метод ультразвуковой диагностики включает регистрацию дифференциально отраженных волн, обычно с помощью приемника, обладающего способностью детектировать звуковые волны с частотой от одного мегагерца (МГц) до десяти МГц. Зарегистрированные волны могут быть объединены в единое изображение, которое подвергается квантованию, а затем квантованные волны могут быть преобразованы в изображение исследуемой ткани.
Техника получения ультразвукового изображения обычно включает также использование контрастных агентов, которые применяют с целью улучшить качество и информативность изображения, получаемого с помощью ультразвука. Примеры контрастных агентов включают, например, суспензии твердых частиц, эмульгированные жидкие капельки, газонаполненные пузырьки [см., например, Hilmann и др. , патент США 4466442 и опубликованные международные заявки WO 92/17212 и WO 92/21382].
Качество ультразвукового изображения существенно улучшается при использовании контрастных агентов. Тем не менее необходимо дальнейшее улучшение, прежде всего в отношении изображений состояния сосудистой сети тканей, перфузированных для снабжения кровью. Соответственно имеется необходимость усовершенствования ультразвуковой техники, включая улучшение контрастных агентов, способных обеспечивать получение необходимых для медицины изображений сосудистой сети и связанных с ней органов.
Отражение звуковых волн от поверхности жидкость-газ чрезвычайно эффективно. Соответственно, пузырьки, включая газонаполненные, могут быть использованы в качестве контрастных агентов. Термин "пузырьки", используемый в данном описании, относится к везикулам, которые обычно характеризуются наличием одной или более мембран или оболочек, окружающих внутреннюю полость, наполненную газом или его предшественником. Примеры пузырьков включают липосомы, мицеллы и им подобные образования. Как более подробно описано ниже, эффективность пузырьков как контрастных агентов зависит от разных параметров, включая, например, размер и/или эластичность пузырька.
Касательно эффекта, связанного с размером пузырька, необходимо отметить следующее. Как известно специалистам в данной области техники, отраженный от пузырька сигнал является функцией его радиуса (r6) (рэлеевское рассеивание). Таким образом, рассеивающая способность пузырька диаметром 4 микрометра (мкм) в 64 раза превышает таковую для пузырька диаметром 2 мкм. В целом справедливо положение, что чем больше пузырек, тем больше величина отраженного им сигнала.
Однако размер пузырька ограничен диаметром капилляра, через который пузырек должен проходить. Очевидно, что контрастные агенты, которые включают пузырьки с диаметром более 10 мкм, могут представлять определенную опасность, поскольку они могут закупорить микрососуды. Соответственно предпочтительно, чтобы около 99% пузырьков в контрастном агенте имело диаметр менее 10 мкм. Средний диаметр пузырька также важен, и он должен быть более 1 мкм или предпочтительно более 2 мкм. Удельное среднее значение диаметра пузырьков должно составлять от 7 до 10 мкм.
Как отмечалось выше, важное значение имеет также эластичность пузырьков. Это связано с тем, что обладающие высокой эластичностью пузырьки могут при необходимости деформироваться и "проскальзывать" через капилляры, что уменьшает возможность их закупорки. Эффективность контрастного агента зависит также и от концентрации пузырьков. В целом чем выше концентрация пузырьков, тем больше отражающая способность контрастного агента.
Другой важной характеристикой, относящейся к эффективности пузырьков как контрастного агента, является стабильность пузырька. В контексте данного описания, в частности в отношении газонаполненных пузырьков, понятие "стабильность пузырька" относится к способности пузырьков сохранять заключенный внутри их объема газ после приложения внешнего давления, превышающего атмосферное давление. Эффективным контрастным агентом считаются пузырьки, которые обычно должны сохранять до 50% захваченного ими газа при воздействии давления в 300 милиметров (мм) ртутного столба (рт.ст.) в течение около одной минуты. Более эффективные пузырьки сохраняют 75% заключенного в них газа при воздействии давления 300 мм рт.ст. в течение одной минуты, а особо эффективные контрастные агенты способны удерживать до 90% заключенного в них газа при таком воздействии. Необходимо также, чтобы после снятия внешнего давления пузырек возвращался бы к своему исходному размеру. Это относится к такому обычно используемому понятию, как "эластичность пузырька".
Пузырьки, которые не обладают требуемой стабильностью, представляют собой слабые контрастные агенты. Если, например, пузырьки выделяют содержащийся в них газ в условиях in vivo, то их отражающая способность уменьшается. Аналогично этому размеры пузырьков с плохой эластичностью будут уменьшаться in vivo, что также приведет к уменьшению их отражающей способности.
Стабильность пузырьков, описанных в известной литературе, отражающей уровень техники, как правило, не соответствует требованиям для их применения в качестве контрастных агентов. Например, известны пузырьки, в том числе и газонаполенные липосомы, которые состоят из липоидальных стенок или мембран [см. , например, Ryan и др., патенты США 4900540 и 4544545; Tickner и др., патент США 4276885; Klaveness и др. , WO 93/13809; Schneider и др., ЕРО 0554213 и WO 91/15244]. Стабильность пузырьков, описанная в упомянутых выше ссылках, была низкой в условиях, когда раствор, в котором были суспендированы пузырьки, разбавляли, например, в условиях in vivo, при этом стенки или мембраны пузырьков становились тоньше, что приводило к повышенной вероятности их разрушения.
Были предприняты различные исследования для улучшения стабильности пузырьков. Такие исследования включали, например, попытки получить пузырьки, в которых мембраны или стенки состояли бы из материалов, укрепленных путем поперечного сшивания. Например, у Kleveness и др., WO 92/17212, описаны пузырьки, содержащие протеины, соединенные с помощью биоразлагаемых сшивающих агентов. Альтернативно этому мембраны пузырьков могут включать соединения, которые сами не являются протеинами, но которые также сшиты с помощью биосовместимых соединений [см. , например, Klaveness и др., WO 92/17436, WO 93/17718, WO 92/21382].
Известные из литературы способы стабилизации пузырьков, включая поперечное сшивание, имеют множество недостатков. Например, описанное выше поперечное сшивание обычно включает использование новых материалов, включая поперечносшитые протеины или другие соединения, для которых пути метабилических превращений неизвестны. Кроме того, поперечное сшивание требует проведения дополнительных химических стадий, включая выделение и очистку поперечно сшитых соединений. Более того, поперечное сшивание увеличивает жесткость мембран или стенок пузырьков. В результате пузырьки приобретают уменьшенную эластичность и, как следствие, пониженную способность к деформации при прохождении через капилляры, что в свою очередь повышает вероятность закупорки сосудов при использовании известных из уровня техники соединений, стабильность которых обеспечена путем поперечного сшивания.
Таким образом, очевидна необходимость в разработке новых и/или обладающих повышенной стабильностью контрастных агентов, а также способов их получения. Настоящее изобретение направлено на решение этой, а также и других важных задач.
Краткое описание изобретения
Настоящее изобретение относится к стабилизации липидных композиций. В частности, один из объектов настоящего изобретения относится к липидной композиции, включающей распределенные в водном носителе липид и вещество, способное стабилизировать композицию. Стабилизирующее вещество нековалентно связано с липидом и присутствует в композиции в количестве, достаточном для покрытия липида, но недостаточном для увеличения вязкости композиции. Кроме того, липидная композиция может при необходимости включать газ и/или предшественники газов. Также при необходимости липидная композиция может содержать дополнительные биоактивные агенты.
Другим объектом изобретения является везикулярная композиция, включающая распределенные в водном носителе везикулы, состоящие из липидов, и вещество, которое способно стабилизировать композицию. Стабилизирующее вещество нековалентно связано с липидом и присутствует в композиции в количествах, которых достаточно для покрытия липида, но недостаточно для увеличения вязкости композиции. Везикулярная композиция при необходимости может дополнительно включать газ и/или предшественники газов. Также при необходимости везикулярная композиция может включать биоактивные агенты.
Еще одним объектом настоящего изобретения является состав для диагностики или терапевтического использования. Состав включает липид и вещество, способное стабилизировать композицию, в сочетании с биоактивными агентами. Стабилизирующее вещество нековалетно связано с липидом и присутствует в количествах, достаточных для покрытия липида, но недостаточных для увеличения вязкости композиции. Состав может при необходимости также включать газ и/или предшественники газов.
Другим объектом настоящего изобретения является способ приготовления стабилизированной липидной композиции. Способ включает совместное объединение липида и стабилизирующего вещества, которое нековалентно связывается с липидом. Стабилизирующее вещество связывается с липидом в тех количествах, которые необходимы для покрытия липида, но недостаточны для повышения вязкости композиции.
Еще один объект настоящего изобретения относится к способу приготовления состава для диагностического или терапевтического использования. Способ включает совместное объединение биоактивного агента и композиции, включающей липид и стабилизирующее вещество, которое нековалентно связывается с липидом. Стабилизирующее вещество присутствут в композиции в количествах, которых необходимо для покрытия липида, но недостаточно для повышения вязкости композиции.
Другой объект настоящего изобретения относится к стабилизированной липидной композиции, которая приготовлена путем объединения липида и стабилизирующего вещества, которое нековалентно связывается с липидом. Стабилизирующее вещество объединяется с липидом в количествах, которых необходимо для покрытия липида, но недостаточно для повышения вязкости композиции.
Еще один объект настоящего изобретения относится к стабилизирующему составу для терапевтического и диагностического использования. Состав приготовлен путем объединения биоактивного агента и композиции, состоящей из липида и вещества, способного стабилизировать состав. Стабилизирующее вещество нековалентно связано с липидом и присутствут в количествах, которых необходимо для покрытия липида, но недостаточно для повышения вязкости состава.
Другим объектом настоящего изобретения является способ получения изображения внутренних органов пациента. Способ включает (I) введение пациенту липидной композиции, содержащей распределенные в среде водного носителя липид, газ или предшественник газа, и вещество, способное стабилизировать композицию, при этом стабилизирующее вещество нековалентно связано с липидом и присутствут в количествах, которых необходимо для покрытия липида, но недостаточно для повышения вязкости композиции; и (II) сканирование пациента с использованием ультразвука с получением визуального изображения внутренних органов.
Объектом настоящего изобретения является далее еще один способ получения изображения внутренних органов пациента. Способ включает (I) введение пациенту везикулярной композиции, включающей распределенные в среде водного носителя везикулы, состоящие из липида, газа или предшественника газа и вещества, способного стабилизировать композицию, при этом стабилизирующее вещество нековалентно связано с липидом и присутствут в количествах, которых необходимо для покрытия липида, но недостаточно для повышения вязкости композиции; и (II) сканирование пациента с использованием ультразвука с получением визуального изображения внутренних органов пациента.
Еще один объект настоящего изобретения относится к способу диагностики патологических изменений тканей у пациента. Способ включает (I) введение пациенту липидной композиции, которая содержит распределенные в среде водного носителя липид, газ или предшественник газа и вещество, способное стабилизировать композицию, при этом стабилизирующее вещество нековалентно связано с липидом и присутствут в количествах, которых необходимо для покрытия липида, но недостаточно для повышения вязкости композиции; и (II) сканирование пациента с использованием ультразвука с получением визуального изображения патологических изменений тканей у пациента.
Еще один объект настоящего изобретения относится к способу диагностики патологических изменений тканей у пациента. Способ включает (I) введение пациенту везикулярной композиции, которая содержит распределенные в водном носителе везикулы, состоящие из липида, газа или предшественника газа и вещества, способного стабилизировать композицию, при этом стабилизирующее вещество нековалентно связано с липидом и присутствует в количествах, которых достаточно для покрытия липида, но недостаточно для повышения вязкости композиции; и (II) сканирование пациента с использованием ультразвука для получения визуального изображения патологических изменений тканей у пациента.
Настоящее изобретение относится также к способу доставки биоактивных агентов в условиях in vivo в терапевтических целях. Способ включает введение пациенту терапевтически эффективного количества состава, содержащего в комбинации с биоактивным агентом липидную композицию, которая состоит из липида и вещества, стабилизирующего композицию. Стабилизирующее вещество нековалентно связано с липидом и присутствут в количествах, которых. достаточно для покрытия липида, но недостаточно для повышения вязкости композиции.
Эти и другие объекты настоящего изобретения более подробно представлены ниже в описании и формуле изобретения.
Подробное описание изобретения
Термины, использованные выше и применяемые далее в описании, имеют следующие значения, если не указано иное.
"Липид" относится к синтетическому или природному амфипатическому соединению, которое состоит из гидрофильного и гидрофобного компонентов. Липиды включают, например, жирные кислоты, нейтральные жиры, фосфатиды, гликолипиды, алифатические спирты и воск, терпены и стероиды.
"Липидная композиция" относится к композиции, которая включает смесь липидных соединений. Примеры липидных композиций могут включать суспензии, эмульсии и везикулярные композиции.
"Липидный состав" относится к композиции, включающей липидное соединение и биоактивный агент.
"Везикула" относится к сферическим образованиям, характеризующимся наличием у них внутреннего объема. Везикулы предпочтительно формируются из липидов, включая различные липиды, представленные в описании настоящего изобретения. В конкретной везикуле липиды могут находиться в форме монослоя или бислоя, и эти моно- или бислойные липиды могут в свою очередь формировать один или более моно- или бислоев. В случае когда присутствует более одного моно- или бислоя, моно- или бислои расположены концентрично. Липидные везикулы по изобретению представляют собой такие образования, которые обычно относят к липосомам, мицеллам, пузырькам, микропузырькам, микросферам и другим им подобным образованиям. Таким образом, липиды могут быть использованы для создания моноламеллярной везикулы (состоящей из одного моно- или бислоя), олиголамеллярной везикулы (содержащей два или около трех монослоев или бислоев) или мультиламеллярной везикулы (состоящей из более чем трех монослоев или бислоев). Внутренний объем везикул может быть заполнен жидкостью, включая, например, водную среду, газом, предшественником газа и/или твердым или растворенным материалом, включая, например, биоактивный агент, если это целесообразно.
"Везикулярная композиция" относится к композиции, которая включает везикулы, состоящие из липидов.
"Везикулярный состав" относится к композиции, состоящей из везикул и биоактивного агента.
Термин "липосомы" относится обычно к сферическим кластерам или агрегатам амфипатических соединений, включающим липидные соединения, как правило, в форме одного или более концентрических замкнутых слоев, например бислоев. Они также могут обозначаться в описании как липидные везикулы.
"Пациент" относится к животным, включая млекопитающих, предпочтительно к людям.
"Биоактивный агент" относится к соединению, которое используют в целях диагностики или лечения, например в способах диагностики заболевания у пациента и/или в способах лечения заболевания пациента. В контексте данного описания "биоактивный агент" относится также к соединению, которое способно вызвать биологический эффект в условиях in vitro и/или in vivo. Биоактивный агент может быть нейтральным, положительно или отрицательно заряженным. Примеры приемлемых биоактивных агентов включают диагностические агенты, фармацевтические препараты, лекарства, синтетические органические молекулы, протеины, пептиды, витамины, стероиды и генетический материал, включая нуклеозиды, нуклеотиды и полинуклеотиды.
"Диагностический агент" относится к любому агенту, который используют в способах диагностики заболевания у пациента. Примеры диагностических агентов могут включать контрастные вещества для использования в диагностических методах, связанных с ультразвуковой, ядерной магнитной резонансной визуализацией изображения или компьютерной томографией пациента.
"Генетический материал" относится обычно к нуклеотидам и полинуклеотидам, включая дезоксирибонуклеиновую кислоту (ДНК) и рибонуклеиновую кислоту (РНК). Генетический материал может быть получен методами синтетической химии, общеизвестными специалистам в данной области техники, или с использованием рекомбинантной методики либо сочетанием этих двух подходов. Молекулы ДНК и РНК могут также включать нуклеотиды неприродного происхождения и могут иметь однонитевую или двунитевую форму. "Генетический материал" относится также к смысловым и антисмысловым ДНК и РНК, которые в свою очередь являются нуклеотидными последовательностями, комплиментарными к специфическим последовательностям нуклеотидов в ДНК и/или РНК.
"Фармацевтические препараты" или "лекарства" относятся к любому лечебному или профилактическому агенту, который используется для воздействия (включая предотвращение, диагностику, облегчение состояния или лечение) на болезнь, недуг, поражение или ранение пациента. Используемые в терапевтических целях протеины, полипептиды и полинуклеотиды включены в общее понятие термина фармацевтические препараты и лекарства.
"Стабилизирующее вещество" относится к веществу, которое является биосовместимым и которое способно вызывать формирование везикул и липидных композиций. В контексте данного описания "стабилизирующее вещество" относится также к веществу, которое является биосовместимым и которое способно улучшить стабильность везикул. В определенных предпочтительных вариантах стабилизирующее вещество представляет собой полимер. В контексте данного описания понятие "полимер" относится к молекулам, образованным путем химического объединения двух или более повторяющихся звеньев. Соответственно в понятие "полимер" включаются, например, димеры, тримеры и олигомеры. В других определенных предпочтительных вариантах стабилизирующее вещество включает неполимерный материал, в том числе, например, мономерные молекулы. Понятие "стабилизирующее вещество" включает также присутствие биоактивных агентов. Стабилизирущее вещество может быть нейтральным или положительно или отрицательно заряженным. Предпочтительным среди нейтральных стабилизирующих веществ являются полярные соединения.
"Стабильность везикул" относится к способности газонаполненных везикул удерживать захваченный ими газ после воздействия на них давления около 300 мм рт. ст. в течение около одной минуты. Стабильность везикул измеряется в процентах (%), представляя собой соотношение между количеством газа, которое было исходно заключено в везикуле и которое осталось в ней после снятия давления. Понятие стабильность везикул включает также представление об "эластичности везикул", т. е. способности везикул возвращаться к исходному размеру после снятия давления.
"Вязкость" относится к внутреннему трению жидкости, которое определяют с использованием стандартных приборов для измерения вязкости, например, вискозиметра.
"Увелечение вязкости" относится к повышению вязкости на величину, превышающую примерно 20%.
"Нековалентная связь" относится к межмолекулярному взаимодействию между двумя или более отдельными молекулами без образования ковалентной связи. Межмолекулярное взаимодействие зависит от многих параметров, включая, например, полярность взаимодействующих молекул, заряд (положительный или отрицательный), если он возникает у взаимодействующих молекул, и т.п. Нековалентная связь предпочтительно относится к ионному взаимодействию, диполь-дипольному взаимодействию, силам ван-дер-Ваальса и их сочетаниям.
"Ионное взаимодействие" относится к межмолекулярному взаимодействию между двумя или более молекулами, каждая из которых заряжена положительно или отрицательно. Таким образом, "ионное взаимодействие" относится, например, к притяжению между первой положительно заряженной молекулой и второй отрицательно заряженной молекулой. Примеры ионных взаимодействий включают, например, притяжение между отрицательно заряженным стабилизирующим веществом, например генетическим материалом, и положительно заряженным липидом, например такой катиноной формой липида, как бромид лауроилтриметиламмония.
"Диполь-дипольное взаимодействие" обычно относится к притяжению, которое возникает между двумя или более полярными молекулами. Например, "диполь-дипольное взаимодействие" относится к притяжению положительного заряженного конца первой полярной молекулы к отрицательно заряженному концу второй полярной молекулы. В качестве примера диполь-дипольного взаимодействия может быть рассмотрено притяжение между электроположительной полярной группировкой ("головкой"), например, "головкой" холина в молекуле фосфатидилхолина и электроотрицательным атомом, например таким гетероатомом, как кислород, азот или сера, который присутствует в стабилизирующем веществе, например полисахариде. "Диполь-дипольное взаимодействие" относится также к внутримолекулярной водородной связи, в которой атом водорода служит мостиком между электроотрицательными атомами отдельных молекул, к одной из которых атом водорода присоединен ковалентной связью, а со второй связан электростатическими силами.
"Силы ван-дер-Ваальса" относятся к силам взаимодействия между неполярными молекулами, и эти силы рассчитываются по правилам квантовой механики. Силы ван-дер-Ваальса обычно связывают со взаимодействием дипольных моментов, которые индуцируются соседними молекулами и связаны с изменением плотности распределения электронов.
Термин "в сочетании с" относится к встраиванию биоактивного агента в липидную композицию в соответствии с настоящим изобретением. Биоактивный агент может сочетаться с липидной композицией любым возможным способом. Например, когда липидная композиция представлена в виде везикулярной композиции, биоактивный агент может быть заключен внутри объема везикулы. Биоактивный агент может быть также интегрирован с слоем(ями) или стенкой(ами) везикулы, например, путем распределения между молекулами липидов, которые содержатся внутри везикулярного слоя(ев) или стенки(ок). Кроме того, можно отметить, что биоактивный агент может располагаться на поверхности везикулы. В этом случае биоактивный агент может вступать в химическое взаимодействие на поверхности везикулы, оставаясь при этом по существу в адгезированном состоянии. Такое взаимодействие может принять форму, например, нековалентной связи. В определенных вариантах такое взаимодействие может приводить к стабилизации везикулы.
Термины "покрытие" и "осуществлять покрытие" относятся к взаимодействию стабилизирующих веществ с липидами и/или везикулами и включают нековалентные взаимодействия.
Настоящее изобретение направлено, в частности, на стабилизацию липидной композиции. Липидная композиция включает распределенные в водном носителе липиды и вещество, способное обеспечивать стабилизацию композиции. Стабилизирующее вещество нековалентно связывается с липидом и присутствует в композиции в количестве, достаточном для покрытия липида, но недостаточном для увеличения вязкости композиции.
Неожиданно было обнаружено, что в сочетании с липидными соединениями предлагаемые стабилизирующие вещества способны вызывать образование везикул. Кроме того, оказалось неожиданным, что стабилизирующие вещества способны улучшить также стабильность образованных везикул. В отличие от известного уровня техники в области стабилизации липидных композиций предлагаемые способы и композиции содержат стабилизирующие вещества, которые нековалентно связываются с липидами. Таким образом, согласно изобретению предлагается простой и эффективный способ стабилизации липидных композиций, прежде всего везикулярных композиций.
В предлагаемых композициях могут использоваться разнообразные липидные соединения. Предпочтительными липидными соединениями являются те, которые в сочетании с предлагаемыми стабилизирующими веществами имеют тенденцию образовывать везикулы. Приемлемые липиды включают, например, фосфолипиды, такие как фосфатидилхолины как с насыщенными, так и с ненасыщенными остатками жирных кислот, включая диолеоилфосфатидилхолин; димиристоилфосфатидилхолин; дипальмитоилфосфатидилхолин; дистеароилфосфатидилхолин; фосфатидилэтаноламины, такие как дипальмитоилфосфатидилэтаноламин, диолеоилфосфатидилэтаноламин, N-сукцинилдиолеоилфосфатидилэтаноламин и 1-гексадецил-2-пальмитоилглицерофосфоэтаноламин; фосфатидилсерин; фосфатидилглицерин; сфинголипиды; гликолипиды, такие как ганглиозид GM1; глюколипиды; сульфатиды; гликосфинголипиды; фосфатидовые кислоты, такие как дипальмитолилфосфатидовая кислота; пальмитиновая кислота; стеариновая кислота; арахидоновая кислота; олеиновая кислота; липиды, несущие полимеры, такие как полиэтиленгликоль или поливинилпирро-лидон; холестерин и гемисукцинат холестерина; 12-(((7'-диэтиламинокумарин-3-ил)карбонил)метиламино) октадекановая кислота; N-[12-(((7'-диэтиламино-кумарин-3-ил)карбонил)метиламино)октадеканоил] -2-аминопальмитиновая кислота; холестерин-4'-триметиламинобутаноат; 1,2-диолеоил-sn-глицерин; 1,2-дипальмитоил-sn-3-сукцинилглицерин; 1,3-дипальмитоил-2-сукцинилглицерин; и пальмитоилгомоцистеин.
Приемлемые липидные соединения включают также липиды, используемые для создания смешанных мицеллярных систем, такие как бромид лаурилтриметиламмония; бромид цетилтриметиламмония; бромид миристилтриметиламмония; хлорид алкилдиметилбензиламмония (где алкил представляет собой, например, С12-, С14- или С15алкил); бромид/хлорид бензилдиметилдодециламмония; бромид/хдорид бензилдиметилгексадециламмония; бромид/хлорид бензилдиметилтетрадециламмония; бромид/хлорид цетилдиметилэтиламмония и бромид/хлорид цетилпиридиния.
Приемлемые липиды для использования в имеющихся композициях также включают липиды, несущие заряд, например, анионные или катионные липиды. Примеры катионных липидов могут включать, например, хлорид N- [1-2,3-диолеоилокси)пропил]-N,N,N-триметиламмония (ДОТМА), диолеоилокси-3-(триметиламмоний)пропан (ДОТПА) и 1,2-диолеоилокси-е-(4'-триметиламмоний) бутаноил-sn-глицерин.
В дополнение к описанным выше липидным соединениям или вместо них представленные липидные композиции могут включать алифатические карбоновые кислоты, например жирные кислоты. Предпочтительно жирные кислоты должны иметь от 5 до 22 атомов углерода в алифатической цепи, которая может быть линейной или разветвленной. Примерами насыщенных жирных кислот являются (изо)лауриновая, (изо)миристиновая, (изо)пальмитиновая и (изо)стеариновая кислоты. В качестве примеров ненасыщенных жирных кислот можно назвать лауролеиновую, физетериновую, миристолеиновую, пальмитолеиновую, петрозелиновую и олеиновую кислоту. Приемлемые жирные кисоты могут также включать, например, жирные кислоты, в которых алифатическая группа представлена изопреноидной или пренильной группами. Кроме того, углеводы, содержащие полимерные участки, также могут быть использованы в представленных композициях липидов. Углеводы, содержащие липиды, описаны, например, в патенте США 4310505, который полностью включен в настоящее описание в качестве ссылки.
Другие липидные соединения, применяемые в представленных липидных композициях в дополнение к приведенным выше примерам, рассмотрены в приведенном ниже описании. При выборе липидов для создания липидных композиций предпочтительно исходить из необходимости проводить оптимизацию требуемых свойств таких композиций, включая стабильность сыворотки и время жизни плазмы крови. Выбор приемлемых липидов для приготовления липидных композиций в дополнение к приведенным выше примерам липидов известен специалистам в данной области техники, основываясь на материалах настоящего изобретения.
Концентрация липидов в представленных липидных композициях может варьироваться и зависит от различных факторов, включая, например, природу конкретных липидов и стабилизирующих веществ, которые применяются в композициях. Неожиданно было обнаружено, что благодаря включению стабилизирующих веществ по изобретению везикулы образуются при существенно более низких концентрациях липидов. Это является большим преимуществом, поскольку уменьшается количество липидных соединений, которые вводятся пациенту. Кроме того, снижаются затраты, связанные с производством представленных липидных композиций, поскольку уменьшается количество необходимых используемых исходных материалов, таких как липиды. В случае таких везикулярных композиций, как липосомы и мицеллы, было обнаружено, что стабильные везикулы образуются даже в том случае, когда они содержат только один бислой или монослой. В общем случае концентрация липидов в представленных липидных композициях находится в пределах от около 0,001 до около 200 мг/мл, при этом предпочтительным является диапазон концентраций от около 0,01 до около 20 мг/мл. Более предпочтительной можно считать концентрацию липидов в диапазоне от около 0,05 до около 10 мг/мл, а концентрации от около 0,1 до около 5 мг/мл являются наиболее предпочтительными.
В соответствии с настоящим изобретением липидные композиции содержат также стабилизирующие вещества. Неожиданно было обнаружено, что стабилизирующие вещества, определение которых приведено выше, способны вызывать образование везикул в липидной композиции. Таким образом, при объединении стабилизирующих веществ с липидными соединениями в соответствии со способом по изобретению липидные соединения претерпевали заданную агрегацию и образовывали везикулы. Как отмечалось ранее, концентрация везикул представляется важной в отношении эффективности контрастного материала, основанного на везикулах. При объединении с липидными соединениями представленные стабилизирующие вещества вызывают формирование везикул в концентрациях, соответствующих эффективным концентрациям контрастных агентов. Предпочтительно, чтобы представленные стабилизирующие вещества вызывали в липидных композициях образование везикул в концентрациях более примерно 1х108 везикул/мл. Более предпочтительно, когда представленные стабилизирующие вещества вызывают образование везикул в концентрациях более примерно 1х109 везикул/мл.
Стабилизирующие вещества также улучшают стабильность образованных везикул. Предпочтительно, чтобы представленные стабилизирующие вещества обеспечивали формирование везикул, имеющих стабильность более примерно 50%. Более предпочтительно, чтобы представленные стабилизирующие вещества вызывали образование везикул со стабильностью по крайней мере около 75%, а стабильность не менее примерно 90% является наиболее предпочтительной.
В определенных вариантах стабилизирующие вещества включают полимер. Предпочтительные полимеры включают полимеры, в которых повторяющиеся звенья содержат одну или более гидроксильных групп (полигидроксиполимеры); полимеры, в которых повторяющиеся звенья содержат одну или более аминогрупп (полиамины); полимеры, в которых повторяющиеся звенья содержат одну или более карбоксильных групп (поликарбоксиполимеры); и полимеры, в которых повторяющиеся звенья содержат один или более сахаридных остатков (полисахариды). Молекулярный вес полимеров может варьироваться и обычно составляет от около 50 до около 5000000, предпочтительно от около 100 до около 50000. Более предпочтительны полимеры с молекулярным весом от около 150 до около 10000 и наиболее предпочтительно от около 800 до около 8000.
Стабилизирующие вещества представляют собой нейтральные, положительно или отрицательно заряженные соединения. Среди нейтральных стабилизирующих веществ предпочтительны соединения липидной и/или масляной природы, полимеры на основе многоатомных спиртов, гликозаминогликаны, углеводы, включая моносахариды, дисахариды и полисахариды, смолы и целлюлозные соединения. Примеры нейтральных стабилизирующих материалов включают, например, масла, такие как арахисовое масло, масло канола, оливковое масло, подсолнечное масло и кукурузное масло; лецитин; сфингомиелин; холистерин и его производные; сквален; терпены и терпеноидные соединения; триглицериды; смолы, такие как ксантан, трагакант, смола из бобов робинии, гуар или карагенан (из красной водоросли Chondrus crispus); метоксилированный пектин; крахмал; агарозу; целлюлозу и полусинтетическую целлюлозу, например метилцеллюлезу, гидроксиэтилцеллюлезу, метоксицеллюлозу и гидроксипропилцеллюлозу; смолу акации; агар; бентониты, включая очищенный бентонит; магму; карбомер 934Р; декстрин; желатин; ди- и тригидроксизамещенные алканы и их полимеры, включая поливиниловый спирт; моно-, ди- и триглицериды; аминоспирты; моносахариды или такие сахарные спирты, как эритроза, треоза, рибоза, арабиноза, ксилоза, ликсоза, фруктоза, сорбит, маннит и седогептулоза, при этом предпочтительными моносахаридами являются фруктоза, манноза, ксилоза, арабиноза, маннит и сорбит; и предпочтительными дисахаридами являются лактоза, сахароза, мальтоза и целлобиоза.
Приемлемые положительно заряженные стабилизирующие вещества включают соединения, содержащие, например, протонированные или четвертичные аминогруппы, включая такие полимеры, в которых повторяющиеся звенья содержат одну или более аминогрупп, такие как пептиды, полипептиды, протеины или липопротеины, например альбумин, или природные липопротеины. Примеры положительно заряженных стабилизирующих веществ включают, например, хитин; алканоламины, такие как моноэтаноламин, диэтаноламин и триэтаноламин и их смеси, включая, например, троламин; полилизин; полиаргинин; полиэтиленимин; хитозан и пептиды, включая меланин-концентрирующий гормон и динорфин. Приемлемые отрицательно заряженные вещества представляют собой соединения, содержащие, например, карбоксильные (СО2 -) группы, включая поликарбоксиполимеры. Примеры отрицательно заряженных стабилизирующих веществ включают, например, карбоксиметилцеллюлозу; соли альгиновой кислоты, такие как альгинаты натрия и кальция; соли гликозаминогликанов, включая соли гиалуроновой кислоты; фосфорилированные и сульфированные производные углеводов; генетический материал, такой как интерлейкин-2 и интерферон; фосфор- и серусодерхащие олигомеры; отрицательно заряженные пептиды, такие как делторфин.
Другие стабилизирующие вещества в дополнение к перечисленным выше примерам известны специалисту в данной области техники на основании материалов настоящего описания.
Важным аспектом настоящего изобретения является тот факт, что стабилизирующие вещества нековалентно связаны с липидами. Это означает, что стабилизация композиций липидов может быть достигнута путем объединения липидов и стабилизирующих веществ в соответствии с описанным в настоящем изобретении способом, который обычно включает смешивание липидов и стабилизирующих веществ. Стабилизация достигается при покрытии липидов стабилизирующим веществом. Таким образом, способ и композиции по настоящему изобретению исключают необходимость ковалентного связывания липидов со стабилизирующими веществами путем использования таких сложных химических реакций, как реакции ковалентного присоединения, которые были положены в основу одного из способов стабилизации композиций в соответствии с известным уровнем техники [см., например, Klaveness и др., WO 92/17212]. Стабилизирующие вещества предпочтительно связываются с липидами путем одного или нескольких следующих возможных взаимодействий: ионное взаимодействие, диполь-дипольное взаимодействие, силы ван-дер-Ваальса или их сочетания.
Не основываясь на какой-либо теории, полагают, что стабилизирующие вещества вызывают образование везикул и стабилизируют образованные везикулы следующим образом. Используемые согласно изобретению стабилизирующие вещества, являясь нейтральными, положительно или отрицательно заряженными, обычно содержат гидрофильные и гидрофобные участки. Полагают, что в предложденных липидных композициях стабилизирующие вещества связываются с липидами таким образом, что гидрофобные участки стабилизирующих веществ взаимодействуют с гидрофобными участками липидов, а гидрофильные участки стабилизирующих веществ взаимодействуют с гидрофильными участками липидов. Подобные взаимодействия, возможно, наблюдаются между, например, положительно заряженными участками полиамина (стабилизирующего вещества) и отрицательно заряженными участками, такими как карбоксильные группы жирных кислот. Такое взаимодействие вносит свой вклад в формирование везикул. Можно предположить, что после образования везикулы стабилизирующие вещества покрывают везикулу таким образом, что гидрофобные участки стабилизирующих веществ взаимодействуют с обычно гидрофобной поверхностью или другими гидрофобными участками везикулы, а гидрофильные участки стабилизирующих веществ направлены наружу в водную среду. Таким образом, везикулы оказываются защищенными "стабилизирующим коконом", действие которого направлено на предотвращение влияния на поверхность везикул веществ, которые могут вызвать их исчезновение.
Как отмечалось выше, стабилизирующие вещества высоко эффективны в процессе образования везикул при относительно низких концентрациях липидов. Таким образом, еще одно преимущество представленного способа и композиции заключается в том, что образуются стабильные везикулы с тонкими стенками, обладающие требуемой эластичностью и деформируемостью. Тем самым предложенные композиции вызывают образование везикул, которые могут легко деформироваться и проходить через кровеносные сосуды, снижая тем самым риск закупорки сосудов.
Концентрация стабилизирущего вещества в представленных липидных композициях может варьироваться в зависимости от конкретных липидов и/или от природы использованных стабилизирующих веществ. Целесообразно, чтобы концентрация стабилизирующего вещества была по крайней мере достаточной для покрытия липида, но недостаточной для повышения вязкости композиции липидов. В предпочтительных вариантах концентрация стабилизирующего вещества составляет от около 0,01 до около 200 мг/мл. Более предпочтительной является концентрация стабилизирующего вещества от около 0,05 до около 5 мг/мл, а наиболее предпочтительна концентрация от около 0,15 до около 2,5 мг/мл.
Неожиданно было обнаружено, что стабилизирующий эффект, вызываемый присутствием стабилизирующих веществ, практически не зависит от вязкости. Также было обнаружено, что вязкость не увеличивается (а если и возрастает, то не более чем на 20%) после того, как представленные стабилизирующие вещества добавлены к композиции, состоящей из одних липидов (без стабилизирующего вещества), для создания композиции по изобретению. Этот факт является неожиданным, поскольку в соответствии с известным уровнем техники стабилизирующие вещества обычно вызывают существенное изменение вязкости липидной композиции с общей тенденцией в сторону ее роста. Предпочтительно, чтобы вязкость возрастала не более чем приблизительно на 15%, а более предпочтительным считается увеличение вязкости не более чем приблизительно на 10%. Еще более предпочтительным считается повышение вязкости не более чем приблизительно на 5%, а наиболее предпочтительным можно считать полное отсутствие увеличения вязкости (0%).
В определенных вариантах осуществления настоящего изобретения было обнаружено, что вязкость уменьшалась после добавления предлагаемых стабилизирующих веществ к композиции, содержащей один только липид (без стабилизирующего вещества), для создания композиций по изобретению. Этот факт был особенно неожиданным, поскольку, как отмечалось выше, в соответствии с известным уровнем техники добавление стабилизирующих веществ к композициям, содержащим только липид (без стабилизирующего вещества), обычно приводит к увеличению вязкости. Предпочтительно, чтобы вязкость уменьшалась приблизительно на 5% или более, предпочтительно на более чем примерно на 10%. Еще более предпочтительным можно считать снижение вязкости приблизительно на 15% и более, а наиболее предпочтительным можно считать уменьшение вязкости приблизительно на 20% и более.
В определенных предпочтительных вариантах осуществления настоящего изобретения липидные композиции включают везикулярные композиции, которые в свою очередь могут представлять собой композиции, содержащие липосомы и/или мицеллы. Известны разнообразные способы приготовления везикулярных композиций, включая, например, встряхивание, сушку, формирование с помощью газа, распылительную сушку и т.п. Приемлемые способы приготовления везикул композиций описаны, например, в заявке на патент США 307305, поданной 16 сентября 1994 г., полное содержание которой включено в настоящеее описание в качестве ссылки. Предпочтительно готовить везикулы из липидов, находящихся в гелеобразном состоянии. В приведенной в конце описания таблице 1 представлены некоторые характеристики липидов и температуры их фазовых переходов.
Ниже описано приготовление композиций, содержащих мицеллы. Мицеллы могут быть получены любым известным специалисту в данной области техники способом. Обычно эти способы включают перевод липидов в суспензию в органическом растворителе, выпаривание растворителя, повторное суспендирование липидов в водной среде, ультразвуковую обработку и центрифугирование. Приведенные ниже способы наряду с другими описаны, например, в работах Canfield и др., Methods in Enzymology, т. 189, с. 418-422 (1990); El-Gorab и др., Biochem. Biophys. Acta, т. 306, с. 58-66 (1973); Colloidal Surfactant, Shinoda K., Nakagana, Tamamushi and Isejura, Academic Press, NY (1963) (в частности "The Formaion of Micelles", Shinoda, глава 1, с. 1-88); Catalysis in Micellar and Macromollecular Systems, Fendler и Fendler, Academic Press, NY (1975). Содержание каждой из этих и последующих публикаций полностью включено в описание настоящего изобретения в качестве ссылок.
Как отмечалось выше, везикулярные композиции могут включать липосомы. В любой конкретной липосоме липидное(ые) соединение(я) может(гут) присутствовать в виде монослоя или бислоя, которые в свою очередь могут образовывать один или более моно- или бислоев. При наличии более одного моно- или бислоя последние располагаются концентрически. Таким образом, липиды можно использовать для приготовления моноламеллярных липосом (состоящих из одного монослоя или бислоя), олиголамеллярных липосом (состоящих из двух или трех монослоев или бислоев) или мультиламеллярных липосом (состоящих из более чем трех монослоев или бислоев).
Известны разнообразные способы приготовления композиций, содержащих липосомы. Очевидно, что липосомы могут быть приготовлены любым известным для специалиста в данной области техники способом. Эти способы включают удаление растворителя диализом, французский пресс, экструзию (в сочетании с методом замораживания-оттаивания или без него), испарение с обращенной фазой, микроэмульгирование и обычный метод замораживания-оттаивания. Липосомы могут быть также приготовлены с помощью различных способов с использованием механических устройств для встряхивания и перемешивания. для этой цели можно использовать, например, механическое устройство для встряхивания Wig-L-BugТМ (фирма Crescent Dental, Lyons, IL). Также может быть использовано обычное оборудование для микроэмульгирования, как, например, MicrofluidizerTM (фирма Microfluidics, Woburn, MA).
Другие способы приготовления композиций, содержащих липосомы, могут включать, например, ультразвуковую обработку, хелатный диализ, гомогенизацию, впрыскивание раствора липида в растворителе, самопроизвольное формирование, выпаривание растворителя, удаление детергента в условиях контролируемого диализа и другие, каждый из которых включает приготовление липосом разного вида. Предпочтительными для приготовления липосом являются способы, включающие методику замораживания-оттаивания. Приемлемые методы замораживания-оттаивания описаны, например, в совместно рассматриваемой заявке на патент США 07/838504, поданной 19 февраля 1992 г., описание которой включено в полном объеме в материалы настоящего изобретения в качестве ссылки. Приготовление липосом можно проводить в растворах, таких как физиологический раствор, водный раствор фосфатного буфера, или в стерильной воде.
Размер липосом при необходимости можно регулировать, используя разные методы, включая экструзию, фильтрацию, ультразвуковую обработку и гомогенизацию. Кроме того, размер липосом можно регулировать путем введения ламинарного потока сердцевинной жидкости в не смешивающуюся с ней оболочку жидкости. Другие способы приготовления липосом определенного размера, а также способы модуляции биораспределения и клиренса полученных липосом известны специалисту в данной области техники на основании материалов настоящего изобретения. Липосомы определенного размера предпочтительно получать с помощью экструзии под давлением через поры заданного диаметра. Липосомы по изобретению могут иметь любой возможный размер, тем не менее, однако, предпочтительно, чтобы липосомы были маленькими, т.е. имели размер менее приблизительно 100 нанометров (нм) по внешнему диаметру.
Многие из нижеследующих, а также другие способы приготовления липосом описаны, например, в патенте США 4728578; в заявке на патент Великобритании GB 2193095 А; в патенте США 4728575; в патенте США 4737323; международной заявке PCT/US 85/01161; у Мауег и др. в Biochimica et Biophysica Acta, т. 858, с. 161-168 (1986); у Hope и др. в Biochimica et Biophysica Acta, т. 812, с. 55-65 (1985); в патенте США 4533254; у Mayhew и др. в Methods in Enzymology, т. 149, с. 64-77 (1987); у Mayhew и др. в Biochimica et Biophysica Acta, т. 755, с. 169-74 (1984); в Cheng и др. в Investigative Radiology, т. 22, с. 47-55 (1987); в международной заявке PCT/US 89/05040; в патенте США 4162282; в патенте США 4310505; в патенте США 4921706; и в Liposome Technology, под ред. Gregoriadis G. т. 1, с. 29-31, 51-67 и 79-108 [CRC Press Inc., Boca Raton, FL 1984], причем описание каждой из этих публикаций включено в материалы настоящего изобретения в полном объеме в качестве ссылок.
Для приготовления везикулярных композиций по настоящему изобретению может быть использован любой из известных способов, однако предпочтительно использовать способ встряхивания. Предпочтительно этот способ включает использование механического устройства для встряхивания типа Wig-L-BugTM (фирма Crescent Dental, Lyons, IL), как это описано в совместно рассматриваемой заявке на патент США 160232, поданной 30 ноября 1993, содержание которой в полном объеме включено в материалы настоящего изобретения в качестве ссылки.
Для специалиста в данной области техники очевидно, что любая липидная композиция и/или липидный состав могут быть лиофилизированы для хранения и восстановлены, например, в водной среде (например, в стерильной воде, растворе фосфатного буфера или физиологическом растворе), путем механического перемешивания. Для предотвращения аглютинации или слияния липидов в ходе лиофилизапии может оказаться целесообразным введение добавок, которые предотвращали бы такое слияние или аглютинацию. Пригодные для этих целей добавки могут включать сорбит, маннит, хлорид натрия, глюкозу, трегалозу, поливинилпирролидон и полиэтиленгликоль, например ПЭГ 400. Эти и другие добавки описаны в литературе, например в соотвествующих разделах Фармакопии США, USP XXII, NF XVII, The United States Pharmacopeia, The National Formulary, United States Pharmacopeial Convention Inc., 12601 Twinbrook Parkway, Rockville, MD 20852, содержание которых полностью включено в материалы настоящего изобретения в качестве ссылок. Преимущество лиофилизированных препаратов обычно заключается в продолжительном сроке хранения.
В предпочтительных вариантах выполнения настоящего в состав липидной композиции изобретения включается газ, например инертный газ. Газы придают липидным композициям повышенную отражающую способность, прежде всего в случае везикулярных композиций, в которых газ заключен внутри везикулы. Это повышает их эффективность как контрастного средства.
Предпочтительными являются газы, которые инертны и биосовместимы, т.е. те газы, которые не вызывают повреждения биологических функций. Предпочтительны газы, выбранные из группы, включающей воздух, инертные газы, такие как гелий, неон, аргон, ксенон, диоксид углерода, азот, фтор, кислород, гексафторид серы, фторуглеводороды, перфторуглеводороды и их смеси. Другие газы, включая указанные выше, известны специалистам в данной области техники на основании материалов настоящего изобретения. В предпочтительном варианте газ представляет собой перфторуглеводород. Предпочтительно перфторуглеводород выбирают из группы, включающей перфторметан, перфторэтан, перфторпропан, перфторбутан, перфторциклобутан и их смеси. Более предпочтительным газом является перфторпропан или перфторбутан, а перфторпропан наиболее предпочтителен. Другим предпочтительным газом является тетрафторид серы.
В определенных предпочтительных вариантах выполнения изобретения газ, например воздух или перфторуглерод, объединяют с жидкими перфторуглеводородами, такими как перфторгексан, перфторгептан, перфтороктилбромид (ПФОБ), перфтордекалин, перфтордодекалин, перфтороктилиодид, перфтортрипропиламин и перфтортрибутиламин.
Может оказаться целесообразным включение в липидную композицию предшественника газообразного соединения. Такие предшественники включают вещества, которые способны превращаться в газ в условиях in vivo. Предпочтительно, чтобы предшественники газа были биосовместимыми, а образуемый в условиях in vivo газ также был биосовместимым.
Среди предшественников газа, которые пригодны для использования в представленных композициях, используют чувствительные к рH агенты. Эти агенты включают соединения, способные к выделению газа, например при воздействии на них нейтральными или кислыми значениями рН. Примеры таких чувствительных к рН агентов включают соли кислот, выбранных из группы, включающей неорганические кислоты, органические кислоты и их смеси. Угольная кислота (Н2СО3) является примером приемлемой неорганической кислоты, а аминомалоновая кислота является примером приемлемой органической кислоты. Другие кислоты, включая неорганические и органические, являются очевидными для специалиста в данной области техники на основании материалов настоящего изобретения.
Предпочтительно, чтобы предшественники газа были солями, выбранными из группы, включающей соли щелочных металлов, соли аммония и их смеси. Более предпочтительно соли выбирают из группы, включающей карбонат, бикарбонат, сесквикарбонат, аминомалонат и их смеси.
Примеры предшественников газов, используемых в липидных композициях в настоящем изобретении, включают карбонат лития, карбонат натрия, карбонат калия, бикарбонат лития, бикарбонат натрия, бикарбонат калия, карбонат магния, карбонат кальция, бикарбонат магния, карбонат аммония, бикарбонат аммония, сесквикарбонат аммония, сесквикарбонат натрия, аминомалонат натрия и аминомалонат аммония. Аминомалонат хорошо известен из уровня техники, а его получение описано, например, в Thanassi, Biochemistry, т. 9, 3, с. 525-532 (1970); у Fitzpatrick и др. в Inorganic Chemistry, т. 13, 3, с. 568-574 (1974); и у Stelmashok и др. в Koordinatsionnaya Khimiya, т. 3, 4, с. 524-527 (1977). Содержание этих публикаций включено в материалы настоящего изобретения в полном объеме в качестве ссылок.
В дополнение к чувствительным к изменению рН агентов или вместо них предшественники газа могут включать соединения, которые чувствительны к изменению температуры. Такие чувствительные к температуре агенты включают вещества, температура кипения которых выше или около 37oС. Примерами таких чувствительных к температуре агентов являются метиллактат, перфторпентан и перфторгексан. Предшественники газа могут быть также такими фотоактивируемыми веществами, как ион диазония и аминомалонат. Как более подробно описано ниже, определенные липидные композиции, прежде всего везикулярные композиции, могут быть получены таким образом, чтобы газ образовывался непосредственно в исследуемой ткани или при воздействии ультразвука на частицу. Примеры предшественников газа описаны, например, в патентах США 5088499 и 5149319. Содержание этих патентов в полном объеме включено в материалы настоящего изобретения в качестве ссылок.
Газообразные соединения и/или предшественники газов предпочтительно включают в липидные композиции по изобретению вне зависимости от физической природы композиции. Таким образом, необходимо отметить, что газы и/или предшественники газов в рамках настоящего изобретения включаются в композиции, в которых липиды агрегированы, например, равномерно, а также в композиции, в которых липиды образуют везикулы, включая мицеллы и липосомы. Включение газов и/или предшественников газов в липидные композиции по настоящему изобретению можно осуществлять любым из приемлемых способов. Например, получение газонаполненных везикул можно осуществить путем встряхивания или иным перемешиванием водных смесей, содержащих газ или предшественник газа и липид по изобретению. Таким образом образуются стабильные везикулы, внутри которых содержится газ или предшественник газа.
Кроме того, газ можно напрямую барботировать через водную смесь с липидами по изобретению. Альтернативно этому можно использовать известный способ введения газа, например, согласно патентам США 5352435 и 5228446, которые в полном объеме включены в материалы настоящего изобретения в качестве ссылок. Соответствующие способы введения газа или предшественника газа в катионные композиции липидов описаны в патенте США 4865836, содержание которого в полном объеме включено в материалы настоящего изобретения в качестве ссылки. Другие способы также известны специалистам в этой области техники на основании материалов настоящего изобретения. Предпочтительно газ вводить в липидные композиции после или во время добавления стабилизирующего вещества и/или в процессе формирования везикул.
В предпочтительных вариантах газы и/или предшественники газов вводят в везикулярные композиции, причем предпочтение отдается мицеллам и липосомам. Как более подробно описано ниже, предпочтительны везикулы, в которые инкапсулирован газ и/или предшественник газа, поскольку обеспечиваются улучшенные параметры отражения in vivo.
В определенных вариантах настоящего изобретения композиции включают также биоактивный агент. Такие композиции обозначаются в данном описании как "липидные составы", и они могут быть использованы для доставки биоактивного агента в терапевтических целях в условиях in vivo. Предпочтительно липидные составы включают везикулярные составы. В везикулярных составах циркуляция и доставка везикул к заданной ткани может контролироваться неинвазивным методом. В случае использования везикул, наполненных газом или его предшественником, возможно применение воздействий ультразвука большой мощности, радиочастот, оптической энергии, например лазерного излучения и/или тепла, для создания гипертермированных областей с целью разрушения везикул в условиях in vivo и тем самым высвобождения заключенного в них газа (или его предшественника) и биоактивного агента. Таким образом, везикулярные составы позволяют контролировать высвобождение биоактивных агентов в условиях in vivo.
Было обнаружено, что определенные биоактивные агенты, которые при необходимости вводят пациенту на основании диагноза в соответствии с курсом лечения и/или в целях профилактики заболевания, также стабилизируют липидные композиции. В этих вариантах биоактивные агенты действуют и как стабилизирующие вещества, и как диагностические или терапевтические средства. Такие биоактивные агенты обычно способны нековалентно связываться с липидными соединениями, например, путем нековалентного ионного взаимодействия, диполь-дипольного взаимодействия, с помощью сил ван-дер-Ваальса или их сочетанием.
Для использования в представленных липидных составах наиболее пригодны те биоактивные агенты, которые одновременно действуют также как стабилизирующие вещества, например, такие генетические материалы, как ДНК и РНК, пептиды и фармацевтические препараты или лекарства, например налидиксиновая кислота и винкристин.
Следует подчеркнуть, что в случае везикулярных композиций, включая мицеллы и липосомы, биоактивный агент заключен внутри везикул, представляющих собой липосомы или мицеллы. В определенных случаях биоактивный агент может быть включен также в стенку мембраны везикулы. Важным является тот факт, что в случае липидных композиций, в которых липид в основном беспорядочно агрегирован или вообще практически не агрегирован, биоактивный агент обычно распределен равномерно в пределах композиции.
В определенных вариантах изобретения целесообразно включать в липидную композицию соединения, которые содержат стабилизирующие вещества, например полимеры, такие как полимер альгиновой кислоты, ковалентно сшитый с биоактивным агентом. В качестве примера такого стабилизирующего вещества можно назвать альгинат налидиксиновой кислоты, в котором стабилизирующее вещество (полимер альгиновой кислоты) ковалентно сшит с биоактивным веществом (налидиксиновой кислотой). Такие стабилизирующие вещества целесообразны, поскольку они способны стабилизировать липидные композиции и одновременно служат источником биоактивного агента. В этой связи важно подчеркнуть, что стабилизация липидных композиций достигается такими стабилизирующими веществами, как это описано выше. Необходимо отметить также, что стабилизирующие вещества после введения гидролизуются в условиях in vivo с образованием биоактивного агента (налидиксиновой кислоты) и стабилизирующего вещества (алгиновой кислоты).
При определенных условиях целесообразно включение одной или более заряженных частиц в липидные композиции. Как описано ниже, такие заряженные частицы вносят свой вклад в эффект стабилизации, обеспечиваемый предлагаемыми стабилизирующими веществами. Примеры приемлемых заряженных частиц включают такие катионы, как ионы металлов или анионы. В качестве примеров катионов можно назвать катионы кальция, магния, марганца, меди, гадолиния или диспрозия или любой другой фармацевтически пригодный катион. Приемлемые анионы включают, например, серу, пероксиды или супероксиды. Анионные частицы могут быть связаны хелатными агентами, например этилендиаминтетрауксусной кислотой (ЭДТК) и диэтилентриаминпентауксусной кислотой (ДТПК).
Не основываясь на какой-либо теории, полагают, что описанные выше заряженные частицы способны формировать мостики, например ионные мостики между липидами и стабилизирующими веществами. Например, такой анион, как сера, может нековалентно связываться с положительно заряженным липидом, например ДОТМА, и положительно заряженным стабилизирующим веществом, например полилизином.
В дополнение к описанным выше стабилизирующим веществам, которые нековалентно связываются с липидами, в определенных случаях целесообразно включить такие стабилизирующие вещества, которые ковалентно связываются с липидами. Такие ковалентно связанные стабилизирующие вещества могут представлять собой, например, стабилизирующие вещества, несущие полимеры, включая липиды, протеины и/или сахариды, несущие полимеры. Примеры таких полимеров включают гидрофильные полимеры, такие, как полиэтиленгликоль (ПЭГ), поливинилпирролидон, полиоксомеры, полисорбаты и поливиниловый спирт. Среди полимеров ПЭГ предпочтительными являются ПЭГ 2000, ПЭГ 5000 и ПЭГ 8000, молекулярный вес которых соответственно составляет 2000, 5000 и 8000. Другие приемлемые полимеры, гидрофильные и иные известны специалистам в данной области техники на основании материалов настоящего изобретения. Полимеры, которые могут быть связаны путем реакций алкилирования или апилирования с липидами, наиболее приемлемы для улучшения стабильности липидных композиций. В качестве примеров липидов, содержащих гидрофильную полимерную часть, можно назвать дипальмитоилфосфатидилэтаноламин-ПЭГ, диолеоилфосфатидилэтаноламин-ПЭГ и дистеарилфосфатидилэтаноламин-ПЭГ.
Другие вещества, которые могут использоваться для приготовления стабилизированных липидных композиций, в дополнение к приведенным выше примерам известны специалистам в данной области техники на основании материалов настоящего изобретения. Например, может оказаться целесообразным включение в липидную композицию антибактериальных агентов или консервантов. Примеры таких веществ включают бензоат натрия, соли четвертичного аммония, азид натрия, метилпарабен, пропилпарабен, сорбиновую кислоту, аскорбил, пальмитат, бутилированный гидроскианизол, бутилированный гидрокситолуол, хлорбутанол, дегидроуксусную кислоту, этилендиамин, монотиоглицерин, бензоат калия, метабисульфит калия, сорбат калия, бисульфит натрия, диоксид серы и органические соли ртути.
Может оказаться целесообразным также включать вещества, которые могут внести свой вклад в стабилизацию липидных композиций и/или формирование везикулярных композиций. Примерами таких веществ являются неионные соединения, включая, например, сложные эфиры оксиэтилированных жирных кислот, оксиэтилированные жирные спирты, простые эфиры оксиэтилированных жирных спиртов, сложные эфиры жирных кислот и полиоксиэтилированного сорбитана, глицериновый и полиэтиленгликолевый диэфир оксистеариновой кислоты, глицериновый и полиэтиленгликолевый диэфир рицинолевой кислоты, этоксилированные стеролы из соевых бобов, этоксилированное касторовое масло, полиоксиэтиленовые-полиоксипропиленовые полимеры и стеараты оксиэтилированной жирной кислоты.
Как отмечалось выше, существует множество способов приготовления липидных композиций в соответствии с настоящим изобретением. Аналогичным образом известно большое число способов приготовления липидных составов. Например, липидный состав может быть приготовлен из смеси липидов, биоактивного агента и газа или предшественника газа. В этом случае липидные композиции приготавливают, как в вышеописанном варианте, путем включения в состав композиции также биоактивного агента. Таким образом, например, могут быть приготовлены мицеллы в присутствии биоактивного агента. В случае липидных композиций, содержащих газ, их приготовление может включать, например, барботирование газа непосредственно через смесь липидных соадинений и стабилизирующего вещества. Альтернативно этому липидные композиции можно приготовить из липидных соединений и газов или предшественников газов. В последнем случае биоактивный агент добавляют в липидную композицию перед ее использованием. Например, в водную смесь липосом и газа добавляют биоактивный агент с последующим перемешиванием с образованием состава, содержащего липосомы. Липосомный состав легко выделяется, поскольку наполненные газом и/или биоактивными агентами липосомы везикул обычно всплывают на поверхность водного раствора. Избыток биоактивного агента может быть регенирирован из остающегося водного раствора.
Составы по изобретению можно использовать в условиях либо in vitro, либо in vivo. В случае применения в условиях in vitro, включая вариант клеточных культур, липидные составы можно добавлять к клеточной культуре, а затем проводить ее инкубирование. В определенных обстоятельствах при использовании липосом энергия, например, энергия ультразвука, может быть приложена к культивируемой среде для разрушения липосом и высвобождения любых терапевтических агентов.
При применении в условиях in vivo составы по изобретению можно вводить пациенту раличными путями в зависимости от выбранного способа введения, а именно, парентерально, орально или интраперитонеально. Парентеральное введение, которое является предпочтительным, включает введение следующими путями: внутривенное, внутримышечное, внутрикишечное, внутриартериальное, подкожное, внутриглазное, интрасиновиальное, трансэпителиальное, включая трансдермальное, легочное путем ингаляции, офтальмологическое, подъязычное и трансбуккальное, местное, включая офтальмологическое, кожное, глазное, ректальное и назальную ингаляцию путем инсуффляции. Внутривенное введение является предпочтительным среди других вариантов парентерального введения.
В случае применения для такой диагностики, как ультразвуковая, липидные композиции, которые могут включать газ или предшественники газа, вводят пациенту. Энергия, предпочтительно энергия ультразвука, прилагается по крайней мере к части тела пациента для получения изображения соответствующей ткани. Таким образом получают визуальное изображение внутреннего органа пациента для получения информации о наличии или отсутствии патологии ткани.
Методика получения изображения с помощью ультразвука хорошо известна из уровня техники и описана, например, у Uhlendorf в "Physics of Ultrasound Contrast Imaging: Scattering in the Linear Range", IEEE Transactions on Ultrasonics, Ferroelectrics, and Frequency Control, т. 14(1), с. 70-79 (1994) и у Sutherland и др., "Color Doppler Myocardial Imaging: A New Techique for the Assessment of Myocardial Function", Journal of the American Society of Echocardiography, т. 7(5), с. 441-458 (1994), содержание которых в полном объеме включено в материалы настоящего изобретения в качестве ссылок.
Ультразвук может быть использован как для диагностики, так и в терапевтических целях. Обычно уровень энергии ультразвука при диагностике недостаточен для разрушения везикул и, как следствие этого, высвобождения и последующего поглощения клетками биоактивных агентов. Более того, при диагностике ультразвуком используются один или несколько звуковых импульсов. Интервалы между этими импульсами позволяют регистировать и анализировать отраженный звуковой сигнал. Ограниченное количество импульсов, используемых при ультразвуковой диагностике, ограничивает и эффективное значение энергии, которая может быть доставлена к исследуемой ткани.
С другой стороны, ультразвук высокой энергии, например ультразвук, генерируемый с помощью терапевтического оборудования, может разрушать везикулы. Обычно ультразвуковые терапевтические приборы используют от 10 до около 100% рабочих циклов в зависимости от области ткани, обрабатываемой ультразвуком. Области тела, которые характеризуются большой мышечной массой, например нижняя часть спины и бедра, а также ткани с развитой сосудистой системой, например сердечная ткань, могут потребовать большего числа рабочих циклов, например вплоть до 100%.
Терапевтические ультразвуковые приборы используют принцип доставки энергии высокого уровня непрерывными ультразвуковыми волнами. Для разрушения везикул предпочтительными можно считать непрерывные ультразвуковые волны, хотя звуковая энергия может быть и импульсной. Если используют импульсную звуковую энергию, то ультразвук должен генерироваться в виде пакета эхосигналов с числом импульсов от около 8 до около 20 в одном пакете. Предпочтительно, чтобы в одном пакете было примерно до 20 импульсов. Кроме того, используемая частота звука может варьироваться от около 0,25 до около 100 мегагерц (МГц). Обычно предпочтительная частота звука для терапевтических целей лежит в диапазоне от около 0,75 до около 3 МГц, а наиболее предпочтительная находится в диапазоне от около 1 до около 2 МГц. Уровень энергии может варьироваться от около 0,5 Вт на квадратный сантиметр (см2) до около 5,0 Вт/см2, предпочтительно от около 0,5 до около 2,5 Вт/см2. Уровень энергии ультразвука, при котором наблюдается гипертермия, обычно составляет от 5 до 50 Вт/см2. Для очень маленьких везикул, например с диаметром менее или порядка 0,5 мкм, предпочтительно использовать более высокие звуковые частоты. Это связано с тем, что более маленькие по размерам везикулы способны более эффективно поглощать энергию повышенных звуковых частот. При использовании очень высоких частот, например выше примерно 10 МГц, звуковая энергия проникает через жидкости и ткани лишь на ограниченную глубину. В этом случае применение ультразвуковой энергии может быть приемлемо для воздействия на кожу и другие поверхностные ткани. Для структур внутренних органов тела обычно необходимо фокусировать ультразвуковую энергию таким образом, чтобы она предпочтительно концентрировалась в фокальной области. В другом варианте ультразвуковая энергия может быть приложена с помощью интерстициальных устройств, внутрисосудистых или внутриполостных катеторов. Такие устройства или катеторы можно использовать, например, в пищеводе для диагностики и/или лечения карциномы пищевода. В дополнение к описанному выше терапевтическому применению представленные композиции можно использовать при карциноме пищевода или в коронарных артериях для лечения артеросклероза, а также для других терапевтических целей, как это описано, например, в патенте США 5149319, содержание которого в полном объеме включено в материалы настоящего изобретения в качестве ссылки.
Приемлемая доза введения и конкретная форма введения могут варьироваться в зависимости от возраста, веса и типа животного, области, подлежащей воздействию, природы конкретного липида и стабилизирующего вещества, присутствия или отсутствия биоактивного агента, предполагаемого диагностического или терапевтического использования, формы состава, например мицеллы или липосомы, и они очевидны для специалиста в данной области техники. Обычно вводят минимальную дозу с последующим ее повышением до достижения требуемого терапевтического эффекта. Количество вводимого липида может меняться и обычно зависит от природы конкретного липида и стабилизирующего вещества.
Ниже изобретение проиллюстрировано на примерах. Примеры 1 и 3 являются действительными примерами. Другие примеры (примеры 2 и 4) являются предположительными. Они служат только для пояснения изобретения и не должны рассматриваться как ограничивающие объем изобретения.
Примеры
Различные используемые в примерах вещества являются коммерчески доступными. Полилизин, альгиновая кислота и хитозан поставляются фирмой Sigma Chemical Co. (St. Luis, МО). Полиэтиленимин поставляется фирмой Aldrich Chemical Co. (Milwaukee, WI).
В следующих примерах аббревиатура "ДПФЭ" обозначает дипальмитоилфосфатидилэтаноламин, аббревиатура "ДПФК" обозначает дипальмитоилфосфатидовую кислоту и аббревиатура "ДПФХ" обозначает дипалмитоилфосфатидилхолин. Аббревиатура "ПЭГ 5000" обозначает полиэтиленгликолевый полимер с молекулярным весом порядка 5000. Аббевиатура "ДПФЭ-ПЭГ-5000" обозначает ДПФЭ, ковалентно сшитый с ПЭГ 5000.
Пример 1
В этом примере описано приготовление и анализ везикулярных композиций согласно настоящему изобретению. Анализ включает определения размера и числа везикул в композиции.
Было приготовлено тринадцать липидных композиций, каждая из которых включала смесь ДПФЭ-ПЭГ 5000 (62 мг), ДПФК (9,2 мг) и ДПФХ (153,2 мг). Исходные маточные растворы (по 10 мг/мл) были составлены из стабилизирующих веществ (полилизина, полиэтиленимина, альгиновой кислоты или хитозана) и деионизованной воды. Маточные растворы добавляли к двенадцати липидным композициям таким образом, чтобы 7,6 мг (5 мас.%), 15,4 мг (10 мас.%) и 30,6 мг (20 мас. %) каждого стабилизирующего вещества было добавлено к образцам липидов. К оставшемуся образцу липида не добавляли стабилизирующего вещества (контроль). Воду добавляли в каждый образец липида. Образцы перемешивали в течение ночи и нагревали до 45oС в течение 1-2 ч и снова перемешивали до получения гомогенной смеси. Затем смеси охлаждали до 4oС и лиофилизировали. Каждый из лиофилизированных образцов (от 10 до 20 мг) ресуспендировали в смеси нормального физиологического раствора:пропиленгликоля:глицерина (8:1:1 по объему) до концентрации 1 мг/мл. Смеси нагревали до 45oС и фильтровали (через фильтр с размером пор 0,22 мкм). Каждую из полученных смесей (1,5 мл) помещали в ампулу объемом 2 мл (объем пространства для заполнения газом 1,1 мл) (фирма VWR, Los Angeles, СА). Эти ампулы закупоривали и встряхивали на приборе Wig-L-BugTM (фирма Crescent Dental Lyons, IL) в течение 1 мин при скорости встряхивания 3300 мин-1 с целью наполнения везикул газом, в качестве которого использовали воздух. Аликвотные пробы (по 20 мкл) каждого образца отбирали и определяли размер везикул на приборе Accusizer Model 770 (фирма Particle Sizing Systems, Santa Barbara, CA).
Результаты анализа приведены в таблице, 2 (см. в конце описания).
Представленные результаты показывают, что композиции по изобретению, состоящие из липидов в сочетании со стабилизирующими веществами, имеют высокие концентрации везикул по сравнению с композициями без стабилизирующих веществ (контроль).
Пример 2(А)
В данном примере проиллюстрировано, что биоактивные агенты, включая пептиды, эффективны в качестве стабилизирующих веществ. Липидные композиции, описанные выше в примере 1, готовили с заменой каждого из использованных в примере 1 стабилизирующих веществ (полилизин, полиэтиленимин, альгиновая кислота и хитозан) на трансмембранный рецептор кистозного фиброза (ТРКФ). Газонаполненные везикулы готовили аналогично примеру 1. Этот пример подтверждает, что ТРКФ действует как стабилизирующее вещество.
Состав, содержащий ТРКФ, вводили внутривенно (1 мл) пациенту, страдающему кистозным фиброзом. Симптомы заболевания у пациента были сняты через 4 недели терапевтического лечения.
Пример 2(Б)
В данном случае повторяли пример 2(А) за исключением того, что винкристин (5 мг) использовали в качестве стабилизирующего вещества вместо таковых, описанных в примере 1. Этот пример демонстрирует, что винкристин действует как стабилизирующее вещество.
Композицию использовали для лечения пациента с карциномой толстой кишки на стадии после ее возможного хирургического удаления, но уже при наличии метастазов в печени. Опухоль уменьшилась с минимальными побочными последствиями.
Пример 3
В этом примере определяли вязкость приготовленных в примере 1 композиций. Использовали вискозиметр типа Bookfield Engineering Labs Viscometer со шпинделем типа СР42 Spindle. Частота вращения шпинделя была равной 1,1 с-1. Результаты приведены в таблице 3 (см. в конце описания).
Представленные выше результаты измерений вязкости показывают, что стабилизирующий эффект, производимый стабилизирующими веществами, не зависит от вязкости. Из полученных данных следует, например, что в контрольной композиции, которая не содержит стабилизирующего вещества и в которой практически нет газонаполненных везикул, ее вязкость близка к значениям вязкости композиций, которые содержат либо альгиновую кислоту, либо хитозан и в которых присутствуют требуемые концентрации газонаполненных везикул. Кроме того, композиции, содержащие полилизин или полиэтиленимин в качестве стабилизирующего вещества, имеют вязкость, значение которой составляет около половины значения вязкости контрольной композиции и композиций, содержащих альгиновую кислоту и хитозан. Как отмечено выше, композиции, включающие полилизин и полиэтиленимин, также обеспечивают требуемую концентрацию газонаполненных везикул.
Пример 4
Этот пример иллюстрирует использование стабилизирующего вещества, которое ковалентно связано с биоактивным агентом.
В круглодонную колбу объемом 250 мл добавяют налидиксиновую кислоту (5 г, 20 ммоль) и полимер альгиновой кислоты (4,5 г, 20 ммоль мономерных эквивалентов), имеющего средний молекулярный вес 240000. Смесь растворяют в диметилформамиде (100 мл) и к этой смеси при перемешивании добавяляют карбонилдиимидазол (3,2 г, 20 ммоль). Полученную смесь перемешивают в течение 1 ч и концентрируют в вакууме. Конечный продукт пропускают через колонку для гель-хроматографии с вытеснением по размеру для получения ковалентно связанного альгината налидиксиновой кислоты.
Липидные композиции готовили аналогично примеру 1 за исключением того, что стабилизирующие вещества (полилизин, полиэтиленимин, альгиновая кислота и хитозан) заменяли альгинатом налидиксиновой кислоты. По методу, описанному в примере 1, готовили газонаполненные везикулы.
Композиции, включающие альгинат налидиксиновой кислоты, затем вводили путем внутривенной инъекции (50 мл) пациенту с грамотрицательной бактериемией (pseudomonas aeruginosa). Бактериемия была ликвидирована предположительно за счет высвобождения налидиксиновой кислоты из альгината налидиксиновой кислоты благодаря расщеплению неспецифическими эстеразами в кровотоке.
Описание к каждому из патентов, патентной публикации и ссылки на публикации или описание этого документа включены в полном объеме в материалы настоящего изобретения.
Различные модификации изобретения в дополнение к описанным в настоящем изобретении очевидны специалисту в данной области техники из настоящего описания. Такие модификации также подпадают под объем настоящего изобретения и формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| АМИНОКИСЛОТЫ-ЛИПИДЫ | 2013 |
|
RU2670618C2 |
| НАЦЕЛИВАЮЩИЕ АМИНОКИСЛОТНЫЕ ЛИПИДЫ | 2013 |
|
RU2654210C2 |
| ЭКСТРАКТ МАГОНИИ ПАДУБОЛИСТНОЙ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ЭТОТ ЭКСТРАКТ | 2004 |
|
RU2388482C2 |
| ЭРИТРОПОЭТИНОВАЯ ЛИПОСОМАЛЬНАЯ ДИСПЕРСИЯ | 1999 |
|
RU2218914C2 |
| ВЫСУШЕННЫЕ ВОССТАНОВЛЕННЫЕ ВЕЗИКУЛЫ ДЛЯ ФАРМАЦЕВТИЧЕСКОГО ПРИМЕНЕНИЯ | 2007 |
|
RU2443412C2 |
| МНОГОСЛОЙНАЯ ВЕЗИКУЛЯРНАЯ КОМПОЗИЦИЯ | 2006 |
|
RU2385711C2 |
| СПОСОБ И КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ НАРУЖНОГО ОТИТА | 2010 |
|
RU2680137C2 |
| ЦЕЛЕВЫЕ ВЕЗИКУЛЯРНЫЕ КОНСТРУКЦИИ ДЛЯ ЗАЩИТЫ КЛЕТКИ И ДЛЯ ЛЕЧЕНИЯ ИНФЕКЦИЙ H. PYLORI | 2000 |
|
RU2207113C2 |
| ЛИПОСОМНЫЙ СОСТАВ И ЕГО ПОЛУЧЕНИЕ | 2013 |
|
RU2649805C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ УМЕНЬШЕНИЯ ОСЛОЖНЕНИЙ ПРИМЕНЕНИЯ СТЕРОИДНЫХ ПРЕПАРАТОВ ПРИ ЛЕЧЕНИИ ОФТАЛЬМОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2013 |
|
RU2660585C2 |

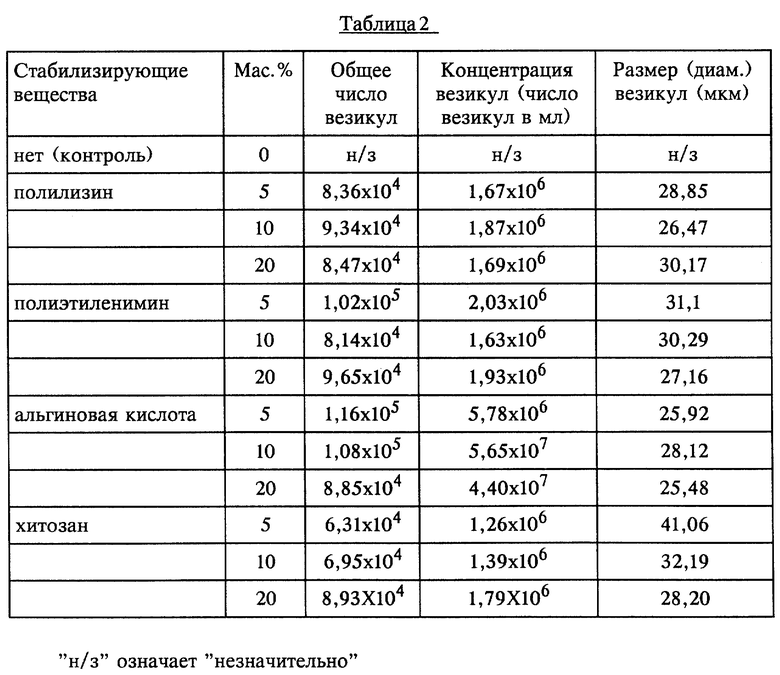

Изобретение относится к диагностике. Описаны композиции, содержащие распределенные в водном носителе липид и вещество, способное стабилизировать композицию. Стабилизирующее вещество нековалентно связывается с липидом и присутствует в количестве, достаточном для покрытия липида, но недостаточном для увеличения вязкости композиции. Композиции особенно пригодны для использования при диагностике, включая ультразвуковую. Композиции могут представлять собой везикулярные композиции, такие как композиции, содержащие мицеллы и липосомы. Композиции проявляют повышенную стабильность. При их использовании уменьшается вероятность закупорки сосудов. 6 с. и 11 з.п.ф-лы, 3 табл.
| US 4636381 A, 13.01.1987 | |||
| Четырехкомпонентный окуляр | 1955 |
|
SU122624A1 |
| US 5380519 A, 10.01.1995 | |||
| Липосомальная везикула для направленного транспорта биологически активных веществ | 1984 |
|
SU1301406A1 |
Авторы
Даты
2002-05-10—Публикация
1996-03-27—Подача