Область техники изобретения
Настоящее изобретение относится к новому классу липидов, в частности к эфир-липидам, имеющим полярную головную группу, и везикулам, содержащим эти липиды, к способам их получения, а также к их применению в медицинских целях.
Предпосылки создания изобретение
Молекулярное распознавание, такое как между рецепторным лигандом, антиген-антитело, ДНК-белком, сахар-лектином, РНК-рыбосомой, и т.д. является важным принципом, лежащим в основе многих биологических систем и применяется в отношении многих искусственно созданных биологических систем для использования в медицинских целях, таких как в искусственно созданных (микро- или нано-) частичных системах, включая полимерные гранулы, везикулярные липиды, микроэмульсии, и т.п.
Одним из важных примеров применения на основе молекулярного распознавания является использование целевой доставки диагностических или терапевтических соединений, таких как противовирусных, химиотерапевтических или визуализирующих средств, к специфицеским сайтам, что позволяет преодолеть ограничения, связанные с неспецифической доставкой (такие как время in vivo клиренса, потенциальная токсичность, проблемы, связанные с перенос агента через мембрану и т.п.) и таким образом очень повышает их эффективность. Различные стратегии на основе распознавания были использованы для улучшения доставки соединений во внутриклеточную среду (т.е. к специфическим клеточным компартментам) целевой клетки для того, чтобы вызвать ее биологическую активность, в частности доставки через специфические транспортеры, используя биологические или искусственные носители, такие как вирусные векторы, катионные полимеры, такие как полилизин, полиаргинин и т.п. (см., например, WO 79/00515, WO 98/52614), липиды-носители, и другие различные конъюгированные системы.
В одном широко используемом способе используют липидные везикулы в качестве искусственных носители, например, липосом, мицелл, наночастиц, которые были в значительной степени разработы и подвержены анализу в качестве носителей в доставке лекарственного средства благодаря и их способности снижать системную экспозицию биологически активного агента, преодолевая таким образом проблемы, связанные с распадом, растворимостью, и т.д. и обеспечивая повышение времени кругооборота крови. В активной целевой доставке биологически активного агента задействованы дериватизирующие липиды липидной везикулы (либо до, либо после образования везикулы) с нацеливающим лигандом, который служит для направления (или нацеливания) везикулы в специфические типы клеток, такие как раковые клетки или клетки, специфичные в отношении определенных тканей и органов, такие как гепатоциты, после введение in vivo (см, например, US 6,316,024 и US 6,214,388; Allen et al., Biochim. Biophys. Acta, 1237:99-108 (1995); Blume et al., Biochim. Biophys. Acta, 1149:180-184 (1993)). Это можно выполнять используя рецепторы, которые сверхэкспрессируются в специфических типах клеток, которые включают, например, рецептор фолиевой кислоты (сверхэкспрессируется во множестве опухолевых тканей, включая опухоли молочной железы, яичника, шейки матки, толстой кишки, почек, и носоглоточную опухоль), рецептор эпидермального фактора роста (EGFR) (сверхэкспрессируется в анапластическом раке щитовидной железы и опухолях молочной железы и легкого), рецептор метастина (сверхэкспрессируется в папиллярном раке щитовидной железы), рецепторные тирозинкиназы семейства ErbB (сверхэкспрессируются в значительной разновидности рака молочной железы), рецептор-2 эпидермального фактора роста (Her2/neu) (сверхэкспрессируется в раке молочной железы), тирозинкиназа-18-рецептор (c-Kit) (сверхэкспрессируется в саркоматодном почечно-клеточном раке), HGF-рецептор c-Met (сверхэкспрессируется в желудочной аденокарциноме), CXCR4 и CCR7 (сверхэкспрессируются в раке молочной железы), эндотелин-А рецептор (сверхэкспрессируется в раке предстательной железы), дельта-рецептор, активируемый пролифератором пероксисом (PPAR-дельта) (сверхэкспрессируется в большинстве колоректальных раковых опухолях), PDGFR А (сверхэкспрессируется в карциноме яичника), BAG-1 (сверхэкспрессируется в различных видах рака легкого), бета-рецептор растворимого типа II TGF (сверхэкспрессируется в раке поджелудочной железы), асиалогликопротеиновый рецептор (сверхэкспрессируется на гепатоцитах), αωβ3 интегриновый рецептор (сверхэкспрессируется в разрастающей сосудистой сети опухоли), и т.д.
Любой агент, который селективно связывается с такой специфической рецепторной клеткой или тканью, которую подвергают лечению или исследованию, может быть присоединен к липидной везикуле и действует в качестве целевого или рецепторного лиганда. Типично, такие нацеливающие лиганды присоединены к поверхности липида или липидной везикулы посредством линкера с длинной цепью (например, полимерной). Например, конъюгаты на основе фолиевой кислоты использовали для обеспечения способа целевой доставки терапевтического соединения, применимого в лечении и/или диагностики заболевания, делая возможным снижение необходимой дозы терапевтических соединений (см. например, WO 02/094185, US 6,335,434, WO 99/66063, US 5,416016). Так же, применение конъюгатов на основе галактозы- и галактозамина для транспорта экзогенных соединений по клеточным мембранам может обеспечить способ целевой доставки для лечения заболевания печени, такого как инфекция HBV и HCV или печеночно-клеточная карцинома, в то же время делая возможным снижение необходимой дозы терапевтических соединений необходимых для лечения (см. например, US 6,030,954).
Другим важным примером применения на основе молекулярного распознавания является использование систем индикации антител, что включает представление как "собственного" белка, так и "инородного" белка (антигены) имунной системе для того, чтобы вызвать активацию, модуляцию и толерантность Т-клеток. Взаимодействия рецепторных лигандов в антиген-представляющих системах, которые участвуют в желаемом иммунном ответе или его отсутствии, являются сложными и их трудно оценить, так как на них влияют различные параметры, такие как плотность лиганда, присутствие сорецепторов, рецепторно-лигандное сродство и условия поверхности. Таким образом, широко используемый подход включал применение природных человеческих клеток (или их частей), основная функция которых состоит в антигенной обработке и представлении. Но, в то время, как системы на основе живых клеток могут быть оптимальными для имитирования взаимодействия «клетка-клетка» для достижения желаемой индукции толерантности или иммунного ответа, они зависят от регулируемой экспрессии поверхностных молекул, включая возможную экспрессию дополнительных "ко-стимулирующих" и/или адгезивных молекул на своей поверхностной мембране на значительном терапевтическом уровне. Известные в настоящее время искусственные системы охватывают диапазон от генно-инженерных внутриклеточных антиген-представляющих везикул, которые несут молекулы, необходимые для представления антигена и активации или ингибирования Т-лимфоцитов на своей поверхности (WO 03/039594), до антиген-представляющих систем на основании биодеградируемых размером в частицу микросфер (WO 07/087341).
Конечно, до сих пор существуют недостатки в вышеуказанных техниках на основе молекулярного распознавания и остается потребность в уровне техники для многогранной и эффективной системе искусственного носителя для применения в целях молекулярного распознавания, как, например, целевая доствка или антигенное представление, включая простые и экономичные способы их получения.
Данная заявка обеспечивает новый класс липидов и везикулы, которые содержат эти липиды для применения в качестве носителя или изобразительной системы, что позволяет преодолеть те ограничения, которые описаны выше.
Краткое описание изобретения
Настоящее изобретение относится к новому классу липидов и везикулам, которые содержат эти липиды для применения в различных медицинских целях. В частности настоящее изобретение относится к эфир-липидным соединениям, которые характеризуются по меньшей мере двумя эфир-связанными углеводородными цепями и головная группа включает короткую, аминокислоту с прямой цепью, имеющую вплоть до 6 атомов углерода, в свободной, защищенной или активированной форме или необязательно дериватизированной по меньшей мере одной спейсерной группой.
В частности, в одном из вариантов осуществления, настоящее изобретение относится к соединению общей формулы I

в которой
Y представляет собой О, N, S или ковалентную связь,
P1 представляет собой Н, Y-защитную группу или Y-активирующую группу или спейсерную группу,
Р2, Р3 представляют собой независимо друг от друга Н, амино-защитную группу или спейсерную группу, или Р2 и Р3 образуют вместе с N, к которому они присоединены, кольцевую структуру,
L представляет собой группу формулы (а)

в которой пунктирная линия представляет собой место присоединения к N,
R1, представляют собой Н или группу формулы -(CH2)2-ORb1,
R2, представляют собой Н или группу формулы -(CH2)2-ORb2,
R2 представляет собой Н или группу формулы -CH2-ORc,
R2' представляет собой Н или группу формулы -ORd или -СН2-ORd,
R3 представляет собой Н или группу формулы -(CH2)2-ORe или -(CH2)3-ORe,
Ra, Rb1, Rb2, Rc, Rd, Re представляют собой независимо друг от друга насыщенную или ненасыщенную, прямую или разветвленную углеводородную цепь,
m представляет собой 1, 2 или 3,
при условии, что по меньшей мере один из R1, R1', R2, R2', R3 не является Н.
Соединения в соответствии с изобретением включают все возможные стереоизомеры соединений, такие как геометрические изомеры, например, Z и Е изомеры (цис- и транс-изомеры), и оптические изомеры, например, диастереомеры и энантиомеры, в чистом виде или в их смесях.
В одном из вариантов осуществления, изобретение относится к недериватизированным липидным соединениям, где P1, Р2, Р3 не представляют собой спейсерную группу. В частности, недериватизированные липидные соединения включают (i) липидные соединения в свободной форме, где P1, Р2, Р3 не представляют собой активирующую или защитную группу, (ii) защищенные липидные соединения, где по меньшей мере один из P1, Р2, Р3 представляет собой защитную группу, и (iii) активированные липидные соединения, где P1 представляет собой активирующую группу.
В другом варианте осуществления, изобретение относится к липид-спейсерным производным, где по меньшей мере один из P1, Р2, Р3 представляет собой спейсерную группу.
Соединения в соответствии с настоящим изобретением включают все возможные перестановки групп R1, R1', R2, R2', R3 и их субструктур Ra, Rb1, Rb2, Rc, Rd, Re.
В первом варианте осуществления соединения формулы I, группа R3 представляет собой Н. В частности, либо (i) R3 представляет собой Н и оба R1 и R1' представляют собой Н, или (ii) R3 представляет собой Н и оба R2 и R2' представляют собой Н. Таким образом, изобретение относится к соединениям формулы Ia,

где L представляет собой группу формулы (а)
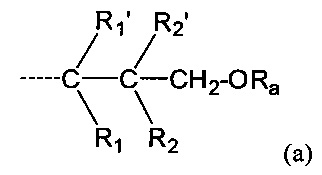
и где Р1, Р2, Р3, Y, R1, R1', R2, R2', Ra, и m имеют значения, как указано выше для соединения формулы I.
В частности, изобретение относится к соединениям формулы Ia, где L представляет собой группу формул (b) или (с)
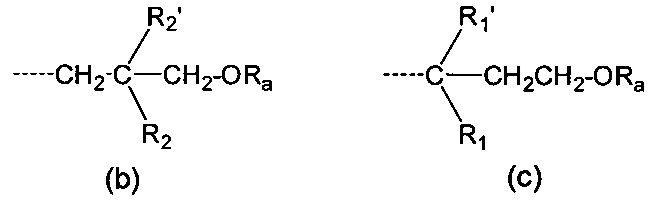
где P1, Р2, Р3, Y, R1, R1', R2, R2', Ra, и m имеют значения, как указано выше, при условии, что в формуле (b) один из R2 и R2' не является Н, и в формуле (с) один из R1 и R1' не является Н.
Во втором варианте осуществления, R1, R1', R2, R2' представляют собой Н и R3 представляет собой либо группу формулы -(CH2)2-ORe либо -(СН2)3-ORe. Таким образом, изобретение относится к соединениям формулы Ib,

где R3 представляет собой группу формулы -(СН2)2-ORe или -(CH2)3-ORe, и
Р1, Р2, Р3, Y, Ra, Re и m имеют значения, как указано выше для группы формулы I.
В другом аспекте настоящее изобретение относится к композициям в форме везикул (заявленные композиции), например, липосомам, мицеллам, наночастицам и т.п. Везикулы в соответствии с изобретением включают по меньшей мере одно соединение согласно изобретению или смесь различных соединений согласно изобретению, необязательно в смеси с одним или несколькими доугими везикулообразующими соединениями.
В другом вспекте настоящее изобретение относится к способу получения соединения и композиции в соответствии с изобретением.
Другой аспект настоящего изобретения относится к набору, который включает соединение или композицию согласно изобретению, предпочтительно в лиофилизированной форме.
Соединения и композиции согласно настоящему изобретению находят свое применение в качестве носителя, например, для целевой доставки одного или нескольких биоактивных агентов или для применения в системе индикации антител. Этот аспект настоящих соединений и композиций является частью международной заявки, подаваемой параллельно, которая полностью включена в данную заявку.
Эти и другие аспекты изобретения станут более ясными из следующего описания и формулы изобретения.
Подробное описание изобретения
Как использовалось выше и по всему описанию, определенные термины, если не указано иначе, следует понимать следующим образом:
Термин "соединение", как он используется в данной заявке, (сам по себе или в комбинации с "настоящее" или "в соответствии с изобретением" или "липидное") относится к соединению в соответствии с изобретением, которое включает линейную, бифункциональную аминокислоту на головной группе, в частности 2-амино-алкандионовую кислоту (которая имеет вплоть до шести атомов углерода), такую как аспарагиновая кислота, глютаминовая кислота, и т.п. Соединения в соответствии с изобретением включают как "недериватизированные (липидные) соединения", которые находятся в свободной форме ("свободные (липидные) соединение"), в защищенной форме ("защищенное (липидное) соединение") или в активированной форме ("активированное (липидное) соединение") и таким образом не несут ковалентно присоединенные спейсерные группы, так и "дериватизированные (липидные) соединения" (или "липидное спейсерное производное"), которые являются конъюгатами недериватизированных (липидных) соединений с одной или несколькими спейсерными группами.
Защищенное или активированное (липидное) соединение относится к соединению в соответствии с изобретением, которое было сайт-специфически модифицировано таким образом, что содержит защитную или активирующую группу, соответственно. Можификация имеет место на головной группе, в частности на реакционноспособных участках аминокислоты, более предпочтительно на N- и/или Y-группах подходящими защитными или активирующими группами (например, в виде Р1, Р2, Р3), соответственно, известными в данной области техники.
Термин "липидное спейсерное производное" относится к соединению в соответствии с изобретением, которое было сайт-специфически модифицировано таким образом, что содержит спейсерную группу. Можификация имеет место на головной группе, в частности на реакционноспособных участках аминокислоты, более предпочтительно на N- и/или Y-группе (или СО-группе, если Y представляет собой ковалентную связь) подходящими спейсерными группами (например, в виде Р1, Р2, Р3) известными в данной области техники с применением известных методов связывания.
Термин "композиция" или "данная композиция" относится к композиции, которая содержит по меньшей мере одно соединение в соответствии с изобретением. Композиции, являющиеся примером, включают везикулы или везикулярные композиции, которые в их широкой трактовке включают любое объединение по меньшей мере рлного липидного соединения в соответствии с изобретением с другими веществами и структурами. Таким образом, пригодные везикулярные композиции включают, но не ограничиваются следующими, липосомы, мицеллы, микросферы, наночастицы и т.п. В одном особенном варианте осуществления везикулярная композиция относится к сферическому объекту, имеющему внутреннюю пустоту или твердое ядро. Везикулы могут быть составлены из искусственных или природных липидов, включая одно или несколько соединений в соответствии с настоящим изобретением, и их смеси. В любой приведенной везикуле, липиды могут быть в форме монослоя или бислоя. В случае более одного моно- или бислоя, моно- или бислои являются обычно концентрическими. Липидные везикулы включают такие объекты, обычно относящиеся к таким как липосомы (т.е. везикула, включающая один или несколько концентрически упорядоченных липидных бислоев с внутренней пустотой), мицеллы (т.е. везикула, включающая один липидный монослой с внутренней пустотой), наносферы, и т.п.. Таким образом, липиды можно использовать в форме однослойной везикулы (включающей монослой или бислой), олиголамеллярной везикулы (включающей приблизительно два или приблизительно три монослоя или бислоя) или многослойной везикулы (включающей более приблизительно трех монослоев или бислоев). Альтернативно их можно использовать для покрытия предсуществующей везикулы, как наночастица, например, внутренняя пустота наносферы. везикулы может быть заполнена жидкостью, включая, например, водную жидкость, газ, газовый предшественник, и/или твердое вещество, включая, например, один или несколько биологически активных агентов. В другом особенном варианте осуществления, везикулярная композиция относится к композициям в форме кластеров, трубок и т.п.
Композиции в соответствии с изобретением могут содержать один или несколько биологически активных агентов, которые в них вставлены или введены или к ним присоединены (ковалентно и нековалентно). В частности, везикулярные композиции в соответствии с изобретением могут содержать во внутренней пустоте один или несколько биологически активных агентов (для доставочной функции) и/или могут быть дериватизированы на своей поверхности одним или несколькими биологически активными агентами (для целевой или изобразительной функции). Это является частью одновременно подаваемой заявки, которая полностью сюда включена.
Термин "солипид" или "везикулообразующий (со-)липид" как используется в данной заявке, относится к липидам, которые могут необязательно присутствовать в качестве дополнительных липидов в липидных композициях в соответствии с изобретением и могут включать нециклические и циклические, насыщенные или ненасыщенные липиды природного или искусственного происхождения. Как используется в данной заявке, солипид может быть нейтральным липидом, катионным липидом или анионным липидом. Катионный липид имеет положительный суммарный заряд и могут включать липиды, такие как N-[1-(2,3-диолеоилокси)пропил]-N,N,N-триметиламмониевые соли, например, метилсульфат (DOTAP), DDAB, бромид диметилдиоктадециламмония; 1,2-диацилокси-3-триметиламмония пропаны, (включая но не ограничиваясь следующими: диолеоил, димиристоил, дилауроил, дипалмитоил и дистеароил; также две разные ацильные цепи могут быть связаны с глицериновым скелетом); N-[1-(2,3-диолоилокси)пропил]-N,N-диметиламин (DODAP); 1,2-диацилокси-3-диметиламмония пропаны, (включая, но не ограничиваясь следующими: диолеоил, димиристоил, дилауроил, дипалмитоил и дистеароил; также две разные ацильные цепи могут быть связаны с глицериновомым скелетом); N-[1-(2,3-диолеилокси)пропил]-N,N,N-триметиламмония хлорид (DOTMA); 1,2-диалкилокси-3-диметиламмония пропаны, (включая но не ограничиваясь следующими: диолеил, димиристил, дилаурил, дипалмитил и дистеарил; также две разные алкильные цепи могут быть связаны с глицериновым скелетом); диоктадециламидоглицилспермин (DOGS); 3β-[N-(N',N'-диметиламино-этан)карбамоил]холестерин (DC-Chol); 2,3-диолеоилокси-N-(2-(сперминкарбоксамидо)-этил)-N,N-диметил-1-пропанам-иний трифтор-ацетат (DOSPA); β-аланил холестерин; цетилтриметиламмония бромид (СТАВ); ди-С14-амидин; N-трет-бутил-N'-тетрадецил-3-тетрадециламино-пропионамидин; 14Dea2; N-(альфа-триметиламмониоацетил)дидодецил-D-глутамат хлорид (TMAG); O,O'-дитетрадиканоил-N-(триметиламмонио-ацетил)диэтаноламин хлорид; 1,3-диолеоилокси-2-(6-карбокси-спермил)-пропиламид (DOSPER); N,N,N',N'-тетраметил-N,N'-бис(2-гидроксилэтил)-2,3-диолеоилокси-1,4-бутан-едиаммония йодид; производные 1-[2-(ацилокси)этил]2-алкил(алкенил)-3-(2-гидроксиэтил)-имидазолиния хлорида (как описано в Solodin et al. (1995) Biochem. 43: 13537-13544), такие как 1-[2-(9(Z)-октадеценоилокси)этил]-2-(8(Z)-гептадеценил-3-(2-гидроксиэтил)имидазолиния хлорид (DOTIM), 1-[2-(гексадиканоилокси)этил]-2-пентадецил-3-(2-гидроксиэтил)имидазолиния хлорид (DPTIM), производные 2,3-диалкилоксипропил четвертично аммониевых соединений, содержащих гидроксиалкильный фрагмент на четвертичном амине (см. например, Feigner et al. J. Biol. Chem. 1994, 269, 2550-2561), такие как: 1,2-диолеоил-3-диметил-гидроксиэтил аммоний бромид (DORI), 1,2-диолеилоксипропил-3-диметил-гидроксиэтиламмония бромид (DORIE), 1,2-диолеилоксипропил-3-диметил-гидроксипропиламмония бромид (DORIE-HP), 1,2-диолеилоксипропил-3-диметил-гидроксибутиламмония бромид (DORIE-HB), 1,2-диолеилоксипропил-3-диметил-гидроксипентиламмония бромид (DORIE-Hpe), 1,2-димиристилоксипропил-3-диметил-гидроксилэтиламмония бромид (DMRIE), 1,2-дипалмитилоксипропил-3-диметил-гидроксиэтиламмония бромид (DPRIE), 1,2-дистерилоксипропил-3-диметил-гидроксиэтиламмония бромид (DSRIE); катионные сложные эфиры ацилкарнитинов (как описано в Santaniello et al. U.S. Pat. No. 5,498,633); катионные трисложные эфиры фосфатидилхолина, т.е. 1,2-диацил-sn-глицерин-3-этилфосфохолины, где углеводородные цепи могут быть насыщенными или ненасыщенными и разветвленными или неразветвленными с длиной цепи от С12 до С24, при этом две ацильные цепи не обязательно являются идентичными. Нейтральные или анионные липиды имеют нейтральный или анионный суммарный заряд, соответственно. Они могут быть выбраны из стеролов или липидов, таких как холестерин, фосфолипиды, лизолипиды, лизофосфолипиды, сфинголипиды или пегилированные липиды с нейтральным или отрицательным суммарным зарядом. Пригодные нейтральные и анионные липиды таким образом включают: фосфатидилсерин, фосфатидилглицерин, фосфатидилиноситол (не ограничиваясь специфическим сахаром), жирные кислоты, стеролы, содержащие карбоновую кислотную группу, например, холестерин, сульфат холестерина и гемисукцинат холестерина, 1,2-диацил-sn-глицеро-3-фосфоэтаноламин, включая, но не ограничиваясь следующими, DOPE, 1,2-диацил-глицеро-3-фосфохолины и сфингомиелин. Жирные кислоты, связанные с глицериновым скелетом, не ограничиваются до специфической длины или количества двойных связей. Фосфолипиды могут также иметь две разные жирные кислоты.
Настоящее изобретение относится к новому классу липидов и везикулам, содержащим эти липиды для применения в различных медицинских целях. В частности настоящее изобретение относится к эфир-липидным соединениям H-L, где L представляет собой липидную группу, которая содержит по меньшей мере две эфир-связанных углеводородных цепей и Н представляет собой головную группу, которая содержит короткую, прямую-цепочечную аминокислоту (ω-аминокислоту), имеющую вплоть до 6 атомов углерода и их производные.
В частности, настоящее изобретение относится к соединению общей формулы I

где
Y представляет собой О, N, S или ковалентную связь,
P1 представляет собой Н, Y-защитную группу или Y-активирующую группу или спейсерную группу,
Р2, Р3 представляют собой независимо друг от друга Н, амино-защитную группу или спейсерную группу, или Р2 и Р3 образуют вместе с N, к которому они присоединены, кольцевую структуру,
L представляет собой группу формулы (а)

где пунктирная линия представляет собой место присоединения к N,
R1, представляют собой Н или группу формулы -(СН2)2-ORb1,
R1', представляют собой Н или группу формулы -(СН2)2-ORb2,
R2 представляет собой Н или группу формулы -СН2-ORc,
R2' представляет собой Н или группу формулы -ORd или -CH2-ORd,
R3 представляет собой Н или группу формулы -(CH2)2-ORe или -(CH2)3-ORe,
Ra, Rb1, Rb2, Rc, Rd, Re представляют собой независимо друг от друга насыщенную или ненасыщенную, прямую или разветвленную углеводородную цепь,
m представляет собой 1, 2 или 3,
при условии, что по меньшей мере один из R1, R1', R2, R2', R3 не является Н.
В первом варианте осуществления соединения формулы I, группа R3 представляет собой Н. В частности, или (i) R3 представляет собой Н, a R1 и R1' представляют собой Н, или (ii) R3 представляет собой Н, a R2 и R2' представляют собой Н.
Таким образом, в данном первом варианте осуществления изобретение относится к соединениям формулы Ia,

где L представляет собой группу формулы (а)

и где P1, Р2, Р3, Y, R1, R1', R2, R2', Ra, и m имеют значения, как указано выше для соединения формулы I.
В частности, изобретение относится к соединениям формулы Ia, где L представляет собой группу формул (b) или (с)

где P1, Р2, Р3, Y, R1, R1', R2, R2', Ra имеют значения, как указано выше, при условии, что в формуле (b) один из R2 и R2' не является Н, и в формуле (с) один из R1 и R1' не является Н.
В одном из предпочтительных вариантов осуществления группы (b) R2 представляет собой Н и R2' представляет собой -ORd или -CH2-ORd. В другом предпочтительном варианте осуществления группы (b) R2 представляет собой CH2-ORc и R2' представляет собой -ORd или R2' представляет собой -СН2-ORd.
Таким образом, изобретение предпочтительно относится к соединениям формулы Ia, где L представляет собой группу формулы (b1), (b2), (b3) или (b4):

где пунктирная линия представляет собой место присоединения к N, и
где Ra, Rc и Rd представляют собой независимо друг от друга насыщенную или ненасыщенную, прямую или разветвленную углеводородную цепь.
В одном из предпочтительных вариантов осуществления группы (с), один из R1 и R1' представляет собой Н. В другом предпочтительном варианте осуществления группы (с) ни R1 ни R1' не представляют собой Н.
Таким образом, изобретение предпочтительно также относится к соединениям, где L представляет собой группу формулы (c1) или (с2):

где Ra, Rb1, Rb2 имеют значения, как указано выше.
Во втором варианте осуществления соединения формулы I, группы R1, R1', R2, R2' представляют собой Н и R3 представляет собой или группу формулы (CH2)2-ORe или -(CH2)3-ORe.
Таким образом, в данном втором варианте осуществления изобретение относится к соединениям формулы Ib,
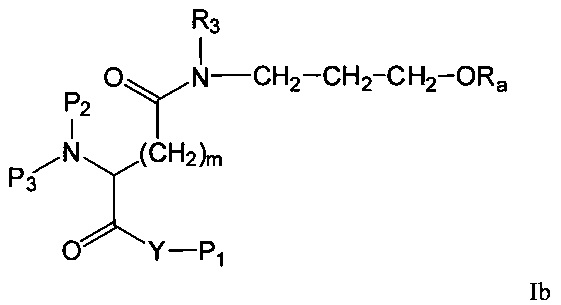
где R3 представляет собой группу формулы -(CH2)2-ORe или -(CH2)3-ORe, и
Р1, P2, Р3, Y, Ra, Re и m имеют значения, как указано выше для группы формулы I.
Таким образом, предпочтительными вариантами осуществления изобретения являются соединения формулы I (или формула Ia), представленные соединениями формул II или III

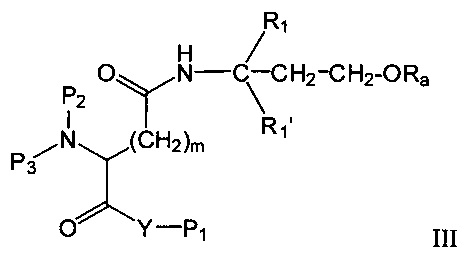
где
Y представляет собой О, N, S или ковалентную связь,
P1 представляет собой Н, Y-защитную группу или Y-активирующую группу или спейсерную группу,
Р2, Р3 представляют собой независимо друг от друга Н, амино-защитную группу или спейсерную группу, или Р2 и Р3 образуют вместе с N, к которому они присоединены, кольцевую структуру,
R1 представляет собой Н или группу формулы -(CH2)2-ORb1,
R1' представляют собой Н или группу формулы -(CH2)2-ORb2,
R2 представляет собой Н или группу формулы -СН2-ORc,
R2' представляет собой Н или группу формулы -ORd или -CH2-ORd,
Ra, Rb1, Rb2, Rc, Rd представляют собой независимо друг от друга насыщенную или ненасыщенную, прямую или разветвленную углеводородную цепь,
m представляет собой 1, 2 или 3,
при условии, что в формуле II один из R2 и R2' не является Н, и в формуле III один из R1 и R1' не является Н.
Более специфическими вариантами осуществления соединений формулы II являются соединения формулы IIa, IIb, IIc или IId,


где
Y представляет собой О, N, S или ковалентную связь,
P1 представляет собой Н, Y-защитную группу или Y-активирующую группу или спейсерную группу,
Р2, Р3 представляют собой независимо друг от друга Н, амино-защитную группу или спейсерную группу, или Р2 и Р3 образуют вместе с N, к которому они присоединены, кольцевую структуру,
Ra, Rc, Rd представляют собой независимо друг от друга насыщенную или ненасыщенную, прямую или разветвленную углеводородную цепь,
m представляет собой 1, 2 или 3.
Более специфическими вариантами осуществления соединений формулы III являются соединения формулы IIIa или IIIb,
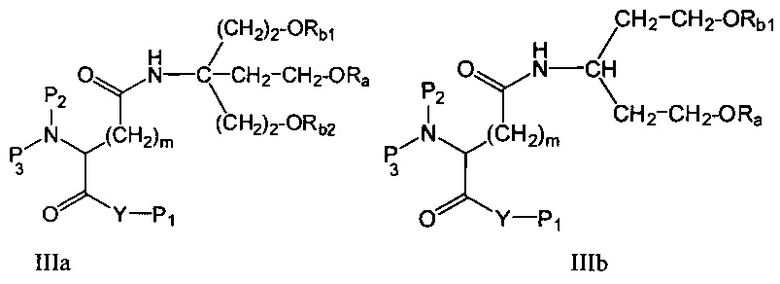
где
Y представляет собой О, N, S или ковалентную связь,
P1 представляет собой Н, Y-защитную группу или Y-активирующую группу или спейсерную группу,
Р2, Р3 представляют собой независимо друг от друга Н, амино-защитную группу или спейсерную группу, или Р2 и Р3 образуют вместе с N, к которому они присоединены, кольцевую структуру,
Ra, Rb1, Rb2 представляют собой независимо друг от друга насыщенную или ненасыщенную, прямую или разветвленную углеводородную цепь, m представляет собой 1, 2 или 3.
Другие предпочтительные варианты осуществления соединений формулы I (или формула Ib) представлены соединениями формул IVa и IVb,
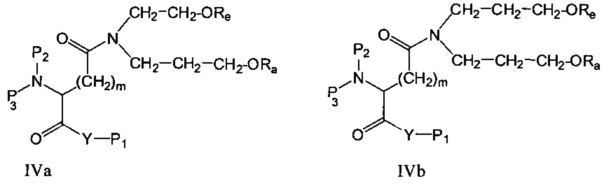
где
Y представляет собой О, N, S или ковалентную связь,
P1 представляет собой Н, Y-защитную группу или Y-активирующую группу или спейсерную группу,
Р2, Р3 представляют собой независимо друг от друга Н, амино-защитную группу или спейсерную группу, или Р2 и Р3 образуют вместе с N, к которому они присоединены, кольцевую структуру,
Ra, Re представляют собой независимо друг от друга насыщенную или ненасыщенную, прямую или разветвленную углеводородную цепь, и
m представляет собой 1, 2 или 3.
Спецмалист в данной области техники примет во внимание, что соединения в соответствии с настоящим изобретением содержат один или несколько хиральные центры и/или двойные связи и поэтому, могут существовать в качестве стереоизомеров, таких как изомеры с двойной связью (т.е., геометрические изомеры, например, Z/E изомеры или цис-/транс-изомеры), энантиомеры или диастереомеры. Соответственно, когда стереохимия на хиральных центрах не указана, изображенные в данной заявке химические структуры охватывают все возможные конфигурации на тех хиральных центрах, которые включают стереоизомерически чистую форму (например, геометрически чистую, энантиомерно чистую или диастереомерно чистую) обогащенную форму (например, геометрически обогащенную, энантиомерно обогащенную или диастереомерно обогащенную) и энантиомерные и стереоизомерные смеси. Отдельные изомеры можно получить, используя соответствующие изомерные формы исходного вещества. Альтернативно, энантиомерные и стереоизомерные смеси могут быть разложены на их компоненты энантиомеры или стереоизомеры с использованием методов разделения или методы хирального синтеза, хорошо известных специалисту в данной области техники. Соединения в соответствии с изобретением, описанные в данной заявке, также могут существовать в некоторых таутомерных формах, включая энольную форму, кето-форму и их смеси. Соответственно, структуры, изображенные в данной заявке, охватывают все возможные таутомерные формы продемонстрированных соединений.
Термин "насыщенная или ненасыщенная, прямая или разветвленная углеводородная цепь" как используется в данной заявке относится к насыщенной или ненасыщенной, прямой или разветвленной углеводородной цепи, которая содержит от 6 до 30, предпочтительно от 10 до 22 атомов углерода.
Термин "насыщенная" в комбинация с углеводородной цепью относится к прямой или разветвленной алкильной цепи, которая содержит от 6 до 30, предпочтительно от 10 до 22 атомов углерода. Примеры включают, но не ограничиваются следующими, каприл (децил), ундецил, лаурил (додедецил), миристил (тетрадецил), цетил (гексадецил), стеарил (октадецил), ннонадецил, арахидил (эйкозил), хенэйкозил, бехенил (докозил), трикозил, тетракозил, пентакозил, включая их разветвленные изомеры, например, изолаурил, антеизолаурил, изомиристил, антеизомиристил, изопалмитил, антеизопалмитил, изостеарил, антеизостеарил или фитанил (3,7,11,15-тетраметил-гексадеканил).
Термин "ненасыщенная" в комбинация с углеводородной цепью указывает, что меньше максимума возможного количества атомов водорода связано с каждым углеродом в цепи, поднимая одну или несколько углерод-углерод двойных или тройных связей. В предпочтительных вариантах осуществления, количество ненасыщенных связей в ненасыщенной углеводородной цепи составляет 1, 2, 3 или 4, предпочтительно 1 или 2.
Примеры алкенильных групп включают, но не ограничиваются следующими, мононенасыщенные алкенилы, такие как деценил, ундеценил, додеценил, пальмитолеил, гептадеценил, октадеценил (элаидил, олеил, рициноленил), нонадеценил, эйкозенил, генэйкозенил, докозенил (эруцил), трикозенил, тетракозенил, пентакозенил, и их изомеры с разветвленной цепью, а также полиненасыщенные алкенилы, такие как октадец-9,12-диенил (линолеил, элаидолинолеил), октадец-9,12,15-триенил (линоленил, элаидолиноленил), 9(Z),11(Е),13(Е)-октадецатриенил (элеостеарил), и эйкоз-5,8,11,14-тетраенил.
Примеры алкинильных групп включают, но не ограничиваются следующими, гексадец-7-инил и октадец-9-инил.
Термин "разветвленный" в комбинация с углеводородом относится к углеводородной цепи, которая содержит линейные ряды атомов углерода в качестве главной цепи с по меньшей мере одним заместителем одного или нескольких атомов углерода в качестве вспомогательной цепи (или разветвленных групп). Примеры вспомогательных цепей включают одну или несколько (С1-6)алкильных групп, такие как метильная, этильная, пропильная, изопропильная, н-бутильная, сек-бутильная группа, трет-бутильная, пентильная, гексильная и т.п., одну или несколько (С1-6)алкенильных групп, такие как винильная, аллильная, пропенильная, изопропенильная, 2-бутенильная и т.п., или одну или несколько (С1-6)алкинильных групп, такие как этинил, пропинил, бутинил и т.п.. Предпочтительными вспомогательными цепями являются (С1-6)алкильные группы, наиболее предпочтительно метил и этил.
Соединения в соответствии с изобретением содержат предпочтительно по меньшей мере две углеводородных цепи, предпочтительно 2, 3, 4, 5 или 6 углеводородных цепей, наиболее предпочтительно 2 или 3 углеводородных цепей, где главные цепи углеводородных цепей являются одинаковыми или различными, предпочтительно одинаковыми, и выбраны из алкильной цепи, алкенильной цепи, и алкинильной цепи, предпочтительно алкильной и алкенильной цепи. В одном из предпочтительных вариантов осуществления, соединения в соответствии с изобретением несут две алкильные цепи, которые могут быть одинаковыми или различными, предпочтительно одинаковыми.
В особом варианте осуществления соединения в соответствии с изобретением углеводородные цепи Ra, Rb1, Rb2, Rc, Rd, Re предпочтительно выбраны из миристила, палмитила, стеарила, олеила, линолеила и фитаноила.
Термины "алкил", "алкокси", "алкенил", "алкинил", как они используются в данной заявке в отношении групп P1, Р2, Р3, имеют следующие значения:
Термин "алкил" относится к прямой или разветвленной алкильной цепи, которая содержит от 1 до 12, предпочтительно от 1 до 8 атомов углерода.
Примеры алкильных групп включают, но не ограничиваются следующими, метил, этил, н-пропил, изо-пропил, н-бутил, изо-бутил, и трет-бутил. Термин "алкокси" относится к -О-алкильному радикалу. Примеры алкокси групп включают, но не ограничиваются следующими, метокси, этокси, и бутокси. Термин "алкенил" относится к прямой или разветвленной ненасыщенной алкильной группе, имеющей одну или несколько углерод-углерод двойных связей. Вышеуказанные алкильные, алкенильные, и алкокси группы могут необязательно быть замещенными дополнительными группами. Примеры заместителей включают, но не ограничиваются следующими, гало, гидроксил, амино, циано, нитро, меркапто, алкоксикарбонил, амидо, карбокси, алкилсульфонил, алкилкарбонил, карбамидо, карбамил, карбоксил, тиоуреидо, тиоцианато, сульфонамидо, арил, гетероарил, циклил, и гетероциклил.
Термин "арил" относится к ароматическому карбоциклическому радикалу, который содержит приблизительно от 6 до приблизительно 10, предпочтительно от 5 до 7 атомов углерода. Арильная группа может необязательно быть замещены с одной или несколькими заместителями арильной группы, которые могут быть одинаковыми или различными, где "заместитель арильной группы" включает алкил, алкенил, алкинил, арил, аралкил, гидрокси, алкокси, арилокси, аралкокси, карбокси, ароил, гало, нитро, тригалометил, циано, алкоксикарбонил, арилоксикарбонил, аралкоксикарбонил, ацилокси, ациламино, ароиламино, карбамоил, алкилкарбамоил, диалкилкарбамоил, арилтио, алкилтио, алкилен и -NRR', где R и R' каждый независимо представляет собой водород, алкил, арил и аралкил. Примерные арильные группы включают замещенные или незамещенные фенил, нафтил, пиренил, антрил, и фенантрил.
Термин "гетероарил" относится к арильному фрагменту, как указано выше, который содержит по меньшей мере один гетероатом (например, N, О, или S). Примеры гетероарильного фрагмента включают фурил, фурилен, флуоренил, пирролил, тиенил, оксазолил, имидазолил, тиазолил, пиридил, пиримидинил, хиназолинил, хинолил, изохинолил и индолил.
Термин "(гетеро)арилокси" относится к (гетеро)арил-О-группе, где (гетеро)арильная группа предварительно описана. Примерные арилокси группы включают фенокси и нафтокси. Термин "(гетеро)аралкил" относится к (гетеро)арил-алкил-группе, где (гетеро)арил и алкил предварительно описаны. Примерными аралкильные группы включают бензил, фенилэтил и нафтилметил. Термин "(гетеро)аралкилокси" относится к (гетеро)аралкил-О-группе, где (гетеро)аралкильная группа предварительно описана. Примерной аралкилокси группой является бензилокси.
Термин "циклоалкил" относится к насыщенному или ненасыщенному, неароматическому, циклическому углеводородному фрагменту, который имеет от 6 до 10 атомов углерода, такие как циклогексил или циклогексен-3-ил. Термин "гетероциклоалкил" относится к циклоалкилу, как указано в данной заявке, который имеет по меньшей мере один кольцевой гетероатом (например, N, О, или S), такой как 4-тетрагидропиранил или 4-пиранил.
Арил, гетероарил, циклоалкил, гетероциклоалкил, как указано в данной заявке, включают как замещенные, так и незамещенные фрагменты, если не указано иначе. Возможные заместители на циклоалкиле, гетероциклоалкиле, ариле и гетероариле включают (С1-С10)алкил, (С2-С10)алкенил, (С2-С10)алкинил, (С3-С8)циклоалкил, (С5-С8)циклоалкенил, (С1-С10)алкокси, арил, арилокси, гетероарил, гетероарилокси, амино, (С1-С10)алкиламино, (С1-С20)диалкиламино, ариламино, диариламино, гидроксил, галоген, тио, (С1-С10)алкилтио, арилтио, (С1-С10)алкилсульфонил, арилсульфонил, ациламино, аминоацил, амидино, гуанидин, уреидо, циано, нитро, ацил, ацилокси, карбоксил, и эфир карбоновой кислоты. Циклоалкил, гетероциклоалкил, арил, и гетероарил также могут быть конденсированы друг с другом.
Группа Y представляет собой О, N, S или ковалентную связь, предпочтительно О или N, наиболее предпочтительно N. Следует понимать, что если группа Y представляет собой ковалентную связь, то -S1-X1 непосредственно связана с СО-группой.
"Защитная группа" представляет собой фрагмент, который может быть селективно присоединен к и удален из особенной химически реактивно функциональной группы в молекулы для предотвращения его участия в нежелательных химических реакциях. Защитная группа будет варьировать в зависимости от типа химически реактивной группы, которая замещена, а также используемых условий реакции и присутствия дополнительных реактивноактивных или защитных групп в молекуле. Следует понимать, что термин "защитная группа" при использовании в отношении N-группы (такой как P1 где Y означает N, Р2 или Р3) в одном из соединений представляет собой амино-защитную группу, при использовании в отношении СОО-группы (такой как P1 где Y означает О) в одном из соединений представляет собой карбоксил-защитную группу, при использовании в отношении СО-группы (такой как P1 где Y означает ковалентную связь) в одном из соединений представляет собой карбонил-защитную группу, и при использовании в отношении S-группы (такой как P1 где Y означает S) в одном из соединений представляет собой серо-защитную группу.
Представители защитных групп для различных функциональных групп, такие как например, группы карбоновых кислот, аминогруппы, гидроксильные группы, тиольные группы, карбонильные группы и т.п., являются хорошо известными специалисту в данной области техники и описано, например, в Т.W. Greene и G.М. Wuts, Protecting groups in Organic Synthesis, Third Edition, Wiley, N.Y., 1999, и ссылках, процитированных в данной заявке.
Для соединений в соответствии с настоящим изобретением, "карбоксил-защитная группа" (например, группа P1 где Y означает О) включает, но не ограничивается следующими: бензгидрил, сложные бензиловые эфиры, такие как бензил, и о- или п-нитробензил, п-метоксибензил, сложные алкиловые эфиры, такие как метил, t-бутил, 4-пиридилметил 2-нафтилметил, 2,2-трихлорэтил, сложные силиловые эфиры, такие как 2-триметилсилил, трет-бутилдиметилсилил, трет-бутилдифенилсилил, 2-(триметилсилил)этил; ортосложные эфиры, такие как триметил- или триэтил ортоацетат; оксазолин, аллил, 2-хлораллил, фенацил, ацетонил, п-метоксифенил. Предпочтительные группы включают бензил, трет-бутил.
Амидная защитная группа (например, группа P1 где Y означает N) включает, но не ограничивается следующими: фталимидную или трифторацетамидную защитную группу.
"Амино-защитная группа" включает как нециклические, так и циклические защитные группы (Р2 и Р3), например каждая из групп Р2 и Р3 может представлять собой защитную группу, которая сожет быть одинаковой или различной или Р2 и Р3 образуют вместе с N, к которому они присоединены, циклическую защитную группу. Стандартные группы включают, но не ограничиваются следующими, карбаматы, такие как Boc (трет-бутилоксикарбонил, Cbz (карбоксибензил), Fmoc (флуоренилметилоксикарбонил), аллок (аллилоксикарбонил), метил- и этил-карбаматы; тритил, бензил, бензилиден, тозил и т.п.; циклические имидные производные, такие как сукцинимид и фталимид; амиды, такие как формил, (не)замещенный ацетил, и бензоил; и триалкилсилильные группы, такие как t-бутилдиметилсилил и триизопропилсилил. Предпочтительные амино-защитные группы включают Boc, Cbz, Fmoc, бензил, ацетил, бензоил, тритил и т.п.
Термины "активированная" или "активирующая," например, как они используються совместно с каким-либо из терминов "группа", "аминная группа" "карбоксильная группа", "спейсерная группа", относятся к химическому фрагменту, и придают более чувствительную химическую функциональность модификации при определенных условиях, так что активированная химическая функциональность может реагировать при соответствующих условиях со второй химической группой, образуя таким образом ковалентную связь.
Например, активирующая группа может превратить слабую уходящую группу в хорошую уходящую ппу или повысить (или понизить) восприимчивость к нуклеофильной атаке или другим химическим трансформациям.
Соответственно, под "карбоксильной активирующей группой" следует понимать фрагмент, который заменяет водород или гидроксил карбоксильной группы, изменяя таким образом химические и электронные свойства карбоксильной группы, так что карбоксильная группа становится более восприимчивой к нуклеофильной атаке или замещению.
В вариантах осуществления, в которых водород карбоксильной группы заменен, примерные карбоксильные активирующие группы включают, например, алкил, арил, аралкил, гетероарил, гетероциклил, алкилкарбонил, арилкарбонил, аралкилкарбонил, гетероарилкарбонил, гетероциклилкарбонил, С(S)O-арил, С(S)O-алкил, силил или замещенный алкилкарбонил. Примером арилкарбоксильной активирующей группы является пентагалофенил, такие как пентафторфенил, и примером алкилкарбонилкарбоксильной активирующей группы является ацетил или трифторацетил. Карбоксильные активирующие группы могут быть необязательно замещенными. Примером замещенной карбоксильной активирующей группы является замещенный алкилкарбонил, например, карбоксил-замещенный алкилкарбонил, такой как сукцинил (3-карбоксилпропионил).
Карбоксильная активация, где водород -С(=O)-ОН группы заменен, может также включать использование связывающих агентов, которые представляют собой фрагменты, которые способствуют реакциям нуклеофильного присоединения, т.е. заместители, которые имеют суммарный электроноакцепторный эффект на карбонил. Такие группы действуют для поддержки или содействия связывания, или для улучшения скорости связывания, карбоксилатных групп с соединениями, которые имеют реакционную функциональность, например, нуклеофилы, включая аминогруппы, как например в образовании амидо функциональности. Связующие вещества являются хорошо известными специалисту в данной области техники и описаны, например, в Larock, R.С., Comprehensive Organic Transformations, VCH Publishers, Inc., NY (1989), и Carey, F.А., и Sundberg, R.J., Advanced Organic Chemistry, 3rd Edition, Plenum Press, NY (1990), описания каждого из которых включены в данную заявку путем ссылки.
Карбоксильная активация, в которой гидроксильная группа -С(=O)-ОН группы заменена, включает, например, замену гидроксила на фрагмент, такой как галогруппа, такая как фтор, хлор, бром или йод, с получением галогенида карбоновой кислоты, который более восприимчивый к нуклеофильной атаке или замещению.
Таким образом, стандартные активирующие или связывающие группы включают, но не ограничиваются следующими, сложный эфиры и амиды, такие как гидроксибензотриазол, имидазол, нитрофенол, пентахлорфенол, N-гидроксисукцинимид, дициклогексилкарбодиимид, N-гидрокси-N-метоксиамин, и т.п.; ангидриды кислот, такие как ангидрид уксусной, муравьиной, сульфоновой, метансульфоновой, этансульфоновой, бензолсульфоновой, или п-толилсульфоновой кислоты, и т.п.; и галогениды кислот, такие как хлорид, бромид, или йодид кислоты.
Активированное карбонильное соединение получают путем введения в реакцию реактивноспособного фрагмента на выбор с карбонильным соединением, с использованием стандартных методик. Активированное карбонильное соединение можно получить in situ, или их можно обеспечить в выделенной форме, при необходимости. Примерные реактивноспособные фрагменты для получения активированных соединений, процитированных выше, включают соответствующие группы, которые включают изотиоцианат, изоцианат, монохлортриазин, дихлортриазин, моно- или ди-галоген-замещенный пиридин, моно- или ди-галозамещенный диазин, малеимид, азиридин, сульфонилгалогенид, галогенид кислоты, сложный гидроксисукцинимидный эфир, сложный гидроксисульфосукцинимидный эфир, сложный имидоэфир, гидразин, азидонитрофенил, азид, 3-(2-пиридил дитио)проприонамид, глиоксал и альдегид.
Термин "спейсерная" или "спейсерная группа" в соединении с группами P1, Р2, Р3 используется в данной заявке в отношении бивалентной разветвленной или неразветвленной химической группы, которая позволяет связываться соединения в соответствии с изобретением с дополнительным фрагментом, т.е. биоактивной группой в достаточной дистанции для исключения какого-либо нежелательного взаимодействия между соединением и дополнительным фрагментом и/или для уменьшения любой стерической изоляции (вызванной самим соединением или любой другой соседней молекулой), что может влиять на биологическую активность дополнительного фрагмента (как, например, родственное связывание лигандов с их рецептором). В зависимости от предназначенного использования конъюгата эфир-липида и биоактивного лиганда, спейсерные группы могут быть разной длины и могут быть (гидролитически, ферментативно и химически) стабильными или могут включать расщепляемую связь. Расщепляемые связи в соответствии с изобретением могут быть выбраны для расщепления с помощью любой формы химического расщепления, например, химического, ферментного, гидролитического и т.п. Примеры расщепляемых линкеров включают, но не ограничиваются следующими, расщепляемые протеазой пептидные линкеры, чувствительные к нуклеазе линкеры нуклеиновой кислоты, чувствительные к липазе липидные линкеры, чувствительные к гликозидазе карбогидратные линкеры, pH-чувствительные линкеры, чувствительные к гипоксии линкеры, фоторасщепляемые линкеры, термолабильные линкеры, ферментно-расщепляемые линкеры, чувствительные к ультразвуку линкеры, рентгено-расщепляемые линкеры, и т.д.
Группы Р1, Р2, Р3 могут представлять собой независимо друг от друга Н, защитную группу или спейсерную группу. В частности P1 представляет собой Н, а Y-защитную группу или Y-активирующую группу или спейсерную группу S1; Р2 представляет собой Н, амино-защитную группу или спейсерную группу S2; и Р3 представляет собой Н, амино-защитную группу или спейсерную группу S3; или Р2 и Р3 образуют вместе с N, к которому они присоединены, кольцевую структуру.
Следует понимать, что спейсеры могут представлять или могут не представлять собой концевую группу, активированную для создания возможности связывания спейсер-модифицированного соединения в соответствии с изобретением с дополнительным фрагментом, таким как биоактивная группа.
В специфических вариантах осуществления, "спейсерная группа" (также называемые группы S1, S2, S3) представляет собой короткую спейсерную группу или длинно-цепочечную спейсерную группу, выбранную из алкиленовой цепи, которая необязательно содержит одну или несколько групп, выбранных из кетона, сложного эфира, эфира, амино, амида, амидина, имидина, карбаматных или тиокарбаматных функций, глицерина, мочевины, тиомочевины, двойных связей или ароматического кольца.
В частности, короткая спейсерная группа (или группы S1, S2, S3) может быть выбрана из (С1-С12)алкила, (С2-С12)алкенила, арила, аралкила, гетероарила.
Длинноцепочечная спейсерная группа (или группы S1, S2, S3) может быть выбрана из полимерных радикалов формулы -W-(CH2-)k-W'-, где k представляет собой целое число между 13 и 3000, и W и W' представляют собой реакционноспособные группы, способные реагировать с амино, карбоксильной, гидрокси или тио группами и где одна или несколько несмежных СН2 групп могут независимо быть заменены на арил, гетероарил, -СН=СН-, -С≡С-, или гидрофильную (или полярную) группу, выбранную из -О-, -СО-, -СО-O-, -O-СО-, -NR'-, -NR'-CO-, -CO-NR'-, -NR'-CO-O-, -O-CO-NR'-, -NR'-CO-NR'-, и -O-CO-O-, где R' представляет собой водород или (С1-С12)алкил. Следует понимать, что замена более одной несмежной СН2 группы на ту же группу, может давать полимерную цепь со специфическим повторяющимся звеном (например, сложный полиэфир, полиэфир, полиимид, и т.д.).
Предпочтительные спейсерные группы включают гидрофильные полимерные радикалы (с повышенной аффинностью для водных растворов), т.е. полимеры, которые содержат повторяющиеся структурные звенья, которые включают одну или несколько вышеуказанных гидрофильных (или полярных) групп в их алкиленовом скелете. Типичные примеры гидрофильных полимерных радикалов включают полиокси(С2-С3)алкилены (например, полиэтиленгликоль (PEG) или полипропиленгликоль (PPG)), полисахариды (например, декстран, пуллулан, хитозан, гиалуроновая кислота), полиамиды (например, полиаминокислоты, полусинтетические пептиды и полинуклеотиды); полисиаловая кислота, сложный полиэфиры (например, полилактид (PLA), полилактид-со-гликолид (PLGA)), поликарбонаты, полиэтиленимины (PEI), полиимиды, поливинилацетат (PVA).
Предпочтительным спейсером является "PEG" или "полиэтиленгликоль", который охватывает любой растворимый в воде поли(этиленоксид). Обычно, "PEG" означает полимер, который содержит большинство, например, >50%, подзвеньев, которые представляют собой -СН2СН2О-. Разные формы PEG могут отличаться молекулярной массой, структурой или конфигурацией (например, разветвленные, линейные, раздвоенные PEGs, мультифункциональные, и т.п.). PEGs для применения в настоящем изобретении могут предпочтительно включать одну из двух следующих структур: "-O(CH2CH2O)m-" или "-CH2CH2O(CH2CH2O)m-СН2СН2-," где m представляет собой от 3 до 3000, и терминальные группы и структура общего PEG может меняться. Как указано выше, в зависимости от применения, PEG может быть в эндкепированной форме. Когда PEG определен как "-O(CH2CH2O)m-" эндкепированная группа представляет собой обычно углерод-содержащую группу, которая обычно состоит из 1-20 углеродов и представляет собой предпочтительно алкил (например, метил, этил или бензил) несмотря на свою насыщенную и ненасыщенную формы, а также арил, гетероарил, циклил, гетероциклил, и замещенные формы любого из вышеуказанных также предусмотрены. Когда PEG определен как "-CH2CH2O(CH2CH2O)m-СН2СН2-", эндкепированная группа представляет собой обычно углерод-содержащую группу, которая обычно состоит из 1-20 атомов углерода и атома кислорода, который ковалентно связан с группой и доступен для ковалентного связывания с одним концом PEG. В этом случае, группа представляет собой обычно алкокси (например, метокси, этокси или бензилокси) и в отношении углерод-содержащей группы может необязательно быть насыщенной и ненасыщенной, а также арил, гетероарил, циклил, гетероциклил, и замещенный формы любого из вышеуказанных. Другой ("неэндкепированные") конец представляет собой обычно гидроксил, амин или активированную группу, которую можно подвергнуть дополнительной химической модификации, когда PEG определен как "-CH2CH2O(СН2СН2О)m-СН2СН2-" дополнительно, эндкепированная группа может также представлять собой силан.
Обзор получения различных функционализированных или активированный PEG концевой группы известен в уровне техники (см. например Zalipsky S., Bioconjug. Chem., 6, 150-165 (1995)).
В предпочтительных вариантах осуществления изобретение относится к соединениям следующих формул V, VI и VII:



где
Y представляет собой О, N, S или ковалентную связь,
P1 представляет собой Н, Y-защитную группу или Y-активирующую группу или спейсерную группу,
Р2, Р3 представляют собой независимо друг от друга Н, амино-защитную группу или спейсерную группу, или Р2 и Р3 образуют вместе с N, к которому они присоединены, кольцевую структуру,
p1, q1, р2, q2, р3, q3 представляют собой независимо друг от друга от 1 до 23, при условии, что сумма p1 и q1, р2 и q2, р3 и q3 составляет от 12 до 24.
В дополнительных аспектах настоящее изобретение относится к способу получения соединения в соответствии с изобретением.
Соединения в соответствии с изобретением являются особенно пригодными для применения для получения везикулярных композиций, таких как липосомы, мицеллы и (липид-покрытые) наночастицы.
Таким образом, в другом аспекте настоящее изобретение относится к везикулярным композициям, которые составлены из по меньшей мере одного соединения в соответствии с изобретением. Такие везикулы включают недериватизированные соединения или дериватизированные соединения, которые содержат спейсерную группу или их смеси. Необязательно везикулярные композиции могут содержать один или несколько других везикулообразующих липидов.
В одном из вариантов осуществления везикула может содержать липид-спейсерные производные в соответствии с изобретением и другие везикулообразующие липиды (со-липиды), предпочтительно в соотношении от 1:200 до 200:1.
Как будет очевидно специалисту в данной области техники, в рамках настоящего изобретения, везикулярные композиции в форме липид-покрытых наночастиц, липосом, мицелл, или других везикул, могут быть легко приготовлены из соединений в соответствии с изобретением с использованием стандартных условий, известных в уровне техники.
В зависимости от желаемых физицеских свойств, везикулярные композиции можно приготовить из соединений в соответствии с изобретением необязательно в комбинации с одним или несколькими солипидами включая стабилизирующие липиды. Особенно стабилизирующие соединения, которые в конечном счете объединенные с настоящими соединениями могут быть выбраны как желательные для оптимизации свойств полученных в результате композиций (и являются быстро опознаваемыми специалистом в данной области техники без чрезмерного экспериментирования).
Везикулярные композиции в соответствии с изобретением являются особенно эффективными в качестве носителей для доставки биоактивных агентов или в качестве антиген-представляющих носителей.
Термин "биоактивный агент", как используется в данной заявке, относится к любому искусственному или природному соединению (в свободной форме, в форме соли или сольватированной или гидратированной форме), имеющему биологическую активность, такому как целевой агент, антигенный агент, терапевтический агент или диагностический агент, предпочтительно терапевтический агент или диагностический агент.
Термин "антиген-представляющая система" (также называемая "система индикации антител"), как используется в данной заявке, относится к природной или искусственной системе, которая (i) может представлять по меньшей мере один антиген (или его часть) таким образом, что по меньшей мере один антиген (или его часть) может быть опознан или связан иммуно-эффекторной молекулой, например, Т-клеточным рецептором с антигеном на поверхности Т-клетки, или (ii) способна представлять по меньшей мере один антиген (или его часть) в форме антиген-МНС комплекса, распознаваемого специфическими эффекторными клетками иммунной системы, и таким образом индуцируя эффективный клеточный иммунный ответ против антигена (или его часть), который представляется.
Мицеллярные везикулярные композиции в соответствии с изобретением можно получить, используя один из множества обычных мицеллярных способов получения, которые будут очевидными для специалиста в данной облисти техники. В этих способах обычно используют суспензию липидных соединений в органическом растворителе, упаривание растворителя, повторное суспендирование в водной среде, обработку ультразвуком и центрифугирование. Вышеуказанные способы, а также другие, рассматриваются, например, в Canfield et al., Methods in Enzymology, Vol. 189, pp. 418-422 (1990); El-Gorab et al, Biochem. Biophys. Acta, Vol. 306, pp. 58-66 (1973); Colloidal Surfactant, Shinoda, et al, Academic Press, N.Y. (1963) (особенно "The Formation of Micelles", Shinoda, Chapter 1, pp. 1-88); Catalysis in Мицеллярные and Macromolecular Systems, Fendler and Fendler, Academic Press, N.Y. (1975). Описания каждой из вышеприведенных публикаций в ключены в данную заявку путем ссылки.
Необязательные стабилизирующие вещества, которые объединяют с соединениями в соответствии с изобретением для стабилизации мицеллярных композиций, которые из них получают, включают лаурилтриметиламмония бромид, цетилтриметиламмония бромид, миристилтриметиламмония бромид, (С12-С16)алкилдиметилбензиламмония хлорид, цетилпиридиния бромид и хлорид, лаурил сульфат, и т.п.. Другие вещества для стабилизации мицеллярных композиций, в дополнение к продемонстрированным выше, будут очевидными для специалиста в данной области техники на основании настоящего описания.
Липосомные везикулярные композиции могут включать одно или несколько недериватизированных соединений и/или одно или несколько дериватизированных соединений (несущих спейсерную группу) необязательно в комбинации с одним или несколькими дополнительными со-липидами и/или одним или несколькими стабилизирующими соединениями. Настоящее(ие) соединение(я) (необязательно в комбинации с солипидами) могут быть в форме монослоя или бислоя. В случае более одного моно- или бислоя, моно- или бислои обычно концентрические. Таким образом, нистоящие соединения (и необязательно солипиды) могут использоваться для образования однослойной липосомы (состоящей из одного монослоя или бислоя), олиголамеллярной липосомы (состоящей из двух или трех монослоев или бислоев) или многослойной липосомы (состоящей из более чем трех монослоев или бислоев).
(Со-)Липиды, которые могут быть использованы в комбинации с настоящими соединениями и в образовании липосомных везикулярных композиций в соответствии с изобретением включают предпочтительно катионные липиды, фосфатидилхолиновые (PC), фосфатидил-DL-глицерин (PG), L-α-фосфотидилэтаноламин (РЕ), холестерин, холестерил гемисукцинат три соль (CHEMS), 1,2-диолеоил-3-триметиламмоний-пропан (DOTAP).
Другие вещества для использования в получении липосомных везикулярных композиций в соответствии с изобретением, в дополнение к вышеуказанным, будут очевидны специалисту в данной области техники на основании настоящего описания.
Количество стабилизирующих веществ, таких как, например, дополнительного амфипатического соединения, которое объединено с настоящими соединениями может варьироваться в зависимости от ряда факторов, включая специфическую структуру выбранного (ых) настоящего(их) соединения(й) в соответствии с изобретением, выбранные специфические стабилизирующие вещества, определенное использование для которых было выбрано, способ доставки, и т.п.. Количество стабилизирующего вещества для объединения с настощими соединениями и соотношение стабилизирующего вещества к настоящему соединению, будет варьировать и легко определяется специалистом в данной области техники на основании настоящего описания. Обычные соотношения, которые являются выше, чем приблизительно 4:1, 3:1 или 2:1, настоящего соединения к стабилизирующему липиду, являются предпочтительными.
Выбор пригодных со-липидов и стабилизирующих соединений для получения липосомных везикулярных композиций в соответствии с изобретением является очевидным для специалиста в данной области техники и его можно достигнуть без дополнительных лишних экспериментирований, на основании настоящего описания.
Широкое разнообразие способов является доступным в связи с получением липосомных везикулярных композиций в соответствии с изобретением. Соответственно, липосомы можно получить с использованием любой одной из ряда обычных методик получения липосом, которая будет очевидна специалисту в данной области техники. Эти методики включают инъекцию этанола, тонкопленочную технологию, гомогенизацию, диализ растворителя, насильственную гидратацию, упаривание обратной фазы, микроэмульгацию и метод простого замораживания - оттаивания, с применением, например, обычного оборудования для микроэмульгации. Дополнительные способы получения липосомных везикулярных композиций в соответствии с изобретением из соединений в соответствии с настоящим изобретением включают, например, обработку ультразвуком, хелатный диализ, гомогенизацию, инфузия растворителя, спонтанное образование, упаривание растворителя, контролируемый детергентный диализ, и другие, каждый из которых включает получение липосом различным образом. Обычно, способы, которые включают этанольную инъекцию, тонкопленочную технологию, гомогенизацию и экструзию являются предпочтительными в отношении получения липосомных композиций в соответствии с изобретением из соединений в соответствии с настоящим изобретением.
Размер липосом можно устанавливать, при желании, с помощью различных технологий, включая экструзию, фильтрацию, обработку ультразвуком и гомогенизацию. Другие способы для установления размера липосом и для модулирования полученного в результате липосомного биораспределения и клиренса липосом будет очевидным для специалиста в данной области техники на основании настоящего описания. Предпочтительно, размер липосом устанавливают путем экструзии под давлением через поры определенного размера. Липосомные композиции в соответствии с изобретением могут быть любого размера, предпочтительно менее чем приблизительно 200 нанометров (нм) во внешнем диаметре.
Везикулярная композиции в форме наночастиц или наночастицы обычно представляют собой маленькие частицы, имеющие типично диаметр менее, чем 1 микрон, предпочтительно в диапазоне приблизительно 25-1000 нм, более предпочтительно в диапазоне приблизительно 50-300 нм, наиболее предпочтительно в диапазоне приблизительно 60-200 нм. Наночастица может иметь любую форму и любое строение. Примеры наночастиц включают нанопорошки, нанокластеры, нанокристаллы, наносферы, нановолокна, и другие конфигурации. Нанополимер относится к полимеру, который при полимеризации собирается в форму наночастицы, такой как, например, наностержень, нановолокно, или наносфера. Наносфера относится к типу наночастицы, которая практически шаровидной формы и может иметь полое ядр или твердое ядро.
В одном из вариантов осуществления, наночастицы имеют структуру ядра матрицы, которая может быть образована с применением всех типов веществ и структур, включая неорганические вещества, такие как металлы, и органические вещества, такие как полимеры, включая физиологически приемлемые полимеры. Неограничивающие примеры таких полимеров включают, например, сложные полиэфиры (такие как поли(молочная кислота), поли(L-лизин), поли(гликолевая кислота) и поли(молочная-со-гликолевая кислота)), поли(молочная кислота-со-лизин), поли(молочная кислота-графт-лизин), полиангидриды (такие как поли(димер жирной кислоты), поли(фумаровая кислота), поли(себациновая кислота), поли(карбоксифеноксипропан), поли(карбоксифеноксигексан), сополимеры этих мономеров и т.п.), поли(ангидрид-со-имиды), поли(амиды), поли(сложный ортоэфиры), поли(иминокарбонаты), поли(уретаны), поли(органофасфазены), поли(фосфаты), поли(этиленвинилацетат) и другие ацил-замещенные ацетаты целлюлозы и их производные, поли(капролактон), поли(карбонаты), поли(аминокислоты), поли(акрилаты), полиацетали, поли(цианоакрилаты), поли(стиролы), поли(винилхлорид), поливинилфторид), поливинил имидазол), хлорсульфированные полиолефины, полиэтиленоксид, сополимеры, полистирол, и их смеси или со-полимеры. Наночастицы также могут включать гидроксипропилцеллюлозу (НРС), N-изопропилакриламид (NIPA), полиэтиленгликоль, поливиниловый спирт (PVA), полиэтиленимин, хитозан, хитин, декстрансульфат, гепарин, хондроитинсульфат, желатин, и т.д. а также их производные, со-полимеры, и их смеси. Не ограничивающий способ создания наночастиц описан, например, в U.S. Publication 2003/0138490. В другом варианте осуществления вещество ядра может быть выбранно из металлов, сплавов, металлоидов, металлов-соединений, таких как металлы-оксиды, неорганических соединений, и веществ на основании углерода, в особенности, углеродных нанотрубок, одномерных наночастиц фуллерена C60, и трехмерных наночастиц фуллерена С70.
Подходящие примеры металлов включают, но не ограничиваются следующими, благородные или платиновые металлы, такие как Ag, Au, Pd, Pt, Rh, Ir, Ru, и Os, переходные металлы, такие как Ti, Cr, Mn, Fe, Co, Ni, Cu, Zn, Zr, Nb, Mo, Та, W, Re, и основную группу металлов, таких как Al, Ga, In, Si, Ge, Sn, Sb, Bi, Те. Было бы желательно, чтобы некоторые металлы основной группы, в частности Si и Ge, также обычно относились к металлоидам. Подходящие примеры сплавов включают, но не ограничиваются следующими, сплавы благородные или платиновые металлов и переходных металлов, в частности сплавы серебра и переходных металлов, таких как Ag/Ni, Ag/Cu, Ag/Co, и платиновых и переходных металлов, таких как Pt/Cu, или сплавы благородных или платиновых, таких как Ru/Pt. Неограничивающие примеры неорганических соединений включают, но не ограничиваются следующими, SiO2, металл-соединения, в частности металлы-оксиды, такие как TiO2 и оксиды железа.
Специалисту в данной области техники будет известно, что выбор вещества зависит от предназначенного использования наночастицы.
Наночастицы необязательно включают функциональную группу, такую как, например, карбоксильную, сульфгидрильную, гидроксильную, или аминогруппу, для связывания ковалентно других соединений, таких как линкеры, с поверхностью наночастицы. В других вариантах осуществления соединения, такие как линкеры, могут быть связанны с наночастицей посредством других межмолекулярных сил, таких как силы Ван-дер-Ваальса, ионные взаимодействия, гидрофобные взаимодействия.
В отдельных вариантах осуществления, наночастицы могут быть связаны с биоактивным агентом (например, вовлеченным, вставленным, встроенным, инкапсулированным, связанным с поверхностью, или связанным еще каким то образом с наночастицей). Предпочтительно такой биоактивный агент связан с наночастицей через соединение в соответствии с изобретением, которое выполняет роль линкера между биоактивным агентом и наночастицей. Эти аспекты настоящих соединений и композиций из них являются частью параллельно подаваемой международной заявки, которая полностью включена в данную заявку.
Наночастицы могут также быть сгрупированы вместе (необязательно с диспергирующим агентом) с образованием нанокластера. Независимое формулирование каждого типа наночастицы перед образованием кластера и специальное расположение наночастиц в кластере может позволить контролировать длительность и концентрацию биоактивного ингредиента.
В одном из вариантов осуществления в соответствии с настоящим изобретением, одно или несколько недериватизированных или дериватизированных соединений в соответствии с изобретением могут быть включены, присоединены к или адсорбированы наночастицей. Предпочтительно, покрытые липидами наночастицы (LCN) могут образовываться из наноразмерных частиц ядра и одного или нескольких соединений в соответствии с настоящим изобретением и необязательно одного или нескольких со-липидов. В любой покрытой липидами наночастице, липиды могут быть в форме монослоя или бислоя. В случае более одного моно- или бислоя, моно- или бислои обычно являются концентрическими. Покрытие наночастиц предпочтительно осуществляют в растворе, который содержит соединения в соответствии с изобретением и давая достаточно временя для того, чтобы соединения покрыли наночастицы (используя методики, известные в уровне техники, см. например, Journal of Controlled Release, Vol 137(1), 69-77, 2009). В любой приведенной покрытой липидами наночастице, липиды могут быть в форме монослоя или бислоя. В случае наличия более одного моно- или бислоя, моно- или бислои обычно являются концентрическими.
Различные способы можно использовать для изготовления наночастиц подходящего размера. Эти способы включают способы упаривания (например, свободное расширение потока, лазерное упаривание, электроэрозия, электровзрывание и химическое газофазное осаждение), физические способы, включающие механическое трение (например, технологий «жемчужного» перетирания, Elan Nanosystems, Ireland), и межфазное смещение с последующим перемещением растворителя.
Как будет понятно специалисту в данной области техники, любые из заявленных соединений и везикулярных композиций, содержащих соединения в соответствии с изобретением, с или без биоактивных агентов, могут быть лиофилизированы для хранения, и воспроизведены, например, в водной среде (такой как стерильная вода или фосфано-буферизированный раствор, или водный селиновый раствор), Предпочтительно, при энергичном перемешивании. При необходимости, могут быть включены добавки для предотвращения слипания или слияния липидов в результате лиофилизации. Пригодные добавки включают, без ограничения, сорбитол, маннитол, хлорид натрия, глюкозу, трегалозу, поливинилпирролидон и поли(этиленгликоль), например, PEG 400.
Как указано выше, настоящие соединения и в частности липосомные композиции в соответствии с настоящим изобретением являются особенно пригодными для применения в качестве носителей для целевой доставки биоактивных агентов, или для применения в качестве системы индикации антител. Таким образом, соединения в соответствии с настоящим изобретением являются особенно применимыми для использования in vitro и/или in vivo в способах лечения болезней, для которых является желаемой или необходимой целевая доставка одного или нескольких специфических биологически активных агентов, а также для использования в способах диагностического применения in vitro/in vivo. Эти аспекты настоящих соединений и композиций из них являются частью параллельно подаваемой международной заявки, которая полностью включена в данную заявку.
В дополнительном аспекте, настоящее изобретение относится к набору, который состоит из контейнера, который делится на отделения для удержания различных элементов набора. Одно отделение может содержать предопределенное количество либо соединения в соответствии с настоящим изобретением или составленную из них везикулярную композицию. В случае везикулярных композиций, может присутствовать или нет pH буфер для установления значения pH композиции на физиологический диапазон от приблизительно 7 до приблизительно 8, или также в лиофилизированной или высушенной замораживанием форме для восстановления на время применения. Также в набор включены другие реагенты и инструкция по применению.
Настоящее изобретение дополнительно описано в следующих примерах.
ПРИМЕРЫ
Вещества: Холестерин и РОРС закупают у Avanti Polar Lipids (Alabaster, AL). Все защищенные аминокислоты приобретают у Novabiochem. Дифенилдиазометановую смолу D-2230 приобретают у Bachem AG. Все другие химикаты и растворители являются чда или выше.
2,3-Бис(тетрадецилокси)пропан-1-амин синтезируют в соответствии с Kokotos et al. Chemistry-A European Journal, 2000, vol. 6, #22, 4211-4217. Аналогичным образом получают бис(3-((Z)-октадец-9-енилокси)пропил)амин из олеил метансульфоната и бис(3-гидроксипропил)амина (см. MaGee et al., J. Journal of Organic Chemistry, 2000, vol. 65, #24, 8367-8371).
Пример 1: Синтез (2S)-2-(((9Н-флуорен-9-ил)метокси)карбониламино)-глютаминовая кислота-α-трет-бутиловый эфир-γ-2,3-бис(тетрадецилокси)пропил-амида

15 г Fmoc-Glu(OSu)OtBu ((2S)-Nα-(9-флуоренилметилоксикарбонил)-глютаминовая кислота-α-трет-бутиловый эфир-γ-N-гидроксисукцинимидный эфир) растворяют в дихлорметане при комнатной температуре. После добавления 15.3 г 2,3-бис(тетрадецилокси)пропан-1-амина, смесь перемешивают в течение 17 часов и упаривают досуха. Остаток растворяют в минимальном количестве дихлорметана и очищают с помощью колоночной хроматографии с использованием SiO2 в качестве твердой фазы и смеси метил-трет-бутиловый эфир/гексан/7:3 в качестве элюента. После упаривания фракций продукта получают 25.5 г (2S)-2-(((9Н-флуорен-9-ил)метокси)карбониламино)-глютаминовая кислота-α-трет-бутиловый эфир-γ-2,3-бис(тетрадецилокси)пропил-амида в виде бесцветного твердого вещества. 1Н-ЯМР в CDCl3 (ТМС в качестве внутреннего стандарта), химический сдвиг в м.д.: 7.76 (d, 2Н, Fmoc), 7.61 (d, 2Н, Fmoc), 7.25-7.43 (m, 4Н, Fmoc), 6.13 (bs, NH, 1H), 5.60 (bs, NH, 1H), 4.39, 4.18-4.25 (d и m, 4H), 3.21-3.62 (m, 9H), 1.97-2.23 (m, 4 H), 1.51-1.60 (m, 4H), 1.47 (s, 9 H), 1.25 (m, 44H, CH2), 0.84-0.91 (m, 6H, 2x алкил-СН3).
Пример 2: Синтез (2S)-2-(((9Н-флуорен-9-ил)метокси)карбониламино)-глютаминовая кислота-γ-2,3-бис(тетрадецилокси)пропил-амида

4.6 г (5.1 ммоль) (2S)-2-(((9Н-флуорен-9-ил)метокси)карбониламино)-глютаминовая кислота-α-трет-бутиловый эфир-γ-2,3-бис(тетрадецилокси)пропил-амида растворяют в 25 мл дихлорметана в 100 мл колбе и обрабатывают 25 мл трифторуксусной кислоты. Через 1 ч сложноэфирную группу полностью расщепляют и раствор выливают в 50 мл холодной воды. Органический слой экстрагируют, промывают водой до достижения нейтрального pH и сушат над Na2SO4. Органический слой отфильтровывают и растворитель упаривают с получением 4.2 г желаемого продукта (5.0 ммоль, выход 98%, ТСХ: MtBE/гексан 7:3; Rf=0.43.)
Пример 3: Синтез (2S)-глютаминовая кислота-γ-(2,3-бис(тетрадецилокси)пропил)амида

5 г (2S)-2-(((9Н-флуорен-9-ил)метокси)карбониламино)-глютаминовая кислота-α-трет-бутиловый эфир-γ-2,3-бис(тетрадецилокси)пропил-амида добавляют к 85 мл N,N-диметилформамида. К смеси добавляют 2.6 мл пиперидина. Смесь перемешивают в течение трех часов при комнатной температуре и затем упаривают досуха в вакууме с получением 5.2 г (2S)-глютаминовая кислота-γ-(2,3-бис(тетрадецилокси)пропил)амида в виде бесцветного твердого вещества, которое можно использовать для получения липидных везикул или для предварительной дериватизации с помощью активного агента или спейсерной группы.
Пример 4: Синтез (R)-2-амино-N1-(2-(4-метоксибензамидо)этил)-N4,N4-бис(3-((Z)-октадец-9-енилокси)пропил)сукцинамида
(а) Синтез N-(2-аминоэтил)-4-метоксибензамида

3.0 г 4-Метоксибензоилхлорида добавляют к 30 мл 1,2-диаминоэтана в дихлорметане при -78°С и затем позволяют нагреться до 23°С. Обработка водным раствором кислота-основание и упаривание досуха в вакууме дает 1.65 г N-(2-аминоэтил)-4-метоксибензамида в виде бледножелтого масла. 1Н-ЯМР в CDCl3 (ТМС в качестве внутреннего стандарта), химический сдвиг в м.д.: 8.53 (t, 1H, NH), 7.91 (d, 2Н, Benz), 6.99 (d, 2Н, Benz), 4.75 (bs, 2Н, NH2), 3.81 (s, 3Н, СН3), 3.39, (dd, 2Н, СН2), 2.82 (t, 2Н, СН2).
(b) Синтез (R)-трет-бутил 3-(((9Н-флуорен-9-ил)метокси)карбониламино)-4-(2-(4-метоксибензамидо)этиламино)-4-оксобутаноат

3.0 г 2 N-(2-аминоэтил)-4-метоксибензамида (полученного на стадии (а)) и 1.70 мл N-метилморфолина в ДМФА (0°С) добавляют к раствору 6.35 г Fmoc-Asp(OtBu)-OH, 1.70 мл N-метилморфолина и 2.00 мл изобутилхлорформиата в этилацетате (-12°С) и перемешивают в течение 3 ч пока позволяют нагреться до 23°С. Разбавление полученной суспензии этилацетатом, с последующей обработкой водным раствором кислота-основание и упаривание досуха в вакууме дает 9.55 г (R)-трет-бутил 3-(((9Н-флуорен-9-ил)метокси)карбониламино)-4-(2-(4-метоксибензамидо)этиламино)-4-оксобутаноата. Это сырое вещество суспендируют в изопропиловом эфире в течение 23 я, затем отфильтровывают и сушат для получения 4.47 г (R)-трет-бутил 3-(((9Н-флуорен-9-ил)метокси)карбониламино)-4-(2-(4-метоксибензамидо)этиламино)-4-оксобутаноата в виде белых кристаллов. 1Н-ЯМР в CDCl3 (ТМС в качестве внутреннего стандарта), химический сдвиг в м.д.: 8.28 (t, 1Н, NH), 8.07 (t, 1H, NH), 7.89 (d, 2Н, Fmoc), 7.81 (d, 2Н, Benz), 7.71-7.60 (m, 2Н, Fmoc и 1Н, NH), 7.46-7.27 (m, 4H, Fmoc), 6.96 (d, 2H, Benz), 4.35-4.20 (m, 3H, Fmoc, и 1H CH), 3.78 (s, 3H, CH3), 3.40-3.20, (m, 4H, 2×CH2), 2.69 (dd, 1H, CH2), 2.46 (dd, 1H, CH2), 1.37 (s, 9H, 3×CH3).
(с) Синтез (R)-3-(((9Н-флуорен-9-ил)метокси)карбониламино)-4-(2-(4-метоксибензамидо)этиламино)-4-оксобутановой кислоты - натрия ацетата

30.0 мл трифторуксусной кислоты добавляют к 3.0 г (R)-трет-бутил 3-(((9Н-флуорен-9-ил)метокси)карбониламино)-4-(2-(4-метоксибензамидо)этиламино)-4-оксобутаноата (полученного на стадии (b)) в дихлорметане при 23°C. После завершения реакции добавляют водн. NaHCO3 для получения белого осадка, который промывают дихлорметаном и сушат с получением 2.55 г (R)-3-(((9H-флуорен-9-ил)метокси)карбониламино)-4-(2-(4-метоксибензамидо)этиламино)-4-оксобутановой кислоты - натрия ацетата в виде белого порошка. 1Н-ЯМР в SO(CD3)/CD3OD, 1:1, (ТМС в качестве внутреннего стандарта), химический сдвиг в м.д.: 7.85-7.79 (m, 2Н, Fmoc и 2Н, Benz), 7.68 (d, 2Н, Fmoc), 7.45-7.29 (m, 4Н, Fmoc), 6.93 (d, 2Н, Benz), 4.51-4.17 (m, 3Н, Fmoc и 1Н, СН), 3.78 (s, 3Н, СН3), 3.47-3.34, (m, 4Н, 2×СН2), 2.82 (dd, 1Н, СН2), 2.63 (dd, 1H, СН2).
(d) Синтез (9Н-флуорен-9-ил)метил (R,Z)-1-(4-метоксифенил)-10-(3-((2)-октадец-9-енилокси)пропил)-1,6,9-триоксо-14-окса-2,5,10-триазадотриаконт-23-ен-7-ил карбамата

0.48 г (R)-3-(((9Н-флуорен-9-ил)метокси)карбониламино)-4-(2-(4-метоксибензамидо)этиламино)-4-оксобутановой кислоты - натрия ацетата (полученного на стадии (с)) в диметилформамиде охлаждают до 10°С и затем 0.46 г бис(3-((2)-октадец-9-енилокси)пропил)амина, после добавляют 0.37 г COMU и 0.20 г DIPEA. После перемешивания при 23°С в течение 20 ч раствор фильтруют через набивку Alox и промывают небольшим количеством диметилформамида. Фильтрат разбавляют этилацетатом, промывают водой и упаривание досуха в вакууме дает 1.12 г оранжевого масла, которое очищают с помощью колоночной хроматографии с получением 0.41 г (9Н-флуорен-9-ил)метил (R,Z)-1-(4-метоксифенил)-10-(3-((2Z)-октадец-9-енилокси)пропил)-1,6,9-триоксо-14-окса-2,5,10-триазадотриаконт-23-ен-7-ил-карбамата. 1Н-ЯМР в CDCl3 (ТМС в качестве внутреннего стандарта), химический сдвиг в м.д.: 7.86 (d, 2Н, Benz), 7.69 (d, 2Н, Fmoc), 7.55 (d, 2Н, Fmoc), 7.42-7.23 (m, 4H, Fmoc и 1H, NH), 6.88 (d, 2H, Benz и 1H, NH), 6.12 (bd, 1H, NH), 5.41-5.26 (m, 4H, 4×CH), 4.60-4.33 (m, 3H, Fmoc), 4.17 (t, 1H, CH), 3.82 (s, 3H, CH3), 3.62-3.23, (m, 16H, 8×CH2 и 1H, CH2), 2.73 (dd, 1H, CH2), 2.05-1.95 (m, 8H, 4×CH2), 1.85-1.65 (m, 4H, 2×CH2), 1.57-1.45 (m, 4H, 2×CH2), 1.24 (bs, 44H, 22×CH2), 0.88 (t, 6H, 2×CH3).
(e) Синтез (R)-2-амино-N1-(2-(4-метоксибензамидо)этил)-N4,N4-бис(3-((Z)-октадец-9-енилокси)пропил)сукцинамида

0.75 г диэтиламина добавляют к 2.12 г (9Н-флуорен-9-ил)метил (R,Z)-l-(4-метоксифенил)-10-(3-((Z)-октадец-9-енилокси)пропил)-1,6,9-триоксо-14-окса-2,5,10-триазадотриаконт-23-ен-7-ил-карбамата (полученного на стадии (d)) в дихлорэтане, перемешивают в течение 26 ч с последующим упариванием досуха в вакууме с получением 1.90 г сырого вещества, которое очищают с помощью адсорбции 20 г Dowex Monosphere и последующей десорбции аммиаком в этаноле с получением 1.09 г (R)-2-амино-N1-(2-(4-метоксибензамидо)этил)-N4,N4-бис(3-((Z)-октадец-9-енилокси)пропил)сукцинамида. 1Н-ЯМР в CDCl3 (ТМС в качестве внутреннего стандарта), химический сдвиг в м.д.: 7.88 (d, 2Н, Benz и 1Н, NH), 7.64 (t, 1Н, NH), 6.89 (d, 2Н, Benz), 5.42-5.26 (m, 4Н, 4×СН), 3.82 (s, 3Н, СН3), 3.65-3.49, (m, 4Н, 2×СН2), 3.42-3.28 (m, 12Н, 6×СН2 и 1H, СН), 2.99 (dd, 1Н, СН2), 2.71 (dd, 1H, СН2), 2.10-1.92 (m, 8Н, 4×СН2 и 2Н, NH2), 1.85-1.67 (m, 4Н, 2×СН2), 1.60-1.47 (m, 4Н, 2×СН2), 1.28 (bs, 44Н, 22×СН2), 0.90 (t, 6Н, 2×СН3). MS: 947.9 [M+Na]+.
Пример 5: Синтез (41S)-1-амино-41-(3-((2,3-бис(тетрадецилокси)пропил)амино)-3-оксопропил)-39-оксо-3,6,9,12,15,18,21,24,27,30,33,36-додекаокса-40-азадотетраконтан-42-овой кислоты

(а) Синтез Fmoc-Glu(DMA)-OtBu смолы:
3.85 г дифенилдиазометановой смолы (3.3 ммоль) дважды промывают 30 мл ДХМ в 100 мл SPPS-реакторе и обрабатывают раствором 4.2 г 2S)-2-(((9H-флуорен-9-ил)метокси)карбониламино)-глютаминовая кислота-γ-2,3-бис(тетрадецилокси)пропил-амида (см. пример 2, 1.5 экв., 5.0 ммоль) в 30 мл ДХМ в течение ночи. Раствор отфильтровывают и смолу промывают ДХМ четыре раза. Для разрушения в конечном итоге непрореагировавшего дифенилдиазометана, смолу обрабатывают 125 мкл уксусной кислоты (0.5 экв., 2.2 ммоль) в 30 мл ДХМ в течение 15 минут и в последствии трижды промывают попеременно 30 мл диметил формами да и изопропанлом. Смолу дважды промывают диизопропиловым эфиром и сушат в течение ночи в вакууме. Получают 6.7 г желаемого продукта (>100% от теоретического, теоретический выход 6.5 г). Загрузку смолы устанавливают до уровня 0.49 ммоль/г путем УФ-измерения содержания продукта отщепления Fmoc при 304 нм (максимальная загрузка теоретически составляет 0.51 ммоль/г).
(б) Синтез H-Glu-OtBu-NH-PEG11-Glu(DMA)-дифенилметиловой смолы:
H-Glu-OtBu-NH-PEG11-Glu(DMA)-дифенилметиловую смолу получают посредством обычного твердофазного синтеза со следующей последовательностью реакций:
1) расщепление Fmoc-группы от смолы Fmoc-Glu(DMA)-OtBu пиперидином в ДМФА,
(2) конденсация Fmoc-NH-PEG11-СООН с использованием HTBU в ДМФА и DIPEA,
(3) расщепление Fmoc-группы от смолы Fmoc-NH-PEG11-Glu(DMA)-OtBu пиперидином в ДМФА,
(в) Расщепление и снятие защиты с H-Glu-OtBu-NH-PEG1l-Glu(DMA)-дифенилметильной смолы:
Желаемое соединение можно получить путем расщепления от смолы, например, обработкой трифторуксусной кислотой и триизопропилсиланом.
Пример 6: Получение анисамид-отделанных липосом
470 мг РОРС, 60 мг Chol и 13.5 мг анисамид-липида (см. пример 4) растворяют в 750 мкл этанола (96%) при 55°С и инъецируют в 4.25 мл PBS pH 7.4. Молярное соотношение используемых липидов составляет 77.99:18.83:1.02:0.27. После экструзии через 100 нм поликарбонатную мембрану липосомы имеют средний размер 110 нм с PDI 0.068. В соответствии с анализом ВЭЖХ содержание анисамид-липида составляет 72% от теоретического значения.
Пример 7: Синтез NH2-PEG8-PA-Glu(DMA)амида

(а) Синтез Fmoc-Glu(DMA)-Sieber смолы: (см. пример 16).
(б) Синтез NH2-PEG8-PA-Glu(DMA)-Sieber смолы:
NH2-PEG8-PA-Glu(DMA)-Sieber смолу получают посредством обычного твердофазного синтеза со следующей последовательностью реакций:
(1) расщепление Fmoc-группы от смолы Fmoc-Glu(DMA)-Sieber пиперидином в ДМФА,
(2) конденсация Fmoc-NH-PEG8-PA с использованием HBTU в ДМФА и DIPEA и в заключение
(3) расщепление Fmoc-группы от смолы Fmoc-NH-PEG8-PA-Glu(DMA)-Sieber пиперидином в ДМФА.
(в) Синтез NH2-PEG8-PA-Glu(DMA)-амида:
Продукт расщепляют от смолы NH2-PEG8-PA-Glu(DMA)-Sieber с использованием трифторуксусной кислоты в дихлорметане. ESI-MC: моноизотопный MW рассчит.=1034.8, MW [М+Н]+=1035.9.
| название | год | авторы | номер документа |
|---|---|---|---|
| НАЦЕЛИВАЮЩИЕ АМИНОКИСЛОТНЫЕ ЛИПИДЫ | 2013 |
|
RU2654210C2 |
| НОВЫЕ ПОВЕРХНОСТНО-АКТИВНЫЕ ВЕЩЕСТВА И ИХ ПРИМЕНЕНИЕ | 2004 |
|
RU2395493C2 |
| ФУЗОГЕННЫЕ СОЕДИНЕНИЯ ДЛЯ ДОСТАВКИ БИОЛОГИЧЕСКИ АКТИВНЫХ МОЛЕКУЛ | 2018 |
|
RU2808990C2 |
| ПЕПТИДЫ, ИНГИБИРУЮЩИЕ НЕЙРОННЫЙ ЭКЗОЦИТОЗ | 2007 |
|
RU2461568C2 |
| СТЕРОИДЫ, ВЫСВОБОЖДАЮЩИЕ ОКСИД АЗОТА | 2008 |
|
RU2442790C2 |
| СОЕДИНЕННЫЕ С ЖЕЛЧНЫМИ КИСЛОТАМИ ПРОИЗВОДНЫЕ ПРОПАНОЛАМИНА, ЛЕКАРСТВЕННОЕ СРЕДСТВО | 1999 |
|
RU2234512C2 |
| СПОСОБ УЛУЧШЕНИЯ СТРУКТУРЫ И/ИЛИ ФУНКЦИЙ АРТЕРИОЛ | 2005 |
|
RU2414236C2 |
| АНТАГОНИСТЫ 3-АМИНОАЛКИЛ-1,4-ДИАЗЕПАН-2-ОН МЕЛАНОКОРТИНА-5 РЕЦЕПТОРА | 2009 |
|
RU2530017C2 |
| ЛИПИДЫ ДЛЯ КОМПОЗИЦИЙ ДЛЯ ДОСТАВКИ ТЕРАПЕВТИЧЕСКИХ АГЕНТОВ | 2013 |
|
RU2658007C2 |
| НОВЫЕ ЛИПИДНЫЕ СОЕДИНЕНИЯ | 2007 |
|
RU2509071C2 |
Изобретение относится к соединениям общей формулы I, которые могут найти применение в качестве носителя в системах доставки лекарственных веществ или для индикации антител. В формуле I Y представляет собой О, NH или ковалентную связь, P1 представляет собой Н, прямой или разветвленный алкил, который содержит от 1 до 12 атомов углерода, возможно замещенный амидной группой, дополнительно замещенной алкоксиарилом, Р2, Р3 представляют собой независимо друг от друга Н, алкоксикарбонил, возможно замещенный флуоренилом, или полиокси(С2-С3)алкилен, замещенный аминогруппой и группой -СО-, L представляет собой группу формулы (а), в которой пунктирная линия представляет собой место присоединения к N, R1 представляет собой Н, R1' представляет собой Н, R2 представляет собой Н, R2' представляет собой Н или группу формулы -ORd или -СН2-ORd, R3 представляет собой Н или группу формулы -(CH2)2-ORe или -(СН2)3-ORe, Ra, Rd, Re представляют собой независимо друг от друга насыщенную или ненасыщенную, прямую или разветвленную углеводородную цепь, которая содержит от 6 до 30 атомов углерода, m представляет собой 1, 2 или 3, при условии, что по меньшей мере один из R1, R1', R2, R2', R3 не является Н. Изобретение относится также к везикулярной композиции и набору для применения в системе доставки лекарственного вещества, которые включают соединение формулы I. 3 н. и 10 з.п. ф-лы, 7 пр.


1. Соединение общей формулы I
 ,
,
в которой
Y представляет собой О, NH или ковалентную связь,
P1 представляет собой Н, прямой или разветвленный алкил, который содержит от 1 до 12 атомов углерода, возможно замещенный амидной группой, дополнительно замещенной алкоксиарилом,
Р2, Р3 представляют собой независимо друг от друга Н, алкоксикарбонил, возможно замещенный флуоренилом, или полиокси(С2-С3)алкилен, замещенный аминогруппой и группой -СО-,
L представляет собой группу формулы (а)
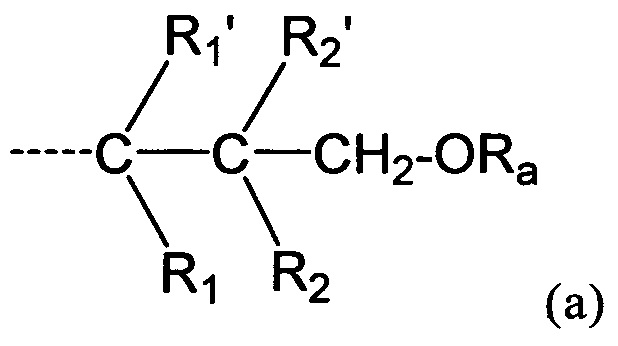 ,
,
в которой пунктирная линия представляет собой место присоединения к N,
R1 представляет собой Н,
R1' представляет собой Н,
R2 представляет собой Н,
R2' представляет собой Н или группу формулы -ORd или -СН2-ORd,
R3 представляет собой Н или группу формулы -(CH2)2-ORe или -(СН2)3-ORe,
Ra, Rd, Re представляют собой независимо друг от друга насыщенную или ненасыщенную, прямую или разветвленную углеводородную цепь, которая содержит от 6 до 30 атомов углерода,
m представляет собой 1, 2 или 3,
при условии, что по меньшей мере один из R1, R1', R2, R2', R3 не является Н.
2. Соединение по п.1, в котором R3 представляет собой Н и
L представляет собой группу формул (b) или (с)
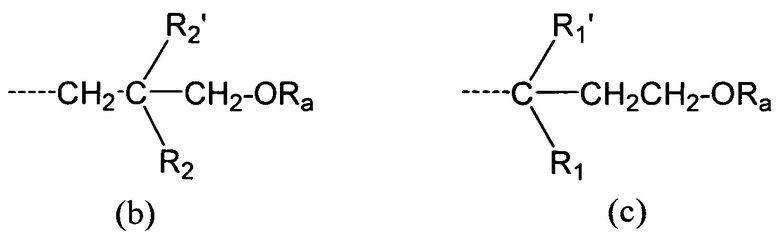 ,
,
в которых пунктирная линия представляет собой место присоединения к N
и P1, Р2, Р3, Y, R1, R1', R2, R2', Ra и m имеют значения, указанные в п.1,
при условии, что в формуле (b) один из R2 и R2' не является Н и в формуле (с) один из R1 и R1' не является Н.
3. Соединение по п.2, в котором L представляет собой группу формулы (b1) или (b2)
 ,
,
в которых пунктирная линия представляет собой место присоединения к N и
Ra и Rd представляют собой независимо друг от друга насыщенную или ненасыщенную, прямую или разветвленную углеводородную цепь, которая содержит от 6 до 30 атомов углерода.
4. Соединение по п.1, в котором
R1, R1', R2, R2' представляют собой Н,
R3 представляет собой группу формулы -(CH2)2-ORe или -(СН2)3-ORe
и P1, P2, Р3, Y, Ra, Re и m имеют значения, указанные в п.1.
5. Соединение по п.1, которое представлено формулами II или III
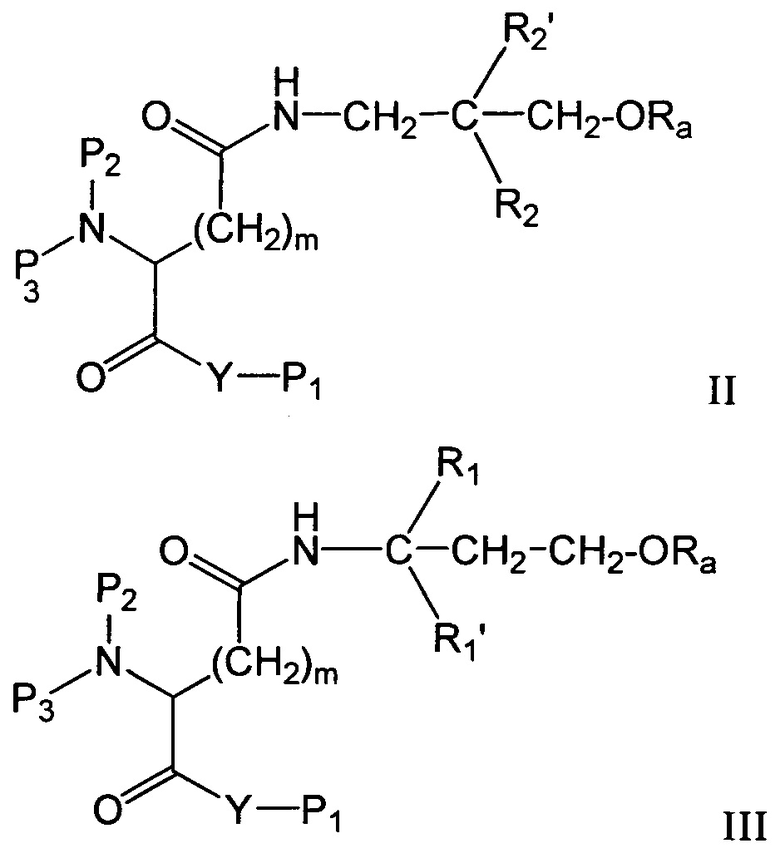 ,
,
в которых
Y представляет собой О, NH или ковалентную связь,
P1 представляет собой Н, прямой или разветвленный алкил, который содержит от 1 до 12 атомов углерода, возможно замещенный амидной группой, дополнительно замещенной алкоксиарилом,
Р2, Р3 представляют собой независимо друг от друга Н, алкоксикарбонил, возможно замещенный флуоренилом, или полиокси(С2-С3)алкилен, замещенный аминогруппой и группой -СО-,
R1 представляет собой Н,
R1' представляет собой Н,
R2 представляет собой Н,
R2' представляет собой Н или группу формулы -ORd или -CH2-ORd,
Ra, Rd представляют собой независимо друг от друга насыщенную или ненасыщенную, прямую или разветвленную углеводородную цепь, которая содержит от 6 до 30 атомов углерода,
m представляет собой 1, 2 или 3,
при условии, что в формуле II один из R2 и R2' не является Н и в формуле III один из R1 и R1' не является Н.
6. Соединение по п.5, которое представлено формулами IIc или IId
 ,
,
в которых
Y представляет собой О, NH или ковалентную связь,
P1 представляет собой Н, прямой или разветвленный алкил, который содержит от 1 до 12 атомов углерода, возможно замещенный амидной группой, дополнительно замещенной алкоксиарилом,
Р2, Р3 представляют собой независимо друг от друга Н, алкоксикарбонил, возможно замещенный флуоренилом, или полиокси(С2-С3)алкилен, замещенный аминогруппой и группой -СО-,
Ra, Rd представляют собой независимо друг от друга насыщенную или ненасыщенную, прямую или разветвленную углеводородную цепь, которая содержит от 6 до 30 атомов углерода,
m представляет собой 1, 2 или 3.
7. Соединение по п.1, которое представлено формулами IVa и IVb
 ,
,
в которых
Y представляет собой О, NH или ковалентную связь,
P1 представляет собой Н, прямой или разветвленный алкил, который содержит от 1 до 12 атомов углерода, возможно замещенный амидной группой, дополнительно замещенной алкоксиарилом,
Р2, Р3 представляют собой независимо друг от друга Н, алкоксикарбонил, возможно замещенный флуоренилом, или полиокси(С2-С3)алкилен, замещенный аминогруппой и группой -СО-,
Ra, Re представляют собой независимо друг от друга насыщенную или ненасыщенную, прямую или разветвленную углеводородную цепь, которая содержит от 6 до 30 атомов углерода, и
m представляет собой 1, 2 или 3.
8. Соединение по любому из предыдущих пунктов, в котором Ra, Rd, Re представляют собой независимо друг от друга прямой или разветвленный С(10-22)алкил, С(10-22)алкенил или С(10-22)алкинил.
9. Соединение по пп.1-7, в котором С(10-22)алкенил и С(10-22)алкинил имеют 1, 2, 3 или 4 ненасыщенных связи, предпочтительно 1 или 2.
10. Соединение по пп.1-7 для применения в системе доставки лекарственного вещества или в качестве системы индикации антител.
11. Везикулярная композиция для применения в системе доставки лекарственного вещества или в качестве системы индикации антител, которая включает по меньшей мере одно соединение формулы I по любому из предыдущих пунктов, необязательно в смеси с одним или несколькими другими везикулообразующими соединениями.
12. Везикулярная композиция по п.11, где везикулярная композиция представляет собой липосому, мицеллу или наночастицу.
13. Набор для применения в системе доставки лекарственного вещества, который включает соединение по пп.1-9 или везикулярную композицию по п.11 или 12.
| Эпоксидная композиция | 1986 |
|
SU1420010A1 |
| Колосоуборка | 1923 |
|
SU2009A1 |
| US 4144036 A, 13.03.1979 | |||
| НОВЫЕ КАТИОННЫЕ И ПОЛИКАТИОННЫЕ АМФИФИЛЬНЫЕ СОЕДИНЕНИЯ, СОДЕРЖАЩИЕ ИХ РЕАГЕНТЫ И ИХ ПРИМЕНЕНИЕ | 1996 |
|
RU2179549C2 |
Авторы
Даты
2018-10-24—Публикация
2013-03-11—Подача