Изобретение относится к новым фторфосфатам лития общей формулы
Li+[PFa(CHbFc(CF3)d)e]-,
где а = 1, 2, 3, 4 или 5, b = 0 или 1, c = 0, 1, 2 или 3, d = 0, 1, 2 или 3 и e = 1, 2, 3 или 4, при условии, что сумма а + е = 6, сумма b + c + d = 3, а b и с не обозначают одновременно 0, при условии, что лиганды (СНbFc(СF3)d) могут быть различными,
к способу получения этих соединений, к их применению в электролитах, а также к изготавливаемым с использованием этих электролитов литиевым батареям.
Изобретение относится также к соединениям общей формулы
[PFa(CHbFc(CF3)d)e], (Iа)
где, как и в формуле (I), b = 0 или 1, с = 0, 1, 2 или 3, d = 0, 1, 2 или 3 и е = 1, 2, 3 или 4, однако а = 1, 2, 3 или 4, которые используют в качестве промежуточных продуктов для получения соединений формулы (I).
Перфторалкилфторфосфораны в качестве исходных материалов для синтеза различных фторфосфорорганических соединений вызывают самый пристальный интерес (N. V. Plavenko: "Reaction of tris(perfluoroalkyl)phosphine oxides and tris(perfluoroalkyl)difluorophosphoranes with fluoride ion", Journ. General Chem. UdSSR, том 59, стр. 469-473, 1989).
Обычно во вторичных литиевых батареях в качестве токопроводящей соли используют гексафторфосфат лития. Недостаток такого технического решения заключается в том, что эта соль обладает относительно невысокой устойчивостью к гидролизу. В связи с этим предпринимались многочисленные попытки найти для этой соли соответствующую замену. Так, например, в международной заявке WO 88/03331 описываются соли циклических перфторалканбис(сульфонил)имидов, в частности также их литиевые соли, которые могут применяться в качестве токопроводящих солей в неводных электролитах для вторичных литиевых батарей. Однако, как показали опыты, получение таких соединений возможно лишь при высоких материально-технических затратах, а по завершении синтеза из них необходимо удалять нежелательные побочные продукты. Кроме того, требуется обязательная очистка солей, поскольку для применения в качестве компонента электролитов для батарей необходимы восстанавливаемые свойства.
С учетом вышеизложенного в основу изобретения была положена задача получить соответствующие токопроводящие соли для электролитов, предназначенные для применения в литиевых батареях. Задачей изобретения является также разработка способа, с помощью которого простым и экономичным путем можно было получать токопроводящие соли по изобретению.
Задача согласно изобретению решается благодаря новым фторфосфатам лития общей формулы
Li+[PFa(CHbFc(CF3)d)e]-, (I)
где а = 1, 2, 3, 4 или 5; b = 0 или 1, с = 0, 1, 2 или 3; d = 0, 1, 2 или 3 и е = 1, 2, 3 или 4, при условии, что сумма а + е = 6, сумма b + c + d = 3, а b и с не обозначают одновременно 0, при условии, что лиганды (СНbFc(СF3)d) могут быть различными,
которые могут заменить гексафторфосфат лития, обычно используемый в качестве токопроводящей соли во вторичных литиевых батареях, а также могут применяться и в смесях между собой.
Объектом изобретения в соответствии с этим являются как новые предлагаемые соли формулы (I), так и способ их получения и соединения общей формулы (Iа)
[PFa(CHbFc(CF3)d)e], (Ia)
где, как и в формуле (I), b = 0 или 1; с = 0, 1, 2 или 3; d = 0, 1, 2 или 3 и е = 1, 2, 3 или 4, однако а = 1, 2, 3 или 4,
которые используют в качестве промежуточных продуктов для получения соединений формулы (I).
Объектом изобретения являются далее также электролиты, содержащие соли по изобретению, и гальванические элементы, которые изготавливают с применением этих электролитов. Такие гальванические элементы могут представлять собой как первичные, так и вторичные батареи, содержащие литиевые соединения формулы (I).
Объектом изобретения являются прежде всего следующие литиевые соли
a)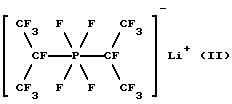
b)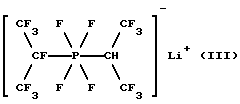
c)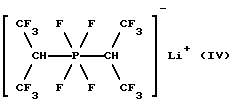
d)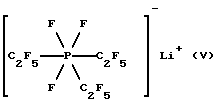
e)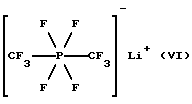
f)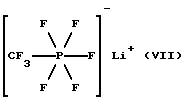
g)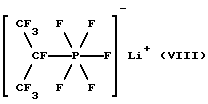
h)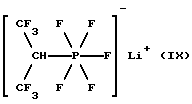
их применение в качестве токопроводящих солей в электролитах, электролиты, содержащие эти соли, а также литиевые батареи, в которых эти соединения содержатся в качестве токопроводящих солей.
Для получения солей по изобретению на первой стадии соответствующие монохлор- или фтор-, дихлор- или дифтор-, хлорфторалкилфосфаны, хлормоно-, хлорди-, хлортри- или хлортетраалкилфосфораны, фтормоно-, фторди-, фтортри- или фтортетраалкилфосфораны или трифтормоногидроалкилфосфораны растворяют в инертном растворителе и по известной технологии подвергают электрохимическому фторированию при температуре в интервале от -15 до 20oС при нормальном давлении. В качестве растворителя для осуществления этой реакции пригоден фтористый водород. Реакцию фторирования прекращают после поглощения 90-150%, прежде всего 110-130% теоретического количества электричества. Это определяют методом кулонометрии.
В зависимости от продолжительности реакции получают смеси продуктов, в составе которых содержатся как полностью насыщенные фтором соединения, так и соединения, фторированные частично. Так, например, при фторировании хлордиизопропилфосфана получают следующие продукты:
a)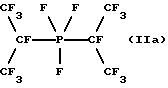 ,
,
b)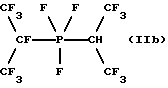 ,
,
c)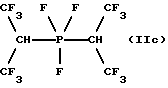 ,
,
d)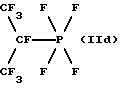 ,
,
e)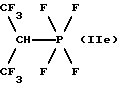 ,
,
Собственно соли формулы (I) согласно изобретению получат благодаря тому, что полученные на первой стадии фторированные алкилфосфораны (II) в виде смеси продуктов, предпочтительно после разделения перегонкой в безводных условиях растворяют с помощью соответствующего апротонного, полярного растворителя, такого, например, как диэтиловый эфир, диметоксиэтаны или их смеси, и подвергают взаимодействию с фторидом лития, в зависимости от реакционной способности, при температуре в интервале от -35 до +60oС, предпочтительно при комнатной температуре, с получением в результате соединений формулы (I).
В электролитах по изобретению могут применяться как чистые соединения формулы (I), так и смеси, получаемые по реакции фторирования. Предпочтительно благодаря восстанавливаемости электролитических свойств применять для приготовления растворов электролитов чистые соединения.
Неожиданно в ходе проведения опытов было установлено, что соединения формулы (I) в апротонных, полярных растворителях проявляют при комнатной температуре устойчивость к гидролизу, а именно, в первую очередь те из них, алкильные остатки, в которых полностью насыщены фтором. При этом устойчивость к гидролизу возрастает по мере увеличения числа атомов фтора в молекуле.
Под апротонными, полярными растворителями имеются в виду такие, как
- нитрилы: ацетонитрил или бензонитрил,
- простые эфиры: диэтиловый эфир, диметоксиэтан, тетрагидрофуран, диоксан или диметилтетрагидрофуран,
- сложные эфиры: метиловый или этиловый эфиры муравьиной кислоты, уксусной кислоты, пропионовой кислоты, а также циклические эфиры, такие, как бутиролактон, и органические карбонаты, как, например, диметилкарбонат, диэтилкарбонат, этилметилкарбонат, этиленкарбонат или пропиленкарбонат,
- амиды: диметилформамид, диэтилформамид, N-метилпирролидин, или
- сульфоны: диметилсульфон, тетраметиленсульфон или другие сульфоланы.
Кроме того, соли по изобретению обладают исключительно высокой растворимостью в указанных растворителях, и низкой гигроскопичностью отличаются прежде всего соединения, полностью насыщенные фтором.
Проведенные опыты показали, что эти соединения исключительно устойчивы. При хранении в сухих условиях в твердом состоянии у перфорированных соединений при температуре ниже 100oС не наблюдается никакого разложения. И при дальнейшем повышении температуры они проявляют термостойкость. Лишь при температурах выше 130oС имеют место небольшие изменения цвета.
При хранении в растворе, например, в диметоксиэтане, даже по истечении нескольких недель не наблюдается никаких изменений цветовой окраски, равно как и образования продуктов разложения.
Уже сам по себе этот фактор обеспечивает без всяких оговорок возможность применения предлагаемых соединений, прежде всего соединений формул III, IV, V, VI и VII, в качестве токопроводящих солей в неводных электролитах для литиевых батарей.
Далее, растворы электролитов, содержащие эти соединения, отличаются сравнительно высокой химической и электрохимической стойкостью. Так, в частности, не наблюдается окисление сопряженного аниона до начала осаждения лития.
Электролиты такого типа наряду с органическими солями лития, каковыми являются соединения формулы (I) по изобретению, содержат в своем составе также один либо несколько неводных органических растворителей и не обязательно другие добавки. При необходимости в электролит в качестве токопроводящих солей, помимо соединений по изобретению, можно добавлять также и другие известные литиевые соли. Более подробные пояснения касательно особенностей таких электролитов, равно как и компоновки и функционального назначения литиевых батарей хорошо известны специалисту в данной области техники. Соединения по изобретению могут применяться в полном соответствии с используемыми в этих целях известными литиевыми соединениями и проявляют при этом исключительно высокую устойчивость. Соответствующие элементы батареи отличаются превосходными свойствами касательно емкости и стабильности напряжения, а также неограниченной работоспособностью в течение длительного периода времени, включающего циклы заряд-разряд и значительно превосходящего средние показатели.
Представленные ниже примеры предназначены для более подробного пояснения настоящего изобретения, не ограничивая его объем и заявляемые признаки.
Пример 1
Бис(гептафторизопропил)трифторфосфоран (IIа) и его производные
По реакции Симмонса диизопропилхлорфосфан электрохимически фторируют в электролизере, содержащем фтористый водород в качестве растворителя. В данном случае применяют цилиндрический электролизер объемом 310 см3, оснащенный никелевыми анодами с эффективной площадью S=3,75 дм2 и катодами с такой же эффективной площадью. Кроме того, электролизер оснащен конденсатором. Температуру элемента электролизера в процессе электролиза поддерживают на уровне -5oС, а температуру конденсатора - на уровне -30oС.
57 г Диизопропилхлорфосфана, растворенных в 200 г фтористоводородной кислоты, порциями добавляют к 235 г предварительно подвергнутой электролизу фтористоводородной кислоты, а именно, следующим образом (см. таблицу).
Газообразные продукты после прохождения через конденсатор и ПТФЭ-ловушек (ПТФЭ означает политетрафторэтилен) охлаждают до -78oС.
Электролиз, осуществляемый при напряжении 4,4-5,4 В и плотности потока 0,30-0,53 А/дм2, завершается после расхода электроэнергии 420 А•ч (131% от теории), и при этом из электролиза собирают 220 г жидкого продукта. После установления температуры на уровне -20oС и отделения нижней фазы от фазы фтористого водорода получают 18 г сырого продукта. Методом 19F-ЯМР-спектроскопии определяют, что этот продукт содержит 75% бис(гептафторизопропил)трифторфосфорана (IIа), 15% гептафторизопропил(1,1,1,3,3,3-гексафторизопропил)трифторфосфорана (IIb) и 10% бис(1,1,1,3,3,3-гексафторизопропил)трифторфосфорана (IIс).
Фракционной перегонкой эту смесь можно разделить на фракции, каждая из которых содержит одно из указанных соединений в качестве главного компонента. Кроме того, после отделения от фазы фтористого водорода из охлаждающих ловушек получают 33 г жидких при низких температурах продуктов. Как показывает 19F-ЯМР-спектроскопический анализ, эти продукты представляют собой преимущественно гептафторизопропилтетрафторфосфоран (IId), 1,1,1,3,3,3-гексафторизопропилтетрафторфосфоран (IIе) и перфторпропан. Путем нагрева до 20oС перфторпропан можно отгонять. Остаток можно разделить фракционной перегонкой на фракции, которые содержат гептафторизопропилтетрафторфосфоран (IId) или 1,1,1,3,3,3-гексафторизопропилтетрафторфосфораны (IIе) в качестве главных компонентов.
Полученные соединения можно охарактеризовать следующими показателями.
Бис(гептафторизопропил)трифторфосфоран (IIа):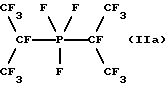
19F-ЯМР, част./млн: (СD3СN-пленка с CCl3F в качестве стандарта), -39,72 dtm (3 F1); -70,15 m (12 F3); -171,78 dm (2 F2); 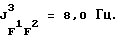
31Р-ЯМР, част./млн: (CD3CN-пленка с 85% Н3РО4 в качестве стандарта), -26,0 qtm; 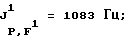
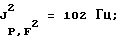
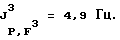
Гептафторизопроггил (1,1,1,3,3,3-гексафторизопропил)трифторфосфоран (IIb):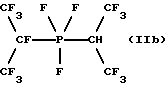
19F-ЯМР, част./млн: (СD3СN-пленка с 85% ССl3F в качестве стандарта), -33,10 dm (3 F1); -59,56 m (6 F4); -70,26 m (6 F3); -171,90 m (1 F2) .
31Р-ЯМР, част./млн: (СD3СN-пленка с 85% Н3РO4 в качестве стандарта), -23,2 qdm; 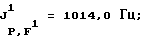
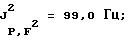
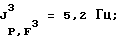
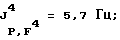
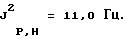
'Н-ЯМР, част/млн: (СD3СN-пленка с ТМС в качестве стандарта), 3,9 dm.
Бис(гекса-1,1,1,3,3,3 -гексафторизопропил)трифторфосфоран (IIc):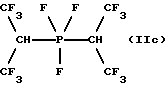
19F-ЯМР, част./млн: (СD3СN-пленка с СС13F в качестве стандарта), -25,96 dm (3 F1); -59,51 m (12 F2);
31Р-ЯМР, част./млн: (CD3CN-пленка с 85% Н3РO4 в качестве стандарта), -20,69 qm; 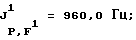
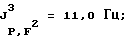
'Н-ЯМР, част/млн: (CD3CN-пленка с ТМС в качестве стандарта), 3,9 dm.
Гептафторизопропилтетрафторфосфоран (IId):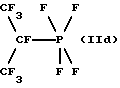
19F-ЯМР, част. /млн: ((СD3СN-пленка с СС13F в качестве стандарта); -30oС): -50,10 dm (4 F1); -72,22 m (6 F3); -172,83 dm (1 F2);
31Р-ЯМР, част./млн: ((СD3СОСD3-пленка с 85% Н3РO4 в качестве стандарта); -40oС): -55,3 pdsep 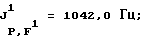
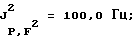
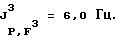
1,1,1,3,3,3-Гексафторизопропилтетрафторфосфораны (IIе):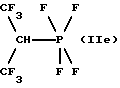
19F-ЯМР, част. /млн: ((СD3СN-пленка с СС13F в качестве стандарта); -30oС): -40,90 dm (4 F1); -61,8 m (6 F2).
31P-ЯMP, част./млн: ((СD3СОСD3-пленка с 85% Н3РО4 в качестве стандарта); -40oС): -50,8 pdsep; 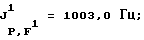
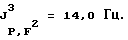 J2 P,Н=27,0 Гц.
J2 P,Н=27,0 Гц.
Пример 2
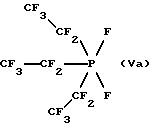
Трис(пентафторэтил)дифторфосфоран (Vа)
Аналогично тому, как это описано в примере 1, из 69 г триэтилфосфиноксидаполучают70гтрис(пентафторэтил)дифторфосфорана(Va).Данные31Р-ЯМР-спектроскопии соответствуют таковым, известным из литературы (V.J. Semenii и др., Журнал общей химии, СССР, 1985 г., том 55, 12, стр. 2716-2720).
31Р-ЯМР, (СD3СОСD3-пленка с 85%-ной Н3РO4 в качестве стандарта) част. /млн: -47,55 tsep; J1 P,F=1003,0 Гц; J2 P,F=122,0 Гц.
Пример 3
Бис(гептафторизопропил)тетрафторфосфат лития (II)
К загруженному в выполненный из ПТФЭ реакционный сосуд раствору из 0,82 г (0,031 моль) LiF и 60 мл подвергнутого предварительной сушке диметоксиэтана в условиях, исключающих присутствие влаги, медленно добавляют при перемешивании магнитной мешалкой 12 г (0,028 моль) бис(гептафторизопропил)трифторфосфорана (IIa), причем температуру за счет охлаждения в ледяной бане поддерживают на уровне комнатной температуры. Затем при той же температуре продолжают перемешивание еще в течение одного часа, добавляя при этом небольшие количества металлического лития. Далее реакционную смесь в течение 24 ч выдерживают при комнатной температуре, затем фильтруют, после чего ее можно непосредственно использовать в качестве электролита для подзарядки батарей. Однако образующийся при реакции бис(гептафторизопропил)тетрафторфосфат лития (II) можно и выделять за счет отгонки растворителя под высоким вакуумом. Выделенный продукт представляет собой комплексную соль лития (II), Li+[(i-С3F7)2РF4]-•2ДМЭ, tпл 126-128oС; термостойкость до 130oС.
Анализ: Li
теоретически: 0,93%,
обнаружено: 1,15%.
Растворитель можно удалять за счет нагрева комплексной соли (II) в течение нескольких дней под высоким вакуумом до температуры 80oС.
Пример 3а
Для получения литиевых солей по изобретению полученную в примере 1 фторфосфорановую смесь можно использовать непосредственно, без фракционной перегонки.
16 г Фторфосфорановой смеси из примера 1, содержащей 75% соединения (IIа), 15% соединения (IIb) и 10% соединения (IIc), добавляли аналогично тому, как описано выше, к раствору из 1,0 г LiF и 80 мл ДМЭ. Полученный раствор также может после фильтрации непосредственно использоваться в качестве электролита. Однако Li-соли можно выделять также из раствора путем кристаллизации, добавляя в этих целях подвергнутый предварительной сушке гексан к ДМЭ-раствору. После перекристаллизации полученного продукта, осуществляемой смесью растворителей из сухого ДМЭ и дибутилового эфира (соотношение 1: 2), получают 13,6 г бис(гептафторизопропил)тетрафторфосфата лития (II) вместе с 6% гептафторизопропил(1,1,1,3,3,3-гексафторизопропил)тетрафторфосфата лития (III).
Структуру солей (II) и (III) определяли с помощью 19F- и 31Р-ЯМР-спектроскопии. ЯМР-спектры определяли в СD3СОСD3-растворах с использованием CCl3F, а в другом случае - 85%-ной H3PО4 в качестве внешних стандартов.
Бис(гептафторизопропил)тетрафторфосфат лития (II):
19F-ЯМР, част./млн: -58,14 dm (4 F1); -71,07 pdd (12 F3); -184,40 dpsep (2 Р2); 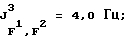
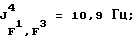
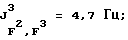
31P-ЯMP, част./млн: -149,27 ptm; -148,42 ptm (CD3CN-pacтвор); 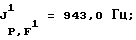
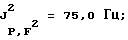
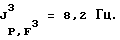
Гептафторизопропил (1,1,1,3,3,3-гексафторизопропил)тетрафторфосфат лития (III):
19F-ЯМР, част./млн: -47,20 dddm (4 F1); -58,01 dpd (6 F4); -70,79 pdd (6 F3); -183,50 dm (1 F2); 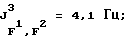
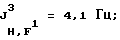
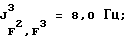
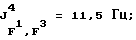
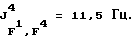
31P-ЯМР, част. /млн: -147,37 pdm; 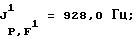
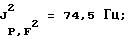
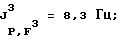
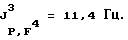
Пример 4
Гептафторизопропилпентафторфосфат лития (VIII)
Гептафторизопропилпентафторфосфат лития (VIII) получают аналогично тому, как это описано в примере 3, взаимодействием фторфосфорана (IId) с LiF в сухом диметоксиэтане. Как указывалось выше, после фильтрации полученный раствор может непосредственно использоваться в качестве раствора электролита или же вышеназванную соль можно выделять за счет отгонки растворителя под высоким вакуумом либо путем кристаллизации, осуществляемой добавлением гексана.
Смесь фторфосфоранов, полученную согласно примеру 1, также можно использовать для приготовления растворов электролита, подвергая ее взаимодействию с LiF без предварительной очистки. Раствор обеих литиевых солей (VIII) и (IX), получаемый в этом случае, также может применяться в качестве электролита для литиевых батарей. Обе соли можно выделять аналогично тому, как это описано выше.
Гептафторизопропилпентафторфосфат лития (VIII):
19F-ЯМР, част. /млн: (растворитель: СD3СОСD3; стандарт: ССl3F): -62,62 dddsep (4 F1); -73,13 p (1 F2); -71,49 pdd (6 F4); -183,72 dpsepm (1 F3); 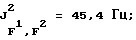
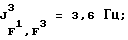
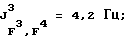
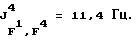
31Р-ЯМР, част. /млн: (растворитель: CD3CN; внешний стандарт: 85%-ная Н3РO4) -148,16 pddsep; 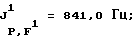
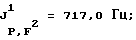
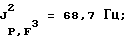
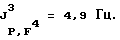
1,1,1,3,3,3-Гексафторизопропилпентафторфосфат лития (IX):
19F-ЯМР, част. /млн: (растворитель: СD3СОСD3; стандарт: CCl3F): -52,95 dddsep (4 F1); -69,04 p (1 F2); -59,40 dp (6 F3); 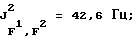
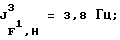
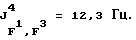
31Р-ЯМР, част. /млн: (растворитель: СD3СN; внешний стандарт: 85%-ная Н3РО4) -145,82 pddsep; 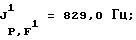
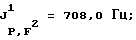 J2 P,H=29,0 Гц;
J2 P,H=29,0 Гц; 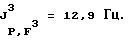
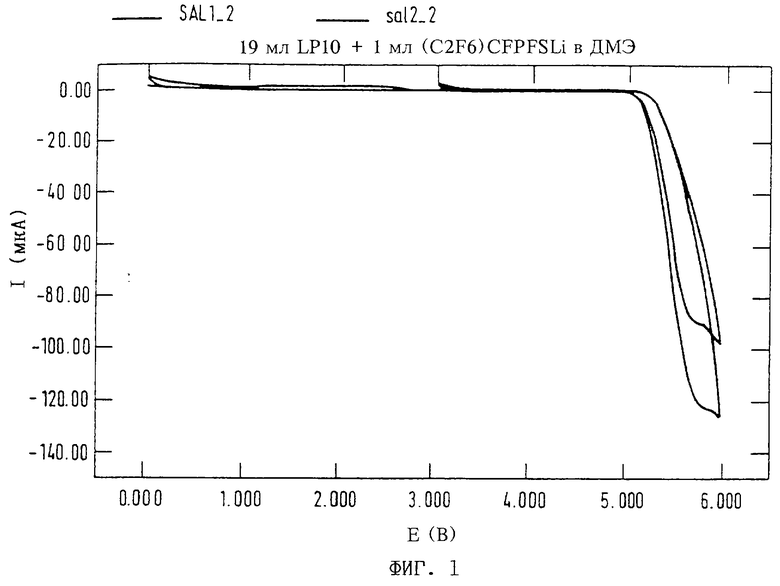
С применением гептафторизопропилпентафторфосфата лития (VIII) проводили опыты на цикличность, результаты которых представлены на фиг. 1. Эти опыты проводили при соблюдении следующих условий:
интервал изменения потенциалов - 0,0-3,0 В; 3,0-6,0 В;
скорость изменения - 100 мВ/с;
рабочий электрод - Pt, поверхность 1,96•10-3 см2;
контрольный электрод - Li;
измерительный электрод - Li;
электрохимическая устойчивость - до 5,0 В.
Пример 5
Трис(пентафторэтил)трифторфосфат лития (V)
Трис(пентафторэтил)трифторфосфат лития (V) получают аналогично примеру 3 взаимодействием соответствующего полученного согласно примеру 2 фторфосфорана (Va) с LiF в подвергнутом предварительной сушке диметоксиэтане. И в этом случае полученный по указанной реакции и после фильтрации реакционный раствор можно непосредственно применять в качестве электролита или же соль (V) можно выделять за счет отгонки растворителя под высоким вакуумом либо путем кристаллизации, осуществляемой добавлением гексана.
Трис(пентафторэтил)трифторфосфат лития (V):
19F-ЯМР, част. /млн: (растворитель: CD3COCD3; стандарт: ССl3F): -87,0 d (2 F1); -43,6 dm (1 F2); -115,3 m (4 F3); -115,7 m (2 F5); -79,7 m (3 F6); -81,3 m (6 F4).
31Р-ЯМР, част. /млн: (растворитель: СD3СОСD3; внешний стандарт: 85%-ная Н3РO4): -149,8 tdpt 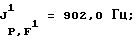
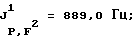
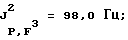
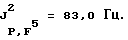
Комплекс трис(пентафторэтил)трифторфосфат лития (V) с ДМЭ имеет tпл 116-118oС и обладает термостойкостью до 130oС.
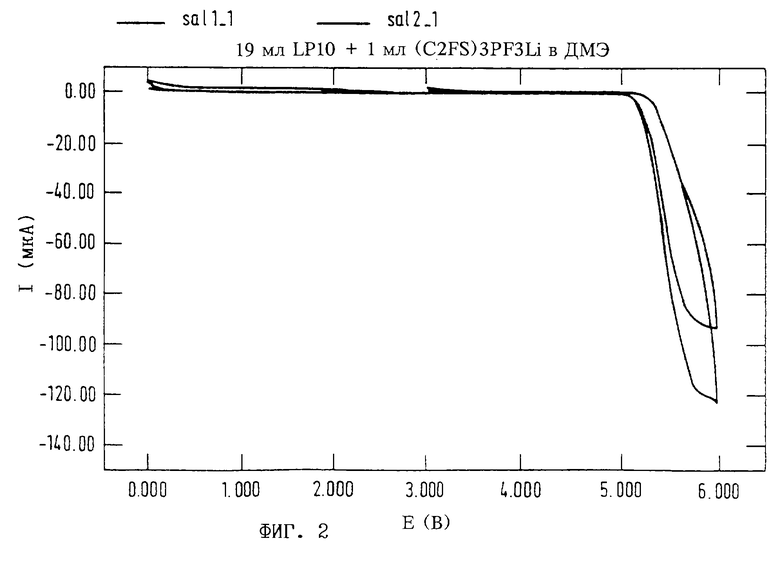
Используя 1 мл трис(пентафторэтил)трифторфосфата лития (V), растворенного в ДМЭ, и добавляя 19 мл LP10, проводили опыты на цикличность. Результаты первого и пятого опытов на цикличность представлены на фиг. 2. Эти опыты проводили при соблюдении следующих условий:
интервал изменения потенциалов - 0,0-3,0 В; 3,0-6,0 В;
скорость изменения - 100 мВ/с;
рабочий электрод - Pt, поверхность 1,96•10-3 см2;
контрольный электрод - Li;
измерительный электрод - Li;
электрохимическая устойчивость - до 5,0 В.
Пример 6
1. Бис(1,1,1,3,3,3-гексафторизопропил)тетрафторфосфат лития (IV)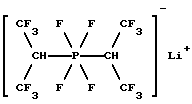
Указанное соединение формулы (IV) получают в смеси с соединениями формулы (II) и (III) в сооветствии с примером 3а.
19F-ЯМР, ррm (растворитель: CD3COD3, базовое соединение: CCl3F): -35,55 d.m (PF4); -58,86 m (4 СF3); J3 P,F=14,1 Hz; J4 P,F=12,2 Hz.
31P-ЯМР, ppm (растворитель: CD3CN, базовое соединение: 85% Н3РO4 в качестве внешнего стандарта): -144,86 quin, m; J1 P,F = 914 Hz;
Пример 7.
2. Бис(трифторметил)тетрафторфосфат лития (VI)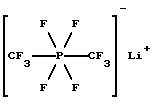
Исходное соединение бис(трифторметил)трифторфосфоран (СF3)2РF3 синтезировано согласно методу, описанному у W. Mahler, Неорг. химия, 2, (1963), 230.
1,5 г (6,64 ммоль) (CF3)2PF3 в 15 мл обезвоженной HF смешивают с 0,21 г (8,08 ммол) сухого фторида лития (LiF) в PFA-колбе при -35oС. Полученную реакционную смесь перемешивают при этой температуре в течение 2 часов и затем выдерживают в течение ночи при -21oС. Избыточное количество LiF отделяют декантацией.
31P-ЯМР-спектр очищенного раствора подтверждает образование соли формулы (VI).
31P-ЯМР, ppm (растворитель: HF, CD3CN, температура: -40oС): -149,86 quin, sep (базовое соединение: 85% Н3РO4 в пленке); -2,45 quin, sep (базовое соединение: PF6 - в качестве внутренного стандарта). j1 P,F = 929 Hz.
Для выделения соли формулы (VI) отгоняют HF. Оставшееся твердое вещество растворяют в смеси этиленкарбонат: диметилкарбонат 1:1 (маc.). 19F-ЯМР-спектр доказывает присутствие в растворе литиевой соли формулы (VI).
19F-ЯМР, ppm (ЕС: DМС 1: 1, СD3СN-плeнка базовое соединение: CCl3F в пленке): -68,63 d, quin (2CF3); -76,86 d,m (PF4); j1 P,F=896 Hz; J2 P,F=147 Hz; J3 F,F=14,2 Hz.
Пример 8.
3. Трифторметилпентафторфосфат лития (VII).
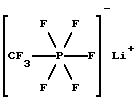
Метилдихлорфосфин CH3PCl2 подвергают электрохимическому фторированию так, как это описано в примере 1. Раствор трифторметилтетрафторфосфорана СF3РF4 в HF собирают после прохождения через ПТФЭ-ловушку. Путем обработки этого раствора LiF получают литиевую соль формулы (VII) непосредственно в растворе HF кислоты.
F-ЯМР, ppm (растворитель: СD3СОСD3-пленка, температура: -50oС, базовое соединение: PF6 - в качестве внутренного стандарта): -2,00 d,m (CF3); -2,33 d,m (PF5); J1 P,F=817 Нz; j2 P,F = 145 Hz;
31P-ЯМР, ppm (растворитель: HF, СD3СОСD3-пленка, температура: -40oС, базовое соединение: 85% Н3РО4 в пленке): -149,10 sex.q.
Для выделения соли формулы (VII) отгоняют HF и оставшийся продукт растворяют диметоксиэтане (ДМЭ).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ОРГАНИЧЕСКИХ СОЛЕЙ, СОДЕРЖАЩИХ АНИОНЫ БИС(ПЕРФТОРАЛКИЛ)ФОСФИНАТА | 2004 |
|
RU2362778C2 |
| ЛИТИЙФТОРАЛКИЛФОСФАТЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЭЛЕКТРОЛИТНЫХ СОЛЕЙ | 2001 |
|
RU2257389C2 |
| СПОСОБ ПОЛУЧЕНИЯ ОНИЕВЫХ СОЛЕЙ С ТЕТРАФТОРБОРАТНЫМ АНИОНОМ, ИМЕЮЩИХ НИЗКОЕ СОДЕРЖАНИЕ ГАЛОГЕНИДОВ | 2005 |
|
RU2415843C2 |
| СТАБИЛЬНЫЕ (CF)N СОЛИ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2000 |
|
RU2257376C2 |
| СОЕДИНЕНИЯ, СОДЕРЖАЩИЕ ОРГАНОФТОРХЛОРФОСФАТНЫЕ АНИОНЫ | 2007 |
|
RU2465278C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЛИТИЕВЫХ КОМПЛЕКСНЫХ СОЛЕЙ ДЛЯ ИСПОЛЬЗОВАНИЯ В ХИМИЧЕСКИХ ИСТОЧНИКАХ ТОКА | 2000 |
|
RU2246499C2 |
| СПОСОБ ПОЛУЧЕНИЯ БИС(ТРИФТОРМЕТИЛ)ИМИДО-СОЛЕЙ | 2002 |
|
RU2278109C2 |
| ИОННЫЕ ЖИДКОСТИ НИЗКОЙ ВЯЗКОСТИ | 2006 |
|
RU2413732C2 |
| СОЛИ С ЦИАНОБОРАТНЫМИ АНИОНАМИ | 2004 |
|
RU2337912C2 |
| ИОННЫЕ ЖИДКОСТИ, СОДЕРЖАЩИЕ АНИОНЫ [N(CF)] | 2003 |
|
RU2351601C2 |

Изобретение относится к новому способу получения фторфосфатов лития общей формулы (I), где а = 1, 2, 3, 4 или 5, b = 0 или 1, с = 0, 1, 2 или 3, d = 0, 1, 2 или 3; е = 1, 2, 3 или 4, при условии, что сумма а+е = 6, сумма b+c+d = 3, а b и с не обозначают одновременно 0, при условии, что лиганды (CHbFc(CF3)d) могут быть различными, причем монохлор- или фтор-, дихлор- или дифтор-, хлорфторалкилфосфаны, хлормоно-, хлорди-, хлортри- или хлортетраалкилфосфораны, фтормоно-, фторди-, фтортри- или фтортетраалкилфосфораны или трифтормоногидроалкилфосфаны подвергают электрохимическому фторированию в инертном растворителе, полученную смесь продуктов при необходимости разделяют перегонкой на различные фторированные продукты и фторированные алкилфосфаны, подвергают в апротонном, полярном растворителе при от -35 до 60oС взаимодействию с фторидом лития. Также раскрыты сами фторфосфаты лития общей формулы (I), электролиты для литиевых батарей на их основе и вторичные литиевые батареи. Изобретение может быть использовано в электротехнике для получения простым и экономичным способом вторичных литиевых батарей, содержащих устойчивые к гидролизу токопроводящие соли. 4 с. и 4 з.п. ф-лы, 2 ил., 1 табл.
Li+[PFa(CHbFc(CF3)d)e]- (I)
Li+[PFa(CHbFc(CF3)d)e] -, (I)
где а = 1, 2, 3, 4 или 5;
b = 0 или 1;
с = 0, 1, 2 или 3;
d = 0, 1, 2 или 3;
е = 1, 2, 3 или 4, при условии, что сумма а+е = 6, сумма b+c+d = 3, а b и с не обозначают одновременно 0,
при условии, что лиганды (CHbFc(CF3)d) могут быть различными, отличающийся тем, что а) монохлор- или фтор-, дихлор- или дифтор-, хлорфторалкилфосфаны, хлормоно-, хлорди-, хлортри- или хлортетраалкилфосфораны, фтормоно-, фторди-, фтортри- или фтортетраалкилфосфораны или трифтормоногидроалкилфосфораны подвергают электрохимическому фторированию в инертном растворителе, б) полученную смесь продуктов при необходимости разделяют перегонкой на различные фторированные продукты и в) фторированные алкилфосфаны подвергают в апротонном, полярном растворителе при от -35 до +60oС взаимодействию с фторидом лития.
Li+[PFa(CHbFc(CF3)d)e] -, (I)
где а = 1, 2, 3, 4 или 5;
b = 0 или 1;
с = 0, 1, 2 или 3; d = 0, 1, 2 или 3 и
е = 1, 2, 3 или 4, при условии, что сумма а+е = 6, сумма b+c+d = 3, а b и с не обозначают одновременно 0,
при условии, что лиганды (CHbFс(CF3)d) могут быть различными.
а)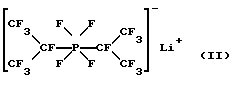
b)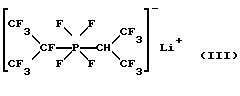
c)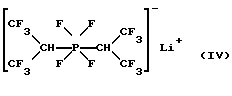
d)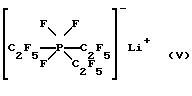
e)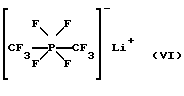
f)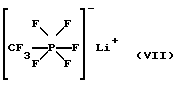
g)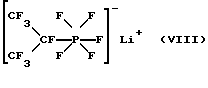
h)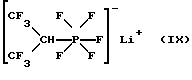
7. Электролиты для литиевых батарей, содержащие фторфосфаты лития общей формулы (1) по пп. 5 и 6.
| RU 2075435 Cl, 20.03.1997 | |||
| US 3723603 А, 27.03.1973 | |||
| US 4613450 А, 23.05.1986. |
Авторы
Даты
2002-07-10—Публикация
1997-09-24—Подача