Изобретение относится к области медицины, в частности к лабораторной диагностике, и может быть использовано для исследования крови.
Известно, что активатор протеина С (АПС) используют для определения уровня протеинов С, S и резистентности фактора V к активированному протеину С.
Наиболее близким по достигаемому положительному результату является способ получения АПС из яда змеи Agkistrodon contortrix (семейство - Agkistrodon; род - contortrix) (Martinoli J.L., Stocker K.F. Fast functional protein С assay using Protac a novel protein С activator // Thrombosis Research, 1986, vol. 43, 3. p.253 - 264). Сущность его заключается в выделении белковой фракции, способной активировать протеин С. Данный активатор под названием "ProtacTM" зарегистрирован фирмой Pentapharm Ltd (Швейцария).
Способ-прототип выполняют следующим образом:
Этап 1. Готовят 5%-ный раствор нативного яда змеи Agkistrodon contortrix в дистиллированной воде. При температуре +2...+5oС в полученный раствор вносят этиловый спирт до конечной концентрации 55 объемных процентов. Образующийся при этом преципитат осаждают центрифугированием (15 мин, 2000 g), супернатант удаляют.
Этап 2. Преципитат растворяют в 0,015 М фосфатном буфере (рН = 6,8) и наносят на колонку гель DEAE Sephadex А-50, уравновешенный тем же буфером. Элюцию ведут 0,015 М фосфатным буфером (рН = 6,8) с возрастающим линейным градиентом концентрации NaCl от 0,0 до 0,4 М.
Содержащие АПС фракции элюата идентифицируют в тесте определения активированного парциального тромбопластинового времени свертывания (АПТВ). Для этого в регистрирующую ячейку коагулометра вносят 0,1 мл АПТВ-реагента, 0,1 мл контрольной нормальной плазмы и 0,1 мл исследуемой фракции (в контроле - тот же объем элюирующего буфера), смесь инкубируют 1 минуту при +37oС, после чего добавляют 0,1 мл раствора кальция хлорида и регистрируют время образования сгустка. При наличии во фракции АПС АПТВ удлиняется, по сравнению с контролем, где 0,1 мл исследуемой фракции заменен на 0,1 мл элюирующего буфера.
Этап 3. Содержащие АПС фракции элюата смешивают и концентрируют методом ультрафильтрации до 1/10 от исходного объема фракций.
Этап 4. Полученный концентрат разводят в 10 раз 0,05 М ацетатным буфером (рН = 5,0) и наносят на колонку с гелем CM Sephadex C-50, уравновешенным тем же буфером. Элюцию ведут 0,05 М ацетатным буфером (рН = 5,0) с возрастающим линейным градиентом NaCl от 0 до 0,6 М.
Этап 5. Фракции, содержащие АПС, идентифицируют в тесте АПТВ (см. Этап 2), смешивают и концентрируют ультрафильтрацией до 1/25 от исходного объема фракций.
Этап 6. Полученный концентрат наносят на колонку с гелем Sephadex G-100. В качестве элюэнта используют 1%-ную уксусную кислоту. Фракции, содержащие АПС, смешивают и лиофильно высушивают.
К недостаткам известного способа следует отнести малую доступность и высокую стоимость яда змеи Agkistrodon contortrix, не встречающейся на территории Российской Федерации и обитающей преимущественно в странах Юго-Восточной Азии.
Положительным результатом заявляемого способа является расширение арсенала реагентов для лабораторной диагностики нарушений в системе протеина С.
Положительный результат заявляемого способа достигается тем, что в качестве источника активатора протеина С используют яд змеи Agkistrodon saxatilis (семейство - Agkistrodon; род - saxatilis).
Способ осуществляют следующим образом:
Реактивы и оборудование:
1. Яд змеи Agkistrodon saxatilis (семейство - Agkistrodon; род - saxatilis), 0,01 г, кристаллический.
2. Гель Sephacryl S-300 HR (Pharmacia, Швеция).
3. Ацетатцеллюлозные мембраны с отбором (отсечкой) по молекулярной массе 20 Кд (Sartorius, Германия).
4. Ячейки для ультрафильтрации (Ultrasart Cell 50, Sartorius, Германия).
5. Трис-HCl буфер (0,02 М, рН = 8,0).
6. Гель DEAE Sepharose FF (Pharmacia, Швеция).
7. Гель SP Sepharose FF (Pharmacia, Швеция).
8. Гель Sephadex G-25 (M) (Pharmacia, Швеция).
9. MES буфер (0,01 М, рН = 6,2).
10. Референтная нормальная пулированная плазма (РНП-плазма), лиофильно высушенная фирмы "Технология-Стандарт", Россия.
11. Каолин (легкая фракция) фирмы "Технология-Стандарт", Россия, с концентрацией взвеси каолина 0,025 мг/мл в трис-НСl буфера (рН = 7,4, 0,05 M).
12. Кефалин фирмы "Технология-Стандарт", Россия, 30 мг лиофильно высушенного реагента, полученного из тканевого тромбопластина человека, во флаконе.
13. Кальция хлорид (СаСl2), 0,025 М раствор, во флаконе, фирмы "Технология-Стандарт", Россия.
14. Азид натрия (Sigma, США).
15. Сахароза, 2%-ный раствор (Merk, Германия).
16. Protac (активатор протеина С из яда змеи Agkistrodon contortrix), лиофильно высушен, на 1,0 мл (производитель "Biomereuox", Франция).
17. Дефицитная по протеину С плазма лиофильно высушенная, на 1,0 мл, (производитель "Biomereuox", Франция).
18. Пробирки стеклянные вместимостью 20 мл.
19. Пенициллиновые флаконы на 10 мл.
20. Хроматографические колонки (размером 26 х 800 мм, 26 х 40 мм, 20 х 26 мм и 15 х 200 мм), производитель (Pharmacia, Швеция).
21. Весы аналитические S-2051 (Sartorius, Германия).
22. Магнитная мешалка MM 3M, Россия.
23. Коллектор фракций (LKB, Швеция).
24. Спектрофотометр СФ-46 (Россия).
25. РН-метр РН-340 (Россия).
Приготовление реактивов
Приготовление раствора яда змеи Agkistrodon saxatilis. К 100 мг кристаллического яда змеи Agkistrodon saxatilis добавляют 5 мл 0,05 М раствора натрия хлорида (NaCI). Раствор яда змеи Agkistrodon saxatilis перемешивают в течение 60 мин на магнитной мешалке при +18...+25oС. Все последующие процедуры приготовления реактивов и выделения АПС проводят при той же температуре.
Приготовление эмульсии кефалина. Во флакон с кефалином вносят 2,0 мл дистиллированной воды. Встряхивают в течение 1 - 2 мин до гомогенной эмульсии. В результате получают 1,5%-ную эмульсию.
Приготовление АПТВ-реагента. Смешивают 0,1 мл эмульсии кефалина с 3 мл взвеси каолина (0,025 мг/мл).
Приготовление раствора Protac. Флакон, содержащий лиофильно высушенный Protac, разводят 1,0 мл дистиллированной воды.
Ход выделения АПС из яда змеи Agkistrodon saxatilis
Этап 1. Раствор яда змеи Agkistrodon saxatilis наносят на колонку (размером 26 х 800 мм), заполненную гелем Sephacryl S-300 HR, уравновешенным 0,05 М раствором натрия хлорида (NaCl). Элюцию ведут этим же раствором, при скорости 60 мл/час. Объем собираемых фракций - 10 мл.
Этап 2. Содержащие АПС фракции элюата идентифицируют в тесте АПТВ. Для этого в регистрирующую ячейку коагулометра вносят 0,1 мл АПТВ-реагента, 0,1 мл контрольной нормальной плазмы и 0,1 мл исследуемой фракции (в контроле - тот же объем элюирующего буфера), смесь инкубируют 1 минуту при +37oС, после чего добавляют 0,1 мл 0,025 М кальция хлорида (CaCl) и регистрируют время образования сгустка. При наличии во фракции АПС АПТВ удлиняется, по сравнению с контролем, где 0,1 мл исследуемой фракции заменен на 0,1 мл элюирующего буфера.
Этап 3. Содержащие АПС фракции элюата смешивают и концентрируют методом ультрафильтрации до 1/10 от исходного объема фракций. Для концентрирования образцов используют ячейки для ультрафильрации и ацетатцеллюлозные мембраны с отбором по молекулярной массе 20 Кд.
Этап 4. Полученный раствор разводят в 10 раз трис-НСl буфером и наносят на колонку (размерами 26 х 40 мм), заполненную гелем DEAE Sepharose FF, который уравновешивают тем же буфером. Элюцию ведут трис-НСl буфером, содержащим линейный градиент хлорида натрия (NaCI) от 0,0 до 0,5 М, со скоростью 450 мл/час. Объем собираемых фракций - 20 мл.
Этап 5. Содержащие АПС фракции элюата идентифицируют (Этап 2), смешивают и концентрируют методом ультрафильтрации через ацетатцеллюлозные мембраны до 1/20 от исходного объема.
Этап 6. Полученный раствор разводят в 10 раз MES буфером и наносят на колонку (размерами 20 х 26 мм), заполненную гелем SP Sepharose FF, уравновешенным тем же буфером. Элюцию ведут MES буфером, содержащим линейный градиент концентрации натрия хлорида (NaCl) от 0,0 до 1,0 М, со скоростью 450 мл/час. Объем собираемых фракций - 10 мл.
Этап 7. Содержащие АПС фракции элюата идентифицируют (см. выше Этап 2) и смешивают.
Этап 8. Полученную смесь обессоливают на колонке с гелем Sephadex G-25 (М). Для этого используют колонку размерами 15 х 200 мм) с гелем, уравновешенным трис-НСl буфером. После нанесения смеси на колонку, элюцию ведут трис-НСl буфером (0,01 М, рН = 8,0), при скорости 200 мл/час. Объем собираемых фракций - 5 мл.
Этап 9. В обессоленный раствор (объемом около 20 мл и имеющий концентрацию белка 0,02 - 0,03 мг/мл) вносят сахарозу до 2%, азид натрия до 0,01%, разливают по 1,0 мл в стеклянные пенициллиновые флаконы и лиофильно высушивают.
Таким образом, из 100 мг кристаллического яда змеи Agkistrodon saxatilis получают 0,4 - 0,6 мг АПС.
Молекулярная масса полученного белка составляет 100 ± 10 Кд (по данным гель-фильтрации), изоэлектрическая точка равна 4,0 ± 0,5 (по данным изоэлектрофореза в полиакриламидном геле).
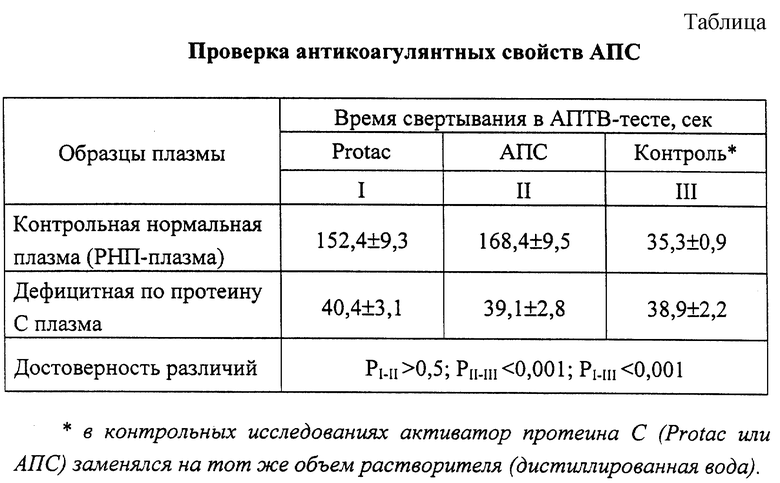
Проверка антикоагулянтных свойств АПС
Для проверки способности полученного АПС активировать протеин С исследовали антикоагулянтный эффект в системе АПТВ контрольной нормальной плазмы (РНП-плазмы). Для этой цели в регистрирующую ячейку коагулометра вносили 0,1 мл АПТВ-реагента, 0,1 мл контрольной нормальной плазмы и 0,1 мл раствора АПС (или 0,1 мл раствора Protac). В контроле вместо одного из активаторов протеина С добавляли тот же объем дистиллированной воды. Смесь инкубировали 5 минут при +37oС, после чего вносили 0,1 мл 0,025М СаCl2 и регистрировали время образования сгустка.
Как видно из таблицы, время свертывания контрольной нормальной плазмы значительно удлиняется после добавления как раствора Protac, так и раствора АПС. В это же время добавление дистиллированной воды не давало антикоагулянтного эффекта.
Для подтверждения механизма антикоагулянтных свойств полученного АПС оценивали АПТВ в дефицитной по протеину С плазме, куда вносился АПС или Protac. Как видно из той же таблицы, в дефицитной по протеину С плазме нет удлинения времени свертывания после добавления как полученного АПС, так и раствора Protac.
Таким образом, получаемый АПС из яда змеи Agkistrodon saxatilis имеет антикоагулянтные свойства, которые реализуются через протеин С (аналогично известной фракции яда змеи Agkistrodon contortrix - Protac).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ТРОМБИНОПОДОБНОГО КОАГУЛИРУЮЩЕГО ФЕРМЕНТА | 2002 |
|
RU2262947C2 |
| ШТАММ ASPERGILLUS OCHRACEUS - ПРОДУЦЕНТ ПРОТЕИНАЗЫ - АКТИВАТОРА ПРОТЕИНА С ПЛАЗМЫ КРОВИ ЧЕЛОВЕКА | 2011 |
|
RU2461616C2 |
| ШТАММ ASPERGILLUS OCHRACEUS - ПРОДУЦЕНТ ПРОТЕИНАЗЫ - АКТИВАТОРА ПРОТЕИНА С ПЛАЗМЫ КРОВИ ЧЕЛОВЕКА | 2011 |
|
RU2461614C2 |
| ШТАММ ASPERGILLUS OCHRACEUS - ПРОДУЦЕНТ ПРОТЕИНАЗЫ - АКТИВАТОРА ПРОТЕИНА С ПЛАЗМЫ КРОВИ ЧЕЛОВЕКА | 2011 |
|
RU2461615C2 |
| ШТАММ ASPERGILLUS OCHRACEUS - ПРОДУЦЕНТ ПРОТЕИНАЗЫ - АКТИВАТОРА ПРОТЕИНА С ПЛАЗМЫ КРОВИ ЧЕЛОВЕКА | 2011 |
|
RU2460772C2 |
| СПОСОБ ПОЛУЧЕНИЯ ТРОМБИНОПОДОБНЫХ ФЕРМЕНТОВ ИЗ ЯДА ЗМЕИ | 2004 |
|
RU2271219C1 |
| ПРЯМОЙ ИНГИБИТОР ТРОМБИНА, ОБЛАДАЮЩИЙ АНТИПРОЛИФЕРАТИВНЫМ ДЕЙСТВИЕМ | 2007 |
|
RU2369615C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОТЕИНАЗЫ - АКТИВАТОРА ПРОТЕИНА С ПЛАЗМЫ КРОВИ | 2011 |
|
RU2468081C2 |
| СПОСОБ ДИАГНОСТИКИ ТРОМБОФИЛИИ, ОБУСЛОВЛЕННОЙ РЕЗИСТЕНТНОСТЬЮ ФАКТОРА V К АКТИВИРОВАННОМУ ПРОТЕИНУ C | 1996 |
|
RU2129282C1 |
| СПОСОБ ПОЛУЧЕНИЯ АКТИВАТОРА ПЛАЗМИНОГЕНА | 2007 |
|
RU2346983C1 |
Изобретение относится к медицине и может быть использовано для исследования крови. Выделяют белковую фракцию из яда змеи Agkristrodon saxatilis путем адсорбции и элюции. Изобретение позволяет расширить арсенал реагентов для лабораторной диагностики. 1 табл.
Способ получения активатора протеина С, заключающийся в выделении белковой фракции из яда змей семейства Agkristrodon путем адсорбции и элюции, отличающийся тем, что в качестве источника активатора протеина С используют яд змеи Agkristrodon saxatilis.
| Trombosis Reseach, v.43, 1986, № 3, p.252-264 | |||
| MARTINOLI J.L | |||
| и др | |||
| Fust functional protein C assoy using Protac a novel protein C activotor | |||
| US 4849403 A, 18.07.1989 | |||
| RU 215646802 C2, 20.09.2000 | |||
| Способ определения активности антитромбина- @ в плазме крови при гепаринотерапии | 1984 |
|
SU1193587A1 |
| СПОСОБ ДИАГНОСТИКИ ТРОМБОФИЛИИ, ОБУСЛОВЛЕННОЙ РЕЗИСТЕНТНОСТЬЮ ФАКТОРА V К АКТИВИРОВАННОМУ ПРОТЕИНУ C | 1996 |
|
RU2129282C1 |
| DE 4041570 A1, 25.06.1992 | |||
| EP 0814164 A2, 29.12.1997 | |||
| Рейдовый причал | 1982 |
|
SU1050960A1 |
Авторы
Даты
2002-07-10—Публикация
2000-11-30—Подача