Изобретение относится к области медицины, в частности к исследованию крови, и может быть использовано для лабораторной диагностики тромбофилии, обусловленной генетическим дефектом фактора V, в результате чего последний приобретает резистентность к активированному протеину C (АПС).
Существует два подхода к диагностике этой формы тромбофилии. Известен способ диагностики тромбофилии путем определения точечной мутации фактора V с помощью цепной полимеразной реакции (PCR-assay) [Bertina R.M., Koeleman B. P.C., Koster T., Rosendaal F.R., Dirven R.J., de Ronde H., van der Velden R. A. , Reitsma P.H. // Mutation in blood coagulation factor V associated with resistance to activated protein C. // Nature, 1994, 369, p.64-67; Dahlback В. // Factor V gene mutation causing inherited resistance to activated protein C as a basis for venous thromboembolism. // J. Internal Medicine, 1995, 237, p. 221-227]. Однако известный способ трудоемок, требует оснащения лаборатории специальным дорогостоящим оборудованием и не может быть использован в повседневной диагностической практике.
Известен способ диагностики тромбофилии, основанный на определении недостаточной способности АПС удлинять свертывание плазмы в активированном парциальном тромбопластиновом тесте (АПТТ). При тромбофилии обусловленной резистентностью фактора V к АПС, время свертывания в этом тесте удлиняется в значительно меньшей степени, чем в контрольной нормальной плазме, в которой АПТТ удлиняется в 2.1 и более раз [Dahlback В., Carlson М., Svensson P..J. // Familial thrombophilia due to a previously unrecognized mechanism characterized by poor anticoagulant response to activated protein C: Prdiction of a cofactor to activated protein C. // Proc.Natl.Acad.Sci.USA, 1993, 90, 1004-8; Gerotriatas G.T., Pithara E., Van Dreden P., Manris P.E. // Comparison of two functional assays for the determination of activated protein С resistance (APC - resistance). First study in Greece. // Thromb.Haemost., 1995, V. 73, N 6, Abst.1781, p.1365]. Известный способ более экономичен и быстро выполним [Dahlback В. // Resistance to Activated Protein С, the Arg506 to Gln Mutation in Factor V Gene, and Venous Thrombosis. Functional tests and DNA-based Assays, Pros and Cons. // Thromb.Haemost, 1995, V.73, N 5, p. 739-742]. Однако для его использования необходимы специальные реактивы: 1) плазма, лишенная фактора V, 2) активированный протеин С. Последний реактив особенно дефицитен и недоступен большинству лабораторий, что делает невозможной диагностику этой формы тромбофилии. Однако в течение ряда лет многие фирмы предлагают в качестве реагента для лабораторных исследований очищенный активатор протеина С из яда щитомордника (Agkistrodon contortrix), - "Protac" (производители: "Behringwerke AG", "Sigma", "BioMerieux" и др.). Этот реагент во многих клинических лабораториях используется для определения содержания протеина С.
Прототипом предлагаемого способа диагностики тромбофилии, обусловленной резистентностью к АПС, является классический метод, предложенный Dahlback [Dahlback В. , Carlson М., Svensson P.J. // Familial thrombophilia due to a previously unrecognized mechanism characterized by poor anticoagulant response to activated protein C: Prediction of a cofactor to activated protein C. // Proc. Natl. Acad. Sci. USA, 1993, 90, 1004-8], основанный на выявлении недостаточного удлинения свертывания в АПТТ после добавления в исследуемую плазму активированного протеина С. В дальнейшем предложены модификации способа, в которых для повышения чувствительности к аномалии фактора V в тест-систему вводят дефицитную по фактору V плазму. Однако существенными недостатками способа являются малая доступность реагента, содержащего стабилизированный активированный протеин С, и недостаточная специфичность диагностикума, поскольку ложноположительные результаты реакции наблюдаются при антифосфолипидном синдроме - наличии в исследуемой плазме антител к мембранным фосфолипидам или волчаночного антикоагулянта (ВА) [Ehrenforth S., Radtke K. P., Zwinge B., Siegert S., Scharrer I. // Acquired APC-resistance in patients with lupus anticoagulants. // Thrombosis and Haemostasis, 1995, V. 73, N 6, Abst. 1791, p. 1368]. Это затрудняет интерпретацию результатов исследования.
Положительными результатами предложенного способа являются получение доступного реагента, содержащего активированный протеин С и достаточное количество факторов свертывания для коагуляции в АПТТ кроме фактора V, такое видоизменение способа прототипа, которое исключало бы получение ложноположительных результатов, связанных с эффектом ВА. Положительные результаты достигаются тем, что для получения основного реагента - активированного протеина С - используют нормальную плазму, лишенную фактора V, но содержащую стандартное количество протеина С, а активация последнего достигается добавлением протака, для устранения эффектов ВА в тесте используют тромбоцитарные фосфолипидные мембраны. Известно, что тромбоциты корригируют гипокоагуляцию в тестируемой смеси, вызываемую ВА [Антикоагулянты волчаночного типа. Клиническое значение, диагностика, лечение. // Методические рекомендации, Барнаул, 1993, с. 11]. В предложенном способе используют компонент тромбоцитарных фосфолипидных мембран, полученный из нормальных тромбоцитов, позволяющий исключить эффект ВА, "Тромбоцитин" фирмы "Технология-Стандарт".
Способ осуществляют следующим образом.
Реактивы и оборудование
1) 3.8% (0.1М) раствор цитрата натрия. Получают растворением 3.8 г тринатрия-цитрата в 100 мл дистиллированной воды.
2) 1.32% (0.1М) раствор оксалата натрия. Получают растворением 1.32 г вещества в 100 мл дистиллированной воды.
3) Буфер Михаэлиса, pH 7.4.
4) Каолин, (легкая фракция) фирма "Технология-Стандарт" (Барнаул), концентрация 0.025 мг/мл, хранится при +2...8 C, (реагент готов к употреблению) перед применением встряхивается до получения гомогенной суспензии.
4) Кефалин фирмы "Технология-Стандарт", флакон содержит 30 мг лиофильно высушенного кефалина, полученного из тканевого тромбопластина человека.
5) Тромбоцитин, фирмы "Технология-Стандарт", 1 мг лиофилизированного препарата отмытых тромбоцитов здорового человека.
6) Хлорид кальция 0.025 М раствор фирмы "Технология-Стандарт".
7) Активатор протеина C из яда (Agkistrodon contortrix) "Protac" (протак) производитель "Behringwerke AG".
8) Центрифуга ОПН-8.
Приготовление реагентов и исследуемых образцов плазмы.
Приготовление раствора кефалина. Во флакон с кефалином вносят 2,0 мл дистиллированной воды. Встряхиванием в течение 1 - 2 минут добиваются гомогенности эмульсии. В результате получают 1,5% эмульсию, которую хранят при температуре +2...+8 C и используют в течение месяца.
Приготовление каолин-кефалиновой смеси. Смешивают 0,1 мл эмульсии кефалина с 3 мл взвеси каолина (0,25 мг/мл).
Приготовление раствора тромбоцитина. Во флакон с сухим тромбоцитином вносят 1,0 мл дистиллированной воды, получают маточный раствор, который хранят при температуре +2...+8oC в течение 2 недель. Для получения рабочего раствора тромбоцитина 0,05 мл маточного раствора необходимо смешать с 5,0 мл буфера Михаэлиса. Используется в день исследования.
Приготовление рабочего раствора протака. Для приготовления рабочего раствора протака необходимо развести активатор протеина C "Protac" в 2 мл буфера Михаэлиса.
Приготовление исследуемой плазмы. Кровь получают из локтевой вены силиконированной иглой в пластиковую пробирку, содержащую 3.8% раствор цитрата натрия (соотношение крови и цитрата 9:1). Кровь центрифугируют 5 мин при 1000 об/мин (200g). Полученную богатую тромбоцитами плазму повторно центрифугируют в течение 20 мин при 3500 об/мин (1200g). Полученную бедную тромбоцитами плазму (БТП) разводят буфером Михаэлиса в соотношении 1:3. Разведенную БТП используют для проведения исследования.
Приготовление лишенной фактора V плазмы донора. Из нормальной донорской крови, стабилизированной оксалатом натрия, получают БТП двойным центрифугированием - вначале 5 мин при 1000 об/мин (200g), затем 20 мин при 3500 об/мин (200g). Полученную БТП инкубируют на водяной бане в течение 24 часов при +37oC, затем расфасовывают по 1 мл в пластиковые пробирки и замораживают при температуре -20oC. Эта бедная тромбоцитами плазма, лишенная фактора V, может храниться в течение двух месяцев. В день проведения анализа ее размораживают и используют для выполнения исследования. Контрольные определения показали, что в этой плазме содержится менее 5% фактора V, тогда как активность протеинов C и S колеблется в пределах 60 - 66% (График). Протромбиновое время такой плазмы должно быть не менее 60 c.
Приготовление реагента, содержащего АПС путем активации протеина C в стандартной БТП, лишенной фактора V, осуществляют следующим образом. B две пробирки добавляют по 0.05 мл лишенной фактора V плазмы донора. В первую пробирку вносят 0.05 мл протака. Во вторую пробирку вместо протака добавляют 0.05 мл буфера Михаэлиса (контроль). Инкубируют на водяной бане обе пробирки 3 мин при температуре +37o.
Ход определения.
1) В первую пробирку с 0.1 мл плазмы, лишенной фактора V, содержащей АПС, после указанной инкубации добавляют 0.1 мл разведенной исследуемой плазмы, 0.1 мл каолин-кефалиновой смеси, 0.05 мл рабочего раствора тромбоцитина, инкубируют смесь на водяной бане 3 мин при температуре +37oC, после чего к ней добавляют 0.1 мл раствора хлорида кальция. Регистрируют время свертывания (t1) при непрерывном помешивании.
2) Во вторую пробирку с 0.1 мл разведенной лишенной фактора V плазмы после инкубации добавляют 0.1 мл разведенной исследуемой плазмы 0.1 мл каолин-кефалиновой смеси, 0.05 мл рабочего раствора тромбоцитина, инкубируют смесь на водяной бане 3 мин при температуре +37o, после чего в нее добавляют 0.1 мл раствора хлорида кальция. При помешивании регистрируют время свертывания (t2).
Оценка полученных результатов.
Определяют отношение Rк для нормальной плазмы и RБ для плазмы исследуемого больного по формулам:
Rк=t1к/t2к
RБ=t1Б/t2Б
В номер Rк превышает 2.1. У больных с резистентностью к АПС это отношение (RБ) снижается пропорционально степени этой резистентности: при умеренной резистентности отношение (RБ) снижается в пределах 2.1 - 1.8, при значительной степени резистентности отношение снижается в пределах 1.79 - 1.5, снижение отношения ниже 0.5 расценивается как тяжелая форма резистентности фактора V в активированному протеину C.
Расчет нормализованного отношения NR:
NR=RБ/Rк
Результаты теста считаются положительными, если NR<0.8.
Провести исследование резистентности фактора V, используя заявляемый способ, доступно большинству лабораторий в медицинских учреждениях. Плазма без фактора V легко приготавливается по описанному выше способу. Она содержит достаточное количество факторов свертывания и антикоагулянтов (протеина C и протеина S) кроме фактора V (График). Для активации протеина C к старой оксалатной плазме добавляют реагент "Protac". Использование плазмы без фактора V позволяет существенно повысить чувствительность заявляемого способа к дефекту исследуемого фактора и исключить влияние на результаты теста антикоагулянтов непрямого действия и дефицита витамин K-зависимых факторов свертывания, поскольку в добавляемой стандартной оксалатной БТП содержится нормальное содержание всех факторов свертывания кроме фактора V.
Заявляемый способ высоко специфичен, его показания зависят только от резистентности АПТТ к АПС и не зависят от влияния BA, действие которого устраняется тромбоцитином.
Для оценки воспроизводимости способа использовано определение коэффициента вариации (в %) при многократном исследовании одних и тех же образцов нормальной плазмы и плазмы больных с резистентностью к протеину C. Заявляемый способ показал хорошую воспроизводимость. Коэффициент вариации не превышал 7%.
Примеры практического использования способа.
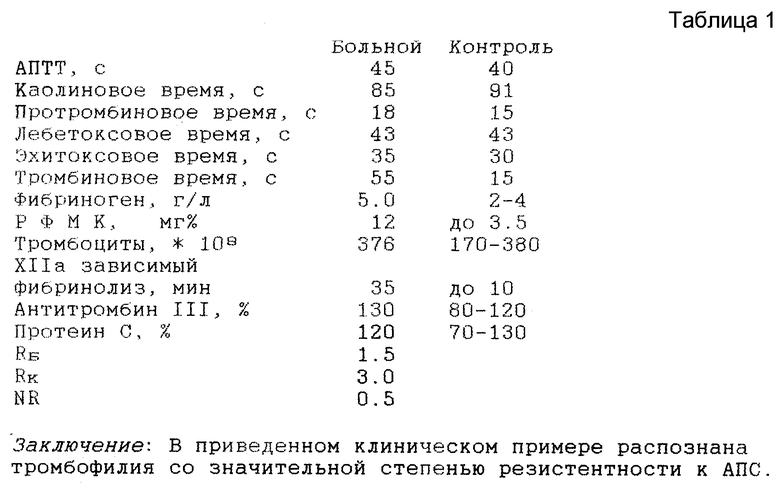
1. Больная В. Г. , 32 лет, поступила в отделение сосудистой хирургии 16.01.96 с жалобами на отеки нижних конечностей, наличие варикозно расширенных вен и мокнущих язв в области голени. Больна с двенадцатилетнего возраста, когда перенесла острый тромбоз поверхностных и глубоких вен голени слева. В 1990 году после удаления варикозно расширенных вен слева в раннем послеоперационном периоде развился тромбоз глубоких вен правой голени. В 1991 году на медиальной поверхности левой голени возникла трофическая язва, которая постепенно увеличилась в размерах. В 1994 году возникла трофическая язва на правой голени. К моменту обследования у больной выявлены отек в области обеих голеней, трофическая язва размером 10•15 см в области левой голени и язва размером 5•8 см на правой голени.
Исследование системы гемостаза 3.1.96 (см. табл.1).
2. Больной Н.Е., 28 лет, поступил в отделение сосудистой хирургии краевой клинической больницы 8.02.96 с жалобами на отеки нижних конечностей, интенсивные боли в области голеней, повышение температуры тела. Болен с 2.02.96, когда без видимой причины появился отек правой нижней конечности, а через 6 часов - отек левой нижней конечности и повысилась температура до 37.8oС. К моменту обследования у больного нижние конечности отечны, цианотичны, болезненны в области голеней. Назначены непрямые антикоагулянты ().
Исследование системы гемостаза 26.2.96 (см. табл.2).
3. Больной В. В. , 43 года, поступил в отделение сосудистой хирургии 28.02.96 с жалобами на одышку при физической нагрузке, колющие боли в грудной клетке справа, сердцебиение, головокружение. Заболевание началось в 39 лет, когда без видимой причины возникла тромбоэмболия в бассейне легочной артерии.
Лечился в отделении сосудистой хирургии. Такие же симптомы возникли 20.02.96, по поводу чего был вновь госпитализирован. Частота дыхания 26 в 1 мин. Число сердечных сокращений 108 в мин. На ЭКГ ритм правильный, синусовая тахикардия (110 в 1 мин) электрическая ось сердца отклонена вправо. Определяются ЭКГ - признаки нагрузки на правый желудочек. На обзорной рентгенограмме органов грудной клетке выявлена инфильтрация справа в нижнем легочном поле. При сканировании легких отмечено ухудшение кровотока в правом легком, а при каваграфии выявлен флотирующий тромб в правой общей подвздошной вене. Диагностирован тромбоз подвздошной вены, осложненный ТЭЛА. Назначены непрямые антикоагулянты (фенилин), имплантирован кава-фильтр "Волан" в нижнюю полую вену.
Исследование системы гемостаза 11.3.96 (см. табл.3).
Заявляемый способ позволяет выявить резистентность фактора V к АПС (клинические примеры NN1, 2). У больного с неидентифицированной тромбофилией этот тест отрицателен (клинический пример N3). На результаты теста не оказывает влияние лечение непрямыми антикоагулянтами (пример N2 и N3). Таким образом, заявляемый способ позволяет снизить стоимость, повысить его доступность для большинства лабораторий и исключить ложноположительные реакции при антифосфолипидном синдроме, при этом способ сохраняет высокую воспроизводимость, характерную для способа-прототипа.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ДИАГНОСТИКИ ТРОМБОФИЛИИ, ОБУСЛОВЛЕННОЙ РЕЗИСТЕНТНОСТЬЮ ФАКТОРА V К АКТИВИРОВАННОМУ ПРОТЕИНУ С | 2001 |
|
RU2205411C2 |
| СПОСОБ КОНТРОЛЯ ЭФФЕКТИВНОСТИ ЗАМЕСТИТЕЛЬНОЙ ТЕРАПИИ ПРИ ДВС-СИНДРОМЕ | 2000 |
|
RU2190855C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ВОЛЧАНОЧНОГО АНТИКОАГУЛЯНТА | 1999 |
|
RU2181203C2 |
| СПОСОБ ДИАГНОСТИКИ АНТИФОСФОЛИПИДНОГО СИНДРОМА | 1995 |
|
RU2104550C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ ГЕПАРИНА | 2003 |
|
RU2249819C2 |
| СПОСОБ ДИАГНОСТИКИ ТРОМБОФИЛИИ, ОБУСЛОВЛЕННОЙ ВЫСОКОЙ АКТИВНОСТЬЮ КОАГУЛЯЦИОННОГО ФАКТОРА VIII | 2002 |
|
RU2227918C1 |
| Способ прогнозирования преэклампсии у беременных при носительстве мутации гена фактор V Лейден 1691 генотип G/A и А/А | 2016 |
|
RU2636228C1 |
| Способ прогнозирования исхода беременности при угрожающих преждевременных родах | 2016 |
|
RU2630573C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АКТИВИРОВАННОГО ФАКТОРА VII В ПЛАЗМЕ КРОВИ | 1991 |
|
RU2034298C1 |
| СПОСОБ ДИАГНОСТИКИ ДИСПЛАЗМИНОГЕНЕМИИ | 2006 |
|
RU2336529C2 |


Способ может быть использован в области медицины, в частности для исследования крови в лабораторной диагностике тромбофилии, обусловленной генетическим дефектом фактора, в результате чего последний приобретает резистентность к активированному протеину С. Для активации протеина С добавляют активатор протеина С в стандартную оксалатную плазму и лишенную фактора V плазму и добавляют в исследуемую смесь фосфолипидные мембраны тромбоцитов. Диагностику осуществляют определением нормализованного отношения (NR) как отношения показателя RБ плазмы исследуемого больного, представляющего собой отношение времени свертывания плазмы больного, плазмы, лишенной фактора V и содержащей активированный протеин С, к времени свертывания разведенной плазмы больного, плазмы, лишенной фактора V, к показателю Rк для нормальной плазмы, представляющей собой такое же отношение времени свертывания для этой плазмы, и при значении NR<0,8 результаты теста считают положительными. Способ более прост в исполнении, высоко специфичен, c хорошей воспроизводимостью. 1 ил., 3 табл.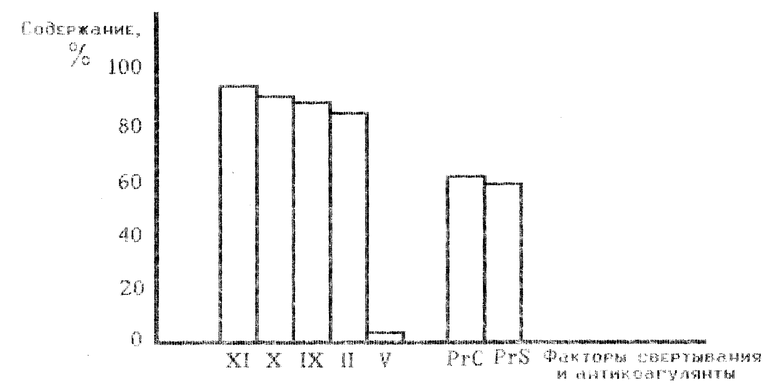
Способ диагностики тромбофилии, обусловленной резистентностью фактора V к активированному протеину С путем применения активированного протеина С для коагуляции в активированном парциальном тромбопластиновом тесте (АПТТ), отличающийся тем, что для активации протеина С добавляют активатор протеина С (протак) в стандартную плазму, лишенную фактора V, и в исследуемую смесь фосфолипидных мембран тромбоцитов, а диагностику осуществляют определением нормализованного отношения (NR), как отношения показателя Rб для плазмы исследуемого больного, представляющего собой отношение времени свертывания плазмы больного, плазмы, лишенной фактора V и содержащей активированный протеин С, к времени свертывания разведенной плазмы больного, плазмы, лишенной фактора V, к показателю Rк для нормальной плазмы, представляющей собой такое же отношение времени свертывания для этой плазмы, и при значении NR < 0,8 результаты теста считают положительными.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Dahlback B., Svensson P.J | |||
| Familial thrombophilia due to a previously unrecognized mechanism characferised by poor anticoagulant Pesponse to activated protein C | |||
| Proc | |||
| Nath | |||
| Acad | |||
| Sci | |||
| USA, 1983, 90.2 | |||
| Гематология и трансфузиология | |||
| Механическая топочная решетка с наклонными частью подвижными, частью неподвижными колосниковыми элементами | 1917 |
|
SU1988A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| RU 2058031 С1, 10.04.96. | |||
Авторы
Даты
1999-04-20—Публикация
1996-08-05—Подача