Область техники
Настоящее изобретение относится к новому производному 5-замещенного-3-оксадиазолил-1,6-нафтиридин-2(1Н)-она или к его фармацевтически приемлемой кислой аддитивной соли, которое является пригодным в качестве лекарственного средства, к его применению в качестве лекарственного препарата и к промежуточным соединениям для получения указанного производного.
Предшествующий уровень техники
Соединения бензодиазепина (БДА), например диазепам, который является характерным представителем таких соединений, обладают анксиолитической активностью, и поэтому они разрабатывались как анксиолитические средства, но, кроме того, они обладают противосудорожным, седативным и гипнотическим действием, и поэтому эти соединения применяют в широком диапазоне областей медицины, например в качестве (1) анксиолитического средства, (2) седативного (гипнотического) средства, (3) миорелаксанта и (4) противоэпилептического лекарственного средства.
Соединения БДА обладают, главным образом, такими фармакологическими действиями, как: (1) адаптирующее действие, (2) гипнотическое действие, (3) действие, вызывающее миорелаксацию, (4) противосудорожное действие. Понятно, что указанные действия проявляются не за счет отдельно взятого независимого механизма, а вызваны близкородственными нейрофармакологическими механизмами.
После 70-х годов с развитием фармакологических исследований БДА соединений были найдены две концепции объяснения механизма проявления их действий, одна из которых представляет собой явление, состоящее в усилении γ-аминобутирокислотного агонистического GABA-эргического нейромедиаторного механизма центральной нервной системы за счет применения БДА лекарственных средств, и другая концепция основана на недавнем обнаружении сайта специфического связывания БДА (рецептор БДА) и доказательстве механизма функциональной связи между рецептором БДА головного мозга и рецептором GABA. В результате этих исследований было установлено, что GABA-эргический нейромедиаторный механизм принимает участие в фармакологических активностях БДА соединений.
Введение БДА соединений вызывает побочные эффекты, например атаксию, гипноз, миорелаксацию или снижение познавательной способности или способности к непроизвольному движению и в дальнейшем невосприимчивость лекарственных средств и лекарственную зависимость, и поэтому для устранения возникающих проблем БДА соединения целесообразно усовершенствовать. Были проведены исследования иных соединений, чем БДА, которые имеют химическую структуру, отличающуюся от структуры БДА соединений, но выполняющих при этом аналогичные функции в механизмах активации. Эти соединения, включающие такие небензодиазепиновые соединения, называют лекарственными веществами, обладающими сродством к рецептору бензодиазепина. В качестве небензодиазепиновых соединений известны, например, соединения, имеющие химические формулы (А), (В) и (С), которые показаны ниже.
Соединения, имеющие формулы (А) и (В) раскрыты в: Journal of Medicinal Chemistry, vol. 34, p. 2060 (1991).
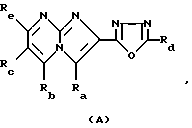
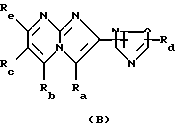
где Ra является атомом водорода, Rb-Rd представляют метильную группу и т.д., и Re является метоксильной группой и т.д.
Соединения формулы (С) представлены в ЕР А2-0588500.
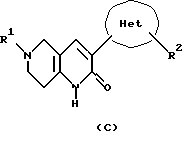
где Het является оксадиазолильной группой, R1 является бензильной группой и т.д., и R2 является метоксильной группой и т.д.
Однако при дальнейших исследованиях среди небензодиазепиновых соединений было найдено определенное соединение, которое имеет подобное высокоселективное сродство к рецептору бензодиазепина (БДА), но которое при этом обладает совершенно противоположной активностью [Braestrup, С. et al., Neuropharmacol, 22, pp. 1451-1457 (1983)]. При приеме этих соединений они проявляют такие фармакологические активности, как: активность, увеличивающую судороги, активность, стимулирующую тревогу, мышечную гипертонию. Поэтому, ранее известные БДА соединения, которые до сих пор применялись в качестве антифобических успокаивающих средств, определены как агонисты, и соединения, имеющие обратные активности, определены как обратные агонисты.
С тех пор как были обнаружены обратные агонисты, проводились интенсивные исследования в отношении корреляции между способом модификации (связывания) и фармакологическими активностями соединений, которые связываются (проявляют сродство) с рецептором БДА. В соответствии с этими исследованиями было обнаружено, что рецептор БДА находится между рецептором GABA (депрессивный нейромедиатор) и каналом для хлоридиона и представляет собой образующую комплекс молекулярную ячейку. Рецептор GABA включает рецептор канала иона типа GABAA и рецептор типа GABAB, регулирующий обмен веществ, и рецептор GABAA образует комплекс с рецептором БДА и каналом для иона хлора. Соединения, связываемые с рецептором БДА, теперь можно классифицировать как агонисты (которые далее подразделены на полные агонисты и частичные агонисты) и обратные агонисты (которые далее подразделены на полные обратные агонисты и частичные обратные агонисты) и антагонисты.
Агонист селективно связывается с соединениями БДА и вследствие этого оказывает влияние на увеличение связывания рецептора GABA и канала для иона Сl, усиливает протекание иона Сl в клетки благодаря увеличению частоты открывания-закрывания канала для иона хлора и затем стимулирует вследствие уменьшения отрицательного электрического заряда активности клеток (увеличивается стимуляция клеток). Считается, что антагонист не изменяет функцию связывания, а ингибирует связывание агониста или обратного агониста с рецептором БДА.
Существует много методов контроля способа связывания соединений с рецептором бензодиазепина, и одним из известных методов является анализ связывания TBPS. Как упоминалось ранее, рецептор GABAA образует комплекс с рецептором БДА соединения и каналом для иона хлора, и известно, что в мембране рецептора GABAA присутствует нейростероидный рецептор, и вокруг канала для иона хлора расположен сайт для опознания TBPS (трет-бутилбициклофосфонотионата). Функция GABA в отношении нервной системы модифицируется и регулируется путем регуляции отверстия канала для иона Сl и переноса иона Сl в клетки в комплексной молекуле рецептора GABAA при осложненных совместных действиях. Известно, что при проверке многих лекарственных средств, которые действуют непосредственно или косвенно на функцию комплекса рецептора GABAA, установлено, что между данными испытаний связывания TBSP и данными испытаний включения иона Сl в клетки имеется хорошая обратная корреляция. Так например, включение иона Сl в клетки уменьшается через посредство агонистов рецептора GABAA (например, мускимола), агонистов нейростероидного рецептора, диазепама, который является характерным агонистом рецептора бензодиазепина, или хлоназепама, который является частичным агонистом и увеличивается через посредство обратного агониста рецептора бензодиазепина [например, DMCM (метил-6, 7-диметокси-4-этил- (β -карболин-3-карбоксилата)] и частичного обратного агониста [например, FG7142 (N-метил- β -карболин-3-карбоксамида)].
Соответственно анализ связывания TBPS является пригодным для пояснения функции рецептора САБАл, биохимического исследования in vitro лекарственных средств, действующих через посредство сайта аллостерического связывания бензодиазепиновых лекарственных средств, комплекса рецептора САВАд и т.д. и механизма действия лекарственных средств.
Большинство из ранее известных соединений БДА, например соединений формул (А), (В) и (С), имеют агонистические свойства. С другой стороны, некоторые соединения имеют наоборот противоположные агонистические свойства, например соединения следующих формул (D) и (Е) (DMCM и FG7142):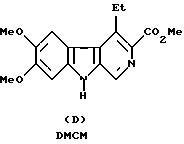
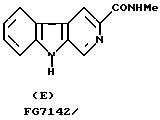
DMCM и FG7142 раскрыты в: Colin R. Gardner, Drugs of the Future, vol. 14, pp. 51-67 (1987).
Кроме этого, многие исследования проводились в отношении корреляции между способом связывания с рецептором бензодиазепина и фармакологическими активностями соединений. Как упоминалось выше, агонисты БДА применяют в качестве анксиолитического средства средства для лечения гипнотических расстройств (лекарственного средства, вызывающего сон) или противоэпилептического средства, но известно, что кроме этих активностей, они также вызывают потерю памяти у животных, включая людей. Соответственно ожидается, что обратные агонисты БДА будут иметь активность, обратную активности, вызывающей потерю памяти, т.е. противоамнезийную активность, психоаналептическую активность. Кроме того, известно, что активность ацетилхолина, который является важным в отношении функции познавательной способности, уменьшается через посредство агонистов БДА, и поэтому предполагается, что обратные агонисты БДА будут проявлять активность, увеличивающую познавательную способность. Таким образом, ожидается, что обратные агонисты БДА могут быть пригодны в качестве психоаналептического лекарственного средства и лекарственного средства для лечения дисмнезии при старческом слабоумии, цереброваскулярном слабоумии и болезни Альцгеймера.
В литературе не имеется сообщений, касающихся соединений настоящего изобретения, которые имеют приведенную здесь выше формулу (I), обладают высокоселективным сродством к рецептору бензодиазепина и в особенности действуют как обратный агонист БДА.
Описание изобретения
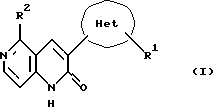
Это изобретение предусматривает новое производное 5-замещенного-3-оксадиазолил-1,6-нафтиридин-2(1Н)-она, имеющее следующую формулу (I):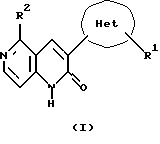
где Het является оксадиазолильной группой,
R1 является атомом водорода, низшей алкильной группой, цикло-низшей алкильной группой, трифторметильной группой, низшей алкенильной группой, низшей алкинильной группой, низшей алкоксильной группой, низшей алкокси-низшей алкильной группой, гидрокси-низшей алкильной группой, замещенной или незамещенной арильной группой или замещенной или незамещенной гетероароматической группой, и
R2 является атомом водорода, низшей алкильной группой, цикло-низшей алкильной группой, цикло-низшей алкилметильной группой, низшей алкенильной группой, цикло-низшей алкенильной группой, низшей алкинильной группой, замещенной или незамещенной арильной группой или замещенной или незамещенной гетероароматической группой,
или его фармацевтически приемлемую кислую аддитивную соль, которые обладают высокоселективным сродством к рецептору бензодиазепина, и применение их в качестве лекарственного средства.
Кроме того, это изобретение предусматривает новые производные 1,6-нафтиридин-2(1Н)-она формулы (I'),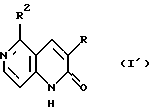
где R является цианогруппой, карбамоильной группой, карбоксильной группой, низшей алкоксикарбонильной группой или замещенной или незамещенной бензилоксиарбонильной группой, и
R2 является низшей алкильной группой, цикло-низшей алкильной группой, низшей алкенильной группой, цикло-низшей алкенильной группой, низшей алкинильной группой, замещенной или незамещенной арильной группой или замещенной или незамещенной гетероароматической группой, при условии, что R2 не является метильной группой или пиридильной группой, которые являются пригодными в качестве промежуточных соединений для получения производных 5-замещенного-3-оксадиазолил-1,6-нафтиридин-2(1Н)-она вышеприведенной формулы (I), полезных в качестве лекарственного средства.
Во время интенсивных исследований небензодиазепиновых соединений, имеющих сродство к интрацеребральному рецептору бензодиазепина, заявители настоящего изобретения обнаружили, что производные 5-замещенного-3-оксадиазолил-1,6-нафтиридин-2(1Н)-она вышеприведенной формулы (I) обладают высокоселективным сродством к рецептору бензодиазепина (БДА) и, следовательно, являются пригодными в качестве агонистического лекарственного средства, обладающего сродством к рецептору бензодиазепина и, что, кроме того, эти соединения включают соединение, обладающее агонистической активностью БДА, и соединение, обладающее обратной агонистической активностью БДА, которые зависят от видов комбинаций заместителей R1 и R2.
Среди соединений настоящего изобретения предпочтительными соединениями являются соединения формулы (I), в которых R1 является C1-С3-алкильной группой, С3-С4-циклоалкильной группой или С2-С3-алкенильной группой и R2 является атомом водорода, С1-С4-алкильной группой, С3-С6-циклоалкильной группой, замещенной или незамещенной арильной группой или замещенной или незамещенной гетероароматической группой.
Более предпочтительными соединениями являются соединения формулы (I), где R1 является C1-С3-алкильной группой или С3-С4-циклоалкильной группой и R2 является атомом водорода, C1-С3-алкильной группой, С3-С4-циклоалкильной группой, замещенной или незамещенной фенильной группой или замещенной или незамещенной гетероароматической группой.
Кроме того, предпочтительными соединениями являются следующие соединения:
3-(5-этил-1,2,4-оксадиазол-3-ил)-5-(2-метилциклопропил)-1,6-нафтиридин-2(1Н)-он,
3-(5-метил-1,2,4-оксадиазол-3-ил)-5-(2-метилфенил)-1,6-нафтиридин-2(1Н)-он,
3-(5-метил-1,2,4-оксадиазол-3-ил)-5-(3-метоксифенил)-1,6-нафтиридин-2(1Н)-он,
3-(5-метил-1,2,4-оксадиазол-3-ил)-5-(4-метоксифенил)-1,6-нафтиридин-2(1Н)-он,
3-(5-этил-1,2,4-оксадиазол-3-ил)-5-(2-тиенил)-1,6-нафтиридин-2(1Н)-он,
3-(5-метил-1,2,4-оксадиазол-3-ил)-5-(4-пиридил)-1,6-нафтиридин-2(1Н)-он,
3-(3-этил-1,2,4-оксадиазол-5-ил)-5-метил-1,6-нафтиридин-2(1Н)-он,
3-(3-этил-1,2,4-оксадиазол-5-ил)-5-(3-фторфенил)-1,6-нафтиридин-2(1Н)-он,
3-(3-метил-1,2,4-оксадиазол-5-ил)-5-(3-метилфенил)-1,6-нафтиридин-2(1Н)-он,
3-(3-метил-1,2,4-оксадиазол-5-ил)-5-(3-метоксифенил)-1,6-нафтиридин-2(1Н)-он,
3-(3-этил-1,2,4-оксадиазол-5-ил)-5-(4-метоксифенил)-1,6-нафтиридин-2(1Н)-он,
3-(3-этил-1,2,4-оксадиазол-5-ил)-5-(4-пиридил)-1,6-нафтиридин-2(1Н)-он и
3-(3-циклопропил-1,2,4-оксадиазол-5-ил)-5-(3-тиенил)-1,6-нафтиридин-2(1Н)-он.
Фармацевтически приемлемая кислая аддитивная соль соединения формулы (I) включает соли с неорганической кислотой, такие как гидрохлорид, гидробромид, гидройодид, сульфат, фосфат и аддититвные соли с органической кислотой, такие как оксалат, малеат, фумарат, малонат, лактат, малат, цитрат, тартрат, бензоат, метансульфонат или тозилат.
Приведенные в описании термины "низшая алкильная группа" и фрагмент группы "низший алкил" означают алкильную группу с прямой или разветвленной цепью, имеющую от 1 до 6 атомов углерода, например метильную, этильную, пропильную, изопропильную, бутильную, изобутильную, трет-бутильную, пентильную и гексильную группы.
Термин "цикло-низшая алкильная группа" означает циклоалкильную группу, имеющую от 3 до 6 атомов углерода, например циклопропильную, циклобутильную, циклопентильную и циклогексильную группы, где кольцо может быть замещено C1-С3-алкильной группой или атомом галогена.
Термин "низшая алкенильная группа" и "низшая алкинильная группа" имеют прямую или разветвленную цепь, имеющую от 2 до 6 атомов углерода, и включают, например, аллильную, 1-пропенильную, пропаргильную и 2-метил-1-этинильные группы.
Термин "цикло-низшая алкенильная группа" означает циклоалкильную группу, имеющую от 5 до 6 атомов углерода, например циклогексенильную группу.
Термин "низшая алкоксильная группа" и фрагмент группы "низший алкокси" означают алкоксильную группы с прямой или разветвленной цепью, имеющую от 1 до 6 атомов углерода, и включают, например, метоксильную, этоксильную, пропоксильную, изопропилокси-, бутилокси-, изобутилокси-, трет-бутилокси-, пентилокси- и гексилоксигруппы.
Термин "арильная группа" и фрагмент группы "арил" означают фенильную группу или нафтильную группу, и их кольцо может необязательно иметь от 1 до 3 заместителей, выбранных из атома галогена, C1-С3-алкильной группы, трифторметильной группы, гидроксильной группы, C1-С3-алкоксильной группы, трифторметоксильной группы, цианогруппы и аминогруппы и нитрогруппы.
Термин "гетероароматическая группа" означает 5- или 6-членную ароматическую гетероциклическую группу, содержащую от 1 до 2 одинаковых или различных гетероатомов, выбранных из атома азота, атома кислорода и атома серы, и включает, например, фурильную, тиенильную, пирролильную, оксазолильную, изоксазолильную, пиридильную, пиридазинильную и пиримидинильную группы, причем эти гетероароматические группы могут необязательно иметь от 1 до 3 заместителей, выбранных из атома галогена, C1-С3-алкильной группы, гидроксильной группы, C1-С3-алкоксильной группы и аминогруппы.
В "замещенной или незамещенной бензоксикарбонильной группе" заместитель выбирают из C1-С3-алкильной группы, C1-С3-алкоксильной группы, цианогруппы и нитрогруппы.
Термин "атом галогена" означает атом фтора, хлора, брома или йода.
Соединения этого изобретения могут быть получены способами 1-4, которые приведены ниже.
(Способ 1)
Соединение формулы (Iа)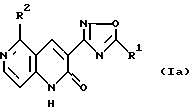
где R1 имеет значения, определенные выше, исключая алкоксигруппу и R2 имеет значения, определенные выше,
или формулы (Ib)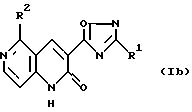
где R1 имеет значения, определенные выше, исключая алкоксигруппу, и R2 имеет значения, определенные выше, могут быть получены реакцией внутримолекулярной циклизации соединения формулы (II)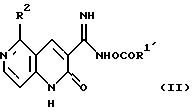
или формулы (III)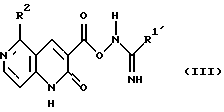
где в формуле (II) и (III) R1' является таким же, как R1, и иным, чем низшая алкоксильная группа, и R2 является таким, как он определен выше.
Реакцию циклизации можно осуществить в присутствии дегитратирующего агента, но ее можно также осуществить путем нагревания соединения в соответствующем растворителе, который не оказывает влияния на реакцию. Растворитель включает ароматические углеводороды (например, бензол, толуол, ксилол), простые эфиры (например, тетрагидрофуран, диоксан), N,N-диметилформамид. Эти растворители могут быть использованы в отдельности или в виде комбинации, состоящей из двух или более растворителей. Температура реакции может изменяться в зависимости от вида исходных веществ и т.д., но обычно она находится в диапазоне от 50 до 150oС, предпочтительно от 80 до 120oС.
(Способ 2)
Когда в соединении формулы (Ia) R1 является низшей алкоксигруппой, соединения могут быть получены реакцией внутримолекулярной циклизации соединения формулы (IV)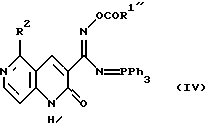
где R1" является низшей алкоксигруппой, Ph означает фенильную группу и R2 является таким, как он определен выше, способом, который описан, например, в: Synthesis, p. 843 (1986).
Реакцию циклизации обычно осуществляют путем нагревания исходного соединения в соответствующем растворителе. Растворитель включает ароматические углеводороды (например, бензол, толуол, ксилол), простые эфиры (например, тетрагидрофуран, диоксан). Температура реакции может изменяться в зависимости от вида исходных веществ и т.д., но обычно она находится в диапазоне от 50 до 150oС, предпочтительно от 80 до 120oС.
(Способ 3)
Когда в соединении формулы (Ib) R1 является низшей алкоксигруппой, соединение может быть получено взаимодействием соединения формулы (V)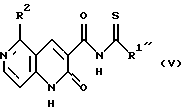
где R1 является низшей алкокси группой и R2 является таким, как он определен выше,
с гидроксиламином способом, подобным тому, который описан, например, в: Journal of Heterocyclic Chemistry, vol. 18, p. 1197 (1981).
Реакцию обычно осуществляют в соответствующем растворителе. Растворитель включает спирты (например, метанол, эта-нол) и воду. Температура реакции может изменяться в зависимости от вида исходных веществ и т.д., но обычно она находится в диапазоне от 50 до 90oС.
(Способ 4)
Соединение формулы (Iс)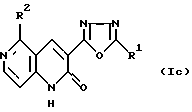
где R1 и R2 являются такими, как определены выше, может быть получено реакцией внутримолекулярной циклизации соединения формулы (VI)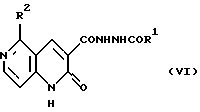
где R1 и R2 являются такими, как определены выше.
Реакцию циклизации можно осуществить в присутствии осушителя, но обычно ее осуществляют путем нагревания соединения в соответствующем растворителе, который не оказывает влияния на реакцию. Растворитель включает ароматические углеводороды (например, бензол, толуол, ксилол), простые эфиры (например, тетрагидрофуран, диоксан), N,N-диметилформамид. Эти растворители могут быть использованы в отдельности или в виде комбинации, состоящей из двух или более растворителей. Температура реакции может изменяться в зависимости от вида исходных веществ и т.д., но обычно она находится в диапазоне от 50 до 150oС, предпочтительно от 80 до 120oС.
Реакцию циклизации можно также осуществить в соответствующем растворителе, который не оказывает влияния на реакцию, в присутствии трехвалентного соединения фосфора (например, трифенилфосфина) и сложного эфира диалкилазодикарбоновой кислоты способом, подобным тому, который описан в ЕР-А2-0588500. Температура реакции может изменяться в зависимости от вида исходных веществ и т. д. , но обычно она находится в диапазоне от 0 до 110oС, предпочтительно от 0 до 60oС.
Соединения (I) этого изобретения, полученные вышеописанными способами 1-4, могут быть выделены и очищены общепринятыми методами, такими как хроматография, перекристаллизация или повторное осаждение.
Соединения (I) этого изобретения могут быть получены в зависимости, например, от вида выбранных исходных веществ, подлежащих применению, от условий реакции и методов, в форме свободного основания или его аддитивной кислой соли. Аддитивная кислая соль может быть превращена в свободное основание путем обработки ее обычным основанием, например карбонатом щелочного металла и гидроксидом щелочного металла. Кроме того, свободное основание может быть превращено в аддитивную кислую соль путем обработки его обычным способом различными кислотами.
Способы получения исходных соединений объяснены ниже.
Соединения формул (II) - (VI), применяемые в вышеприведенных способах 1-4, являются новыми соединениями и могут быть получены способом, который показан на следующей реакционной схеме 1.
Реакционная схема 1.
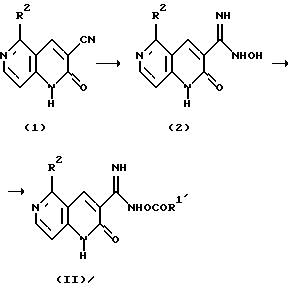
где R1' является таким же, как R1, исключая низшую алкоксигруппу, и R2 является таким, как он определен выше.
Соединение (1) подвергают взаимодействию с гидроксиламином обычным способом с получением соединения (2), которое подвергают взаимодействию с реакционноспособным в карбоксильной группе производным карбоновой кислоты формулы: R1'COOH (где R1' является таким, как он определен выше) в присутствии основания с получением соединения формулы (II).
Применяемое в вышеприведенном способе 1 соединение формулы (III) может быть получено способом, показанным на следующей реакционной схеме 2.
Реакционная схема 2.
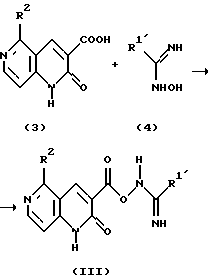
где R1' является таким же, как R1, исключая низшую алкоксигруппу, и R2 является таким, как он определен выше.
Соединение (3) или его реакционноспособное в карбоксильной группе производное подвергают взаимодействию с различными амидоксимами (4) в условиях реакции, применяемых в обычном амидировании, с получением соединения формулы (III).
Применяемое в вышеприведенном способе 2 соединение формулы (IV) может быть получено способом, показанным на следующей реакционной схеме 3.
Реакционная схема 3.
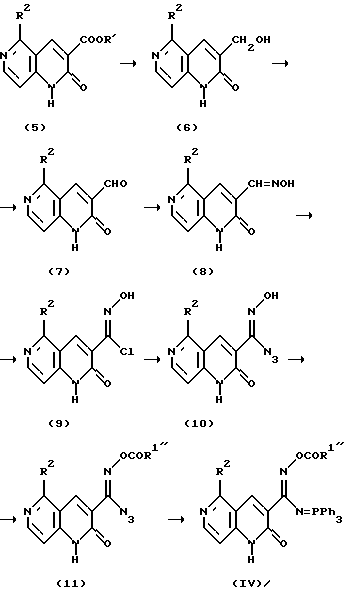
где R1" является низшей алкоксигруппой, R1 является низшей алкильной группой или замещенной или незамещенной бензильной группой, Ph означает фенильную группу и R2 является таким, как он определен выше.
Соединение (5) восстанавливают восстанавливающим агентом, таким как боргидрид натрия, боргидрид тетрабутиламмония, литийалюминийгидрид, в соответствующем растворителе с получением соединения (6), которое затем окисляют активным диоксидом марганца в соответствующем растворителе с получением соединения (7).
Соединение (7) подвергают взаимодействию с гидроксиламином при условиях, применяемых для обычной реакции образования оксима, с получением соединения (8), которое затем подвергают взаимодействию с N-хлорсукцинимидом способом, подобным тому, который описан, например, в: Journal of Organic Chemistry, vol. 45, p. 3916 (1980) с получением соединения (9).
Соединение (9) подвергают взаимодействию с азидом натрия в соответствующем растворителе способом, подобным тому, который описан, например, в: Synthesis, p. 102 (1979) с получением соединения (10), которое затем подвергают взаимодействию с соединением формулы: XCOR1" (где Х является атомом галогена и R1" является низшей алкоксигруппой) в соответствующем растворителе способом, подобным тому, который описан, например, в: Synthesis, p. 843 (1986) с получением соединения (11), которое затем подвергают взаимодействию с трифенилфосфином с получением соединения формулы (IV).
Применяемое в вышеприведенном способе 3 соединение формулы (V) может быть получено способом, показанным на следующей реакционной схеме 4.
Реакционная схема 4.
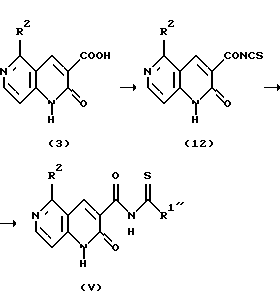
где R1" является низшей алкоксигруппой, и R2 является таким, как он определен выше.
Соединение (3) или его реакционноспособное в карбоксильной группе производное подвергают взаимодействию с тиоцианатом щелочного металла в соответствующем растворителе с получением соединения (12), которое затем подвергают алкоголизу с получением соединения (V).
Применяемое в вышеприведенном способе 4 соединение формулы (VI) может быть получено способом, показанным на следующей реакционной схеме 5.
Реакционная схема 5.
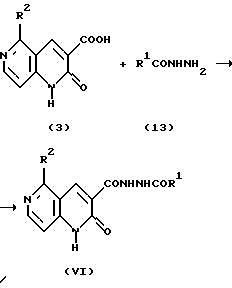
где R1 и R2 являются такими, как они определены выше.
Соединение (3) или его реакционноспособное в карбоксильной группе производное подвергают взаимодействию с гидразидом (13) формулы R1ONHNH2 (где R1 является таким, как он определен выше) посредством обычной реакции амидирования с получением соединения формулы (VI).
Соединение формулы (VI) может быть также получено двухстадийной реакцией, т.е. взаимодействием соединения (3) или его реакционноспособного в карбоксильной группе производного с гидразином в обычной реакции амидирования и последующего взаимодействия полученного соединения с реакционноспособным в карбоксильной группе производным карбоновой кислоты формулы R1OOH (где R1 является таким, как он определен выше).
Способ получения промежуточного соединения формулы (I') объяснен ниже.
Соединения формулы (I'), где R является цианогруппой или карбоксильной группой, т. е. соединение (1) и соединение (3), применяемые в реакционной схеме 1 и реакционной схеме 2, могут быть получены способом, который описан, например, в: Journal of Heterocyclic Chemistry, vol. 21, p. 2085 (1990) или в: Journal of Medicinal Chemistry, vol. 35, p. 4858 (1992), который показан на следующей реакционной схеме 6.
Реакционная схема 6.
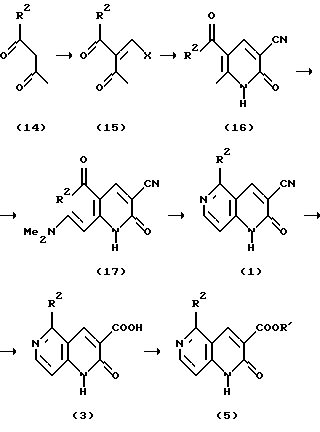
где Х является динизшей алкиламиногруппой, циклической аминогруппой, гидроксильной группой, атомом галогена или низшей алкоксигруппой, R' является низшей алкильной группой или замещенной или незамещенной бензильной группой, и R2 является таким, как он определен выше.
Как видно из реакционной схемы, соединение (16) может быть получено взаимодействием соединения (14) с N,N-диметилформамиддиметилацеталем или сложным эфиром ортомуравьиной кислоты в соответствующем растворителе способом, подобным тому, который описан, например, в: Heterocycles, vol. 29, р. 1517 (1989) или в: Journal of Heterocyclic Chemistry, vol. 27, p. 511 (1990) с получением соединения (15) и последующего его взаимодействия с цианоацетамидом в присутствии соответствующего основания.
Полученное таким способом соединение (16) затем подвергают взаимодействию с N,N-диметилформамиддиметилацеталем в соответствующем растворителе с получением соединения (17), которое после этого подвергают взаимодействию с аммиаком или солью аммония в соответствующем растворителе с получением соединения (1). Полученное таким способом соединение (1) гидролизуют кислотой или щелочью обычным способом с получением соединения (3).
Кроме того, соединения формулы (I'), где R является низшей алкоксикарбонильной группой или замещенной или незамещенной бензилоксикарбонильной группой, например соединения (5), могут быть получены этерификацией соединения (1) или соединения (3) посредством обычного способа.
Фармакологические эксперименты
Фармакологические свойства соединений (I) настоящего изобретения проиллюстрированы следующими экспериментами с представителями соединений.
Эксперимент 1. Анализ связывания рецептора бензодиазепина
Анализ связывания рецептора бензодиазепина проводили в соответствии с методом, раскрытым в: Life Science, vol. 20, р. 2101 (1977).
Неочищенную фракцию синаптической пластины, полученной из мозга крыс Wistar (возрастом от 7 до 8 недель) суспендировали в 15 мМ буфера Трис-НСl (рН 7,4), содержащего 118 мМ хлорида натрия, 4,8 мМ хлорида калия, 1,28 мМ хлорида кальция и 1,2 мМ сульфата магния при концентрации мозга 1 г (масса во влажном состоянии) на 20 мл буфера с получением источника мембраны рецептора. В качестве меченого лиганда применяли [3Н]-диазепам.
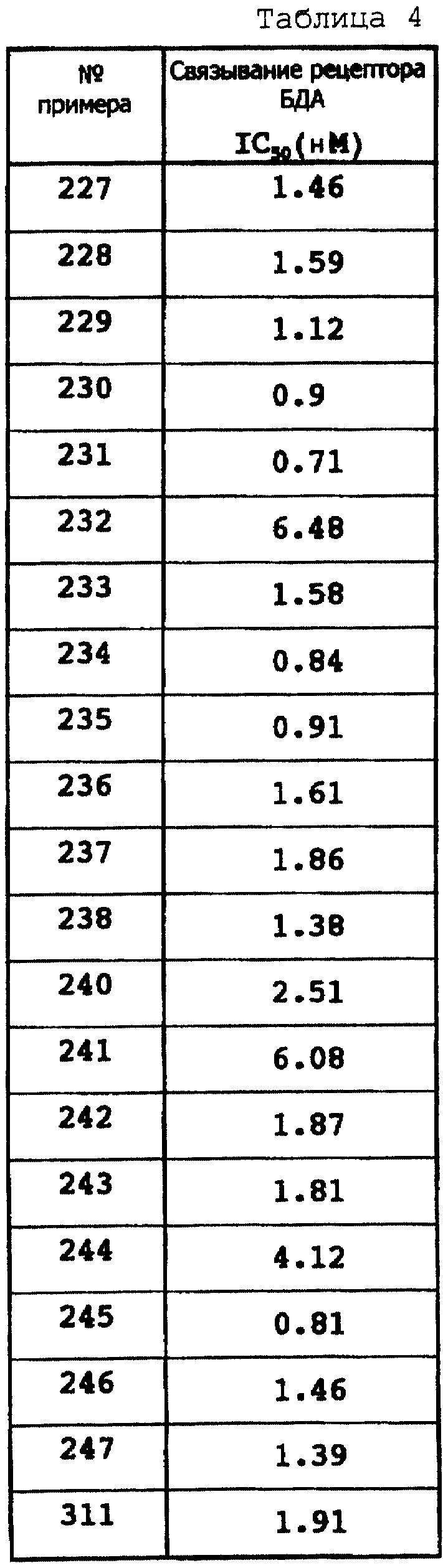
В пробирку (конечный объем: 1 мл) добавили испытуемое соединение (известное количество), [3Н]-диазепам (конечная концентрация 1,5 нМ), мембрану рецептора и вышеприведенный буфер. Реакцию инициировали добавлением мембраны рецептора. Пробирку инкубировали при 0oС в течение 20 минут, и реакционную смесь подвергли быстрой фильтрации через стекловолоконный фильтр Whatman GF/B, прикрепленный к приспособлению для сбора клеток, выросших в культуре (изготовленному Brandell). Сразу же после фильтрации собранную, связанную с меченым лигандом мембрану рецептора три раза промывали 50 мМ трис-НСl буфера (рН 7,7, 5 мл для каждой промывки)? охлажденного льдом. Для определения количества [3Н] -диазепама, связанного с мембраной рецептора (полное связывание), посредством сцинтилляционного счетчика для жидких радиоактивных веществ измеряли радиоактивность на фильтре. Отдельно повторяли эти же самые процедуры, за исключением того, что добавляли 1 мкм диазепама и таким образом измеряли количество [3Н]-диазепама, связанного с мембраной рецептора (неспецифическое связывание). Для получения специфического связывания из полного связывания вычли неспецифическое связывание. На основе полученного таким образом специфического связывания достоверно определяли ингибирующую активность (IC50) испытуемого соединения.
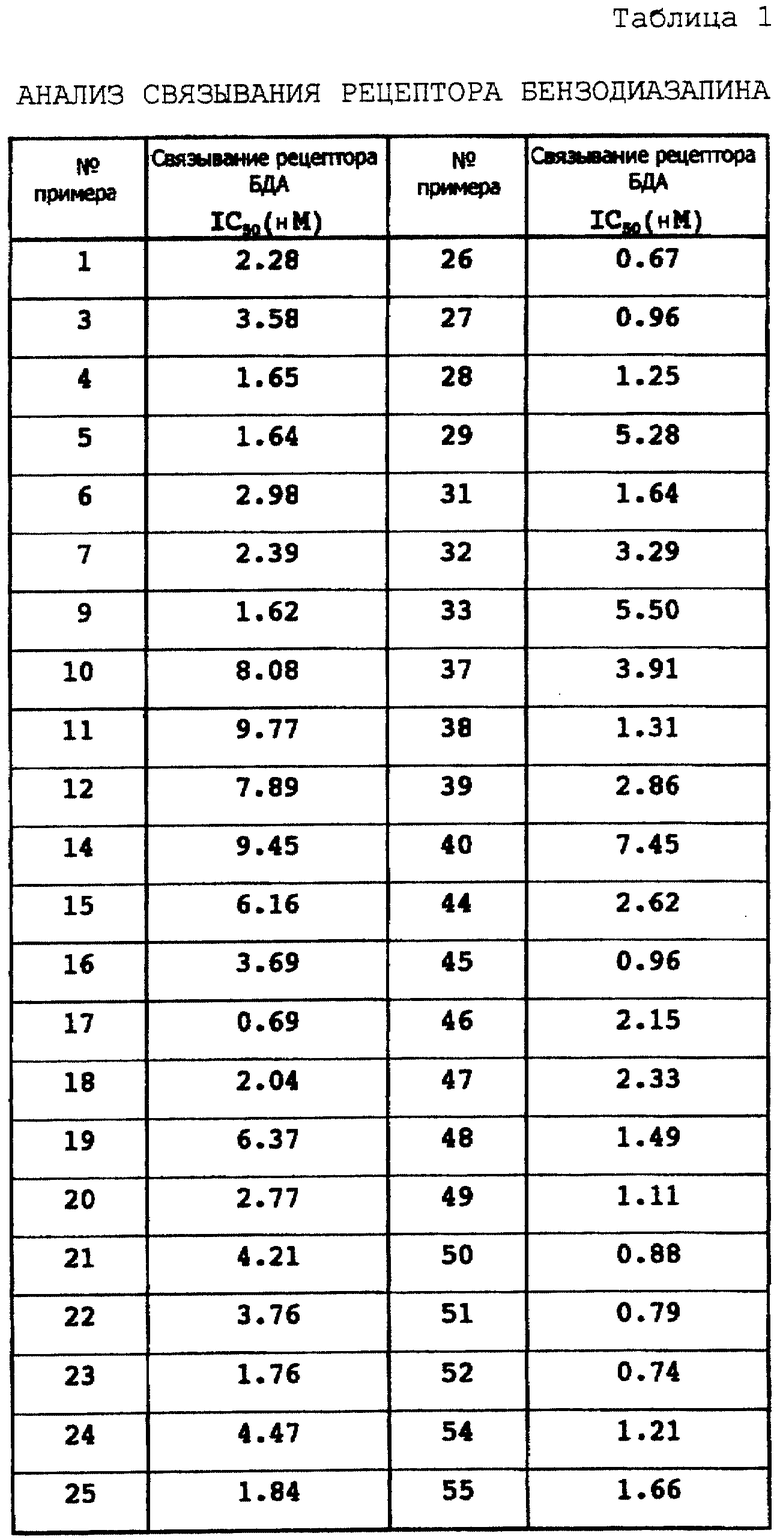
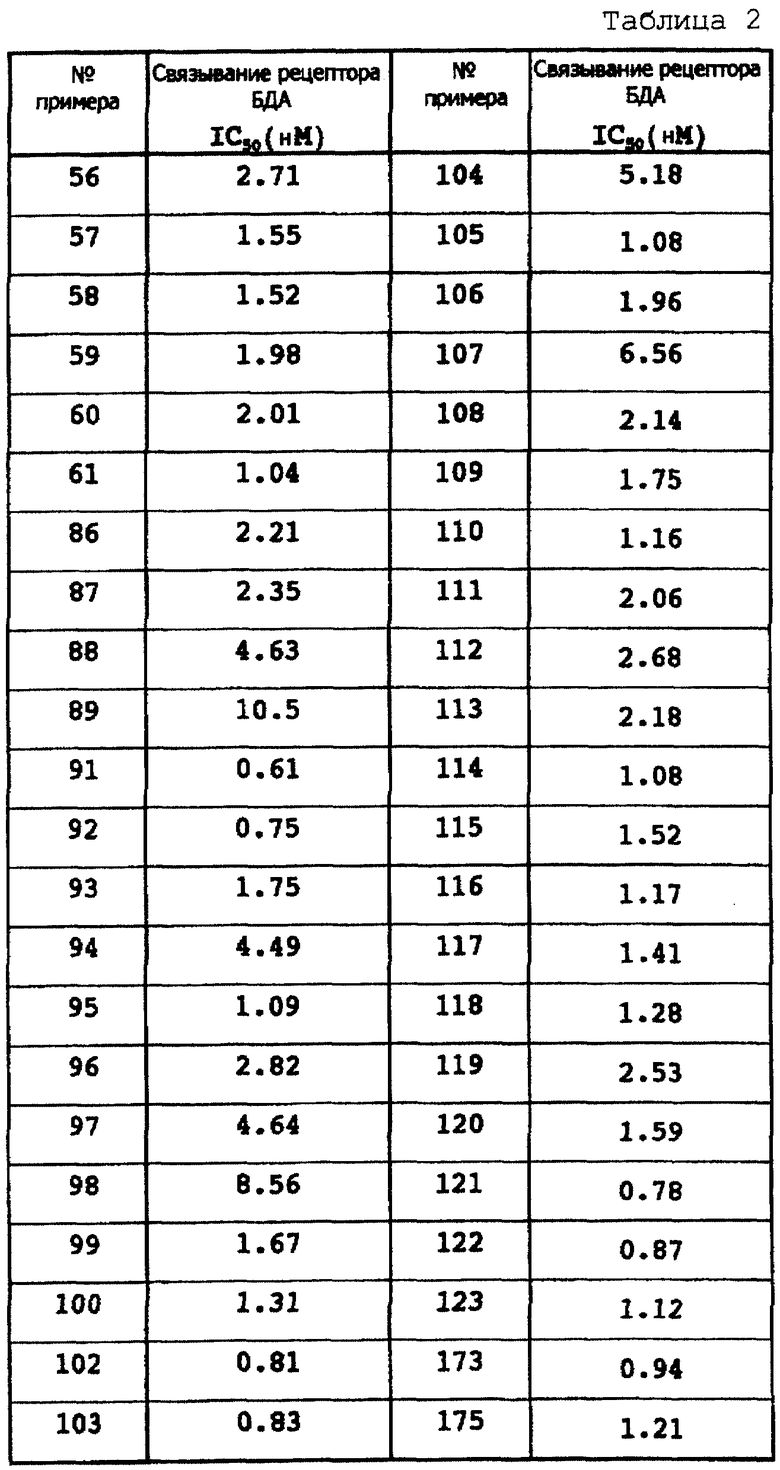
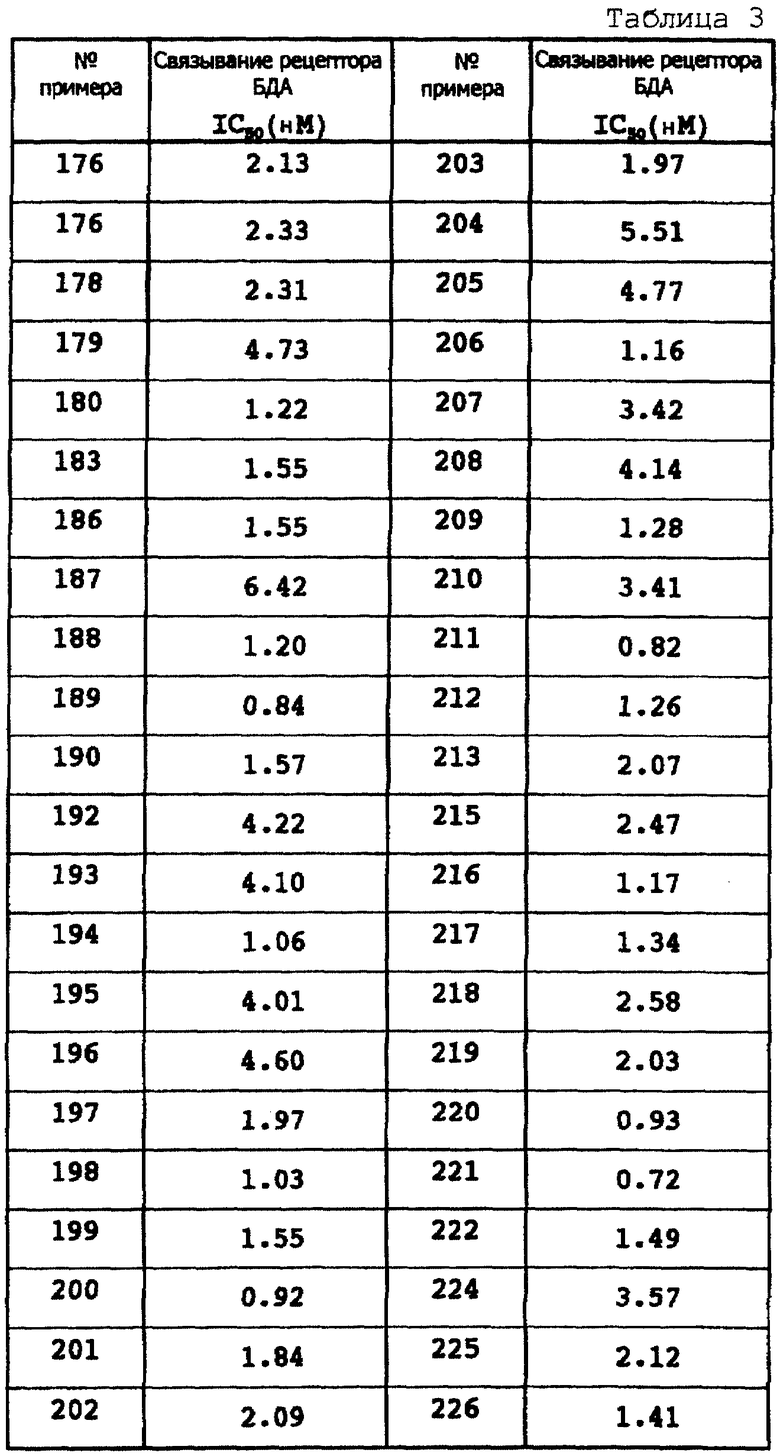
Результаты показаны в следующих таблицах 1-4.
Эксперимент 2. Анализ связывания TBPS
(Метод)
Анализ связывания TBPS (трет-бутилбициклофосфонотионата) и получение образца мембраны осуществили способом, подобным тому, который описан Biggio, G. et al. [сравни: European Journal of Pharmacology, vol. 161, pp. 173-180 (1989)].
Образец мембраны получили из коры головного мозга крыс Wistar (возрастом от 7 до 8 недель) посредством следующей процедуры. К коре головного мозга добавили 50-кратный объем охлажденного льдом буфера (50 мМ трис-цитратного буфера, содержащего 100 мМ хлорида натрия, рН 7,4) и смесь гомогенизировали при 0-4oС и затем центрифугировали при 20000 g в течение 20 минут. Полученные таким образом гранулы сразу же подвергали гомогенизации в буфере и центрифугированию посредством той же самой процедуры, которая описана выше, и затем выдерживали в замороженном состоянии при -80oС в течение более 20 часов. В день испытаний замороженные гранулы оттаивали и затем дважды подвергали описанной выше процедуре гомогенизации-центрифугирования. Полученные таким образом гранулы суспендировали в буфере при концентрации 1 г (масса во влажном состоянии) на 25 мл буфера с получением образца мембраны, применяемого в анализе связывания.
Анализ связывания осуществляли посредством следующей процедуры с применением в качестве меченого лиганда [35S] TBPS (конечная концентрация 0,4 нМ) и в качестве немеченого лиганда Picrotoxin (пикротоксина) (конечная концентрация 100 мкм) в присутствии GABA (конечная концентрация 1 мкм).
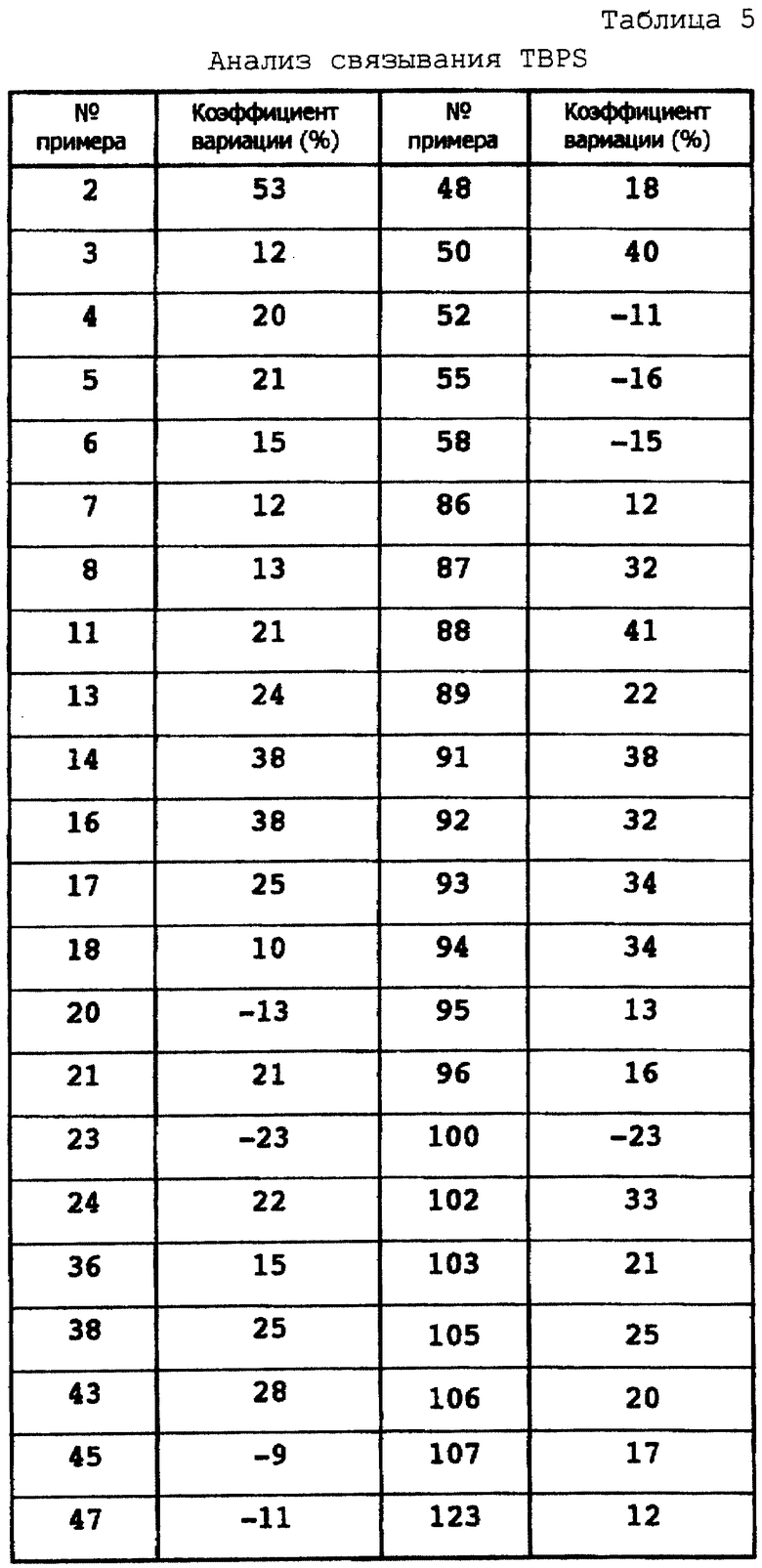
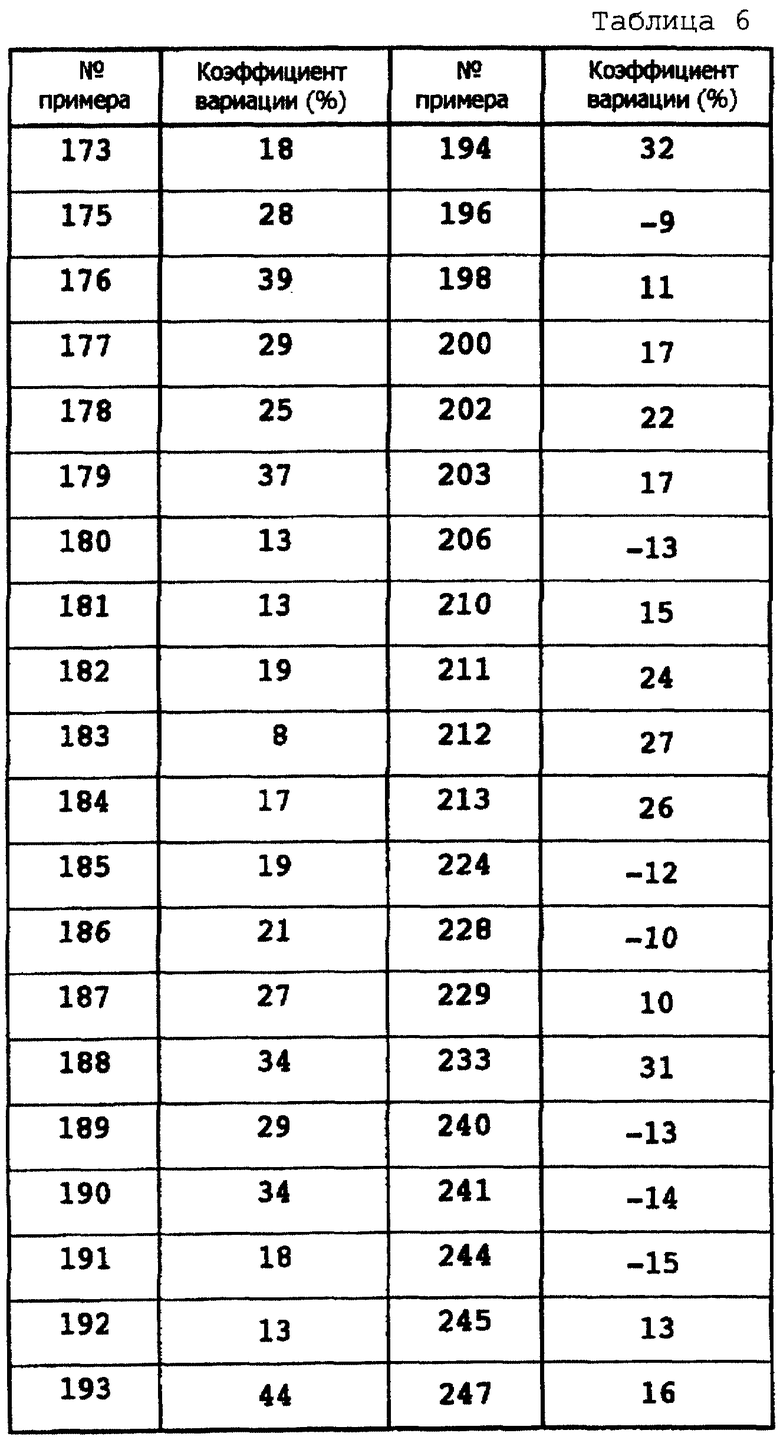
В пробирку (конечный объем 1 мл) добавляли испытуемое соединение (известное количество), меченый лиганд [35S], образец мембраны, GABA и буфер. Реакцию инициировали добавлением образца мембраны (200 мкл). Пробирку инкубировали при 25oС в течение 90 минут, и реакцию завершали фильтрацией через стекловолоконный фильтр Wattman GF/B (который предварительно на один день погрузили в 0,01% полиэтиленимин), прикрепленный к приспособлению для сбора клеток, выросших в культуре (изготовленному Brandell), и вследствие этого связанную с меченым лигандом мембрану собирали на фильтре. Сразу же после фильтрации собранную, связанную с меченым лигандом мембрану три раза промывали 50 мМ трис-НСl буфера (рН 7,7, 5 мл для каждой промывки), охлажденного льдом. Затем фильтр помещали в пробирку для жидких радиоактивных веществ и добавляли в нее смесь для сцинтилляции жидкости (ACS-II, производимую Amersham, США, 10 мл) и выдерживали в течение заданного количества времени. После этого для определения величины полного связывания посредством сцинтилляционного счетчика для жидких радиоактивных веществ (тип 2000СА, изготавливаемый Paccard, США) измеряли радиоактивность на фильтре. Для определения величины неспецифического связывания отдельно повторяли эти же самые процедуры в присутствии Picrotoxin (пикротоксина). Из величины полного связывания вычли величину неспецифического связывания, при этом получили величину специфического связывания. Связывающую активность испытуемого соединения вычислили с помощью коэффициента вариации, т.е. отношения величины специфического связывания испытуемого соединения к величине специфического связывания контрольного соединения (с применением растворителя).
(Критерий оценки)
Значение +% означает проявление обратных агонистических свойств, значение -% означает проявление агонистических свойств и 0% означает проявление антагонистических свойств.
Результаты показаны в таблицах 5 и 6.
Эксперимент 3. Испытание влияния роста активности на вызванные пентилентетразолом судороги
Известно, что обратные агонисты рецептора бензодиазепина увеличивают судороги, вызванные пентилентетразолом [смотри: Progress in Neuro-Psychopharmacology and Biological Psychiatry, vol. 12, p. 951 (1988)]. Некоторые соединения настоящего изобретения испытывали на их способность увеличивать вызванные пентилентетразолом судороги.
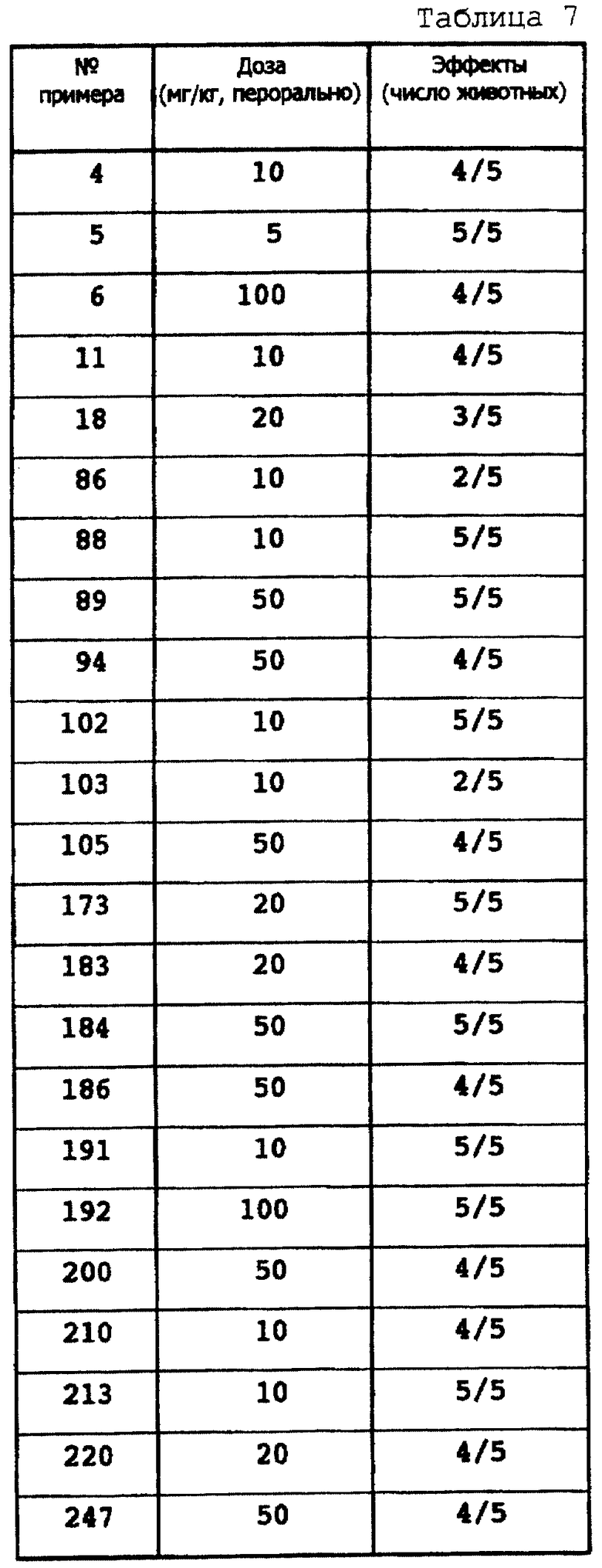
Испытуемое соединение (соединения, приведенные в рабочих примерах) вводили перорально мышам-самцам ddy (масса тела 22-25 г, пять мышей/группу) в количестве 5-100 мг/кг. Через 15 минут мышам подкожно вводили пентилентетразол (70 мг/кг - количество вышеуказанного соединения, которое в отдельности не вызывает тонические судороги), и сразу же мышей в течение 30 минут обследовали на появление тонических судорог в задней части ноги. Результаты выражали в виде числа мышей, взятых из пяти, у которых наблюдалось увеличение судороги. Результаты показаны в таблице 7.
Как следует из вышеприведенных результатов, соединения, представленные в настоящем изобретении, показали высокоселективное сродство к рецептору бензодиазепина и, следовательно, они являются пригодными в качестве лекарственного средства, действующего на рецептор бензодиазепина. Хотя некоторые из соединений этого изобретения обладают также агонистическими свойствами, соединения этого изобретения являются в особенности пригодными в качестве обратного агониста. Ожидается, что соединения, имеющие обратные агонистические свойства, можно будет использовать, например, в качестве психоаналептического средства или лекарственного средства для лечения дисмнезии при старческом слабоумии или болезни Альцгеймера в клинических областях, полностью отличающихся от областей, в которых применяются агонисты.
Фармацевтическое применение соединений этого изобретения
Когда соединения этого изобретения применяют в качестве лекарственного средства, действующего на рецептор бензодиазепина, их можно ввести или перорально, парентерально? или внутриректально, но предпочтительно перорально. Доза соединений изменяется в зависимости от способа их введения, состояния и возраста больных или от вида лечения (например? с целью профилактики заболеваний или их лечения) и подобных факторов, но обычно она находится в диапазоне от 0,01 до 10 мг/кг/день, предпочтительно в диапазоне от 0,02 до 5 мг/кг/день.
Соединения настоящего изобретения могут быть введены в форме обычного лекарственного препарата в смеси с общепринятым фармацевтически приемлемым носителем или разбавителем. Фармацевтически приемлемый носитель или разбавитель может быть любым таким общепринятым носителем или разбавителем, который применяют в этой области и который не взаимодействует с соединением настоящего изобретения, они включают, например, лактозу, глюкозу, маннит, декстран, крахмал, белый сахар, алюмометасиликат магния, синтетический силикат алюминия, кристаллическую целлюлозу, натрийкарбоксиметилцеллюлозу, кальцийкарбоксиметилцеллюлозу, гидроксипропиловый крахмал, ионообменные смолы, метилцеллюлозу, желатин, аравийскую камедь, гидроксипропилцеллюлозу, низкозамещенную гидроксипропилцеллюлозу, гидроксипропилметилцеллюлозу, поливинилпирролидон, поливиниловый спирт, маловязкий кремниевый ангидрид, стеарат магния, тальк, карбоксивиниловый полимер, оксид титана, сложный эфир сорбитана и жирной кислоты, натрийлаурилсульфат, глицерин, сложный эфир глицерина и жирной кислоты, очищенный ланолин, глицерожелатин, полисорбат, макрогель, растительное масло, воск, жидкий парафин, белый вазелин, неионогенное поверхностно-активное вещество, пропиленгликоль, воду и подобные вещества.
Лекарственные препараты представляют таблетки, капсулы, гранулы, порошки, сиропы, суспензии, суппозитории, гели, препараты для инъекций и подобные лекарственные формы. Эти препараты могут быть получены известными способами. Когда получают жидкий препарат, он сначала может быть в форме твердого препарата, который при применении растворяют или суспендируют в воде или растворителе. Кроме того, таблетки или гранулы могут быть покрыты общепринятым способом; препараты для инъекций получают растворением соединения (I) настоящего изобретения или его аддитивной кислой соли в дистиллированной воде, предназначенной для инъекций, и в физиологическом растворе, а в случае необходимости, в изотоническом растворе, и к ним дополнительно могут быть добавлены регуляторы рН, буферы или консерванты.
Такие лекарственные препараты могут содержать соединение настоящего изобретения в количестве более 0,01% по весу, предпочтительно 0,05-70% по весу, и могут также содержать другие фармакологически активные ингредиенты.
Наилучший вариант осуществления изобретения
Соединения этого изобретения проиллюстрированы в следующих примерах. Символы в таблицах имеют следующие значения. Me: метил, Et: этил, п-Рг: н-пропил, i-Pr: изопропил, с-Рr: циклопропил, n-Bu: н-бутил, t-Bu: трет-бутил, Ph: фенил. Положение заместителей указано подобно тому, как указано далее, например, 3-Me-Ph означает 3-метилфенил.
Пример 1
Получение 3-(5-циклопропил-1,2,4-оксадиазол-3-ил)-5-метил-1,6-нафтиридин-2(1Н)-она.
(1) К раствору гидроксиламингидрохлорида (4,17 г) в воде (50 мл) при перемешивании и охлаждении льдом добавляют карбонат натрия (3,18 г). Затем к раствору добавляют этанол (200 мл) и 1,2-дигидро-5-метил-2-оксо-1,6-нафтиридин-3-карбонитрил (3,70 г) и смесь в течение 2 часов нагревают в колбе с обратным холодильником. После отгонки растворителя при пониженном давлении к остатку добавляют воду и осажденные кристаллы отделяют фильтрацией. Продукт последовательно промывают водой, изопропанолом, диизопропиловым эфиром и сушат, при этом получают 1,2-дигидро-5-метил-2-оксо-1,6-нафтиридин-3-амидоксим (4,2 г). Это соединение применяют в следующей реакции без очистки.
(2) К суспензии вышеуказанного амидоксима (1,09 г), карбоната натрия (0,83 г) и метилэтилкетона (200 мл) при перемешивании и охлаждении льдом добавляют циклопропанкарбонилхлорид (0,57 г), и смесь перемешивают при комнатной температуре в течение ночи. После отгонки растворителя при пониженном давлении к остатку добавляют воду и фильтрацией отделяют осажденные кристаллы, последовательно промывают их водой, изопропанолом и диизопропиловым эфиром и затем сушат. К полученным кристаллам добавляют диметилформамид (DMF) (ДМФ) (50 мл) и смесь перемешивают при 130oС в течение 5 часов. После отгонки растворителя при пониженном давлении к остатку добавляют изопропанол и фильтрацией отделяют кристаллы. Полученные кристаллы перекристаллизовывают из этанол-хлороформа, при этом получают названное соединение (0,65 г) в виде бесцветных кристаллов. Температура плавления 259-260oС.
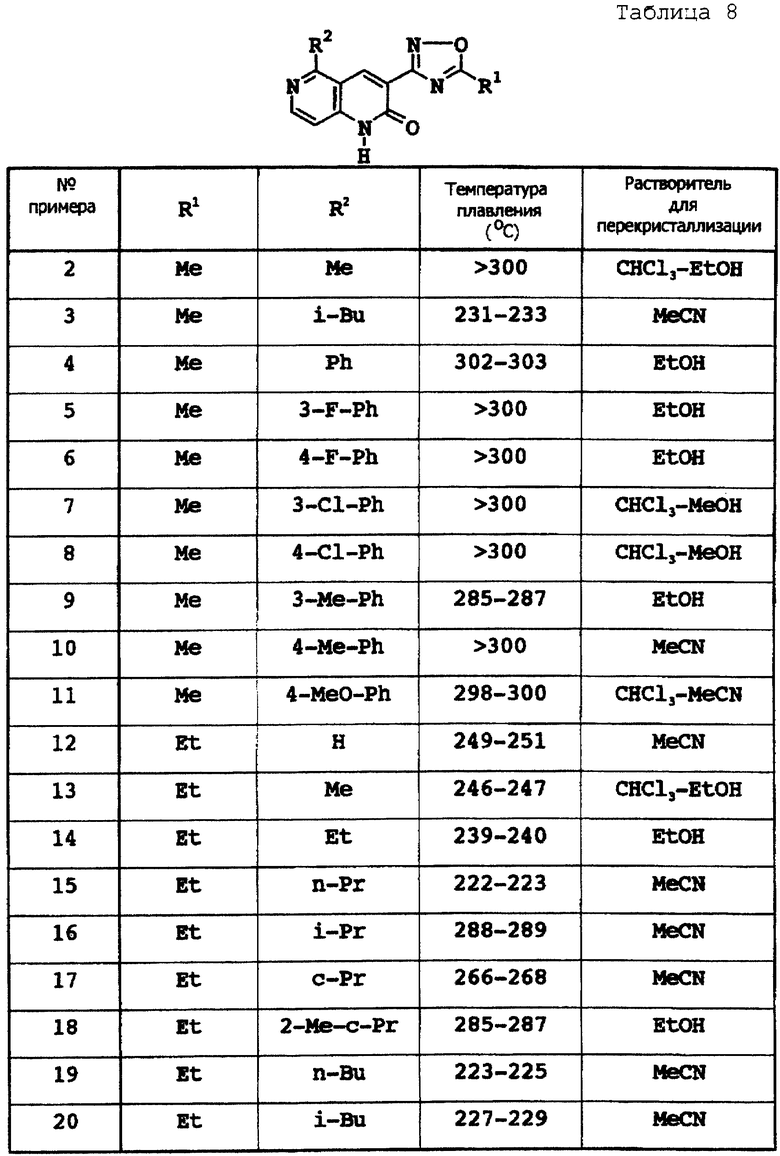
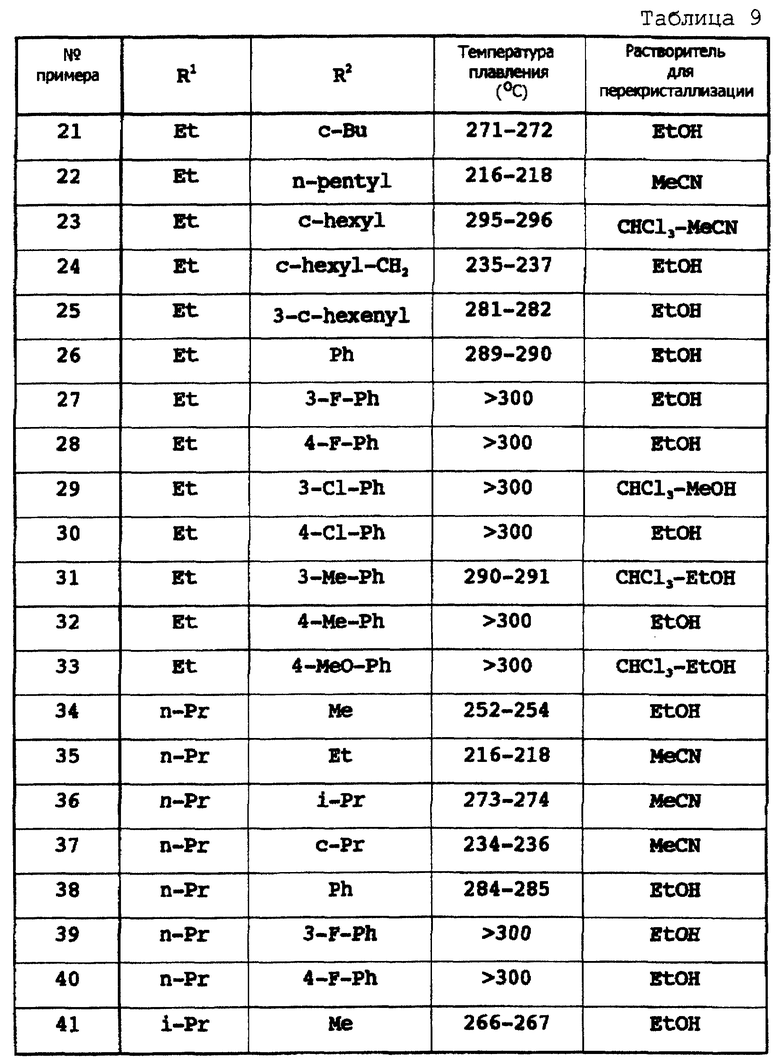
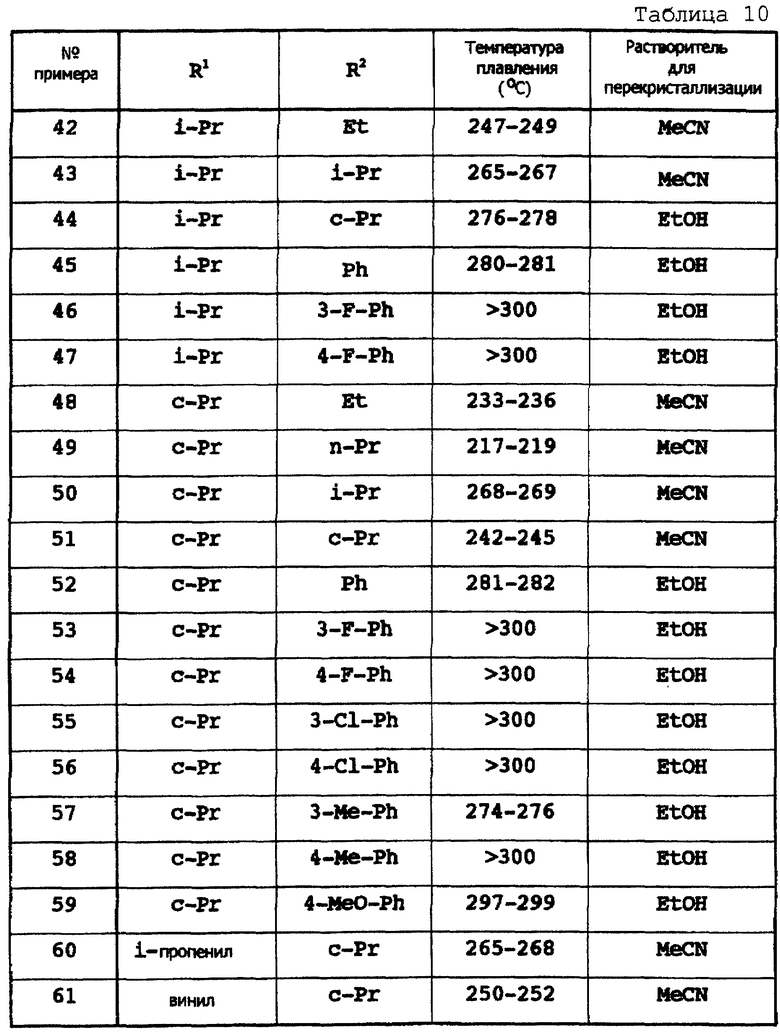
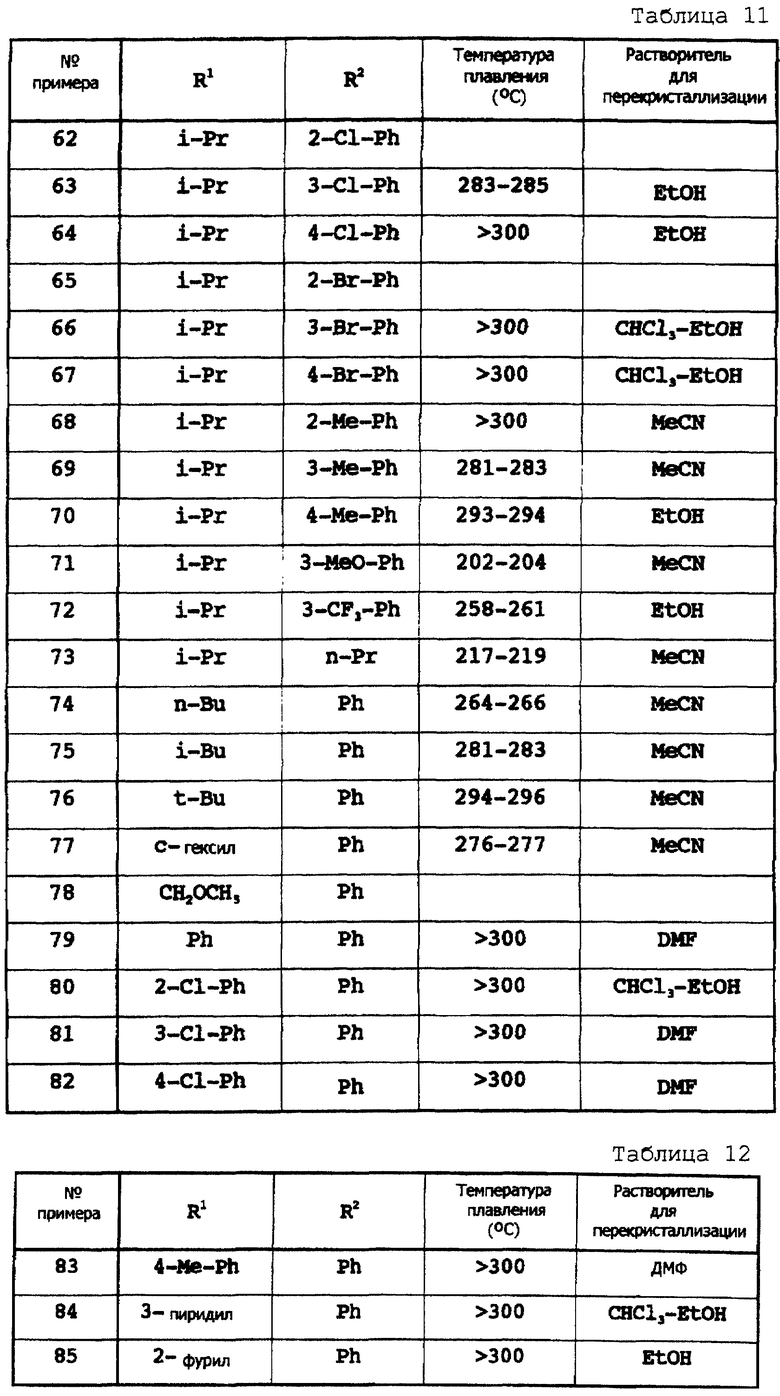
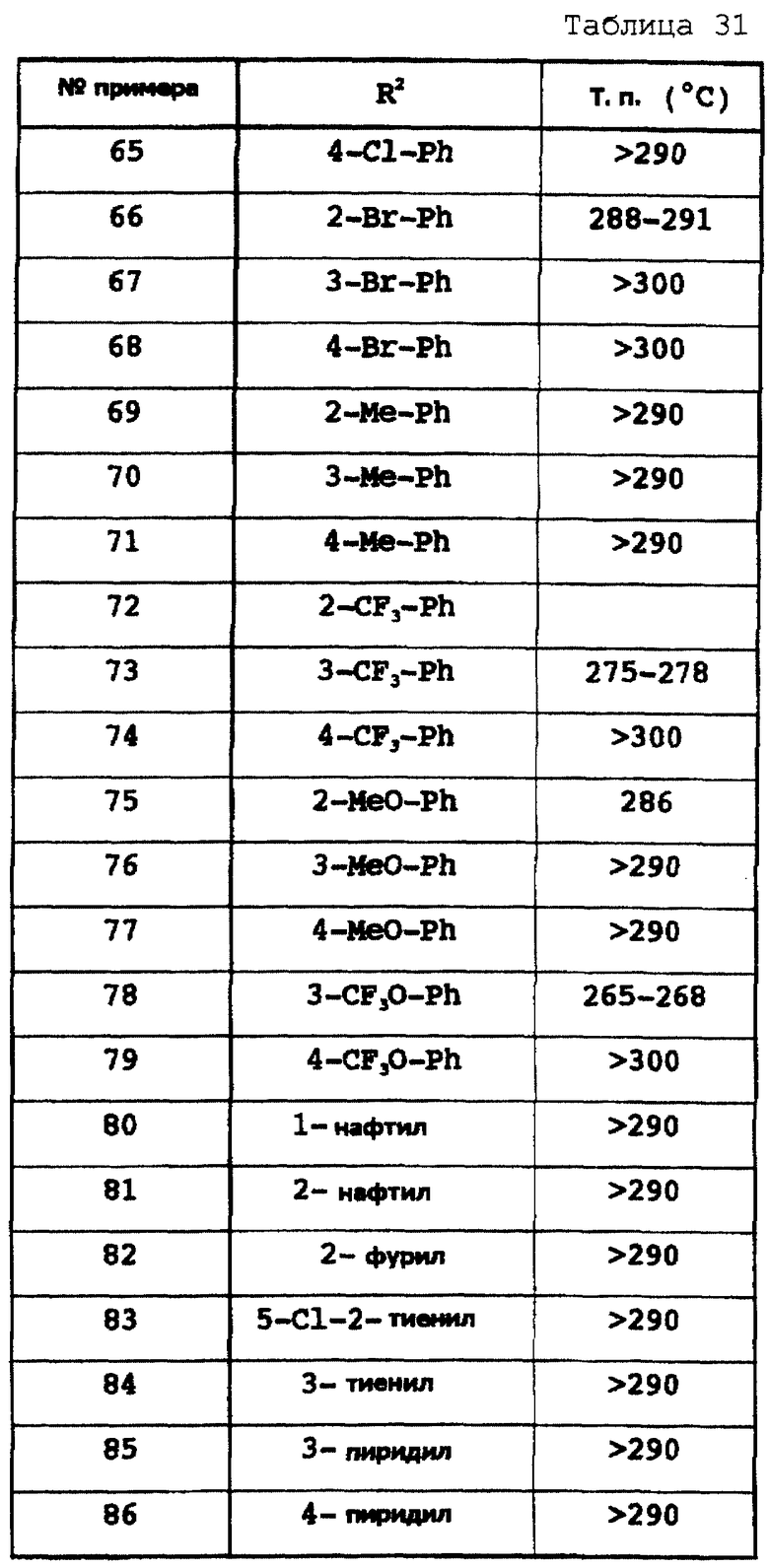
Примеры 2-85
Соответствующие исходные вещества подвергают взаимодействию тем же самым способом, который описан в примере 1, при этом получают соединения примеров 2-85, которые показаны в таблицах 8-12.
Пример 86
Получение 3-(5-метил-1,2, 4-оксадиазол-3-ил)-5- (3-метоксифенил)-1,6-нафтиридин-2(1Н)-она
К раствору уксусной кислоты (0,90 г) в ДМФ (100 мл) добавляют N,N'-карбонилдиимидазол (2,43 г) и смесь перемешивают при 70oС в течение 3 часов. К раствору добавляют 1,2-дигидро-5-(3-метоксифенил)-2-оксо-1,6-нафтиридин-3-амидоксим (3,10 г), полученный тем же самым способом, который описан в примере 1 (1), и смесь перемешивают при 70oС в течение 2-х часов и затем при 130oС в течение 1 часа. Реакционную смесь концентрируют при пониженном давлении досуха, к остатку добавляют воду, и осажденные кристаллы отделяют фильтрацией и последовательно промывают водой, изопропанолом и диизопропиловым эфиром и затем сушат. Полученные кристаллы хроматографируют на колонке с силикагелем и элюируют смесью хлороформ-метанол (50:1). Полученные кристаллы перекристаллизовывают из смеси хлороформ-этанол, при этом получают названное соединение (2,22 г) в виде бесцветных кристаллов. Температура плавления: 286-288oС. Гидрохлорид названного соединения (перекристаллизованный из этанола) имеет температуру плавления: 281-282oС.
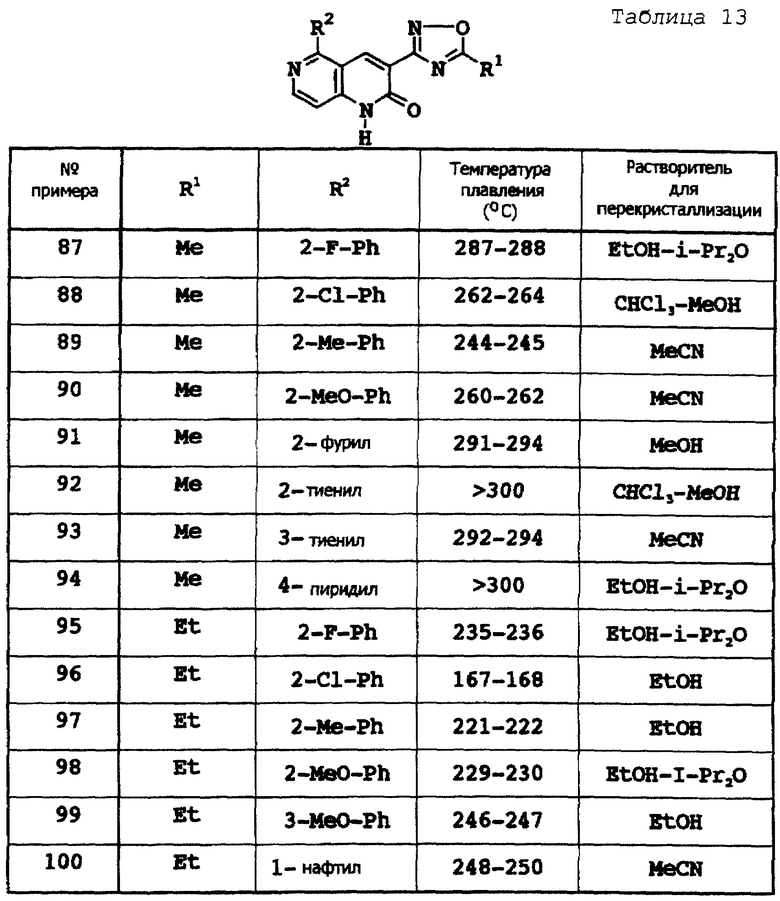
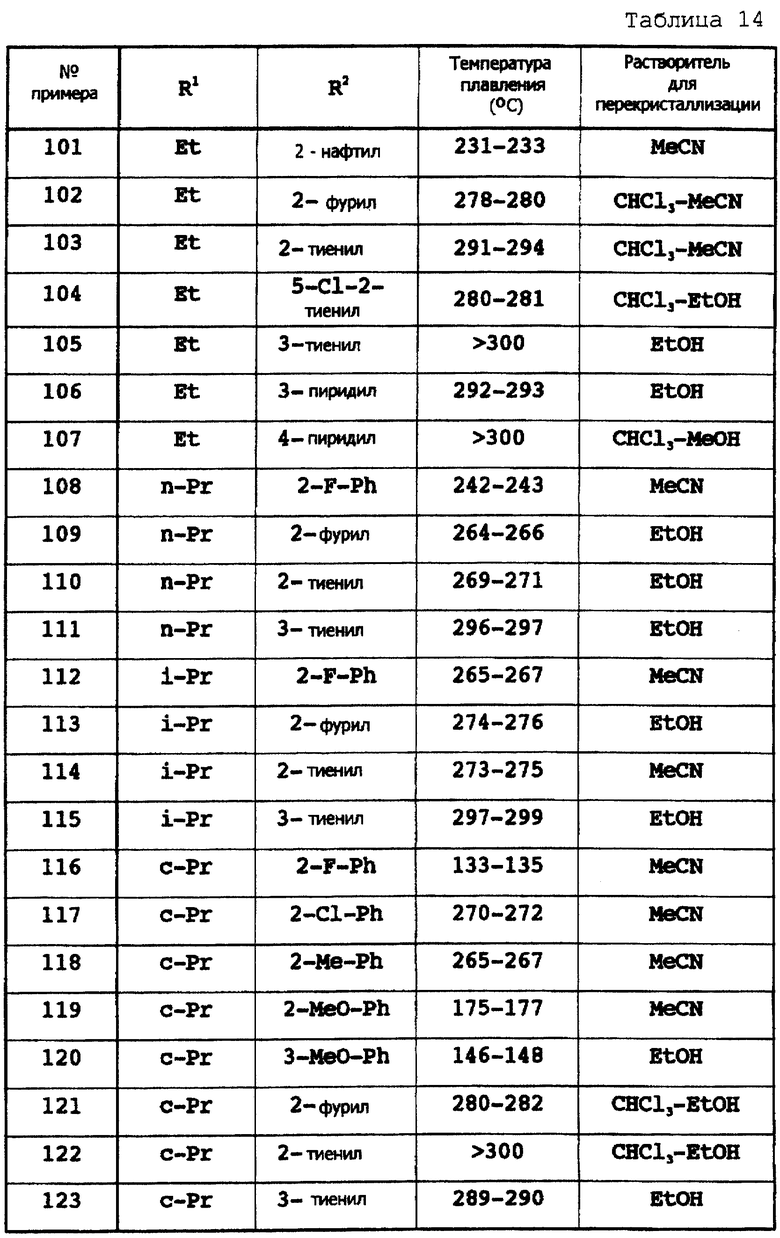
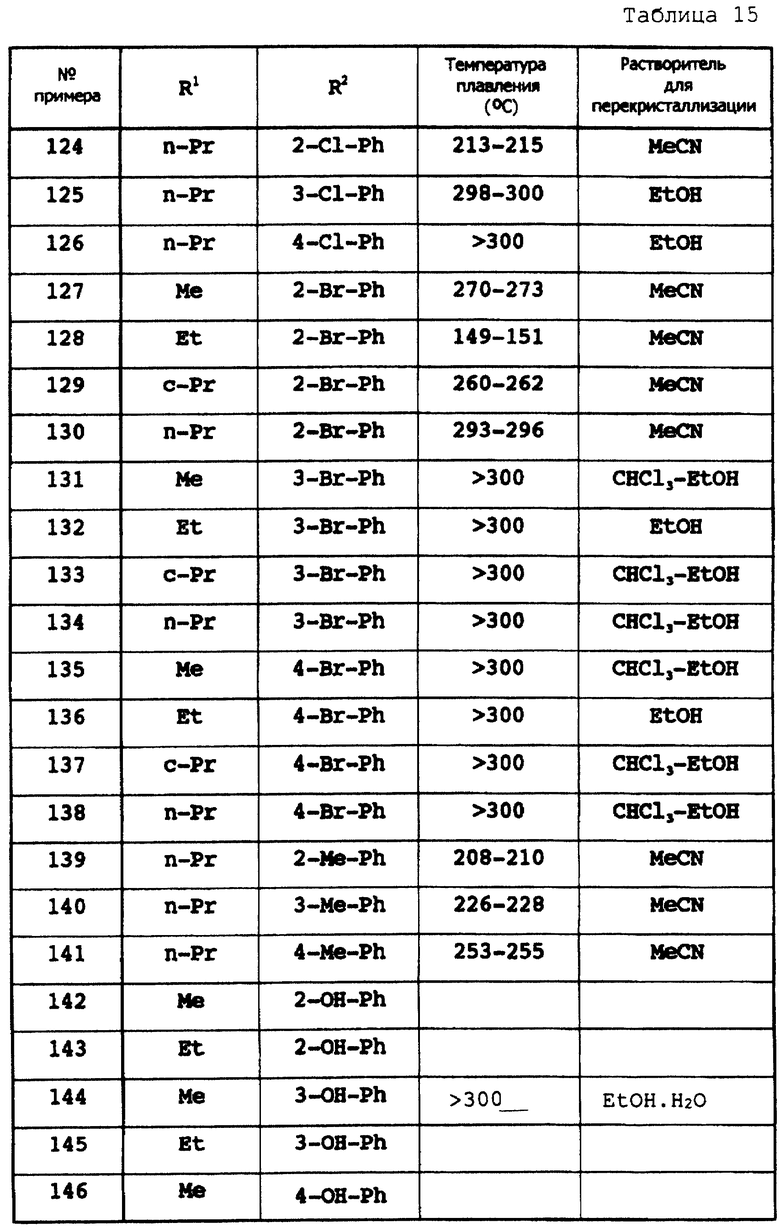
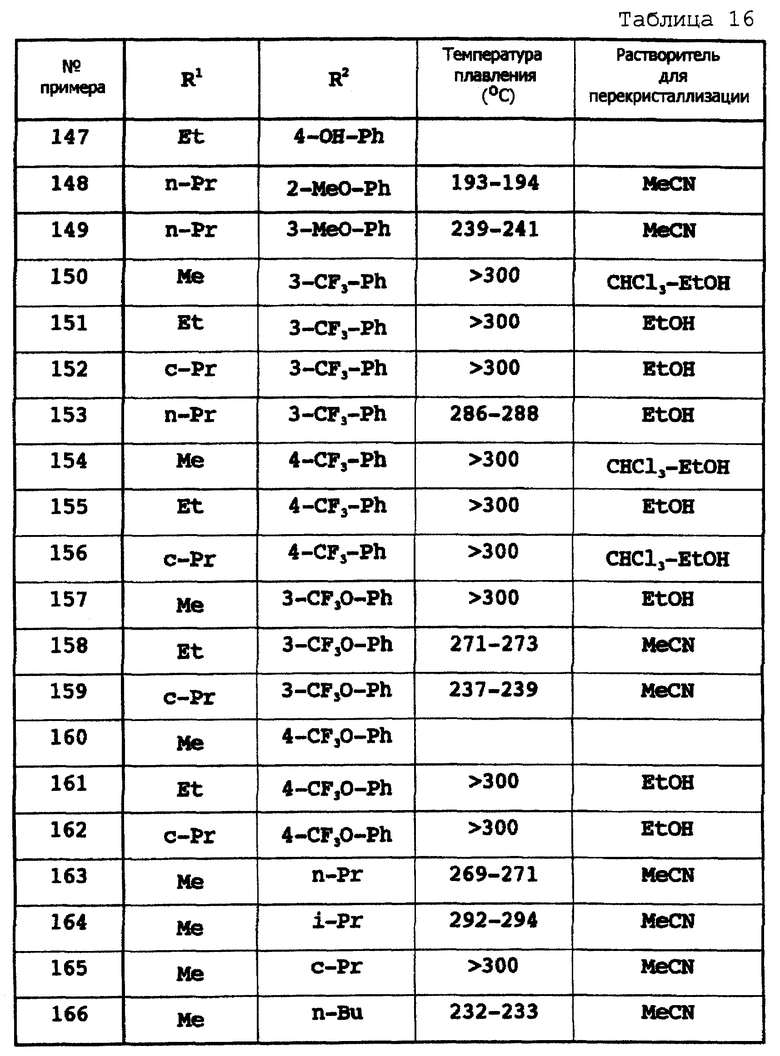
Примеры 87-172
Соответствующие исходные вещества подвергают взаимодействию тем же самым способом, который описан в примере 86, при этом получают соединения примеров 87-172, которые показаны в таблицах 13-17.
Пример 173
Получение 3-(3-этил-1,2, 4-оксадиазол-5-ил)-5-(2-тиенил)-1,6-нафтиридин-2(1Н)-она
К раствору 1,2-дигидро-5-(2-тиенил)-2-оксо-1,6-нафтиридин-3-карбоновой кислоты (3,81 г) в ДМФ (50 мл) добавляют N,N'-карбонилдиимидазол (3,41 г) и смесь перемешивают при 70oС в течение 4 часов. К раствору добавляют амидоксим пропионовой кислоты (1,85 г), и смесь перемешивают при 70oС в течение 1 часа и затем при 130oС в течение 2 часов. Реакционную смесь концентрируют при пониженном давлении досуха, к остатку добавляют воду, и осажденные кристаллы отделяют фильтрацией и последовательно промывают водой, изопропанолом и диизопропиловым эфиром и затем сушат. Полученные кристаллы подвергают хроматографии на колонке с силикагелем и элюируют смесью хлороформ-метанол (50: 1). Полученные кристаллы перекристаллизовывают из смеси хлороформ-этанол, при этом получают названное соединение (2,60 г) в виде бесцветных кристаллов. Температура плавления: 265-268oС.
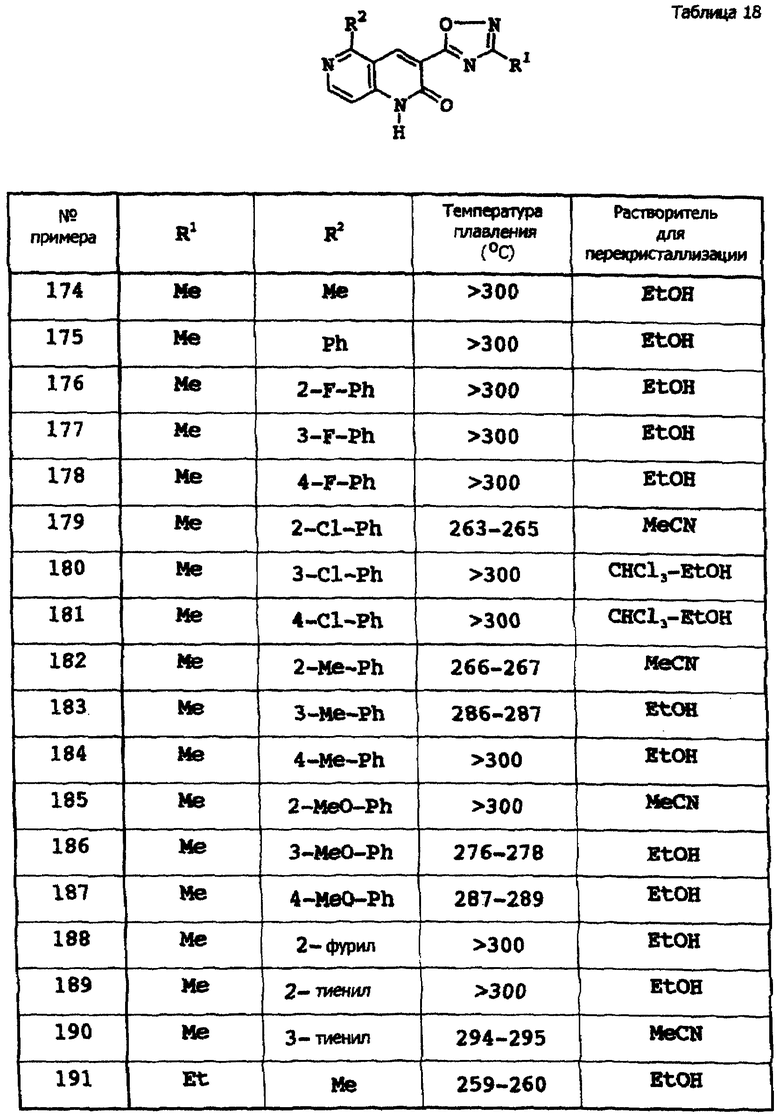
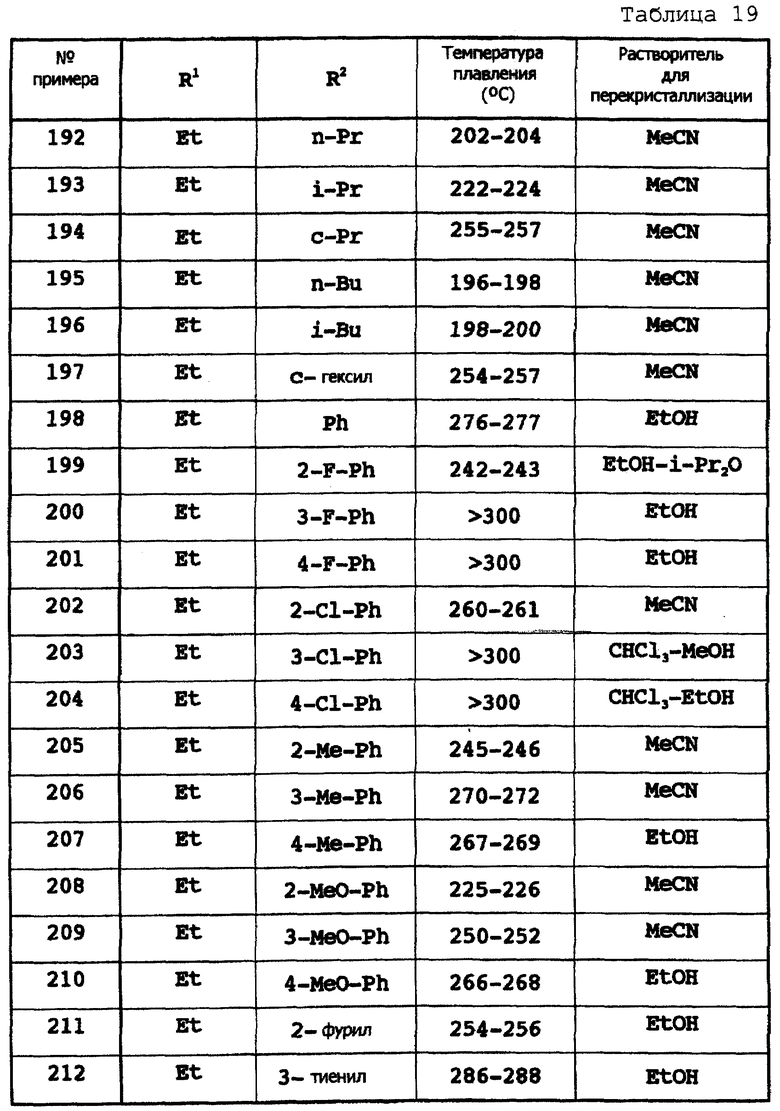
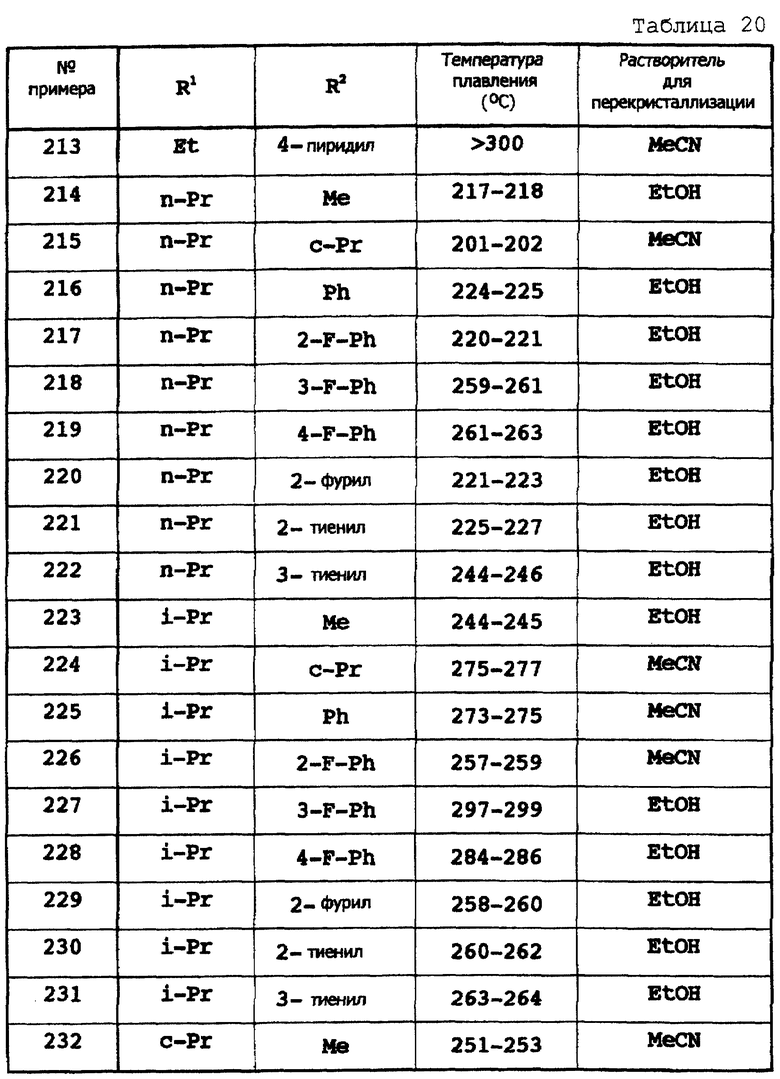
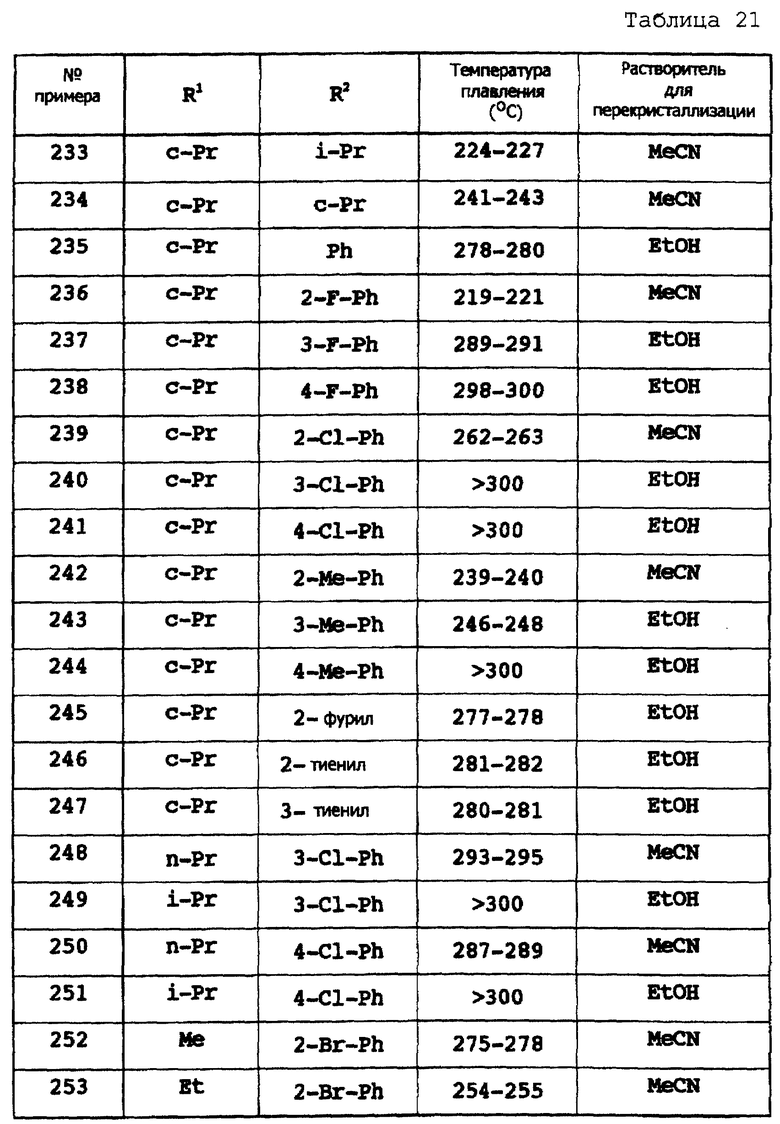
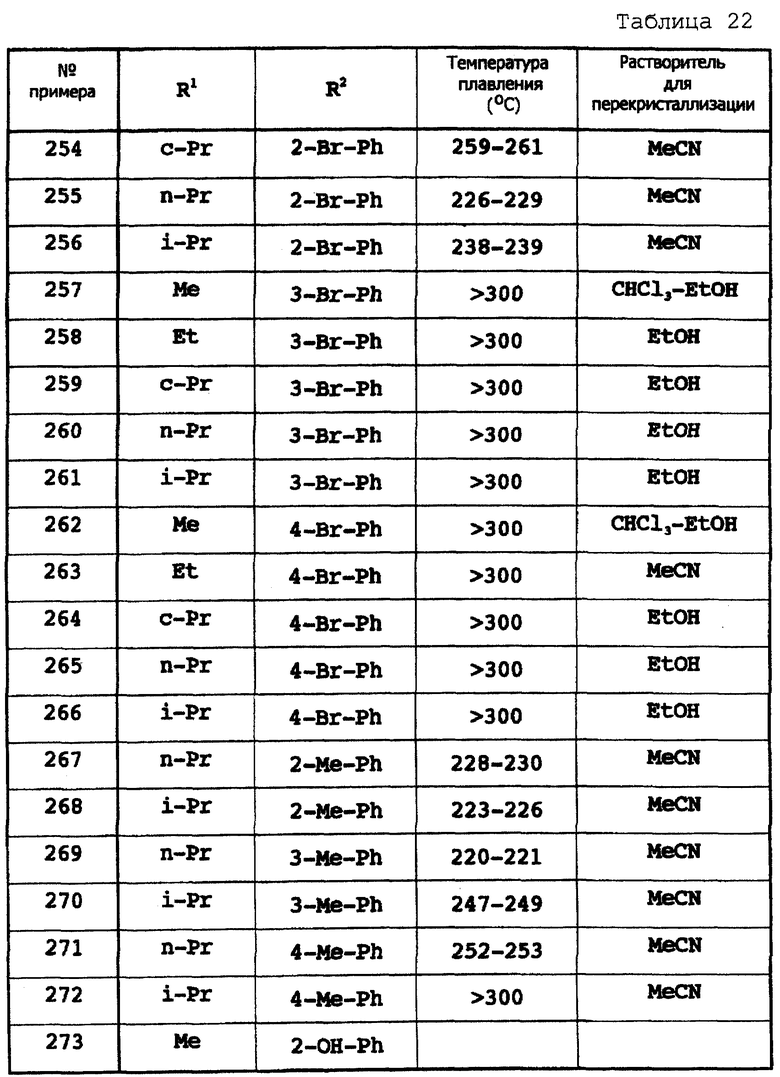
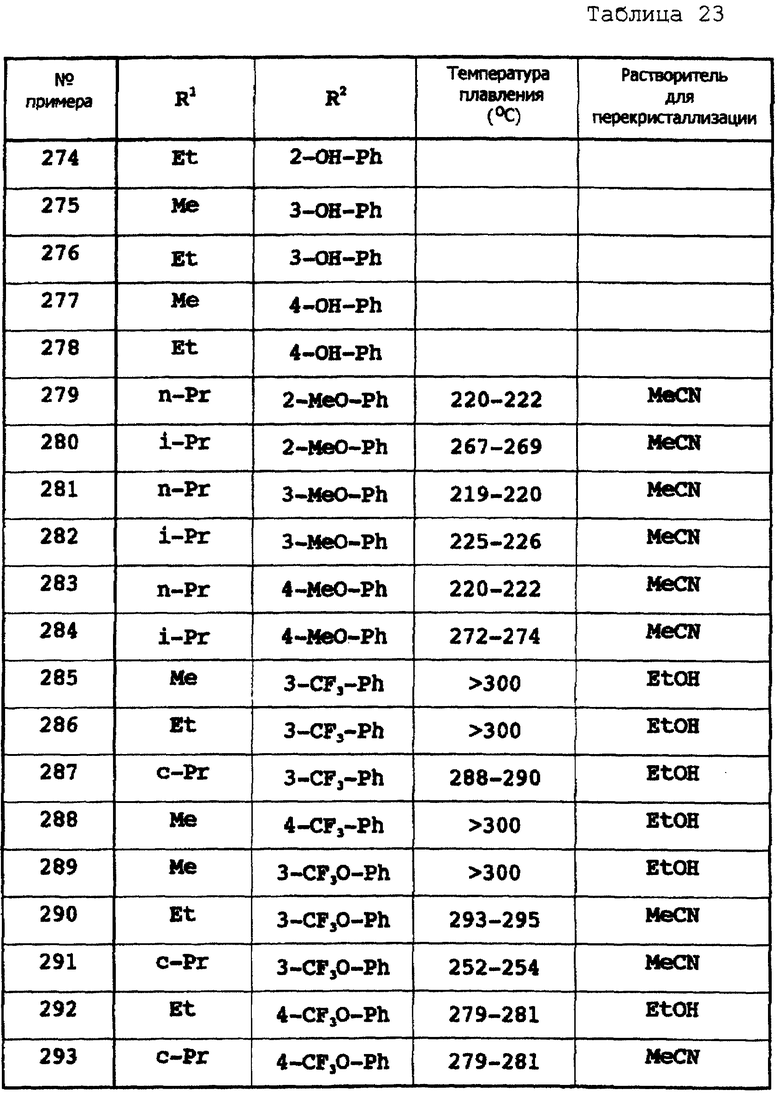
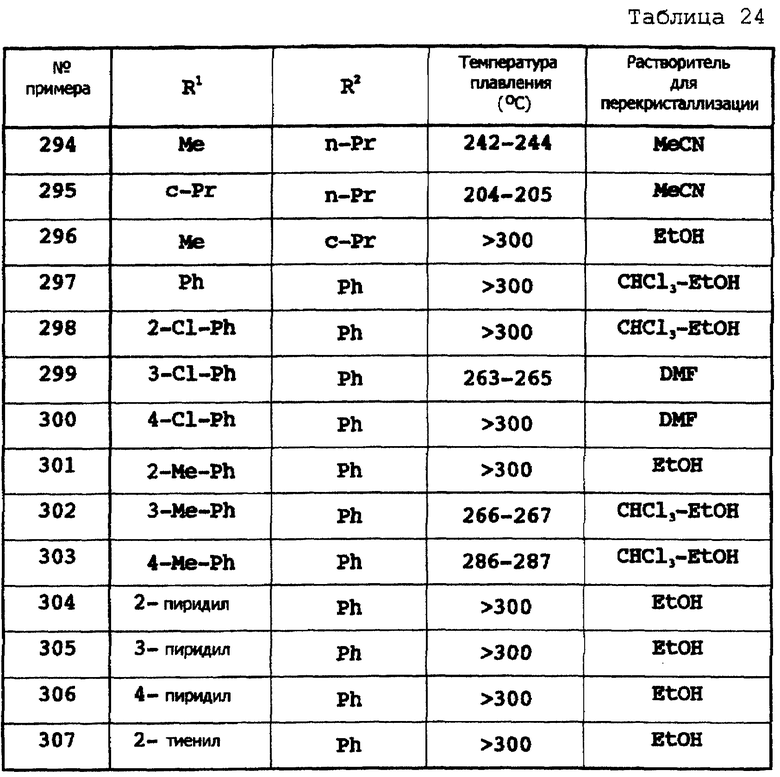
Примеры 174-307
Соответствующие исходные вещества подвергают взаимодействию тем же самым способом, который описан в примере 173, при этом получают соединения примеров 174-307, которые показаны в таблицах 18-24.
Пример 308
Получение 3-(5-этил-1,3,4-оксадиазол-2-ил)-5-(2-тиенил)-1, 6-нафтиридин-2(1H)-она
(1) Раствор 1,2-дигидро-5-(2-тиенил)-2-оксо-1,6-нафтиридин-3-карбоновой кислоты (1,36 г) и N,N'-карбонилдиимидазола (1,22 г) в ДМФ (50 мл) перемешивают при 70oС в течение 4 часов. К раствору добавляют пропионилгидразид (0,53 г), и смесь перемешивают при 70oС в течение 2 часов. Реакционную смесь концентрируют при пониженном давлении досуха, к остатку добавляют изопропанол и осажденные кристаллы отделяет фильтрацией. Продукт последовательно промывают изопропанолом и диизопропиловым эфиром и сушат, при этом получают 1,2-дигидро-N'-пропионил-5-(2-тиенил)-2-оксо-1,6-нафтиридин-3-карбогидразид (1,21 г) в виде желтых кристаллов. Это соединение применяют в следующей реакции без очистки.
(2) К суспензии вышеуказанного карбогидразида (1,09 г), трифенилфосфина (1,57 г) и триэтиламина (1,06 г) в тетрагидрофуране (ТГФ) (50 мл) при охлаждении льдом добавляют по каплям диэтилазодикарбоксилат (1,04 г). Смесь перемешивают при 70oС в течение 4 часов. После охлаждения к смеси добавляют воду, и затем смесь концентрируют при пониженном давлении и к остатку добавляют изопропанол. Осажденные кристаллы отделяют фильтрацией и сушат. Полученные кристаллы подвергают хромато-графии на колонке с силикагелем и элюируют смесью хлороформ-метанол (50: 1). Кристаллы перекристаллизовывают из этанола, получив при этом названное соединение (0,21 г) в виде бесцветных кристаллов. Температура плавления > 300oС.
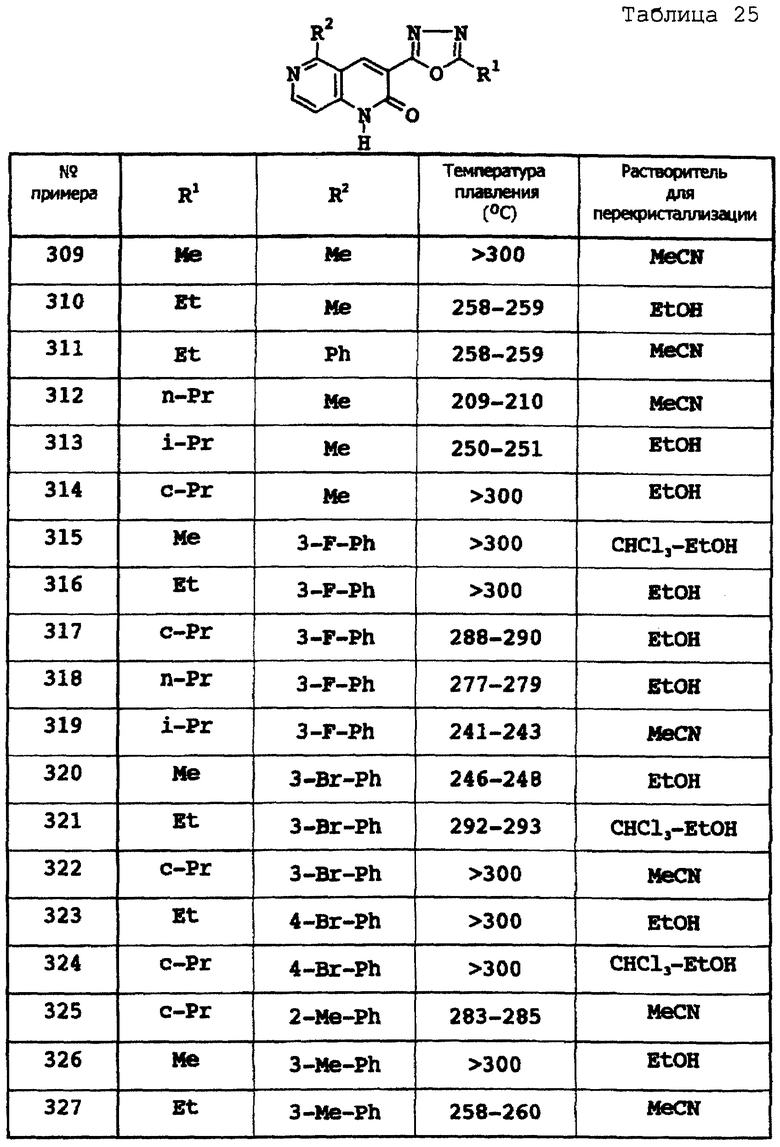
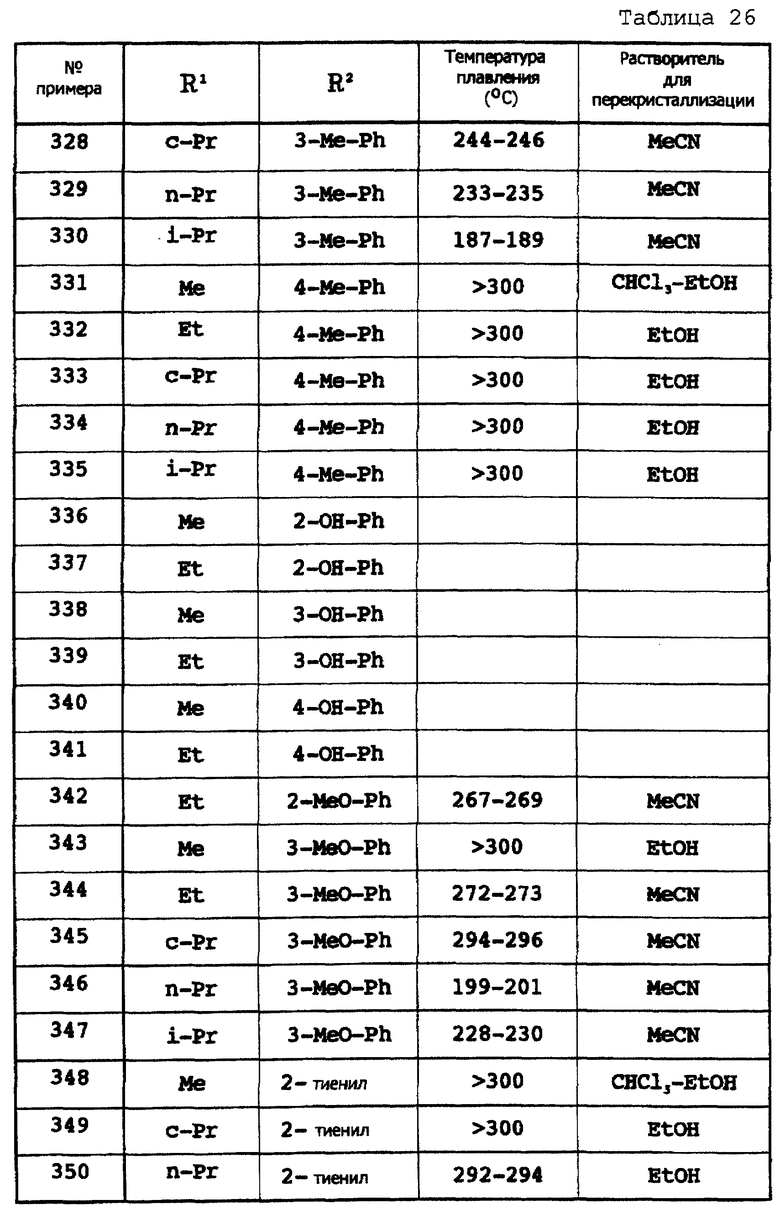
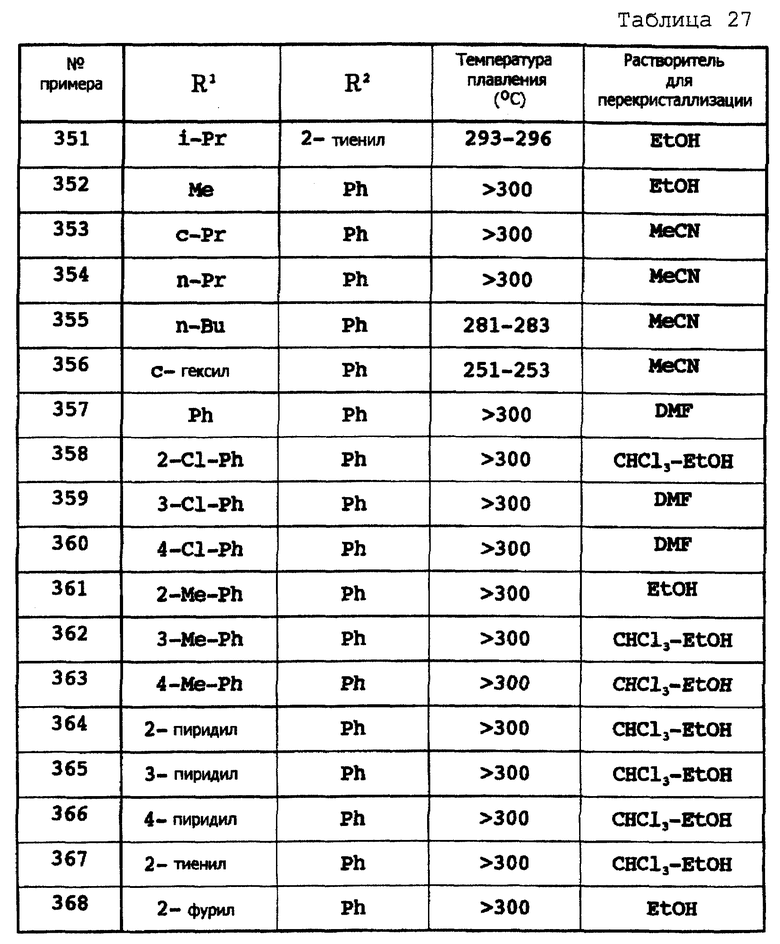
Примеры 309 - 368
Соответствующие исходные вещества подвергают взаимодействию тем же самым способом, который описан в примере 308, при этом получают соединения примеров 309-368, которые показаны в таблицах 25-27.
Пример 369
Получение 1,2-дигидро-5-метил-2-оксо-1,6-нафтиридин-3-карбонитрила
(1) При комнатной температуре в течение 3 часов перемешивают смесь ацетилацетона (41 мл), N,N-диметилформамиддиметилацеталя (106,2 мл) и ТГФ (200 мл). После отгонки растворителя при пониженном давлении остаток добавляют по каплям к раствору, полученному растворением металлического натрия (13,8 г) в этаноле (600 мл) и добавлением к раствору цианоацетамида (33,6 г), и смесь нагревают в течение одного часа в колбе с обратным холодильником. Реакционную смесь охлаждают льдом и осажденные кристаллы отделяют фильтрацией. Кристаллы растворяют в воде (1 литр) и затем слегка подкисляют 3 н. хлористо-водородной кислотой. Осажденные кристаллы отделяют фильтрацией и перекристаллизовывают из ДМФ-метанола, при этом получают 5-ацетил-6-метил-1,2-дигидро-2-оксо-3-пиридинкарбонитрил (60 г) в виде бесцветных кристаллов. Температура плавления: 230oС.
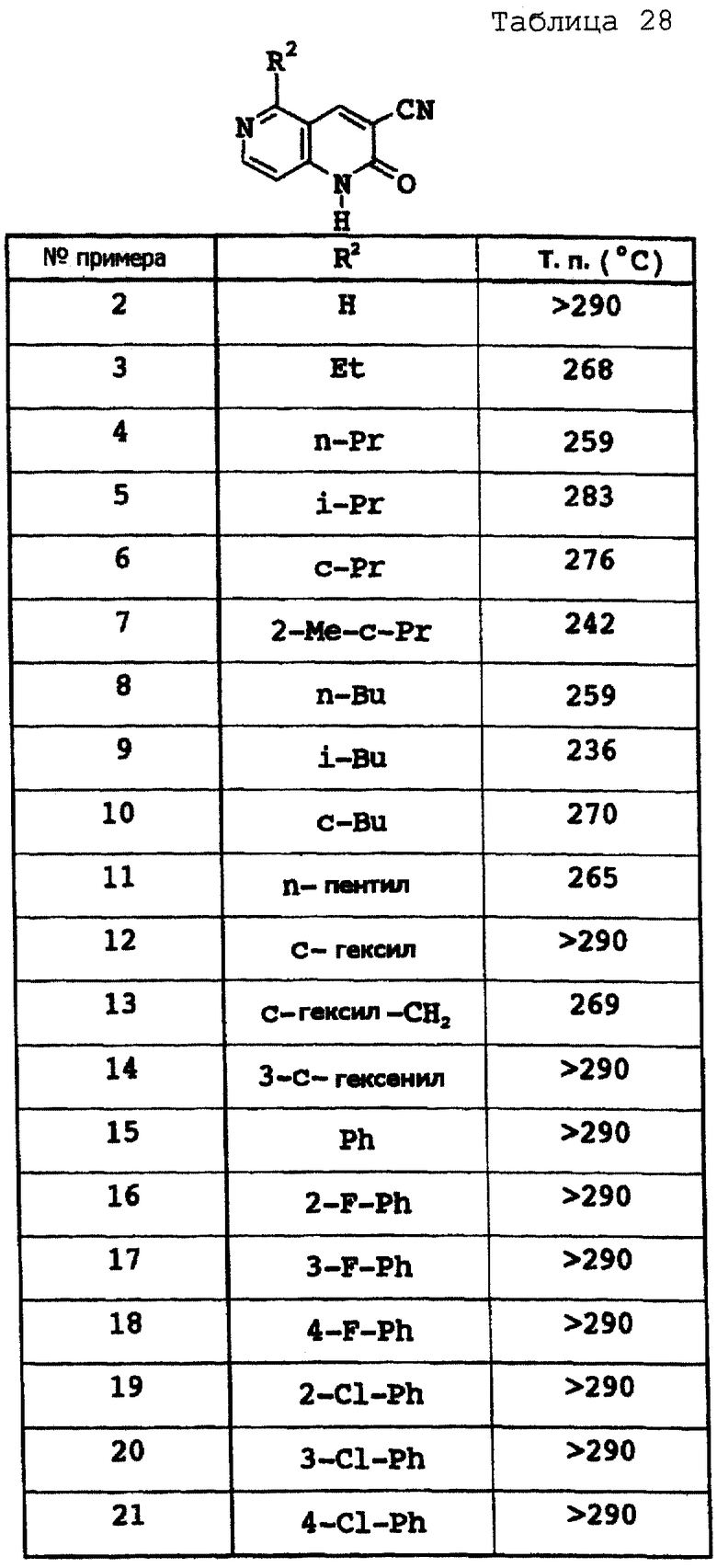
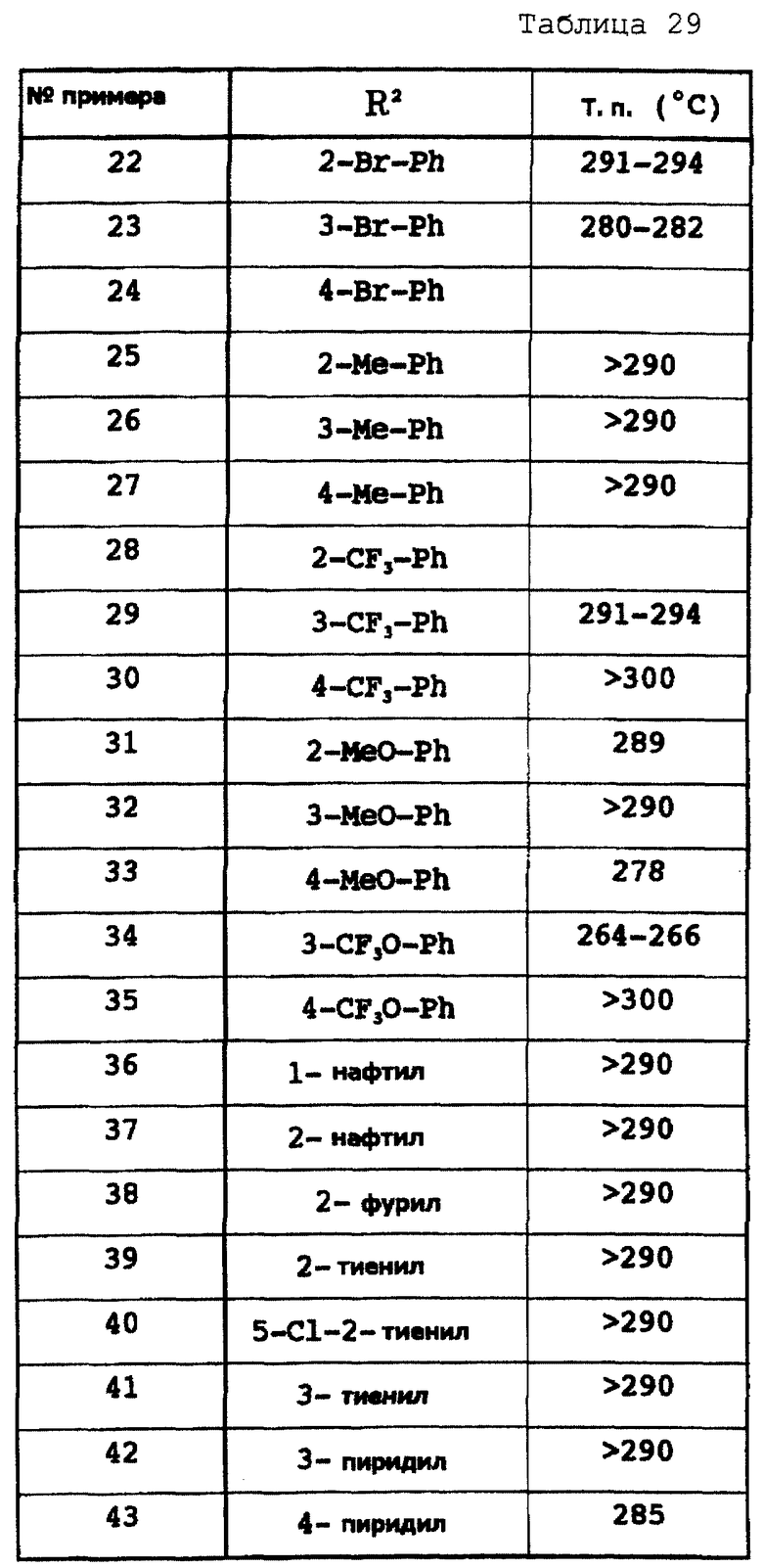
(2) При комнатной температуре в течение всей ночи перемешивают раствор вышеуказанного карбонитрила (30 г), N,N-диметилформамиддиметилацеталя (25 мл) и ДМФ (150 мл). Осажденные кристаллы отделяют фильтрацией, промывают метанолом и затем сушат. Полученные таким образом кристаллы и ацетат аммония (21,9 г) добавляют к ДМФ (300 мл), и смесь перемешивают в течение 3 часов при 130oС. Реакционную смесь концентрируют при пониженном давлении, к остатку добавляют воду и полученные кристаллы отделяют фильтрацией и перекристаллизовывают из ДМФ, при этом получают названное соединение (соединение 1) (25 г) в виде бесцветных кристаллов. Температура плавления 278oС.
Соответствующие исходные вещества подвергают взаимодействию тем же самым способом, который описан в примере 369, при этом получают соединения из соединений 2-43, которые показаны в таблицах 28-29.
Пример 370
Получение 1,2-дигидро-5-(2-тиенил)-2-оксо-1,6-нафтиридин-3-карбоновой кислоты
Смесь 1,2-дигидро-5-(2-тиенил)-2-оксо-1,6-нафтиридин-3-карбонитрила (10,0 г), этанола (300 мл) и 10 н. NaOH (300 мл) в течение всей ночи нагревают в колбе с обратным холодильником. После охлаждения реакционную смесь нейтрализуют уксусной кислотой, и осажденные кристаллы отделяют фильтрацией, последовательно промывают водой, изопропанолом и диизопропиловым эфиром и затем сушат, при этом получают названное соединение (соединение 44) (10,5 г) в виде бледно-желтых кристаллов. Температура плавления: 278oС.
Соответствующие исходные вещества подвергают взаимодействию тем же самым способом, который описан в примере 370, при этом получают соединения из соединений примеров 45 - 86, которые показаны в таблицах 30-31.
Препарат 1
Капсулы:
3-(5-Метил-1,2,4-оксадиазол-3-ил)-5-(3- метоксифенил)-1,6-нафтиридин-2(1Н)-он - 5,0 г
Кукурузный крахмал - 57 г
Лактоза - 10 г
Кристаллическая целлюлоза - 25 г
Гидроксипропилцеллюлоза - 2 г
Маловязкий кремниевый ангидрид - 0,5 г
Стеарат магния - 0,5 г
Вышеуказанные компоненты смешали в соответствии с общепринятым способом и перемешали, полученные гранулы заключили в 1000 капсул, при этом получили препарат в виде капсул (вес каждой из которых составил 100 мг).
Препарат 2
Таблетки:
3-(5-Метил-1,2,4-оксадиазол-3-ил)-5-(3-метоксифенил)1,6-нафтиридин-2(1Н)-он - 5 г
Кукурузный крахмал - 20 г
Лактоза - 30 г
Гидроксипропилцеллюлоза - 5 г
Низкозамещенная гидроксипропилцеллюлоза - 10 г
Вышеуказанные компоненты смешивают в соответствии с общепринятым способом и перемешивают к ним добавляют маловязкий кремниевый ангидрид и стеарат магния и смесь таблетируют, получая при этом таблетки, содержащие 5 мг активного ингредиента в каждой таблетке.
Препарат 3
Порошок:
3-(5-метил-1,2,4-оксадиазол-3-ил)-5-(3-метоксифенил) -1,6-нафтиридин-2(Н)-он - 5 г
Кукурузный крахмал - 173 г
Лактоза - 300 г
Гидроксипропилцеллюлоза - 20 г
Вышеуказанные компоненты смешивают в соответствии с общепринятым способом и перемешивают, измельчают и к ним добавляют маловязкий кремниевый ангидрид (0,5), при 50-кратном растирании получают растертый в порошок препарат.
Промышленное применение
Соединения этого изобретения обладают высокоселективным сродством к рецептору бензодиазепина и являются пригодными в качестве лекарственного средства, действующего на рецептор бензодиазепина. Хотя некоторые из соединений настоящего изобретения обладают агонистическими свойствами, соединения этого изобретения являются в особенности пригодными в качестве обратных агонистов. Ожидается, что соединения, обладающие обратными агонистическими свойствами, найдут применение в качестве психоаналептического средства или лекарственного средства для лечения дисмнезии при старческом слабоумии или болезни Альцгеймера в клинических областях, совершенно отличающихся от областей, в которых применяют агонисты.


Настоящее изобретение относится к производным 5-замещенного-3-оксадиазолил-1,6-нафтиридин-2(1Н)-она формулы (I), где Het является оксадиазолилом, R1 является Н, низшим алкилом, циклонизшим алкилом, трифторметилом, низшим алкенилом, низшим алкинилом, низшим алкокси, низшим алкоксинизшим алкилом, гидроксинизшим алкилом, замещенной или незамещенной арильной или замещенной или незамещенной гетероароматической группой, и R2 является Н, низшим алкилом, циклонизшим алкилом, циклонизшим алкилметилом, низшим алкенилом, циклонизшим алкенилом, низшим алкинилом, замещенной или незамещенной арильной или замещенной или незамещенной гетероароматической группой, или их фармацевтически приемлемым аддитивным кислым солям, которые обладают высокоселективным сродством к рецептору бензодиазепина и являются в особенности пригодными, например, в качестве психоаналептического средства или лекарственного средства для лечения дисмнезии при старческом слабоумии или болезни Альцгеймера. Описаны также фармацевтическая композиция и промежуточные соединения, используемые в синтезе соединений формулы I. 3 с. и 4 з.п. ф-лы, 31 табл.
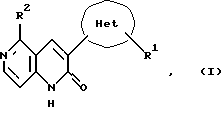
где Het является оксадиазолильной группой;
R1 является атомом водорода, низшей алкильной группой, циклонизшей алкильной группой, трифторметильной группой, низшей алкенильной группой, низшей алкоксигруппой, низшей алкоксинизшей алкильной группой, гидроксинизшей алкильной группой, замещенной или незамещенной арильной группой или замещенной или незамещенной гетероароматической группой, при этом арильная группа - фенил или нафтил и гетероароматическая группа - фурил, тиенил или пиридил;
R2 является атомом водорода, низшей алкильной группой, циклонизшей алкильной группой, циклонизшей алкилметильной группой, низшей алкенильной группой, циклонизшей алкенильной группой, замещенной или незамещенной арильной группой или замещенной или незамещенной гетероароматической группой, при этом арильная группа - фенил или нафтил, гетероароматическая группа - тиенил, фурил или пиридил;
или его фармацевтически приемлемая аддитивная кислая соль.
3-(5-этил-1,2,4-оксадиазол-3-ил)-5-(2-метилциклопропил)-1,6-нафтиридин-2(1Н)-он,
3-(5-метил-1,2,4-оксадиазол-3-ил)-5-(2-метилфенил)-1,6-нафтиридин-2(1Н)-он,
3-(5-метил-1,2,4-оксадиазол-3-ил)-5-(2-метоксифенил)-1,6-нафтиридин-2(1Н)-он,
3-(5-этил-1,2,4-оксадиазол-3-ил)-5-(2-тиенил)-1,6-нафтиридин-2(1Н)-он,
3-(5-метил-1,2,4-оксадиазол-3-ил)-5-(4-пиридил)-1,6-нафтиридин-2(1Н)-он,
3-(3-этил-1,2,4-оксадиазол-5-ил)-5-метил-1,6-нафтиридин-2(1Н)-он,
3-(3-этил-1,2,4-оксадиазол-5-ил)-5-(3-фторфенил)-1,6-нафтиридин-2(1Н)-он,
3-(3-метил-1,2,4-оксадиазол-5-ил)-5-(3-метилфенил)-1,6-нафтиридин-2(1Н)-он,
3-(3-метил-1,2,4-оксадиазол-5-ил)-5-(3-метоксифенил)-1,6-нафтиридин-2(1Н)-он,
3-(3-этил-1,2,4-оксадиазол-5-ил)-5-(4-метоксифенил)-1,6-нафтиридин-2(1Н)-он,
3-(3-этил-1,2,4-оксадиазол-5-ил)-5-(4-пиридил)-1,6-нафтиридин-2(1Н)-он, и
3-(3-циклопропил-1,2,4-оксадиазол-5-ил)-5-(3-тиенил)-1,6-нафтиридин-2 (1Н)-он.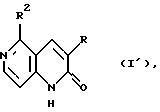
где R является цианогруппой, карбамоильной группой, карбоксильной группой, низшей алкоксикарбонильной группой или замещенной или незамещенной бензилоксикарбонильной группой;
R2 является низшей алкенильной группой, циклонизшей алкенильной группой, замещенной ариальной группой, причем арильная группа выбрана из фенила или нафтила.
| Способ дезодорации молока и жидких молочных продуктов | 1974 |
|
SU516392A1 |
| Способ контроля качества химического закрепления грунтов силикатизацией | 1974 |
|
SU588500A1 |
| Нижняя подушка к гладильному прессу | 1955 |
|
SU101952A1 |
Авторы
Даты
2002-08-27—Публикация
1998-07-14—Подача