Область техники, к которой относится изобретение
Настоящее изобретение относится к производным пурина и их фармацевтически применимым солям, которые ингибируют фермент, фактор Ха, вследствие чего они полезны в качестве коагулянтов. Кроме того, настоящее изобретение относится к фармацевтическим композициям, содержащим указанные производные или их фармацевтически применимые соли, а также к способам их применения.
Описание уровня техники
Фактор Ха является представителем класса трипсиноподобных серинпротеазных ферментов. В результате поочередного связывания факторов Ха и Va с ионами кальция и фосфолипидом образуется протромбиназный комплекс, который превращает протромбин в тромбин. В свою очередь, тромбин превращает фибриноген в фибрин, который полимеризуется с образованием нерастворимого фибрина.
В процессе свертывания крови протромбиназный комплекс является точкой конвергенции внутреннего (поверхностно активированного) и внешнего (тканевый фактор поврежденного сосуда) путей (Biochemistry (1991), т.30, стр.10363, и Cell (1988), т.53, стр. 505-518). Модель процесса коагуляции была дополнительно уточнена с открытием природы действия ингибитора пути метаболизма тканевого фактора (TFPI) (Seminars in Hematology (1992), т.29, стр. 159-161). TFPI представляет собой циркулирующий мультидоменовый серинпротеазный ингибитор с тремя доменами Kunitz-типа, который конкурирует с фактором Va за фактор Ха. Сразу после образования бинарный комплекс фактора Ха и TFPI становится мощным ингибитором комплекса фактора VIIa и тканевого фактора.
Фактор Ха может активироваться двумя различными комплексами, комплексом тканевый фактор-VIIa в пути "Ха бурст" и комплексом фактор IXa-VIIIA (TENaзa) в пути "устойчивый Ха" системы крови. После повреждения сосуда путь "Ха бурст" активируется посредством тканевого фактора (TF). Усиление регулирования процесса свертывания крови имеет место при увеличении продуцирования фактора Ха путем "устойчивого Ха". Снижение регулирования процесса свертывания крови проходит при образовании комплекса фактора Xa-TFPI, который не только удаляет фактор Ха, но также ингибирует дополнительно образование фактора по пути "Ха бурст". Поэтому в действительности процесс свертывания крови регулируется фактором Ха.
Главное преимущество ингибирования фактора Ха по сравнению с тромбином для предотвращения коагуляции состоит в целевом действии фактора Ха, тогда как тромбин выполняет множество функций. Тромбин, не только катализирует превращение фибриногена в фибрин, фактора VIII в фактор VIIIА, фактора V в фактор Va и фактора XI в ХIа, но также активирует тромбоциты, представляет собой моноцитный хемотактический фактор и митоген для лимфоцитов и клеток гладкой мышцы. Тромбин активирует протеин С, являющийся in vivo антикоагулянтным дезактиватором факторов Va и VIIIa, при связывании с тромбомодулином. В системе кровообращения тромбин быстро дезактивируется антитромбином III (ATIII) и гепариновым софактором II (HCII) в реакции, которая катализируется гепарином или другими протеогликансвязанными гликозаминогликанами, тогда как тромбин в тканях дезактивируется протеазой, нексином. Тромбин выполняет свои функции клеточной активации через уникальный тромбиновый рецептор - "связанный лиганд" (Cell (1991), т.64, стр. 1057), который требует наличия того же сайта анионного связывания и активного сайта, которые используются в связывании и расщеплении фибриногена, а также в связывании тромбомодулином и активации протеина С. Таким образом, различные группы in vivo молекулярных мишеней конкурируют за связывание тромбина, и последующие протеолитические события будут иметь различные физиологические последствия в зависимости от того, какой тип клетки и какой рецептор, модулятор, субстрат или ингибитор связывают тромбин.
Опубликованные данные, касающиеся белков типа антистазина и антикоагулянтного пептида (ТАР), демонстрируют, что ингибиторы фактора Ха являются эффективными антикоагулянтами (Thrombosis and Haemostasis (1992), т. 67, стр. 371-376, и Science (1990), т.248, стр. 593-596).
Активный сайт фактора Ха может блокироваться ингибитором механистического типа (mechanism-based) или ингибитором прочного связывания (ингибитор прочного связывания отличается от ингибитора механистического типа отсутствием ковалентной связи между ферментом и ингибитором). Известны два типа ингибиторов механистического типа, обратимые и необратимые ингибиторы, которые отличаются друг от друга по легкости гидролиза связи фермент - ингибитор (Thrombosis Res (1992), т. 67, стр. 221-231, и Trends Pharmacol. Sci. (1987), т. 8, стр. 303-307). Ряд соединений гуанидина могут служить примерами ингибиторов прочного связывания (Trombosis Res. (1980), т. 19, стр.339-349). Было также показано, что системы типа арилсульфонил-аргинин-пиперидин-карбоновая кислота являются прочно связывающими ингибиторами тромбина (Biochem. (1984), т.23, стр. 85-90), как и ряд ариламидинсодержащих соединений, включающих 3-амидинофениларильные производные (Thrombosis Res. (1983), т. 29, стр.635-642) и бис(амидино)бензилциклокетоны (Trombosis Res. (1980), т. 17, стр. 545-548). Однако эти соединения демонстрируют плохую селективность в отношении фактора Ха.
Ссылки, относящиеся к данному изобретению
В опубликованной заявке на европейский патент 0540051 (Nagahara с сотр.) описаны ароматические амидиновые производные, которые как отмечается, способны проявлять сильное антикоагулянтное действие по механизму обратимого ингибирования фактора Ха.
Синтез α,α-бис(амидинобензилиден)циклоалканонов и α,α-бис(амидинобензил)циклоалканонов описан в Pharmazie (1977), т.32, 3, стр.141-145. Эти соединения раскрыты как ингибиторы протеазы серина.
Краткое изложение сущности изобретения
Настоящее изобретение относится к соединениям или их фармацевтически применимым солям, которые ингибируют человеческий фактор Ха и поэтому полезны в качестве фармакологических агентов для лечения болезненных состояний, характеризующихся тромботической активностью.
В соответствии с одним из аспектов настоящее изобретение относится к соединениям, выбранным из группы, отвечающей следующим формулам: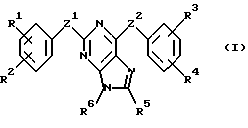

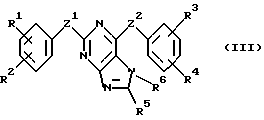
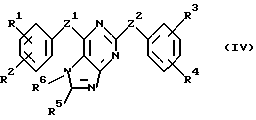
в которых
Z1 и Z2 независимо представляют собой -О-, -N(R10)- или -ОСН2-;
R1 и R4 независимо представляют собой водород, галоген, алкил, -OR10, -С(О)OR10, -C(O)N(R10)R11, -N(R10)R11, -N(R10)С(O)R11 или -N(H)S(O)2R13;
R2 представляет собой -C(NH)NH2, -С(NH)N(H)OR10, -C(NH)N(H)C(O)-O-R13, -C(NH)N(H)C(O)R10, -C(NH)N(H)S(O)2R13 или -C(NH)N(H)C(O)N(H)R10;
R3 представляет собой галоген, алкил, галоалкил, галоалкокси, уреидо, циано, гуанидино, -OR10, -C(NH)NH2, -C(NH)N(H)OR10, -C(O)N(R10)Rll, -R12-C(О)N(R10)R11, -CH-(OH)C(O)-N(R10)R11, -N(R10)R11, -Rl2-N(R10)Rll, -C(O)OR10, -R12-C(O)OR10, -N-(R10)С(O)R10, (1,2)-тетрагидропиримидинил (необязательно замещенный алкилом), (1,2)-имидазолил (необязательно замещенный алкилом) или (1,2)-имидазолинил (необязательно замещенный алкилом);
R5 представляет собой водород, галоген, алкил, циклоалкил, галоалкил, арил, аралкил, алкилтио, гидрокси, меркапто, алкокси или -N(R10)R11,
R6 представляет собой (C(R7) (R8)n)-R9 (где n имеет значение в интервале 1-4), водород, алкил, арил (необязательно замещенный галогеном, алкилом, гидрокси, алкокси, аралкокси, амино, диалкиламино, моноалкиламино, карбокси, алкоксикарбонилом, аминокарбонилом, моноалкиламинокарбонилом или диалкиламинокарбонилом) или аралкил (необязательно замещенный галогеном, алкилом, арилом, алкокси, аралкилом, амино, диалкиламино, моноалкиламино, карбокси, алкоксикарбонилом, аминокарбонилом, моноалкиламинокарбонилом, диалкиламинокарбонилом);
каждый R7 независимо представляет собой водород, алкил, алкенил, алкинил, галоалкил, галоалкенил, циклоалкил, циклоалкилалкил, -С(О)OR10, -R12-C(О)OR10, -R12-C(О)N(R10)R11, -C(O)-R12-N(R10)R11, -R12-C(O)R10, -R12-C(О)N(R10)N(R10)R11, -R12-C(R10)(OR10)R12-N(R10)R11, -С(R10)(OR10)С(О)OR11, -R12-C(R10)(С(О)OR10)2, -C(R10)(N(R10)R11)C(O)OR10,
-R12C(R10)(N(R10)R11)C(O)OR10, -С(R10)(OR10)R11, -R12-N(R10)R11, -R12-N(R10)C(O)OR13, -R12-N(R10)C(O)R11, -R12-N(R10)С(NR10)R13, -R12-N(R10)S(O)2R13, -R12-N(R10)C(O)N(R10)R11, -R12-N(R10)С(NR10)N(R10)R11,
-R12-N(R10)С(NR10)N(R10)N(R10)R11, -R12-N(R10)-R12-C(R10)(N(R10)R11)C(O)OR10, -R12-N(R10)S(O)R11, -R12-O(R10),
-R12-ON(R10)C(NR10)N(R10)R11, -R12-OS(О)2OR10, -R12-P(O)(OR10)R11, -R12-OP(O)(OR10)2, -R12-P(O)(OR10)2, -R12-SR10, -R12-S-R12-C(O)ОR10, -R12-S-R12-N(R10)R11, -R12-S-R12-C(R10) (N(R10)R11)C(O)OR10, -R12-S-R12-N(R10)C(O)OR10, -R12-S-R12-N(R10)C(O)R10, -R12-S-S-R12-C(R10)(N(R10)R11)С(O)OR10, -R12-SC(O)N(R10)R11, R12-SC(S)N(R10)R11, R12-S(O)R10, R12-S(O)2R13, R12-S(O)OR10, R12-S(O)2OR10, R12-S(O)2N(R10)R11,
R12-S(O)N(R10)R11
или каждый R7 независимо представляет собой арил (необязательно замещенный одним или более заместителями, выбранными из группы, состоящей из алкила, галогена, галоалки-ла, галоалкокси, OR10, SR10, N(R10)R11, С(О)OR10, С(О)N(R10)R11, S(O)2OR10 и ОР(O)(OR10)2),
или каждый R7 представляет собой аралкил (необязательно замещенный одним или более заместителями, выбранными из группы, состоящей из алкила, галогена, галоалкила, галоалкокси, OR10, SR10, N(R10)R11, С(О)OR10, C(O)N(R10)R11, S(O)2OR10 и ОР(O)(OR10)2),
или каждый R7 представляет собой гетероциклил (необязательно замещенный одним или более заместителями, выбранными из группы, состоящей из алкила, галогена, галоалкила, галоалкокси, аралкила, OR10, С(О)OR10, N(R10)R11, C(O)N(R10)R11, S(O)2OR10 и ОР(O)(OR10)2),
или каждый R7 представляет собой гетероциклилалкил (в котором гетероциклильный радикал необязательно замещен одним или более заместителями, выбранными из группы, состоящей из алкила, галогена, галоалкила, галоалкокси, аралкила, OR10, SR10, С(О)OR10, N(R10)R11, C(O)N(R10)R11, S(O)2OR10 и OP(O)(OR10)2),
или каждый R7 представляет собой адамантил (необязательно замещенный алкилом, галогеном, галоалкилом, галоалкокси, OR10, SR10, С(О)OR10, N(R10)R11, С(О)N(R10)R11, S(O)2OR10 и ОР(O)(OR10)2),
или каждый R7 представляет собой адамантилалкил (в котором адамантильный радикал необязательно замещен алкилом, галогеном, галоалкилом, галоалкокси, OR10, SR10, С(О)OR10, N(R10)R11, C(O)N(R10)R11, S(O)2OR10 и ОР(O)(ОR)10)2);
каждый R8 независимо представляет собой водород, алкил, циклоалкил или арил;
R9 представляет собой -С(О)OR10 или -С(O)N(R10)R11;
каждый R10 и R11 независимо представляет собой водород, алкил, арил (необязательно замещенный галогеном, алкилом, гидрокси, алкокси, аралкокси, амино, диалкиламино, моноалкиламино, карбокси, алкоксикарбонилом, аминокарбонилом, моноалкиламинокарбонилом или диалкиламинокарбонилом) или аралкил (необязательно замещенный галогеном, алкилом, арилом, гидрокси, алкокси, аралкилом, амино, диалкиламино, моноалкиламино, карбокси, алкоксикарбонилом, аминокарбонилом, моноалкиламинокарбонилом или диалкиламинокарбонилом);
R12 представляет собой прямую или разветвленную алкиленовую цепь, а
R13 представляет собой алкил, арил (необязательно замещенный галогеном, алкилом, гидрокси, алкокси, аралкокси, амино, диалкиламино, моноалкиламино, карбокси, алкоксикарбонилом, аминокарбонилом, моноалкиламинокарбонилом или диалкиламинокарбонилом) или аралкил (необязательно замещенный галогеном, алкилом, арилом, гидрокси, алкокси, аралкилом, амино, диалкиламино, моноалкиламино, карбокси, алкоксикарбонилом, аминокарбонилом, моноалкиламинокарбонилом или диалкиламинокарбонилом),
в виде индивидуального стереоизомера или смеси стериоизомеров, или их фармацевтически приемлемым солям.
Согласно другому аспекту настоящее изобретение относится к композициям, полезным для лечения болезненных состояний человека, характеризующихся тромботической активностью, которые включают терапевтически эффективное количество описанного выше соединения изобретения или его фармацевтически приемлемой соли и фармацевтически применимый наполнитель.
В соответствии с другим аспектом настоящее изобретение относится к способу лечения человека в болезненном состоянии, характеризующимся тромботической активностью, который включает введение человеку, нуждающемуся в лечении, терапевтически эффективного количества описанного выше соединения изобретения.
Согласно еще одному аспекту настоящее изобретение относится к способу лечения болезненного состояния человека, ослабляемого ингибированием фактора Ха, который включает введение нуждающемуся в лечении человеку терапевтически эффективного количества описанного выше соединения изобретения.
Другой аспект настоящего изобретения включает способ ингибирования человеческого фактора Ха in vitro или in vivo введением соединения настоящего изобретения.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Обозначения
Если не оговорено особо, то используемые в тексте описания и формулы изобретения термины имеют следующие значения.
Термин "алкил" относится к одновалентному или двухвалентному радикалу с прямой или разветвленной цепью, состоящей исключительно из углерода и водорода, не имеющему ненасыщенности и содержащему от одного до шести углеродных атомов, например к метилу, этилу, н-пропилу, 1-метилэтилу (изо-пропилу), н-бутилу, н-пентилу, 1,1-диметилэтилу (трет-бутилу) и т.п.
Термин "алкенил" относится к одновалентному или двухвалентному радикалу с прямой и разветвленной цепью, состоящему исключительно из углерода и водорода, содержащему, по крайней мере, одну двойную связь и от одного до шести углеродных атомов, например, к такому радикалу, как этенил, проп-1-енил, бут-1-енил, пент-1-енил, пента-1,4-диенил и т.п.
Термин "алкинил" относится к одновалентному или двухвалентному радикалу с прямой и разветвленной цепью, состоящему исключительно из углерода и водорода, содержащему, по крайней мере, одну тройную связь и от одного до шести углеродных атомов, представляющему собой, например, этинил, проп-1-инил, бут-1-инил, пент-1-инил, пент-3-инил и т.п.
Термин "алкокси" относится к радикалу формулы -ORa, в которой Ra представляет собой алкил, имеющий указанные выше значения, представляющему собой, например, метокси, н-пропокси, 1-метилэтокси(изо-пропокси), н-бутокси, н-пентокси, 1,1-диметилэтокси (трет-бутокси) и т.п.
Термин "алкоксикарбонил" относится к радикалу формулы -С(О)ORa, где Ra представляет собой алкил, имеющий указанные выше значения, например метоксикарбонилу, этоксикарбонилу, н-пропоксикарбонилу, изо-пропоксикарбонилу, трет-бутоксикарбонилу т.п.
Термин "алкилен" относится к двухвалентному радикалу с прямой или разветвленной цепью, состоящему исключительно из углерода и водорода, не имеющему ненасыщенности и содержащему от одного до шести углеродных атомов, представляющему собой, например, метилен, этилен, пропилен, н-бутилен и т.п.
Термин "алкилтио" относится к радикалу формулы -SRa, где Ra представляет собой алкил, имеющий указанные выше значения, представляющему собой, например, метилтио, этилтио, н-пропилтио, трет-бутилтио и т.п.
Термин "амидино" относится к радикалу -C(NH)-NH2.
Термин "аминокарбонил" относится к радикалу -C(O)NH2.
Термин "арил" относится к фенильному или нафтильному радикалу.
Термин "аралкил" относится к радикалу формулы RaRb, где Ra, представляет собой алкил, имеющий указанные выше значения, а Rb, представляет собой арил, имеющий указанные выше значения, например бензил.
Термин "аралкокси" относится к радикалу формулы ORc, где Rc представляет собой аралкил, имеющий указанные выше значения, например бензилокси и т.п.
Термин "циклоалкил" относится к стабильному 3-7 членному моноциклическому насыщенному радикалу, состоящему исключительно из атомов углерода и водорода, представляющему собой, например, циклопропил, циклобутил, циклопентил, циклогексил и т.п.
Термин "циклоалкилалкил" относится к алкильному радикалу, имеющему указанные выше значения, замещенному указанными выше циклоалкильными радикалами, представляющему собой, например, (циклобутил)метил, 2-(циклопентил)этил, 3-(циклогексил)пропил и т.п.
Термин "диалкиламино" относится к радикалу формулы -NRaRa, где каждый Ra независимо представляет собой алкильный радикал, имеющий указанные выше значения, представляющему собой, например, диметиламино, метилэтиламино, диэтиламино, дипропиламино, этилпропиламино и т.п.
Термин "диалкиламинокарбонил" относится к радикалу формулы -C(O)-NRaRa, где каждый Ra независимо представляет собой алкильный радикал, имеющий указанные выше значения, представляющему собой, например, диметиламинокарбонил, метилэти-ламинокарбонил, диэтиламинокарбонил, дипропиламинокарбонил, этилпропиламинокарбонил и т.п.
Термин "галоген" относится к брому, иоду, хлору или фтору.
Термин "галоалкил" относится к алкильному радикалу, имеющему указанные выше значения, который замещен одним или более атомами галогена, представляющему собой, например, трифторметил, дифторметил, трихлорметил, 2-трифторэтил, 3-бром-2-фторпропил, 1-бромметил-2-бромэтил и т.п.
Термин "галоалкенил" относится к алкенильному радикалу, имеющему указанные выше значения, который замещен одним или более указанными выше атомами галогена, представляющему собой, например, 2-дифторэтенил, 3-бром-2-фторпроп-1-енил и т.п.
Термин "галоалкокси" относится к радикалу формулы -ORf, где Rf представляет собой галоалкил, имеющий указанные выше значения, например к трифторметокси, дифторметокси, трихлорметокси, 2-трифторэтокси, 1-фторметил-2-фторэтокси, 3-бром-2-фторпропокси, 1-бромметил-2-бромэтокси и т.п.
Термин "гетероциклил" относится к стабильному 3-10-членному моноциклическому или бициклическому радикалу, который может быть насыщенным или ненасыщенным и который состоит из атомов углерода и одного - трех гетероатомов, выбранных из группы, состоящей из азота, кислорода и серы, где атомы азота, углерода или серы могут быть необязательно окислены, а атом азота необязательно может быть кватернизован. Гетероциклильный радикал может быть присоединен к основной структуре по любому гетероатому или атому углерода при условии, что в результате получается стабильная структура. Примеры таких гетероциклических радикалов включают, но не ограничиваются ими, пиперидинил, пиперазинил, 2-оксопиперазинил, 2-оксопиперидинил, 2-оксопипирролидинил, 2-оксоазепинил, азепинил, пирролил, 4-пиперидонил, пирролидинил, пиразолил, имидазолил, имидазолинил, имидазолидинил, пиридинил, пиразинил, пиримидинил, пиридазинил, оксазолил, оксазолидинил, триазолил, инданил, изоксазолил, изоксазолидинил, морфолинил, тиазолил, тиазолидинил, изотиазолил, хинуклидинил, изотиазолидинил, индолил, изоиндолил, индолинил, изоиндолинил, октагидроиндолил, октагидроизоиндолил, хинолил, изохинолил, декагидроизохинолил, бензимидазолил, тиадиазолил, бензопиранил, бензотиазолил, бензоксазолил, фурил, тетрагидрофурил, тетрагидропиранил, тиенил, бензотиенил, тиаморфолинил, тиаморфолинилсульфоксид, тиаморфолинилсульфон и оксадиазолил. Предпочтительные гетероциклильные радикалы настоящего изобретения представляют собой индолил, имидазолил, тиазолил, изоксазолил, триазолил, пиридинил тиенил, бензотиенил, фурил и 3,4-дигидро-2,3-диоксо-1(2Н)-пиримидинил.
Термин "гетероциклилалкил" относится к радикалу формулы -RaRg, где Ra представляет собой алкильный радикал, имеющий указанные выше значения, a Rg представляет собой гетероциклильный радикал, имеющий указанные выше значения, который представляет собой, например, индолинилметил или имидазолилметил и т.п.
Термин "(1,2)-имидазолил" относится к имидазолильному радикалу, присоединенному в положении 1 или положении 2.
Термин "(1,2)-имидазолинил" относится к 4,5-дигидроимидазолильному радикалу, присоединенному в положении 1 или положении 2.
Термин "моноалкиламино" относится к радикалу формулы -NHRa, где Ra, представляет собой алкильный радикал, имеющий указанные выше значения, например такому радикалу, как метиламино, этиламино, пропиламино и т.п.
Термин "моноалкиламинокарбонил" относится к радикалу формулы -С(О)NHRa, где Ra представляет собой алкильный радикал, имеющий указанные выше значения, например такому радикалу, как метиламинокарбонил, этиламинокарбонил, пропиламинокарбонил и т.п.
Термин "(1,2)-тетрагидропиримидинил" относится к тетрагидропиримидинилу, присоединенному в положении 1 или положении 2.
Термин "адамантилалкил" относится к радикалу формулы -RaRh, где Ra представляет собой алкильный радикал, имеющий указанные выше значения, a Rh представляет собой адамантильный радикал, например такому радикалу, как адамантилметил, 2-адамантилэтил и т.п.
Термины "необязательный" или "необязательно" означают, что описанные далее события или случаи могут как иметь, так и не иметь места и что описание включает примеры, когда указанное событие или случай имеют место и примеры, когда этого не происходит. Так, например, фраза "необязательно замещенный арил" обозначает, что арильный радикал может быть или не быть замещенным и такое определение включает как замещенные арильные радикалы, так и незамещенные арильные радикалы.
Термин "фармацевтически приемлемая соль" включает как соли присоединения кислоты, так и соли присоединения основания.
Термин "фармацевтически приемлемая соль присоединения кислоты" относится к таким солям, которые сохраняют биологическую эффективность и свойства свободного основания, которые не являются нежелательным в биологическом или каком-либо ином отношении, которые образуются в присутствии таких неорганических кислот, как хлористоводородная кислота, бромистоводородная кислота, серная кислота, азотная кислота, фосфорная кислота и т.п., и таких органических кислот, как уксусная кислота, трифторуксусная кислота, пропионовая кислота, гликолевая кислота, пировиноградная кислота, щавелевая кислота, малеиновая кислота, малоновая кислота, янтарная кислота, фумаровая кислота, винная кислота, лимонная кислота, бензойная кислота, коричная кислота, миндальная кислота, метансульфокислота, этансульфокислота, п-толуолсульфокислота, салициловая кислота и т.п.
Фраза "фармацевтически применимая соль присоединения основания" относится к тем солям, которые сохраняют биологическую эффективность и свойства свободных кислот, которые не являются нежелательными в биологическом или каком-либо ином отношении. Такие соли получают в результате присоединения неорганического основания или органического основания к свободной кислоте. Соли, являющиеся производными неорганических оснований, включают, но не ограничиваются ими, соли натрия, калия, лития, аммония, кальция, магния, железа, цинка, меди, марганца, алюминия и т.д. Предпочтительные неорганические соли представляют собой соли аммония, натрия, калия, кальция и магния. Соли, являющиеся производными органических оснований, включают, но не ограничиваются ими, соли первичных, вторичных и третичных аминов, замещенных аминов, включающих замещенные амины природного происхождения, циклических аминов и основных ионообменных смол, как изопропиламин, триметиламин, диэтиламин, триэтиламин, трипропиламин, этаноламин, 2-диметиламиноэтанол, 2-диэтиламиноэтанол, триметамин, дициклогексиламин, лизин, аргинин, гистидин, кофеин, прокаин, гидрабамин, холин, этилендиамин, глюкозамин, метилглюкамин, теобромин, пурины, пиперазин, пиперидин, Х-этилпиперидин, полиаминовые смолы и т. д. Особенно предпочтительные органические основания включают изопропиламин, диэтиламин, этаноламин, триметамин, дициклогексиламин, холин и кофеин.
Термин "терапевтически эффективное количество" относится к такому количеству соединения изобретения, которое, при его введении человеку, нуждающемуся в лечении, является достаточным для лечения, как указано ниже, болезненных состояний, характеризующихся тромботической активностью. Количество соединения изобретения, которое является "терапевтически эффективным количеством" будет изменяться в зависимости от природы соединения, типа болезненного состояния и его тяжести, а также возраста пациента, подлежащего лечению, может быть легко установлено с помощью общепринятых методов специалистом среднего уровня в данной области техники на основании данного описания.
Используемые в тексте термины "лечение" или "терапия", охватывают лечение болезненного состояния людей, характеризующегося тромботической активностью, и включают:
(i) профилактику возникновения болезненного состояния у людей в тех случаях, когда человек предрасположен к такому болезненному состоянию, но диагноз такой болезни у него еще не поставлен;
(ii) подавление болезненного состояния, т.е. купирование его развития, или
(iii) ослабление болезненного состояния, т.е. обеспечение регресса болезненного состояния.
Выход в каждой из реакций, описанных здесь, выражен в процентах от теоретического выхода.
Соединения изобретения или их фармацевтически приемлемые соли могут иметь в своей структуре асимметричный атом углерода. В связи с этим соединения изобретения и их фармацевтически приемлемые соли могут существовать в виде индивидуальных стереоизомеров, рацематов и в виде смесей энантиомеров и диастереомеров. Все такие индивидуальные стереоизомеры, рацематы и их смеси входят в объем настоящего изобретения.
Следует отметить, что в этих случаях, когда R1 является таким же заместителем, как R3, R2 имеет то же значение, как R4, и Z1 и Z2 имеют одинаковые значения, соединения формулы (I) являются такими же, как соединения формулы (II), а соединения формулы (III) идентичны соединениям формулы (IV).
Используемая в описании номенклатура представляет собой модифицированную номенклатуру I.U.P.A.C., где соединения изобретения названы как производные пурина. Так, например, соединение изобретения, выбранное из формулы (II), в которой оба Z1 и Z2 представляют собой -О-; R1 представляет собой -OR10, где R10 - фенил; R2 представляет собой -C(NH)NH2; R3 представляет собой -С(O)N(R10)R11, где оба R10 и R11 представляют собой метил; R4 представляет собой водород; R5 - этил, а R6 представляет собой (C(R7)(R8)n-R9, где n равно 1; R7 представляет собой водород; R8 - этил, а R9 представляет собой -С(О)OR10, где R10 представляет собой метил, т.е. соединение формулы
названо как 2-(3-диметиламинокарбонилфенокси)-6-(2-фенокси-4-амидинофенокси)-(1-метоксикарбонилпропил)-8-этилпурин.
Применение и способы введения
А. Применение.
Соединения настоящего изобретения являются ингибиторами фактора Ха и поэтому полезны для лечения болезненных состояний, характеризующихся тромботической активностью, основанной на роли фактора Ха в системе свертывания крови (см. выше раздел "Область техники, к которой относится изобретение"). Основное главное назначение соединений изобретения состоит в профилактике у пациентов группы долговременного риска после инфаркта миокарда. Дополнительные показания касаются профилактики глубокого тромбофлебита вен (DVT), после ортопедической хирургии или профилактики отдельных пациентов после скоротечных ишемических приступов. Соединения настоящего изобретения могут также использоваться в тех случаях, для которых в последнее время используют кумарин, например в случае DVT или других типов хирургического вмешательства, таких как шунтирование коронарной артерии и подкожная транслюминарная коронарная ангиопластика. Соединения изобретения также полезны для лечения тромботических осложнений, связанных с острым промиелоцитным лейкозом, диабетом, множественными миеломами, диссеминированным внутрисосудистым свертыванием, связанным с септическим шоком, молниеносной пурпуры, связанной с инфекцией, дыхательного дистресс-синдрома взрослых, неустойчивой стенокардии и тромботических осложнений, связанных с протезированием аорты или сосудов. Соединения изобретения также пригодны для профилактики тромботических заболеваний, особенно у пациентов с высоким риском развития такого заболевания.
Кроме этого, соединения настоящего изобретения также применяются в качестве in vitro диагностических реагентов для селективного ингибирования фактора Ха, не сопровождающегося ингибированием других компонентов системы свертывания крови.
В. Тестирование.
В качестве основного биотеста для демонстрации ингибирующего действия соединений изобретения в отношении фактора Ха применяют простой хромогенный анализ, в котором используют только протеазу серина, подлежащее испытанию соединение изобретения, субстрат и буфер (см., например, Thrombosis Res. (1979), т. 16, стр.245-254). Так, например, в основном тесте можно использовать четыре протеазы серина человеческой ткани, свободный фактор Ха, протромбиназу, тромбин (II) и тканевый активатор плазминогена (tPA). Тест на ТРА с успехом использовали ранее для демонстрации нежелательных побочных эффектов при ингибировании фибринолитического процесса (см., например, J. Med. Chem. (1993), т.36, стр.314-319). Другой биотест, используемый для демонстрации полезности соединений изобретения для ингибирования фактора Ха, демонстрирует активность испытуемых соединений в отношении свободного фактора Ха в цитратной плазме. Так, например, антикоагулянтную эффективность соединений изобретения оценивают с использованием протромбинового времени (РТ) или времени частично активированного тромбопластина (аРТТ), тогда как селективность соединений изобретения проверяют с помощью теста на тромбиновое время свертывания крови (ТСТ). Корреляция Ki в главном энзимном тесте с Ki для свободного фактора Ха в цитратной плазме позволяет осуществить скрининг в отношении соединений, которые взаимодействуют с другими компонентами плазмы или инактивируются ими. Корреляция значений Ki с длительностью РТ является обязательной in vitro демонстрацией того, что активность в анализе на ингибирование свободного фактора Ха транслируется на активность в клиническом анализе на свертывание крови. Кроме этого, продолжительность РТ в цитратной плазме может использоваться для измерения длительности действия в последующих фармакодинамических исследованиях.
Дополнительную информацию, касающуюся тестов, демонстрирующих активность соединений изобретения, можно найти в работах R.Lottenberg с сотр. Methods in Еnzymology (1981), т.80, стр.341-361, и H.Ohno с сотр. Trombosis Research (1980), т.19, стр.579-588.
С. Основные способы введения.
Введение соединений изобретения или их фармацевтически приемлемых солей, в чистом виде или в виде подходящей фармацевтической композиции, может проводиться любым приемлемым способом введения или с помощью агентов, используемых для аналогичных применений. Так, например, введение может осуществляться перорально, назально, парентерально, местно, трансдермально или ректально в виде твердой, полутвердой, лиофилизированной порошкообразной или жидкой дозированных форм, например в виде таблеток, суппозиториев, пилюль, мягких эластичных и твердых желатиновых капсул, порошков, растворов, суспензий или аэрозолей и т.п., предпочтительно в единичной дозированной форме, подходящей для простого введения точных доз. Композиции включают обычный фармацевтический носитель или эксципиент, и соединение изобретения в качестве активного агента, а также дополнительно может содержать другие медицинские агенты, фармацевтические агенты, носители, адъюванты и т.п.
Обычно в зависимости от предполагаемого способа введения фармацевтически приемлемые композиции содержат от 1 до 99 вес. % соединения(ий) изобретения или его фармацевтически приемлемой соли и 99-1 вес. % подходящего фармацевтического эксципиента. Предпочтительно композиция содержит 5-75 вес. % соединения(ий) изобретения или его фармацевтически приемлемой соли, причем остаток составляет подходящие фармацевтические эксципиенты.
Предпочтительным способом введения является пероральное введение с использованием общепринятого режима приема ежедневных доз, который может регулироваться в зависимости от степени тяжести болезненного состояния, подлежащего лечению. Фармацевтически приемлемую композицию, содержащую соединение изобретения или его фармацевтически приемлемую соль, предназначенную для такого перорального введения, получают путем введения любых традиционно эксципиентов, например, таких как фармацевтические сорта маннита, лактоза, крахмал, предварительно желатинированный крахмал, стеарат магния, сахарин натрия, тальк, эфирные производные целюлозы, глюкоза, сахароза, цитрат, пропилгаллат и т.п. Такие композиции могут иметь форму растворов, суспензий, таблеток, драже, капсул, порошков, рецептур пролонгированного действия и т.п.
Предпочтительно такие композиции выпускаются в виде капсулы, каплеты (caplet) или таблетки и поэтому содержат такой наполнитель, как лактоза, сахароза, вторичный кислый фосфат кальция и т.п.; такой разрыхлитель, как натрийкроскармелоза или ее производные; такой смазывающий агент, как стеарат магния и т. п., и такой связывающий агент, как крахмал, аравийская камедь, поливинилпирролидон, желатина, эфирные производные целлюлозы и т.п.
Соединения настоящего изобретения или их фармацевтически приемлемые соли также могут быть сформированы в виде суппозиториев с использованием, например, 0.5-50% активного ингредиента, находящегося в носителе, который медленно растворяется в организме, например, таком как полиоксиэтиленгликоли и полиэтиленгликоли (PEG), например PEG 1000 (96%) и PEG 4000 (4%).
Жидкие фармацевтически приемлемые композиции могут быть, например, получены растворением, диспергированием и т.п. соединения изобретения (0.5-20%) или его фармацевтически применимой соли и необязательных фармацевтических адъювантов в таком носителе, как, например, вода, физиологический раствор, водный раствор декстрозы, глицерин, этанол и т.п. с получением раствора или суспензии.
Если желательно, то фармацевтическая композиция изобретения может также содержать небольшие количества таких вспомогательных веществ, как смачивающие или эмульгирующие агенты, буферные агенты, изменяющие значение рН, антиокислители, и т.п., например, такие как лимонная кислота, монолаурат сорбита, олеат триэтаноламина, бутилированный гидрокситолуол и т.п.
Существующие способы получения таких дозированных форм известны или очевидны для специалиста в данной области, см., например, Remington's Pharmaceutical Sciences, 18 издание (Mack Publishing Company, Easton, Pennsylvania, 1990). В любом случае, применяемая композиция будет содержать терапевтически эффективное количество соединения изобретения или его фармацевтически приемлемой соли, предназначенное для лечения болезненного состояния, облегчаемого ингибированием фактора Ха в соответствии с методами настоящего изобретения.
Соединения изобретения или их фармацевтически приемлемые соли вводят в терапевтически эффективном количестве, которое будет изменяться в зависимости от ряда факторов, включающих активность конкретного используемого соединения, метаболическую устойчивость и длительность действия соединения, возраст, вес тела, общее состояние здоровья, пол пациента, диету, вид и время введения, скорость выделения, комбинацию лекарств, тяжесть конкретного болезненного состояния и вид терапии, применяемой для пациента. Обычно терапевтически эффективная дневная доза соединения изобретения или его фармацевтически приемлемой соли составляет от 0.14 до примерно 14,3 мг/кг веса тела в день, предпочтительно 0.7-10 мг/кг веса тела в день и наиболее предпочтительно 1.4-7.2 мг/кг веса тела в день. Так, например, при введении пациенту весом 70 кг интервал соединения изобретения или его фармацевтически приемлемой соли должен составлять от примерно 10 мг до 1.0 г в день, предпочтительно от 50 мг до примерно 700 мг в день и наиболее предпочтительно от 100 мг до 500 мг в день.
Описание предпочтительных воплощений изобретения
Из соединений, описанных выше в разделе "Краткое содержание изобретения", предпочтительная группа включает соединения, в которых Z1 и Z2 независимо представляют собой -О- или -OCH2-, каждый из R1 и R4 независимо представляет водород, галоген или -OR10, -R2 представляет собой -C(NH)NH2, -C(NH)N(H)S(O2)R13 или -С(NH)N(Н)С(О)N(Н)R10; R3 представляет собой уреидо, гуанидино, -С(O)N(R10)R11, -N(R10)R11, -С(О)OR10, -N(R10)С(О)R10, (1, 2)-тетрагидропиримидинил, необязательно замещенный алкилом, (1,2)-имидазолил, необязательно замещенный алкилом, или (1,2)-имидазолинил, необязательно замещенный алкилом; R5 представляет собой водород, галоген, алкил, галоалкил, арил или аралкил; R6 представляет собой алкил, арил, аралкил или (С(R7)(R8)n)-R9 (где n равно 1); R7 представляет собой алкил, -R12-C(O)OR10, -R12-C(О)N(R10)R11, -R12-C(R10)(С(O)OR10)2, -R12-N(R10)R11, -R12-N(R10)C(NR10)R13, -R12-N(R10)C(O)N(R10)R11, -R12-N(R10)C(NR10)N(R10)R11,
-R12-OR10, -R12-OP(O)(OR10)2, -R12-SR10, -R12-S(O)2R13 либо R7 представляет собой аралкил (необязательно замещенный одним или более заместителями, выбранными из группы, состоящей из алкила, галогена, галоалкила, галоалкокси, -OR10, -SR10, -С(О)OR10, N(R10)R11, -C(O)N(R10)R11, -S(O)2OR10 и -ОР(O)(OR10)2), или R7 представляет собой гетероциклилалкил (в котором гетероциклильный радикал необязательно замещен одним или более заместителями, выбранными из группы, состоящей из алкила, галогена, галоалкила, галоалкокси, аралкила, -OR10, -SR10, -C(O)OR10, -N(R10)R11, -C(O)N(R10)R11, -S(O)2OR10 и -ОР(О)(OR10)2); R8 независимо представляет собой алкил; R9 представляет собой -С(О)OR10 или -C(O)N(R10)R11; каждый из радикалов R10 и R11 независимо представляет собой водород, алкил, арил (необязательно замещенный галогеном, алкилом, гидрокси, алкокси, аралкокси, амино, диалкиламино, моноалкиламино, карбокси, алкоксикарбонилом, аминокарбонилом, моноалкиламинокарбонилом или диалкиламинокарбонилом) или аралкил (необязательно замещенный галогеном, алкилом, арилом, гидрокси, алкокси, аралкилом, амино, диалкиламино, моноалкиламино, карбокси, алкоксикарбонилом, аминокарбонилом, моноалкиламинокарбонилом или диалкиламинокарбонилом);
R12 представляет собой нормальную или разветвленную алкиленовую цепь, а R13 представляет собой алкил, арил (необязательно замещенный галогеном, алкилом, гидрокси, алкокси, аралкокси, амино, диалкиламино, моноалкиламино, карбокси, алкоксикарбонилом, аминокарбонилом, моноалкиламинокарбонилом или диалкиламинокарбонилом) или аралкил (необязательно замещенный галогеном, алкилом, арилом, гидрокси, алкокси, аралкилом, амино, диалкиламино, моноалкиламино, карбокси, алкоксикарбонилом, аминокарбонилом, моноалкиламинокарбонилом или диалкиламинокарбонилом).
Из указанной выше группы соединений, предпочтительная подгруппа включает соединения, в которых Z1 и Z2 независимо представляют собой -О-; R1 представляет собой водород или -OR10; R2 представляет собой -C(NH)NH2; R3 представляет собой -С(О)N(R10)R11, (1,2)-тетрагидропиримидинил, необязательно замещенный алкилом, (1,2)-имидазолил, необязательно замещенный алкилом, или (1,2)-имидазолинил, необязательно замещенный алкилом; R4 представляет собой водород; R5 представляет собой алкил или аралкил; R6 представляет собой алкил, аралкил или -(C(R7) (R8)n)-R9; R7 представляет собой алкил, -R12-C(O)OR10, -R12-C(O)N(R10)R11, -R12-C(R10)(С(О)OR10)2, -R12-N(R10)R11,
-R12-N(R10)C(NR10)R13, -R12-N(R10)С(О)N(R10)R11, -R12-N(R10)C(NR10)N(R10)R11, -R12-OR10, -R12-OP(O)(OR10)2, -R12-SR10, -R12-S(O)2R13 или R7 представляет собой аралкил (необязательно замещенный одним или более заместителями, выбранными из группы, состоящей из галогена, галоалкила, гидрокси и ОР(O)(OR10)2) или R7 представляет собой имидазолилалкил или индолилалкил; R8 представляет собой водород или алкил; R9 представляет собой -С(О)OR10 или -С(О)N(R10)R11; каждый из R10 и R11 независимо представляет собой водород или алкил; R12 представляет собой нормальную или разветвленную алкиленовую цепь; а R13 представляет собой алкил или арил.
Из этой подгруппы соединений предпочтительный класс включает соединения, в которых каждый из Z1 и Z2 независимо представляет собой -О-; R1 представляет собой водород; R2 представляет собой -C(NH)NH2, R3 представляет собой -С(О)N(R10)R11, (1, 2)-тетрагидропиримидинил (необязательно замещенный алкилом, (1,2)-имидазолил (необязательно замещенный алкилом) или (1,2)-имидазолинил (необязательно замещенный алкилом); R4 представляет собой водород; R5 представляет собой алкил; R6 представляет собой аралкил или -(C(R7)(R8)n)-R9; R7 представляет собой алкил, -R12-C(О)OR10, -R12-C(О)N(R10)R11, -R12-C(R10)(С(О)OR10)2, -R12-N(R10)R11, -R12-N(R10)С(NR10)R13, -R12-N(R10)C(O)N(R10)R11, -R12-N(R10)C(NR10)N(R10)R11,
-R12-OR10, -R12-OP(O)(OR10)2, -R12-SR10, -R12-S(O)2R13; или R7 представляет собой аралкил (необязательно замещенный одним или более заместителями, выбранными из группы, состоящей из галогена, галоалкила, гидрокси и ОР(O)(OR10)2), или R7 представляет собой имидазолилалкил или индолилалкил; R8 представляет собой водород или алкил; R9 представляет собой -С(О)OR10 или -С(О)N(R10)R11; каждый из R10 и R11 независимо представляет собой водород или алкил; R12 представляет собой нормальную или разветвленную алкиленовую цепь, а R13 представляет собой алкил или арил.
Предпочтительный подкласс из этого класса соединений включает соединения, в которых R3 представляет собой -С(O)N(R10)R11, (1, 2)-имидазолил (необязательно замещенный алкилом) или (1,2)-имидазолинил (необязательно замещенный алкилом); R4 представляет собой водород; R5 представляет собой алкил; R6 представляет собой аралкил или -(C(R7)(R8)n)-R9; R7 представляет собой алкил, -R12-C(О)OR10, -R12-C(О)N(R10)R11, -R12-C(R10) (C(O)OR10)2, -R12-N(R10)R11, -R12-N(R10)C(NR10)R13, -R12-N(R10)С(O)N(R10)R11, -R12-N(R10)C(NR10)N(R10)R11, -R12-OR10, -R12-OP(O)(OR10)2, -R12-SR10, -R12-S(O)2R13; R8 представляет собой водород; R9 представляет собой -С(О)OR10; каждый из R10 и R11 независимо представляет собой водород или алкил; R12 представляет собой нормальную или разветвленную алкиленовую цепь, а R13 представляет собой алкил или арил.
Предпочтительными соединениями такого подкласса являются те, в которых R3 представляет собой -С(O)N(R10)R11; R4 представляет собой водород; R5 представляет собой метил или этил; R6 представляет собой бензил, а R10 и R11 независимо представляют собой водород или метил.
Более предпочтительными соединениями этого подкласса являются те соединения формулы (I) или (II), в которой R3 представляет собой -С(О)N(R10)R11, где каждый из R10 и R11 представляет собой метил, R4 представляет собой водород, R5 представляет собой метил, а R6 представляет собой бензил, а именно 2-(2-гидрокси-5-цианофенокси)-(3-диметиламинокарбонил)фенокси-8-метил-9-бензилпурин и 6-(2-гидрокси-5-цианофенокси)-2-(3-диметиламинокарбонил)фенокси-8-метил-9-бензилпурин.
Получение соединений изобретения
Следующее ниже описание получения соединений изобретения относится к получению соединений формулы (I) и (II). Однако понятно, что аналогичные синтетические методики могут использоваться и для получения соединений формулы (III) и (IV). Следует также иметь в виду, что в следующем ниже описании, комбинации заместителей и/или радикалов (например, R7 и R8) в указанных соединениях допустимы лишь в том случае, когда такие комбинации дают устойчивые соединения.
А. Получение соединений формулы (IIа).
Соединения формулы (IIа) представляют собой такие соединения формулы (II), в которых оба Z1 и Z2 представляют собой -О-, a R2 представляет собой -C(NH)NH2. Такие соединения могут быть получены в соответствии со следующей реакционной схемой 1, в которой R1 и R4 независимо представляют собой водород, галоген, алкил, OR10, -C(O)OR10, -С(O)N(R10)R11, -N(R10)R11, -N(R10)C(O)R10 или N(H)S(O)2R13; R3 представляет собой галоген, алкил, галоалкил, галоалкокси, уреидо, циано, гуанидино, -OR10, -C(NH)NH2, -С(NH)N(Н)OR10 , -С(О)N(R10)R11, -R12-C(O)N(R10)R11, СH(ОН)C(О)N(R10)R11, -R12-N(R10)R11, -С(О)OR10, -R12-C(О)OR10, -N(R10)C(O)R10, (1,2)-тетрагидропиримидинил (необязательно замещенный алкилом), (1,2)-имидазолил (необязательно замещенный алкилом) или (1,2)-имидазолинил (необязательно замещенный алкилом); R5 представляет собой водород, алкил, циклоалкил, галоалкил, арил или аралкил; R6 представляет собой водород, алкил, арил (необязательно замещенный галогеном, алкилом, гидрокси, алкокси, аралкокси, амино, диалкиламино, моноалкиламино, карбокси, алкоксикарбонилом, аминокарбонилом, моноалкиламинокарбонилом или диалкиламинокарбонилом) или аралкил (необязательно замещенный галогеном, алкилом, арилом, гидрокси, алкокси, аралкилом, амино, диалкиламино, моноалкиламино, карбокси, алкоксикарбонилом, аминокарбонилом, моноалкиламинокарбонилом или диалкиламинокарбонилом); каждый из R10 и R11 независимо представляет собой водород, алкил, арил (необязательно замещенный галогеном, алкилом, гидрокси, алкокси, аралкокси, амино, диалкиламино, моноалкиламино, карбокси, алкоксикарбонилом, аминокарбонилом, моноалкиламинокарбонилом или диалкиламинокарбонилом) или аралкил (необязательно замещенный галогеном, алкилом, арилом, гидрокси, алкокси, аралкилом, амино, диалкиламино, моноалкиламино, карбокси, алкоксикарбонилом, аминокарбонилом, моноалкиламинокарбонилом или диалкиламинокарбонилом); R12 представляет собой нормальную или разветвленную алкиленовую цепь, а R13 представляет собой представляет собой алкил, арил (необязательно замещенный галогеном, алкилом, гидрокси, алкокси, амино, диалкиламино, моноалкиламино, карбокси, алкоксикарбонилом, аминокарбонилом, моноалкиламинокарбонилом или диалкиламинокарбонилом) или аралкил (необязательно замещенный галогеном, алкилом, арилом, гидрокси, алкокси, аралкилом, амино, диалкиламино, моноалкиламино, карбокcи, алкоксикарбонилом, аминокарбонилом, моноалкиламино карбонилом или диалкиламинокарбонилом), а R14 представляет собой алкил (см. схему 1 в конце описания).
Соединения формулы (А), формулы (В), формулы (D), формулы (G) и формулы (К) представляют собой коммерчески доступные вещества, поставляемые, например, Aldrich Chemical Co. или Sigma Chemical Co., или ICN Biomedical, либо они могут быть получены способами, известными специалистам в данной области техники.
Обычно соединения формулы (IIНа) получают обработкой соединения формулы (А) в среде такого апротонного растворителя, как ацетонитрил, при температурах в интервале от -10 до 10oС, предпочтительно при 0oС, эквимолярным количеством соединения формулы (В) в присутствии основания, например карбоната цезия. Реакционную смесь перемешивают при комнатной температуре в течение 12-20 часов, предпочтительно в течение 16 часов. Затем соединение формулы (С) выделяют из реакционной смеси такими стандартными способами, как экстракция, удаление растворителя в вакууме и флэш- хроматография.
Соединение формулы (С) в среде апротонного растворителя, предпочтительно в среде ацетонитрила, при температурах от -10 до 10oС, предпочтительно при 0oС, в присутствии основания, предпочтительно карбоната цезия, обрабатывают эквимолярным количеством соединения формулы (D). Полученную в результате смесь нагревают до 50oС в течение 3-6 часов, предпочтительно в течение 4 часов. Соединение формулы (Е) выделяют из реакционной смеси такими стандартными методами, как фильтрация, удаление растворителей в вакууме и флэш-хроматография.
Затем соединение формулы (Е) в среде такого протонного растворителя, как метанол, при температурах в интервале от -10 до10oС, предпочтительно при 0oС, обрабатывают таким сильным окисляющим агентом, как метабисульфит калия (KHSO5) в воде. Полученную в результате реакционную смесь перемешивают при температуре окружающей среды в течение 12-16 часов, предпочтительно в течение 15 часов. Полученную смесь концентрируют и экстрагируют таким апротонным растворителем, как метиленхлорид с получением соответствующего сульфонильного соединения формулы (F).
Соединение формулы (F) растворяют в апротонном растворителе, предпочтительно ацетонитриле, при температурах в интервале от -10oС до 10oС, предпочтительно при 0oС, в присутствии основания, предпочтительно карбоната цезия. Затем в раствор добавляют соединение формулы (G) и полученную реакционную смесь перемешивали при температуре окружающей среды в течение 12-16 часов, предпочтительно в течение 16 часов. Затем соединение формулы (Н) выделяют из реакционной смеси стандартными способами, такими как удаление растворителя в вакууме и флэш-хроматография.
Соединение формулы (Н) восстанавливают в стандартных условиях, например, с использованием Zn/HCl. Полученное в результате аминосоединение формулы (J) выделяют из реакционной смеси с помощью таких стандартных методик, как нейтрализация слабым основанием, например NaHCO3, последующей экстракцией таким органическим растворителем, как этилиацетат и удалением растворителя в вакууме. Соединение формулы (J) обрабатывают имидатом формулы (К) в таком полярном растворителе, как смесь тетрагидрофурана (THF) и этанола при температурах в интервале 60-75oС, предпочтительно при 70oС, в течение 2-4 часов, предпочтительно в течение 3 часов. Затем это соединение нагревают в вакууме, при температуре в интервале от 150 до 200oС, предпочтительно при 170oС, в течение 1-3 часов, предпочтительно в течение 2 часов. Затем реакционную смесь концентрируют с получением масла, которое далее очищают стандартными методами (фильтрация, экстракция и удаление растворителя в вакууме) с получением пурина формулы (L).
Соединение формулы (L) растворяют в спирте, предпочтительно этаноле, при 0oС и полученный раствор затем насыщают газообразной минеральной кислотой, предпочтительно хлористоводородной кислотой. Реакционную смесь герметично закрывают и дают нагреться до температуры окружающей среды в течение времени от 12 до 16 часов. Затем реакционную смесь концентрируют и к концентрированной смеси добавляют такой полярный растворитель, как эфир. Полученный в результате осадок растворяют в спирте, предпочтительно в этаноле, полученный раствор охлаждают до 0oС и затем обрабатывают безводным аммиаком (газ) в течение 5-20 минут. Реакционную смесь герметично закрывают и нагревают при температуре в интервале от комнатной до 100oС, предпочтительно при 60oС, в течение 2-6 часов, предпочтительно в течение 2 часов. Затем реакционную смесь охлаждают и выпаривают растворители. Соединение формулы (IIа) выделяют из реакционной смеси такими стандартными методами, как фильтрация, выпаривание растворителей и очистка методом препаративной ЖХВД.
Альтернативно полученный выше раствор можно обрабатывать не безводным аммиаком, а соединением формулы NH2OR10 с получением соединения формулы (II), в котором R2 представляет собой -C(NH)N(H)OR10.
Соединения формулы (IIа), в которой R3 представляет собой -C(NH)NH2 или -С(NH)N(H)OR10, получают из соответствующих цианопроизводных методом, аналогичным описанному выше для соединений формулы (L).
Кроме этого, соединения формулы (IIа), в которой R1, R2, R4 или R6 содержат группу -С(O)N(R10)R11 или группу -С(О)OR10 (где каждый из R10 и R11 независимо представляет собой алкил, необязательно замещенный арил или необязательно замещенный аралкил), могут быть гидролизованы в кислых условиях с целью получения соединений изобретения, в которых R1, R2, R4 или R6 содержат карбоксигруппу.
Кроме этого, соединения формулы (IIа), в которой R1, R2, R4 или R6 содержат группу -С(О)OR10, в которой R10 представляет собой водород, алкил, необязательно замещенный арил или необязательно замещенный аралкил, могут быть амидированы в стандартных условиях амидирования, с образованием соответствующих соединений формулы (IIа), в которой R1, R2, R4 или R6 содержат группу -С(O)N(R10)R11, в которой R10 и R11 независимо представляют собой водород, алкил, необязательно замещенный арил или необязательно замещенный аралкил.
Кроме этого, соединения формулы (IIа), в которой R1, R2, R4 или R6 содержат аминогруппу, могут быть обработаны соответствующими алкилирующими агентами с получением соответствующих соединений формулы (IIа), в которой R1, R2, R4 или R6 содержат -N(R10)R11 или -N(R10)С(О)R11, где каждый из R10 и R11 независимо представляет собой водород, алкил, необязательно замещенный арил или необязательно замещенный аралкил.
Соединения формулы (IIа) могут быть дополнительно обработаны соответствующим галогенангидридом, предпочтительно хлорангидридом, или соответствующим ангидридом, или его эквивалентом с образованием соединений изобретения, в которых R2 представляет собой -С(NH)N(Н)С(О)R10, где R10 представляет собой водород, алкил, необязательно замещенный арил или обязательно замещенный аралкил. Альтернативно соединения формулы (IIа) могут быть дополнительно обработаны карбамоилхлоридами или их эквивалентами с образованием соединений изобретения, в которых R2 представляет собой -С(NH)N(Н)С(О)OR13, где R13 имеет значения, указанные в разделе "Краткое изложение сущности изобретения".
Альтернативно соединения формулы (IIа) могут быть дополнительно обработаны соединениями формулы R13-S(O)2-имидазол, где R13 имеет значения, указанные в разделе "Краткое изложение сущности изобретения", в среде такого полярного растворителя, как метиленхлорид при температуре окружающей среды с получением соединений изобретения, в которых R2 представляет собой -C(NH)N(H)C(O)OR13.
Альтернативно соединения формулы (IIа) могут быть дополнительно обработаны соответствующим образом N-R10-замещенным фенилкарбаматом в среде полярного растворителя, предпочтительно метиленхлорида, при температуре окружающей среды в течение 6-24 часов, предпочтительно в течение 12 часов, с получением соединений изобретения, в которых R2 представляет собой -C(NH)N(H)C(O)N(H)R10.
Кроме этого, соединения формулы (IIа), в которой R6 представляет собой водород, могут быть обработаны по методике, описанной в Dusert P., Eur. J. Med. Chem. (1980), т. 15, 3, стр.199, с образованием соединений формулы (IIа), в которой R6 представляет собой -(C(R7)(R8)n)-R9. Так, например, соединение формулы (IIа), в которой R6 представляет собой водород, может быть вначале обработано таким сильным основанием, как гидрид натрия, в среде такого апротонного растворителя, как DMF, с последующей обработкой эквимолярным количеством соединения формулы X(C(R7)(R8)n)-R9, в которой Х представляет собой бром или хлор, a n, R7, R8 и R9 имеют значения, указанные в разделе "Краткое изложение сущности изобретения". Затем реакционную смесь перемешивают в течение 2-6 часов, предпочтительно в течение 4 часов, при температуре в интервале от температуры окружающей среды до 80oС. Соединения формулы (IIа), в которой R6 представляет собой -(С(R7)(R8)n)-R9, далее может быть выделено из реакционной смеси стандартными методами.
Альтернативно соединения формулы, в которой R5 представляет собой водород, могут быть обработаны по методу, аналогичному описанному в Stevenson T. M., J. Org. Chem. (1984), т.49, 12, стр.2158, c получением соединений формулы (IIа), в которой R5 представляет собой галоген. Так, например, соединение формулы (IIа), в которой R5 представляет собой водород, может быть обработано мягким электрофильным галогенирующим агентом, таким как N-бромсукцинамид или N-хлорсукцинамид, в среде четыреххлористого углерода с образованием соединения формулы (IIа), в которой R5 представляет собой хлор или бром.
Помимо этого соединения формулы (J) могут быть обработаны N,N-карбонилдиимидазолом или N, N-тиокарбонилдиимидазолом в соответствующих условиях проведения реакции с образованием соединений формулы (L), в которой R5 представляет собой гидроксигруппу (в качестве карбонильного таутомера) или меркаптогруппу. Полученное таким образом соединение может быть обработано тем же методом, что описан выше, с получением соединения формулы (IIа), в которой R5 представляет собой гидрокси или меркапто.
Кроме этого, соединения формулы (J) могут быть обработаны тиоизоцианатом формулы R10NCS, где R10 имеет значения, указанные выше в разделе "Краткое изложение сущности изобретения", по методу описанному в Omar А. с сотр., Synthesis (1977), стр. 864; Ram S., Org. Prep. Proceed. Int. (1985), т.17, 3, стр. 125, или Janssen F., J. Med. Chem. (1985), т.28, 12, стр.1925, с получением соединения формулы (L), в которой R5 представляет собой -N(H)R10. Это соединение может быть затем обработано таким стандартным алкилирующим агентом, как галоалкил формулы R11X или галогенангидрид формулы R11C(O)X, где Х представляет собой галоген, а R11 имеет значения, указанные выше в разделе "Краткое изложение сущности изобретения", с образованием соединения формулы (L), в которой R5 представляет собой -NR10R11 и в которой азот в положении 5 находится в алкилированном состоянии.
Соединение формулы (IIа), в которой R5 представляет собой меркаптогруппу, может быть дополнительно обработано таким галоалкилом, как бромистый метил, в среде такого диполярного растворителя, как диметилсульфоксид и в присутствии такого мягкого основания, как карбонат калия, с образованием соединения формулы (IIа), в которой R5 представляет собой алкилтиогруппу.
Аналогичным образом соединение формулы (IIа), в которой R5 представляет собой гидрокси, может быть дополнительно обработано галогеналкилом, в присутствии такого сильного основания, как гидрид натрия и в среде такого апротонного растворителя, как ДМФ, с образованием соединения формулы (IIа), в которой R5 представляет собой алкокси.
В. Получение соединений формулы (Iа).
Соединения формулы (Iа) представляют собой соединения формулы (I), в которой Z1 и Z2 представляют собой -О-, а R2 представляет собой -C(NH)NH2. Такие соединения могут быть получены, как проиллюстрировано на следующей реакционной схемой 2, в которой Х представляет собой галоген; каждый R1 и R4 независимо представляют собой водород, галоген, алкил, OR10, -С(О)OR10, -C(O)N(R10)R11, -N(R10)R11, -N(R10)С(О)R10 или -N(Н)S(О)2-R13; R3 представляет собой галоген, алкил, галоалкил, галоалкокси, уреидо, циано, гуанидино, -OR10, -C(NH)NH2, -C(NH)N(H)OR10, -C(O)N(R10)R11, -R12-C(О)N(R10)R11, CH(OH)C(O)N(R10)R11, -R12-N(R10)R11, -C(O)OR10, -R12-C(O)OR10, -N(R10)С(O)R10, (1,2)-тетрагидропиримидинил (необязательно замещенный алкилом), (1,2)-имидазолил (необязательно замещенный алкилом) или (1,2)-имидазолинил (необязательно замещенный алкилом); R5 представляет собой водород, алкил, циклоалкил, галоалкил, арил или аралкил; R6 представляет собой алкил, арил (необязательно замещенный галогеном, алкилом, гидрокси, алкокси, аралкокси, амино, диалкиламино, моноалкиламино, циано, карбокси, алкоксикарбонилом, аминокарбонилом, моноалкиламинокарбонилом или диалкиламинокарбонилом) или аралкил (необязательно замещенный гало, алкилом, арилом, алкокси, аралкилом, амино, диалкиламино, моноалкиламино, циано, карбокси, алкоксикарбонилом, аминокарбонилом, моноалкиламинокарбонилом или диалкиламинокарбонилом); каждый из R10 и R11 независимо представляет собой водород, алкил, арил (необязательно замещенный гало, алкилом, гидрокси, алкокси, аралкокси, амино, диалкиламино, моноалкиламино, циано, карбокси, алкоксикарбонилом, аминокарбонилом, моноалкиламинокарбонилом или диалкиламинокарбонилом) или аралкил (необязательно замещенный гало, алкилом, арилом, гидрокси, алкокси, аралкилом, амино, диалкиламино, моноалкиламино, циано, карбокси, алкоксикарбонилом, аминокарбонилом, моноалкиламинокарбонилом или диалкиламинокарбонилом); R12 представляет собой нормальную или разветвленную алкиленовую цепь; R13 представляет собой алкил, арил (необязательно замещенный гало, алкилом, гидрокси, алкокси, аралкокси, амино, диалкиламино, моноалкиламино, циано, карбокси, алкоксикарбонилом, аминокарбонилом, моноалкиламинокарбонилом или диалкиламинокарбонилом) или аралкил (необязательно замещенный гало, алкилом, арилом, гидрокси, алкокси, аралкилом, амино, диалкиламино, моноалкиламино, циано, карбокси, алкоксикарбонилом, аминокарбонилом, моноалкиламинокарбонилом или диалкиламинокарбонилом), a R14 представляет собой алкил (см. схему 2).
В общем, соединения формулы (Iа) получают первоначальной обработкой соединения формулы (А) соединением формулы (G) по способу, аналогичному описанному выше для получения соединений формулы (Н) из соединений формулы (F) и (G), с образованием соединения формулы (М). Затем соединение формулы (М) обрабатывают соединением формулы (D) по способу, аналогичному описанному выше для соединения формулы (С), с получением соединения формулы (N). Соединение формулы (N) окисляют в соответствующее соединение формулы (О) по способу, аналогичному описанному выше для соединений формулы (Е). Соединение формулы (О) обрабатывают соединением формулы (В) по способу, аналогичному описанному выше для соединения формулы (А), с получением соединения формулы (Р), которое затем восстанавливают в соответствующее соединение формулы (Q), по способу, аналогичному описанному выше для соединений формулы (Н). Далее соединение формулы (Q) обрабатывают алкиламидатом формулы (К), по методике, аналогичной описанной выше для соединения формулы (J), с получением соединения формулы (R), которое превращают в соответствующее производное амидина формулы (Iа), по методике, аналогичной описанной выше для соединения формулы (L).
Кроме этого, все превращения различных заместителей, описанные выше для соединений формулы (IIа), применимы к соединениям формулы (Iа) с получением дополнительных соединений изобретения, не отраженных в предшествующей реакционной схеме.
Кроме этого, аналогичные реакции могут быть осуществлены с использованием тех же исходных материалов и промежуточных продуктов с получением соответствующих соединений формулы (III) и соединений формулы (IV).
Следует также отметить, что все соединения изобретения, которые существуют в виде свободного основания или свободной кислоты, могут быть превращены в их фармацевтически приемлемые соли в результате обработки соответствующей неорганической или органической кислотой, или соответствующим неорганическим или органическим основанием. Соли соединений изобретения также могут быть превращены в свободное основание или свободную кислоту, либо в другую соль с помощью способов, известных специалистам в области химии.
Следующие ниже конкретные препаративные примеры и примеры представлены в качестве руководства для практического применения настоящего изобретения и они не ограничивают объем изобретения.
Препаративный пример 1
Соединения формулы (С) и формулы (Р).
А. К 4,6-дихлор-5-нитро-2-метилтиопиримидину (5.0 г, 20.8 ммоля) в 200 мл ацетонитрила при 0oС, добавляли карбонат цезия (8.82 г, 27.1 ммоля) с последующим добавлением 3-гидрокси-4-бензилоксибензонитрила (4.69 г, 20.8 ммоля) и полученную в результате смесь перемешивали в течение 16 часов.
Летучие вещества выпаривали и остаток подвергали хроматографической обработке на силикагеле (гексан/этилацетат, 2:1) с получением 5.0 г 2-метилтио-4-хлор-5-нитро-6-(2-бензилокси-5-цианофенокси)пиримидина, соединения формулы (С).
В. Аналогичным способом получали следующие соединения формулы (С):
2-метилтио-4-хлор-5-нитро-6-(2-метокси-5-цианофенокси)пиримидин;
2-метилтио-4-хлор-5-нитро-6-(2-этокси-5-цианофенокси)пиримидин;
2-метилтио-4-хлор-5-нитро-6-(3-метокси-5-цианофенокси)пиримидин;
2-метилтио-4-хлор-5-нитро-6-(3-этокси-5-цианофенокси)пиримидин;
2-метилтио-4-хлор-5-нитро-6-(2-фенокси-5-цианофенокси)пиримидин;
2-метилтио-4-хлор-5-нитро-6-(3-фенокси-5-цианофенокси)пиримидин;
2-метилтио-4-хлор-5-нитро-6-(3-хлор-5-цианофенокси)пиримидин;
2-метилтио-4-хлор-5-нитро-6-(3-бром-5-цианофенокси)пиримидин;
2-метилтио-4-хлор-5-нитро-6-(2-метил-5-цианофенокси)пиримидин;
2-метилтио-4-хлор-5-нитро-6-(3-метил-4-цианофенокси)пиримидин;
2-метилтио-4-хлор-5-нитро-6-(2-нитро-5-цианофенокси)пиримидин;
2-метилтио-4-хлор-5-нитро-6-(3-нитро-4-цианофенокси)пиримидин;
2-метилтио-4-хлор-5-нитро-6-(2-карбокси-5-цианофенокси)пиримидин;
2-метилтио-4-хлор-5-нитро-6-(3-карбокси-4-цианофенокси)пиримидин;
2-метилтио-4-хлор-5-нитро-6-(2-трет-бутоксикарбонил-5-цианофенокси)пиримидин;
2-метилтио-4-хлор-5-нитро-6-(3-трет-бутоксикарбонил-4-цианофенокси)пиримидин;
2-метилтио-4-хлор-5-нитро-6-(2-аминокарбонил-5-цианофенокси)пиримидин;
2-метилтио-4-хлор-5-нитро-6-(3-аминокарбонил-4-цианофенокси)пиримидин;
2-метилтио-4-хлор-5-нитро-6-(2-диметиламино-5-цианофенокси)пиримидин;
2-метилтио-4-хлор-5-нитро-6-(3-диметиламино-4-цианофенокси)пиримидин;
2-метилтио-4-хлор-5-нитро-6-(2-диметиламино-5-цианофенокси)пиримидин и
2-метилтио-4-хлор-5-нитро-6-(3-диметиламино-4-цианофенокси)пиримидин.
С. Аналогичным образом 2-метилсульфонил-4-бензиламино-5-нитро-6-(3-диметиламинокарбонилфенокси)пиримидин обрабатывали 3-гидрокси-4-бензилоксинитрилом в присутствии карбоната цезия с получением 2-(2-бензилокси-5-цианофенокси)-4-бензиламино-5-нитро-6-(3-диметиламинокарбонилфенокси)пиримидина, соединения формулы (Р).
D. Аналогичным способом получали следующие соединения формулы (Р):
2-(2-бензилокси-5-цианофенокси)-4-бензиламино-5-нитро-6-(3-диметиламинокарбонилфенокси)пиримидин;
2-(2-метокси-5-цианофенокси)-4-бензиламино-5-нитро-6-(3-диметиламинокарбонилфенокси)пиримидин;
2-(2-этокси-5-цианофенокси)-4-бензиламино-5-нитро-6-(3-диметиламинокарбонилфенокси)пиримидин;
2-(2-фенокси-5-цианофенокси)-4-бензиламино-5-нитро-6-(3-диметиламинокарбонилфенокси)пиримидин;
2-(2-хлор-5-цианофенокси)-4-бензиламино-5-нитро-6-(3-диметиламинокарбонилфенокси)пиримидин;
2-(2-метил-5-цианофенокси)-4-бензиламино-5-нитро-6-(3-диметиламинокарбонилфенокси)пиримидин;
2-(2-трет-бутил-5-цианофенокси)-4-бензиламино-5-нитро-6-(3-диметиламинокарбонилфенокси)пиримидин;
2-(2-нитро-5-цианофенокси)-4-бензиламино-5-нитро-6-(3-диметиламинокарбонилфенокси)пиримидин;
2-(2-карбокси-5-цианофенокси)-4-бензиламино-5-нитро-6-(3-диметиламинокарбонилфенокси)пиримидин;
2-(2-бензилоксикарбонил-5-цианофенокси)-4-бензиламино-5-нитро-6-(3-диметиламинокарбонилфенокси)пиримидин;
2-(2-диэтиламинокарбонил-5-цианофенокси)-4-бензиламино-5-нитро-6-(3-диметиламинокарбонилфенокси)пиримидин;
2-(2-амино-5-цианофенокси)-4-бензиламино-5-нитро-6-(3-диметиламинокарбонилфенокси)пиримидин;
2-(2-бензилокси-5-цианофенокси)-4-бензиламино-5-нитро-6-(3-(1-метилимидазолин-2-ил)фенокси)пиримидин;
2-(2-метокси-5-цианофенокси)-4-бензиламино-5-нитро-6-(3-(2-(трет-бутоксикарбонил)этил)фенокси)пиримидин;
2-(2-этокси-5-цианофенокси)-4-бензиламино-5-нитро-6-(3-(трет-бутоксикарбонил)фенокси)пиримидин;
2-(2-фенокси-5-цианофенокси)-4-бензиламино-5-нитро-6-(3-карбоксифенокси)пиримидин;
2-(2-хлор-5-цианофенокси)-4-бензиламино-5-нитро-6-(3-(2-аминоэтил)фенокси)пиримидин;
2-(2-метил-5-цианофенокси)-4-бензиламино-5-нитро-6-(3-(бензилокси)фенокси)пиримидин;
2-(2-трет-бутил-5-цианофенокси)-4-бензиламино-5-нитро-6-(3-этоксифенокси)пиримидин,
2-(2-нитро-5-цианофенокси)-4-бензиламино-5-нитро-6-(3-гуанидинофенокси)пиримидин;
2-(2-карбокси-5-цианофенокси)-4-бензиламино-5-нитро-6-(3-уреидофенокси)пиримидин;
2-(2-бензилоксикарбонил-5-цианофенокси)-4-бензиламино-5-нитро-6-(3-аминофенокси)пиримидин;
2-(2-диэтиламинокарбонил-5-цианофенокси)-4-бензиламино-5-нитро-6-(3-нитрофенокси)пиримидин и
2-(2-амино-5-цианофенокси)-4-бензиламино-5-нитро-6-(3-трифторметоксифенокси)пиримидин.
Препаративный пример 2
Соединения формулы (Е) и формулы (N).
А. К 6-(2-бензилокси-5-цианофенокси)-4-хлор-5-нитро-2-метилтиопиримидину (2.5 г, 5.83 ммоля) в 50 мл ацетонитрила при 0oС добавляли карбонат цезия (2.47 г, 7.58 ммоля) с последующим добавлением бензиламина (0.64 мл) и реакционную смесь нагревали в течение 4 часов при 50oС. Реакционную смесь фильтровали, фильтрат выпаривали и остаток подвергали хроматографической обработке на силикагеле (этилацетат/гексан) с получением 1.82 г (65%) 6-(2-бензилокси-5-цианофенокси-4-(бензил)амино-5-нитро-2-метилтиопиримидина, соединения формулы (Е).
В. Аналогичным образом получали следующие соединения формулы (Е):
2-метилтио-4-(бензил)амино-5-нитро-6-(2-метокси-5-цианофенокси)пиримидин;
2-метилтио-4-(бензил)амино-5-нитро-6-(2-этокси-5-цианофенокси)пиримидин;
2-метилтио-4-(бензил)амино-5-нитро-6-(3-метокси-5-цианофенокси)пиримидин;
2-метилтио-4-(бензил)амино-5-нитро-6-(3-этокси-5-цианофенокси)пиримидин;
2-метилтио-4-(бензил)амино-5-нитро-6-(2-фенокси-5-цианофенокси)пиримидин;
2-метилтио-4-(бензил)амино-5-нитро-6-(3-фенокси-5-цианофенокси)пиримидин;
2-метилтио-4-(бензил)амина-5-нитро-6-(2-хлор-5-цианофенокси)пиримидин;
2-метилтио-4-(бензил)амино-5-нитро-6-(3-бром-5-цианофенокси)пиримидин;
2-метилтио-4-(бензил)амино-5-нитро-6-(2-метил-5-цианофенокси)пиримидин;
2-метилтио-4-(бензил)амино-5-нитро-6-(3-метил-4-цианофенокси)пиримидин;
2-метилтио-4-(бензил)амино-5-нитро-6-(2-нитро-5-цианофенокси)пиримидин;
2-метилтио-4-(бензил)амино-5-нитро-6-(3-нитро-4-цианофенокси)пиримидин;
2-метилтио-4-(бензил)амина-5-нитро-6-(2-карбокси-5-цианофенокси)пиримидин;
2-метилтио-4-(бензил)амино-5-нитро-6-(3-карбокси-4-цианофенокси)пиримидин;
2-метилтио-4-(бензил)амино-5-нитро-6-(2-трет-бутоксикарбонил-5-цианофенокси)пиримидин;
2-метилтио-4-(бензил)амино-5-нитро-6-(3-трет-бутоксикарбонил-4-цианофенокси)пиримидин;
2-метилтио-4-(бензил)амино-5-нитро-6-(2-аминокарбонил-5-цианофенокси)пиримидин;
2-метилтио-4-(бензил)амино-5-нитро-6-(3-аминокарбонил-4-цианофенокси)пиримидин;
2-метилтио-4-(бензил)амино-5-нитро-6-(2-диметиламино-5-цианофенокси)пиримидин;
2-метилтио-4-(бензил)амино-5-нитро-6-(3-диметиламино-4-цианофенокси)пиримидин;
2-метилтио-4-амино-5-нитро-6-(2-метокси-5-цианофенокси)пиримидин;
2-метилтио-4-амино-5-нитро-6-(2-этокси-5-цианофенокси)пиримидин;
2-метилтио-4-амино-5-нитро-6-(3-метокси-5-цианофенокси)пиримидин;
2-метилтио-4-амино-5-нитро-6-(3-этокси-5-цианофенокси)пиримидин;
2-метилтио-4-амино-5-нитро-6-(2-фенокси-5-цианофенокси)пиримидин;
2-метилтио-4-амино-5-нитро-6-(3-фенокси-5-цианофенокси)пиримидин;
2-метилтио-4-амино-5-нитро-6-(2-хлор-5-цианофенокси)пиримидин;
2-метилтио-4-амино-5-нитро-6-(3-бром-5-цианофенокси)пиримидин;
2-метилтио-4-амино-5-нитро-6-(2-метил-5-цианофенокси)пиримидин;
2-метилтио-4-амино-5-нитро-6-(3-метил-4-цианофенокси)пиримидин;
2-метилтио-4-амино-5-нитро-6-(2-нитро-5-цианофенокси)пиримидин;
2-метилтио-4-амино-5-нитро-6-(3-нитро-4-цианофенокси)пиримидин;
2-метилтио-4-амино-5-нитро-6-(2-карбокси-5-цианофенокси)пиримидин;
2-метилтио-4-амино-5-нитро-6-(3-карбокси-4-цианофенокси)пиримидин;
2-метилтио-4-амино-5-нитро-6-(2-трет-бутокси-5-цианофенокси)пиримидин;
2-метилтио-4-амино-5-нитро-6-(3-трет-бутокси-4-цианофенокси)пиримидин;
2-метилтио-4-амино-5-нитро-6-(2-аминокарбонил-5-цианофенокси)пиримидин;
2-метилтио-4-амино-5-нитро-6-(3-аминокарбонил-4-цианофенокси)пиримидин;
2-метилтио-4-амино-5-нитро-6-(2-диметиламино-5-цианофенокси)пиримидин и
2-метилтио-4-амино-5-нитро-6-(3-диметиламино-4-цианофенокси)пиримидин.
С. Аналогичным образом к 2-метилтио-4-хлор-5-нитро-6-(3-диметиламинокарбонилфенокси)пиримидину (3.19 г, 8.65 ммоля), соединению формулы (М) в 90 мл ацетонитрила при 0oС добавляли карбонат цезия (3.66 г, 11.2 ммоля) с последующим добавлением бензиламина (0.95 мл, 8.65 ммоля). Реакционную смесь нагревали при 75oС в течение 4 часов. Реакционную смесь фильтровали, фильтрат выпаривали и остаток подвергали хроматографической обработке на силикагеле (этилацетат/метанол, 10: 1) с получением 1.76 г (48%) 2-метилтио-4-(бензил)амино-5-нитро-6-(3-диметиламинокарбонилфенокси)пиримидина, соединения формулы (N).
D. Аналогичным образом получали следующие соединения формулы (N):
2-метилтио-4-бензиламино-5-нитро-6-(3-(2-(диметиламинокарбонил)этил)фенокси)пиримидин;
2-метилтио-4-бензиламино-5-нитро-6-(3-(2-(диметиламинокарбонил)этил)-5-метоксифенокси)пиримидин;
2-метилтио-4-бензиламино-5-нитро-6-(3-(2-(диметиламинокарбонил)этил)-5-хлорфенокси)пиримидин;
2-метилтио-4-бензиламино-5-нитро-6-(3-хлор-5-метоксифенокси)пиримидин;
2-метилтио-4-бензиламино-5-нитро-6-(3-трифторметил-5-(диметиламинокарбонил)фенокси)пиримидин;
2-метилтио-4-бензиламино-5-нитро-6-(3-гуанидинофенокси)пиримидин;
2-метилтио-4-бензиламино-5-нитро-6-(3-уреидофенокси)пиримидин;
2-метилтио-4-бензиламино-5-нитро-6-(3-нитрофенокси)пиримидин;
2-метилтио-4-бензиламино-5-нитро-6-(3-гуанидино-5-метилфенокси)пиримидин;
2-метилтио-4-бензиламино-5-нитро-6-(3-уреидо-5-метилфенокси)пиримидин и
2-метилтио-4-бензиламино-5-нитро-6-(3-нитро-5-аминофенокси)пиримидин.
Препаративный пример 3
Соединения формул (F) и (О).
А. К 2-метилтио-4-бензиламино-5-нитро-6-(2-бензилокси-5-циано-фенокси) пиримидину (1.82 г, 3.76 ммоля) в 40 мл МеОН и 40 мл диоксана при 0oC добавляли метабисульфит калия (KHSO5) (3.59 г, 11.3 ммоля) в 40 мл воды. Суспензии давали нагреваться до температуры окружающей среды и затем перемешивали в течение 15 часов. Реакционную смесь концентрировали до объема 25 мл и экстрагировали метиленхлоридом (200 мл). Органический слой сушили (Nа2SO4), выпаривали и подвергали хроматографической обработке на силикагеле (2:1, гексан/этилацетат) с получением 0.26 г 2-метилсульфонил-4-бензиламино-5-нитро-6-(2-бензилокси-5-цианофенокси)пиримидина, соединения формулы (F), в виде белого твердого вещества.
В. Аналогичным образом получали следующие соединения формулы (F):
2-метилсульфонил-4-(бензил)амино-5-нитро-6-(2-метокси-5-цианофенокси)пиримидин;
2-метилсульфонил-4-(бензил)амино-5-нитро-6-(2-этокси-5-цианофенокси)пиримидин;
2-метилсульфонил-4-(бензил)амино-5-нитро-6-(3-метокси-5-цианофенокси)пиримидин;
2-метилсульфонил-4-(бензил)амино-5-нитро-6-(3-этокси-5-цианофенокси)пиримидин;
2-метилсульфонил-4-(бензил)амина-5-нитро-6-(2-фенокси-5-цианофенокси)пиримидин;
2-метилсульфонил-4-(бензил)амино-5-нитро-6-(3-фенокси-5-цианофенокси)пиримидин;
2-метилсульфонил-4-(бензил)амино-5-нитро-6-(2-хлор-5-цианофенокси)пиримидин;
2-метилсульфонил-4-(бензил)амино-5-нитро-6-(3-бром-5-цианофенокси)пиримидин;
2-метилсульфонил-4-(бензил)амино-5-нитро-6-(2-метил-5-цианофенокси)пиримидин;
2-метилсульфонил-4-(бензил)амино-5-нитро-6-(3-метил-4-цианофенокси)пиримидин;
2-метилсульфонил-4-(бензил)амино-5-нитро-6-(2-нитро-5-цианофенокси)пиримидин;
2-метилсульфонил-4-(бензил)амино-5-нитро-6-(3-нитро-4-цианофенокси)пиримидин;
2-метилсульфонил-4-(бензил)амино-5-нитро-6-(2-карбокси-5-цианофенокси)пиримидин;
2-метилсульфонил-4-(бензил)амино-5-нитро-6-(3-карбокси-4-цианофенокси)пиримидин;
2-метилсульфонил-4-(бензил)амино-5-нитро-6-(2-трет-бутоксикарбонил-5-цианофенокси)пиримидин;
2-метилсульфонил-4-(бензил)амино-5-нитро-6-(3-трет-бутоксикарбонил-4-цианофенокси)пиримидин;
2-метилсульфонил-4-(бензил)амино-5-нитро-6-(2-аминокарбонил-5-цианофенокси)пиримидин;
2-метилсульфонил-4-(бензил)амино-5-нитро-6-(3-аминокарбонил-4-цианофенокси)пиримидин;
2-метилсульфонил-4-(бензил)амино-5-нитро-6-(2-диметиламино-5-цианофенокси)пиримидин;
2-метилсульфонил-4-(бензил)амино-5-нитро-6-(3-диметиламино-4-цианофенокси)пиримидин;
2-метилсульфонил-4-амино-5-нитро-6-(2-метокси-5-цианофенокси)пиримидин;
2-метилсульфонил-4-амино-5-нитро-6-(2-этокси-5-цианофенокси)пиримидин;
2-метилсульфонил-4-амино-5-нитро-6-(3-метокси-5-цианофенокси)пиримидин;
2-метилсульфонил-4-амино-5-нитро-6-(3-этокси-5-цианофенокси)пиримидин;
2-метилсульфонил-4-амино-5-нитро-6-(2-фенокси-5-цианофенокси)пиримидин;
2-метилсульфонил-4-амино-5-нитро-6-(3-фенокси-5-цианофенокси)пиримидин;
2-метилсульфонил-4-амино-5-нитро-6-(2-хлор-5-цианофенокси)пиримидин;
2-метилсульфонил-4-амино-5-нитро-6-(3-бром-5-цианофенокси)пиримидин;
2-метилсульфонил-4-амино-5-нитро-6-(2-метил-5-цианофенокси)пиримидин;
2-метилсульфонил-4-амино-5-нитро-6-(3-метил-4-цианофенокси)пиримидин;
2-метилсульфонил-4-амино-5-нитро-6-(2-нитро-5-цианофенокси)пиримидин;
2-метилсульфонил-4-амино-5-нитро-6-(3-нитро-4-цианофенокси)пиримидин;
2-метилсульфонил-4-амино-5-нитро-6-(2-карбокси-5-цианофенокси)пиримидин;
2-метилсульфонил-4-амино-5-нитро-6-(3-карбокси-4-цианофенокси)пиримидин;
2-метилсульфонил-4-амино-5-нитро-6-(2-трет-бутоксикарбонил-5-цианофенокси)пиримидин;
2-метилсульфонил-4-амино-5-нитро-6-(3-трет-бутоксикарбонил-4-цианофенокси)пиримидин;
2-метилсульфонил-4-амино-5-нитро-6-(2-аминокарбонил-5-цианофенокси)пиримидин;
2-метилсульфонил-4-амино-5-нитро-6-(3-аминокарбонил-4-цианофенокси)пиримидин;
2-метилсульфонил-4-амино-5-нитро-6-(2-диметиламино-5-цианофенокси)пиримидин и
2-метилсульфонил-4-амино-5-нитро-6-(3-диметиламино-4-цианофенокси)пиримидин.
С. Аналогичным образом 2-метилтио-4-бензиламино-5-нитро-6-(3-диметиламинокарбонилфенокси)пиримидин, соединение формулы (N), окисляли с получением 2-метилсульфонил-4-бензиламино-5-нитро-6-(3-диметиламинокарбонилфенокси)пиримидина, соединения формулы (О).
D. Аналогичным образом получали следующие соединения формулы (О):
2-метилсульфонил-4-бензиламино-5-нитро-6-(3-(2-(диметиламинокарбонил)этил)фенокси)пиримидин;
2-метилсульфонил-4-бензиламино-5-нитро-6-(3-(2-(диметиламинокарбонил)этил)-5-метоксифенокси)пиримидин;
2-метилсульфонил-4-бензиламино-5-нитро-6-(3-(2-(диметиламинокарбонил)этил)-5-хлорфенокси)пиримидин;
2-метилсульфонил-4-бензиламино-5-нитро-6-(3-хлор-5-метоксифенокси)пиримидин;
2-метилсульфонил-4-бензиламино-5-нитро-6-(3-трифторметил-5-(диметиламинокарбонил)феноксипиримидин;
2-метилсульфонил-4-бензиламино-5-нитро-6-(3-гуанидинофенокси)пиримидин;
2-метилсульфонил-4-бензиламино-5-нитро-6-(3-уреидофенокси)пиримидин;
2-метилсульфонил-4-бензиламино-5-нитро-6-(3-нитрофенокси)пиримидин;
2-метилсульфонил-4-бензиламино-5-нитро-6-(3-гуанидино-5-метилфенокси)пиримидин;
2-метилсульфонил-4-бензиламино-5-нитро-6-(3-уреидо-5-метилфенокси)пиримидин и
2-метилсульфонил-4-бензиламино-5-нитро-6-(3-нитро-5-аминофенокси)пиримидин.
Препаративный пример 4
Соединения формул (Н) и (М).
А. К 2-метилсульфонил-4-бензиламино-5-нитро-6-(2-бензилокси-5-цианофенокси)пиримидину, соединению формулы (F) (0.69 г, 1.38 ммоля), в 15 мл ацетонитрила при 0oС добавляли карбонат цезия (0.58 г, 1.80 ммоля) с последующим добавлением 3-(диметиламинокарбонил)фенола (0.20 г, 1.24 ммоля) и реакционную смесь перемешивали в течение 16 часов. Летучие вещества выпаривали, а остаток подвергали хроматографической очистке на силикагеле (СН2Сl2/этилацетат, 7: 2) с получением 0.29 г 2-(3-диметиламинокарбонилфенокси)-4-бензиламино-5-нитро-6-(2-бензилокси-5-циано-фенокси) пиримидина, соединения формулы (Н).
В. Аналогичным образом, получали следующие соединения формулы (Н):
2-(3-метилфенокси)-4-(бензил)амино-5-нитро-6-(2-метокси-5-цианофенокси)пиримидин;
2-(3-хлор-5-метоксифенокси)-4-(бензил)амино-5-нитро-6-(2-этокси-5-цианофенокси)пиримидин;
2-(4-трифторметилфенокси)-4-(бензил)амино-5-нитро-6-(3-метокси-5-цианофенокси)пиримидин;
2-(3,5-динитрофенокси)-4-(бензил)амино-5-нитро-6-(3-этокси-5-цианофенокси)пиримидин;
2-(3-гуанидино-5-метилфенокси)-4-(бензил)амино-5-нитро-6-(2-фенокси-5-цианофенокси)пиримидин;
2-(3-уреидофенокси)-4-(бензил)амино-5-нитро-6-(3-фенокси-5-цианофенокси)пиримидин;
2-(3-(2-хлорэтил)-5-метилфенокси)-4-(бензил)амино-5-нитро-6-(2-хлор-5-цианофенокси)пиримидин;
2-(3-диметиламинокарбонилфенокси)-4-(бензил)амино-5-нитро-6-(3-бром-5-цианофенокси)пиримидин;
2-(4-этоксикарбонилфенокси)-4-(бензил)амино-5-нитро-6-(2-метил-5-цианофенокси)пиримидин;
2-(3-метилимидазол-2-ил)фенокси)-4-(бензил)амино-5-нитро-6-(2-метил-5-цианофенокси)пиримидин;
2-(3-диметиламинофенокси)-4-(бензил)амино-5-нитро-6-(3-метил-4-цианофенокси)пиримидин;
2-(3-(1-метилимидазолин-2-ил)фенокси-4-(бензил)амино-5-нитро-6-(2-нитро-5-цианофенокси)пиримидин;
2-(3-трет-бутоксикарбонилфенокси)-4-(бензил)амино-5-нитро-6-(3-нитро-4-цианофенокси)пиримидин;
2-(3-(1-метилимидазолин-2-ил)фенокси-4-(бензил)амино-5-нитро-6-(2-карбокси-4-цианофенокси)пиримидин;
2-(3-(1-метилимидазолин-2-ил)фенокси-4-(бензил)амино-5-нитро-6-(3-карбокси-4-цианофенокси)пиримидин;
2-(3-(1-метилимидазолин-2-ил)фенокси-4-(бензил)амино-5-нитро-6-(2-трет-бутоксикарбонил-5-цианофенокси)пиримидин;
2-(3-(1-метилимидазолин-2-ил)фенокси-4-(бензил)амино-5-нитро-6-(3-трет-бутоксикарбонил-4-цианофенокси)пиримидин;
2-(3-(1-метилимидазолин-2-ил)фенокси-4-(бензил)амино-5-нитро-6-(2-аминокарбонил-5-цианофенокси)пиримидин;
2-(3-(1-метилимидазолин-2-ил)фенокси-4-(бензил)амино-5-нитро-6-(3-аминокарбонил-4-цианофенокси)пиримидин;
2-(3-(1-метилимидазолин-2-ил)фенокси-4-(бензил)амино-5-нитро-6-(2-диметиламино-5-цианофенокси)пиримидин;
2-(3-(1-метилимидазолин-2-ил)фенокси-4-(бензил)амино-5-нитро-6-(3-диметиламино-4-цианофенокси)пиримидин;
2-(3-(1-метилимидазолин-2-ил)фенокси-4-амино-5-нитро-6-(2-метокси-5-цианофенокси)пиримидин;
2-(3-(1-метилимидазолин-2-ил)фенокси-4-амино-5-нитро-6-(2-этокси-5-цианофенокси)пиримидин;
2-(3-(1-метилимидазолин-2-ил)фенокси-4-амино-5-нитро-6-(3-метокси-5-цианофенокси)пиримидин;
2-(3-(1-метилимидазолин-2-ил)фенокси-4-амино-5-нитро-6-(3-этокси-5-цианофенокси)пиримидин;
2-(3-(1-метилимидазолин-2-ил)фенокси-4-амино-5-нитро-6-(2-фенокси-5-цианофенокси)пиримидин;
2-(3-диметиламинокарбонилфенокси)-4-амино-5-нитро-6-(3-фенокси-5-цианофенокси)пиримидин;
2-(3-диметиламинокарбонилфенокси)-4-амино-5-нитро-6-(2-хлор-5-цианофенокси)пиримидин;
2-(3-диметиламинокарбонилфенокси)-4-амино-5-нитро-6-(3-бром-5-цианофенокси)пиримидин;
2-(3-диметиламинокарбонилфенокси)-4-амино-5-нитро-6-(2-метил-5-цианофенокси)пиримидин;
2-(3-диметиламинокарбонилфенокси)-4-амино-5-нитро-6-(3-метил-4-цианофенокси)пиримидин;
2-(3-диметиламинокарбонилфенокси)-4-амино-5-нитро-6-(2-нитро-5-цианофенокси)пиримидин;
2-(3-диметиламинокарбонилфенокси)-4-амино-5-нитро-6-(3-нитро-5-цианофенокси)пиримидин;
2-(3-гуанидинофенокси)-4-амино-5-нитро-6-(2-карбокси-5-цианофенокси)пиримидин;
2-(3-гуанидинофенокси)-4-амино-5-нитро-6-(3-карбокси-4-цианофенокси)пиримидин;
2-(3-гуанидинофенокси)-4-амино-5-нитро-6-(2-трет-бутоксикарбонил-5-цианофенокси)пиримидин;
2-(3-гуанидинофенокси)-4-амино-5-нитро-6-(3-трет-бутоксикарбонил-4-цианофенокси)пиримидин;
2-(3-гуанидинофенокси)-4-амино-5-нитро-6-(2-аминокарбонил-5-цианофенокси)пиримидин;
2-(3-гуанидинофенокси)-4-амино-5-нитро-6-(3-аминокарбонил-4-цианофенокси)пиримидин;
2-(3-гуанидинофенокси)-4-амино-5-нитро-6-(2-диметиламино-5-цианофенокси)пиримидин и
2-(3-гуанидинофенокси)-4-амино-5-нитро-6-(3-диметиламино-4-цианофенокси)пиримидин.
С. Аналогичным образом 2-метилтио-5-нитро-4,6-дихлорпиримидин обрабатывали 3-(диметиламинокарбонил)фенолом в присутствии карбоната цезия с получением 2-метилтио-5-нитро-4-хлор-6-(3-диметиламинокарбонилфенокси)пиримидина, соединения формулы (М).
D. Аналогичным методом получали следующие соединения формулы (М):
2-метилтио-4-хлор-5-нитро-6-(3-(2-диметиламинокарбонил)этил)фенокси)пиримидин;
2-метилтио-4-хлор-5-нитро-6-(3-(2-диметиламинокарбонил)этил)-5-метоксифенокси)пиримидин;
2-метилтио-4-хлор-5-нитро-6-(3-(2-диметиламинокарбонил)этил)-5-хлорфенокси)пиримидин;
2-метилтио-4-хлор-5-нитро-6-(3-хлор-5-метоксифенокси)пиримидин;
2-метилтио-4-хлор-5-нитро-6-(3-трифторметил-5-(диметиламинокарбонил)феноксипиримидин;
2-метилтио-4-хлор-5-нитро-6-(3-гуанидинофенокси)пиримидин;
2-метилтио-4-хлор-5-нитро-6-(3-уреидофенокси)пиримидин;
2-метилтио-4-хлор-5-нитро-6-(3-нитрофенокси)пиримидин;
2-метилтио-4-хлор-5-нитро-6-(3-гуанидино-5-метилфенокси)пиримидин;
2-метилтио-4-хлор-5-нитро-6-(3-уреидо-5-метилфенокси)пиримидин и
2-метилтио-4-хлор-5-нитро-6-(3-нитро-5-аминофенокси)пиримидин.
Препаративный пример 5
Соединения формулы (J) и формулы (Q).
А. 2-(3-Диметиламинокарбонилфенокси)-4-бензиламино-5-нитро-6-(2-бензилокси-5-цианофенокси)пиримидин, соединение формулы (Н) (0.29 г, 0.47 ммоля), и 0.1 г гранулированного цинка смешивали с 10 мл THF и 1.0 мл 10% водной НСl. Реакционную смесь нагревали при 80oС в течение 90 минут. Летучие вещества выпаривали. Добавляли насыщенный водный раствор NaHCO3 и раствор экстрагировали этилацетатом (300 мл). Органический слой сушили (Na2SO4) и выпаривали с образованием 0.27 г 2-(3-диметиламинокарбонилфенокси)-4-бензиламино-5-амино-6-(2-бензилокси-5-цианофенокси)пиримидина, соединения формулы (J).
В. Аналогичным методом получали следующие соединения формулы (J):
2-(3-метилфенокси)-4-(бензил)амино-5-амино-6-(2-метокси-5-цианофенокси)пиримидин;
2-(3-хлор-5-метоксифенокси)-4-(бензил)амино-5-амино-6-(2-этокси-5-цианофенокси)пиримидин;
2-(4-трифторметилфенокси)-4-(бензил)амино-5-амино-6-(3-метокси-5-цианофенокси)пиримидин;
2-(3,5-диаминофенокси)-4-(бензил)амино-5-амино-6-(3-этокси-5-цианофенокси)пиримидин;
2-(3-гуанидино-5-метилфенокси)-4-(бензил)амино-5-амино-6-(2-фенокси-5-цианофенокси)пиримидин;
2-(3-уреидофенокси)-4-(бензил)амино-5-амино-6-(3-фенокси-5-цианофенокси)пиримидин;
2-(3-(2-хлорэтил)-5-метилфенокси)-4-(бензил)амино-5-амино-6-(2-хлор-5-цианофенокси)пиримидин;
2-(3-диметиламинокарбонилфенокси)-4-(бензил)амино-5-амино-6-(3-бром-5-цианофенокси)пиримидин;
2-(4-этоксикарбонилфенокси)-4-(бензил)амино-5-амино-6-(2-метил-5-цианофенокси)пиримидин;
2-(3-(1-метилимидазол-2-ил)фенокси)-4-(бензил)амино-5-амино-6-(2-метил-5-цианофенокси)пиримидин;
2-(3-диметиламинофенокси)-4-(бензил)амино-5-амино-6-(3-метил-4-цианофенокси)пиримидин;
2-(3-(1-метилимидазолин-2-ил)фенокси-4-(бензил)амино-5-амино-6-(2-амино-4-цианофенокси)пиримидин;
2-(3-трет-бутоксикарбонилфенокси)-4-(бензил)амино-5-амино-6-(3-амино-4-цианофенокси)пиримидин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-4-(бензил)амино-5-амино-6-(2-карбокси-5-цианофенокси)пиримидин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-4-(бензил)амино-5-амино-6-(3-карбокси-4-цианофенокси)пиримидин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-4-(бензил)амино-5-амино-6-(2-трет-бутоксикарбонил-5-цианофенокси)пиримидин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-4-(бензил)амино-5-амино-6-(3-трет-бутоксикарбонил-4-цианофенокси)пиримидин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-4-(бензил)амино-5-амино-6-(2-аминокарбонил-5-цианофенокси)пиримидин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-4-(бензил)амино-5-амино-6-(3-аминокарбонил-4-цианофенокси)пиримидин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-4-(бензил)амино-5-амино-6-(2-диметиламино-5-цианофенокси)пиримидин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-4-(бензил)амино-5-амино-6-(3-диметиламино-4-цианофенокси)пиримидин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-4-(бензил)амино-5-амино-6-(2-диметиламино-5-цианофенокси)пиримидин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-4-(бензил)амино-5-амино-6-(3-диметиламино-4-цианофенокси)пиримидин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-4,5-диамино-6-(2-метокси-5-цианофенокси)пиримидин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-4,5-диамино-6-(2-этокси-5-цианофенокси)пиримидин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-4,5-диамино-6-(3-метокси-5-цианофенокси)пиримидин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-4,5-диамино-6-(3-этокси-5-цианофенокси)пиримидин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-4,5-диамино-6-(2-фенокси-5-цианофенокси)пиримидин;
2-(3-диметиламинокарбонилфенокси)-4,5-диамино-6-(3-фенокси-5-цианофенокси)пиримидин;
2-(3-диметиламинокарбонилфенокси)-4,5-диамино-6-(2-хлор-5-цианофенокси)пиримидин;
2-(3-диметиламинокарбонилфенокси)-4,5-диамино-6-(3-бром-5-цианофенокси)пиримидин;
2-(3-диметиламинокарбонилфенокси)-4,5-диамино-6-(2-метил-5-цианофенокси)пиримидин;
2-(3-диметиламинокарбонилфенокси)-4,5-диамино-6-(3-метил-4-цианофенокси)пиримидин;
2-(3-диметиламинокарбонилфенокси)-4,5-диамино-6-(2-амино-5-цианофенокси)пиримидин;
2-(3-диметиламинокарбонилфенокси)-4,5-диамино-6-(3-амино-4-цианофенокси)пиримидин;
2-(3-гуанидинофенокси)-4,5-диамино-6-(2-карбокси-5-цианофенокси)пиримидин;
2-(3-гуанидинофенокси)-4,5-диамино-6-(3-карбокси-4-цианофенокси)пиримидин;
2-(3-гуанидинофенокси)-4,5-диамино-6-(2-трет-бутоксикарбонил-5-цианофенокси)пиримидин;
2-(3-гуанидинофенокси)-4,5-диамино-6-(3-трет-бутоксикарбонил-4-цианофенокси)пиримидин;
2-(3-гуанидинофенокси)-4,5-диамино-6-(2-аминокарбонил-5-цианофенокси)пиримидин;
2-(3-гуанидинофенокси)-4,5-диамино-6-(3-аминокарбонил-4-цианофенокси)пиримидин;
2-(3-гуанидинофенокси)-4,5-диамино-6-(2-диметиламино-5-цианофенокси)пиримидин и
2-(3-гуанидинофенокси)-4,5-диамино-6-(3-диметиламино-4-цианофенокси)пиримидин.
С. Аналогичным образом 2-(2-бензилокси-5-цианофенокси)-4-бензиламино-5-нитро-6-(3-диметиламинокарбонил)феноксипиримидин (1.2 г, 1.95 ммоля), соединение формулы (Р), восстанавливали с получением 130 г 2-(2-бензилокси-5-цианофенокси)-4-бензиламино-5-амино-6-(3-диметиламинокарбонил)феноксипиримидина, соединения формулы (Q).
D. Аналогичным методом получали следующие соединения формулы (Q):
2-(2-бензилокси-5-цианофенокси)-4-(бензил)амино-5-амино-6-(3-диметиламинокарбонилфенокси)пиримидин;
2-(2-метокси-5-цианофенокси)-4-(бензил)амино-5-амино-6-(3-диметиламинокарбонилфенокси)пиримидин;
2-(2-этокси-5-цианофенокси)-4-(бензил)амино-5-амино-6-(3-диметиламинокарбонилфенокси)пиримидин;
2-(2-фенокси-5-цианофенокси)-4-(бензил)амино-5-амино-6-(3-диметиламинокарбонилфенокси)пиримидин;
2-(2-хлор-5-цианофенокси)-4-(бензил)амино-5-амино-6-(3-диметиламинокарбонилфенокси)пиримидин;
2-(2-метил-5-цианофенокси)-4-(бензил)амино-5-амино-6-(3-диметиламинокарбонилфенокси)пиримидин;
2-(2-трет-бутил-5-цианофенокси)-4-(бензил)амино-5-амино-6-(3-диметиламинокарбонилфенокси)пиримидин;
2-(2-амино-5-цианофенокси)-4-(бензил)амино-5-амино-6-(3-диметиламинокарбонилфенокси)пиримидин;
2-(2-карбокси-5-цианофенокси)-4-(бензил)амино-5-амино-6-(3-диметиламинокарбонилфенокси)пиримидин;
2-(2-бензилоксикарбонил-5-цианофенокси)-4-(бензил)амино-5-амино-6-(3-диметиламинокарбонилфенокси)пиримидин;
2-(2-диэтиламинокарбонил-5-цианофенокси)-4-(бензил)амино-5-амино-6-(3-диметиламинокарбонилфенокси)пиримидин;
2-(2-амино-5-цианофенокси)-4-(бензил)амино-5-амино-6-(3-диметиламинокарбонилфенокси)пиримидин;
2-(2-бензилокси-5-цианофенокси)-4-(бензил)амино-5-амино-6-(3-(1-метилимидазолин-2-ил)фенокси)пиримидин;
2-(2-метокси-5-цианофенокси)-4-(бензил)амино-5-амино-6-(3-(2-(трет-бутоксикарбонил)этил)фенокси)пиримидин;
2-(2-этокси-5-цианофенокси)-4-(бензил)амино-5-амино-6-(3-трет-бутоксикарбонилфенокси)пиримидин;
2-(2-фенокси-5-цианофенокси)-4-(бензил)амино-5-амино-6-(3-карбоксифенокси)пиримидин;
2-(2-хлор-5-цианофенокси)-4-(бензил)амино-5-амино-6-(3-(2-амино-этил)фенокси)пиримидин;
2-(2-метил-5-цианофенокси)-4-(бензил)амино-5-амино-6-(3-(бензилокси)фенокси)пиримидин;
2-(2-трет-бутил-5-цианофенокси)-4-(бензил)амино-5-амино-6-(3-(этоксифенокси)пиримидин;
2-(2-амино-5-цианофенокси)-4-(бензил)амино-5-амино-6-(3-гуанидинофенокси)пиримидин;
2-(2-карбокси-5-цианофенокси)-4-(бензил)амино-5-амино-6-(3-уреидофенокси)пиримидин;
2-(2-бензилоксикарбонил-5-цианофенокси)-4-(бензил)амино-5-амино-6-(3-аминофенокси)пиримидин;
2-(2-диэтиламинокарбонил-5-цианофенокси)-4-(бензил)амино-5-амино-6-(3-аминофенокси)пиримидин и
2-(2-амино-5-цианофенокси)-4-(бензил)амино-5-амино-6-(3-трифторметоксифенокси)пиримидин.
Препаративный пример 6
Соединения формул (L) и (R).
А. 2-(3-Диметиламинокарбонилфенокси)-4-(бензил)амино-5-амино-6-(2-бензилокси-5-цианофенокси)пиримидин, соединение формулы (J) (0.26 г, 0.44 ммоля), обрабатывали гидрохлоридом этилимидата (0.17 г, 1.3 ммоля) в среде THF/этанол при 80oС в течение 6 часов и затем концентрировали до образования масла. Остаток нагревали на песчаной бане в вакууме, при 170oС в течение 2 часов, охлаждали и фильтровали через слой оксида кремния, проводя элюирование 5% метанолом в хлористом метилене. В результате выпаривания летучих веществ получали 0.20 г 2-(3-диметиламинокарбонилфенокси)-6-(2-бензилокси-5-цианофенокси)-8-метил-9-бензилпурина, соединения формулы (L).
В. Аналогичным образом получали следующие соединения формулы (L):
2-(3-метилфенокси)-6-(2-метокси-5-цианофенокси)-8-метил-9-бензилпурин;
2-(3-хлор-5-метилфенокси)-6-(2-этокси-5-цианофенокси)-8-метил-9-бензилпурин;
2-(4-трифторметилфенокси)-6-(3-метокси-5-цианофенокси)-8-метил-9-бензилпурин;
2-(3,5-диаминофенокси)-6-(3-этокси-5-цианофенокси)-8-метил-9-бензилпурин;
2-(3-гуанидино-5-метилфенокси)-6-(2-фенокси-5-цианофенокси)-8-метил-9-бензилпурин;
2-(3-уреидофенокси)-6-(3-фенокси-5-цианофенокси)-8-метил-9-бензилпурин;
2-(3-(2-хлорэтил)-5-метилфенокси)-6-(2-хлор-5-цианофенокси)-8-метил-9-бензилпурин;
2-(3-диметиламинокарбонилфенокси)-6-(3-бром-5-цианофенокси)-8-метил-9-бензилпурин;
2-(4-этоксикарбонилфенокси)-6-(2-метил-5-цианофенокси)-8-метил-9-бензилпурин;
2-(3-(1-метилимидазол-2-ил)фенокси)-6-(2-метил-5-цианофенокси)-8-метил-9-бензилпурин;
2-(3-диметиламинофенокси)-6-(3-метил-4-цианофенокси)-8-метил-9-бензилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(2-амино-5-цианофенокси)-8-метил-9-бензилпурин;
2-(3-трет-бутоксикарбонилфенокси)-6-(3-амино-4-цианофенокси)-8-метил-9-бензилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(2-карбокси-5-цианофенокси)-8-метил-9-бензилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(3-карбокси-4-цианофенокси)-8-метил-9-бензилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(2-трет-бутоксикарбонил-5-цианофенокси)-8-метил-9-бензилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(3-трет-бутоксикарбонил-4-цианофенокси)-8-метил-9-бензилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(2-аминокарбонил-5-цианофенокси)-8-метил-9-бензилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(3-аминокарбонил-4-цианофенокси)-8-метил-9-бензилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(2-диметиламино-5-цианофенокси)-8-метил-9-бензилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(3-диметиламино-4-цианофенокси)-8-метил-9-бензилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(2-метокси-5-цианофенокси)-8-метилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(2-этокси-5-цианофенокси)-8-метилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(3-метокси-5-цианофенокси)-8-метилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(3-этокси-5-цианофенокси)-8-метилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(2-фенокси-5-цианофенокси)-8-метилпурин;
2-(3-диметиламинокарбонилфенокси)-6-(3-фенокси-5-цианофенокси)-8-метилпурин;
2-(3-диметиламинокарбонилфенокси)-6-(2-хлор-5-цианофенокси)-8-метилпурин;
2-(3-диметиламинокарбонилфенокси)-6-(3-бром-5-цианофенокси)-8-метилпурин;
2-(3-диметиламинокарбонилфенокси)-6-(2-метил-5-цианофенокси)-8-метилпурин;
2-(3-диметиламинокарбонил)фенокси)-6-(3-метил-4-цианофенокси)-8-метилпурин;
2-(3-диметиламинокарбонил)фенокси)-6-(2-амино-5-цианофенокси)-8-метилпурин;
2-(3-диметиламинокарбонил)фенокси)-6-(3-амино-4-цианофенокси)-8-метилпурин;
2-(3-гуанидинфенокси)-6-(2-карбокси-5-цианофенокси)-8-метилпурин;
2-(3-гуанидинфенокси)-6-(3-карбокси-4-цианофенокси)-8-метилпурин;
2-(3-гуанидинфенокси)-6-(2-трет-бутоксикарбонил-5-цианофенокси)-8-метилпурин;
2-(3-гуанидинфенокси)-6-(3-трет-бутоксикарбонил-4-цианофенокси)-8-метилпурин;
2-(3-гуанидинфенокси)-6-(2-аминокарбонил-5-цианофенокси)-8-метилпурин;
2-(3-гуанидинфенокси)-6-(3-аминокарбонил-4-цианофенокси)-8-метилпурин;
2-(3-гуанидинфенокси)-6-(2-диметиламино-5-цианофенокси)-8-метилпурин;
2-(3-гуанидинфенокси)-6-(3-диметиламино-4-цианофенокси)-8-метилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(2-метокси-5-цианофенокси)-8-этилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(2-этокси-5-цианофенокси)-8-этилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(3-метокси-5-цианофенокси)-8-этилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(3-этокси-5-цианофенокси)-8-этилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(2-фенокси-5-цианофенокси)-8-этилпурин;
2-(3-диметиламинокарбонилфенокси)-6-(3-фенокси-5-цианофенокси)-8-этилпурин;
2-(3-диметиламинокарбонилфенокси)-6-(2-хлор-5-цианофенокси)-8-бензилпурин;
2-(3-диметиламинокарбонилфенокси)-6-(3-бром-5-цианофенокси)-8-бензилпурин;
2-(3-диметиламинокарбонилфенокси)-6-(2-метил-5-цианофенокси)-8-бензилпурин;
2-(3-диметиламинокарбонилфенокси)-6-(2-метил-5-цианофенокси)-8-фенилпурин;
2-(3-диметиламинокарбонилфенокси)-6-(3-метил-4-цианофенокси)-8-фенилпурин;
2-(3-диметиламинокарбонилфенокси)-6-(2-амино-5-цианофенокси)-8-фенилпурин;
2-(3-диметиламинокарбонилфенокси)-6-(3-амино-4-цианофенокси)-8-фенилпурин;
2-(3-гуанидинофенокси)-6-(2-карбокси-5-цианофенокси)-8-трет-бутилпурин;
2-(3-гуанидинофенокси)-6-(3-карбокси-4-цианофенокси)-8-трет-бутилпурин;
2-(3-гуанидинофенокси)-6-(2-трет-бутоксикарбонил-5-цианофенокси)-8-трет-бутилпурин;
2-(3-гуанидинофенокси)-6-(3-трет-бутоксикарбонил-4-цианофенокси)-8-трифторметилпурин;
2-(3-гуанидинофенокси)-6-(2-аминокарбонил-5-цианофенокси)-8-трифторметилпурин;
2-(3-гуанидинофенокси)-6-(3-аминокарбонил-4-цианофенокси)-8-этилпурин;
2-(3-гуанидинофенокси)-6-(2-диметиламино-5-цианофенокси)-8-этилпурин.
С. Аналогичным образом в результате обработки 2-(2-бензилокси-5-цианофенокси)-4-(бензил)амино-5-амино-6-(3-диметиламинокарбонил)феноксипиримидина (1.14 г, 1.94 ммоля) гидрохлоридом этилимидата (0.31 г, 2.53 ммоля) получали 0.65 г 2-(2-бензилокси-5-цианофенокси)-6-(3-диметиламинокарбонил)фенокси-8-метил-9-бензилпурин, соединение формулы (R).
D. Аналогичным образом получали следующие соединения формулы (R):
2-(2-бензилокси-5-цианофенокси)-6-(3-диметиламинокарбонилфенокси-8-метил-9-бензилпурин;
2-(2-метокси-5-цианофенокси)-6-(3-диметиламинокарбонилфенокси-8-метил-9-бензилпурин;
2-(2-этокси-5-цианофенокси)-6-(3-диметиламинокарбонилфенокси-8-метил-9-бензилпурин;
2-(2-фенокси-5-цианофенокси)-6-(3-диметиламинокарбонилфенокси-8-метил-9-бензилпурин;
2-(2-хлор-5-цианофенокси)-6-(3-диметиламинокарбонилфенокси-8-метил-9-бензилпурин;
2-(2-метил-5-цианофенокси)-6-(3-диметиламинокарбонилфенокси-8-метил-9-бензилпурин;
2-(2-трет-бутил-5-цианофенокси)-6-(3-диметиламинокарбонилфенокси-8-метил-9-бензилпурин;
2-(2-амино-5-цианофенокси)-6-(3-диметиламинокарбонилфенокси-8-метил-9-бензилпурин;
2-(2-карбокси-5-цианофенокси)-6-(3-диметиламинокарбонилфенокси-8-метил-9-бензилпурин;
2-(2-бензилоксикарбонил-5-цианофенокси)-6-(3-диметиламинокарбонилфенокси-8-метил-9-бензилпурин;
2-(2-диэтиламинокарбонил-5-цианофенокси)-6-(3-диметиламинокарбонилфенокси-8-метил-9-бензилпурин;
2-(2-амино-5-цианофенокси)-6-(3-диметиламинокарбонилфенокси-8-метил-9-бензилпурин;
2-(2-бензилокси-5-цианофенокси)-6-(3-(1-метилимидазолин-2-ил)фенокси-8-метил-9-бензилпурин;
2-(2-метокси-5-цианофенокси)-6-(3-(2-трет-бутоксикарбонил)этил)фенокси-8-метил-9-бензилпурин;
2-(2-этокси-5-цианофенокси)-6-(3-трет-бутоксикарбонилфенокси-8-метил-9-бензилпурин;
2-(2-фенокси-5-цианофенокси)-6-(3-карбоксифенокси-8-метил-9-бензилпурин;
2-(2-хлор-5-цианофенокси)-6-(3-(2-аминоэтил)фенокси-8-метил-9-бензилпурин;
2-(2-метил-5-цианофенокси)-6-(3-(бензилокси)фенокси-8-метил-9-бензилпурин;
2-(2-трет-бутил-5-цианофенокси)-6-(3-этоксифенокси-8-метил-9-бензилпурин;
2-(2-амино-5-цианофенокси)-6-(3-гуанидинофенокси-8-метил-9-бензилпурин;
2-(2-карбокси-5-цианофенокси)-6-(3-уреидофенокси-8-метил-9-бензилпурин;
2-(2-бензилоксикарбонил-5-цианофенокси)-6-(3-аминофенокси-8-метил-9-бензилпурин;
2-(2-диэтиламинокарбонил-5-цианофенокси)-6-(3-аминофенокси-8-метил-9-бензилпурин;
2-(2-амино-5-цианофенокси)-6-(3-трифторметоксифенокси-8-метил-9-бензилпурин;
2-(2-бензилокси-5-цианофенокси)-6-(3-диметиламинокарбонилфенокси-8-метилпурин;
2-(2-метокси-5-цианофенокси)-6-(3-диметиламинокарбонилфенокси-8-метилпурин;
2-(2-этокси-5-цианофенокси)-6-(3-диметиламинокарбонилфенокси-8-метилпурин;
2-(2-фенокси-5-цианофенокси)-6-(3-диметиламинокарбонилфенокси-8-метилпурин;
2-(2-хлор-5-цианофенокси)-6-(3-диметиламинокарбонилфенокси-8-метилпурин;
2-(2-метил-5-цианофенокси)-6-(3-диметиламинокарбонилфенокси-8-метилпурин;
2-(2-трет-бутил-5-цианофенокси)-6-(3-диметиламинокарбонилфенокси-8-метилпурин;
2-(2-амино-5-цианофенокси)-6-(3-диметиламинокарбонилфенокси-8-метилпурин;
2-(2-карбокси-5-цианофенокси)-6-(3-диметиламинокарбонилфенокси-8-метилпурин;
2-(2-бензилоксикарбонил-5-цианофенокси)-6-(3-диметиламинокарбонилфенокси-8-метилпурин;
2-(2-диэтиламинокарбонил-5-цианофенокси)-6-(3-диметиламинокарбонилфенокси-8-метилпурин;
2-(2-амино-5-цианофенокси)-6-(3-диметиламинокарбонилфенокси-8-метилпурин;
2-(2-бензилокси-5-цианофенокси)-6-(3-(1-метилимидазолин-2-ил)фенокси-8-метилпурин;
2-(2-метокси-5-цианофенокси)-6-(3-(2-трет-бутоксикарбонил)этил)фенокси-8-метилпурин;
2-(2-этокси-5-цианофенокси)-6-(3-трет-бутоксикарбонилфенокси-8-метилпурин;
2-(2-фенокси-5-цианофенокси)-6-(3-карбоксифенокси-8-метилпурин;
2-(2-хлор-5-цианофенокси)-6-(3-(2-аминоэтил)фенокси-8-метилпурин;
2-(2-метил-5-цианофенокси)-6-(3-(бензилокси)фенокси-8-метилпурин;
2-(2-трет-бутил-5-цианофенокси)-6-(3-этоксифенокси-8-метилпурин;
2-(2-амино-5-цианофенокси)-6-(3-гуанидинофенокси-8-метилпурин;
2-(2-карбокси-5-цианофенокси)-6-(3-уреидофенокси-8-метилпурин;
2-(2-бензилоксикарбонил-5-цианофенокси)-6-(3-аминофенокси-8-метилпурин;
2-(2-диэтиламинокарбонил-5-цианофенокси)-6-(3-аминофенокси-8-метилпурин;
2-(2-амино-5-цианофенокси)-6-(3-трифторметоксифенокси-8-этилпурин;
2-(2-метил-5-цианофенокси)-6-(3-диметиламинокарбонил-фенокси-8-этилпурин;
2-(2-трет-бутил-5-цианофенокси)-6-(3-диметиламинокарбонилфенокси-8-этилпурин;
2-(2-амино-5-цианофенокси)-6-(3-диметиламинокарбонилфенокси-8-этилпурин;
2-(2-карбокси-5-цианофенокси)-6-(3-диметиламинокарбонилфенокси-8-этилпурин;
2-(2-бензилоксикарбонил-5-цианофенокси)-6-(3-диметиламинокарбонилфенокси-8-этилпурин;
2-(2-диэтиламинокарбонил-5-цианофенокси)-6-(3-диметиламинокарбонилфенокси-8-этилпурин;
2-(2-амино-5-цианофенокси)-6-(3-диметиламинокарбонилфенокси-8-этил-9-этилпурин;
2-(2-бензилокси-5-цианофенокси)-6-(3-(1-метилимидазолин-2-ил)фенокси-8-этил-9-этилпурин;
2-(2-метокси-5-цианофенокси)-6-(3-(2-бутоксикарбонил)этил)фенокси-6-этил-9-этилпурин;
2-(2-этокси-5-цианофенокси)-6-(3-бутоксикарбонилфенокси-8-этил-9-этилпурин;
2-(2-фенокси-5-цианофенокси)-6-(3-карбоксифенокси-8-этил-9-этилпурин;
2-(2-хлор-5-цианофенокси)-6-(3-(2-аминоэтил)фенокси-8-этил-9-этилпурин;
2-(2-метил-5-цианофенокси)-6-(3-(бензилокси)фенокси-8-этил-9-этилпурин;
2-(2-трет-бутил-5-цианофенокси)-6-(3-этоксифенокси-8-этил-9-этилпурин;
2-(2-амино-5-цианофенокси)-6-(3-гуанидинофенокси-8-этил-9-этилпурин;
2-(2-карбокси-5-цианофенокси)-6-(3-уреидофенокси-8-этил-9-этилпурин;
2-(2-бензилоксикарбонил-5-цианофенокси)-6-(3-аминофенокси-8-этил-9-этилпурин;
2-(2-диэтиламинокарбонил-5-цианофенокси)-6-(3-аминофенокси-8-этил-9-этилпурин и
2-(2-амино-5-цианофенокси)-6-(3-трифторметоксифенокси-8-этил-9-этилпурин.
Пример 1
Соединения формул (I) и (II).
А. 6-(2-Бензилокси-5-цианофенокси)-2-(3-диметиламинокарбонил)фенокси-8-метил-9-бензилпурин (0.2 г, 0.33 ммоля) растворяли в 5.0 мл этанола в сосуде, работающем под давлением, при 0oС и раствор насыщали газообразной НС1. Сосуд герметично закрывали и реакционной смеси давали нагреваться до температуры окружающей среды в течение 16 часов. Затем реакционную смесь концентрировали до объема 20 мл и добавляли эфир. Полученный в результате осадок растворяли в 30 мл этанола, охлаждали до 0oС и через полученный раствор в течение 10 минут барботировали газообразный аммиак. Реакционную смесь герметично закрывали и нагревали в течение 2 часов при 60oС. Реакционной смеси давали охлаждаться, сосуд со смесью осторожно откупоривали и летучие соединения выпаривали с получением 0.152 г сырого продукта. В результате очистки методом препаративной ЖХВД получали 0.015 г 6-(2-гидрокси-5-амидинофенокси)-2-(3-диметиламинокарбонил)фенокси-8-метил-9-бензипурина, соединения формулы (II).
ЯМР-спектр (DMSO-d6): 9.10 (шир. с, 2), 8.80 (шир. с, 2), 7.80 (д, 1), 7.70 (д, 1), 7.10-7.50 (м, 10), 5.40 (с, 2), 3.00 (шир. с, 6), 2.70 (с, 3).
В. Аналогичным способом получали следующие соединения формулы (II):
2-(3-метилфенокси)-6-(2-метокси-5-амидинофенокси)-8-метил-9-бензилпурин;
2-(3-хлор-5-метоксифенокси)-6-(2-этокси-5-амидинофенокси)-8-метил-9-бензилпурин;
2-(4-трифторметилфенокси)-6-(3-метокси-5-амидинофенокси)-8-метил-9-бензилпурин;
2-(3,5-диаминофенокси)-6-(3-этокси-5-амидинофенокси)-8-метил-9-бензилпурин;
2-(3-гуанидино-5-метилфенокси)-6-(2-фенокси-5-амидинофенокси)-8-метил-9-бензилпурин;
2-(3-уреидофенокси)-6-(3-фенокси-5-амидинофенокси)-8-метил-9-бензилпурин;
2-(3-(2-хлорэтил)-5-метилфенокси)-6-(2-хлор-5-амидинофенокси)-8-метил-9-бензилпурин;
2-(3-диметиламинокарбонилфенокси)-6-(3-бром-5-амидинофенокси)-8-метил-9-бензилпурин;
2-(4-этоксикарбонилфенокси)-6-(2-метил-5-амидинофенокси)-8-метил-9-бензилпурин;
2-(3-(1-метилимидазол-2-ил)фенокси)-6-(2-метил-5-амидинофенокси)-8-метил-9-бензилпурин;
2-(3-диметиламинофенокси)-6-(3-метил-4-амидинофенокси)-8-метил-9-бензилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси-6-(2-амино-5-амидинофенокси)-8-метил-9-бензилпурин;
2-(3-трет-бутоксикарбонилфенокси)-6-(3-амино-4-амидинофенокси)-8-метил-9-бензилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(2-карбокси-5-амидинофенокси)-8-метил-9-бензилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(3-карбокси-4-амидинофенокси)-8-метил-9-бензилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(2-трет-бутоксикарбонил-5-амидинофенокси)-8-метил-9-бензилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(3-трет-бутоксикарбонил-4-амидинофенокси)-8-метил-9-бензилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(2-аминокарбонил-5-амидинофенокси)-8-метил-9-бензилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(3-аминокарбонил-4-амидинофенокси)-8-метил-9-бензилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(2-диметиламино-5-амидинофенокси)-8-метил-9-бензилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(3-диметиламино-4-амидинофенокси) -8-метил-9-бензилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(2-метокси-5-амидинофенокси)-8-метилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(2-этокси-5-амидинофенокси)-8-метилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(3-метокси-5-амидинофенокси)-8-метилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(3-этокси-5-амидинофенокси)-8-метилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(2-фенокси-5-амидинофенокси)-8-метилпурин;
2-(3-диметиламинокарбонилфенокси)-6-(3-фенокси-5-амидинофенокси)-8-метилпурин;
2-(3-диметиламинокарбонилфенокси)-6-(2-хлор-5-амидинофенокси)-8-метилпурин;
2-(3-диметиламинокарбонилфенокси)-6-(3-бром-5-амидинофенокси)-8-метилпурин;
2-(3-диметиламинокарбонилфенокси)-6-(2-метил-5-амидинофенокси)-8-метилпурин;
2-(3-диметиламинокарбонилфенокси)-6-(3-метил-4-амидинофенокси)-8-метилпурин;
2-(3-диметиламинокарбонилфенокси)-6-(2-амино-5-амидинофенокси)-8-метилпурин;
2-(3-диметиламинокарбонилфенокси)-6-(3-амино-4-амидинофенокси)-8-метилпурин;
2-(3-гуанидинофенокси)-6-(2-карбокси-5-амидинофенокси)8-метилпурин;
2-(3-гуанидинофенокси)-6-(3-карбокси-4-амидинофенокси)-8-метилпурин;
2-(3-гуанидинофенокси)-6-(2-трет-бутоксикарбонил-5-амидинофенокси)-8-метилпурин;
2-(3-гуанидинофенокси)-6-(3-трет-бутоксикарбонил-4-амидинофенокси)-8-метилпурин;
2-(3-гуанидинофенокси)-6-(2-аминокарбонил-5-амидинофенокси)-8-метилпурин;
2-(3-гуанидинофенокси)-6-(3-аминокарбонил-4-амидинофенокси)-8-метилпурин;
2-(3-гуанидинофенокси)-6-(2-диметиламино-5-амидинофенокси)-8-метилпурин;
2-(3-гуанидинофенокси)-6-(3-диметиламино-4-амидинофенокси)-8-метилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(2-метокси-5-амидинофенокси)-8-этилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(2-этокси-5-амидинофенокси)-8-этилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(3-метокси-5-амидинофенокси)-8-этилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(3-этокси-5-амидинофенокси)-8-этилпурин;
2-(3-(1-метилимидазолин-2-ил)фенокси)-6-(2-фенокси-5-амидинофенокси)-8-этилпурин;
2-(3-диметиламинокарбонилфенокси)-6-(3-фенокси-5-амидинофенокси)-8-этилпурин;
2-(3-диметиламинокарбонилфенокси)-6-(2-хлор-5-амидинофенокси)-8-бензилпурин;
2-(3-диметиламинокарбонилфенокси)-6-(3-бром-5-амидинофенокси)-8-бензилпурин;
2-(3-диметиламинокарбонилфенокси)-6-(2-метил-5-амидинофенокси)-8-бензилпурин;
2-(3-диметиламинокарбонилфенокси)-6-(2-метил-5-амидинофенокси)-8-фенилпурин;
2-(3-диметиламинокарбонилфенокси)-6-(3-метил-4-амидинофенокси)-8-фенилпурин;
2-(3-диметиламинокарбонилфенокси)-6-(2-амино-5-амидинофенокси)-8-фенилпурин;
2-(3-диметиламинокарбонилфенокси)-6-(3-амино-4-амидинофенокси)-8-фенилпурин;
2-(3-гуанидинофенокси)-6-(2-карбокси-5-амидинофенокси)-8-трет-бутилпурин;
2-(3-гуанидинофенокси)-6-(3-карбокси-4-амидинофенокси)-8-трет-бутилпурин;
2-(3-гуанидинофенокси)-6-(2-трет-бутоксикарбонил-5-амидинофенокси)-8-трет-бутилпурин;
2-(3-гуанидинофенокси)-6-(3-трет-бутоксикарбонил-4-амидинофенокси)-8-трифторметилпурин;
2-(3-гуанидинофенокси)-6-(2-аминокарбонил-5-амидинофенокси)-8-трифторметилпурин;
2-(3-гуанидинофенокси)-6-(3-аминокарбонил-4-амидинофенокси)-8-этилпурин;
2-(3-гуанидинофенокси)-6-(2-диметиламино-5-амидинофенокси)-8-этилпурин.
С. Аналогичным способом 2-(2-бензилокси-5-цианофенокси)-6-(3-диметиламинокарбонил)фенокси-8-метил-9-бензилпурин (0.65 г) превращали в 2-(2-гидрокси-5-амидинофенокси)-6-(3-диметиламинокарбонил)фенокси-8-метил-9-бензилпурин (0.39 г), соединение формулы (I).
Спектр ЯМР (DMSO-d6): 9.10 (шир. с, 2), 8.80 (шир. с, 2), 7.70 (д, 1), 7.65 (д, 1), 7.50 (дд, 1), 7.25-7.40 (м, 8), 7.10 (д, 1), 5.40 (с, 2), 3.00 (с, 3), 2.90 (с, 3), 2.70 (с, 3).
D. Аналогичным образом получали следующие соединения формулы (I):
2-(2-гидрокси-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-бензилпурин;
2-(2-метокси-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-бензилпурин;
2-(2-этокси-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-бензилпурин;
2-(2-фенокси-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-бензилпурин;
2-(2-хлор-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-бензилпурин;
2-(2-метил-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-бензилпурин;
2-(2-трет-бутил-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-бензилпурин;
2-(2-амино-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-бензилпурин;
2-(2-карбокси-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-бензилпурин;
2-(2-бензилоксикарбонил-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-бензилпурин;
2-(2-диэтиламинокарбонил-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)- 8-метил-9-бензилпурин;
2-(2-амино-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-бензилпурин;
2-(2-гидрокси-5-амидинофенокси)-6-(3-(1-метилимидазолин-2-ил)фенокси)-8-метил-9-бензилпурин;
2-(2-метокси-5-амидинофенокси)-6-(3-(2-(трет-бутоксикарбонил)-этил)фенокси)-8-метил-9-бензилпурин;
2-(2-этокси-5-амидинофенокси)-6-(3-трет-бутоксикарбонилфенокси)-8-метил-9-бензилпурин;
2-(2-фенокси-5-амидинофенокси)-6-(3-карбоксифенокси)-8-метил-9-бензилпурин;
2-(2-хлор-5-амидинофенокси)-6-(3-(2-аминоэтил)фенокси)-8-метил-9-бензилпурин;
2-(2-метил-5-амидинофенокси)-6-(3-гидроксифенокси)-8-метил-9-бензилпурин;
2-(2-трет-бутил-5-амидинофенокси)-6-(3-этоксифенокси)-8-метил-9-бензилпурин;
2-(2-амино-5-амидинофенокси)-6-(3-гуанидинофенокси)-8-метил-9-бензилпурин;
2-(2-карбокси-5-амидинофенокси)-6-(3-уреидофенокси)-8-метил-9-бензилпурин;
2-(2-бензилоксикарбонил-5-амидинофенокси)-6-(3-аминофенокси)-8-метил-9-бензилпурин;
2-(2-диэтиламинокарбонил-5-амидинофенокси)-6-(3-аминофенокси)-8-метил-9-бензилпурин;
2-(2-амино-5-амидинофенокси)-6-(3-трифторметоксифенокси)-8-метил-9-бензилпурин;
2-(2-гидрокси-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метилпурин;
2-(2-метокси-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метилпурин;
2-(2-этокси-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метилпурин;
2-(2-фенокси-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метилпурин;
2-(2-хлор-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метилпурин;
2-(2-метил-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метилпурин;
2-(2-трет-бутил-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метилпурин;
2-(2-амино-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метилпурин;
2-(2-карбокси-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метилпурин;
2-(2-бензилоксикарбонил-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метилпурин;
2-(2-диэтиламинокарбонил-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метилпурин;
2-(2-амино-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метилпурин;
2-(2-гидрокси-5-амидинофенокси)-6-(3-(1-метилимидазолин-2-ил)фенокси)-8-метилпурин;
2-(2-метокси-5-амидинофенокси)-6-(3-(2-(трет-бутоксикарбонил)этил)фенокси)-8-метилпурин;
2-(2-этокси-5-амидинофенокси)-6-(3-трет-бутоксикарбонилфенокси)-8-метилпурин;
2-(2-фенокси-5-амидинофенокси)-6-(3-карбоксифенокси)-8-метилпурин;
2-(2-хлор-5-амидинофенокси)-6-(3-(2-аминоэтил)фенокси)-8-метилпурин;
2-(2-метил-5-амидинофенокси)-6-(3-гидроксифенокси)-8-метилпурин;
2-(2-трет-бутил-5-амидинофенокси)-6-(3-этоксифенокси)-8-метилпурин;
2-(2-амино-5-амидинофенокси)-6-(3-гуанидинофенокси)-8-метилпурин;
2-(2-карбокси-5-амидинофенокси)-6-(3-уреидофенокси)-8-метилпурин;
2-(2-бензилоксикарбонил-5-амидинофенокси)-6-(3-аминофенокси)-8-метилпурин;
2-(2-диэтиламинокарбонил-5-амидинофенокси)-6-(3-аминофенокси)-8-метилпурин;
2-(2-амино-5-амидинофенокси)-6-(3-трифторметоксифенокси)-8-этилпурин;
2-(2-метил-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-этилпурин;
2-(2-трет-бутил-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-этилпурин;
2-(2-амино-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-этилпурин;
2-(2-карбокси-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-этилпурин;
2-(2-бензилоксикарбонил-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-этилпурин;
2-(2-диэтиламинокарбонил-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-этилпурин;
2-(2-амино-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-этил-9-этилпурин;
2-(2-гидрокси-5-амидинофенокси)-6-(3-(1-метилимидазолин-2-ил)фенокси)-8-этил-9-этилпурин;
2-(2-метокси-5-амидинофенокси)-6-(3-(2-(трет-бутоксикарбонил)этил)фенокси)-8-этил-9-этилпурин;
2-(2-этокси-5-амидинофенокси)-6-(3-трет-бутоксикарбонилфенокси)-8-этил-9-этилпурин;
2-(2-фенокси-5-амидинофенокси)-6-(3-карбоксифенокси)-8-этил-9-этилпурин;
2-(2-хлор-5-амидинофенокси)-6-(3-(2-аминоэтил)фенокси)-8-этил-9-этилпурин;
2-(2-метил-5-амидинофенокси)-6-(3-гидроксифенокси)-8-этил-9-этилпурин;
2-(2-трет-бутил-5-амидинофенокси)-6-(3-этоксифенокси)-8-этил-9-этилпурин;
2-(2-амино-5-амидинофенокси)-6-(3-гуанидинофенокси)-8-этил-9-этилпурин;
2-(2-карбокси-5-амидинофенокси)-6-(3-уреидофенокси)-8-этил-9-этилпурин;
2-(2-бензилоксикарбонил-5-амидинофенокси)-6-(3-аминофенокси)-8-этил-9-этилпурин;
2-(2-диэтиламинокарбонил-5-амидинофенокси)-6-(3-аминофенокси)-8-этил-9-этилпурин и
2-(2-амино-5-амидинофенокси)-6-(3-трифторметоксифенокси)-8-этил-9-этилпурин.
Е. Полученные выше соединения формулы (I) и формулы (II), в которых R5 представляет собой водород, могут быть также обработаны по способу, аналогичному описанному Dusert Р., Eur. J. Med. Chem. (1980), т.3, стр. 199, с целью получения следующих соединений:
2-(2-гидрокси-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1-карбоксиэтил)пурин;
2-(2-гидрокси-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1-этоксикарбонилэтил)пурин;
2-(2-гидрокси-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1-аминокарбонилэтил)пурин;
2-(2-метокси-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1-карбокси-2-метилпропил)пурин;
2-(2-метокси-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1-(этоксикарбонил)-2-метилпропил)пурин;
2-(2-метокси-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1-(аминокарбонил)-2-метилпропил)пурин;
2-(2-этокси-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1-карбокси-3-метилбутил)пурин;
2-(2-этокси-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1-(этоксикарбонил)-3-метилбутил)пурин;
2-(2-этокси-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1-(аминокарбонил)-3-метилбутил)пурин;
2-(2-фенокси-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1-(карбокси-2-метилбутил)пурин;
2-(2-фенокси-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1-(этоксикарбонил)-2-метилбутил)пурин;
2-(2-фенокси-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1-(аминокарбонил)-2-метилбутил)пурин;
2-(2-хлор-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1-карбокси-2-фенилэтил)пурин;
2-(2-хлор-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1-этоксикарбонил)-2-фенилэтил)пурин;
2-(2-хлор-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1-аминокарбонил)-2-фенилэтил)пурин;
2-(2-метил-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1-карбокси-2-(4-меркаптофенил)этил)пурин;
2-(2-метил-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1-(этоксикарбонил)-2-(4-меркаптофенил)этил)пурин;
2-(2-метил-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1-(аминокарбонил)-2-(4-меркаптофенил)этил)пурин;
2-(2-трет-бутил-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1-карбокси)-2-(индолин-3-ил)этил)пурин;
2-(2-трет-бутил-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1-(этоксикарбонил)-2-(индолин-3-ил)этил)пурин;
2-(2-трет-бутил-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1-(аминокарбонил)-2-(индолин-3-ил)этил)пурин;
2-(2-амино-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1-карбокси-2-(имидазол-4-ил)этил)пурин;
2-(2-амино-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1-(этоксикарбонил)-2-(имидазол-4-ил)этил)пурин;
2-(2-амино-6-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1-(аминокарбонил)-2-(имидазол-4-ил)этил)пурин;
2-(2-карбокси-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1-карбокси-2-гидроксиэтил)пурин;
2-(2-карбокси-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1-(этоксикарбонил)-2-гидроксиэтил)пурин;
2-(2-карбокси-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1-(аминокарбонил)-2-гидроксиэтил)пурин;
2-(2-бензилоксикарбонил-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1-карбокси-2-гидроксипропил)пурин;
2-(2-бензилоксикарбонил-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1-(этоксикарбонил)-2-гидроксипропил)пурин;
2-(2-бензилоксикарбонил-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1-(аминокарбонил)-2-гидроксипропил)пурин;
2-(2-диэтиламинокарбонил-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1-карбокси-2-(аминокарбонил)этил)пурин;
2-(2-диэтиламинокарбонил-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1-(этоксикарбонил)-2-(аминокарбонил)этил)пурин;
2-(2-диэтиламинокарбонил-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1,2-ди(аминокарбонил)этил)пурин;
2-(2-амино-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1-карбокси-3-(аминокарбонил)пропил)пурин;
2-(2-амино-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1-(этоксикарбонил)-3-(аминокарбонил)пропил)пурин;
2-(2-амино-5-амидинофенокси)-6-(3-диметиламинокарбонилфенокси)-8-метил-9-(1,3-ди(аминокарбонил)пропил)пурин;
2-(2-гидрокси-5-амидинофенокси)-6-(3-(1-метилимидазолин-2-ил)фенокси)-8-метил-9-(1,2-дикарбоксиэтил)пурин;
2-(2-гидрокси-5-амидинофенокси)-6-(3-(1-метилимидазолин-2-ил)фенокси)-8-метил-9-(1,2-ди(этоксикарбонил)этил)пурин;
2-(2-метокси-5-амидинофенокси)-6-(3-(2-(трет-бутоксикарбонил)этил)фенокси)-8-метил-9-(1,3-дикарбоксипропил)пурин;
2-(2-метокси-5-амидинофенокси)-6-(3-(2-(трет-бутоксикарбонил)этил)фенокси)-8-метил-9-(1,3-ди(этоксикарбонил)пропил)пурин;
2-(2-этокси-5-амидинофенокси)-6-(3-трет-бутоксикарбонилфенокси)-8-метил-9-(1-карбокси-5-аминопентил)пурин;
2-(2-этокси-5-амидинофенокси)-6-(3-трет-бутоксикарбонилфенокси)-8-метил-9-(1-(этоксикарбонил)-5-аминопентил)пурин;
2-(2-этокси-5-амидинофенокси)-6-(3-трет-бутоксикарбонилфенокси)-8-метил-9-(1-(аминокарбонил)-5-аминопентил)пурин;
2-(2-фенокси-5-амидинофенокси)-6-(3-карбоксифенокси)-8-метил-9-(1-карбокси-4-гуанидинобутил)пурин;
2-(2-фенокси-5-амидинофенокси)-6-(3-карбоксифенокси)-8-метил-9-(1-(этоксикарбонил)-4-гуанидинобутил)пурин и
2-(2-фенокси-5-амидинофенокси)-6-(3-карбоксифенокси)-8-метил-9-(1-(аминокарбонил)-4-гуанидинобутил)пурин.
Пример 2
Этот пример иллюстрирует получение типичных фармацевтических композиций для перорального введения, содержащих соединение изобретения или его фармацевтически приемлемую соль, например 2-(3-диметиламинокарбонилфенокси)-6-(2-гидрокси-4-амидинофенокси)-9-(1-метоксикарбонилпропил)-8-метил-9-бензилпурин:
А. Ингредиенты - % вес./вес.
Соединение изобретения - 20.0%
Лактоза - 79.5%
Стеарат магния - 0.5%
Указанные ингредиенты перемешивали и помещали в желатиновые капсулы с твердой оболочкой в количестве по 100 мг на капсулу.
В. Ингредиенты - % вес./вес.
Соединение изобретения - 20.0%
Стеарат магния - 0.9%
Крахмал - 8.6%
Лактоза - 79.6%
PVP (поливинипирролидин) - 0.9%
Указанные выше ингредиенты, за исключением стеарата магния, смешивали и гранулировали с использованием воды в качестве гранулирующей жидкости. Затем препарат сушили, смешивали со стеаратом магния и формировали в таблетки с применением соответствующей таблетирующей машины.
С. Ингредиенты
Соединение изобретения - 0.1 г
Пропиленгликоль - 20.0 г
Полиэтиленгликоль 400 - 20.0 г
Полисорбат 80 - 1.0 г
Вода - До 100 мл
Соединение изобретения растворяли в пропиленгликоле, полиэтиленгликоле 400 и полисорбате 80. Затем при перемешивании добавляли достаточное количество воды для получения 100 мл раствора, который фильтровали и распределяли в соответствующие емкости.
D. Ингредиенты - % вес./вес.
Соединение изобретения - 20.0%
Арахисовое масло - 78.0%
Span 60 - 2.0%
Указанные выше ингредиенты расплавляли, смешивали и заполняли ими мягкие эластичные капсулы.
Е. Ингредиенты - % вес./вес.
Соединение изобретения - 1.0%
Метил- или карбоксиметилцеллюлоза - 2.0%
0.9% физиологический раствор - До 100 мл
Соединение изобретения растворяли в смеси целлюлоза/физиологический раствор, фильтровали и помещали в емкости для использования.
Пример 3
Этот пример иллюстрирует получение типичной фармацевтической препаративной формы, предназначенной для парентерального введения, содержащей соединение изобретения или его фармацевтически приемлемую соль, например 2-(3-диметиламинокарбонилфенокси)-6-(2-фенокси-4-амидинофенокси)-9-(1-метоксикарбонилпропил)-8-метилпурин.
Ингредиенты
Соединение изобретения - 0.02 г
Пропиленгликоль - 20.0 г
Полиэтиленгликоль 400 - 20.0 г
Полисорбат 80 - 1.0 г
0.9% физиологический раствор - До 100 мл
Соединение изобретения растворяли в пропиленгликоле, полиэтиленгликоле 400 и полисорбате 80. Затем при перемешивании добавляли достаточное количество 0.9% физиологического раствора для получения 100 мл раствора для внутреннего введения, который фильтровали через 0.2 мкм мембранный фильтр и упаковывали в стерильных условиях.
Пример 4
Этот пример иллюстрирует получение типичной фармацевтической композиции, в виде суппозитория, содержащей соединение изобретения или его фармацевтически приемлемую соль, например 2-(3-диметиламинокарбонилфенокси)-6-(2-фенокси-4-амидинофенокси)-9-(1-метоксикарбонилпропил)-6-этил-9-бензилпурин:
Ингредиенты - % вес./вес.
Соединение изобретения - 1.0%
Полиэтиленгликоль 1000 - 74.5%
Полиэтиленгликоль 4000 - 24.5%
Ингредиенты расплавляли и смешивали на паровой бане, после чего заливали в формы, рассчитанные на общий вес 2.5 г.
Пример 5
Этот пример иллюстрирует получение типичной фармацевтической препаративной формы, предназначенной для инсуффляции, содержащей соединение изобретения или его фармацевтически приемлемую соль, например 2-(3-диметиламинокарбонилфенокси)-6-(2-фенокси-4-амидинофенокси)-9-(1-метоксикарбонилпропил)-8-этил-9-бензилпурин:
Ингредиенты - % вес./вес.
Микронизированное соединение изобретения - 1.0%
Микронизированная лактоза - 99.0%
Ингредиенты измельчали, смешивали и помещали в инсуффлятор, снабженный дозирующим насосом.
Пример 6
Этот пример иллюстрирует получение типичной фармацевтической препаративной формы, пригодной для распыления, содержащей соединение изобретения или его фармацевтически приемлемую соль, например 2-(3-диметиламинокарбонилфенокси)-6-(2-фенокси-4-амидинофенокси)-9-(1-метоксикарбонилпропил)-8-этилпурин:
Ингредиенты - % вес./вес.
Соединение изобретения - 0.005%
Вода - 89.995%
Этанол - 10.000%
Соединение изобретения растворяли в этаноле и смешивали с водой. Затем препаративную форму помещали в устройство для распыления, снабженное дозирующим насосом.
Пример 7
Этот пример иллюстрирует получение типичной фармацевтической препаративной формы в виде аэрозоля, содержащей соединение изобретения или его фармацевтически приемлемую соль, например 2-(3-диметиламинокарбонилфенокси)-6-(2-фенокси-4-амидинофенокси)-9-(1-метоксикарбонилпропил)-8-этилпурин.
Ингредиенты - % вес./вес.
Соединение изобретения - 0.10%
Пропеллент 11/12 - 98.90%
Олеиновая кислота - 1.00%
Соединение изобретения диспергировали в олеиновой кислоте и пропелленте. Полученную в результате смесь затем заливали в аэрозольный контейнер, снабженный мерным клапаном.
Пример 8
(In vitro тест на фактор Ха, тромбин и тканевый активатор плазминогена)
Этот тест демонстрирует активность соединений изобретения в отношении фактора Ха, тромбина и тканевого активатора плазминогена. Активности определяли по начальной скорости ферментативного расщепления белка п-нитроанилида. Продукт расщепления, п-нитроанилин, поглощает при длине волны 405 нм с коэффициентом молярной экстинции 9920 М-1см-1.
Реагенты и растворы
Диметилсульфоксид (DMSO)(Baker, для анализа).
Аналитический буфер:
50 мМ Трис-НСl, 150 мМ NaCl, 2.5 мМ CaCl2 и 0.1% полиэтиленгликоля 6000, рН 7.5.
Термины (Enzyme Research Lab.):
1. Исходный раствор человеческого фактора Ха: 0.281 мг/мл в аналитическом буфере, хранящийся при -80oС (рабочий раствор (2Х): 106 нг/мл или 2 нМ в аналитическом буфере, приготовленный перед использованием).
2. Исходный раствор человеческого тромбина: хранение при -80oС (рабочий раствор (2Х): 1200 нг/мл или 40 нМ в аналитическом буфере, приготовленный перед использованием).
3. Исходный раствор тканевого активатора плазминогена человека (tPA) (две цепочки Sigma) 1 мг/мл, хранение при -80oС (рабочий раствор (2Х): 1361 нг/мл в аналитическом буфере, приготовленный перед использованием).
Хромогенные субстраты (Pharmacia Hepar Inc.):
1. Исходный раствор S2222 (для анализа на Fxa): 6 мМ в dН2О, хранящийся при 4oС (рабочий раствор (4Х): 656 мкМ в аналитическом буфере).
2. Исходный раствор S2302 (анализ на тромбин): 10 мМ в dH2O, хранящийся при 4oС (рабочий раствор (4Х): 1200 мкМ в аналитическом буфере).
3. Исходный раствор S2288 (анализ на tPA): 10 мМ в dH2O, хранящийся при 4oС (рабочий раствор (4Х): 1484 мкМ в аналитическом буфере).
(Все рабочие растворы субстрата готовили на пятый день анализа).
Стандартный исходный раствор соединения-ингибитора: 5 мМ в DMSO, хранящийся при -20oС.
Исходные растворы испытуемых соединений (соединения изобретения): 10 мМ в DMSO, хранящиеся при -20oС.
Методика анализа
Анализы проводили в 96-луночных планшетах для микротитрования общим объемом 200 мкл. Аналитические компоненты применяли при конечной концентрации 50 мМ Трис-НСl, 150 мМ NaCl, 2.5 мМ CaCl2, 0.1% полиэтиленгликоля 6000, рН 7.5, в отсутствие или в присутствии стандартного соединения ингибитора или испытуемых соединений, а также фермента и субстрата при следующих концентрациях: (1) 1 нМ фактора Ха и 164 мкМ S2222; (2) 20 нМ тромбина и 300 мкМ S2302 и (3) 10 нМ tPa и 371 мкМ S2288. Концентрации стандартного соединения ингибитора в анализе составляли 5 мкМ - 0.021 мкМ в 1-3 разбавлении. Концентрация испытуемых соединений в анализе обычно составляла 10 - 0.041 мкМ в 1-3 разбавлении. В случае активных испытуемых соединений используемые концентрации в анализе на фактор Ха дополнительно разбавляли в 100 раз (100-0.41 нМ) или 1000 раз (10-0.041 нМ). Все используемые концентрации субстрата равны значениям их Km в условиях проведения анализа. Анализы проводили при температуре окружающей среды.
Первая стадия анализа состояла в приготовлении 10 мМ исходных растворов испытуемого соединения в ДМСО (для активных испытуемых соединений, 10 мM исходные растворы для анализа на фактор Ха дополнительно разбавляли до концентрации 0.1-0.01 нМ), после чего, по следующей ниже методике, готовили рабочие растворы испытуемого соединения (4Х) путем серийных разбавлении 10 мМ исходных растворов с помощью Biomek 1000 (или Multiprobe 204) в микропланшетах с 96 глубокими лунками.
(a) Готовили 40 мкМ рабочий раствор путем разбавления 10 мМ исходного раствора в 1-250 раз в аналитическом буфере, применяя 2 стадии разбавления: 1-100 и 1-2,5.
(b) Готовили пять других серийных разбавлении (1:3) 40 мкМ раствора (по 600 мкл дня каждой концентрации). Все партии из шести разбавленных растворов испытуемого соединения использовали в анализе. Стандартный ингибитор (5 мМ исходный раствор) или ДМСО (контроль) подвергали всем стадиям разбавления, что описаны выше для испытуемых соединений.
На следующей стадии анализа 50 мкл порции рабочих растворов испытуемых соединений (4Х) (от 40 мкМ до 0.164 мкМ), попарно, распределяли по титрометрическим микропланшетам в присутствии Biomek или МР204. К ним добавляли по 100 мкл рабочего раствора фермента (2Х) с Biomek или МР204. Полученные в результате растворы инкубировали при температуре окружающей среды в течение 10 минут.
К этим растворам добавляли по 50 мкл рабочего раствора субстрата (4Х) с Biomek или МР204.
Кинетику ферментативной реакции измеряли при температуре окружающей среды и длине волны 405 нМ, отбирая пробы с интервалами в 10 секунд в течение 5 минут, с использованием считывающего устройства THERMOmax для планшета.
Вычисление Кi для испытуемых соединений.
Скорости ферментативных реакций рассчитывали как mOD/мин на основании данных в первые две минуты измерений. Значения IC50 определяли путем обработки данных по log-logit уравнению (линейное) или уравнению Morrison (нелинейное) с использованием развернутой страницы EXCEL. Значения Ki получали делением IC50 на 2. Как общепринято, значения Ki (фактор Ха), меньшие 3 нМ, рассчитывали из уравнения Morrison.
При испытании в таком анализе соединения изобретения демонстрировали способность к селективному ингибированию человеческого фактора Ха и человеческого тромбина.
Пример 9
(In vitro тест в отношении человеческой протромбиназы)
Этот тест демонстрирует способность соединений изобретения ингибировать протромбиназу. Протромбиназа (PTase) катализирует активацию протромбина с образованием фрагмента 1.2 плюс тромбина с образованием мейзотромбина в качестве промежуточного продукта. Этот анализ представляет собой анализ по эквивалентной точке. Активность протромбиназы измеряли по активности тромбина (один из продуктов реакции) или по количеству тромбина, определенному по стандартной кривой зависимости количества образовавшегося тромбина/время (нМ vs mOD/мин). Для определения IC50 (PTase) соединений изобретения активность PTase выражали через активность тромбина (mOD/мин).
Материалы
1. Рабочий раствор человеческого фактора Ха (Haemotologic Technologies Inc. , Cat# HCVA-0110): 1.0 мг/мл в 50% глицерина, 2 мМ CaCl2, хранение при -20oС.
2. Рабочий раствор человеческого фактора Ха (Enzyme Res. Lab. Cat# HFXa 1011): 0.281 мг/мл в аналитическом буфере (без BSA), хранение при -20oС.
3. Рабочий раствор человеческого протромбина (FII) (Enzyme Res. Lab., Cat# HP1002): FII разбавленный до 4.85 мг/мл в аналитическом буфере (без BSA), хранящийся при -80oС.
Фосфолипидные (PCPS) везикулы:
PCPS везикулы (80% PC, 20% PS) готовили по модифицированному методу Barenholz с сотр., Biochemistry (1977), т. 16, стр. 2806-2810.
Фосфатидилсерин (Avanti Polar Lipids, Inc., Cat# 840032):
10 мг/мл в хлороформе, очищенный от мозга, хранящийся при -20oС в атмосфере азота или аргона.
Фосфатидилхолин (Avanti Polar Lipids, Inc., Cat# 850457): 50 мг/мл в хлороформе, синтетический 16:0-18:1 Пальмитоил-Олеил, хранящийся при -20oС в атмосфере азота или аргона.
Рабочий раствор Spectrozyme-TH (American Diagnostica Inc., Cat# 238L., 50 мкмолей, хранящийся при комнатной температуре): растворено 50 мкмолей в 10 мл dH2O.
BSA (Sigma Chem. Co., Cat# A-7888, фракция V, степень чистоты RIA).
Аналитический буфер: 50 мМ Tris-HCl, pH 7.5, 150 мМ CaCl2, 0.1% PEG 6000 (BDH), 0.05% BSA (Sigma, фракция V, степень чистоты RIA).
Для однопланшетного (one plate) анализа, готовили следующие рабочие растворы:
1. Протромбиназный комплекс.
(a) 100 мкМ PCPS (27.5 мкл исходного раствора PCPS (4.36 мМ) разбавляли аналитическим буфером до конечного объема 1200 мкл.
(b) 25 нМ человеческого фактора Va: 5.08 мкл исходного раствора Va (1 мг/мл) разбавляли аналитическим буфером до конечного объема 1200 мкл.
(c) 5 нМ человеческого фактора Ха: Ха исходный раствор (0.281 мг/мл) разбавляли в соотношении 1: 1.220.000 аналитическим буфером. Готовили, по крайней мере, 1200 мкл.
Объединяли равные объемы (1100 мкл) каждого из компонентов в последовательности PCPS, Va и Ха. Смеси выстаивали при температуре окружающей среды в течение 5-10 минут и немедленно использовали или хранили на льду (приводя к температуре окружающей среды перед использованием.
2. 6 мкМ человеческого протромбина (FII): 124 мкл исходного раствора FII (4.58 мг/мл) разбавляли аналитическим буфером до конечного объема 1400 мкл.
3. 20 мМ А/аналитический буфер: 0.8 мл 0.5 М EDTA (pH 8.5) плюс 19.2 мл аналитического буфера.
4. 0.2 мМ Spectrozyme-TH/EDTA буфер: 0.44 мл исходного раствора SPTH (5 мМ) плюс 10.56 мл 20 мМ EDTA/аналитический буфер.
5. Испытуемые соединения (соединения изобретения):
Готовили рабочий раствор (5Х) из 10 мМ исходного раствора (ДМСО) и делали серии разбавлений в соотношении 1:3. Соединения анализировали при 6 концентрациях, дублируя эксперимент.
Методика и условия теста
Протромбиназную реакцию осуществляли в 50 мкл смеси, содержащей PTase (20 мкМ PCPS, 5 нМ hFVA и 1 пМ hFXa), 1.2 мкМ человеческого фактора II и различные концентрации испытуемых соединений (5-0.021 мкМ или более низкий интервал концентраций). Реакцию начинали путем добавления PTase и в течение 6 минут смесь инкубировали при комнатной температуре. Реакцию прекращали путем добавления смеси EDTA/буфер до конечной концентрации 10 мМ. Затем при температуре окружающей среды с помощью считывающего устройства в микропланшете THERMOmax измеряли активность тромбина (продукт) в присутствии 0.1 мМ Spetrozyme-TH в качестве субстрата при длине волны 405 нМ в течение 5 минут (с интервалами в 10 секунд). Реакции проводили в 96-луночных микротитрометрических планшетах.
На первой стадии анализа 10 мкл разбавленного испытуемого соединения (5Х) или буфера добавляли в планшеты попарно. Затем в каждую лунку добавляли 10 мкл протромбина (hFII)(5X). Далее в каждую лунку добавляли еще по 30 мкл PTase и содержимое лунки перемешивали в течение 30 секунд. Затем планшеты инкубировали в течение 6 минут при температуре окружающей среды.
На следующей стадии анализа в каждую лунку, для остановки реакции, добавляли 50 мкл 20 мМ EDTA (в аналитическом буфере). Полученные растворы перемешивали в течение 10 секунд. После этого в каждую лунку добавляли по 100 мкл 0.2 мМ спектрозима. Скорость реакции тромбина измеряли при длине волны 405 нМ в течение 5 минут, с 10-секундными интервалами, с помощью считывающего устройства для микропланшета Molecular Devices.
Расчеты:
Скорость реакции тромбина выражали в mOD/мин с использованием значений OD за пять минут протекания реакции. Значения IC50 рассчитывали с использованием программы обработки log-logit кривой.
При испытании в таком анализе соединения изобретения демонстрировали способность к ингибированию протромбиназы.
Пример 10
(In vivo анализ)
Следующий анализ демонстрирует способность соединений изобретения действовать как антикоагулянты.
Самцов крыс (250-330 г) анестезировали с помощью пентобарбитала натрия (90 мг/кг, вн. бр.) и подготавливали к хирургическому вмешательству. Левую каротидную артерию каннюлировали для измерения кровяного давления, а также для отбора образцов крови с целью фиксирования параметров свертывания крови (протромбиновое время (РТ) и активированное неполное тромбопластиновое время (аРТТ)). Хвостовую вену канюлировали для введения испытуемых соединений (т. е. соединений изобретения и стандартов) и вливания тромбопластина. Разрезом по серединной линии вскрывали брюшную полость и брюшную полую вену изолировали на расстоянии 2-3 см от почечной вены. Все венозные ветви на этом 2-3 см сегменте брюшной полой вены лигировали. После всех хирургических вмешательств животным давали стабилизироваться перед началом эксперимента. Испытуемые соединения вводили в виде внутривенного болюса (t=0). Через три минуты (t=3) начинали 5-минутное вливание тромбопластина. Через две минуты вливания (t= 5) брюшную полую вену зашивали по ближайшему и удаленному концам. Сосуд оставляли на месте в течение 60 минут, после чего его иссекали у животного, открывали щель, сгусток крови, если он имелся, тщательно удаляли и взвешивали. Статистический анализ полученных результатов проводили с использованием теста Wilcoxin-matched-pair signed rank test.
При испытании в этом анализе соединения изобретения демонстрируют способность к ингибированию свертывания крови.
Хотя настоящее изобретение описано со ссылкой на конкретные варианты изобретения, специалисту в данной области должно быть понятно, что могут быть осуществлены различные изменения и приняты эквивалентные решения, не выходящие за объем изобретения. Кроме этого, могут быть произведены различные модификации и заменены соответствующие эквиваленты, без нарушения объема изобретения. Помимо этого, могут быть произведены многие модификации с целью адаптации к конкретной ситуации, материала, композиции, способа, стадии или стадий процесса, к целям, сущности и объему настоящего изобретения. Предусматривается, что все такие модификации охватываются объемом прилагаемой формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| БИЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ ПИРИМИДИНА И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1997 |
|
RU2198884C2 |
| ИНГИБИТОР EGFR И ЕГО ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ | 2015 |
|
RU2702631C2 |
| 5-ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ 1,1-ДИОКСО-1,2,5-ТИАЗОЛИДИН-3-ОНА В КАЧЕСТВЕ ИНГИБИТОРОВ РТРазы 1В | 2003 |
|
RU2349589C2 |
| КОМБИНАЦИИ АКТИВАТОРА (АКТИВАТОРОВ) РЕЦЕПТОРА, АКТИВИРУЕМОГО ПРОЛИФЕРАТОРОМ ПЕРОКСИСОМ (РАПП), И ИНГИБИТОРА (ИНГИБИТОРОВ) ВСАСЫВАНИЯ СТЕРИНА И ЛЕЧЕНИЕ ЗАБОЛЕВАНИЙ СОСУДОВ | 2008 |
|
RU2483724C2 |
| НОВЫЕ БИСПИДИНОВЫЕ СОЕДИНЕНИЯ, ПОЛЕЗНЫЕ ПРИ ЛЕЧЕНИИ СЕРДЕЧНЫХ АРИТМИЙ | 2000 |
|
RU2250903C2 |
| ИНГИБИТОРЫ ФОСФОИНОЗИТИД-3-КИНАЗЫ И СОДЕРЖАЩИЕ ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 2007 |
|
RU2437888C2 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ПИРАЗОЛА, ПРОМЕЖУТОЧНЫЕ ДЛЯ ИХ ПОЛУЧЕНИЯ, ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ И СПОСОБ БОРЬБЫ С СОРНЯКАМИ | 1993 |
|
RU2137771C1 |
| ИНГИБИТОРЫ ФЕРМЕНТА ДИАЦИЛГЛИЦЕРИН-О-АЦИЛТРАНСФЕРАЗЫ ТИПА 1 | 2008 |
|
RU2486186C2 |
| ПРОИЗВОДНЫЕ ТИЕНО[2,3-d]ПИРИМИДИН-2,4(1Н,3Н)-ДИОНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ЕЕ ПОЛУЧЕНИЯ, СПОСОБ ИММУНОСУПРЕССИИ И СПОСОБ ЛЕЧЕНИЯ ИЛИ СНИЖЕНИЯ РИСКА ОБСТРУКЦИИ ДЫХАТЕЛЬНЫХ ПУТЕЙ | 1998 |
|
RU2225410C2 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ПИРАЗОЛА И СРЕДСТВО, ОБЛАДАЮЩЕЕ ГЕРБИЦИДНОЙ АКТИВНОСТЬЮ | 1995 |
|
RU2154644C2 |
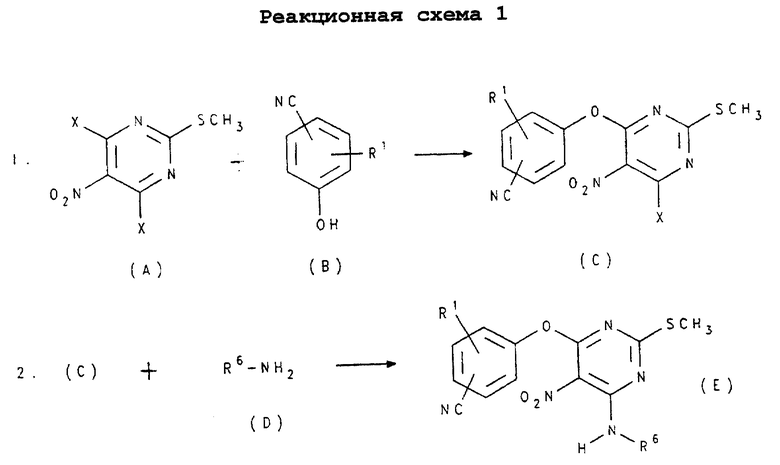

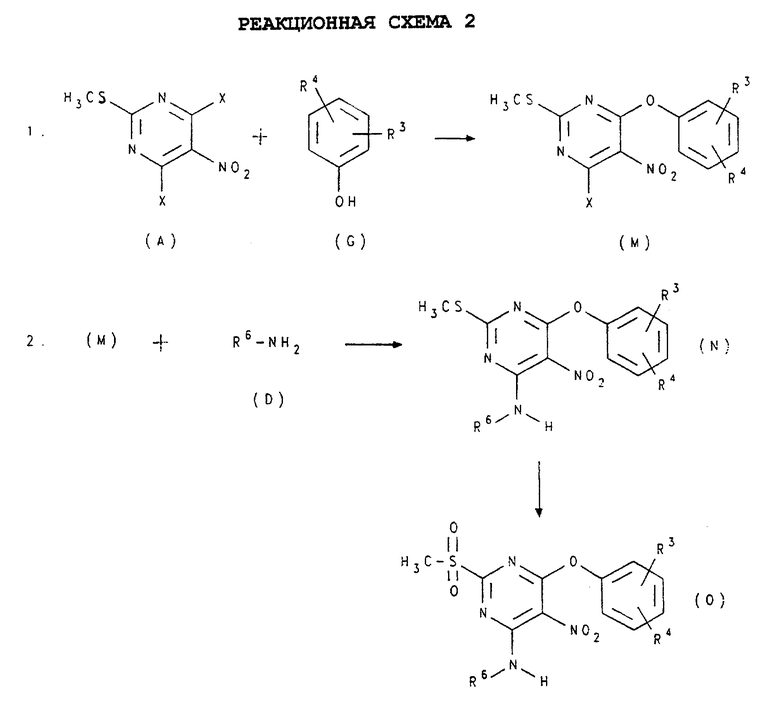
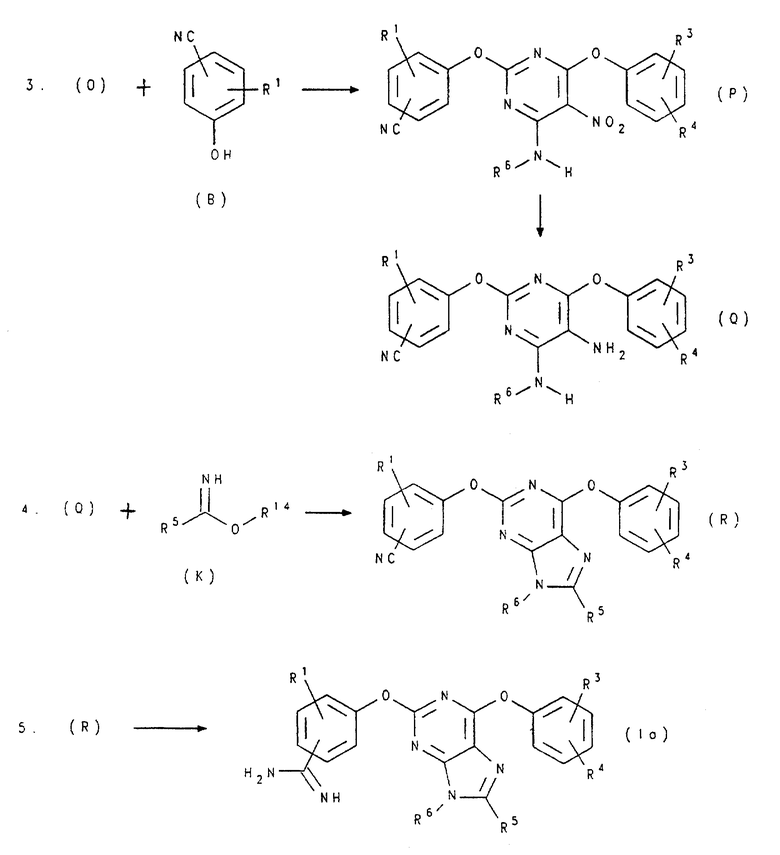

Изобретение относится к новым производным пурина формул I, II, III и IV, фармацевтической композиции на их основе и способу лечения болезненного состояния, характеризующегося тромботической активностью. В соединениях I, II, III и IV, в которых Z1 и Z2 каждый представляет -О-; R1 представляет водород или OR10; R2 представляет собой -C(NH)NH2; R3 представляет собой -С(О)N(R10)R11, (1,2)-тетрагидропиримидинил (необязательно замещенный алкилом), (1,2)-имидазолил (необязательно замещенный алкилом) или (1,2)-имидазолинил (необязательно замещенный алкилом); R4 представляет собой водород; R5 представляет собой алкил или аралкил; R6 представляет собой алкил, аралкил или (C(R7)(R8)n)-R9; R7 представляет собой алкил, -R12-С(O)OR10, -R12-C(O)N(R10)R11, -R12-C(R10)(C(O)OR10)2, -R12-N(R10)R11, -R12-N(R10)C(NR10)R13, -R12-N(R10)C(O)N(R10)R11, -R12-N(R10)C(NR10)N(R10)R11,
-R12-OR10, -R12-OP(O)(OR10)2, -R12-SR10, -R12-S(O)2R13 или R7 представляет собой аралкил (необязательно замещенный одним или более заместителями, выбранными из группы, состоящей из галогена, галоалкила, гидрокси и ОР(O)(ОR10)2, или R7 представляет собой имидазолилалкил или индолилалкил; R8 представляет собой водород или алкил; R9 представляет собой -C(O)OR10 или -C(O)N(R10)R11; каждый из R10 и R11 независимо представляет собой водород или алкил; R12 представляет собой прямую или разветвленную алкиленовую цепь и R13 представляет собой алкил или арил. Изобретение также относится к фармацевтической композиции, обладающей ингибирующей активностью по отношению к фактору Ха, которая включает терапевтически эффективное количество соединений I, II, III и IV, и способу лечения болезненного состояния человека, заключающемуся в ведении терапевтически эффективного количества указанных соединений. 3 с. и 5 з.п.ф-лы, 1 табл.
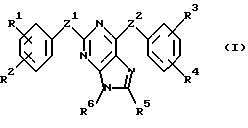
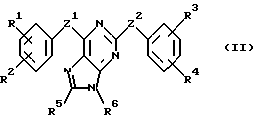
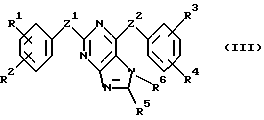
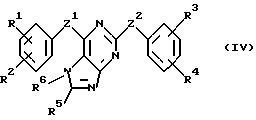
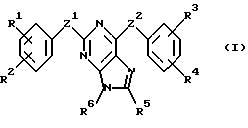
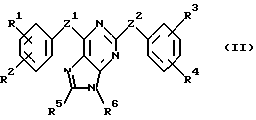
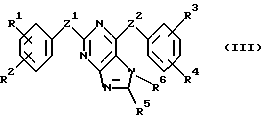
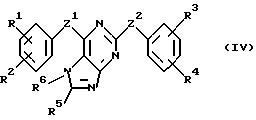
в которых Z1 и Z2 каждый представляет собой -О-;
R1 представляет водород или -OR10;
R2 представляет собой -C(NH)NH2;
R3 представляет собой -C(O)N(R10)R11, (1,2)-тетрагидропиримидинил (необязательно замещенный алкилом), (1,2)-имидазолил (необязательно замещенный алкилом) или (1,2)-имидазолинил (необязательно замещенный алкилом);
R4 представляет собой водород;
R5 представляет собой алкил или аралкил;
R6 представляет собой алкил, аралкил или (C(R7)(R8)n)-R9;
R7 представляет собой алкил, -R12-С(O)OR10, -R12-C(O)N(R10)R11, -R12-C(R10)(C(O)OR10)2, -R12-N(R10)R11, -R12-N(R10)C(NR10)R13, -R12-N(R10)C(O)N(R10)R11, -R12-N(R10)C(NR10)N(R10)R11, -R12-OR10, -R12-ОР(O)(ОR10)2, -R12-SR10, -R12-S(O)2R13 или R7 представляет собой аралкил (неoбязательно замещенный одним или более заместителями, выбранными из группы, состоящей из галогена, галоалкила, гидрокси и OP(O)(OR10)2), или R7 представляет собой имидазолилалкил или индолилалкил;
R8 представляет собой водород или алкил;
R9 представляет собой -C(O)OR10 или -C(O)N(R10)R11;
каждый из R10 и R11 независимо представляет собой водород или алкил;
R12 представляет собой прямую или разветвленную алкиленовую цепь;
R13 представляет собой алкил или арил,
в виде отдельных стереоизомеров или их смеси, или их фармацевтически приемлемая соль.
-R12-OR10, -R12-OP(O)(OR10)2, -R12-SR10, -R12-S(O)2R13 или R7 представляет собой аралкил (небязательно замещенный одним или более заместителями, выбранными из группы, состоящей из галогена, галоалкила, гидрокси и OP(O)(OR10)2), или R7 представляет собой имидазолилалкил или индолилалкил; R8 представляет собой водород или алкил; R9 представляет собой -C(O)OR10 или -C(O)N(R10)R11; каждый из R10 и R11 независимо представляет собой водород или алкил; R12 представляет собой прямую или разветвленную алкиленовую цепь и R13 представляет собой алкил или арил.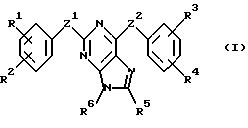

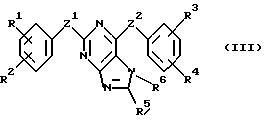
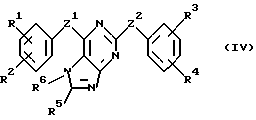
где Z1 и Z2 каждый представляет собой -О-;
R1 представляет водород или -OR10;
R2 представляет собой -C(NH)NH2;
R3 представляет собой -C(O)N(R10)R11, (1,2)-тетрагидропиримидинил (необязательно замещенный алкилом), (1,2)-имидазолил (необязательно замещенный алкилом) или (1,2)-имидазолинил (необязательно замещенный алкилом);
R4 представляет собой водород;
R5 представляет собой алкил или аралкил;
R6 представляет собой алкил, аралкил или (C(R7)(R8)n-R9;
R7 представляет собой алкил, -R12-С(O)OR10, -R12-C(O)N(R10)R11, -R12-C(R10)(C(O)OR10)2, -R12-N(R10)R11, -R12-N(R10)C(NR10)R13, -R12-N(R10)C(O)N(R10)R11, -R12-N(R10)C(NR10)N(R10)R11, -R12-OR10, -R12-OP(O)(OR10)2, -R12-SR10, -R12-S(O)2R13 или R7 представляет собой аралкил (небязательно замещенный одним или более заместителями, выбранными из группы, состоящей из галогена, галоалкила, гидрокси и OP(O)(OR10)2), или R7 представляет собой имидазолилалкил или индолилалкил;
R8 представляет собой водород или алкил;
R9 представляет собой -C(O)OR10 или -С(O)N(R10)R11;
каждый из R10 и R11 независимо представляет собой водород или алкил;
R12 представляет собой прямую или разветвленную алкиленовую цепь;
R13 представляет собой алкил или арил,
в виде индивидуального стереоизомера или их смеси, или их фармацевтически приемлемая соль и фармацевтически приемлемый эксципиент.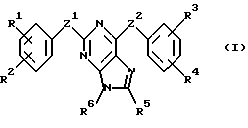
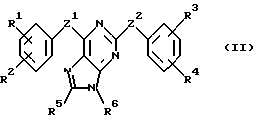
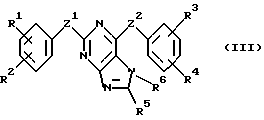
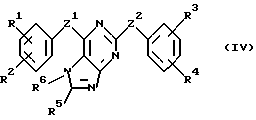
где Z1 и Z2 каждый представляет собой -О-;
R1 представляет водород или -OR10;
R2 представляет собой -C(NH)NH2;
R3 представляет собой -C(O)N(R10)R11, (1,2)-тетрагидропиримидинил (необязательно замещенный алкилом), (1,2)-имидазолил (необязательно замещенный алкилом) или (1,2)-имидазолинил (необязательно замещенный алкилом);
R4 представляет собой водород;
R5 представляет собой алкил или аралкил;
R6 представляет собой алкил, аралкил или (C(R7)(R8)n)-R9;
R7 представляет собой алкил, -R12-C(O)OR10, -R12-C(O)N(R10)R11, -R12-С(R10)(С(O)OR10)2, -R12-N(R10)R11, -R12-N(R10)C(NR10)R13, -R12-N(R10)C(O)N(R10)R11, -R12-N(R10)C(NR10)N(R10)R11, -R12-OR10, -R12-ОР(O)(ОR10)2, -R12-SR10, -R12-S(O)2R13, или R7 представляет собой аралкил (небязательно замещенный одним или более заместителями, выбранными из группы, состоящей из галогена, галоалкила, гидрокси и ОР(O)(ОR10)2), или R7 представляет собой имидазолилалкил или индолилалкил;
R8 представляет собой водород или алкил;
R9 представляет собой -C(O)OR10 или -C(O)N(R10)R11;
каждый из R10 и R11 независимо представляет собой водород или алкил;
R12 представляет собой прямую или разветвленную алкиленовую цепь,
R13 представляет собой алкил или арил,
в виде индивидульного стереоизомера или их смеси, или их фармацевтически приемлемой соли.
| US 4064169 A, 20.12.1977 | |||
| Пружинный стартер | 1975 |
|
SU540051A1 |
| RU 94042466 А, 20.07.1996 | |||
| DE 4333705 А1, 15.10.1995 | |||
| Планшайба для точной расточки лекал и выработок | 1922 |
|
SU1976A1 |
| DIE PHARMAZIE,1977, v.32, №3, с.141-145. | |||
Авторы
Даты
2002-10-27—Публикация
1997-08-14—Подача