Предлагаемое изобретение относится к области медицины и может быть использовано в сосудистой хирургии.
Реконструктивные операции на кровеносных сосудах всегда связаны с выделением сосудов из окружающих тканей, вскрытием просвета сосуда, удалением патологически измененной внутренней оболочки, имплантацией инородных тел. Это, несомненно, сопровождается разрушением естественных путей питания и иннервации сосудистой стенки, нарушением процессов регенерации артериальной стенки и возникновением асептического воспаления в зоне реконструкции. [Riles Th. S. , Lamparello P. J., Giangola С. et. al. Rupture of the vein patch: a vein complication of carotid endarterectomy. // Surgery.-1990.-V. 107. -N1. -P.10-12., Seebaner L, Holzmann Т., Geibdorfer K. et. al. Longterm results following implantation of a new small diameter bovine vessel xenograft. // International Congress of Angiology,-1985.-P.60-66]. Есть все основания полагать, что индуцированные хирургическим вмешательством дегенеративные и воспалительные процессы в сосудистой стенке играют немаловажную роль в генезе рестенозов и реокклюзий кровеносных сосудов. Особенно это является актуальным для артерий среднего и мелкого калибра [Марцинкявичюс А., Трипонис В. , Пикелите Р., Трипонене Д. Влияние прогрессирования атеросклероза на отдаленные результаты реконструкции аорты и периферических артерий. // Кардиология.-1988.-Т.28.- 6.-С.12-16., Taylor L.M., Loboa L., Porter J. M. The clinical course of carotid bifurcation stenosis as determined by duplex scanning. // J. Vasc. Surg.-1988.-V.8-N 3.-P.255-261].
Локальные воспалительные процессы в сосудистой стенке изучены недостаточно в развитии рестенозов и реокклюзий, поэтому традиционные методы их профилактики сводятся к устранению всех возможных послеоперационных осложнений. Работу проводят по нескольким основным направлениям:
1. контроль за свертывающей системой крови и своевременная ее коррекция;
2. интраоперационное создание атромбогенной поверхности в зоне реконструктивной операции;
3. влияние на циркуляторные факторы гемостаза;
4. профилактика прогрессирования окклюзирующего заболевания;
5. лечение сопутствующего заболевания.
С целью решения этих задач в послеоперационном периоде используют методы многолетнего введения антикоагулянтов кумаринового ряда, тромболитических препаратов, лекарственных смесей внутриартериально для снятия периферического ангиоспазма. Проводят также дезагрегантную терапию с применением ацетисалициловой кислоты (АСК) или ее водорастворимой формы ацелизина (соль АСК с лизином и глицином).
Как отмечают некоторые исследователи, на фоне системного лечения ацелизином клинически наблюдается благоприятное течение раневого процесса: менее выражены боль и отек мягких тканей после операции на голове и шее, отсутствуют клинические и рентгенологические признаки анастомозитов после операций на желудке и кишечнике. Но системное применение лекарственных препаратов, особенно длительное, очень часто сопровождается побочными явлениями. Например, использование ацелизина может вызывать аллергические реакции, усиливать действие антикоагулянтов, ульцерогенное действие других нестероидных противовоспалительных средств (НПВС) и кортикостероидов. Кроме того, препараты АСК противопоказаны при бронхиальной астме, язвенной болезни, кровотечении, гипокоагуляции. Также наблюдаются неоднозначные сдвиги показателей гемокоагуляции в зависимости от дозы ацелизина [Ленковски Ф., Нейринк Н. Г., Глезер С.В. Применение ацетилсалициловой кислоты при ИБС. // Терапевтич. Архив.-1996.- 8.-С.79-83].
В качестве местного противовоспалительного средства для профилактики асептических воспалений применение АСК (ацелизина) неизвестно.
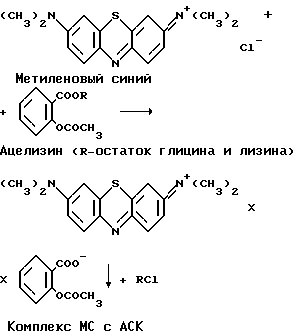
Авторами предлагается способ профилактики асептического воспаления сосудов посредством местного применения ацелизина. Так как ацелизин является хорошо растворимой в воде лекарственной формой АСК и не способен длительно удерживаться на поверхности тканей сосуда, для фиксации лекарства непосредственно в сосудистой стенке (медии или адвентиции) или на поверхности аутовенозного трансплантата используют краситель метиленовый синий (МС), [Машковский М.Д. Лекарственные средства. - Харьков: Торсинг, 1997. -Т. 2. - 590 С. ]. Иммобилизация АСК в составе комплекса с красителем на поверхности тканей сосуда происходит благодаря следующим свойствам красителя:
во-первых, прочно связываться с элементами соединительной ткани коллагеном и гликозаминогликанами;
во-вторых, способности молекул МС ассоциировать между собой с образованием ди-, три-..., мультимеров (явление метахромазии) [Ghosh А.К., Mukeree P. Multiple association equilibria in the self association of methylene blue and other dyes. // JACS. - 1970. - V. 92. - N 22. - Р. 6408-6412];
в-третьих, взаимодействовать с веществами анионного характера с образованием комплексов менее растворимых в воде, чем исходные реагенты.
Агрегированные молекулы красителя, частично уже связанные с поверхностью биоматериала, имеют возможность присоединять дополнительное количество других молекул с отрицательным зарядом, например АСК.
Предлагаемое изобретение иллюстрируется следующими примером.
Пример. При проведении операции эндартерэктомии после вскрытия кровеносного сосуда и удаления пораженной внутренней оболочки (интимы) поверхность медии и адвентиции обрабатывают 1%-ным водным раствором МС в течение 8-10 мин, после чего избыток красителя убирают салфеткой, затем на окрашенную поверхность наносят раствор ацелизина (0,1 г АСК в мл раствора). Время экспозиции составляет 8-10 мин. Таким же образом обрабатывают и аутовенозные трансплантаты.
Количество иммобилизованной АСК на поверхности биоматериалов определяют следующим образом. Фрагменты кадаверных тканей человека крупных кровеносных сосудов и аутовенозных трансплантатов с измеренной площадью сначала окрашивают 1%-ным раствором МС в течение 8-10 мин, избыток красителя убирают, затем наносят раствор ацелизина (0,5 г в 5 мл) и выдерживают 8-10 мин, избыток лекарства убирают салфеткой. Если нанесение лекарств производят на поверхности медии, промывку тканей осуществляют проточной водой, если ткани обрабатывают со стороны адвентиции, то их погружают в физраствор на определенное время, таким образом приблизительно имитируя те условия, в которых находятся кровеносные сосуды. Для извлечения АСК из состава комплекса с МС фрагменты сосудов помещают в 10%-ный раствор HCl и производят экстракцию АСК в виде свободной кислоты диэтиловым эфиром. После нескольких экстракций эфирные вытяжки объединяют, эфир испаряют, АСК растворяют в этиловом спирте и титруют водной щелочью в присутствии фенолфталеина. Контрольное титрование проводят аналогично, используя эфирный экстракт не обработанного лекарствами фрагмента ткани. Результат контрольного опыта вычитают из результатов экспериментов. Концентрацию АСК на 1 см2 поверхности рассчитывают по уравнению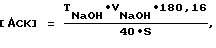
где ТNaOH - титр щелочи, мг/мл, VNaOH - объем щелочи, затраченный на титрование АСК; 180,16 и 40 - молекулярные массы АСК и NaOH соответственно; S - площадь фрагмента ткани.
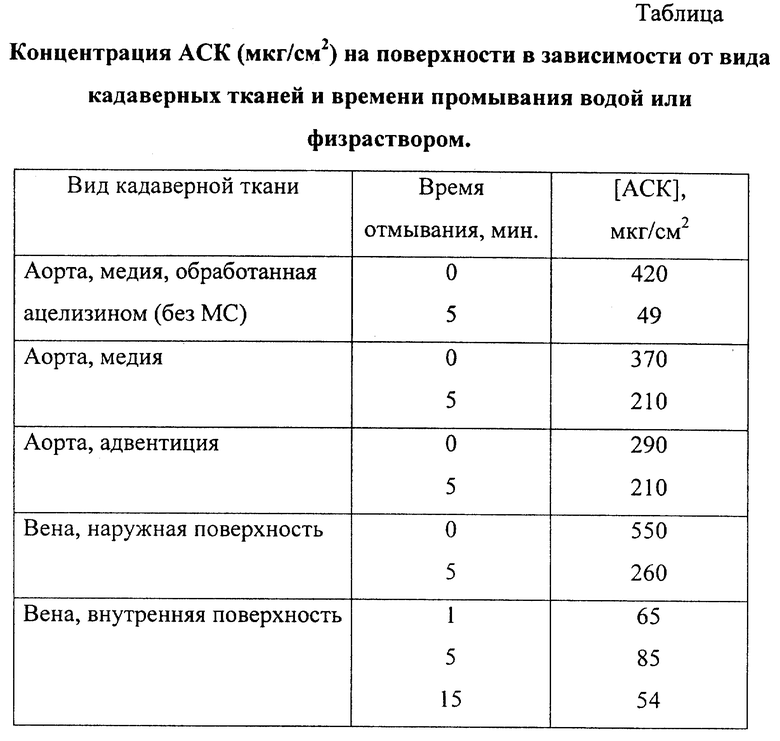
Как следует из результатов, приведенных в таблице, прочность связывания АСК и, следовательно, ее концентрация зависят от характера поверхности биоматериала.
Морфологическая картина результатов интраоперационного применения комплекса МС-АСК для профилактики асептического воспаления при операциях на магистральных сосудах.
Данный способ изучали в эксперименте на беспородных собаках обоего пола. Были сформированы 4 группы по 10 животных в каждой группе. Животным 1 группы в позицию сонной артерии были вшиты аутовенозные шунты с обработкой МС-ацелизин. Во 2-ю группу входили животные с подобной операцией без обработки. Животным 3-й группы в артериотомную рану была вшита аутовенозная заплата с обработкой МС-ацелизин. В 4-ю группу входили животные с подобной операцией без обработки. В каждой группе животных забор материала для гистологических исследований производили на 40-е и 90-е сутки после операции. Материал фиксировали в 10% забуференном формалине по Лилли. Срезы окрашивали гематоксилином и эозином, толуидиновым синим по Ван-Гизону, проводилась импрегнация серебром по Жухину.
В группах животных, где операции проводили без обработки аутотрансплантата и паравазальной клетчатки, значительно чаще встречались пристеночные тромбы в области анастомозов по сравнению с группами, где выполняли обработку МС-ацелизин. При этом на 40-е сутки наблюдалось активное тромбообразование с агрегацией эритроцитов на свежих фибриновых массах, под которыми располагался слой деградированного фибрина с мононуклеарными клетками (макрофаги, моноциты, лимфоциты). Далее была расположена незрелая грануляционная ткань, врастающая в медию. На 90-е сутки отмечались организованные тромбы, содержащие зрелые сосуды, и с поверхности сосудистого просвета покрытые интимой артерии. Интима артерии в области анатомоза в группах животных без обработки на 40-е сутки характеризовалась выраженным разволокнением и мультипликацией ретикулярных волокон (импрегнация по Жухину), очаговой пролиферацией эндотелиоцитов со сниженным содержанием кислых гликозаминогликанов по сравнению с таковыми после обработки МС-ацелизин. На 90-е сутки данные различия нивелировались. Интима в этот период имела сформированную сеть ретикулярных волокон, имеющих преимущественно продольную ориентацию. Кислые гликозаминогликаны отмечались преимущественно по поверхности. Медиальная оболочка артерий в группах животных без обработки на 40-е сутки характеризовалась выраженной пролиферацией гладкомышечных клеток, которая к 90-м суткам останавливалась на фоне склеротических изменений в медии. После обработки МС-ацелизин склероз медии на 90-е сутки не отмечался. В области шовного материала на 40-е сутки еще встречались очаги фибриноидного некроза, причем чаще они наблюдались в анастомозах без обработки. В паравазальной клетчатке интенсивность лимфогистиоцитарной инфильтрации была значительно ниже после обработки МС-ацелизин на 40-е сутки. Состояние аутотрансплантатов в исследуемых группах специфических особенностей не имело. На 40-е и 90-е сутки они имели тонкую интиму с подлежащими оформленными соединительнотканными элементами.
Как следует из гистологических исследований, обработка аутотрансплантатов и паравазальной клетчатки МС-ацелизин стабилизирует тканевый гомеостаз в области анастомоза, что в последующем может значительно снизить количество рестенозов и реокклюзий в послеоперационном периоде.
ЛИТЕРАТУРА
1. Riles Th.S., Lamparello P.J., Giangola C. et al. Rupture of the vein patch: a vein complication of carotid endarterectomy. // Surgery.-1990.-V. 107.-N1.-P.10-12.
2. Seebaner L. , Holzmann Т. , Geibdorfer K. et al. Longterm results following implantation of a new small diameter bovine vessel xenograft. // International Congress of Angiology. -1985. - P.60-66.
3. Марцинкявичюс А. , Трипонис В., Пикелите Р., Трипонене Д. Влияние прогрессирования атеросклероза на отдаленные результаты реконструкции аорты и периферических артерий. // Кардиология. -1988. -Т.28. - 6. -С.12-16.
4. Taylor L.M., Loboa L., Porter J.M. The clinical course of carotid bifurcation stenosis as determined by duplex scanning. // J. Vase. Surg. -1988. -V.8. -N3. -P.255-261.
5. Ленковски Ф., Нейринк Н.Г., Глезер С.В. Применение ацетилсалициловой кислоты при ИБС. // Терапевтич. Архив. -1996. - 8. -С.79-83.
6. Машковский М.Д. Лекарственные средства. - Харьков: Торсинг, 1997. -Т. 2. -590С.
7. Ghosh A. K., Mukeree P. Multiple association equilibria in the self association of methylene blue and other dyes. // JACS. - 1970. - V. 92. - N 22. -Р. 6408-6412.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОФИЛАКТИКИ РЕОККЛЮЗИЙ ПРИ ОПЕРАЦИЯХ НА МАГИСТРАЛЬНЫХ СОСУДАХ | 1999 |
|
RU2185171C2 |
| СПОСОБ ФОРМИРОВАНИЯ АНТИКОАГУЛЯНТНОЙ ПОВЕРХНОСТИ | 1998 |
|
RU2152217C1 |
| СПОСОБ ФОРМИРОВАНИЯ ГЕПАРИНИЗИРОВАННОЙ ПОВЕРХНОСТИ | 1998 |
|
RU2155593C2 |
| СПОСОБ ФОРМИРОВАНИЯ ГЕПАРИНИЗИРОВАННОЙ ПОВЕРХНОСТИ | 1998 |
|
RU2137507C1 |
| СПОСОБ ЗАЩИТЫ АНАСТОМОЗОВ ПРИ РЕЗЕКЦИЯХ КИШЕЧНИКА | 2000 |
|
RU2192256C2 |
| СПОСОБ АНТИБАКТЕРИАЛЬНОЙ ЗАЩИТЫ АНАСТОМОЗОВ ПРИ РЕЗЕКЦИЯХ КИШЕЧНИКА | 1999 |
|
RU2184545C2 |
| СПОСОБ ПОЛУЧЕНИЯ МОДИФИЦИРОВАННОЙ ГИАЛУРОНОВОЙ КИСЛОТЫ | 2000 |
|
RU2191782C2 |
| СПОСОБ ПОЛУЧЕНИЯ МАТЕРИАЛА С АНТИМИКРОБНЫМИ СВОЙСТВАМИ | 1998 |
|
RU2157244C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОТЕЗОВ КРОВЕНОСНЫХ СОСУДОВ | 2001 |
|
RU2241414C2 |
| ОРГАНИЧЕСКИЕ КОМПЛЕКСЫ ЦЕФАЛОСПОРИНОВЫХ АНТИБИОТИКОВ, ОБЛАДАЮЩИЕ АНТИМИКРОБНЫМИ СВОЙСТВАМИ | 1999 |
|
RU2184737C2 |
Изобретение относится к медицине, а именно к сосудистой хирургии, и предназначено для профилактики асептического воспаления при операциях на магистральных сосудах. Поверхность тканей кровеносных сосудов предварительно обрабатывают 1%-ным водным раствором метиленового синего в течение 8-10 мин. Затем наносят раствор ацелизина и выдерживают 8-10 мин. Раствор ацелизина содержит 0,1 г ацетилсалициловой кислоты в 1 мл водного раствора. Способ позволяет иммобилизировать ацелизин с помошью метиленового синего на поверхности сосудов. Это снижает количество рестенозов и реокклюзий в послеоперационном периоде. 1 табл.
Способ профилактики асептического воспаления при операциях на магистральных сосудах путем использования ацелизина, отличающийся тем, что поверхность тканей кровеносных сосудов или аутовенозных трансплантатов предварительно обрабатывают 1%-ным водным раствором красителя метиленового синего в течение 8-10 мин, после чего наносят раствор ацелизина, содержащий 0,1 г ацетилсалициловой кислоты в 1 мл водного раствора, и выдерживают 8-10 мин.
| ВАБИЩЕВИЧ А.В | |||
| и др | |||
| Профилактика тромбообразования и улучшение реологических свойств крови при операциях с микрохирургической техникой | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Возможности использования ацелизина - производного ацетилсалициловой кислоты | |||
| - Анестезиология и реаниматология, 1999, № 5, с | |||
| Способ запрессовки не выдержавших гидравлической пробы отливок | 1923 |
|
SU51A1 |
| СРЕДСТВО ДЛЯ СНИЖЕНИЯ АГРЕГАЦИИ ТРОМБОЦИТОВ В КРОВЕНОСНОЙ СИСТЕМЕ | 1995 |
|
RU2095064C1 |
| СПОСОБ ОБЩЕГО ОБЕЗБОЛИВАНИЯ | 1991 |
|
RU2016586C1 |
Авторы
Даты
2002-03-27—Публикация
1999-06-25—Подача