Язвенные болезни желудка и кишечника, ГЭРБ (желудочная эзофагитная рефлюксная болезнь) и вообще гастриты являются хроническими заболеваниями с временными обострениями и ослаблениями, случающимися в возрасте 30 лет и более. Антагонисты H2-рецепторов были введены в практику в 1976 году и, не считая известных побочных действий, являются хорошо толерантными и достаточно эффективными для заживления язв.
Позднее было показано, что откачивающие кислоту ингибиторы, такие как Омепразол, известный под товарным знаком Losec®, ингибируют выделение избытка желудочной кислоты в большей степени, действуют более быстро и излечивают большой процент кишечных и желудочных язв. Главная проблема состоит в том, что однажды вылеченные кишечные/желудочные язвы и устраненный ГЭРБ повторяются вновь вместе с изжогой. Более 80% язвенных болезней можно ожидать вновь через год и почти 100% через два года после прекращения курса лечения.
Объяснение высокой степени повторяемости ГЭРБ, наиболее вероятно, связано с колонизацией в оболочке пищевода и желудка патогенетического Campylobacter (Heliobacter pylori). Уже в восьмидесятых годах в отдельных исследованиях было показано, что вероятность возобновления кишечной/желудочной язв впечатляюще сократится, если уничтожить связанную с Heliobacter pylori инфекцию.
Билл и Пауэр (Scand. J. Gastroent. 1993, 196: 7-11), обобщив данные восьми исследований, показали, что при уничтожении Heliobacter pylori (те. когда этот организм не обнаруживается в течение 6-24 месяца после лечения) кишечная язва возобновляется у 3% пациентов по сравнению с 65% у тех, у которых все еще присутствует этот организм.
Фактически у всех больных кишечной язвой присутствует Heliobacter pylori (ГП). Более 70% желудочных язв показывают наличие ГП. Однако недавние исследования показали, что уничтожение ГП является обязательным условием для уменьшения вероятности возобновления кишечной/желудочной язв.
Грэхем и др. (Am Intern Med 1992, 116:705-708) выбрали случайным образом 26 больных желудочной язвой и назначили им прием либо одного ранитидина, либо тройную терапию (тетрациклином, метрондиазолом и субсалицилатом висмута) вместе с ранитидином. После годичного наблюдения уровень возобновления язвы был равен 74% у больных, лечившихся одним ранитидином по сравнению с только 13% у тех, кто лечился посредством тройной терапии и ранитидином.
Недавно, при комплексном исследовании желудочной язвы в Германии, 130 больных были выбраны случайным образом для приема либо 20 мг омепразола ежедневно, либо для тройной терапии, включающей субсалицилат висмута (600 мг три раза в день в течение 8 недель) плюс амоксициллин (500 мг два раза в день) и тинидазол (1 г ежедневно) - в течение 1-10 дней (BayerdUrffer и др., J. Med. Sci. 1992, 161: Suppl. 10:30). Уровень повторного заболевания к 6 месяцам был равен только 3% у больных, прошедших лечение, с отрицательным ГП по сравнению с 33% у тех, кто сохранил наличие ГП.
Таким образом было доказано, что висмутовые соли эффективно уничтожают ГП и обладают лечащим эффектом для пищеводных и желудочных оболочек и надолго улучшают клинические симптомы ГЭРБ.
Наиболее известное висмутовое лекарство De NoIR, содержащее субцитрат висмута, связанный с пептидом и произведенный в виде коллоидного раствора, покрывающего оболочки пищевода и желудка, таким образом эффективно уничтожающего ГП и заживляющего оболочки. Однако другие неучтенные факторы включаются с большой вероятностью в патогенез ГЭРБ.
Одним из наиболее важных факторов является уменьшение возможности заболевания нижнего сфинктера пищевода HCП, вызывающего обратную регургитацию высоко кислотного компонента желудка в нижнюю часть пищевода. Оболочка пищевода подвергается деторическому эффекту желудочного сока, начинает раздражаться, и, в конце концов, на ней возникает язва вследствие постоянного повторяющегося притока (субъективно определенного как изжога).
Для устранения изжоги, обратных притоков и отрыжки уже много лет используется альгиновый препарат с торговой маркой Гавискон®. Гавискон® включает в себя альгиновую кислоту в смеси с бикарбонатом натрия и вызывает в желудке специальную пену, "зонтоподобно" препятствующую проникновению содержимого желудка в пищевод. В то же время Гавискон® буферирует желудочный сок и остается в желудке в течение достаточно долгого времени.
Краткое изложение изобретения.
Целью настоящего изобретения является создание нового препарата для лечения гастрита, обратного эзофагита, дуоденита, диспепсии и язвы. Он должен быть эффективен для удаления Campylobacter такого, как Heliobacter pylori (ГП), в дальнейшем он должен активно препятствовать обратному оттоку содержимого желудка.
Целью создания этого препарата является также лечение и предохранение от других инфекционных заболеваний пищеварительного тракта, таких как диарея (понос) и других видов бактериального энтероколитиса.
Цель изобретения была достигнута созданием фармацевтического препарата, содержащего смесь цитрата висмута и альгината и другие реакционные продукты, особенно альгинат висмута. Смесь альгината и висмута будет обеспечивать как защиту слизистой оболочки, так и уничтожение Campylobacter типа ГП.
Препарат, заявленный в изобретении, может также содержать одно или более антибиотическое вещество для того, чтобы обеспечить более высокую и стабильную степень уничтожения нежелательных микроорганизмов. Такими антибиотическими веществами могут быть амоксициллин® и/или метронизадол.
Предпочтительно, если лекарство будет также содержать агенты, такие как бикарбонат натрия, которые в кислой среде желудка будут вспенивать альгинат висмута и в то же время обеспечивать буферный эффект в кислотном желудочном соке.
Описание изобретения.
Таким образом, поставленная задача была решена тем, что фармацевтический препарат для лечения гастритов, рефлюкс-эзофагитов, дуоденитов, диспепсии и язвы, содержащий соединение висмута, согласно изобретению содержат цитрат висмута, альгинат и альгинат висмута.
В качестве альгината он может содержать, в частности, альгинат натрия, калия и/или кальция.
Фармацевтический препарат предпочтительно содержит одно или более антибиотическое вещество.
В качестве антибиотических веществ препарат может содержать эффективные против Campylobacter, особенно Heliobacter pylons, например, амоксициллин или метронизадол.
Фармацевтический препарат может дополнительно содержать агент, предпочтительно бикарбонат натрия, который будет вызывать нейтрализацию кислой среды желудка и вспенивание альгината висмута.
Фармацевтический препарат может содержать медленно высвобождаемый агент.
Альгинат висмута в соответствии с изобретением альгинатный препарат менее токсичен, чем другие известные препараты висмута, благодаря его медленной абсорбции и меньшему росту концентрации в плазме. Ионы висмута крепко связываются с альгинатом. Это будет препятствовать или по крайней мере замедлять возможные нефротоксичные эффекты висмута и другие системные эффекты, о которых сообщается в медицинской литературе для других более легко абсорбирующихся висмутовых лекарств. Висмут действует в определенном месте, но он легко проходит, почти не абсорбируясь, через весь пищеварительный тракт.
Препарат на основе альгината висмута в соответствии с настоящим изобретением может быть приготовлен смешением цитрата висмута и аммония или субцитрата висмута и аммония с альгинатом натрия, калия и/или кальция. Для нейтрализации кислой желудочной среды или достижения пенообразовательного эффекта можно добавлять бикарбонат натрия (NаНСО3). Одновременно в реакционную среду можно добавить хлорид кальция, который вызывает образование пузырей альгината кальция. Целью такого микрокапсулирования является замедление диссоциации и процессов диффузии альгината висмута. Покрытие альгинатом кальция предназначено для того, чтобы ослабить быструю диффузию и диссоциацию ионов висмута из альгината висмута и дальнейшее их впитывание в кровеносную систему. Высокая концентрация висмута в плазме является предпосылкой возникновения осложнений, описанных для различных висмутовых препаратов.
Альгинат висмута можно использовать отдельно при монотерапии ГЭРБ благодаря высокой скорости уничтожения Н. pylori в его присутствии. Его также можно использовать совместно с антимикробными агентами при двойной, тройной и четверной терапии. Такими антимикробными агентами могут быть амоксициллин® и/или метронидазол® (тинидазол®). Эти антимикробные агенты можно объединять с альгинатом висмута в одно лекарство либо давать их отдельно. Альгинат висмута можно также использовать в смеси с сукралфатом в двойной или в смеси с сукралфатом и амоксициллином в тройной терапии.
Согласно нашему Исследованию 5, описанному ниже, в котором проводилось одногодичное наблюдение с серологическим изучением крови после 1, 6 и 12 месяцев, только у одного пациента из группы, лечившейся биогастрином (висмутовое альгинатное лекарство, заявленное в изобретении) + амоксициллин®, и ни у одного из больных с чувствительностью к метронизадолу и лечившимися биогастрином + амоксициллин® (Фазигин Пфайзер), был замечен положительный тест на кровеносную сыворотку, в то время как у более чем 30% больных, лечившихся смесью лозек® и амоксициллин® наблюдался индекс повторной инфекции (положительная серология). Следует заметить, что Н. pylori не обнаруживает сопротивления висмуту, такого как на метронизадол или амоксициллин®.
Исследование показало, что биогастрин + амоксициллин® и биогастрин + тинидазол® превосходят омепразол + амоксициллин® по сроку уничтожения Н. pylori и сравнимы по срокам устранения симптомов ГЭРБ.
Антимикробное лечение (амоксициллин®, фторхиноланы, метронизадол и т.д.) не обеспечивает достаточный уровень уничтожения, когда применяется отдельно. Метронизадол, употребляющийся отдельно, приводит почти всегда к лекарственной сопротивляемости. Сопротивляемость значительно уменьшается, когда метронизадол (тинидазол®) объединяют с альгинатом висмута (биогастрин).
Опыт показывает, что хотя достаточно легко устранить микроорганизм на время, уничтожить его окончательно достаточно сложно, возможно потому, что микроб остается на желудочной оболочке и в желудочных впадинах, где уровень антибиотика может не достичь бактерицидного уровня. Это означает, что назначенный антибиотик приостанавливает на некоторое время размножение "спрятавшихся" в местах убежища оставшихся бактерий, и реальное число бактерий превышает уровень обнаруженных.
В случае ГЭРБ может быть рекомендована даже просто монотерапия альгинатом висмута с ожидаемым уровнем уничтожения ГП 40-60%, но в этом случае высока вероятность повторных симптомов изжоги и плохого пищеварения. Монотерапия альгинатом висмута превосходит лечение как гавиксоном®, так и Де Нол® (КВС- Коллоидный Висмутовый Субстрат), принимающимися по отдельности (Исследование 5, см. ниже).
Спирт - Heliobacter Pylori.
Heliobacter Pylori обладает очень активной алкогольдегидрогеназой (АДГ). Даже в присутствии очень маленькой концентрации этанола после приема так называемых слабоалкогольных напитков у больных, зараженных ГП, образуется очень токсичный (свободные радикалы, производящие карценогены и иммуногены) ацетальдегид (АЦА). АЦА легко присоединяется к белкам, поступающим в желудочную среду. Образование аддуктов АЦА-белок ведет к разрушению клеток и вызывает ответную имунную реакцию и, как следствие, наносит раны желудочной оболочке. Более того, АЦА затормаживает размножение желудочных эпителиальных клеток в антральной оболочке. Этот патогеничный фактор необходимо лечить, так как он замедляет нормальное восстановление и защиту желудочной оболочки. Наблюдается рост доказательств, подтверждающих ассоциацию спирта с присутствующей Heliobacter pylori. Различные висмутовые соединения даже очень маленькой концентрации селективно ослабляют активную АДГ цитозольных Heliobacter pylori на 93%!
Предварительные данные свидетельствуют о том, что добавление омепразола к биогастрину или билгастрозолу существенно увеличивает степень уничтожения в НИР- (Nitroimidozol и Metronizadol) резистентных больных.
Поэтому биогастрин является возможным вариантом лекарства для всех пациентов с ГЭРБ или НГ (Неязвенный гастрит) и кишечными или желудочными болезнями, которые употребляют некоторые количества спирта, особенно для тех, кто чувствует возрастание симптомов изжоги, деториации или других форм растройства пищеварения после выпивания даже небольшого количества вина или другого алкогольного напитка.
Мочевина - аммиак
Heliobacter pylori характеризуется высоким уровнем мочевинной активности, которая метаболизирует мочевину до аммиака. Было сделано предположение, что аммиак цитотоксичен для клеток желудочной оболочки (Bawer M.R. и др. J Clin. Pathol. 1988, 41: 597), поскольку увеличивается обратная водородная диффузия (Hazell, S.L. Lee.A. Lancet. 1986: 15-17) и стимулируется выделение кислоты в желудке (Switch, J.T.L. et al Gut. 1990; 31: 522-525). Желудочная оболочка у зараженных Heliobacter pylori людей характеризуется большой аккумуляцией нейтрофилов (Morns, А и др. Am. J. Gastroenterolog. 1987; 82; 192-199). Активированные нейтрофилы генерируют многокислородные анионы и пероксид водорода.
Миэлопероксидаза, которая обычно выделяется во внеклеточное пространство, может катализировать окисление хлорида пероксидом водорода до монохлорамина и хлорноватистой кислоты. Известно, что монохлорамин является исключительно реакционным и токсичным веществом благодаря его высоким гипофильным свойствам и низкой молекулярной массе (Thomas, EL. Grisham, М.D., Jefferson, M.M. Method Enzymolog. 1986, 132: 585-593. Mucarami et al., Gastroenterology 1990, 98: A210 and Morishita и др.. Europ. J. Gastroenterol. & Hepat, 1993; 5. Suppl. 1: 5133-5136) не так давно показали, что антинейтрофильная сыворотка и таурин (связывающий монохлорамин) защищает крыс и людей от повреждения желудочной оболочки, причиняемых аммиаком и heliobacter pylori (у больных с желудочной язвой).
Альгинат висмута буферирует аммиак и благодаря его устраняющему действию обладает бесспорным защитным эффектом от бактериальной активности.
Прием лекарств
Альгинат висмута и антимикробные агенты могут приниматься по отдельности или совместно в одном препарате. Формой лекарства могут быть либо таблетки, либо капсулы, покрытые медленно высвобождающимся агентом, например альгинатом кальция, либо в жидкой форме. Все вещества, добавляемые в лекарство, должны быть фармакологически приемлемыми и нетоксичными в добавленных дозах.
Когда при монотерапии применяется не связанный образец альгината висмута, его назначенная доза должна составлять 1-2 капсулы 3 раза в день, в каждой по 500 мг альгината висмута.
Доза образца альгината висмута в смеси с амоксициллином составляет 2 капсулы три раза в день, каждая капсула содержит 500 мг альгината висмута и 250 мг амоксициллина.
Доза образца альгината висмута в смеси с фимидазолом® и амоксициллином должна составлять 2 капсулы три раза в день, по 250 мг альгината висмута + 250 мг тинидазола® + 250 мг амоксициллина в каждой капсуле.
Как упоминалось выше, возможным вариантом употребления антимикробных агентов является их прием по отдельности. Доза для сочетания альгината висмута и сукральфатом составляет 500 мг альгината висмута вместе с 1 г сукральфата три раза в день. При тройной терапии употребляется сочетание вышеупомянутого состава вместе с 250 мг амоксициллина три раза в день.
Пример
Во всех исследованиях, описанных ниже, использовалось лекарство, названное биогастрин, которое готовится смешением следующих веществ:
Протанал LF 200 RB - 40,00 г
Цитрат аммония и висмута 10301 - 345,00 г
Провидон К30 - 95,00 г
Хлорид кальция - 20,00 г - 500,00 г
Протанал LF 200 RB был получен из Пронова, Драммен, Норвегия. Вместо Протанал LF 200 RB может использоваться любой другой альгинат различной вязкости, выделяющийся из морских водорослей типа laminaria и/или ascophylum nodosum, произведенный любой фирмой, обрабатывающей морские ресурсы.
Цитрат висмута и аммония 10301, содержащий висмут 43-461, получен от Ридел-де-Хайн. Также может использоваться любой другой поставщик цитрата висмута и аммония или субцитрата висмута и аммония. Конечный продукт может покрываться лецитином и, если необходимо, в дальнейшем микрокапсулирован с образованием гранул.
Гранулы могут использоваться в саше. В другом варианте крупинки альгината кальция, содержащие альгинат висмута, помещаются прямо в капсулы.
Восприимчивость Н. pylori к альгинату висмута (биогастрин) и к субцитрату висмута (De NoIR) изучалась in vitro.
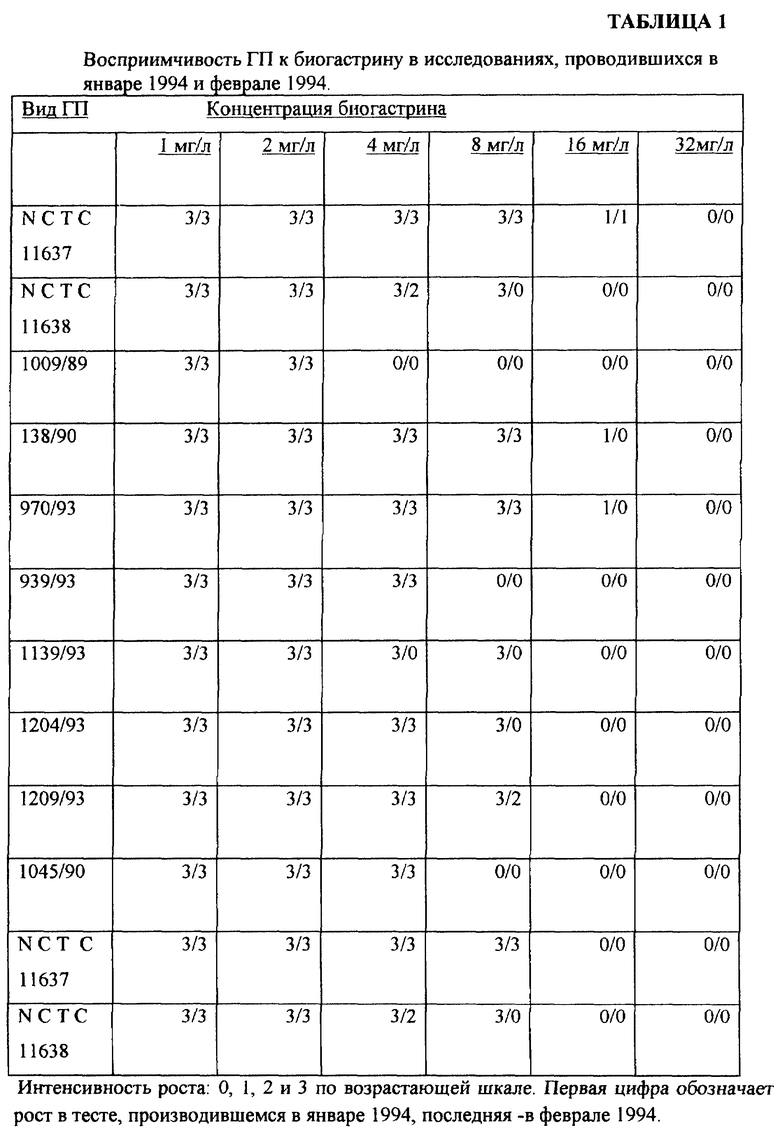
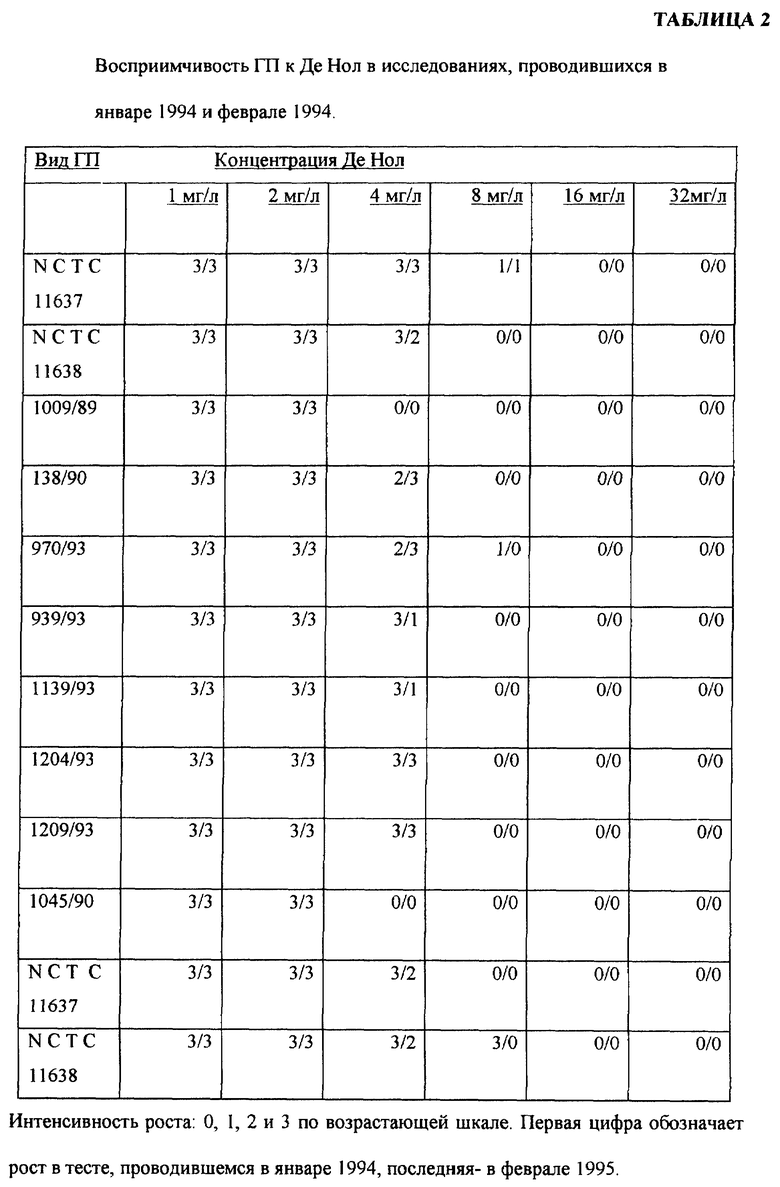
Биогастрин вначале растворяли в физиологической среде и разбавляли ее до концентраций 0, 1, 2, 4, 8, 16 и 32 мг/л. Растворы смешивали с бруцеллезным агаром и из них изготавливали 7 культурных пластинок. На них помещали 10 различных видов ГП (Таблица 1). To же самое проделывали с Де Нол (Таблица 2). Пластинки выдерживали 48 часов при 35 градусах Цельсия, используя атмосферу, содержащую кислород (5%), диоксид углерода (10%) и азот (85%). После этого визуально определяли рост ГП. Минимальная концентрация, при которой наблюдался рост ГП, обозначалась МИК.
Для изготовления исходной культуры десять видов ГП были привиты коровьему скоту, выдерживались в нем 24 часа, а потом разбавлялись до плотности 0,5 по шкале Мак-Фарланда.
МИК определяли дважды: в январе и феврале 1994 года.
Биогастрин, альгинат висмута были приобретены у Кротекс Интернешнл АБ, Аским, Швеция и Де Нол у Алгол, Хельсинки, Финляндия. МИК биогастрина изменялась от 4 мг/л до 32 мг/л, среднее значение было равно 16 мг/л в исследовании, проводившемся в январе 1994, и 8 мг/л в исследовании, проводившемся в феврале 1994. МИК Де Нол изменялась от 4мг/л до 8 мг/л, среднее равнялось 8 мг/л в обоих исследованиях. Результаты представлены в подробностях в Таблицах 1 и 2. Биогастрин содержал 34% металлического висмута и 90% Де Нол.
Так как весовой процент висмута в биогастрине составляет 34%, а в Де Нол 90%, средние значения МИК должны быть скорректированы для того, чтобы получить достоверное сопоставление. После поправки средние показатели биогастрина составляли 5,44 и 2,72 мг висмута/л и в DE-NOL - 7,20 мг/л. Поэтому восприимчивость ГП к биогастрину достаточно близка с восприимчивостью к Де Нол. Хотя биогастрин в этих тестах показывает несколько лучшую МИК по сравнению с Де Нол, это отличие достаточно несущественно. Оптическое определение МИК необъективно из-за заниженной оценки МИК и поэтому не дает достоверных сравнительных характеристик этих лекарств.
Тем не менее биогастрин показывает более хорошую антигеликобактериальную эффективность in vitro.
Исследование 1.
Целью исследования явилось сравнение терапевтических показателей биогастрина и симетидина (тагамет) на группе пациентов с большой выносливостью и достаточной сопротивляемостью обратным эффектам лечения.
Пациенты и методики:
20 пациентов - 8 мужчин и 12 женщин были отобраны для исследования. Исключающими критериями был возраст - моложе 65 лет, отсутствие каких-либо сердечно-сосудистых, почечных и метаболических заболеваний (диабета), отсутствие лечения, кроме лечения гастрофагитного рефлюкса и по крайней мере пятилетняя история рефлюкс-эзофагита с терапевтическими резистентными симптомами изжоги и отрыжки. Диагностический контроль прогрессирования рефлюкс-эзофагита осуществлялся средствами:
а) эндоскопического исследования;
б) внутриэзофагитного наблюдения рН в течение 24 часов (известное из предшествующего пребывания в больнице);
в) подробная запись всех симптомов, сообщаемых пациентами (см. описание выше).
Все пациенты опрашивались для подсчета их клинических симптомов изжоги, регургитации, постурального симдрома средствами визуальной сравнительной шкалы - ВСШ для каждого симптома.
Для контроля присутствия campylobacter биопсические образцы отбирались во время эндоскопии.
Образцы затем оценивали:
а. гистологически;
б. отмечанием активности на грамм красящих веществ и мочевины.
Все пациенты после отбора для исследования лечили тагаметом с нашими наружными присадками без антикислот, и это лечение применялось в течение последних шести месяцев, предшествующих исследованию. Все пациенты подвергались эндоскопическому обследованию, причем проявлялась эндоскопическая картина, соответствующая уровням 2, 3 (в согласии с определительной классификацией Savary и Miller - для определения см. выше). Ни один из пациентов не употреблял антибиотики во время обследования.
После принятия неофициального словесного согласия все пациенты случайно отбирались в двойном закрытом протоколе либо в группу, употребляющую цимитидин (тагамет) 800 мг на ночь и биогастрин (2 капсулы 3 раза в день - через 30 минут после каждого приема пищи), либо в группу, употребляющую цимитидин и плацебо.
(Это было первое исследование, и мы не рискнули отказаться от Tagamet. Целью этого исследования поэтому было определение, улучшает ли лекарственный эффект добавление биогастрина к уже осуществлявшемуся лечению с рецепторными блокерами Н2 при терапии резистентных больных по сравнению с плацебо).
Описанное выше лечение прерывалось после 3 недель, пациентам, у которых были замечены улучшения, назначалось дополнительное трехнедельное лечение, в то время как лечение цимитидином прерывалось и после этого возобновлялось только лечение биогастрином (той же дозировкой 3 капсулы 3 раза в день). Пациенты, у которых не было обнаружено улучшений, лечились после этого тагаметом.
В группе с плацебо пациенты без улучшений лечились в течение этого периода (период В) тем же способом.
Результаты
Из 10 пациентов, лечившихся цимитидином и биогастрином, у восьми наблюдалось четкое улучшение при эндоскопическом обследовании. Во время начала исследования трое имели уровень 3, четверо уровень 2 и трое уровень 1 (в соответствии с Савари и Миллером), но уже после трех недель лечения тагаметом и биогастрином у восьми пациентов наблюдалась нормальная или почти нормальная картина слизистой оболочки пищевода. В противоположность этому в группе людей, лечившихся плацебо + тагаметом, у шести пациентов не наблюдалось улучшений, у одного произошло улучшение со 2 на 1 уровень, у одного с 3 на 2 уровень.
Разница была четкой и значительной. Средний уровень эзофагитной эрозии и язв уменьшился с 48+0,5 до 3,8+0,4 в группе плацебо - тагамет.
Положительная отметка для КП (campylobacter pyloris) была найдена в девяти (положительная гистология в восьми) случаях.
Шесть из девяти пациентов были определены в группу со смешанным лечением биогастрином + тагаметом. Какой бы сильной ни была культура capylobacter, лечение биогастрином + тагаметом приводило к уничтожению КП с отрицательным результатом на культуру при анализе теста мочи и улучшенной гистологией.
В противоположность этому у трех пациентов при исходном присутствии КП КП не уничтожилась и после завершения трехнедельного лечения - плацебо + тагаметом.
Период В проводили открытым методом.
Из шести пациентов без улучшений (предварительно лечившихся плацебо + тагаметом) все показали симптоматическое и эндоскопическое улучшение. (У троих уровень улучшился до 0, у одного от 3 до 1 и у двух от 2 до 0). У троих пациентов с положительным тестом на культуру КП после периода А, после приема биогастрина во время периода В этот тест стал отрицательным. У всех пациентов, лечившихся одним биогастрином во время периода В (всего 12 пациентов), не наблюдалось симптоматических признаков возвращения и вообще никаких симптомов рефлюкс-эзофагита.
Был сделан вывод, что введение биогастрина пациентам с хроническим, лечебно-резистентным рефлюкс-эзофагитом, получающим рецепторные блокеры Н2, приводит к четкому симптоматическому улучшению состояния (уменьшению изжоги и регургитации).
Субъективное симптоматическое улучшение (засвидетельствованное отметкой ВСШ) было связано с улучшением эндоскопической картины пищеводной оболочки и уничтожением campylobacter pylori.
У пациентов с наблюдаемым улучшением после первого трехнедельного курса лечения (тагамет + биогастрин) продолжение лечения одним биогастрином оказалось достаточным для поддержания первично полученного состояния отсутствия симптомов.
Предположили, что добавление биогастрина к лечебному арсеналу для изначально терапевтически резистентных пациентов обещает быть новым лечебным подходом. В случаях положительного теста на культуру КП наличие КП в биопсиновом материале является ясным показателем для назначения лечения биогастрином.
Исследование 2
Целью этого исследования планировалось сравнение терапевтического эффекта сукралфата и биогастрина. Оба лекарства обладают несколькими сходствами - сроком заживляющего эффекта оболочки, связывающими свойствами желудочной и пищеводной эпителий, простагландиновым синтезом и защитным эффектом оттока кислотного компонента. Для вызова обостренных симптомов изначально компетентно лечившиеся больные принимали небуферированный аспирин в течение двух недель. В этом специфическом исследовании мы провоцировали обострение симптомов для того, чтобы облегчить сравнение и сопоставление показателей.
Двадцать два пациента были набраны для определения лекарственного эффекта сукральфата (Сюккоза Хессл, Мелндал, Швеция) или биогастрина. Кандидатуры всех пациентов рассматривались после тщательной проверки их хронического расстройства пищеварения и эзофагита (Гастроэзофагитная рефлюксная болезнь (ГЭРБ)) с основными симптомами изжоги и регургитации, требующими единичного лечения антикислотами. Для провоцирования обострения симптомов все 22 пациента принимали небуферированный аспирин - 500 мг два раза в день в течение двух недель.
В то же время пациенты принимали либо сукралфат 1 г - 4 раза в день в виде 10 мл дозы саше, содержащей 10 мл смеси (группа 11 пациентов), или биогастрин 1 г три раза в день ежедневно (в виде 3 мл коллоидного раствора, группа В (11 пациентов). После первой недели группа S поменяла сукральфат на биогастрин, а группа В - биогастрин на сукралфат. Исследование проводилось двойным закрытым образом.
Перед началом исследования всех пациентов подвергали эндоскопическому обследованию - определению уровня 1-2 не эрозийного, не язвенного, не стенотического эзофагита или ГЭРБ (который считался включаемым признаком). Другим критерием явилось отсутствие какого-либо другого лечения медикаментами, кроме антикислотами, и отсутствие сердечных, почечных, печенных и метаболичных болезней. Возраст пациентов изменялся от 28 до 62 лет (среднее 37+8), а масса тела от 61 до 87 кг (средняя 74+6) и ВМI 22-28 кг/м (среднее 24,2+31,1 кг/м).
Перед распределением на группы все пациенты находились одну неделю без какого-либо лечения.
Результаты
После недельного приема аспирина семь пациентов группы S и один группы В сообщили о изжоге и частой регургитации.
Во время второй недели все пациенты группы S, которые сообщали об изжоге и регургитации во время первой недели, сообщили о значительных улучшениях их симптомов после установления лечения биогастрином в периоде В.
Это исследование показывает, что биогастрин превосходит сукральфат в защите против влияния типичных блокеров простагландного синтеза, вызывающих обычные симптомы рефлюкс-эзофагита.
Биогастрин предпочтительно использовать в виде коллоидного раствора.
Исследование 3
Исследование было задумано как дополняющее вспомогательное испытание к Исследованию 1.
Цель исследования заключалась в подтверждении первичных выводов о том, что лечение резистентных пациентов с рефлюкс-эзофагитом должно проводиться биогастрином.
Семь пациентов, страдающих изжогой и частой регургитацией, несмотря на длительное лечение ранитидином (Зентек Глаксо) - 150 мг 2 раза в день, исследовали стандартной эндоскопией. У трех пациентов эндоскопия обнаружила уровень 3 и у четырех уровень 2 эндоскопической картины (согласно Miller и Savary).
Все семь пациентов принимали биогастрин по 1 г четыре раза в день (и Зентек, как и ранее) в течение одной недели. Из семи пациентов пять сообщили о четком облегчении симптомов, эти пять пациентов принимали биогастрин еще дополнительно шесть недель как единственное лекарство. У всех пациентов сохранялось неизменным улучшение симптомов. Эндоскопическое обследование проводилось после третьей, шестой и двенадцатой недели лечения.
После первых шести недель эндоскопическое обследование у трех пациентов обнаружило улучшение уровня с 3 до 1 и с 2 до 0 у двоих других. После дополнительного шестинедельного лечения эндоскопия не обнаружила никаких патологических изменений в оболочке пищевода и желудка.
Это исследование, подобно исследованию 1, показало, что биогастрин может быть полезен для всех больных, резистентных к стандартному лечению рецепторными блокерами Н2. Добавление биогастрина к обычному лечению (Зантак или Тагамет) позволяет достигать быстрого улучшения, после которого можно использовать отдельную монотерапию одним биогастрином.
Исследование 4.
Целью исследования было дать оценку терапевтическому эффекту биогастрина по сравнению с гависконом относительно главного назначения гавискона - устранению боли/дискомфорта, возникающих от рефлюкса - регургитации и изжоги. Как и раньше, из-за малого опыта применения биогастрина мы не рискнули проводить исследование классическим методом, т.е. двойным закрытым способом, поэтому медицинская команда, ответственная за лечение, выбрала пошаговую, более безопасную форму клинического определения.
Шестнадцать пациентов с симптоматическим (реальным и записанным в медицинскую карту) и эндоскопически определенным эзофагитом, лечившиеся непрерывно ранитидином (Зантак - Глаксо 150 мг 2 раза в день) и альгиновой кислотой (Гавискон - Ферринг) 2 г 4 раза в день, были отобраны для исследования.
Все пациенты сообщали о некоторых проблемах оттока и/или изжоги по крайней мере 3 раза в день, несмотря на лечение. Критерием включения было повторяющееся лечение и обострения эзофагита в течение последних четырех лет. Все пациенты обследовались эндоскопически, и эндоскопическая картина показала эндоскопический уровень от 3 до 2 (в соответствии с Савари и Миллером).
Все пациенты дали осознанное согласие поменять гавискон на биогастрин 1 г (3 мл) три раза в день. Из шестнадцати пациентов, задействованных в исследовании, двенадцать сообщили о значительном улучшении, касающемся симптомов изжоги, и 10 сообщили о полном освобождении от регургитации. Эндоскопия, проводившаяся на четвертую неделю после смены курса лечения, показала, что у 10 пациентов эндоскопическая картина улучшилась с уровня 3 до уровня 2 и у 6 пациентов с 1 до 0 (нет патологических изменений).
После дополнительного четырехнедельного лечения у всех пациентов, кроме одного, наблюдался эндоскопический уровень 0. Двенадцать пациентов из этой группы прекратили лечение ранитидином после первых четырех недель и сохранили лишь лечение одним биогастрином в течение последующих четырех недель. Кроме того, два пациента сделали то же самое после шестой недели из-за значительного улучшения симптомов и последние две недели лечились только биогастрином.
Это исследование подтвердило эффективность биогастрина в отношении улучшения обычной симптоматики рефлюкс-эзофагита. Это исследование показывает, что биогастрин действует, наиболее вероятно, подобно гавискону, создавая затвор из коллоидного альгината висмута, усиливающего природную защиту тела (нижнего пищеводного сфинктера) вокруг отверстий, предохраняя попадание на чувствительную пищеводную оболочку кислотного компонента желудочного сока (движение вверх во время отрыжки).
Таким образом, можно сделать вывод о том, что существенное улучшение, достигнутое у нескольких терапевтически резистентных пациентов (достигнутое способом, отличным от стандартного лечения), наиболее вероятно связано со специфическим действием биогастрина на campylobacter. (Отбор пациентов для исследования и их терапевтическая резистентность показывают, что пациенты, принимавшие участие в исследованиях, были заражены КП) Коллоидный "затвор" альгината висмута, влияющий на рефлюксную регургитацию, наиболее вероятно способствует улучшению симптомов.
Для подтверждения предварительных результатов необходимо дальнейшее исследование.
Исследование 5
Недавно было показано, что омепразол и омепразол + амоксициллин эффективны для улучшения симптомов и уничтожения Heliobacter pylori при ГЭРБ (гастроэзофагитное рефлюксное заболевание). Однако эта форма терапии требует непрерывного лечения из-за возобновления интенсивности обоих симптомов (обратному оттоку и изжоге) и рецидива (повторной колонизации) Heliobacter pylori.
Было показано, что биогастрин вместе с метронидазолом ослабляет интенсивность и увеличивает степень уничтожения при двойной, тройной и четверной терапии. Целью настоящего исследования явилось изучение долгосрочных эффектов при двухнедельной терапии.
Оценка была направлена на определение степени уничтожения (гистология + бактериальная культура) и плазменной серологии.
Все обследования проводились в течение 6 недель, 6 месяцев и 12 месяцев после прекращения лечения, результаты сравнивались со стандартным лечением Лозек + амоксициллин.
Пациенты и лечение
(А) Шестьдесят три пациента со средним возрастом 47,4 года (диапазон 24,2-60,7), которые обследовались на наличие гастро-эзофагитной рефлюксной болезни (ГЭРБ) и у которых гистология бактериальной культуры показала инфицирование Heliobacter pylori (ГП), были включены и случайным образом разделены на три группы. Группа 1 принимала омепразол + амоксициллин (20 мг два раза в день и амоксициллин 500 мг три раза в день).
Группа 2 принимала биогастрин + амоксициллин (биогастрин 500 мг и амоксициллин 500 мг три раза в день).
Группа 3 принимала только биогастрин (500 мг три раза в день и тинидазол 50 мг два раза в день).
Вышеупомянутое исследование проводилось во всех группах в течение двух недель. Не было существенных отличий в возрасте, весе тела, длительности и степени тяжести ГЭРБ (гастроскопия, гистологическое определение и симптоматика - в особенности интенсивность и частота изжоги).
Критерием уничтожения бактерии было отсутствие бактерии при проверке биопсичных образцов гистологией, бактериальной культурой или обоими способами.
Обследование
Два слизистых образца были взяты из верхней части двенадцатиперстной кишки, антрального отдела желудка для гистологии и один из верхней части двенадцатиперстной кишки и шишковидного тела для бактериальной оценки. Для гистологических исследований использовались Гематоксилин-эозин и Giemsa.
Образцы для выращивания Heliobacter pylori помещали в 0,5 мл 20% глюкозы, перетирались в ступке и прививались к селективным и неселективным отдельным пластинкам в течение 4 час.
Уровень антител к Heliobacter pylori измеряли отдельно для IgG, IgA и IgM ферментным иммуноаналитическим методом. Использованными антигенами были кислый глицериновый экстракт и бактериальный гомогенат, полученные ультрацентрифугированием из Heliobacter pylori вида NCTC 11637.
Оптические показания были преобразованы в обратные к конечно-точечным титрам. Конечно-точечными титрами была разбавленная сыворотка при предельном уровне, определенная по оптической плотности абсолютного эталонного сывороточного объема при постоянном разбавлении. Отдельные эталонные объемы использовались для иммуноглобулинов A, G и М. Их помещали на каждую микротитрическую пластину, и все образцы пациентов изучались при тройном разбавлении, согласно Kosunen и др, Lancet. 1992:339:893-895.
Образцы были взяты до лечения и затем после 6 (+/2) недели и 6 (+/2) месяца от начала лечения и включали биопсичные образцы для гистологии и бактериальных культур, сывороточные образцы для циркуляции антител к Heliobacter pylori.
Все пациенты дали осознанное согласие после того, как были осведомлены о протоколе исследования. Только пациенты с диспепсией и изжогой, по крайней мере от 1 до 3 месяцев не лечившиеся коллоидным субстратом висмута, антибиотиками, рецепторами Н2, антагонистами или омепразолом (блокер белкового транспорта), были допущены для исследования. Пациенты с недавней предысторией обнаруженного или доказанного кишечно-желудочного кровотечения или предысторией желудочной хирургии были исключены.
Лечение проводилось во время всего двухнедельного периода. Два пациента перестали участвовать по независимым семейным обстоятельствам.
Результаты
До лечения все 63 пациента были заражены бактерией и имели гистологически и гастроскопически определенные активные хронические гастрит и эзофагит. Почти все пациенты обладали повышенным титром циркуляции антител к Heliobacter pylori. Повышенные титры IgG-антител были найдены у 98% пациентов, IgA- у 94% и IgM- у 48% пациентов.
В группе 1 (омепразол + амоксициллин) восемьдесят два процента пациентов сообщили о значительном облегчении симптомов изжоги и диспепсии.
В группе 2 (биогастрин + амоксициллин) соответствующее число равнялось восьмидесяти процентам.
В группе 3 (биогастрин + тинидазол) восемьдесят четыре процента (для метронизадол/тинидазол - восприимчивых и 68% для метронизадол - резистентных пациентов).
Через шесть недель после прекращения лечения Heliobacter pylori была уничтожена у 74% пациентов, принадлежащих к 1 группе, и у 72% во 2 группе. В третей группе уничтожение Heliobacter pylori было найдено у 82% среди пациентов, зараженных видом ГП, восприимчивым к метронизадол/тинидазолу и у 54% среди пациентов с ГП, не восприимчивым к метронизадол/тинидазолу.
Уровень IgG-антител медленно уменьшался к 6 неделям у 70% пациентов в группе 1 и в 72% в группе 2. В группе 3 значительное уменьшение было найдено у 78% у восприимчивых к метронизадолу и 48% среди не восприимчивых к метронизадолу пациентов.
IgA-титры уменьшались у 64% пациентов группы 1, 72% группы 2 и 60% группы 3 (78% среди восприимчивых к метронизадолу и 43% среди резистентных к метронизадолу пациентов).
Через 6 месяцев после прекращения лечения IgG-титр у пациентов с отсутствием бактерий был в среднем 22% по отношению к уровню до лечения, a IgA-титр 36%.
12-месячные образцы пациентов без бактерий показали, что титры антител непрерывно убывают. Почти у всех пациентов падение IgG и IgA титров составило более 50%.
Восемь пациентов среди освободившихся от симптомов в группе 1 испытали сильную изжогу после прекращения лечения и были вынуждены начать альтернативное лечение (гавискон и сульфакрат) во время первого шестимесячного периода. То же самое случилось с 2 пациентами 2 группы и 4 пациентами 3 группы. Все последние пациенты принадлежали к пациентам, резистентным к метронизадолу и с присутствием ГП на момент 6-месячного теста.
IgM уменьшался у 67% пациентов группы 1, 71% группы 2 и 64% группы 3 (но у 74% восприимчивых к метронизадолу пациентов).
У пациентов с уничтоженной бактерией титры антител продолжали падать после 6 недель, у пациентов с сохраненной бактерией титры продолжали оставаться высокими на протяжении наблюдаемого периода.
Через шесть месяцев после прекращения лечения только у 64% пациентов группы 1 реакции на ГП все еще не было. Процент пациентов с отрицательным тестом на ГП в группе 2 не изменился и составлял 72% и в группе 3 уменьшился с 54% до 45% у резистентных к метронизадолу пациентов, сохранился высоким и почти не изменился у восприимчивых к метронизадолу пациентов - 80%.
Через 12 месяцев после лечения уровень уничтожения был 56% для группы 1, 72% для группы 2 и 42 и 80% в группе 3 для резистентных к метронизадолу и восприимчивых к нему пациентов соответственно.
Обсуждение
Результаты данного исследования ясно показывают высокую чувствительность 50% падения InG титра как индикатора бактериального уничтожения уже к 6 неделям. Чувствительность этого теста возрастает со временем, и уменьшение становится более специфичным при 6 и 12 месяцев соответственно.
Титры 40% и меньше относительно уровня до начала лечения были замечены только у пациентов с отрицательным тестом на бактерию сразу же после прекращения лечения.
Эффективность всех трех методов лечения сопоставима по периоду улучшения основных симптомов, связанных с ГЭРБ по тесту, проводимому после 6 недель.
Сопоставимой была и скорость уничтожения ГП (исключая более высокую скорость уничтожения у пациентов, чувствительных к метронизадол/тинизадолу, и более низкий уровень у пациентов, резистентных к метронизадолу, лечившихся биогастрозолом).
Однако у пациентов группы 1 (омепразол + амоксициллин®) наблюдалась высокая степень повторного заражения Heliobacter pylori.
То же самое остается верным для детороидальной симптоматики и необходимости повторного назначения антирефлюксного и антикислотного лечения. В той же мере подобная ситуация наблюдалась для пациентов, резистентных к метронизадолу/тинизадолу, лечившихся комбинацией биогастрина и тинидазола. 84% пациентов группы 1 и 26% пациентов группы 3 просили о назначении повторного лечения (гавискон + сукралфат).
Результаты настоящего исследования поэтому показывают, что двойная терапия с биогастрином выглядит предпочтительнее сочетания омепразол + амоксициллин из-за более высокой степени уничтожения, определяемой после 6 и 12 месяцев после прекращения 2-недельного лечения.
Результаты данного исследования также показывают, что двойное лечение сочетанием блокеров белкового выкачивания и ампициллина не является достаточным для долгого периода времени и тройное лечение или двойное лечение биогастрином, амоксициллином и тинидазолом дает гораздо лучшие долгосрочные результаты по отношению как к уничтожению Heliobacter pylori, так и к улучшению основных симптомов ГЭРБ.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ ЖЕЛУДОЧНО-КИШЕЧНОГО ТРАКТА, АССОЦИИРОВАННЫХ С HELICOBACTER PYLORI | 2004 |
|
RU2278682C2 |
| СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКИХ ГАСТРОДУОДЕНИТОВ, АССОЦИИРОВАННЫХ С ИНФЕКЦИЕЙ, ВЫЗВАННОЙ БАКТЕРИЯМИ Helicobacter pylori, ПРИ АЛЛЕРГИЧЕСКИХ ЗАБОЛЕВАНИЯХ | 2011 |
|
RU2472498C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ГАСТРОЭЗОФАГЕАЛЬНОЙ РЕФЛЮКСНОЙ БОЛЕЗНИ | 2012 |
|
RU2501549C1 |
| СПОСОБ ДИАГНОСТИКИ СТЕПЕНИ АКТИВНОСТИ АНТРАЛЬНОГО ХЕЛИКОБАКТЕР-АССОЦИИРОВАННОГО ГАСТРИТА У БОЛЬНЫХ БРОНХИАЛЬНОЙ АСТМОЙ | 2009 |
|
RU2394499C1 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ ЯЗВЕННОЙ БОЛЕЗНЬЮ | 2006 |
|
RU2329810C1 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ ОТ HELICOBACTER PYLORI | 2014 |
|
RU2671400C2 |
| СПОСОБ ЛЕЧЕНИЯ ЯЗВЕННОЙ БОЛЕЗНИ ЖЕЛУДКА И ДВЕНАДЦАТИПЕРСТНОЙ КИШКИ | 2006 |
|
RU2294204C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ГАСТРОЭНТЕРОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 1995 |
|
RU2076708C1 |
| СПОСОБ ЛЕЧЕНИЯ ИНФЕКЦИИ HELICOBACTER PYLORI У ВЗРОСЛЫХ | 2019 |
|
RU2699567C1 |
| СПОСОБ ЛЕЧЕНИЯ ЯЗВЕННОЙ БОЛЕЗНИ ЖЕЛУДКА И ДВЕНАДЦАТИПЕРСТНОЙ КИШКИ, АССОЦИИРОВАННОЙ С HELICOBACTER PYLORI | 2006 |
|
RU2308949C1 |
Изобретение относится к области фармакологии и касается фармацевтических препаратов для лечения гастритов, рефлюкс-эзофагитов, дуоденитов, диспепсии и язвы. Изобретение заключается в том, что фармацевтический препарат содержит смесь цитрата висмута и альгината и любые полученные реакционные продукты, особенно альгинат висмута. Кроме того, препарат может содержать одно или более антибиотическое вещество. Также к реакционной среде может быть добавлен компонент, содержащий кальций, например хлорид кальция, для образования микрокапсул альгината кальция, который будет действовать как медленно высвобождаемое покрытие. Препарат также может содержать агент, как, например, бикарбонат натрия. Изобретение обеспечивает эффективность для удаления Campylobacter, такого, как Heliobacter pylori, в дальнейшем он должен активно препятствовать обратному оттоку содержимого желудка. 6 з.п. ф-лы, 2 табл.
| BAYERD URFEER J.MED.SCI, 1992, 161, Suppl | |||
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| УСТАНОВКА ДЛЯ ПЕРЕРАБОТКИ ЗЕЛЕНИ ПИХТЫ | 2002 |
|
RU2221843C1 |
| Устройство гибкого элемента паропровода | 1955 |
|
SU101294A1 |
| РЕГУЛИРУЮЩИЙ ОРГАН | 0 |
|
SU244832A1 |
Авторы
Даты
2002-11-27—Публикация
1997-03-27—Подача